-
水、能源和营养物质(氮、磷)是影响人类社会生存和发展的重要资源。低能耗、高效率地实现污水中氮磷元素的去除是全球水处理领域面临的突出难题。在日常生活中,人类新陈代谢产生的大部分物质会通过尿液排放出来,尤其是尿液中N元素的含量可以高达10 000 mg·L−1[1-2]。尿液贡献了城镇生活污水中约80%的氮,但其自身体积却仅占污水总体积的不足1%[3]。N元素在工业及农业上非常有用,但其排放到水体中却会产生污染。因此,在厕所废水排放前,降低其含氮量,减少其对环境的危害是非常必要的。目前,活性污泥工艺是厕所废水处理中使用较为广泛的一种方法,但其水力停留时间较长、处理效率也较低。
微生物电解池技术(microbial electrolysis cell,MEC)是在外加电压下,电活性微生物参与的阳极氧化耦合阴极还原的过程。采用MEC处理低C/N或高氨氮废水,通常是在阳极利用有机物或氨氮作为电子供体,在阴极以硝酸盐或亚硝酸盐为电子受体实现脱氮的过程。该技术是通过外加电势差实现废水中化学能的转化,在阴极实现无需外加碳源、偶联阳极氧化的自养脱氮新工艺[4-8]。现有MEC脱氮处理的相关研究,多数采用低C/N模拟废水或配制的高含氮废水(氨氮或硝态氮),尚未见实际厕所废水(以尿液为主)MEC处理工艺的相关研究。
本研究以合成钛棒为导体,碳毡作为阳极和阴极的微生物附着填料,通过构建三维单室无膜MEC反应装置,探讨了在4种不同外加微电压下单室无膜MEC装置针对尿液废水的处理效果,并对其最佳反应条件和微生物菌群进行了优化和分析评价,旨在为以尿液为主的厕所废水低能耗处理提供参考。
全文HTML
-
与常规不锈钢材料相比,合成钛棒是一种具有良好的导电性、耐腐蚀耐氧化的新型金属材料,因其具有良好的导电性,已被广泛应用于工业生产和实际生活当中[9-11]。碳毡因其具有良好的吸附性和经济性,被用作微生物电解池的阳极和阴极材料[12]。碳毡在使用前须先用1 mol·L−1的HCl浸泡24 h,以去除电极表面的杂质,然后用去离子水进行冲洗至中性,最后再用超声波清洗仪清洗30 min后,常温晾晒干燥使用。
-
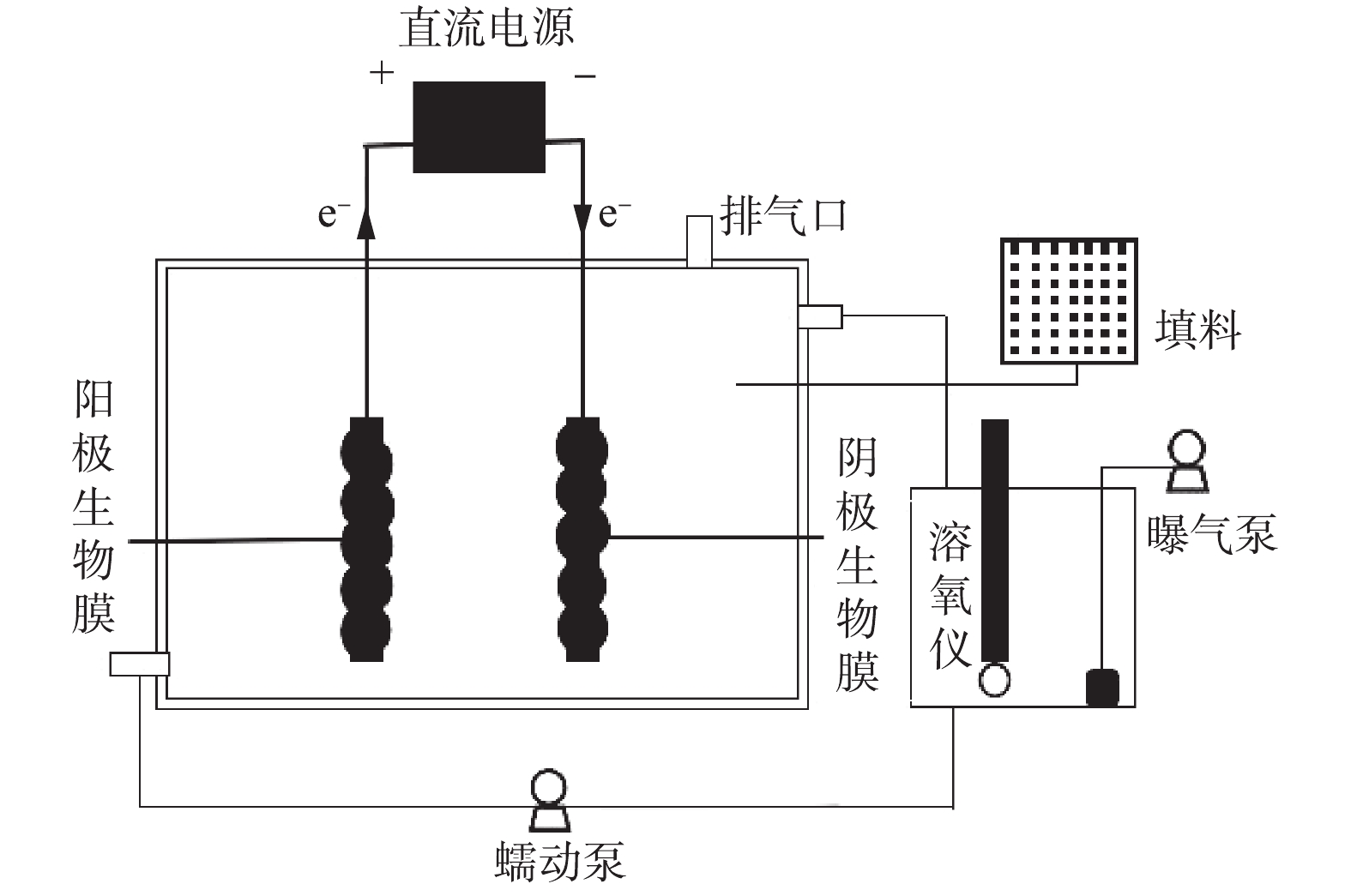
MEC实验装置结构示意图如图1所示。装置采用透明有机玻璃制作,长为18 cm,宽为5 cm,高为14 cm,并在顶端设置一个单向排气孔。单室无膜MEC装置有效容积为960 mL,在阴阳电极之间加入直流电源提供外加微电压,并记录实时电流。装置中硝化生物膜和反硝化生物膜分别用于构建单室电解池的生物阳极和阴极,电极两端分别连接直流电源器的正负极,其余各部分通过钛丝相互连接,外电路中串联一个10 Ω的小电阻。电解池中添加玻璃珠和碳柱颗粒混合填料,以形成三维电解池,玻璃珠和碳柱颗粒体积比为4∶1。
-
COD采用重铬酸钾法测定,
${\rm{NH}}_4^ + $ -N采用纳氏试剂光度法测定,${\rm{NO}}_2^ - $ -N采用1-萘基-乙二胺光度法测定,${\rm{NO}}_3^ - $ -N采用紫外分光光度法测定,TN采用碱性过硫酸钾紫外分光光度法测定,pH采用pH计测定,浊度采用浊度仪测定,微生物菌群采用16S DNA测序法测定。
1.1. 钛棒和碳毡
1.2. 实验装置
1.3. 分析测试方法
-
在初始驯化阶段,采用人工配制尿液,以8 cm×15 cm碳毡为载体,分别进行硝化生物膜和反硝化生物膜的培养。培养液成分为0.3 g·L−1 KH2PO4、1.0 g·L−1 NaHPO4·12H2O、0.5 g·L−1 NaCl、2.0 g·L−1 NaCO3、0.1 g·L−1 MgSO4·7H2O、0.01 g·L−1 CaCl2。硝化生物膜池额外添加浓度为0.5~1.5 g·L−1的NH4Cl,反硝化生物膜池额外添加浓度为0.8 g·L−1的KNO3和0.9 g·L−1的乙酸盐,这种模拟尿液浓度类似实际尿液稀释10倍[13-14]。在初始启动阶段,硝化及反硝化生物膜池每间隔24 h取样,连续观察
${\rm{NH}}_4^ + $ -N和${\rm{NO}}_2^ - $ -N浓度变化情况,当${\rm{NH}}_4^ + $ -N转化率达到50%左右,置换90%溶液,开始下一周期运行,重复多次,直到转化率稳定。检测进出水TN、${\rm{NH}}_4^ + $ -N以及出水${\rm{NO}}_2^ - $ -N和${\rm{NO}}_3^ - $ -N,当${\rm{NH}}_4^ + $ -N至${\rm{NO}}_2^ - $ -N转化率稳定在50%以上,则认为硝化生物膜驯化成熟。反硝化生物膜在初始培养液中曝氩气15 min[15],去除培养基中的溶解氧,形成厌氧环境。驯化40 d后,阳极和阴极碳毡表面清晰可见分别附着了一层硝化膜和反硝化膜,手感滑腻。驯化成熟的阳极硝化膜与阴极反硝化膜,分别连接正、负极后,开始间歇进水实验。在MEC装置启动时,取宜兴某景区厕所废水960 mL,加入到自制的单室无膜MEC装置内,顶空体积为100 mL。实验用厕所废水水质浓度如下:${\rm{NH}}_4^ + $ -N为100~140 mg·L−1、${\rm{NO}}_2^ - $ -N为5~10 mg·L−1、${\rm{NO}}_3^ - $ -N为1~5 mg·L−1、TN为120~180 mg·L−1、pH为6~8、浊度为30~40 NTU。采用不同电压,分3个周期连续运行,即分别在0.4、0.6、0.8、1.0 V恒定电压下,连续运行3个周期,研究了在不同外加电压下${\rm{NH}}_4^ + $ -N、${\rm{NO}}_2^ - $ -N、${\rm{NO}}_3^ - $ -N和TN的变化情况。 -
短程硝化反硝化生物脱氮工艺区别于传统硝化反硝化之处在于,
${\rm{NH}}_4^ + $ -N生成${\rm{NO}}_2^ - $ -N后,经过一系列反应直接生成N2[16-18]。与传统硝化反硝化技术相比,短程硝化反硝化因减少生成${\rm{NO}}_3^ - $ -N这一过程,降低了DO需求,增加了氮的脱除效率。高溶解氧有利于阳极氮的氨氧化,较低的DO有利于实现阴极反硝化,POCHANA等[19]认为,DO超过0.8 mg·L−1,就会对反硝化产生干扰。所以如何控制阴极和阳极之间DO的互相影响,寻找最佳溶解氧浓度非常关键。此外,根据微氧环境下废水处理原理,当废水处于微氧环境条件下,存在内源硝化反硝化等氮的多途径转化,可有效减少脱氮过程中对碳源的需求[20]。为在硝化阶段控制${\rm{NH}}_4^ + $ -N能够更有效地氧化为${\rm{NO}}_2^ - $ -N,本研究采用了间歇曝气的方法,使用转子流量计调节曝气量为40 mL·min−1,控制DO在0.4~0.7 mg·L−1的较低浓度。 -
在单室无膜MEC装置稳定运行阶段,分别施加不同外加电压,对微生物进行电极诱导和驯化,采用间歇进水方式,每5 d为一个周期,每周期末,置换反应器(容积为2 L)中90%的水,即补充1.8 L原水,进行下一个周期的运行,连续运行3个周期。
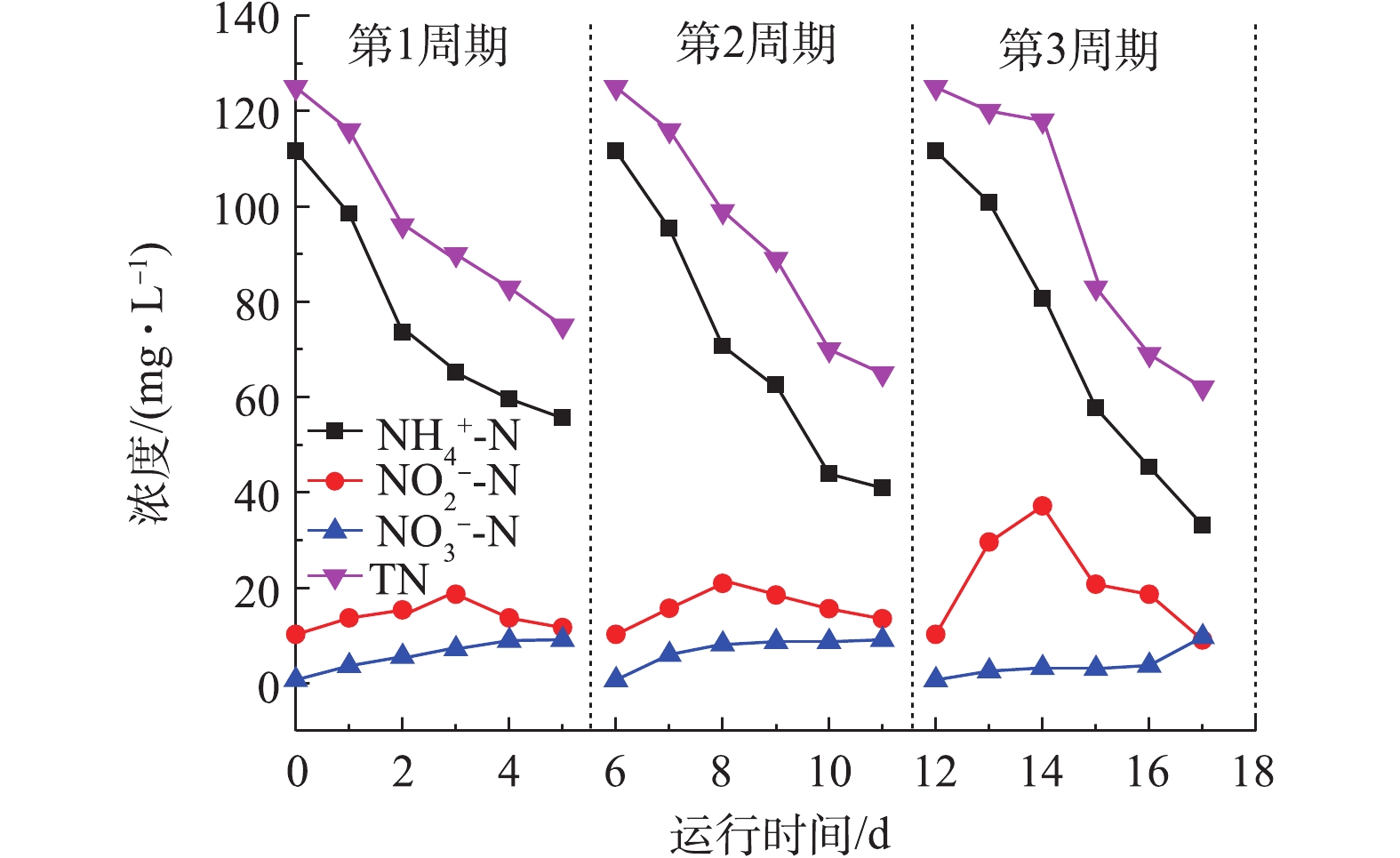
在恒定外加电压为0.4 V条件下,MEC对厕所废水的处理效果如图2所示。由图2可知,在经单室无膜MEC装置处理后,
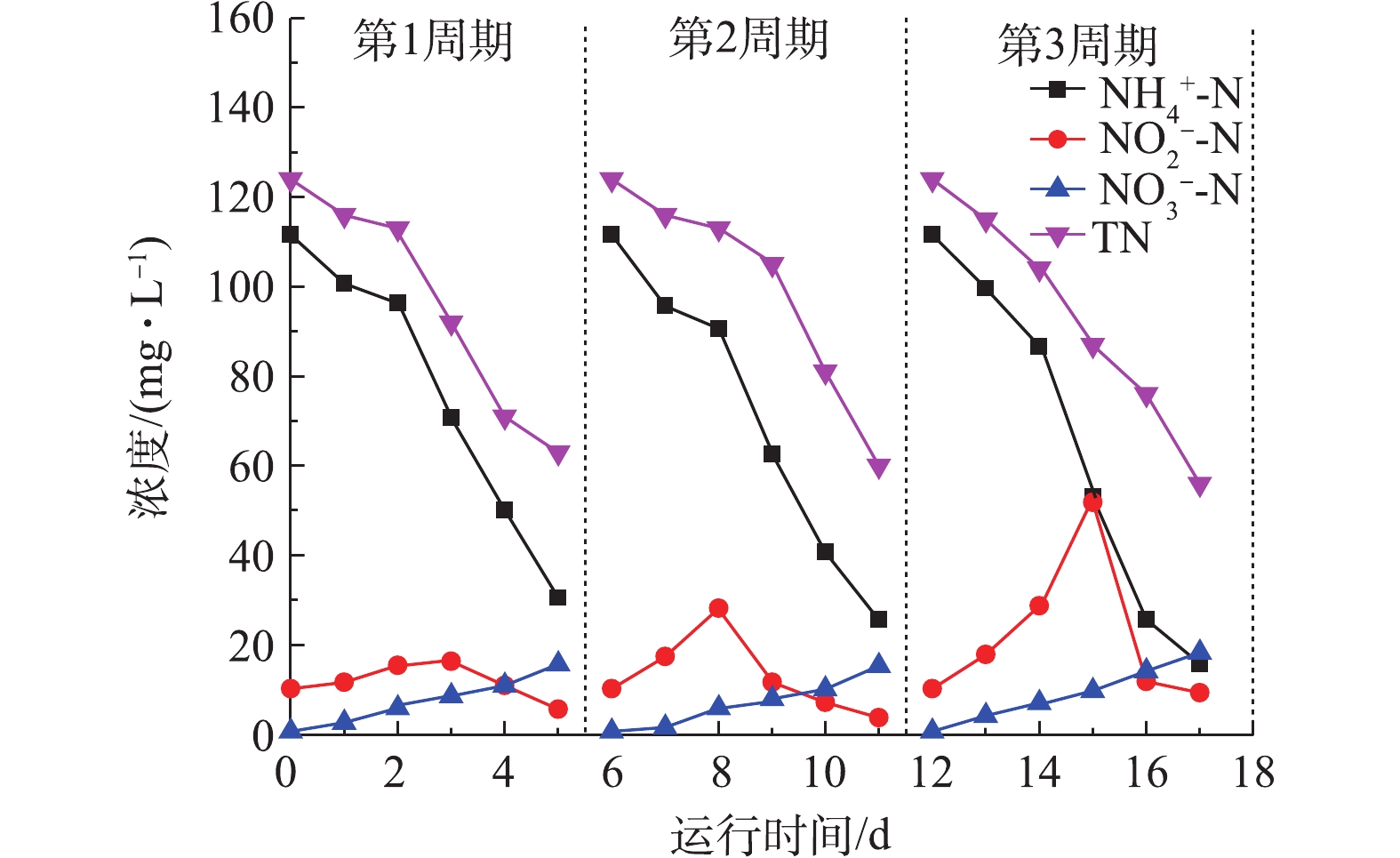
${\rm{NH}}_4^ + $ -N和TN分别从116 mg·L−1和125.05 mg·L−1降至33.11 mg·L−1和62.01 mg·L−1,去除率分别为70.33%和50.41%。${\rm{NH}}_4^ + $ -N的去除速率在前半程较快,在后半程明显降低。这是由于在初始实验阶段,装置刚施加电压,产电微生物需要一定时间适应并繁殖,此时阳极生物膜上常规硝化细菌仍占多数,产电细菌较少,主要反应仍为常规硝化反应;随着反应时间的延长,产电细菌和自养硝化细菌不断繁殖,而异养硝化细菌会相应减少,${\rm{NH}}_4^ + $ -N的去除速率逐渐降低。随着实验的进行,${\rm{NH}}_4^ + $ -N总去除率不断增加,这说明微生物菌群的丰度和数量逐渐丰富。${\rm{NO}}_2^ - $ -N浓度呈现先升高后降低的趋势,而${\rm{NO}}_3^ - $ -N没有明显增加,这说明在恒定微电压并控制DO浓度条件下,装置中发生了短程硝化反硝化反应。在恒定外加电压为0.6 V条件下,MEC对厕所废水的处理效果如3所示。由图3可知,经单室无膜MEC装置处理后,
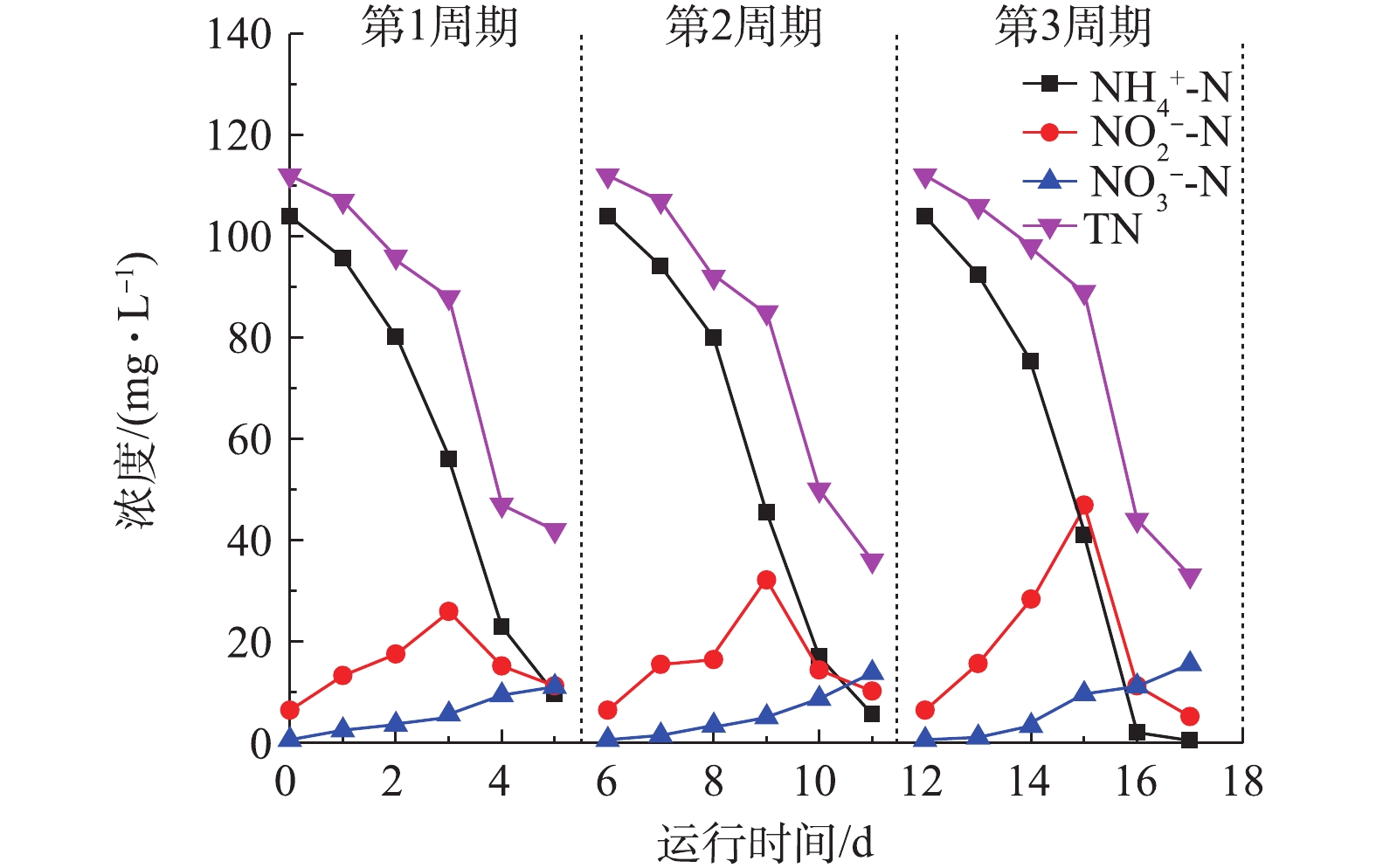
${\rm{NH}}_4^ + $ -N和TN分别从111.6 mg·L−1和120.03 mg·L−1降至15.77 mg·L−1和56.03 mg·L−1,去除率分别为85.87%和54.83%。较之0.4 V恒定电压下${\rm{NH}}_4^ + $ -N和TN去除率有小幅提升,说明在一定范围内随着电压升高,单室无膜MEC装置的脱氮效果逐渐增强。相比后半程${\rm{NH}}_4^ + $ -N的去除速率,前半程${\rm{NH}}_4^ + $ -N去除速率较低。这说明:在前半程,以${\rm{NH}}_4^ + $ -N向${\rm{NO}}_2^ - $ -N的转化为主导,且由于控制了DO浓度,反应速率受到抑制;在后半程,由于装置中${\rm{NO}}_2^ - $ -N有了一定的积累,反应逐渐以${\rm{NH}}_4^ + $ -N偶联${\rm{NO}}_2^ - $ -N生成氮气为主导,所以TN去除速率有了明显提升。在恒定电压为0.8 V条件下,MEC对厕所废水的处理效果如图4所示。由图4可知,经单室无膜MEC装置处理后,
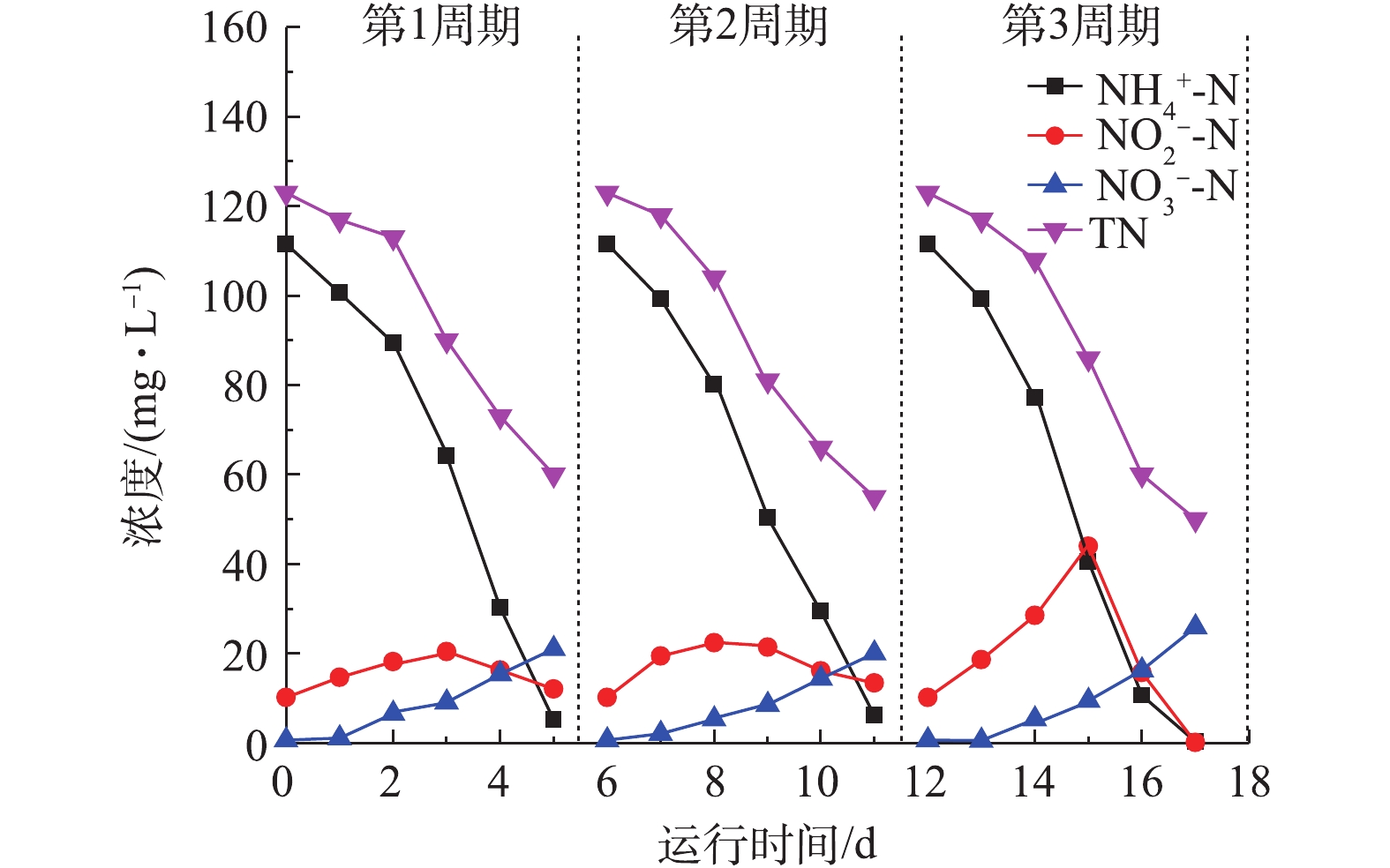
${\rm{NH}}_4^ + $ -N和TN分别从103.06 mg·L−1和112.02 mg·L−1降至0.45 mg·L−1和33.04 mg·L−1,其去除率分别为99.56%和70.51%。${\rm{NO}}_2^ - $ -N最大累积量为46.94 mg·L−1,低于初始${\rm{NH}}_4^ + $ -N含量的50%。这说明在初始阶段,就有${\rm{NH}}_4^ + $ -N和${\rm{NO}}_2^ - $ -N偶联生成N2溢出。由图4可知,在第3周期后半程,${\rm{NH}}_4^ + $ -N和${\rm{NO}}_2^ - $ -N的去除速率几乎相等,说明在0.8 V恒定电压下,单室无膜MEC装置达到了预期的短程硝化反硝化反应,${\rm{NH}}_4^ + $ -N和${\rm{NO}}_2^ - $ -N达到同步去除的效果,这与占国强[4]的研究结论相似。此时,发生的主要反应是在严格控制DO条件下,一部分${\rm{NH}}_4^ + $ -N首先氧化为${\rm{NO}}_2^ - $ -N,然后${\rm{NO}}_2^ - $ -N和剩余${\rm{NH}}_4^ + $ -N通过外加微电压作用偶联生成N2溢出。在恒定电压为1.0 V条件下,MEC对厕所废水的处理效果如图5所示。由图5可知,经单室无膜MEC装置处理后,
${\rm{NH}}_4^ + $ -N和TN分别从111.6 mg·L−1和123.02 mg·L−1降至0.32 mg·L−1和50.04 mg·L−1,其去除率分别为99.71%和59.32%。${\rm{NO}}_2^ - $ -N累积量为41.36 mg·L−1,较0.8 V下有所下降,而${\rm{NO}}_3^ - $ -N的累积量明显升高,并且TN的去除效果较0.8 V下也有所下降。这应该与外加电压有关,过高的外加电压导致电化学反应产生H2和O2,产生的O2会使一部分${\rm{NO}}_2^ - $ -N氧化为${\rm{NO}}_3^ - $ -N,而过多的H2会导致反硝化过程中出现“氢抑制”现象,进而出现出水TN偏高的现象。这也与ZHAN等[5]报道的结果相吻合,故为避免电解水的影响并保证短程硝化反硝化的顺利进行,确定MEC装置的外加电压不宜超过0.8 V。 -
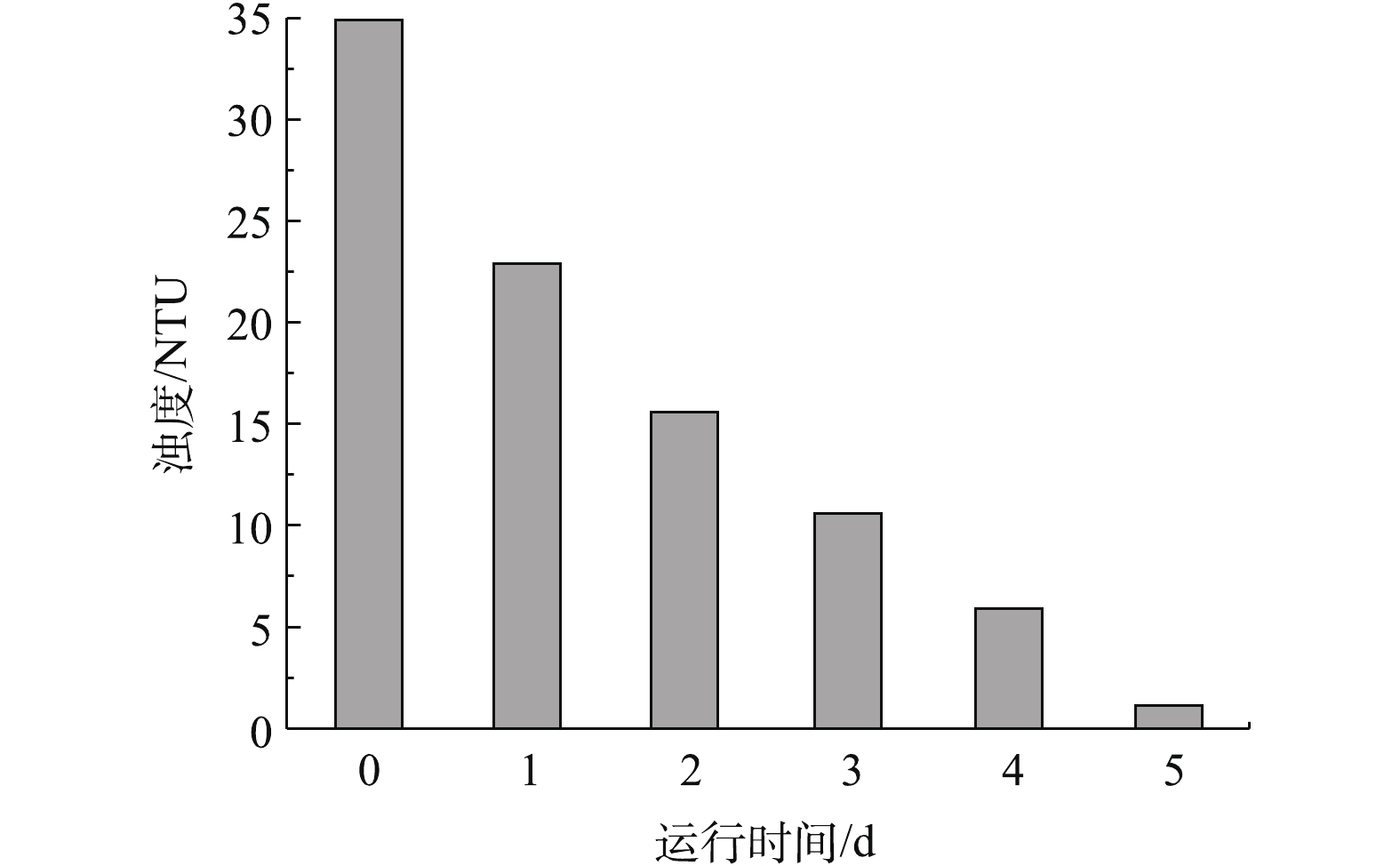
单室无膜MEC装置还对厕所废水浊度具有一定的去除效果。由图6可知,原水浊度为34.9 NTU,经处理后,出水浊度下降至1.12 NTU,其去除率可达96.79%。这主要归因于以下3点:其一,碳毡及其表面生物膜具有一定的吸附能力,它对水中部分悬浮物的吸附导致水体浊度降低;其二,在通电状态下,废水中胶体之间的静电斥力被消除,能够相互凝聚成大颗粒而沉淀下来;其三,尿液中偶氮型色素与阴极之间的电子转移引起了偶氮双键的断裂也可致使浊度降低。
-
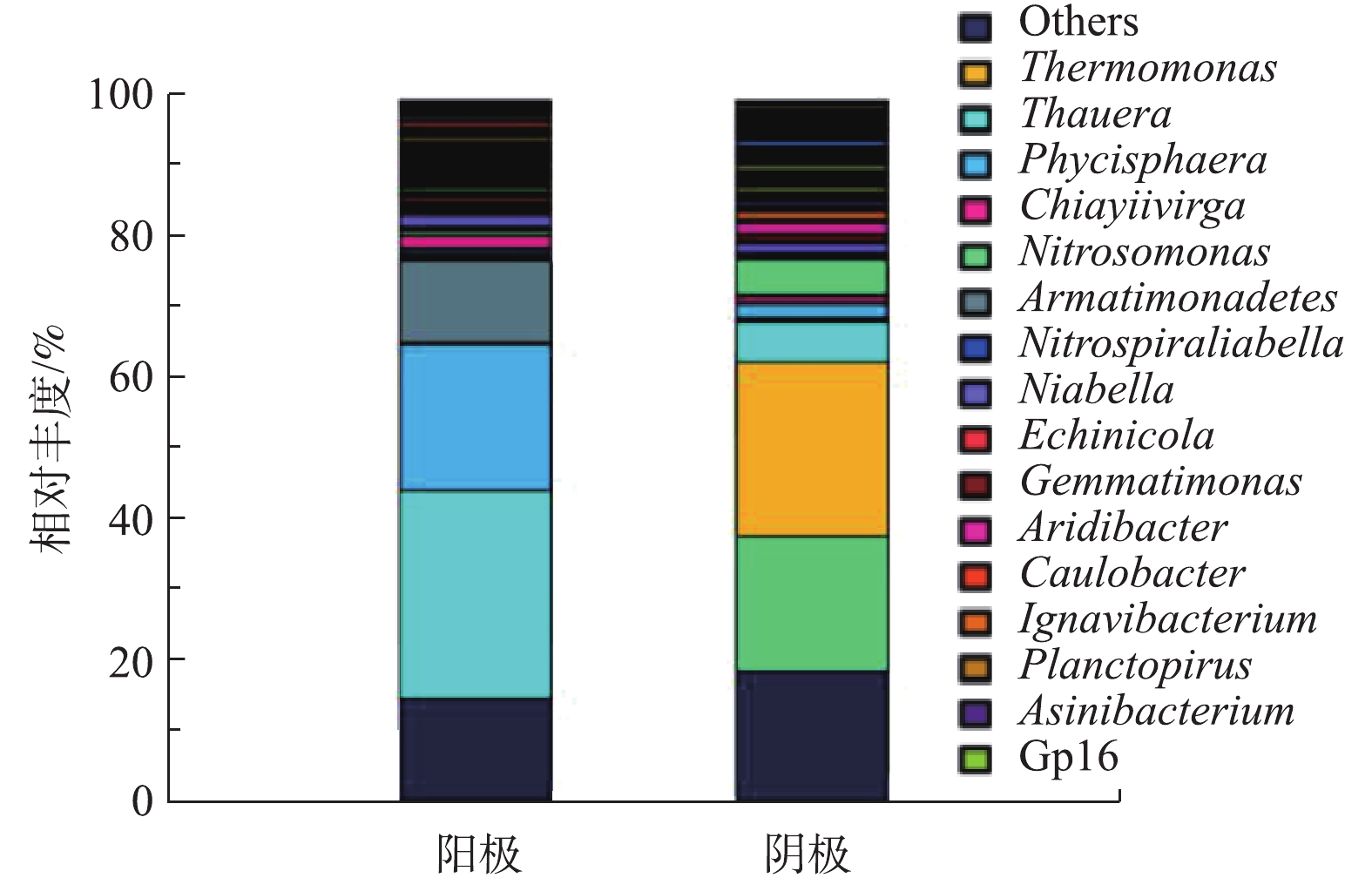
MEC 阳极和阴极生物膜的高通量测序结果如图7所示。从阳阴极生物膜外观上可以看出,阳极生物膜厚度比阴极厚。由图7可知,MEC阳极优势菌群为Thauera、Phycisphaera以及Nitrospiral等,其丰度分别为28.7%、20.8%、16.2%,菌群多样性比较丰富,相对丰度较为均匀。Thauera是一种具有较高电化学活性的微生物菌属[21];Nitrospiral属于亚硝化单胞菌属,其在生物燃料电池中可以促进氨氮厌氧氧化产电[22]。MEC阴极优势菌群为Nitrosomonas和Thermomonas,其丰度分别为18.6%和28.4%。有研究[23]表明,Thermomonas在自养反硝化反应中起到关键作用,在利用无机碳源进行自养反硝化方面具有更强的竞争力。Nitrosomonas菌属是一类能够参与阴极金属还原的菌群,在生物阴极还原方面起到重要作用[24]。
2.1. MEC装置的启动及运行
2.2. DO对MEC处理效果的影响
2.3. 外加电压对脱氮处理效果的影响
2.4. 0.8 V恒定电压下厕所废水浊度去除效果
2.5. 菌群功能分析
-
1)通过构建单室无膜微生物电解池,在间歇曝气条件下处理宜兴某景区尿液废水,并以外加微电压的方式,扩大阳极和阴极间的电势差,可以促进
${\rm{NH}}_4^ + $ -N自身的化学能转化,将其用于阴极的自养反硝化,可以实现脱氮目的。2)控制合适DO浓度对MEC的稳定运行至关重要,本研究通过间歇曝气的方法可实现在微电压条件下的脱氮。
3)随着MEC外加电压的逐渐增加,
${\rm{NH}}_4^ + $ -N的去除率由70.33%升高至99.71%,TN的去除率由50.41%升高至70.51%。这说明在一定范围内,外加微电压能够有效促进反应的进行。4) 16S rDNA分子生物学分析结果表明,在该体系中,Nitrosomonas菌属对厕所废水脱氮起到了主导作用。





 下载:
下载: