-
近年来,由于人口的增长和污水处理厂的扩建,污泥的数量大大增加,成为污水处理的主要副产物[1]。欧盟每年至少产生5000万t含水率约为80%的污泥[2],而我国污泥年产量也达到3200 — 5200万t,并以每年约10%的速度增长[3]。污泥中通常含有多种有毒物质,如重金属、难降解有机物、寄生虫卵和致病性微生物。因此,安全有效处理处置污泥至关重要[4]。近年来,热解已发展成为一种安全可持续的污泥处理技术[5],这是因为热解技术不仅可以减少污泥体积、杀死污泥病原微生物,还可以生成可利用的热解气、液态生物燃料和污泥生物炭[6]。污泥生物炭是污泥热解后产生的固体碳质残渣[7],由于其具有比表面积较大、孔隙结构复杂和表面官能团丰富等特点[8],目前已被广泛地应用为土壤改良修复剂[7, 9]和水处理吸附剂[10],且具有更为广阔的应用潜力。然而研究表明,污泥热解后80%的重金属都富集在污泥生物炭中[11],这是由于热解温度(300—600 °C)低于污泥中大多数重金属化合物的沸点,因而大部分重金属残留于污泥生物炭中并造成重金属的富集[12];且污泥生物炭中的重金属可能在酸雨等特定环境条件下,由于pH的变化而浸出,这将导致对环境的进一步污染[13];释放的重金属也可以通过食物链迁移,对人类健康构成威胁[14]。如何将重金属固定在污泥生物炭中使其不易释放一直是污泥无害化处理和资源化利用的难题。有研究表明,污泥生物炭的重金属固定效率依赖于其特定的化学形态[15]。因此,深入了解污泥生物炭中重金属形态分布的特征及影响因素,是探索污泥生物炭中重金属固定化新途径的前提[16-17]。
本文将首先总结污泥及污泥生物炭的重金属及其形态分布研究现状,然后从预处理方式、热解条件和添加剂三个方面,来探讨不同参数对污泥热解生物炭的重金属形态分布的影响及机理。
-
当前,对沉积物中重金属的毒性分析常用化学提取方法,根据提取程序的不同可分为单级、 连续提取法。常用的单级提取剂有水、酸溶液、盐溶液和螯合剂,单级提取法适用于快速判断沉积物的重金属污染程度,然而它不能提取出沉积物中不同形态的重金属[18]。连续提取法则是使用一系列提取力度渐增的提取剂来提取沉积物中不同化学形态的重金属,并应用ICP等仪器测定各形态的含量,目前使用最广泛的是Tessier5步连续提取法以及欧共体标准物质局(Community Bureau of Reference)提出的 BCR三步提取法[19]。
-
重金属的生物有效性指重金属能被生物吸收或对生物产生毒性的性状[20]。 研究表明,重金属的化学形态在很大程度上决定了重金属的迁移率、生物有效性和生态毒性[21- 22]。Huang等[15]总结了基于BCR法和Tessier法的重金属的化学形态与其生态毒性和生物有效性之间的关系,如表1所示。其中改进的BCR法中的酸提取态与Tessier 5步法中的可交换态及碳酸盐结合态之和相对应[15]。为了便于说明,本文后续提到的重金属形态分析均采用BCR提取法。BCR法提取的四种重金属形态的生物有效性和生态毒性依次下降:F1 > F2 > F3 > F4 [12]。
-
近年来,多种重金属污染风险评价指标被应用在各种关于污泥热解生物炭的重金属风险评估的研究中[15],最常用的3种重金属污染风险评价方法归纳如表2所示,其中的潜在生态风险因子(ER)和潜在生态风险指数(RI)的公式包含了(F1+F2+F3)/F4,因此在一定程度上可以反映出重金属形态变化的情况:ER和RI的值越大,表明污泥生物炭中的重金属潜在生态风险越高,即不稳定形态的重金属含量占总量的百分比越高;而风险评估指数(RAC)则是反映单一重金属的F1形态含量的变化情况。
-
近年来,重金属因其对全球环境和人类健康的不良影响而受到人们广泛的关注,重金属的存在限制了污泥在生产生活中的应用[24]。锌(Zn)、铜(Cu)、镍(Ni)、铅(Pb)、铬(Cr)、镉(Cd)、砷(As)、锰(Mn)以及汞(Hg)等重金属是限制污泥用途的主要元素[25]。研究发现,污泥中重金属含量一般随着城市规模的增大而增多[26]。如表3所示为近五年来一些研究中的市政污水污泥中的重金属含量,一般而言,市政污泥中的锌、铜和铬的浓度最高,其次是镍、锰和铅,而镉、砷和汞的含量则相对较低[27]。市政污水污泥中Zn的含量在绝大多数研究中是最多的,这可能与产业大规模使用镀锌管道等因素有关[14, 17]。
重金属的迁移率、生物有效性及其生态毒性,都强烈依赖于其化学形态[36]。因此,研究污泥生物炭中重金属的化学形态是十分重要的[16-17]。需要对污泥生物炭中的重金属形态分布及转化行为进行研究,以期为污泥的处理处置提供一定的参考和依据[25]。如图1为近5年来研究的市政污水污泥重金属的形态分布,市政污水污泥分别取自石河子市[17]、辽宁某市[37]、西安市[38]、广州市[39]、厦门市[12]、乌鲁木齐市[40]、山东省某市[25]、哈尔滨市[33]、上海市[13]以及浙江临安市[14]的污水处理厂。
污泥的重金属形态分析表明,Cu主要以可氧化形态(F3)存在; Zn和Cd主要以酸提取态(F1)和可还原态(F2)存在; Pb主要以残渣态(F4)存在; Cr和Ni主要以可氧化态(F3)和残渣态(F4)存在。其中不具备生态毒性和生物有效性的残渣态含量百分比:Cu约为1.12%—64.08%,Zn约为0.73%—41.61%,Ni约为8.02%—68.95%,Cr约为17.41%—88.38%,Cd约为20.75%—98.06%,Pb约为5%—100%。这些结果表明,污泥中Zn和Cd的生物有效性较强,Cu、Cr和Ni的生物有效性次之, Pb的生物有效性较弱。不同文献中污泥的重金属形态分布略有差异,这种差异可能与不同的污泥类型有关[25]。
-
污泥生物炭中的重金属含量一般要高于原污泥,即污泥中的重金属富集在污泥生物炭中[11, 38, 41]。这主要是因为热解温度(300—600 °C)低于大多数重金属化合物的沸点,污泥中的有机物热稳定性要高于重金属[25],有机物转化为气态或液态的转化率约为30%—50% [6, 42],使得污泥中的有机物转化高于重金属的挥发逸出,因而大部分重金属仍残留在污泥生物炭中[12]造成了重金属的富集。污泥生物炭中大部分重金属(如Cu、Cr、Zn、Ni、Mn)的残留率在80%以上[11, 38, 43],而Cd、Pb、Hg等重金属在较高温度下(>600 °C)的残留率会低于80% [44],这是由于沸点较低的重金属在较高热解温度下变成金属蒸汽挥发逸出,在热解温度高于600 °C时,重金属的热挥发性依次为Cu < Cr < Ni < Mn < Pb < As < Zn < Cd≈Hg[30]。重金属的迁移转化特性主要由其各自的沸点及其对应的形式决定[39],因此相对沸点较低的金属(如Pb、Zn和Cd)比沸点较高的金属(如Ni、Cr和Cu)更容易从热解反应过程中被去除[39]。
将污泥中的重金属固定在污泥热解炭中以降低重金属释放到环境中的潜力被称为重金属固定化[14]。其本质上是将污泥中的重金属从弱的结合形态(F1和F2形态)转化为更稳定的形态(F3和F4形态),这种形态上的转变可称为重金属形态稳定化[16],反之可称为重金属形态活化[17]。研究表明,热解可促进污泥中的酸提取态(F1)、可还原态(F2)的重金属受热分解转化为残渣态(F3)[11],有利于重金属形态的稳定化。改善热解条件可以使得重金属的形态更趋于稳定化,从而大大降低污泥生物炭对环境的生态风险。此外,由于生物质废弃物具有重金属含量低、含碳量高等特点[45],将污水污泥与其它生物质废弃物混合热解可以“稀释”污泥中的重金属含量且增加污泥生物炭的含碳量,而近年的研究表明,某些生物质废弃物与污泥的混合热解甚至可以促进污泥中重金属形态向更稳定的形态转变[40-41]。为了固定化更多的重金属,改良污泥预处理方法、改善热解条件以及加入添加剂与污泥共热解已成为目前的研究热点。
-
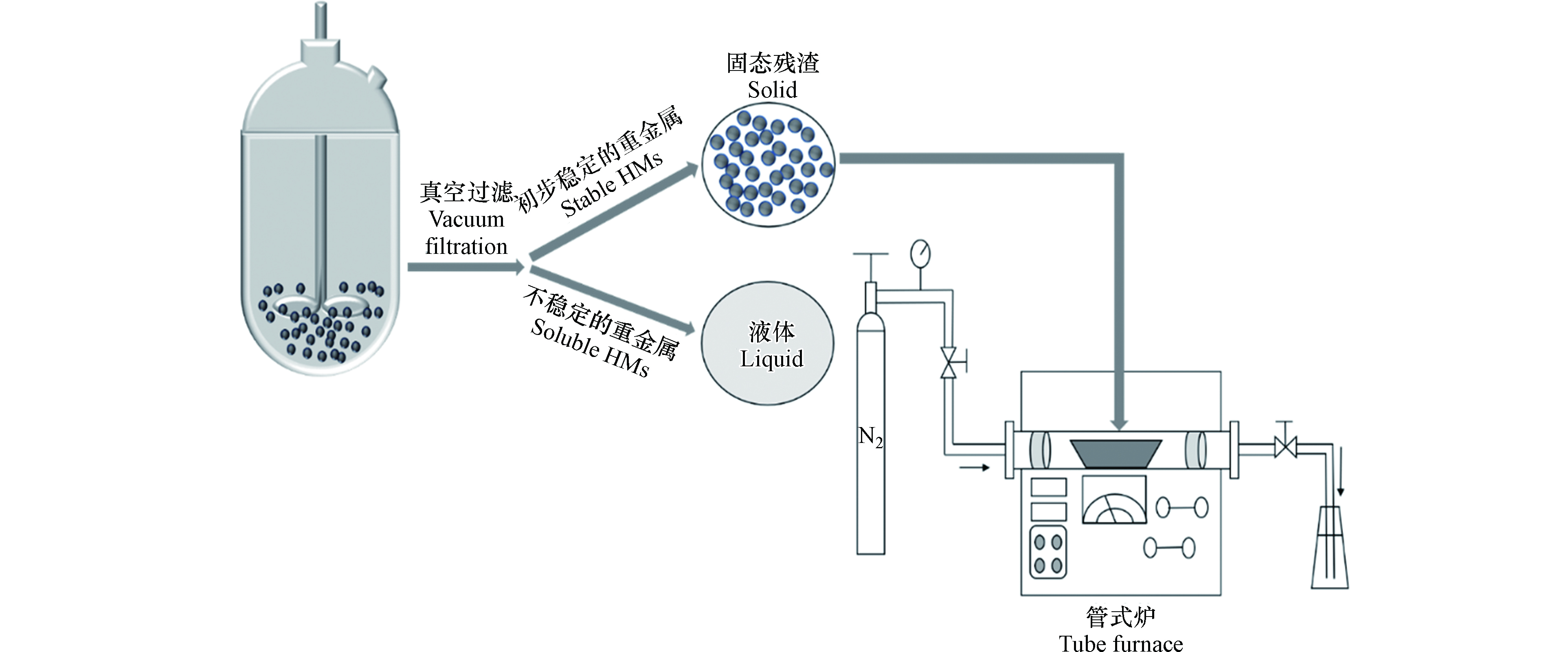
由于污泥含水率高,在热解前需要进行脱水预处理。目前大部分研究均采用在105 °C的烘箱干燥24 h的方法[46],此方法具有操作简单以及安全性强的优点,然而此方法的脱水效率较低且能耗较高[47];近年来,产生了一种新型预处理方法—水热预处理(hydrothermal treatment , HTT):即在低温(150—350 °C)和自压下将污泥样品水热处理一段时间后,再利用热解技术将水热后的固态残渣转化为污泥生物炭[31]。如图2为水热预处理与热解联用流程图。
通过水热预处理,一方面可以增强污泥脱水和减少污泥体积,另一方面,对污泥的预处理比起常规干燥法有更好地稳定污泥热解炭中重金属的效果[48]。Liu等[25]发现,水热预处理后的污泥热解炭与常规干燥预处理后的污泥热解炭相比,水热预处理促进了热解炭中Zn、Cu、Mn、Ni、Pb以及Cr的F1和F2形态向F4形态转化,重金属的F4含量增多了约1.4%—33%,该预处理方法有利于将污泥中重金属的不稳定组分转化为更稳定的组分。Wang等[49]系统研究了HTT工艺对于污泥热解炭中重金属 (Cu、Zn、Cr、Ni、Pb和Cd)的形态分布影响,发现HTT工艺可促进污泥热解炭中Zn、Ni和Cd的酸溶态(F1)和可还原态(F2)组分向可氧化态(F3)和残渣态(F4)组分转化,重金属的F1+F2含量下降13%—20%,大大降低了污泥热解炭中重金属的潜在风险。这些影响可能归因于在HTT过程中重金属的部分酸溶态组分、可还原态组分被提取并释放在液相中[15],而另一些不稳定的重金属组分通过络合、沉淀、吸附或其他反应向更稳定的组分转化并且保留在固体残渣中[25]。综上所述,水热预处理降低了污泥热解炭中部分重金属(Zn、Ni、Cd、Mn以及Cr)的酸提取态和可还原态组分,降低了重金属的潜在风险[25, 50],是一种很有前途的稳定化污泥热解炭中重金属的预处理方法。
-
污泥生物炭的物理化学性质既取决于原料,也取决于热解条件[10]。其中,对污泥生物炭中重金属形态分布产生影响的热解条件主要有热解温度和热解时间。
-
热解温度是决定重金属在生物炭中形态分布的关键因素[12]。随着热解温度的升高,污水污泥中有机物的降解和转化得到了加强,生物炭中重金属的含量也会增加[14];热解温度在一定范围内(300—600 °C)提高有利于污泥中的重金属(Cu、Zn、Mn、Ni、Cd和Pb)从不稳定的形态(F1和F2)转化为相对稳定的形态(F3、F4)[11- 12, 14, 30, 38, 43],从而降低了污泥生物炭中重金属的生物有效性,降低了污泥生物炭潜在的环境风险[14]。
Jin等[14]研究发现,随着热解温度从400 °C 升高到600 °C,污泥热解炭中重金属(Cu、Zn、Cr、Ni、Pb以及Mn)的不稳定形态占稳定形态的比例(F1+F2+F3)/F4降低了53.10%—92.85%,这表明热解温度的升高促进了污泥生物炭中重金属由不稳定形态转化为残渣态,从而大大降低了重金属的潜在风险。Wang等[43]发现随着热解温度由300 °C升高至700 °C,污泥炭中重金属(Cu、Zn、Cr、Ni、Pb以及Mn)的不稳定形态占稳定形态的比例(F1+F2+F3)/F4降低了30%—70%,大大降低了重金属的生物有效性。而Chanaka等[11]研究发现当热解温度由300 °C升高到600 °C时,促进了污泥炭中重金属(Cu、Zn、Ni以及Mn)的F1和F2形态转化为F3和F4形态,即热解温度的升高促进了重金属向稳定的形态转化;然而当热解温度继续升高至700—800 °C时,重金属由稳定形态(F3、F4)转化为不稳定形态(F1、F2),这与高温(700 °C以上)促进重金属卤化物的生成有关。
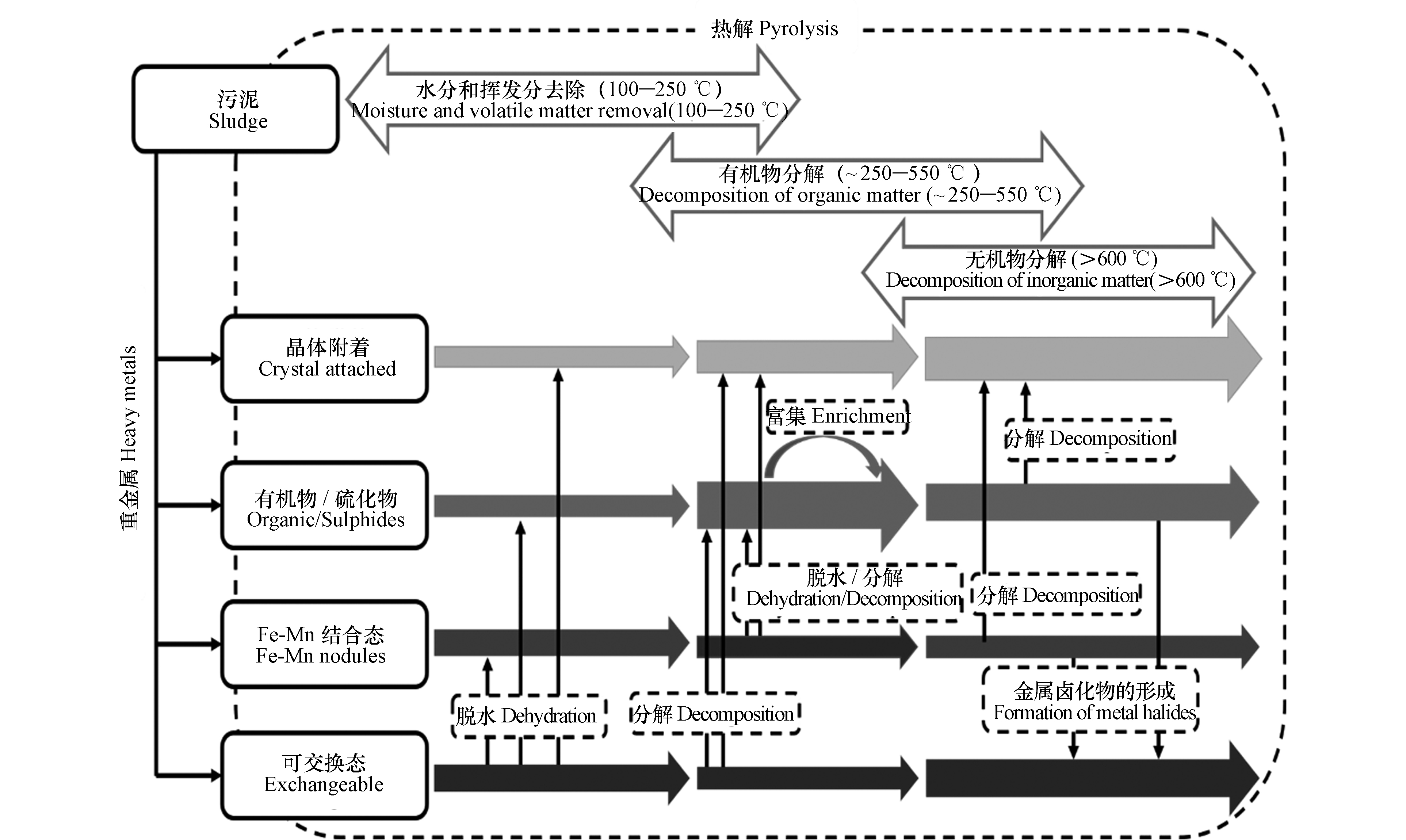
Chanaka等[11]提出了图3所示的污泥热解过程中重金属形态转化示意图。当热解温度升至100—250 °C时污泥处于水分和挥发分去除阶段,污泥中的重金属(Mn、Ni、Cu、Zn、Cd和Pb)由于脱水效应从F1形态向更稳定形态转变,这可能是由于热解过程中间隙水、毛细管水和吸附水的消除促进污泥炭中的重金属由无定形矿物转化为晶体稳定形态[51],由于脱水导致的局部金属离子环境和键合结构的变化可能是导致形态转化的分子机制[52];当温度升至250 —550 °C时,会发生F1形态的重金属分解以及Fe-Mn结合态重金属的脱水或分解,均可以使得重金属的形态趋于稳定化转变;当热解温度>600 °C时,无机物大量分解,Fe-Mn化合物与有机物/硫化物中的重金属释放转化为晶体稳定形态,然而此时含氟化合物的各种反应导致金属卤化物的形成,可能将Mn、Zn和Cu的F2和F3组分转化为F1组分。并且在热解温度>600 °C时,部分重金属分解会进入热解油和热解气中,造成更大的环境风险,不利于重金属在固体残渣中的固定化[53]。
综上所述,污泥在适当的温度(300—600 °C)下进行热解,污泥生物炭中的重金属的形态可由酸溶态/可还原态转化为更稳定的可氧化性/残渣态形式,大大降低生物炭中的重金属毒性。其中,在600 °C左右的温度下热解污泥是在大多数情况下的最适宜温度[14, 38]。
-
热解时间是影响污泥生物炭重金属形态分布的另一个重要因素,污泥生物炭中重金属的富集和形态的转化都需要一定的时间来完成[29]。一般而言,较长的热解时间有利于污泥生物炭中重金属的富集[54],在不同的热解温度条件下,热解时间对重金属在生物炭中的富集效果不同:Xu等[55]发现在700 °C随着热解时间从1 h延长到4 h,重金属(Cu、Zn、Cr、Mn 和Ni)在污泥炭中富集。而在800 °C时,随着热解时间的增加Cr、Ni和Cu的总量略有增加,而Zn、Pb和Cd的总量则有所减少[29],如前所述,这取决于重金属的挥发性和质量损失。
热解时间的延长促进了生物炭中重金属形态的稳定化[54],这是由于较长的停留时间能够提供更多的能量进而促使更多的F1形态的重金属分解转化为其他形态[13]。在不同的反应温度下,反应时间对污泥生物炭中重金属形态的影响是不同的。Wang等 [54]研究发现,延长热解时间(600 °C,30—150 min)促进了污泥生物炭中的Ni、Zn、Cd、Pb的F1、F2、F3形态转变为F4,Cu、Cr形态由F1、F2转变为F3、F4,重金属F4形态的比例可由5%—70%(30 min)提高至50%—95%(150 min),因而大大降低了生物炭中重金属的潜在环境风险。Xu等[55]研究发现:延长热解时间(700 °C,1—2 h)有利于重金属(Zn、Cu、Pb、Ni、Mn以及Cr)由F1形态转变为F4形态,F1形态的比例随着热解时间的增加降低了46.0%—80.1%;当热解时间继续延长(2—4 h),Pb和Mn的部分稳定形态(F3、F4)转变为了酸溶态(F1),这可能与这两种重金属挥发性较强有关,这一结果与Diao等[56]的发现相反,Diao等发现当热解时间由1 h增加到4 h(700 °C)时,Zn、Pb、Mn和Ni的稳定形态(F3+F4)比例由50%—80%增加至55%—95%,此条件下稳定化效果最佳。
热解时间是影响污泥热解炭重金属形态分布的一个重要因素,热解时间过短,会导致污泥热解不充分,重金属的形态转化所需的时间以及能量不足,不利于污泥生物炭的重金属稳定化[29];而热解时间过长则会降低污泥处理效率,消耗能源与财力,更严重的结果是促使重金属挥发到液相、气相当中去, 造成更大的环境污染[57]。然而目前为止,关于停留时间对污泥热解过程中重金属组分转化的影响的研究还非常有限[58]。为了在污泥的无害化和资源化利用中达到相对平衡,寻求合适的热解停留时间具有重要意义。
-
将废弃生物质与污水污泥共热解是可持续资源回收的可行策略。废弃生物质主要包括农业废弃物和林业废弃物。一般来说,生物炭中重金属含量随着生物质添加量的增加而降低,主要是由于添加生物质引起的“稀释效应”[59]。更重要的是,近年来研究人员发现:一些废弃生物质的添加可以促使生物炭中重金属的流动组分(F1、F2)向稳定组分(F3、F4)的转化,进而增强重金属的固定化作用,达到降低重金属毒性和风险的目的。如表4所示为近几年来对污水污泥与农林废弃物共热解过程中重金属的迁移转化行为,稻壳[41]、棉花秸秆[40]、竹木屑[16]、榛子壳[28]及核桃壳[23]等农林废弃物对污泥共热解过程中金属形态稳定化具有协同作用,促进了污泥生物炭中重金属的F4形态含量的提高。然而,也有文献表明稻草[58]、杉木屑[60]与污泥共热解对生物炭的重金属形态分布无明显改变。可见由于农林废弃物的组成不同,在污泥和农林废弃物共热解过程中对不同种类重金属的影响也可能不同。
目前在污泥热解过程中添加不同农林废弃物对生物炭重金属形态转化的机理研究尚不够深入,图4总结了农林废弃物与污泥共热解形成的生物炭重金属稳定化机理,主要有以下四点:1)热解装置内形成还原性气氛,铁、锰氧化物被还原[64],重金属的碳酸盐会发生分解[16, 58],与之结合的重金属(F1、F2)被释放;在共热解过程中,更多的有机质分解为酚类、酸类和芳香族化合物[41],在生物炭表面富集大量的官能团(羧基、羟基、酚羟基、酰胺[65]等)[66]。这些官能团可以通过配位反应与重金属络合形成强而稳定的配合物(如F3) [40]。从而导致重金属形态F1、F2减少,F3形态增加。2)与污泥生物炭相比,共热解制得的生物炭具有更大的芳香团簇[12]。降低了污泥基生物炭的亲水性[67],导致重金属的流动性降低;芳香结构可以提供π电子与重金属离子键合[12],从而达到固定重金属的目的[61]。3)共热解过程中生物质废弃物的引入促进了还原性气氛的产生,导致重金属矿物盐和氢氧化物转化为具有高热稳定性的氧化物或硫化物[39, 54]。4)添加生物质废弃物与污泥共热解产生的生物炭结构更加疏松多孔、比表面积和微孔体积增大,可以吸附和再稳定部分释放的重金属[58];Xiao等[68]揭示了稻壳衍生生物炭中存在C-Si-C结构。Jin等[69]也发现,污泥生物炭中有机组分与无机组分的结合。因此部分重金属可能被封装在生物质与污泥形成的特殊结构中[16]。
在污泥热解过程中加入其他生物质是否能对污泥基生物炭的重金属稳定化产生协同效应,且生物质废弃物中的纤维素、木质素以及半纤维素的含量对于稳定化污泥生物炭中的重金属形态分布的影响有待进一步研究。
-
催化剂在污泥热解过程中起着重要作用,部分催化剂不仅可以显著提高污泥生物炭的特性,而且可以改变生物炭中重金属的形态分布特性[70]。污泥热解中催化作用可以分为内催化和外催化两个部分:内催化主要由污泥自身所含的无机矿物质(CaO、Fe2O3、SiO2、Al2O3及TiO2等)引起[71],例如重金属氧化物与 CaO 都能与 CO2反应,从而影响重金属碳酸盐结合态(F1)的含量[72];酸性气体可与无机组分如Al2O3、SiO2、Fe2O3和TiO2反应形成共结晶化合物(F4)[73],从而促进了重金属形态的稳定化。外催化剂则为外部添加CaO [32, 72, 74]、Fe2O3 [72]、CaSO4 [70]以及Ca-膨润土[32]等。近几年来,有少数学者研究了其他的新型催化剂包括抗生素菌渣[75]、重金属[13]、塑料[76]及挖掘废渣[31]等。这些外部催化剂对污泥生物炭中的重金属具有稳定化作用,可以不同程度地降低生物炭中重金属的浸出,促进重金属形态从不稳定态向稳定态转化[72];然而也有少数催化剂(如CaSO4、CuCl2以及聚氯乙烯)对于污泥炭中个别重金属(如Cu、Ni以及Cr)具有活化作用,促进了重金属形态由F4的稳定态向F1、F2转变[13, 70, 76]。近年来催化剂对于污泥重金属形态转化的影响如表5所示。
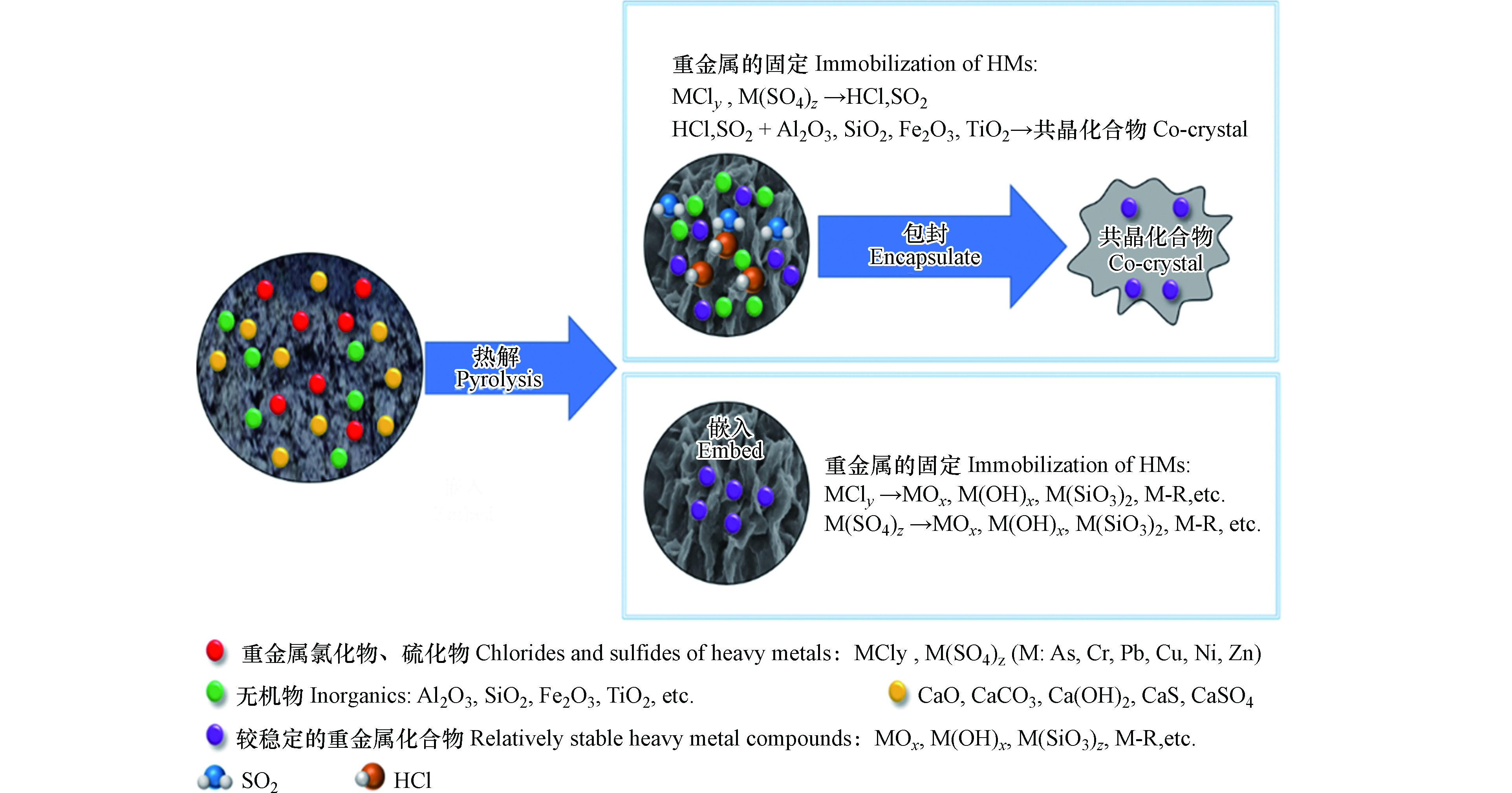
目前在污泥热解过程中添加不同催化剂对污泥生物炭重金属形态转化的机理尚且有限,Liu等[70]以CaSO4作为污泥热解催化剂,研究发现CaSO4在热解过程中,可以与污泥形成具有高强度和化学稳定性的晶体[77],从而促进重金属的固定化。污泥中的无机物可催化CaSO4分解生成CaS、CaO、CaCO3和Ca(OH)2 [72],可以促进更多的重金属固化。如图5所示是碱性催化剂(CaO、CaSO4、CaCO3、 Ca(OH)2及CaS)的机理图。1)重金属的氯化物、硫化物可以与CaO反应生成M(OH)x、MOx以及M(SiO3)2沉淀,CaO促进了污泥炭孔洞的发育,热解后镶嵌在生物炭的孔洞里;2)部分重金属氯化物、硫化物在催化热解作用下生成的酸性气体(HCl、SO2)可与无机组分(Al2O3、SiO2、Fe2O3、TiO2)反应形成共结晶化合物[73],从而包封重金属,促进污泥生物炭中重金属F4形态含量的提高。
如何避免催化剂活化污泥炭中的部分重金属有待进一步研究,制备对重金属具有稳定的固定化效果的新型催化剂以及多种催化剂复配,是今后的研究重点。
-
本文从污泥及污泥生物炭的重金属含量及形态分布研究现状出发,总结了预处理方式、热解条件以及添加剂三方面对于污泥生物炭的重金属形态分布转化的影响,重点分析了农林废弃物与催化剂对于污泥生物炭中重金属形态转变的机理。
研究发现,采用水热预处理的方式可以降低污泥生物炭中重金属的酸提取态(F1)和可还原态(F2)组分,从而初步稳定重金属;一般来说,增大热解温度(≤600 °C)以及适当延长热解时间可以促进污泥生物炭中的重金属赋存形态转变为更稳定形态;添加高木质素和纤维素含量的农林废弃物(如稻壳、榛子壳和棉花秸秆等)以及添加碱性催化剂(如Ca(OH)2、CaO和CaCO3等)可以促进重金属形态的稳定化。然而对于上述影响因素的研究大多停留在实验现象阶段,不同影响因素对于污泥生物炭重金属形态变化的机理需要进一步研究。
近年来,污泥热解生物炭的重金属形态分布的研究不断地取得进展,但目前的研究尚且有限,在以下几个方面的研究还需进一步完善:1)其他热解条件对于重金属形态分布的影响:如热解方式、升温速率、热解气氛、气体通入速率以及加热阶段(一段热解、二段热解);2)开发新型添加剂:其他的农林废弃物、微藻类以及复配催化剂的添加对于污泥热解处理过程中重金属形态分布的影响;3)对于污泥热解生物炭的重金属浸出能力与其形态分布的关系研究还不够深入,对于改性污泥热解生物炭的重金属形态分布也需要广泛研究。
污泥热解生物炭中重金属化学形态分布的影响因素研究进展
Research progress on influence factors on heavy metals chemical speciation distribution in sludge pyrolysis biochar
-
摘要: 重金属生态风险问题一直制约着污泥及污泥热解生物炭的资源化利用,而重金属生态风险在很大程度上取决于其化学形态。近年来,污泥及其生物炭的重金属形态分布研究得到了广泛关注,已成为当前环境科学的研究热点。本文首先综述分析了市政污水污泥的重金属含量及其形态分布特征,然后从预处理方式(常规干燥、水热)、热解条件(温度、时间)以及添加剂(农林废弃物、催化剂)三方面分析了影响污泥热解生物炭的重金属形态分布关键因子及机理,通过调控这些影响因素可以促进污泥生物炭中的重金属由不稳定形态(酸提取态F1及可还原态F2)向稳定形态(可氧化态F3和残渣态F4)转变,从而降低污泥生物炭的重金属潜在生态风险。最后,基于研究现状提出了未来的研究方向。本文可为进一步研究污泥热解生物炭的重金属固定化提供重要参考。Abstract: The ecological risk of heavy metals has been restricting the resource utilization of sludge and its pyrolytic biochar. And the risk depends on the chemical speciation of heavy metals. Recently, the research on the speciation distribution of heavy metals in sludge and biochar has received extensive attention, which becomes a research hotspot in environmental science. This paper reviewed the analysis of the heavy metal content of sewage sludge and its distribution characteristics. And then the key factors and mechanism affecting the speciation distribution of heavy metals in sludge pyrolysis biochar were analyzed from three aspects: pretreatment methods (conventional drying, hydrothermal pretreatment), pyrolysis conditions (temperature, time) and additives (agricultural, forestry wastes and catalysts). By adjusting these influencing factors, the heavy metal speciation of sludge biochar can be changed from unstable forms (exchangeable and acid soluble fraction F1 and reducible fraction F2) to stable forms (oxidizable fraction F3 and residual fraction F4). So this reduces the potential ecological risk of heavy metals in sludge biochar. Finally, the future research direction was proposed based on the current research. This paper provides an important reference for the further study on the immobilization of heavy metals in sludge pyrolysis biochar.
-
Key words:
- sludge biochar /
- pyrolysis /
- heavy metal /
- chemical speciation /
- mechanism
-

-
表 1 Tessier法及改进的BCR法的生态毒性与生物有效性[12, 15]
Table 1. Chemical forms, ecotoxicity and bioavailability of heavy metals by Tessier and Improved BCR methods[12, 15]
Tessier 5 步法
Tessier 5 steps method改进BCR法
Improved BCR method生态毒性及生物有效性
Ecotoxicity and bioavailability可交换态(F1) 酸提取态(F1) 直接的生态毒性及生物有效性 碳酸盐结合态(F2) 铁锰氧化物结合态(F3) 可还原态(F2) 直接的生态毒性及生物有效性 有机硫化物结合态(F4) 可氧化态(F3) 潜在的生态毒性及生物有效性 残渣态(F5) 残渣态(F4) 几乎不具备生态毒性和生物有效性 表 2 污泥热解过程中的重金属污染程度及生态风险评价指标
Table 2. Various assessment indices applied to evaluate the contamination and ecological risk of heavy metals during the pyrolysis treatment of sewage sludge
指数名称
Index name描述
Description分类
Category参考文献
References潜在生态风险因子(ER):
单一重金属的生态风险$ {C}_{f}={C}_{i}/{C}_{n} $ $ {E}_{r}={T}_{r}\times {C}_{f} $
式中,$ {C}_{f} $ $ {C}_{i} $ $ {C}_{n} $ $ {T}_{r} $
毒性响应因子ER≤40 低风险
40<ER≤80 中等风险
80<ER≤160 相当大风险
160<ER≤320 高风险
320<ER 极高风险[15] 潜在生态风险指数(RI):
多种金属生态风险$ \mathrm{R}\mathrm{I}=\displaystyle\sum _{n=1}^{n}{E}_{r}^{n} $
式中,n为重金属的种类数RI≤150 低风险
150<ER≤300 中等风险
300<ER≤600 相当大风险
600<RI 高风险[14] 风险评估指数(RAC):
单一重金属生态风险$ \mathrm{R}\mathrm{A}\mathrm{C}=\frac{{C}_{{\rm{F}}1}}{\displaystyle\sum _{i=1}^{n}{C}_{{\rm{F}}i}}\times 100\% $
式中,$ {C}_{{\rm{F}}1} $ $ \displaystyle\sum _{i=1}^{n}{C}_{Fi} $ RAC≤1% 无风险
1%<RAC≤10% 低风险
10%<RAC≤30% 中等风险
30%<RAC≤50% 高风险
50%<RAC 极高风险[23] 表 3 市政污水污泥中的重金属含量(mg·kg-1)
Table 3. Heavy metals’ contents in municipal sewage sludge
类型
TypeCu Zn Cd Cr Ni Mn Pb As Hg 参考文献References 市政污水污泥 117.53 666.67 6.30 61.38 77.27 — 110.28 — — [28] 4917.58 6709.81 5.26 5469.95 752.25 — 62.95 — — [29] 279.71 1287.83 1.78 103.82 33.91 227.91 59.77 15.66 1.33 [30] 181.70 1126.28 4.58 150.65 140.79 811.53 150.72 — 3.10 [25] 571.05 2649.72 — 442.62 115.05 — 26.77 — — [31] 290.97 1202.18 — 416.02 40.62 — 41.45 16.21 — [32] 266.06 1345.51 2.12 514.24 84.64 1065.83 — — — [17] −1200 −2500 — −500 −100 −750 −90 — — [16] 925.60 2956.90 — 59.70 24.50 — 57.50 — — [13] 3323.90 2424.20 1.65 1983.80 422.00 — 69.70 — — [12] 1217.71 2579.81 — 449.21 112.10 748.31 95.11 — — [14] 127.9 1055.2 3.4 74.8 30.3 — 30.4 — — [33] 498.4 1548.7 1.6 424.5 203.4 624.7 — 25.1 — [34] 6.56 441.23 0.38 17.22 141.63 — 2.36 — — [35] 含量范围 5—5000 400—7000 0.3—10 15—5500 20—800 200—1100 2—160 −20 −3 表 4 污泥与农林废弃物共热解过程中重金属形态分布行为
Table 4. Speciation and distribution of heavy metals during the co-pyrolysis of sludge and agricultural and forestry wastes
生物质
Biomass重金属
Heavy metals添加量/%
Addition rate热解温度/°C
Temperature主要工作
Main work参考文献
References稻壳 Cu、Zn、Pb、Cr、Mn、Ni 50 400 、700 纯污泥炭RI=432,稻壳-污泥炭RI=40 [41] 稻草 Cu、Zn、Pb、Cr、Cd、Ni 10—40 600 Cu:F4比例提高5%—10%,Cd:F4比例提高20%—50% [61] 棉花秸秆 Cu、Zn、Pb、Cr、Ni、Mn 50 300—600 污泥炭RI=30.83—52.88,棉花秸秆-污泥炭RI=4.81—6.11 [40] 玉米秸秆 Cu、Zn、Pb、Ni、Cr、Mn 25—75 600 Mn、Ni、Pb:F4比例提高5%—20% [62] 榛子壳 Cu、Zn、Pb、Cr、Cd、Ni 50 300—700 F1、F2→F3、F4,RI=147.31—339.54 [28] 竹木屑 Cu、Zn、Pb、Cr、Mn、Ni 50 400—600 F1、F2、F3→F4,污泥炭RI=109.1—425.3,竹木屑-污泥炭RI=43.1—92.1 [16] 核桃壳 Cu、Zn、Cd、Cr、Ni 20 500 Cu、Ni、Cr:F1、F2→F3、F4
污泥炭RAC=0.74%—43.32%,核桃壳-污泥炭RAC=0.62%—38.7%[23] Pb 、Cu、Zn、Cr、Ni 5、7、9 350—600 污泥炭RI=5.81,核桃壳-污泥炭RI=4.95 [63] 表 5 近年来催化剂对于污泥重金属形态分布的影响
Table 5. Effect of catalysts on the speciation and distribution of heavy metals in sludge in recent years
催化剂 Catalyst 主要成分
Main component添加量/%wt
Addition rate形态转化
Form transformation主要工作
Main work参考文献
ReferencesCaO
Fe2O3__ 10 F1、F2、F3→F4 (Zn、Pb、Cr、Cu、Ni、Cd) RI = 28.19—48.76(无催化剂)
RI = 15.17—20.43(CaO)
RI = 16.88—21.79(Fe2O3)[72] CaSO4 __ 2.5、5、7.5、10、12.5、15 F1、F2→F4(Zn、Pb、Cr)
F4→F1、F3(Cu)
F4→F1、F2、F3(Ni)Cr、Pb、Cu、Ni 和Zn (F3+F4)/总量:
97%、89%、100%、87%和54%[70] CaO
高岭土
Ca-膨润土SiO2、Al2O3 20 F1、F3→F4(Ni)
F3→F4(Pb)
F1、F2→F4(As)RI = 7.55—9.13(CaO)
RI = 8.14—11.10(高岭土)
RI = 10.67—12.57(Ca-膨润土)[32] CuCl2 __ 0.5、0.6、0.8、1.0 F1、F2→F3、F4(Pb、Ni)
F3→F4(Zn)
F4→F2、F3(Cr)(F3+F4)/总量:Cr降低10%,
Ni提高13%[13] 挖掘废渣 复杂有机物以及营养物质 25 F1、F2→F3、F4(Cr、Cu、Zn) RI由116.8降至50以下 [31] 抗生素菌渣 抗生素、蛋白质、脂肪以及糖 10、25、50 F1、F2、F3→F4(Cu、Zn)
F1、F2→F3、F4(Ni、Cd、Pb)RI由131.47降至75.55 [75] 塑料 聚乙烯、聚丙烯、聚苯乙烯、聚氯乙烯 20 F1、F2→F3、F4(Cr、Ni、Cu、Zn、Cr) RI:污泥炭=107.86
塑料-污泥炭=71.48—105.27[76] -
[1] GENG H, XU Y, ZHENG L K, et al. An overview of removing heavy metals from sewage sludge: Achievements and perspectives [J]. Environmental Pollution, 2020, 266: 115375. doi: 10.1016/j.envpol.2020.115375 [2] WANG L P, CHANG Y Z, LI A M. Hydrothermal carbonization for energy-efficient processing of sewage sludge: A review [J]. Renewable and Sustainable Energy Reviews, 2019, 108: 423-440. doi: 10.1016/j.rser.2019.04.011 [3] YANG G, ZHANG G M, WANG H C. Current state of sludge production, management, treatment and disposal in China [J]. Water Research, 2015, 78: 60-73. doi: 10.1016/j.watres.2015.04.002 [4] NGO P L, UDUGAMA I A, GERNAEY K V, et al. Mechanisms, status, and challenges of thermal hydrolysis and advanced thermal hydrolysis processes in sewage sludge treatment [J]. Chemosphere, 2021, 281: 130890. doi: 10.1016/j.chemosphere.2021.130890 [5] SHARMA H B, SARMAH A K, DUBEY B. Hydrothermal carbonization of renewable waste biomass for solid biofuel production: A discussion on process mechanism, the influence of process parameters, environmental performance and fuel properties of hydrochar [J]. Renewable and Sustainable Energy Reviews, 2020, 123: 109761. doi: 10.1016/j.rser.2020.109761 [6] GAO N B, KAMRAN K, QUAN C, et al. Thermochemical conversion of sewage sludge: A critical review [J]. Progress in Energy and Combustion Science, 2020, 79: 100843. doi: 10.1016/j.pecs.2020.100843 [7] WANG J L, WANG S Z. Preparation, modification and environmental application of biochar: A review [J]. Journal of Cleaner Production, 2019, 227: 1002-1022. doi: 10.1016/j.jclepro.2019.04.282 [8] LI Y H, CHANG F M, HUANG B, et al. Activated carbon preparation from pyrolysis char of sewage sludge and its adsorption performance for organic compounds in sewage [J]. Fuel, 2020, 266: 117053. doi: 10.1016/j.fuel.2020.117053 [9] YUE Y, CUI L, LIN Q M, et al. Efficiency of sewage sludge biochar in improving urban soil properties and promoting grass growth [J]. Chemosphere, 2017, 173: 551-556. doi: 10.1016/j.chemosphere.2017.01.096 [10] STREIT A F M, CÔRTES L N, DRUZIAN S P, et al. Development of high quality activated carbon from biological sludge and its application for dyes removal from aqueous solutions [J]. Science of the Total Environment, 2019, 660: 277-287. doi: 10.1016/j.scitotenv.2019.01.027 [11] W D C U, VEKSHA A, GIANNIS A, et al. Insights into the speciation of heavy metals during pyrolysis of industrial sludge [J]. Science of the Total Environment, 2019, 691: 232-242. doi: 10.1016/j.scitotenv.2019.07.095 [12] WANG X D, CHI Q Q, LIU X J, et al. Influence of pyrolysis temperature on characteristics and environmental risk of heavy metals in pyrolyzed biochar made from hydrothermally treated sewage sludge [J]. Chemosphere, 2019, 216: 698-706. doi: 10.1016/j.chemosphere.2018.10.189 [13] CHEN F F, HU Y Y, DOU X M, et al. Chemical forms of heavy metals in pyrolytic char of heavy metal-implanted sewage sludge and their impacts on leaching behaviors [J]. Journal of Analytical and Applied Pyrolysis, 2015, 116: 152-160. doi: 10.1016/j.jaap.2015.09.015 [14] JIN J W, LI Y N, ZHANG J Y, et al. Influence of pyrolysis temperature on properties and environmental safety of heavy metals in biochars derived from municipal sewage sludge [J]. Journal of Hazardous Materials, 2016, 320: 417-426. doi: 10.1016/j.jhazmat.2016.08.050 [15] HUANG H J, YUAN X Z. The migration and transformation behaviors of heavy metals during the hydrothermal treatment of sewage sludge [J]. Bioresource Technology, 2016, 200: 991-998. doi: 10.1016/j.biortech.2015.10.099 [16] JIN J W, WANG M Y, CAO Y C, et al. Cumulative effects of bamboo sawdust addition on pyrolysis of sewage sludge: Biochar properties and environmental risk from metals [J]. Bioresource Technology, 2017, 228: 218-226. doi: 10.1016/j.biortech.2016.12.103 [17] LI Z J, DENG H, YANG L, et al. Influence of potassium hydroxide activation on characteristics and environmental risk of heavy metals in chars derived from municipal sewage sludge [J]. Bioresource Technology, 2018, 256: 216-223. doi: 10.1016/j.biortech.2018.02.013 [18] SAKAN S, POPOVIĆ A, ŠKRIVANJ S, et al. Comparison of single extraction procedures and the application of an index for the assessment of heavy metal bioavailability in river sediments [J]. Environmental Science and Pollution Research, 2016, 23(21): 21485-21500. doi: 10.1007/s11356-016-7341-6 [19] GABARRÓN M, ZORNOZA R, MARTÍNEZ-MARTÍNEZ S, et al. Effect of land use and soil properties in the feasibility of two sequential extraction procedures for metals fractionation [J]. Chemosphere, 2019, 218: 266-272. doi: 10.1016/j.chemosphere.2018.11.114 [20] HE L Z, ZHONG H, LIU G X, et al. Remediation of heavy metal contaminated soils by biochar: Mechanisms, potential risks and applications in China [J]. Environmental Pollution, 2019, 252: 846-855. doi: 10.1016/j.envpol.2019.05.151 [21] LEGROS S, LEVARD C, MARCATO-ROMAIN C E, et al. Anaerobic digestion alters copper and zinc speciation [J]. Environmental Science & Technology, 2017, 51(18): 10326-10334. [22] HUANG R X, ZHANG B, SAAD E M, et al. Speciation evolution of zinc and copper during pyrolysis and hydrothermal carbonization treatments of sewage sludges [J]. Water Research, 2018, 132: 260-269. doi: 10.1016/j.watres.2018.01.009 [23] LIU Y C, LIU Q, CHEN M Y, et al. Evaluation of migration of heavy metals and performance of product during co-pyrolysis process of municipal sewage sludge and walnut shell [J]. Environmental Science and Pollution Research, 2017, 24(27): 22082-22090. doi: 10.1007/s11356-017-9858-8 [24] REN J, DAI L, TAO L. Stabilization of heavy metals in sewage sludge by attapulgite [J]. Journal of the Air & Waste Management Association, 2021, 71(3): 392-399. [25] LIU T T, LIU Z G, ZHENG Q F, et al. Effect of hydrothermal carbonization on migration and environmental risk of heavy metals in sewage sludge during pyrolysis [J]. Bioresource Technology, 2018, 247: 282-290. doi: 10.1016/j.biortech.2017.09.090 [26] ADAR E, KARATOP B, İNCE M, et al. Comparison of methods for sustainable energy management with sewage sludge in Turkey based on SWOT-FAHP analysis [J]. Renewable and Sustainable Energy Reviews, 2016, 62: 429-440. doi: 10.1016/j.rser.2016.05.007 [27] KATARZYNA I. The impact of sewage sludge treatment on the content of selected heavy metals and their fractions [J]. Environmental Research, 2017, 156: 19-22. doi: 10.1016/j.envres.2017.02.035 [28] ZHAO B, XU X Y, XU S C, et al. Surface characteristics and potential ecological risk evaluation of heavy metals in the bio-char produced by co-pyrolysis from municipal sewage sludge and hazelnut shell with zinc chloride [J]. Bioresource Technology, 2017, 243: 375-383. doi: 10.1016/j.biortech.2017.06.032 [29] CHEN Z, YU G W, WANG Y, et al. Fate of heavy metals during co-disposal of municipal solid waste incineration fly ash and sewage sludge by hydrothermal coupling pyrolysis process [J]. Waste Management, 2020, 109: 28-37. doi: 10.1016/j.wasman.2020.04.048 [30] ZHANG Z Y, JU R, ZHOU H T, et al. Migration characteristics of heavy metals during sludge pyrolysis [J]. Waste Management, 2021, 120: 25-32. doi: 10.1016/j.wasman.2020.11.018 [31] CHEN G Y, TIAN S, LIU B, et al. Stabilization of heavy metals during co-pyrolysis of sewage sludge and excavated waste [J]. Waste Management, 2020, 103: 268-275. doi: 10.1016/j.wasman.2019.12.031 [32] LIU Y, RAN C M, SIDDIQUI A R, et al. Characterization and analysis of sludge char prepared from bench-scale fluidized bed pyrolysis of sewage sludge [J]. Energy, 2020, 200: 117398. doi: 10.1016/j.energy.2020.117398 [33] YU M, ZHANG J, TIAN Y. Change of heavy metal speciation, mobility, bioavailability, and ecological risk during potassium ferrate treatment of waste-activated sludge [J]. Environmental Science and Pollution Research, 2018, 25(14): 13569-13578. doi: 10.1007/s11356-018-1511-7 [34] QIU C S, BI Y, ZHENG J X, et al. Effect of ozonation treatment on the chemical speciation distributions of heavy metals in sewage sludge and subsequent bioleaching process [J]. Environmental Science and Pollution Research, 2020, 27(16): 19946-19954. doi: 10.1007/s11356-020-08539-0 [35] CHEN Z, YU G W, WANG Y, et al. Research on synergistically hydrothermal treatment of municipal solid waste incineration fly ash and sewage sludge [J]. Waste Management, 2019, 100: 182-190. doi: 10.1016/j.wasman.2019.09.006 [36] KHADHAR S, SDIRI A, CHEKIRBEN A, et al. Integration of sequential extraction, chemical analysis and statistical tools for the availability risk assessment of heavy metals in sludge amended soils [J]. Environmental Pollution, 2020, 263: 114543. doi: 10.1016/j.envpol.2020.114543 [37] ZHAO B, XU X Y, ZENG F Q, et al. The hierarchical porous structure bio-char assessments produced by co-pyrolysis of municipal sewage sludge and hazelnut shell and Cu(II) adsorption kinetics [J]. Environmental Science and Pollution Research, 2018, 25(20): 19423-19435. doi: 10.1007/s11356-018-2079-y [38] LI B B, DING S X, FAN H H, et al. Experimental investigation into the effect of pyrolysis on chemical forms of heavy metals in sewage sludge biochar (SSB), with brief ecological risk assessment [J]. Materials, 2021, 14(2): 447. doi: 10.3390/ma14020447 [39] LU T, YUAN H R, WANG Y Z, et al. Characteristic of heavy metals in biochar derived from sewage sludge [J]. Journal of Material Cycles and Waste Management, 2016, 18(4): 725-733. doi: 10.1007/s10163-015-0366-y [40] WANG Z P, SHU X Q, ZHU H N, et al. Characteristics of biochars prepared by co-pyrolysis of sewage sludge and cotton stalk intended for use as soil amendments [J]. Environmental Technology, 2020, 41(11): 1347-1357. doi: 10.1080/09593330.2018.1534891 [41] ZHANG J, JIN J W, WANG M Y, et al. Co-pyrolysis of sewage sludge and rice husk/ bamboo sawdust for biochar with high aromaticity and low metal mobility [J]. Environmental Research, 2020, 191: 110034. doi: 10.1016/j.envres.2020.110034 [42] CHEN J C, ZHANG J H, LIU J Y, et al. Co-pyrolytic mechanisms, kinetics, emissions and products of biomass and sewage sludge in N2, CO2 and mixed atmospheres [J]. Chemical Engineering Journal, 2020, 397: 125372. doi: 10.1016/j.cej.2020.125372 [43] WANG X D, LI C X, LI Z W, et al. Effect of pyrolysis temperature on characteristics, chemical speciation and risk evaluation of heavy metals in biochar derived from textile dyeing sludge [J]. Ecotoxicology and Environmental Safety, 2019, 168: 45-52. doi: 10.1016/j.ecoenv.2018.10.022 [44] HAN H D, HU S, SYED-HASSAN S S A, et al. Effects of reaction conditions on the emission behaviors of arsenic, cadmium and lead during sewage sludge pyrolysis [J]. Bioresource Technology, 2017, 236: 138-145. doi: 10.1016/j.biortech.2017.03.112 [45] SINGH S, KUMAR V, DATTA S, et al. Current advancement and future prospect of biosorbents for bioremediation [J]. Science of the Total Environment, 2020, 709: 135895. doi: 10.1016/j.scitotenv.2019.135895 [46] DOU X M, CHEN D Z, HU Y Y, et al. Carbonization of heavy metal impregnated sewage sludge oriented towards potential co-disposal [J]. Journal of Hazardous Materials, 2017, 321: 132-145. doi: 10.1016/j.jhazmat.2016.09.010 [47] RAHEEM A, SIKARWAR V S, HE J, et al. Opportunities and challenges in sustainable treatment and resource reuse of sewage sludge: A review [J]. Chemical Engineering Journal, 2018, 337: 616-641. doi: 10.1016/j.cej.2017.12.149 [48] XU X W, JIANG E C. Treatment of urban sludge by hydrothermal carbonization [J]. Bioresource Technology, 2017, 238: 182-187. doi: 10.1016/j.biortech.2017.03.174 [49] WANG X D, LI C X, ZHANG B, et al. Migration and risk assessment of heavy metals in sewage sludge during hydrothermal treatment combined with pyrolysis [J]. Bioresource Technology, 2016, 221: 560-567. doi: 10.1016/j.biortech.2016.09.069 [50] LI C X, XIE S Y, WANG Y, et al. Simultaneous heavy metal immobilization and antibiotics removal during synergetic treatment of sewage sludge and pig manure [J]. Environmental Science and Pollution Research, 2020, 27(24): 30323-30332. doi: 10.1007/s11356-020-09230-0 [51] ŚWIERCZEK L, CIEŚLIK B M, KONIECZKA P. The potential of raw sewage sludge in construction industry—A review [J]. Journal of Cleaner Production, 2018, 200: 342-356. doi: 10.1016/j.jclepro.2018.07.188 [52] WENG H X, MA X W, FU F X, et al. Transformation of heavy metal speciation during sludge drying: Mechanistic insights [J]. Journal of Hazardous Materials, 2014, 265: 96-103. doi: 10.1016/j.jhazmat.2013.11.051 [53] HE J, STREZOV V, KAN T, et al. Effect of temperature on heavy metal(loid) deportment during pyrolysis of Avicennia marina biomass obtained from phytoremediation [J]. Bioresource Technology, 2019, 278: 214-222. doi: 10.1016/j.biortech.2019.01.101 [54] WANG Z P, LIU K, XIE L K, et al. Effects of residence time on characteristics of biochars prepared via co-pyrolysis of sewage sludge and cotton stalks [J]. Journal of Analytical and Applied Pyrolysis, 2019, 142: 104659. doi: 10.1016/j.jaap.2019.104659 [55] 许思涵, 王敏艳, 张进, 等. 热解时间对污泥炭特性及其重金属生态风险水平的影响 [J]. 环境工程, 2020, 38(03): 162-167. doi: 10.13205/j.hjgc.202003027 XU S H, WANG M Y, ZHANG J, et al. Effect of pyrolysis time on characteristics and heavy metal ecological risks in biochar made from wastewater sludge [J]. Environmental Engineering, 2020, 38(03): 162-167(in Chinese). doi: 10.13205/j.hjgc.202003027
[56] 刁韩杰. 不同热解条件对污泥炭特性及重金属行为的影响[D]. 杭州: 浙江农林大学, 2019. DIAO H J. Effects of different pyrolysis conditions on carbon characteristics and heavy metal behavior of sludge[D]. Hangzhou: Zhejiang Agriculture & Forestry University, 2019(in Chinese).
[57] NAEIMEH V, LARSERIK Å, AURéLIE C, et al. Pyrolysis of municipal sewage sludge to investigate char and phosphorous yield together with heavy-metal removal—experimental and by thermodynamic calculations [J]. Energies, 2021, 14(5): 1477. doi: 10.3390/en14051477 [58] HUANG H J, YANG T, LAI F Y, et al. Co-pyrolysis of sewage sludge and sawdust/rice straw for the production of biochar [J]. Journal of Analytical and Applied Pyrolysis, 2017, 125: 61-68. doi: 10.1016/j.jaap.2017.04.018 [59] ZHOU Y, LIU Y Z, JIANG W B, et al. Effects of pyrolysis temperature and addition proportions of corncob on the distribution of products and potential energy recovery during the preparation of sludge activated carbon [J]. Chemosphere, 2019, 221: 175-183. doi: 10.1016/j.chemosphere.2019.01.026 [60] YANG Y Q, CUI M H, REN Y G, et al. Towards Understanding the Mechanism of Heavy Metals Immobilization in Biochar Derived from Co-pyrolysis of Sawdust and Sewage Sludge [J]. Bulletin of Environmental Contamination and Toxicology, 2020, 104(4): 489-496. doi: 10.1007/s00128-020-02801-4 [61] XIE S Y, YU G W, LI C X, et al. Treatment of high-ash industrial sludge for producing improved char with low heavy metal toxicity [J]. Journal of Analytical and Applied Pyrolysis, 2020, 150: 104866. doi: 10.1016/j.jaap.2020.104866 [62] 蔡尽忠, 李火金, 邓盈. 玉米秸秆与污泥混合热解对生物碳特性及重金属的影响(英文) [J]. 农业工程学报, 2020, 36(6): 239-245. CAI J Z, LI H J, DENG Y. Effects of maize stovers and sewage sludge co-pyrolysis on characteristics and heavy metals in biochar [J]. Transactions of the Chinese Society of Agricultural Engineering, 2020, 36(6): 239-245(in Chinese).
[63] GONG Z Q, LIU C, WANG M, et al. Experimental study on catalytic pyrolysis of oil sludge under mild temperature [J]. Science of the Total Environment, 2020, 708: 135039. doi: 10.1016/j.scitotenv.2019.135039 [64] WANG Z P, XIE L K, LIU K, et al. Co-pyrolysis of sewage sludge and cotton stalks [J]. Waste Management, 2019, 89: 430-438. doi: 10.1016/j.wasman.2019.04.033 [65] WANG Z P, WANG J, XIE L K, et al. Influence of the addition of cotton stalk during Co-pyrolysis with sewage sludge on the properties, surface characteristics, and ecological risks of biochars [J]. Journal of Thermal Science, 2019, 28(4): 755-762. doi: 10.1007/s11630-019-1100-1 [66] FAN J P, LI Y, YU H Y, et al. Using sewage sludge with high ash content for biochar production and Cu(Ⅱ) sorption [J]. Science of the Total Environment, 2020, 713: 136663. doi: 10.1016/j.scitotenv.2020.136663 [67] RAJAPAKSHA A U, VITHANAGE M, AHMAD M, et al. Enhanced sulfamethazine removal by steam-activated invasive plant-derived biochar [J]. Journal of Hazardous Materials, 2015, 290: 43-50. doi: 10.1016/j.jhazmat.2015.02.046 [68] XIAO X, CHEN B L, ZHU L Z. Transformation, morphology, and dissolution of silicon and carbon in rice straw-derived biochars under different pyrolytic temperatures [J]. Environmental Science & Technology, 2014, 48(6): 3411-3419. [69] JINDO K, MIZUMOTO H, SAWADA Y, et al. Physical and chemical characterization of biochars derived from different agricultural residues [J]. Biogeosciences, 2014, 11(23): 6613-6621. doi: 10.5194/bg-11-6613-2014 [70] LIU L H, HUANG L, HUANG R, et al. Immobilization of heavy metals in biochar derived from co-pyrolysis of sewage sludge and calcium sulfate [J]. Journal of Hazardous Materials, 2021, 403: 123648. doi: 10.1016/j.jhazmat.2020.123648 [71] YANG P H, ZHOU P, LI Y, et al. Recent development in pyrolytic catalysts of oil sludge [J]. Petroleum Science and Technology, 2018, 36(7): 520-524. doi: 10.1080/10916466.2018.1431661 [72] SUN S C, HUANG X F, LIN J H, et al. Study on the effects of catalysts on the immobilization efficiency and mechanism of heavy metals during the microwave pyrolysis of sludge [J]. Waste Management, 2018, 77: 131-139. doi: 10.1016/j.wasman.2018.04.046 [73] HU H Y, LIU H, ZHANG Q, et al. Sintering characteristics of CaO-rich municipal solid waste incineration fly ash through the addition of Si/Al-rich ash residues [J]. Journal of Material Cycles and Waste Management, 2016, 18(2): 340-347. doi: 10.1007/s10163-014-0341-z [74] GONG Z Q, LIU L, ZHANG H T, et al. Study on the migration characteristics of As, Pb, and Ni during oily sludge incineration with CaO additive [J]. Energy & Fuels, 2020, 34(12): 16341-16349. [75] LI Y F, HONG C, WANG Z Q, et al. Fractal characteristics of biochars derived from Penicillin v potassium residue pyrolysis [J]. Journal of Analytical and Applied Pyrolysis, 2019, 141: 104636. doi: 10.1016/j.jaap.2019.104636 [76] 汪刚, 余广炜, 谢胜禹, 等. 添加不同塑料与污泥混合热解对生物炭中重金属的影响 [J]. 燃料化学学报, 2019, 47(5): 611-620. doi: 10.3969/j.issn.0253-2409.2019.05.013 WANG G, YU G W, XIE S Y, et al. Effect of co-pyrolysis of different plastics with sewage sludge on heavy metals in the biochar [J]. Journal of Fuel Chemistry and Technology, 2019, 47(5): 611-620(in Chinese). doi: 10.3969/j.issn.0253-2409.2019.05.013
[77] LI J, YU G W, XIE S Y, et al. Immobilization of heavy metals in ceramsite produced from sewage sludge biochar [J]. Science of the Total Environment, 2018, 628-629: 131-140. doi: 10.1016/j.scitotenv.2018.02.036 -




 下载:
下载: