-
纳米乳化油是由植物油、食用表面活性剂、去离子水按照一定比例混合,然后通过相升温转变技术制备而成的乳浊液[1]. 在污染地下水原位修复过程中,乳化油作为长效缓释碳源和电子供体,原位注入含水层,强化土著微生物实现污染物的高效降解[2],如氯代烃[3]、Cr(Ⅵ)[4-5]、放射性U(Ⅵ)[6]、硝酸盐[7-8]等污染物. 由于纳米乳化油具有较高的动力学稳定性[9-11],可在包气带和含水层中形成一定的反应带,实现对污染物的原位修复[12]. 然而,在天然含水多孔介质中水化学类型、含盐量和pH可能会影响纳米乳化油表面性质[13-14],进一步影响纳米液滴的分散、迁移和释放[15],阻碍地下水污染的修复[16-17]. 已有食品与医药等领域的相关研究证实,纳米乳液的稳定性受到离子强度的影响. Mei等报道在石蜡纳米乳化油中添加不同类型及浓度的离子,引起液滴表面Zeta电位的变化,甚至出现表面电荷的反转,且高价态离子对乳液稳定性的影响更为显著[18]. Qian等证明富含β‐胡萝卜素的纳米乳化油在低pH和高离子强度下,由于静电屏蔽效应容易发生液滴的聚集[19]. Ren等证明聚氧丙烯表面活性剂制备的纳米乳化油在0—50 mmol·L−1 NaCl体系中,液滴平均粒径有所下降,粒径分布曲线变窄,峰值变陡,表面张力降低,且促使了乳液的失稳[20].
由上述报道可以看出,食品与医药领域的研究中涉及的离子组分相对单一,且不同离子类型及浓度对纳米乳化油的影响不尽相同. 在实际地下水中,离子组分众多,除Na+与Cl−外,还存在大量Ca2+、HCO3−、
${\rm{SO}}_4^{2 - } $ 等,主要离子组分组合常形成不同的水化学类型. 有关天然地下水环境中不同水化学类型对纳米乳化油稳定性的报道甚少,纳米乳化油的团聚和失稳将影响其在饱和多孔介质中的分散性与迁移性,从而影响原位生物修复污染物的效率. 因此,为进一步明晰地下水水化学类型对纳米乳化油稳定性的影响,本文选取了3种典型水化学类型以及不同含盐量溶液,分别考察了对纳米乳化油稳定性的影响,表征了纳米乳化油表面电性和流变特性,并结合稳定性动力学指数(turbiscan stability index,TSI)、扩展DLVO理论[21]分析了纳米乳化油稳定性的机制,以期为研究天然水化学条件下纳米乳化油在饱和多孔介质中的迁移和归趋提供必要支撑. -
实验试剂:纳米乳化油制备所用材料有金龙鱼大豆油、吐温80(Tween80)、司班80(Span80),购自天津光复精细化工研究院;模拟配制地下水化学类型的试剂包括:重碳酸钠(NaHCO3)、重碳酸钙(Ca(HCO3)2)、硫酸钠(Na2SO4),购自国药化学试剂有限公司. 所有试剂无需纯化,配备过程均用去离子水完成.
实验设备:电动增力搅拌器 JJ‐1,常州市环宇科技仪器厂;恒温水浴箱 HH‐M6,上海赫田科学仪器有限公司;超声波清洗机 DFD‐700,高电电子仪器厂;数字旋转黏度计 NDJ‐5S,上海恒平科学仪器有限公司;Zetasizer Nano‐ZS90,Malvern仪器公司;Turbiscan Tower,Formulaction仪器公司.
-
纳米乳化油的制备:称取15 g大豆油和15 g非离子表面活性剂(Tween80和Span80)于锥形瓶中,使用电动增力搅拌器在1800 r·min−1条件下混匀1 min,随后在1500 r·min−1条件下每隔1 min加入10 mL去离子水,共加入70 mL去离子水. 利用相升温转变技术,将锥形瓶放入超声波仪器中,55 ℃条件下超声25 min,取出冷却并静置24 h待用[22].
水化学溶液的配制:用分析天平称取0.3 g、0.7 g、1.0 g、3.0 g的NaHCO3、Ca(HCO3)2和Na2SO4粉末分别倒入各自1 L的棕色容量瓶中,加入去离子水定容,即配成不同水化学类型及含盐量溶液.
本实验共设计4组,其中3组为不同地下水化学类型及含盐量溶液,另外1组以去离子水作为空白对照组. 为减少其他离子组分的干扰,本实验配制不同水化学类型溶液时,未引入其他离子组分. 首先,将配制完成的3种水化学类型溶液各取10 mL加入不同的离心管中,再分别加入10 mg的纳米乳化油,在25 ℃,170 r·min−1条件下平置振荡15 min,密封放置24 h后对纳米乳化油进行相应的表征. 具体的地下水水化学类型及含盐量设置见表1.
-
粒径:Zetasizer Nano-ZS90利用动态光散射技术,通过测试液滴布朗运动信息,并根据斯托克斯-爱因斯坦方程得到纳米乳液的粒径分布和平均粒径. 在测试前,为防止多重散射效应,将纳米乳化油用去离子水稀释1000倍,分散介质和纳米乳化油的折射率分别设置为1.33和1.45.
Zeta电位:Zetasizer Nano-ZS90利用激光多普勒效应测量纳米乳液电泳速度,根据亨利方程得到Zeta电位. 在分析前,将纳米乳化油用去离子水稀释1000倍,分散介质和纳米乳化油的折射率分别设置为1.33和1.45.
TSI值:Turbiscan Tower运用多重光散射原理,通过透射光和背射光信号,能够得到纳米乳化油光通量的变化情况. 测试时,将20 mL纳米乳化油装入样品池中(无需稀释),每间隔1 h扫描一次,连续扫描24 h.采用Turbiscan Lab Expert分析纳米乳化油的动力学变化. 测试工作委托大昌华嘉仪器公司完成.
-
TSI值反映了纳米乳化油稳定性,TSI值越大,体系越不稳定,可由式(1)-式(3)计算.
式中,
$ B_{\text{s}} $ 为背散射光强度(无量纲);$ \lambda ^{\text{*}} $ 为光子传送的平均自由光程(μm);$ \varphi $ 为颗粒体积比;g为不对称因子、$ Q_{\text{s}} $ 为散射效率,可由米氏光散射理论求得;d为液滴平均直径(μm);$ X_{\text{i}} $ 为每小时测量的平均散射强度(无量纲);$ X_{\text{BS}} $ 为$ X_{\text{i}} $ 的平均测量值(无量纲);n为扫描次数;TSI为稳定性动力学指数(无量纲). -
根据扩展DLVO理论,纳米液滴的聚集和分离主要取决于范德华力、静电斥力、空间位阻斥力的受力情况,其中空间位阻斥力又包括空间渗透斥力和空间弹性斥力. 它的受力之和能够反映体系的稳定性,可由式(4)计算.
式中,VT为总势能(J);VVdw为范德华力势能(J);VEI为静电排斥势能(J);Vosm为空间渗透排斥势能(J);Vel为空间弹性排斥势能(J).
其中范德华力势能可由式(5)和式(6)计算.
式中,A为Hamaker常数(J);
${{d}}_{\mathrm{c}}$ 为粒子直径(m);${h}$ 为两粒子之间距离(m);$ \lambda $ 为相互作用的特征波长(nm),设置为100 nm;${{A}}_{\text{11}}$ 为水的Hamaker常数(3.7×10−20 J);$ A_{\text{22}} $ 为纳米乳化油的Hamaker常数(5.0×10−21 J)[23-24].静电排斥势能可由式(7)和式(8)计算.
式中,
$ {d}_{\text{c}} $ 为粒子直径(m);$ {\phi }_{\text{1}} $ 和$ {\phi }_{\text{2}} $ 分别为液滴与液滴的表面电势(mV),通常用Zeta电位代替;$\varepsilon$ 为溶液介电常数(78.5);${h}$ 为液滴表面到液滴表面的距离(m);$ \textit{κ} $ 为德拜-胡克尔倒数长度(m−1);e为电荷电量(−1.602×10−19 C);${{n}}_{{i}\text{,0}}$ 为溶液电解质浓度(mol·L−1);${{z}}_{{i}}$ 为离子化合价;k为玻尔兹曼常数(1.381×10−23 J·K−1);${T}$ 表示绝对温度(295 K).空间位阻势能是吸附在油滴表面的非离子表面活性剂层产生压缩和重叠引起的排斥力,它的值等于渗透排斥势能(Vosm)和弹性排斥势能(Vel)之和,分别利用式(9)-式(11)和式(12)-式(13)计算.
式中,
$ {d}_{\text{c}} $ 为粒子直径(m);${h}$ 为液滴之间的距离(m);$ {\varphi }_{\text{x}} $ 为被吸附的聚合物所占表面的体积分数(0.03) [25-26];$ {v}_{\text{1}} $ 为单位聚合物分子的体积(2.98×10−29 m3);$ \textit{χ} $ 为Flory‐Huggins 参数(0.49) [27];L为被吸附聚合物在表面层形成的厚度(5 nm);${{M}}_{\text{w}}$ 为聚合物的相对分子质量(1310);$ {\rho }_{\text{x}} $ 为聚合物的密度(1.064 kg·m−3). -
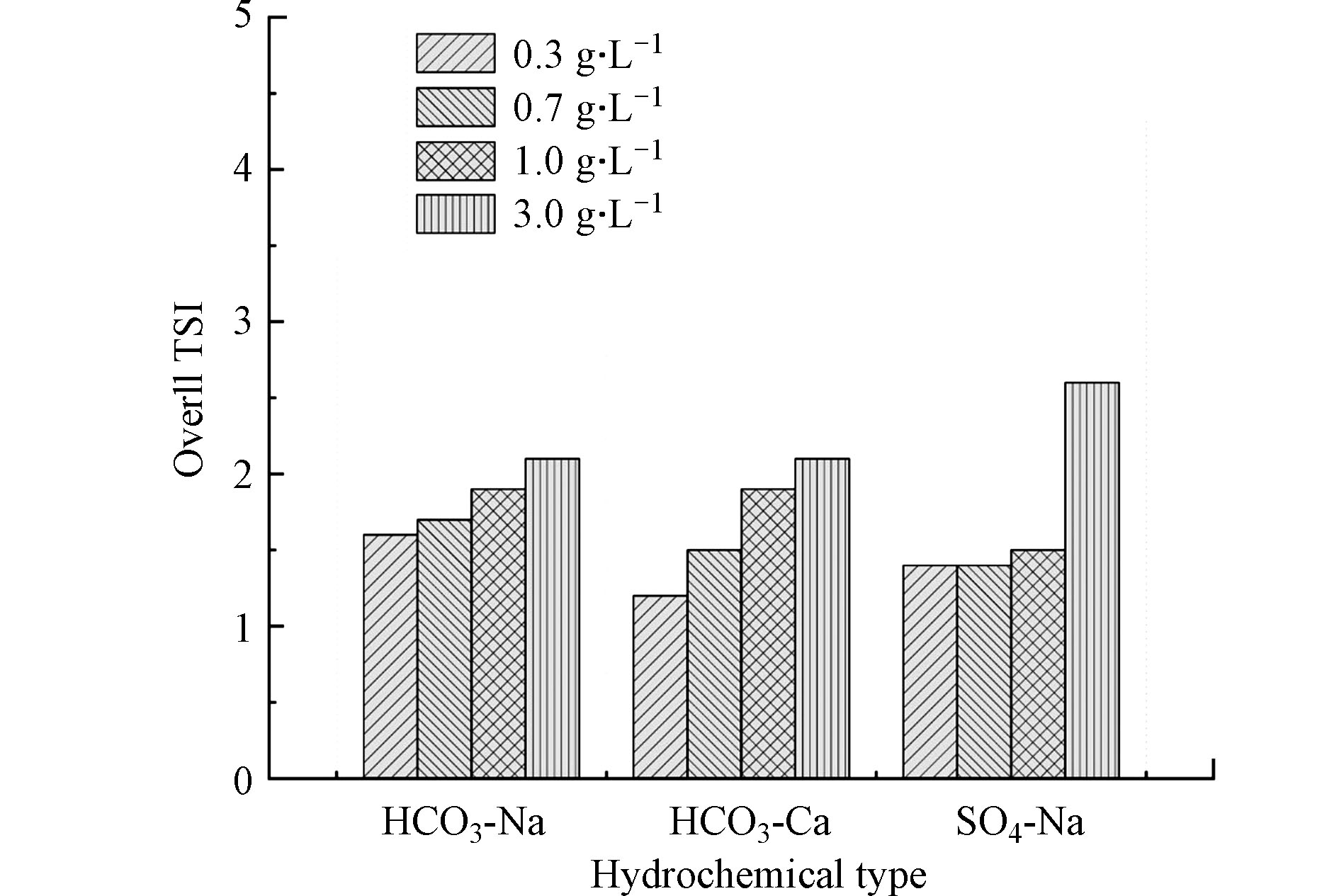
采用Turbiscan Lab Expert分析了24 h后纳米乳化油的整体稳定性,得到水化学类型作用下纳米乳化油的整体TSI值结果. 如图1所示,HCO3-Na和HCO3-Ca型水影响下纳米乳化油的TSI值呈上升趋势,表明在HCO3型水中,纳米乳化油随含盐量的增加稳定性降低. 去离子水中的纳米乳化油TSI值为1.4,当含盐量为0.3 g·L−1时,HCO3-Na和HCO3-Ca 型水影响下的TSI值分别升高14%和降低14 %;当含盐量为0.7、1.0、3.0 g·L−1时,HCO3-Na型水影响下的TSI值分别升高21%、36%、50%;HCO3-Ca型水影响下的TSI值分别升高7%、36%、50%,表明含盐量越高HCO3-Na和HCO3-Ca型水对纳米乳化油稳定性的影响程度越相近.
与HCO3型水相比,随含盐量增加,SO4-Na型水对纳米乳化油的TSI值表现出较大差异. 0.3 g·L−1、0.7 g·L−1、1.0 g·L−1时,TSI值变化微弱;3.0 g·L−1时,TSI值显著升高86%,表明SO4-Na型水对纳米乳化油稳定性存在明显的高低浓度效应.低含盐量的SO4-Na型水对纳米乳化油稳定性影响微弱,高含盐量时纳米乳化油的稳定性急剧降低. 由此可见,水化学特征对纳米乳化油稳定性的影响体现在含盐量和水化学类型两个方面,低含盐量对纳米乳化油稳定性影响较小,而在高含盐量水中,水化学类型均不利于纳米乳化油的稳定[28],其中SO4-Na型的影响远大于HCO3-Na和HCO3-Ca型. 因此,需要重点关注高含盐量水对纳米乳化油稳定性的影响.
-
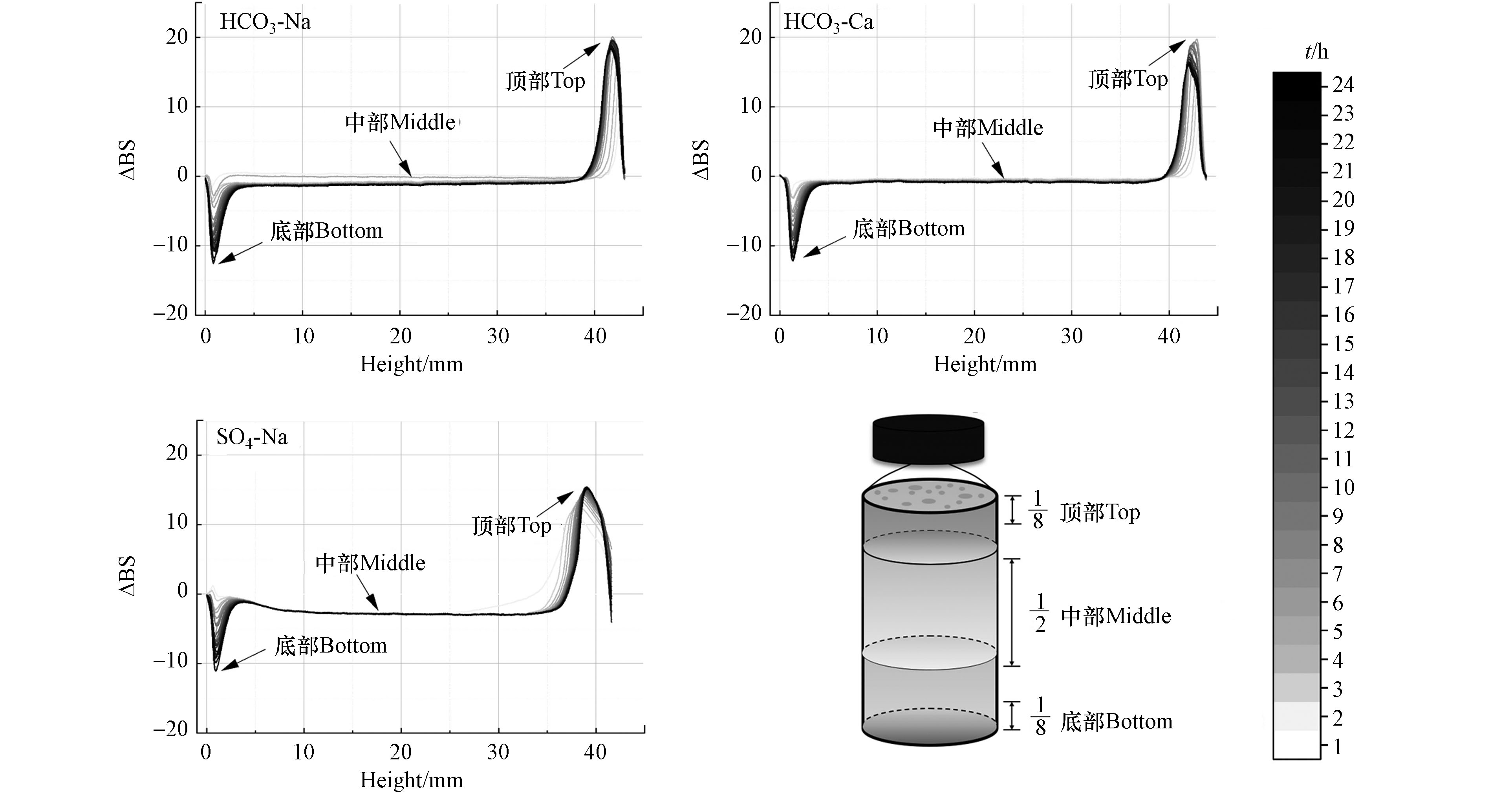
为进一步探讨高含盐量水对纳米乳化油稳定性的影响,对比了3.0 g·L−1的HCO3-Na、HCO3-Ca和SO4-Na型影响下纳米乳化油的光通量变化曲线(图2). 光通量变化曲线随时间的延长局部差异显著,表现在不同层位光通量的增降特征.体系中底部光通量减弱,顶部光通量增强,说明底部液滴逐渐向顶部跃迁. 基于该结果识别具有特征性的层位,并划分出顶部、中部、底部,其中分别占测试总体积的12.5%、50%、12.5%,比较分析水化学类型影响下,纳米乳化油顶部、中部、底部TSI值的变化.
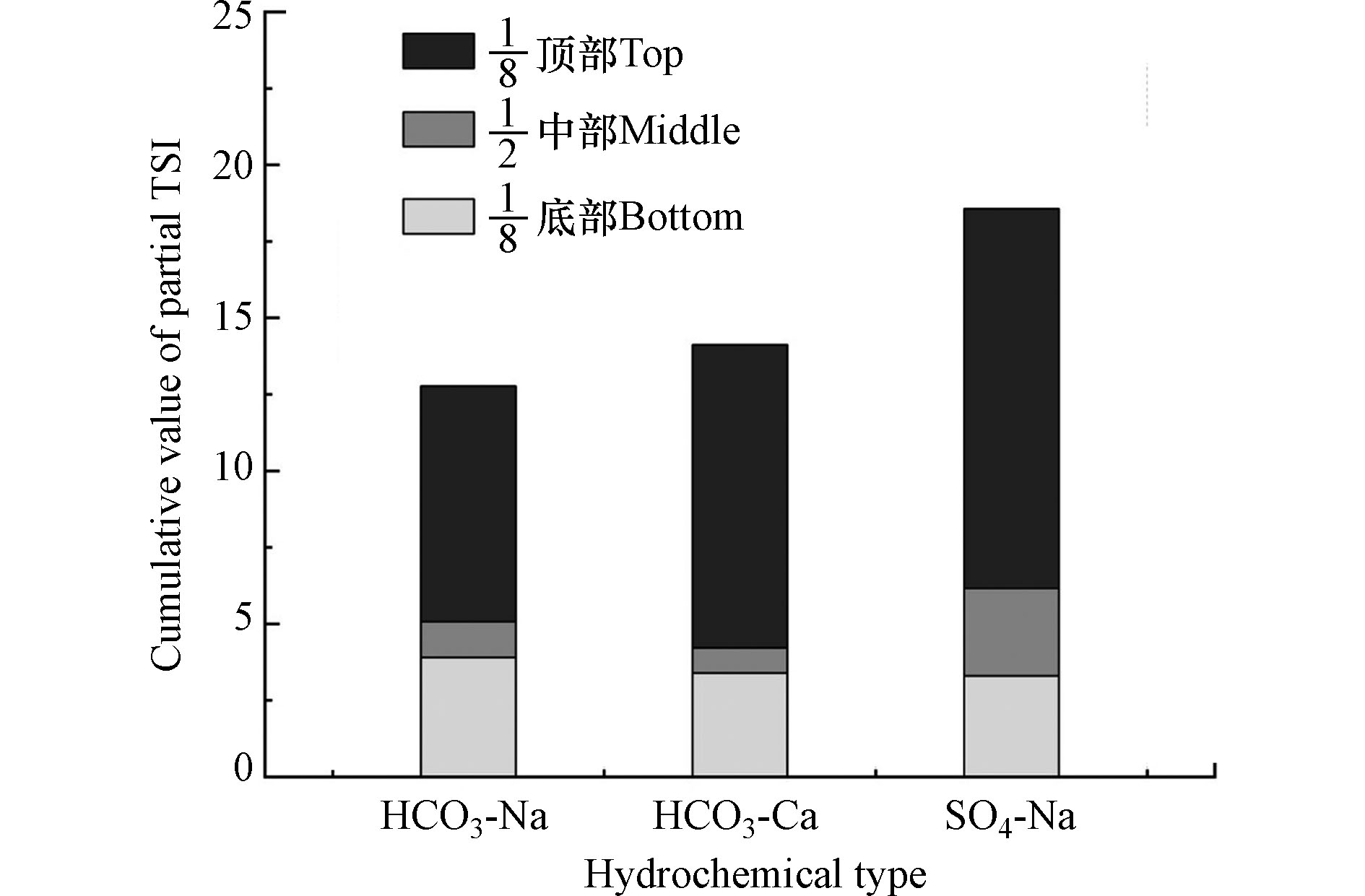
如图3所示,HCO3-Na、HCO3-Ca和SO4-Na型水影响下,纳米乳化油顶部、中部、底部的TSI值分别为7.7、9.9、12.4,1.2、0.8、2.8以及3.8、3.5、3.3. 由此可以看出,水化学类型影响下纳米乳化油顶部TSI值最大,其次是底部,最小是中部,说明纳米乳化油整体稳定性降低是由顶部失稳引起. 对顶部而言,TSI值越高,表明液滴从底部向顶部扩散速度越快,顶部液滴不断聚集,随时间延长顶部逐渐出现乳化层[29]. 其中,3种水化学类型对乳化油顶部的影响程度由大到小的顺序为:SO4-Na型>HCO3-Ca型>HCO3-Na型,说明在不同类型的体系中,离子强度越高,引起水相与油相的密度差越大,液滴上浮和乳化现象越显著[30-31].
与顶部相比,纳米乳化油中部所占体积最多,一定程度上决定纳米乳化油在多孔介质中的传质效率. 在水化学类型影响下纳米乳化油中部TSI值最低,但SO4-Na型比HCO3-Na和HCO3-Ca型水对纳米乳化油中部的敏感程度要强,且不利于纳米乳化油的稳定. 在3种水化学类型体系中,纳米乳化油底部的TSI值相差无几,表明水化学特征对纳米乳化油底部差异的影响不显著.
-
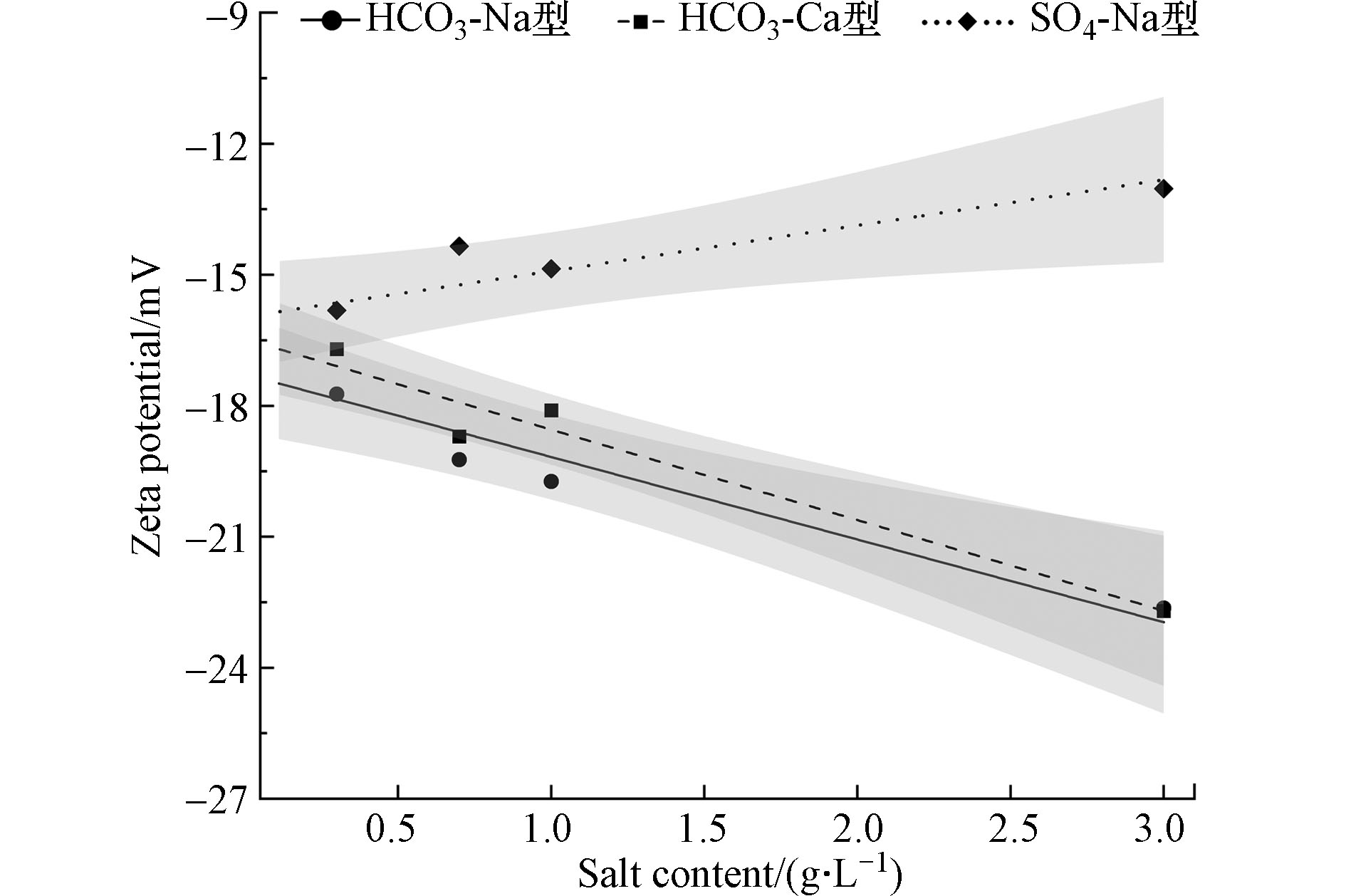
在去离子水中纳米乳化油的Zeta电位值是−16.51 mV,说明液滴表面带负电荷,而环境介质pH、阴阳离子类型和含量会影响纳米液滴的表面电荷和表面性质,进一步影响纳米乳化油的迁移性和分散性. 由图4可见,在HCO3-Na与HCO3-Ca型水中,Zeta电位与含盐量呈负相关性,线性拟合的相关性R2值分别为0.93和0.96;在SO4-Na型水中,Zeta电位与含盐量呈正相关性,R2值为0.84. HCO3-Na与HCO3-Ca型相比,阳离子不同,但Zeta电位变化趋势一致;HCO3-Na与SO4-Na型相比,阴离子不同,其中SO4型水中的纳米乳化油Zeta电位绝对值减小,HCO3型的Zeta电位绝对值增加,表明在水化学体系中不同阴离子使液滴表面电荷发生明显的改变[18].
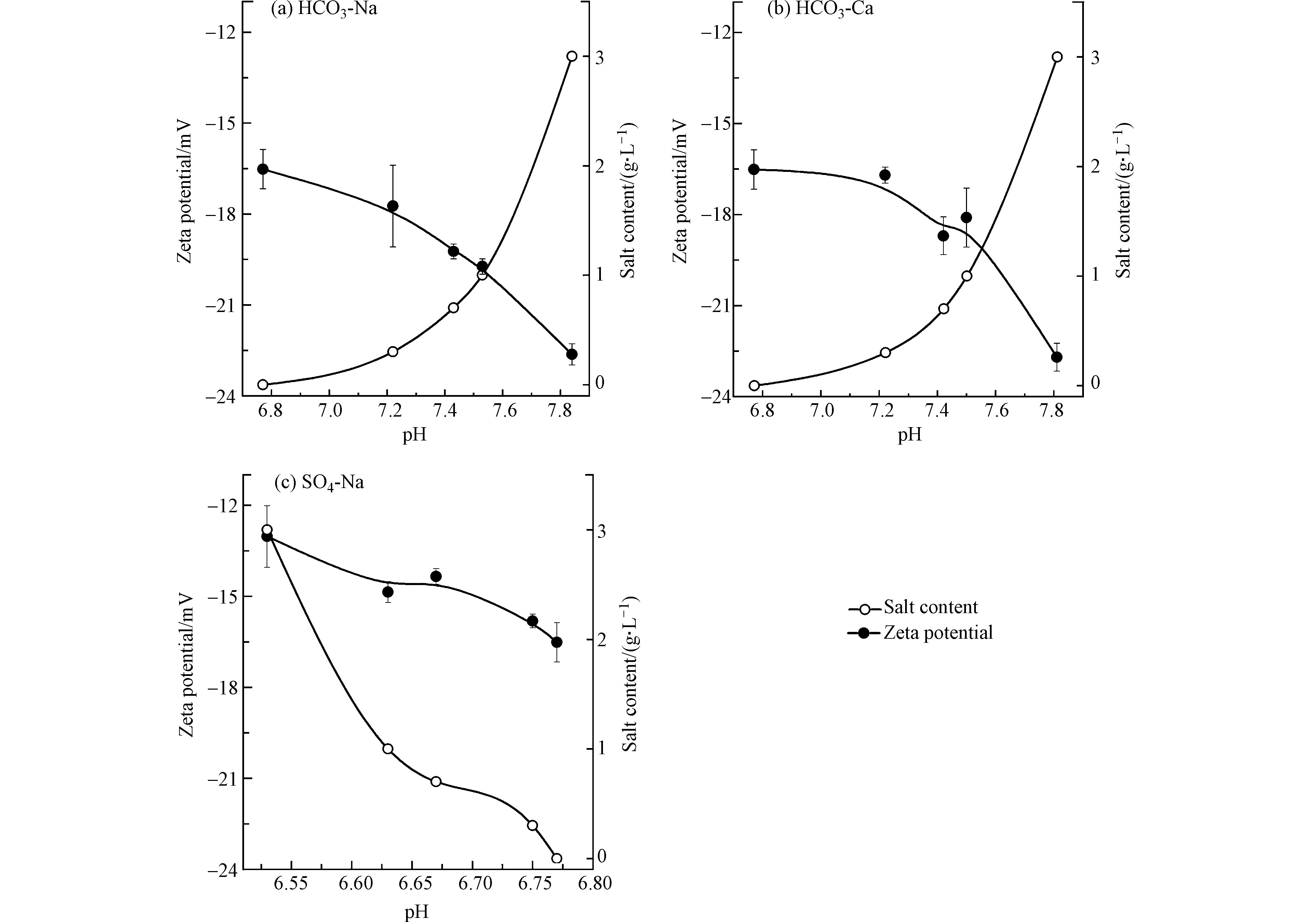
3种水化学体系中pH随含盐量的增加而发生变化. HCO3-Na和HCO3-Ca型体系中pH随含盐量的增加呈非线性上升,Zeta电位绝对值随pH增加而增大(图5(a)和(b));SO4-Na型体系中pH随含盐量的增加而降低,Zeta电位绝对值随pH降低而减小(图5(c)),表明Zeta电位变化可能与体系中pH有关. 据报道,液滴带负电荷是由于非离子表面活性剂的亲水基优先吸附OH-,使油水界面层的水分子与OH-形成氢键[32]. 首先,HCO3-为弱电解质,在水溶液中呈弱碱性,容易电离更多OH-,导致Zeta电位降低. 其次,霍夫梅斯特序列认为相同阳离子条件下,不同阴离子对纳米胶体的影响大相径庭,作用能力强的阴离子使大分子亲水基周围的水分子减少,导致胶体的水化层变薄,所带负电荷降低.
${\rm{SO}}_4^{2 - } $ 为强电解质,作用能力强于HCO3-,且随含盐量的增加pH也略有降低[33]. 综上可知,在水化学体系中强电解质和低pH是液滴表面负电性减弱的原因. -
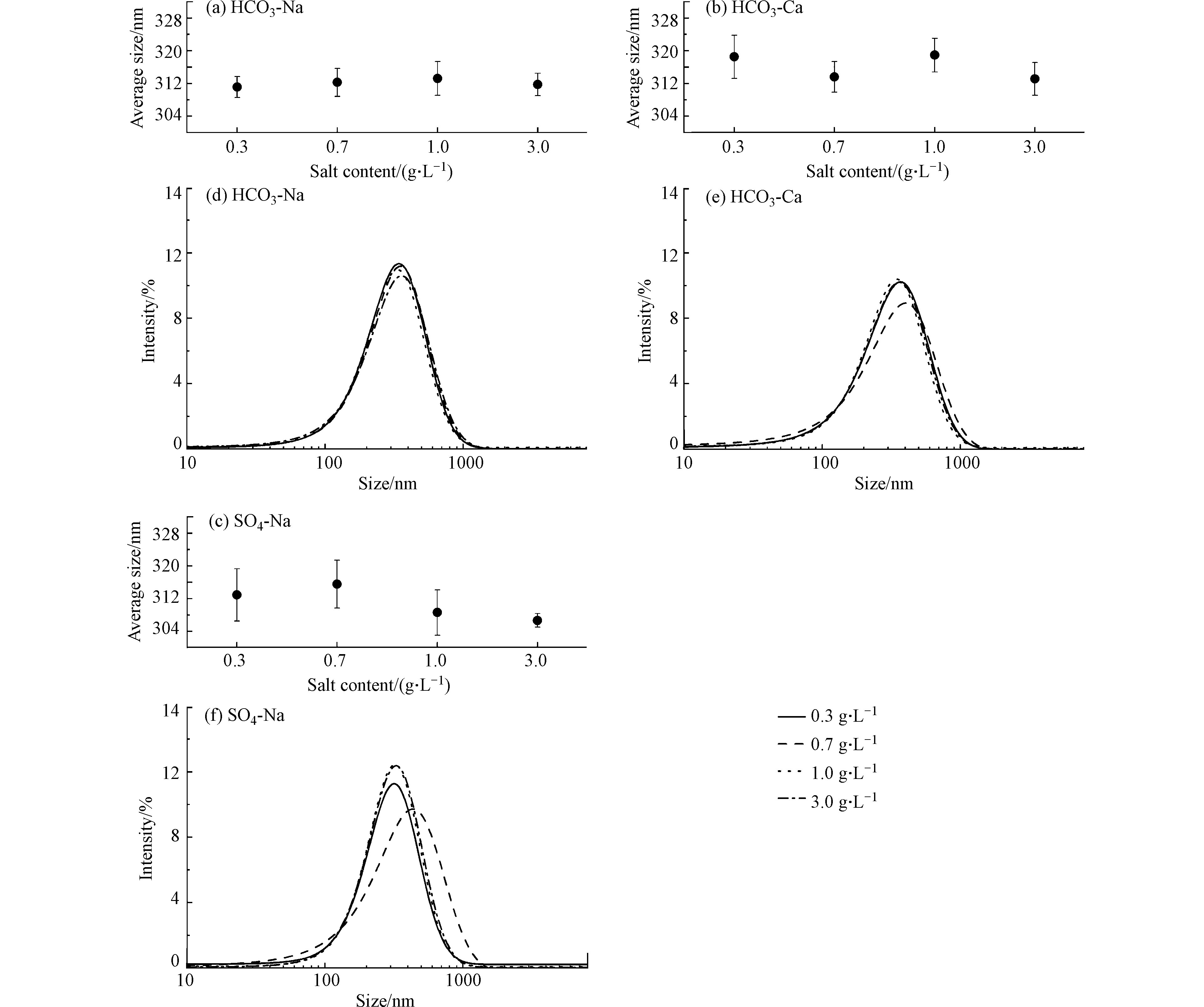
粒径尺寸及分布能进一步反映水化学特征对纳米乳化油微观状态的影响[34].所有水化学类型溶液中,液滴粒径近似正态分布,均值粒径所占权重最多,小粒径和大粒径占比较少. 由于液滴时刻在做布朗运动,存在选择随机性. 水化学特征下,随含盐量增加,纳米乳化油的平均粒径略有波动(图6),但含盐量为3.0 g·L−1的体系中,SO4型水中的纳米液滴粒径分布曲线更加陡峭,且等效的平均粒径稍显降低(图6(c))[35]. 相同含盐量下,SO4型比HCO3型的离子强度高,体系中的离子会影响纳米液滴表面膜的厚度,离子强度越高,纳米液滴最外层的水化膜减小越明显,等效的流体力学直径也略有降低.
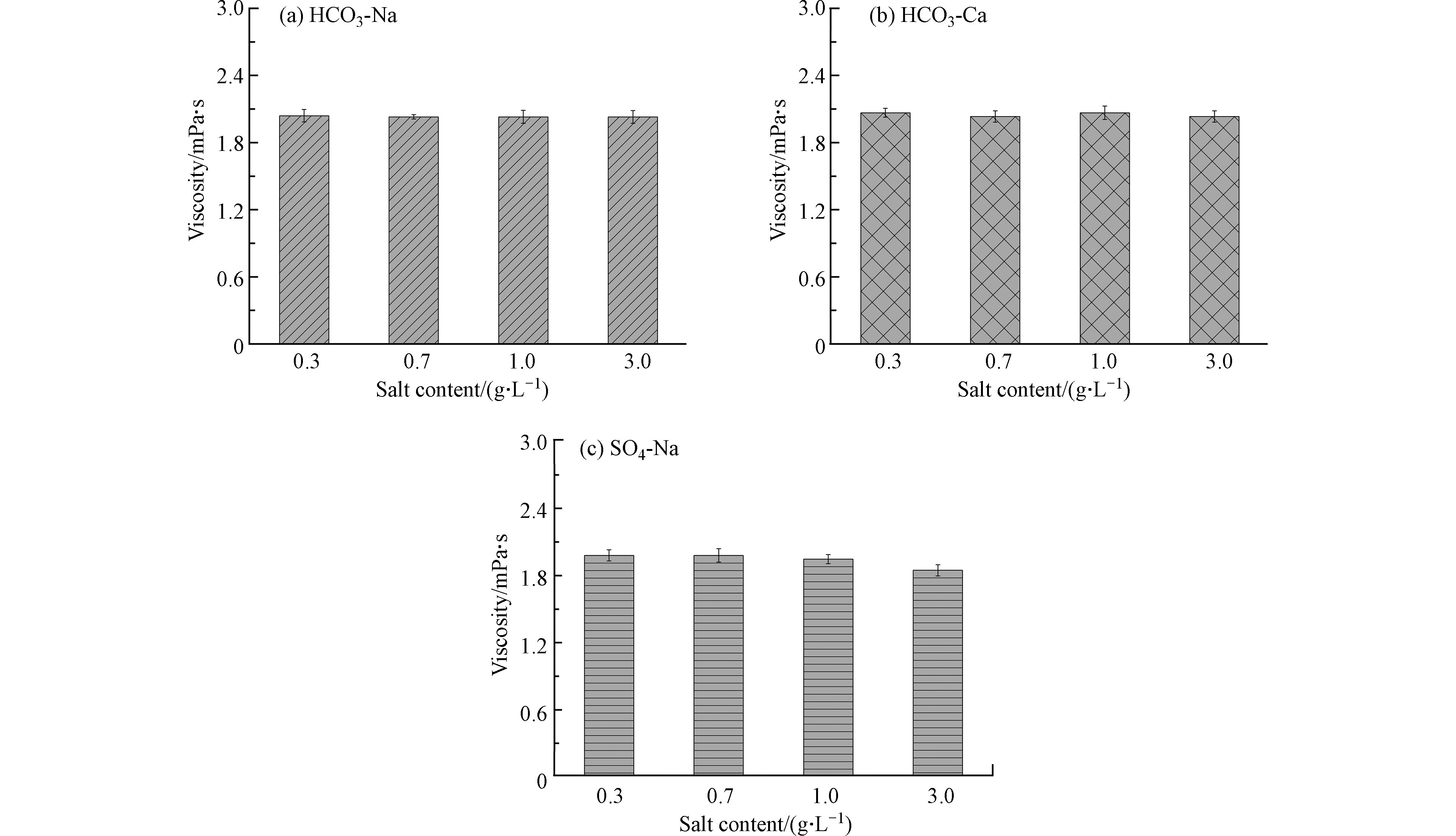
HCO3-Na和HCO3-Ca型体系中的纳米乳化油随含盐量增加,黏度无显著变化(图7(a)和(b));SO4-Na型体系中,随含盐量增加黏度略有降低(图7(c)).在SO4型水中,
${\rm{SO}}_4^{2 - } $ 附近更易吸引周围的水分子,导致非离子表面活性剂亲水基与水分子的交联降低,从而促使黏弹性略有降低[36-37]. -
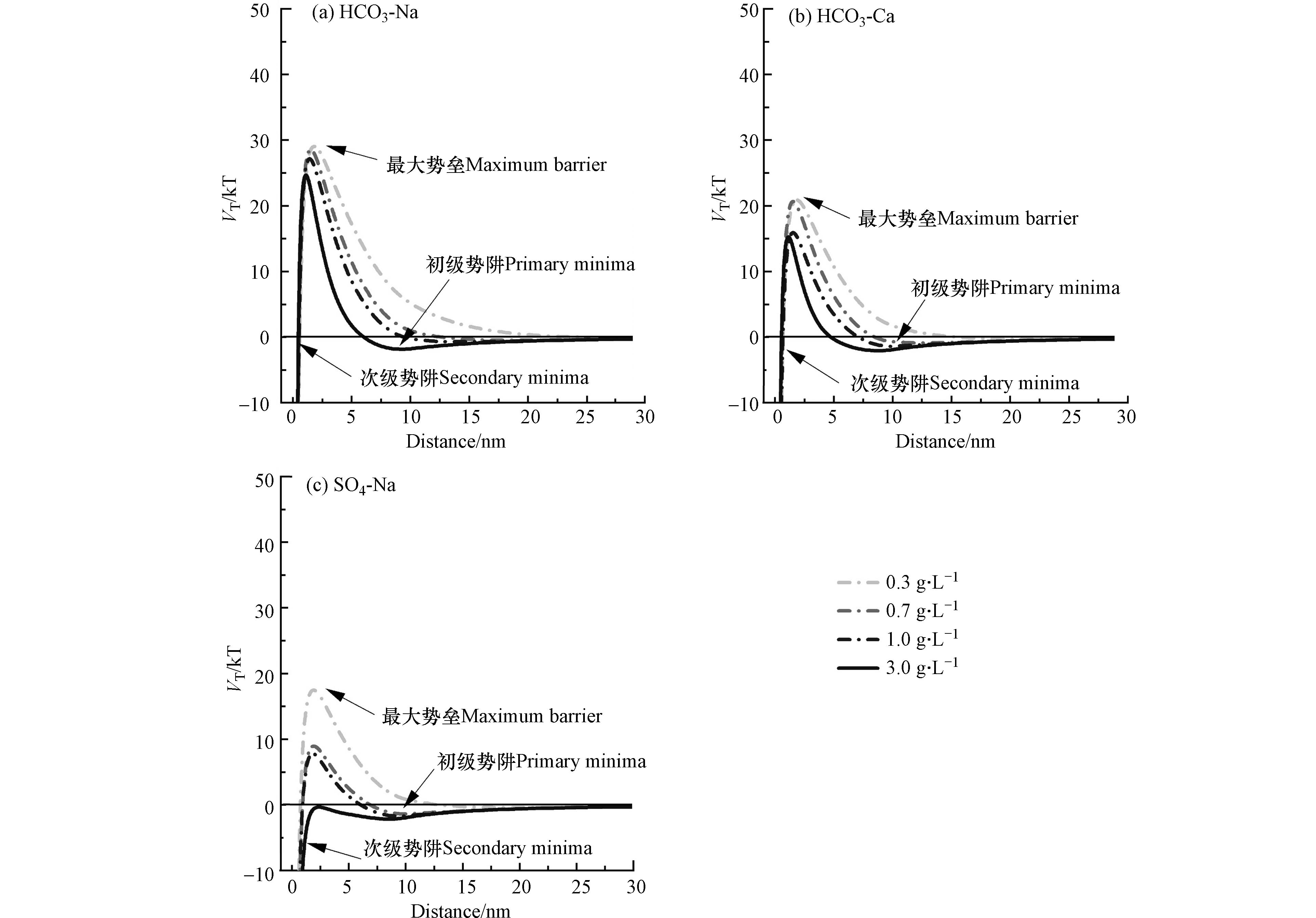
基于纳米液滴之间的相互作用关系,利用扩展DLVO理论,计算了水化学特征下纳米液滴随距离变化的总势能(VT).如图8所示,含盐量增加,VT随间距的缩小陷入次级势阱,此时液滴之间能够发生可逆的聚集[38].液滴进一步靠近,聚集的液滴能被再次分散,这是由于静电斥力和空间位阻斥力迅速增加,VT逐渐上升并出现最大势垒,液滴的动能只有跃过最大势垒才会发生不可逆的聚集.对于斥力减小,最大势垒降低,液滴之间随距离的缩小,引力剧增,较大动能的液滴跃过势垒进入初级势阱,此时体系出现不可逆的聚集,所以最大势垒的高低能够体现纳米乳化油的稳定性.体系中含盐量增加,最大势垒降低,说明高含盐量(3.0 g·L−1)不利于纳米乳化油的稳定.在天然高含盐量的含水层中,纳米乳化油的滞留堵塞可能与这一因素有关.
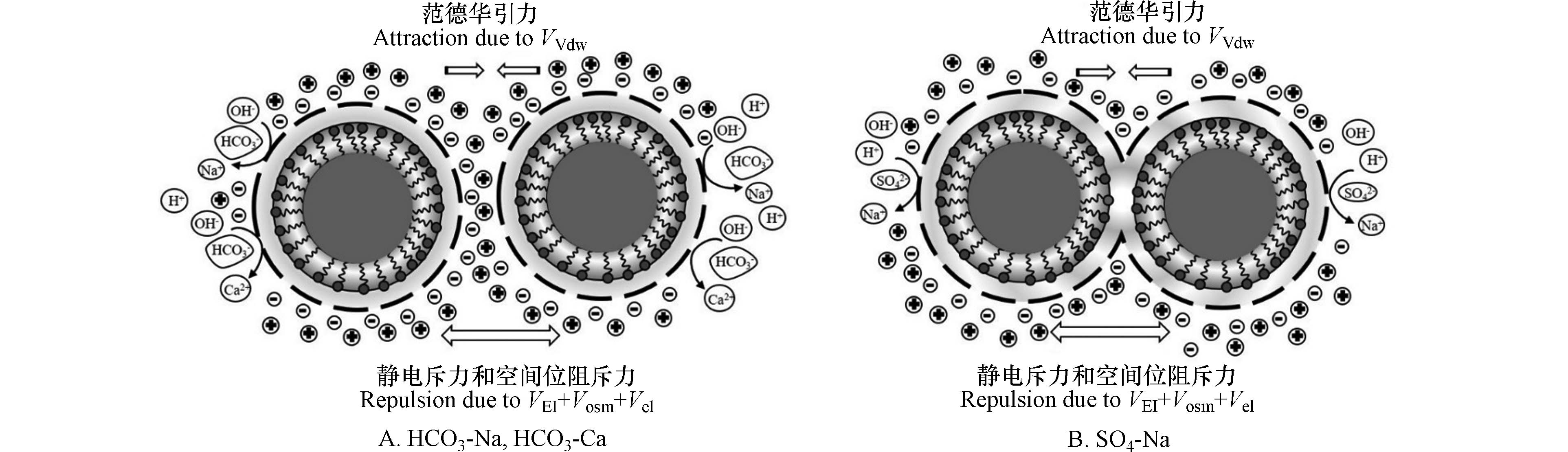
通过对比TSI值,发现最大势垒与TSI值呈现良好的对应关系,水化学特征对纳米乳化油稳定性的影响遵循高含盐量大于低含盐量,且高含盐量(3.0 g·L−1)中的SO4型大于HCO3型. 相同含盐量下,SO4-Na型水中的最大势垒显著降低,含盐量为3.0 g·L−1时,势垒(−0.3 kT,2.3 nm)消失,表明液滴易发生不可逆的聚集而加速乳液的失稳.由此说明,高强度离子下液滴表面负电性、粒径和黏度的减小是导致纳米乳化油稳定性降低的内在原因,它们分别影响了双电层的厚度,油水界面膜的水化层强度,进而减弱了液滴间的静电斥力和空间位阻斥力(图9). 液滴在HCO3型体系中的最大势垒高于SO4型,由于HCO3型体系中非离子表面活性剂优先吸附周围的OH-,使液滴表面负电性增强,虽然离子强度的增加会影响液滴界面的膜强度,但二者的叠加减缓了最大势垒的降低.高含盐量(3.0 g·L−1)下,HCO3-Ca型水中的纳米液滴最大势垒 (15.2 kT,1.1 nm)低于HCO3-Na型(24.6 kT,1.1 nm)(图8(a)和(b)),这是由于Ca2+比Na+的化合价高,高价态离子对纳米液滴表面的影响更为显著. 然而,在低含盐量下,最大势垒与TSI值有一定差异,扩展DLVO理论不能完全解释纳米乳化油的稳定性,说明低含盐量影响下内在机理更加复杂,有待于进一步深入研究.
-
(1)随含盐量增加,纳米乳化油稳定性表现出较大差异.低含盐量(小于1.0 g·L−1)下,HCO3-Na型和HCO3-Ca型水中的纳米乳化油稳定性逐渐降低,高含盐量(3.0 g·L−1)水中稳定性分别降低50%;在低含盐量(小于1.0 g·L−1)的SO4-Na型水中,纳米乳化油稳定性变化不明显,高含盐量(3.0 g·L−1)水中稳定性降低86%.纳米乳化油顶部的失稳是导致整体稳定性降低的原因.
(2)在HCO3型水中,纳米乳化油Zeta电位的绝对值增加;SO4型水中Zeta电位的绝对值降低,由于HCO3型水呈弱碱性,体系中更多的OH-易被非离子表面活性剂的亲水基吸附,而使纳米乳化油表面负电性增加.在HCO3型水中,纳米乳化油流变特性无显著变化;高含盐量(3.0 g·L−1)的SO4-Na型水中,粒径分布变陡,平均粒径和黏度略有减小.
(3)扩展DLVO理论模型有效解释了纳米乳化油稳定性变化,3种水化学特征对纳米乳化油稳定性的影响遵循高含盐量大于低含盐量,且高含盐量(3.0 g·L−1)中的SO4型大于HCO3型.这是由于离子强度增加,导致纳米液滴双电层被压缩,油水表面膜强度减小,静电斥力和空间位阻斥力降低,进而随间距的缩小范德华力剧增,液滴聚集上浮,体系稳定性降低.
地下水水化学特征对纳米乳化油稳定性的影响
Effect of groundwater hydrochemical characteristics on the stability of nano-emulsified oil
-
摘要: 原位强化土著微生物修复地下水污染的应用中,纳米乳化油的迁移性和分散性制约其修复效果,其中地下水水化学特征引起的纳米乳化油聚集和失稳可能是阻碍修复效率的重要影响因素. 据此,本文选取常见的HCO3-Na、HCO3-Ca、SO4-Na的3种典型地下水化学类型,配制不同含盐量的水化学溶液,探讨水化学类型及含盐量对纳米乳化油稳定性的影响. 结果表明,在HCO3-Na和HCO3-Ca型水中,纳米乳化油稳定性随含盐量增加而逐渐降低;在含盐量为3.0 g·L−1的SO4-Na型水中,纳米乳化油稳定性急剧降低. 进一步分析发现,整体稳定性降低是由顶部失稳引起,而不同阴离子是导致纳米乳化油稳定性差异的主要原因. 主要体现在表面电性和流变特性上,在HCO3型水中,纳米乳化油Zeta电位与含盐量呈负相关,其流变特性变化不显著;在SO4型水中,纳米乳化油Zeta电位与含盐量呈正相关,含盐量为3.0 g·L−1时,平均粒径和黏度均略有减小. 采用扩展DLVO理论进一步分析纳米乳化油稳定性降低的原因,发现含盐量增加影响纳米液滴双电层厚度和油水界面膜强度,从而造成纳米液滴静电斥力和空间位阻斥力的降低,其中高含盐量(3.0 g·L−1)的SO4型体系更不利于纳米乳化油的稳定.Abstract: The migration and dispersivity of nano-emulsified oil restrict its efficiency in groundwater pollution remediation by in-situ strengthening indigenous microorganisms, in which the aggregation and instability of nano-emulsified oil caused by hydrochemical characteristics may be an important factor. Therefore, three groundwater chemical types, i.e., HCO3-Na, HCO3-Ca and SO4-Na were prepared with different salt content in this work to investigate the effects of hydrochemical types and salt content on the stability of nano-emulsified oil. The results showed that the stability of nano-emulsified oil decreased gradually with increase of salt content in HCO3-Na and HCO3-Ca type waters. In SO4-Na type water with salt content of 3.0 g·L−1, the stability of nano-emulsified oil decreased sharply. Further analysis demonstrated that the reduction of overall stability was caused by instability in the top section, and different anions were the main reason for the difference in stability of nano-emulsified oil, mainly reflecting in the interface electrical properties and rheological properties. Zeta potential of nano-emulsified oil was negatively correlated with salt content in HCO3 type water, whereas it was positively correlated with salt content in SO4 type water. The changes of nano-emulsified oil rheological properties in HCO3 type water were not significant. In comparison, the average size and viscosity of nano-emulsified oil in SO4-Na type water with salt content of 3.0 g·L−1 decreased slightly. The reason of stability reduction in nano-emulsified oil was further analyzed by extended DLVO theory. It was found that the increase of salt content affected the thickness of electric double layer and the strength of oil-water interface film of nanodroplets, resulting in decrease in the electrostatic repulsion and steric hindrance repulsion of nanodroplets. The SO4 system with high salt content (e.g., 3.0 g·L−1) was more unfavorable to the stability of nano-emulsified oil.
-
Key words:
- hydrochemical types /
- nano-emulsified oil /
- stability /
- salt content /
- extended DLVO theory
-

-
表 1 水化学类型和含盐量的设置
Table 1. Hydrochemical types and salt content settings
水化学类型(Hydrochemical types) 含盐量/( g∙L−1) 去离子水 — — — — HCO3-Na 0.3 0.7 1.0 3.0 HCO3-Ca 0.3 0.7 1.0 3.0 SO4-Na 0.3 0.7 1.0 3.0 -
[1] FENG J, ESQUENA J, RODRIGUEZ-ABREU C, et al. Key features of nano-emulsion formation by the phase inversion temperature method [J]. Journal of Dispersion Science and Technology, 2020, 42(7): 1073-1081. [2] DING L J, DONG J, BAI J, et al. Migration and evolution of an in situ bioreactive zone formed with emulsified vegetable oil for the long-term remediation of nitrobenzene-contaminated groundwater [J]. Journal of Hydrology, 2021, 593: 125914. doi: 10.1016/j.jhydrol.2020.125914 [3] BORDEN R C, RICHARDSON S D, BODOUR A A. Enhanced reductive dechlorination of trichloroethene in an acidic DNAPL impacted aquifer [J]. Journal of Environmental Management, 2019, 237(3): 617-628. [4] 郑家传, 张建荣, 刘希雯, 等. 污染场地六价铬的还原和微生物稳定化研究 [J]. 环境科学, 2014, 35(10): 3882-3887. ZHENG J C, ZHANG J R, LIU X W, et al. Bioremediation of chromium(Ⅵ) contaminated site by reduction and microbial stabilization of chromium [J]. Environmental Science, 2014, 35(10): 3882-3887(in Chinese).
[5] ZHANG J Q, WU J, CHAO J B, et al. Simultaneous removal of nitrate, copper and hexavalent chromium from water by aluminum-iron alloy particles [J]. Journal of Contaminant Hydrology, 2019, 227(104): 103541. [6] LI B, WU W M, WATSON D B, et al. Bacterial community shift and coexisting/coexcluding patterns revealed by network analysis in a uranium-contaminated site after bioreduction followed by reoxidation[J]. Applied and Environmental Microbiology, 2018, 84(9):e02885-17. [7] 连玉倩, 何江涛, 梁雨, 等. 纳米乳化油强化硝酸盐反硝化产气变化研究 [J]. 中国环境科学, 2018, 38(6): 2105-2115. doi: 10.3969/j.issn.1000-6923.2018.06.013 LIAN Y Q, HE J T, LIANG Y, et al. Simulation experiments on gas change in enhanced denitrification of nitrate process by nano emulsified oil [J]. China Environmental Science, 2018, 38(6): 2105-2115(in Chinese). doi: 10.3969/j.issn.1000-6923.2018.06.013
[8] 黄斯艺, 何江涛, 劳天颖, 等. 纳米乳化油修复硝酸盐污染地下水过程中的微生物特征模拟实验研究 [J]. 环境科学学报, 2020, 40(4): 1242-1249. HUANG S Y, HE J T, LAO T Y, et al. Experimental study of microbial characteristics in the process of in situ nitrate pollution remediation by nano emulsified oil [J]. Acta Scientiae Circumstantiae, 2020, 40(4): 1242-1249(in Chinese).
[9] CAPEK I. Degradation of kinetically-stable O/W emulsions [J]. Advances in Colloid and Interface Science, 2004, 107(2/3): 125-155. doi: 10.1016/S0001-8686(03)00115-5 [10] ASWATHANARAYAN J B, VITTAL R R. Nanoemulsions and their potential applications in food industry [J]. Frontiers in Sustainable Food Systems, 2019, 3: 95. doi: 10.3389/fsufs.2019.00095 [11] SARI T P, MANN B, KUMAR R, et al. Preparation and characterization of nanoemulsion encapsulating curcumin [J]. Food Hydrocolloids, 2015, 43: 540-546. doi: 10.1016/j.foodhyd.2014.07.011 [12] MULLER K A, ESFAHANI S G, CHAPRA S C, et al. Transport and retention of concentrated oil-in-water emulsions in porous media [J]. Environmental Science & Technology, 2018, 52(7): 4256-4264. [13] 方华, 沈冰冰, 荆洁, 等. 水中C60纳米颗粒的稳定性研究 [J]. 环境科学, 2014, 35(4): 1337-1342. FANG H, SHEN B B, JING J, et al. Stability of C60 nanoparticles in aquatic systems [J]. Environmental Science, 2014, 35(4): 1337-1342(in Chinese).
[14] TORKZABAN S, BRADFORD S A, VANDERZALM J L, et al. Colloid release and clogging in porous media: Effects of solution ionic strength and flow velocity [J]. Journal of Contaminant Hydrology, 2015, 181: 161-171. doi: 10.1016/j.jconhyd.2015.06.005 [15] LI T T, JIN Y, HUANG Y F, et al. Observed dependence of colloid detachment on the concentration of initially attached colloids and collector surface heterogeneity in porous media [J]. Environmental Science & Technology, 2017, 51(5): 2811-2820. [16] LINDOW N L, BORDEN R C. Anaerobic bioremediation of acid mine drainage using emulsified soybean oil [J]. Mine Water and the Environment, 2005, 24(4): 199-208. doi: 10.1007/s10230-005-0096-9 [17] COULIBALY K M, BORDEN R C. Impact of edible oil injection on the permeability of aquifer sands [J]. Journal of Contaminant Hydrology, 2004, 71(1/4): 219-237. doi: 10.1016/j.jconhyd.2003.10.002 [18] MEI Z, XU J, SUN D J. O/W nano-emulsions with tunable PIT induced by inorganic salts [J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2011, 375(1/3): 102-108. [19] QIAN C, DECKER E A, XIAO H, et al. Physical and chemical stability of β-carotene-enriched nanoemulsions: Influence of pH, ionic strength, temperature, and emulsifier type [J]. Food Chemistry, 2012, 132(3): 1221-1229. doi: 10.1016/j.foodchem.2011.11.091 [20] REN G H, SUN Z C, WANG Z Z, et al. Nanoemulsion formation by the phase inversion temperature method using polyoxypropylene surfactants [J]. Journal of Colloid and Interface Science, 2019, 540: 177-184. doi: 10.1016/j.jcis.2019.01.018 [21] 陈宗淇, 王光信, 徐桂英. 胶体与界面化学[M]. 北京: 高等教育出版社, 2001. CHEN Z Q, WANG G X, XU G Y. Colloid and interface chemistry[M]. Beijing: Higher Education Press, 2001(in Chinese).
[22] HE B N, HE J T, ZOU H, et al. Pore-scale identification of residual morphology and genetic mechanisms of nano emulsified vegetable oil in porous media using 3D X-ray microtomography [J]. Science of the Total Environment, 2021, 763: 143015. doi: 10.1016/j.scitotenv.2020.143015 [23] HERRINGTON T M, MIDMORE B R, SAHI S S. Influence of non-ionic surfactants on the equilibrium distance of approach of emulsion droplets [J]. Journal of the Chemical Society, Faraday Transactions 1, 1982, 78(9): 2711-2720. doi: 10.1039/f19827802711 [24] AISHWARYA S, SHANTHI J, SWATHI R. Surface energy calculation using Hamaker's constant for polymer/silane hydrophobic thin films [J]. Materials Letters, 2019, 253: 409-411. doi: 10.1016/j.matlet.2019.07.123 [25] DUTTA N, GREEN D. Nanoparticle stability in semidilute and concentrated polymer solutions [J]. Langmuir, 2008, 24(10): 5260-5269. doi: 10.1021/la7027516 [26] DICKINSON E. Strategies to control and inhibit the flocculation of protein-stabilized oil-in-water emulsions [J]. Food Hydrocolloids, 2019, 96: 209-223. doi: 10.1016/j.foodhyd.2019.05.021 [27] VINCENT B. The calculation of depletion layer thickness as a function of bulk polymer concentration [J]. Colloids and Surfaces, 1990, 50: 241-249. doi: 10.1016/0166-6622(90)80267-8 [28] DU Y, YIN L J, HAN Q H, et al. Effect of NaCas/Tween 80 ratios and environmental stresses on the physical stability of perilla oil-in-water emulsions [J]. Journal of Food Processing and Preservation, 2018, 42(4): e13568. doi: 10.1111/jfpp.13568 [29] KOWALSKA M, ŻBIKOWSKA A. Study of stability of sesame oil-in-water emulsions determined using an optical analyzer and measurement of particle size and distribution [J]. Journal of Dispersion Science and Technology, 2016, 37(10): 1408-1414. doi: 10.1080/01932691.2015.1111143 [30] RAHMAN M, RUB M A, HOQUE M A, et al. Clouding and thermodynamic behaviours of nonionic surfactant: Effects of cefixime trihydrate drug and different electrolytes [J]. Journal of Molecular Liquids, 2020, 312(2): 113366. [31] LIU Y, WEI Z C, DENG Y Y, et al. Comparison of the effects of different food-grade emulsifiers on the properties and stability of a casein-maltodextrin-soybean oil compound emulsion [J]. Molecules, 2020, 25(3): 458. doi: 10.3390/molecules25030458 [32] ROLDAN-CRUZ C, VERNON-CARTER E J, ALVAREZ-RAMIREZ J. Assessing the stability of Tween 80-based O/W emulsions with cyclic voltammetry and electrical impedance spectroscopy [J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2016, 511: 145-152. [33] 李晓佩, 黄昆, 林洁媛, 等. Hofmeister离子序列及其调控水溶液中大分子溶质行为的作用机制 [J]. 化学进展, 2014, 26(8): 1285-1291. LI X P, HUANG K, LIN J Y, et al. Hofmeister ion series and its mechanism of action on affecting the behavior of macromolecular solutes in aqueous solution [J]. Progress in Chemistry, 2014, 26(8): 1285-1291(in Chinese).
[34] NAZARZADEH E, ANTHONYPILLAI T, SAJJADI S. On the growth mechanisms of nanoemulsions [J]. Journal of Colloid and Interface Science, 2013, 397: 154-162. doi: 10.1016/j.jcis.2012.12.018 [35] YOSHIHARA K, OHSHIMA H, MOMOZAWA N, et al. Binding constants of symmetric or antisymmetric electrolytes and aggregation numbers of oil-in-water type microemulsions with a nonionic surfactant [J]. Langmuir, 1995, 11(8): 2979-2984. doi: 10.1021/la00008a022 [36] FAN Y X, WANG Y L. Self-assembly and functions of star-shaped oligomeric surfactants [J]. Langmuir, 2018, 34(38): 11220-11241. doi: 10.1021/acs.langmuir.8b00290 [37] SHARIF A A M, ASTARAKI A M, AZAR P A, et al. The effect of NaCl and Na2SO4 concentration in aqueous phase on the phase inversion temperature O/W nanoemulsions [J]. Arabian Journal of Chemistry, 2012, 5(1): 41-44. doi: 10.1016/j.arabjc.2010.07.021 [38] TUFENKJI N, ELIMELECH M. Breakdown of colloid filtration theory: Role of the secondary energy minimum and surface charge heterogeneities [J]. Langmuir, 2005, 21(3): 841-852. doi: 10.1021/la048102g -



 下载:
下载: