-
近年来我国经济的飞速发展,城市生活污水污泥产量连年攀升,随之而来的是污泥处理的压力。一方面,剩余污泥含有重金属、有机污染物和病原微生物等有毒有害物质,如果处理不当,会给环境造成严重污染。另一方面,污泥是一种拥有巨大潜力的生物资源,其有机质含量在50%左右,含有丰富的蛋白质、多糖、腐殖酸和核酸[1]。在传统污水二级生化处理中,进水中近90%的磷和部分的氮最终会转移至污泥中,因此剩余污泥含有丰富的有机质和氮磷养分,若不加以合理利用是一种资源浪费。
污泥固相中营养物质的有效释放是实现污泥有机质和氮磷回收的重要前提。污泥的破解方法有各种物理化学法,如热水解、超声、高压均质法等。碱处理作为一种常用的化学预处理方法,具有操作方便、设备简单、效率高等优点。首选NaOH作为处理试剂,其比Ca(OH)2有更高的增溶效率[2]。碱法常常与其他工艺(如超声[3]、热处理[4]和高压均质法[5]等)联合处理,联合处理对污泥具有更高效的破解能力。微波法在污泥处理中的潜力已得到广泛认可[6],微波产生的热效应和非热效应能高效破解污泥,所以碱联合微波组合工艺拥有巨大潜力。
为了回收利用污泥上清液中丰富的营养物质,可通过磷酸铵镁沉淀法回收氮和磷,其产物鸟粪石可作缓释肥料。但实际应用中受各种因素(例如高离子强度、高碱度和Ca2+干扰)限制[7],且磷酸铵镁沉淀法只能回收PO43--P和NH4+-N等形式的无机盐,上清液中丰富的有机质仍无法利用。硅烷交联剂是一种两性表面活性剂,一个分子中同时拥有烷氧基和有机官能团,烷氧基水解产生的硅烷醇基团能以共价键的形式与无机材料结合,有机官能团与聚合物作用,可显著提高无机/聚合物表面附着力[8]。因此,硅烷交联剂有望解决污泥上清液中有机质无法高值利用的问题。硅烷交联剂成本低、环境友好,被广泛应用于复合材料、纳米材料等表面改性。近年来学者们将其应用于环境领域,Zhou等使用(3-氨基丙基)三乙氧基硅烷有效分离水溶性腐殖酸[9]。甲基三乙酰氧基硅烷(MTAC),常温下为无色透明液体,低温下为白色结晶体,结构式为CH3—Si—(COOCH3)3,其酰氧基相较于其他基团(如甲氧基、乙氧基)更为活泼,分解速度也更快[10]。并且根据美国环境保护署的数据资料显示,MTAC的半数致死浓度(LD50)为2060 mg·kg−1,属于低毒化合物。MTAC与水就能交联,生成具有良好生物相容性的聚硅氧烷和易生物降解的乙酸,且污泥上清液中氮元素的嵌入能够加速聚硅氧烷的水解,从而提高其生物降解性[11]。因此,MTAC的交联聚合反应是一种从污泥上清液中回收有机质和氮磷的有效途径。
本研究采用碱联合微波组合工艺预处理污泥,投加MTAC回收上清液中有机质和氮磷,研究了碱联合微波处理对污泥中有机质及氮磷的释出的影响并优化反应条件,探究了MTAC交联聚合回收污泥上清液营养物质的可行性,利用扫描电镜-能谱(SEM-EDS)、傅里叶红外光谱图(FTIR)、X射线光电子能谱分析(XPS)和热重差示扫描量热法(TG-DSC)对絮凝聚合物进行形态和化学构造分析,旨在探究交联聚合法分离回收有机质和氮磷的机制。
-
试验所用污泥取自上海某城镇污水处理厂污泥浓缩池,该厂采用A2O活性污泥处理工艺,污泥取回后过筛去除直径大于4 mm的杂质,保存在4 ℃冰箱备用。具体理化性质如表1。
-
本试验分别投加梯度剂量(0.32、0.48、0.64、0.80、0.96、1.12、1.28 g·L−1)的NaOH于250 mL污泥中,用磁力搅拌器(150 r·min−1)保证反应充分进行,间隔固定时(10、20、30、40 min),取样分析以确定NaOH的最佳剂量。污泥经碱处理最佳条件后,用不同功率(160、320、480、640、800 W)微波照射,间隔固定时间(30、60、90、120 s),取样分析以确定碱联合微波处理最佳条件。污泥经碱联合微波最佳条件处理后,在3000 r·min−1下离心10 min得到污泥上清液,投加梯度剂量(0.038、0.076、0.134、0.189 mol·L−1)的硅烷交联剂-甲基三乙酰氧基硅烷(MTAC)待反应完全,离心得到聚合后的上清液,真空干燥得到的絮凝沉淀物用于后续分析。
-
污泥的TS、VS 和上清液中的SCOD、TN和TP根据美国APHA标准方法测定[12];用雷磁pH计(PHS-25,中国)测定pH;SPS采用苯酚-硫酸法测定[13];SPN采用福林酚试剂法测定[14]。絮凝聚合物采用扫描电镜-能谱(SEM-EDS)观察其微观形貌及元素组成;傅里叶红外光谱仪(FT-IR)表征其表面官能团;X射线光电子能谱仪(XPS)评估聚合物表面组成和化合价状态;比表面积和孔径分布由BET确定。
-
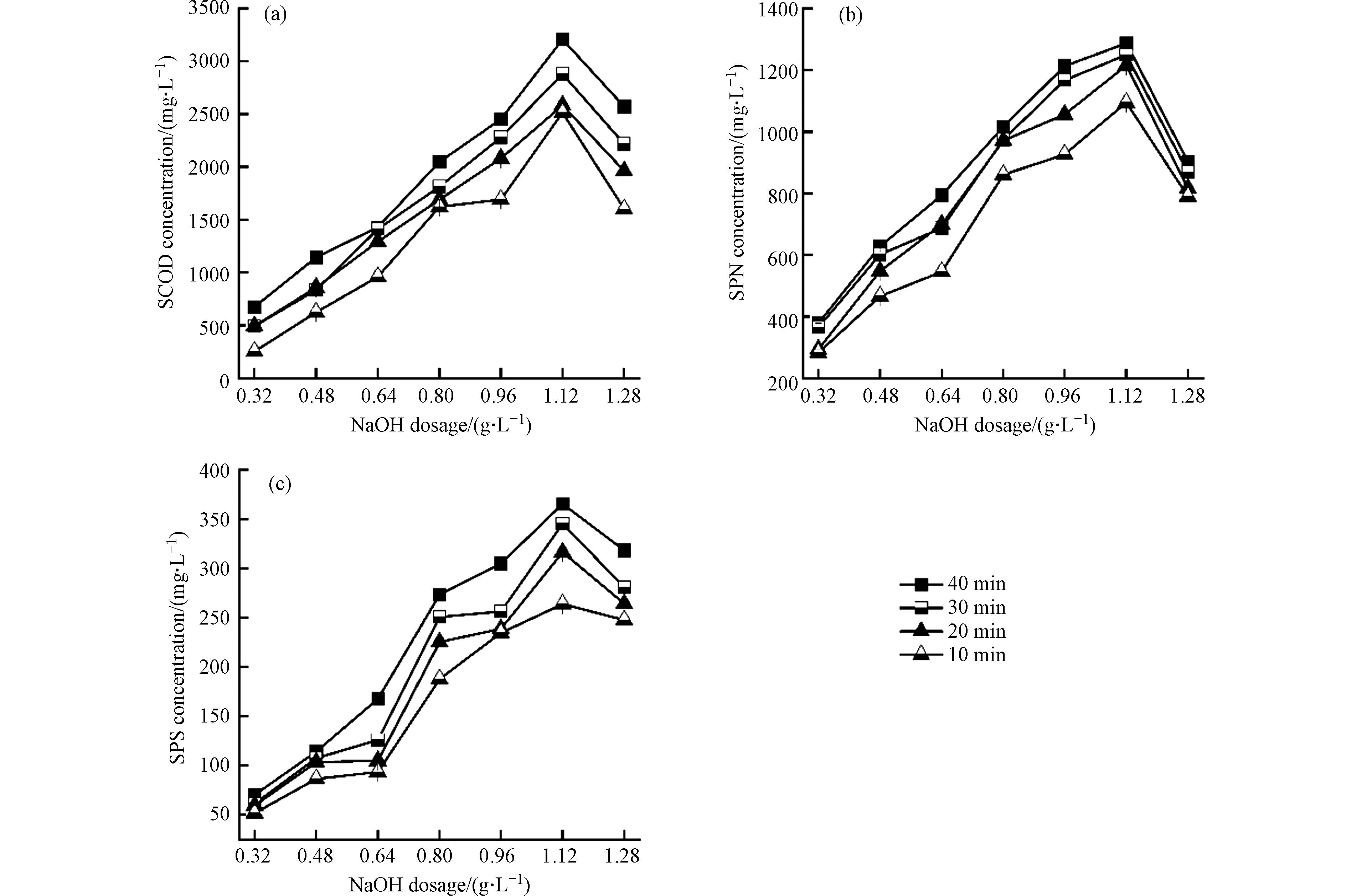
在碱预处理过程中,细胞结构被破坏,污泥细胞中的有机物释放至液相中,致使溶解性有机质增加。蛋白质和碳水化合物是SCOD的主要成分,可检测SCOD、SPN和SPS的浓度评价有机物质的溶出效果。如图1所示,相同NaOH投加量下污泥中SCOD、SPN和SPS的浓度随时间递增而变高。NaOH剂量为1.12 g·L−1,污泥碱解30 min时,SCOD为2878.44 mg·L−1,相比原始污泥276.95 mg·L−1增加了9.39倍;当碱解40 min后SCOD为3206.72 mg·L−1,比原污泥增加了10.58倍。因为碱处理条件下,有机物的溶出分为两个阶段:前30 min快速增溶阶段和之后的缓慢阶段[15]。
NaOH剂量也是影响有机物溶出的重要因素,如图1所示,SCOD、SPN和SPS的浓度皆随着NaOH剂量增加而增加。碱解40 min后,当NaOH剂量为1.12 g·L−1时污泥的SCOD、SPN和SPS的浓度最高,分别为3206.72、1248.86、365.34 mg·L−1;当NaOH剂量超过1.12 g·L−1时,SCOD、SPN和SPS的浓度均有所下降。这是因为污泥中绝大多数有机物位于细胞内,碱处理时羟基自由基以多种方式与细胞壁发生反应,如与细胞壁中脂质的皂化反应,从而破坏微生物结构[16],释放出絮体内和细胞内的有机物质。而低剂量的NaOH仅能破坏污泥细胞外层的絮体结构,无法破坏内层的细胞结构,故而有机物的溶出效果不佳。最佳剂量为1.12 g·L−1时,此时pH约为11,细胞难以维持平衡渗透压发生破裂,细胞壁、细胞膜和细胞核等被大幅损伤[17],细胞内物质大量释出。当NaOH剂量进一步提高时,较弱和较敏感的细胞被选择性优先破坏后,污泥不再进一步发生分解[17],此外,极端的碱性环境会改变蛋白质空间结构使其失去自然结构同时引起RNA水解和脂质皂化[15]。基于上述结果,NaOH最佳剂量为1.12 g·L−1,碱解时间确定为40 min以确保有机质充分溶出。
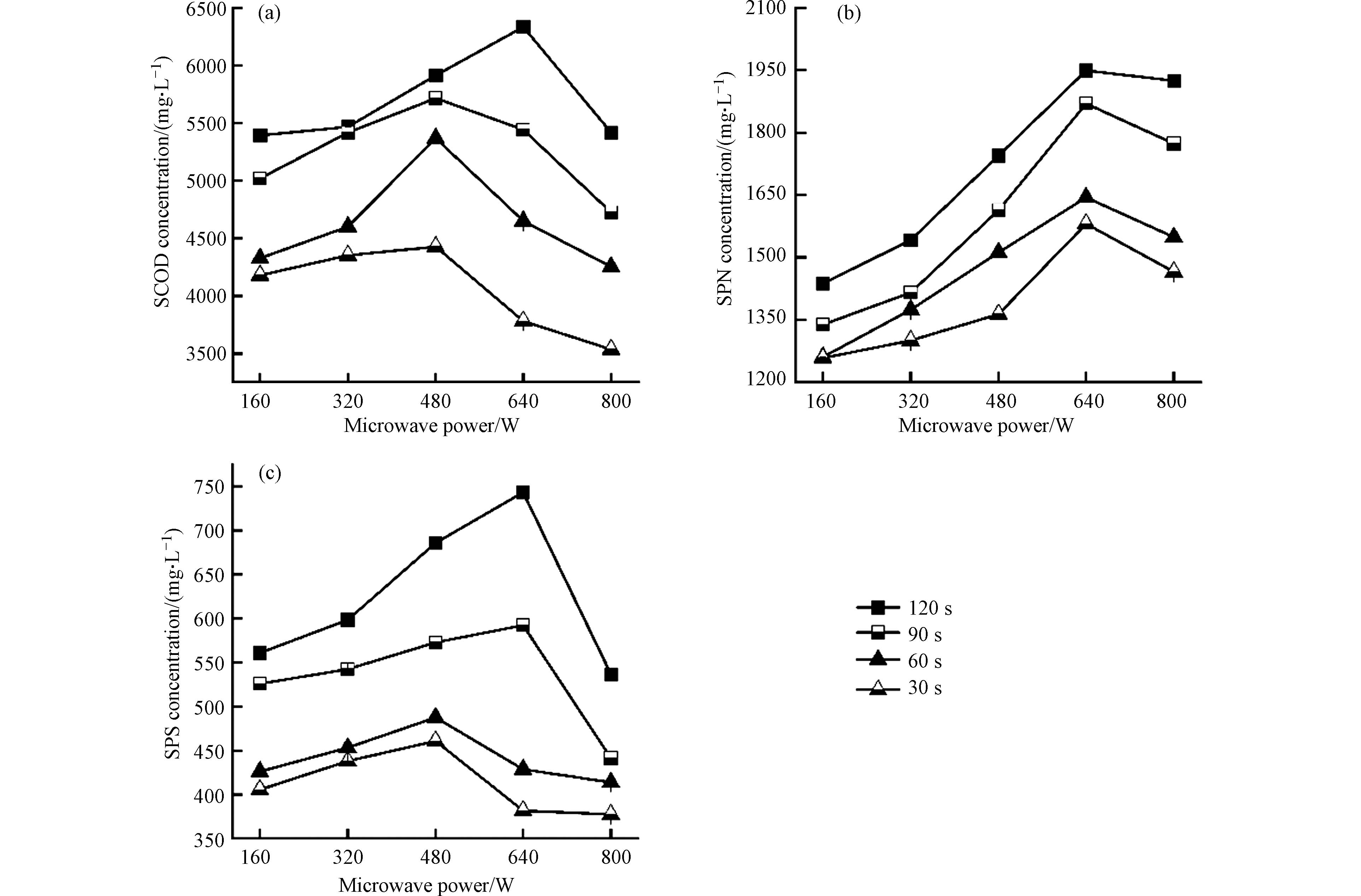
为了进一步增加污泥中有机质及氮磷的释出,在上述最佳碱处理条件(NaOH剂量1.12 g·L−1,40 min)基础上再对污泥进行微波辐射,比较了不同微波辐射功率和辐射时间的影响。如图2所示,观察到随着微波功率和反应时间的增加,SCOD、SPN和SPS的浓度都逐渐增加,最高达到了6335.56、1949.76、743.08 mg·L−1 (微波功率640 W,辐射时间120 s),比单独碱处理后的浓度分别增加了97.57%、55.88%、103.39%。SCOD和SPS较SPN增溶更明显,与Lise等的结果一致[18]。在微波照射下,污泥中细胞膜等大分子极化侧链中偶极子取向快速的变化导致氢键等维持大分子结构的次级键断裂产生的非热效应[19],使得污泥絮体进一步被破坏。同时污泥中存在的偶极分子(如水、蛋白质和脂质等)相互作用,由此产生的分子旋转导致摩擦产生热效应[20], 温度的升高不仅使得有机物的溶解度增加,也使得污泥细胞破裂更彻底,从而释放出更多胞内物质。当微波功率进一步提高时,SCOD、SPN和SPS浓度均出现了不同程度的降低,因为更高的辐射能量能够分解大分子有机物为小分子[21],但也会使得一些易挥发有机质挥发,同时也会改变有机物的性质例如降低了蛋白质在水中的溶解度。较高的温度环境下,含游离氨基的化合物和羰基化合物发生缩聚反应,生成类黑精、吡嗪化合物等不溶于水且难生物降解的物质[22],降低了蛋白质和糖在水中的溶解度,这也是SPN和SPS浓度下降的原因。同时考虑到更高功率的微波辐射和反应时间会产生更高的能耗,因此在碱处理基础上,微波选择功率640 W,辐射时间120 s时, SCOD、SPS和SPN较原污泥分别增溶了29.16、10.48、21.16倍,最大限度释放出了污泥中有机质。
-
污泥经单独碱处理和联合处理后,总氮的释放如图3(a)和(b)所示,低剂量的NaOH仅释放出了絮体结构中的,未能破解细胞,故TN溶出效果不显著,随着NaOH剂量的增加,细胞内的含氮物质如氨基酸、蛋白质等释放出来。当NaOH剂量继续提高,高pH值环境使得部分氨氮转化为氨气从污泥中逸出[23],故TN浓度略有下降。相比于碱处理,微波照射对TN的溶出的效果不显著。低功率,短时间的微波辐射对氮溶出效果提升有限,高功率较长时间的辐射最高能够提升51.35%,较原污泥增加了5.15倍,是因为热效应导致蛋白质和氨基酸等有机物氨化。
污泥中主要含磷化合物为聚磷酸盐且不稳定。如图3(c)和(d)所示,与TN释放规律类似,低碱投加量仅释放出絮体的胞外磷,高剂量的NaOH破解了细胞后,胞内的多聚磷分解为焦磷酸盐和磷酸盐[24],同时由磷脂双分子层组成的细胞膜破裂也导致磷脂释放。一些结合态的磷在碱性条件下也更易释放到液相中。碱联合微波辐射对磷的释放效果比单独碱处理最高提升了25.13%,较原污泥增加了6.54倍。功率和反应时间的进一步增加使温度升高,污泥系统的重金属不断释放,并且与释出的磷形成沉淀导致TP浓度有所降低。
-
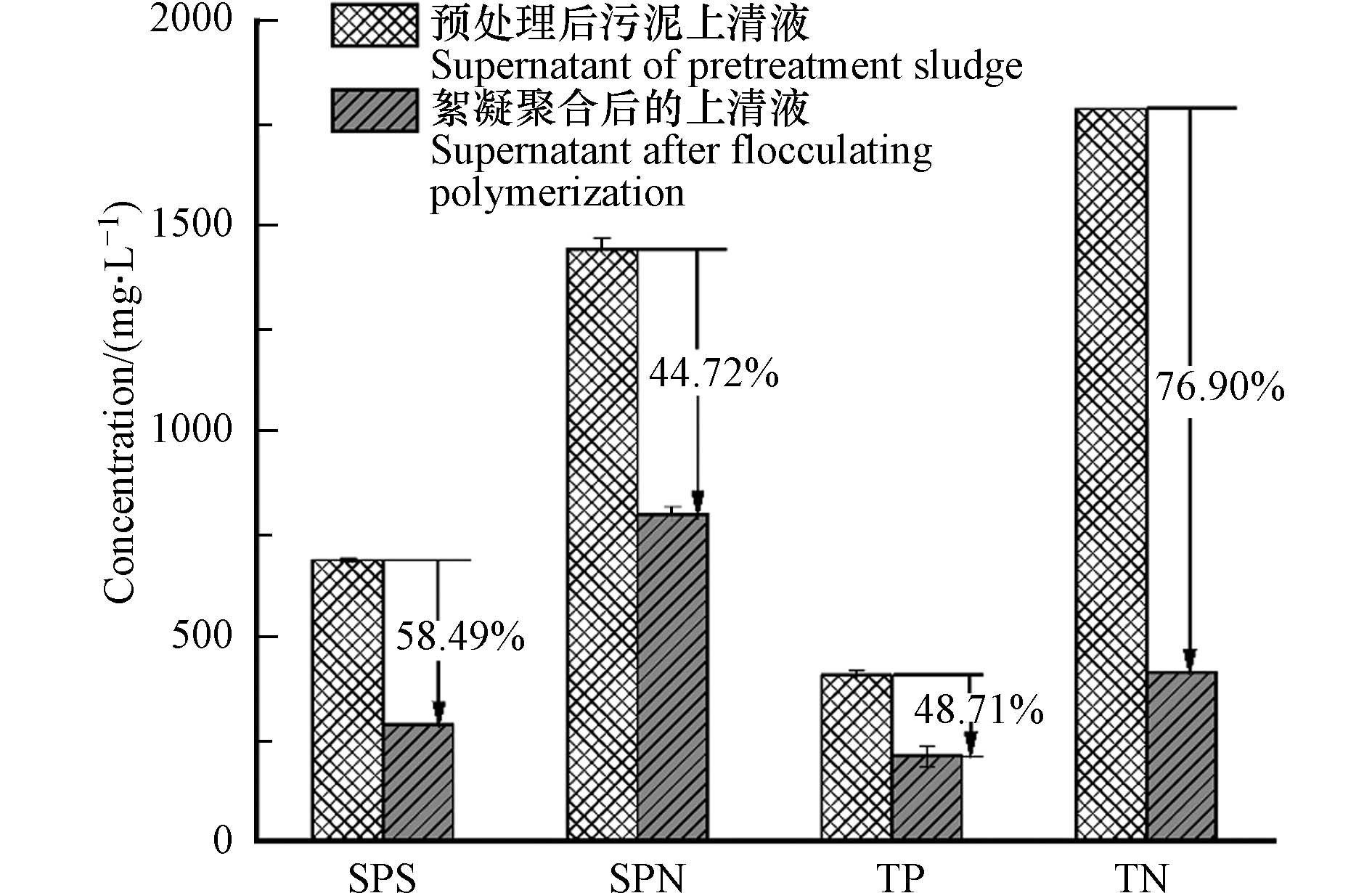
污泥经碱和微波联合预处理后分离出上清液,此时的上清液中含有从污泥中释出的大量有机质,通过投加交联剂MTAC,与上清液中有机质交联聚合生成絮凝聚合物从而达到分离回收的效果。具体回收效果如图4所示,TN的回收率高达76.90%,SPS、SPN、TP也分别分离回收了44.72%、58.49%、48.71%。Wei等[25]用磷酸铵镁沉淀法实现了46.88%磷酸盐回收和16.54%的氨氮回收,本研究的氮磷回收率更高。相较于传统的超声辅助酶解法[26]和热预处理酶解辅助法[27]单纯的提取回收蛋白质,本研究的交联聚合回收法不仅能够提取回收蛋白质等有机氮,还能通过交联和吸附作用将污泥上清液中NH4+-N和NOx-N等无机氮固定下来,高TN回收率也说明了这一点。氮磷高效回收的同时还实现了有机质的分离回收,弥补了鸟粪石沉淀法和层状双氢氧化物合成法只能单纯的回收氮磷或碳源的缺点,而且本研究的方法操作更加简便、快捷和高效。综上所述,MTAC能够有效交联聚合回收污泥上清液中的有机质及氮磷。
-
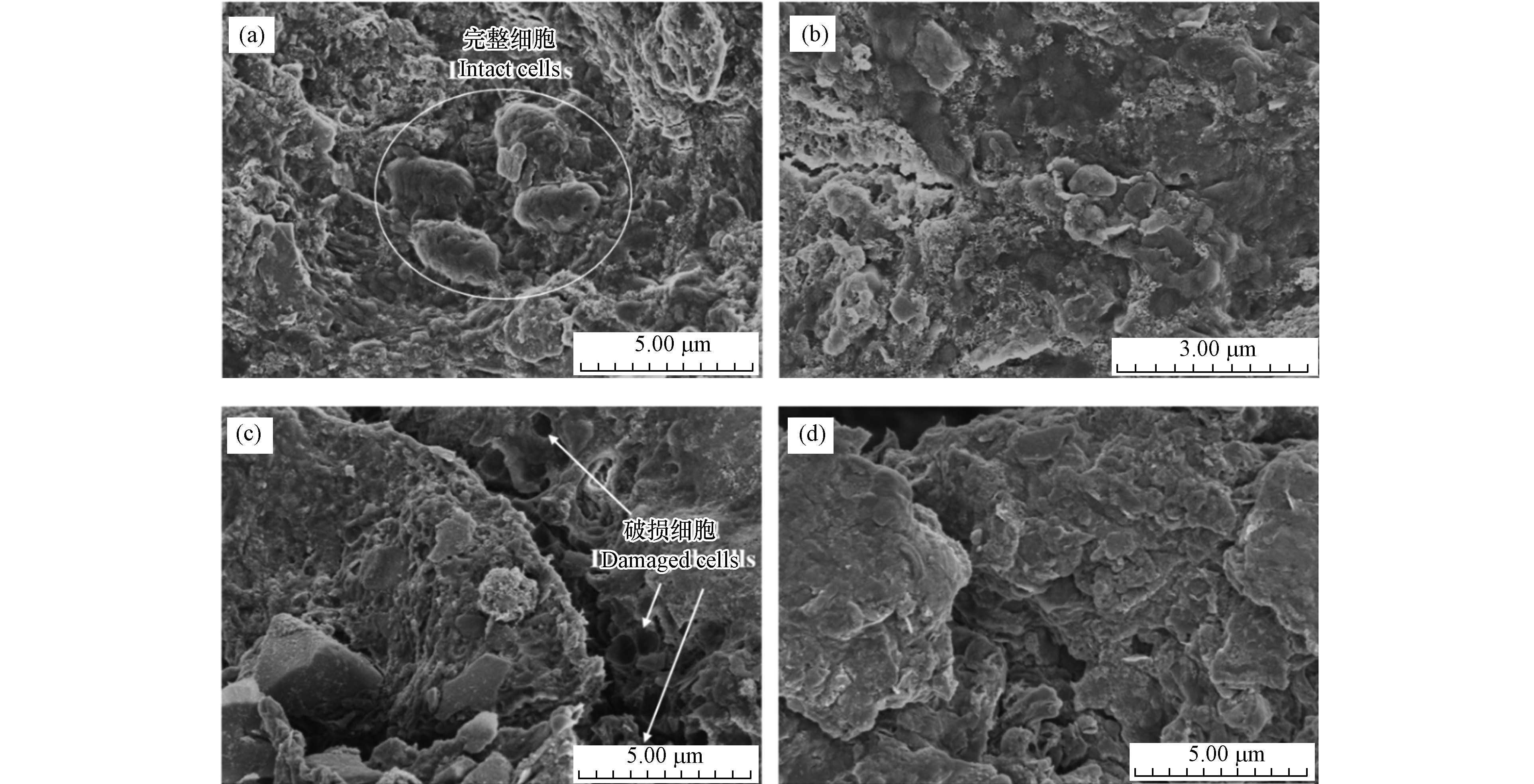
SEM表征可以直观地观察到预处理前后污泥絮体的微观形态变化,原泥、碱处理及其联合微波处理后的污泥表面形态如图5所示,原污泥中可以看到完整饱满的微生物细胞,表面被胞外聚合物所包裹。经过低剂量(0.48 g·L−1、40 min)的碱处理后,污泥表面塌陷,不再光滑,但仍能观察到完整的微生物细胞,这也直观证明了低剂量NaOH仅能破坏污泥絮体外部结构,对细胞的破坏作用十分有限。污泥经最佳碱处理条件(1.12 g·L−1、40 min)处理后,污泥絮体被破碎,观察到明显的空洞和破碎细胞,表明污泥细胞出现大量破损,释放出胞内物质,与肖本益等[28]观察到的结果一致。碱联合微波处理后,污泥中的微生物细胞彻底破碎,已观察不到细胞结构,说明碱和微波协同作用能进一步破解污泥细胞结构,污泥细胞的破裂导致大量有机物的溶出。这些有机质在微波热效应导致的高温环境下又重新结合在污泥表面,使其比原污泥表面更加粗糙和不规则[29-30]。
-
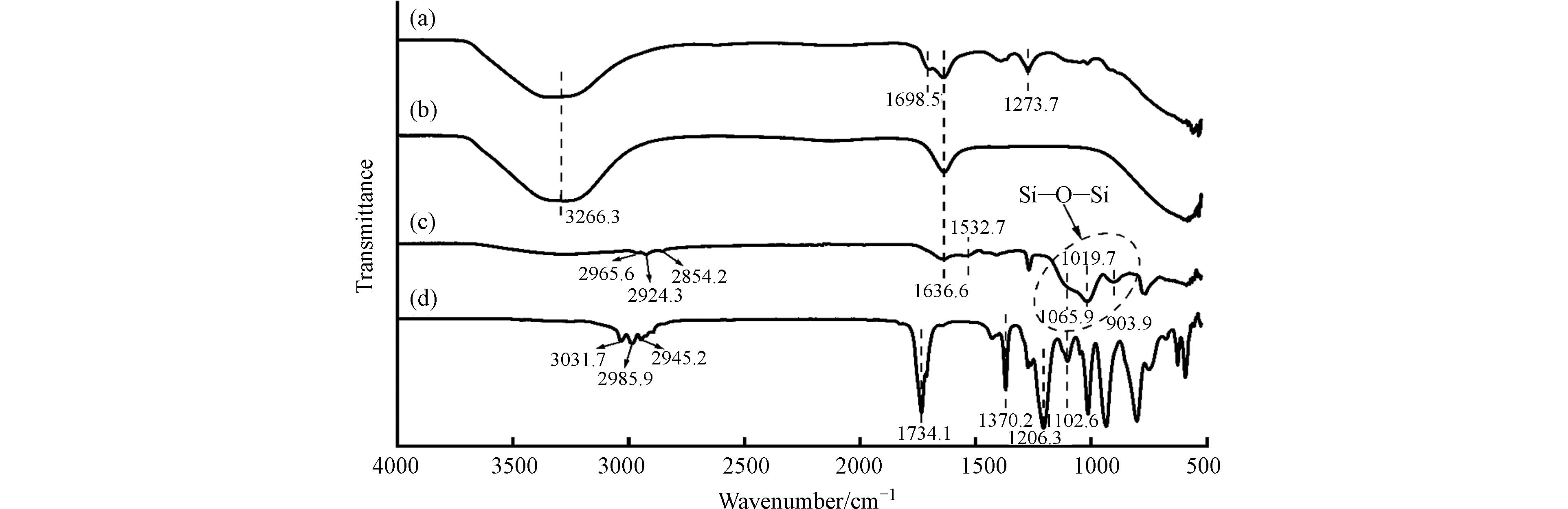
图6显示了预处理后污泥上清液、聚合反应后的上清液、絮凝聚合物和交联剂MTAC的FTIR光谱图。向预处理后污泥上清液中加入交联剂MTAC后,对比图6(a)和(b)可发现,MTAC中C=O (1734.1 cm−1)、—O—CO—CH3(1370.2 cm−1)、Si—O—COCH3(1102.6 cm−1)几处关键的官能团特征峰消失,这是MTAC水解导致的。随着絮凝物的形成,在1065、1019.7 、903.9 cm−1处出现了新的峰,表明形成了Si—O—Si和Si—O—C骨架基团[9]。MTAC中3031.7 、2985.9 、2945.2 cm−1处的特征峰是由Si—CH3中C—H振动产生的[31]。交联剂与污泥上清液反应后,絮凝聚合物中对应的Si—CH3特征峰出现明显的红移现象(2965.6 、2924.3 、2854.2 cm−1),且峰的强度较MTAC有所下降。上述结果证明了MTAC加入后污泥上清液与其发生了水解缩合作用。
图6(c)和(d)中位于3200.0—3600.0 cm−1的宽峰对应交联剂加入前后上清液中的—OH基团。预处理后污泥上清液中1698.5 cm−1和1636.6 cm−1两处特征峰,分别对应于蛋白质中酰胺Ⅰ带的伯酰胺和叔酰胺基团的振动[32],而1273.7 cm−1处特征峰归因于P=O的振动[33]。聚合后的上清液中伯酰胺和P=O基团特征峰消失,同时在生成的聚合絮凝物中出现了1636.6 cm−1和1532.7 cm−1两处峰,分别来自叔酰胺基团和酰胺Ⅱ带中C—N 拉伸伴随着 N—H 面内弯曲产生的振动[34]。上述种种变化表明了预处理后污泥的上清液中的一些含磷物质和含氮物质如蛋白质等参与MTAC的水解自缩合过程发生了共组装反应。
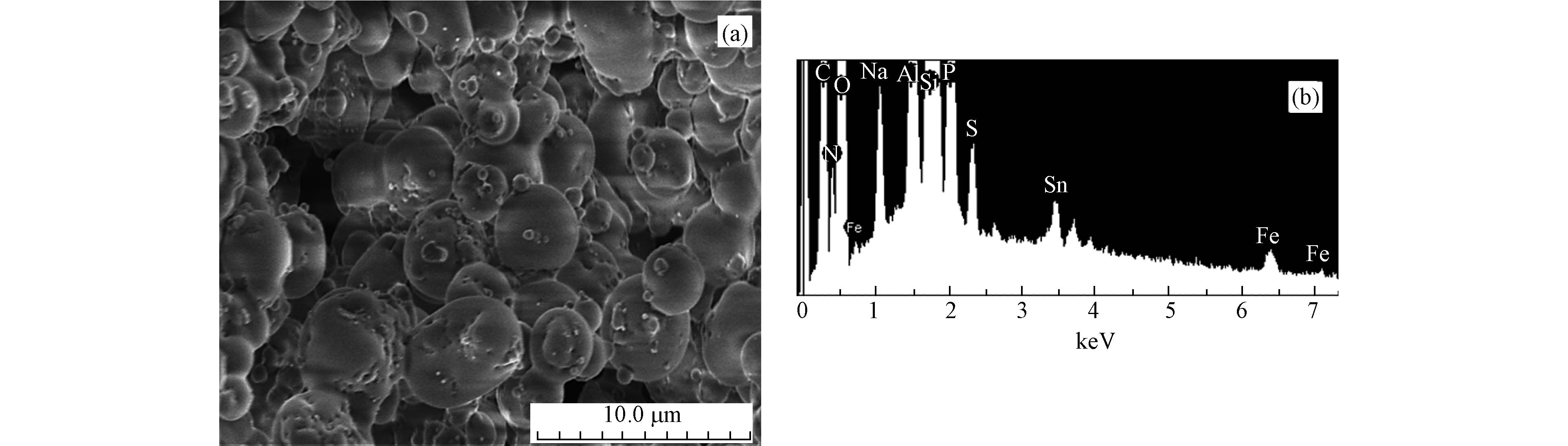
为进一步分析MTAC与污泥上清液的絮凝机理,对生成的絮凝聚合物进行XPS表征。如图7(a)所示,絮凝物的主要特征元素为O 1s、C 1s、N 1s、P 2p和Si 2p,元素含量测定结果表明N、P元素的占比分别为2.85%和0.95%。交联剂MTAC为不含N、P的硅氧类物质,故絮凝物中含有的N、P元素均来源于污泥上清液,这也间接证明了污泥上清液中的蛋白质和磷酸盐等含氮磷化合物被MTAC有效固定回收。
图7(b)和(c)显示了絮凝聚合物的C 1s和O 1s高分辨率光谱,其中C 1s的光谱根据分峰,能表明絮凝物中不同形态C元素的相对丰度等信息。由图7(b)可知,C分别和0、1和2个氧原子结合形成不同形态。其中最低的结合能为284.8 eV,表明以C—C形式存在;最高的结合能为289.2 eV,是以O=C—O形式存在。中间结合能为286.1 eV和287.8 eV,分别对应C—O和酰胺键O=C—N两种C的形态。由图7(c)可知,絮凝聚合物的O1s具有3个主要的峰。其中,533.0 eV处对应酰胺键O=C—N,这与FT-IR结果一致,531.5 eV对应于C=O中的氧形态[35],而在530.0 eV则主要为水分子中或者吸附的—OH基团。
-
图8(a)为絮凝聚合物SEM图像,观察到聚合物表面存在凹陷空洞,主要为微孔和介孔(表2) ,并吸附了细小的有机胶体。球状聚合物相互连接呈现出紧凑结构,因为MTAC加入到预处理污泥的上清液后,通过水解、缩合共组装等过程,形成笼形低聚硅氧烷聚合物(Cage-like arranged oligomeric silanes,CLAOs)[36],其可作为溶解性有机质的吸附架桥物。图8(b)清晰展示了絮凝聚合物主要由C、O、Si、N和P等元素组成,与XPS元素比的结果吻合。再次证实MTAC对有机质和氮磷类化合物的吸附固定作用。
-
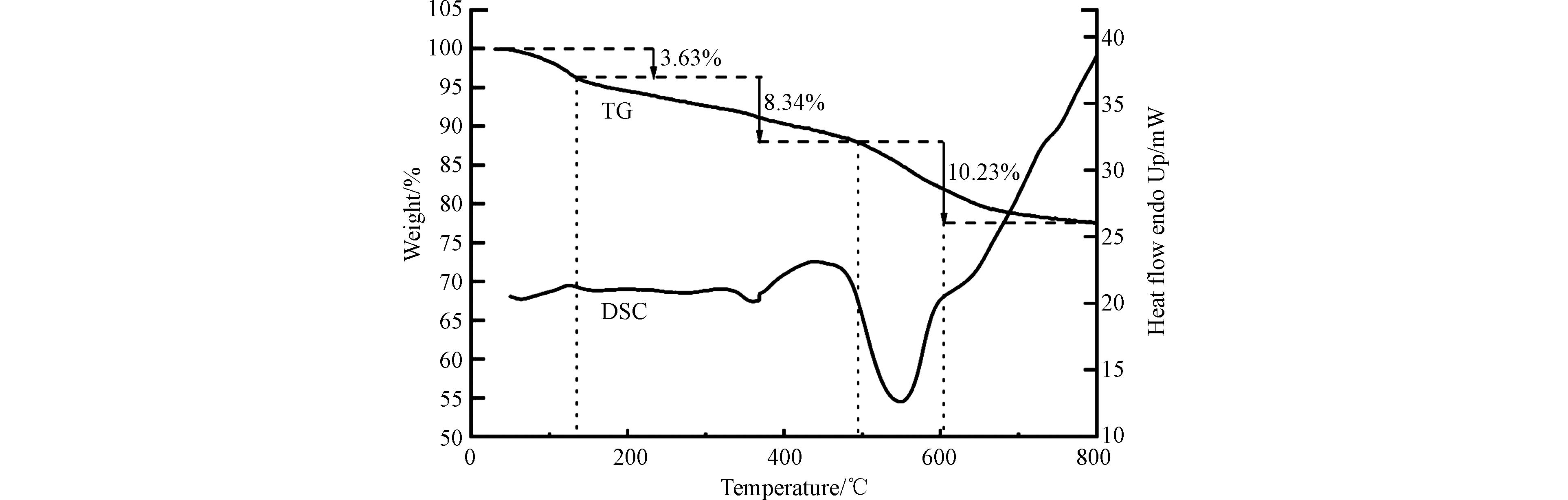
如图9所示,TG-DSC曲线表明絮凝聚合物出现了3个明显的失重温度区域,其热分解过程可分为3个阶段:水分蒸发、有机分挥发和无机分热解。絮凝聚合物的TG-DSC曲线,其中,在<135℃的区间失重3.63%,为样品中的水分蒸发去除的过程,对应于DSC曲线上有一微弱吸热峰。在135—495℃区间缓慢失重过程中重量损失了8.34%,是因为絮凝聚合物中从上清液中交联聚合回收的有机质在此温度区间挥发热解,对应于DSC曲线上450℃处明显的放热峰。还观察到495—800℃之间的重量快速损失,损失重量最大,达到了10.23%,这归结于絮凝聚合物中硅氧烷的分解和固定碳的燃烧,而DSC曲线上550℃处的强放热峰也证明了这一点。此外,絮凝聚合物在800℃的残留率为77.50%,这说明交联生成的絮凝聚合物具有较强的热稳定性。
-
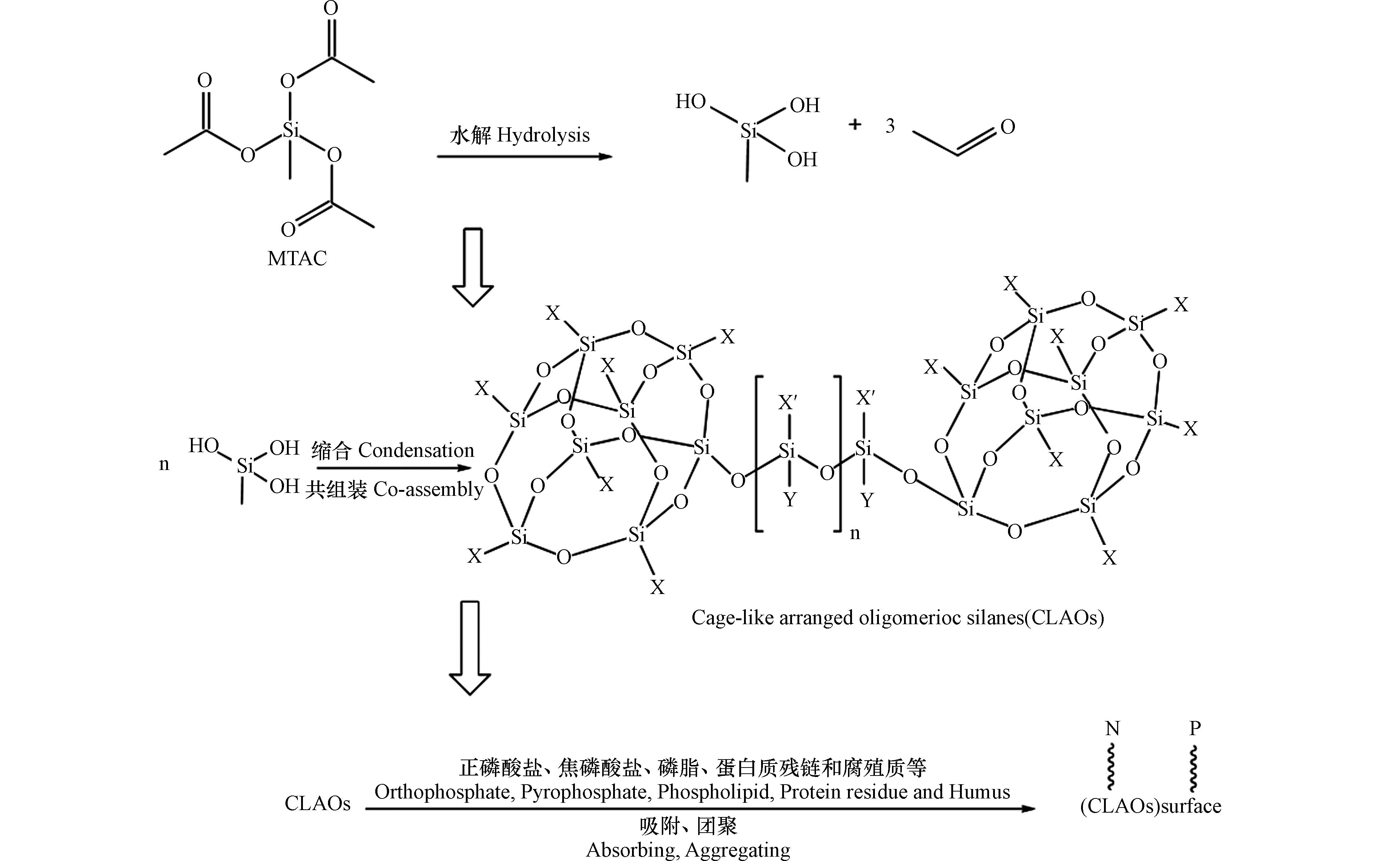
通过分析絮凝聚合物的特性,推测了MTAC交联聚合预处理污泥上清液中有机质的分子机制。如图10所示,首先,MTAC在污泥上清液中水解形成硅烷醇和乙酸,随后污泥上清液中的酰胺基、腐殖酸、富里酸与硅烷醇缩合,并共组装成低聚硅氧烷聚合物骨架[9, 35]。大量尺寸较小的絮凝聚合物形成后,互相积聚交联生成尺寸更大的絮凝聚合物;最后,由此形成的絮凝聚合物进一步团聚,产生吸附架桥作用,吸附预处理后污泥上清液中如正磷酸盐、焦磷酸盐、蛋白质残链、氨氮和腐殖质等物质,然后在重力下固液分离,最终实现上清液中营养物质的聚合回收。
-
(1) 碱联合微波法能高效破解污泥,最佳联合条件下(NaOH剂量1.12 g·L−1污泥、碱处理时间40 min,微波辐射功率640 W、微波辐射时间 120 s) ,SCOD、SPS、SPN、TP和TN比原始污泥增溶了29.16、10.48、21.16、5.15、6.54倍。
(2) 甲基三乙酰氧基硅烷能有效地交联聚合污泥上清液中氮磷及有机质,SPS、SPN、TP和TN的分离回收率分别达到了44.72%、58.49%、48.71%和76.90%。
(3) 絮凝聚合物含有丰富的有机组分和氮磷营养元素,表面孔径丰富且性质稳定,具有充当缓释碳源、肥料和作土壤改良剂的潜力。
碱联合微波预处理污泥及交联聚合回收上清液中有机质和氮磷
Crosslinking polymerization to recover organic matter and nitrogen/phosphorus from the supernatant of sludge combined alkali-microwave pretreated sludge
-
摘要: 从污泥中回收有机组分是实现污泥的妥善处理和资源再利用的理想途径。本研究系统考察了碱联合微波处理下污泥中有机质及氮磷的释放特征,同时使用甲基三乙酰氧基硅烷(methyltriacetoxysilane,MTAC)以絮凝聚合物的形式回收污泥上清液中的营养物质,并探究其内在机制。结果表明,碱联合微波处理能有效加速污泥的溶解和胞内物质释放,最佳处理条件为NaOH剂量1.12 g·L−1污泥、碱处理时间40 min,微波辐射功率640 W、微波辐射时间 120 s。碱联合微波处理比单独碱处理SCOD溶出浓度提高了97.6%,TN和TP分别增加了51.35%和25.13%。MTAC与上清液中营养物质通过交联、絮凝和团聚作用,有效地分离回收了营养物质,其中蛋白质、多糖、TN和TP回收率分别高达44.72%、58.49%、76.90%和48.71%。本研究证实了碱联合微波处理污泥,以MTAC为交联剂进行化学聚合,是一种污泥高效处置和资源回收的简单的替代策略。Abstract: Recovery of high-value products is an ideal option to achieve proper treatment and resource recycling of sludge. In this study, the release behaviors of organic matter and nitrogen/phosphorus during sludge pretreatment by the combined alkali-microwave process were systematically investigated, and methyltriacetoxysilane (MTAC) was used to recover nutrients from sludge supernatant by crosslinking polymerization method. The results showed that combined alkali-microwave could effectively accelerate sludge dissolution and intracellular substance release, and the optimal treatment conditions were observed to be 1.12 g·L−1 NaOH-sludge for 40 min and microwave radiation power 640 W for 120 s. Under the optimal conditions, SCOD concentration in supernatant increased by 97.6%, and TN and TP increased by 51.35% and 25.13%, compared with the alkali treatment alone. MTAC effectively separated and recovered nutrients from the supernatant through chemical cross-linking, flocculation, and agglomeration. The recovery efficiencies of protein, polysaccharide, TN, and TP reached 44.72%, 58.49%, 76.90%, and 48.71%. Our current study demonstrated that combined alkali-microwave pretreatment, followed by chemical polymerization with MTAC as the crosslinking agent, can be a simple and alternative strategy for highly efficient disposal and resource recovery from sewage sludge.
-

-
表 1 污泥的基本理化特性
Table 1. Physicochemical characteristics of the sludge
含水率/%
Moisture
contentpH 总固体/
(g·L−1)
TS挥发性固体/
(g·L−1)
VS溶解性化学需氧量/
(mg·L−1)
SCOD溶解性蛋白质/
(mg·L−1)
SPN溶解性多糖/
(mg·L−1)
SPS总磷/
(mg·L−1)
TP总氮/
(mg·L−1)
TN97.76 ± 0.3 6.80 ± 0.2 22.4 ± 0.6 10.4 ± 0.4 181.75 ± 13.1 84.16 ± 5.3 26.34 ± 2.8 70.44 ± 6.1 2.70 ± 0.1 表 2 絮凝聚合物的BET表面积和孔径分析结果
Table 2. BET surface area and pore size analysis results of flocculated polymer
BET表面积/(m2·g−1)
BET surface area微孔/介孔表面积/( m2·g−1)
Micropore/Mesoporous surface area孔体积/(cm3·g−1)
Pore volume微孔/介孔体积/(cm3·g−1)
Micropore/Mesoporous volume孔径/nm
Pore diameter9.0554 3.9485/5.1068 0.011328 0.001799/0.009529 50.0374 -
[1] JUNG J M. Single-photon ionisation of liquid methanol and ethanol [J]. Chemical Physics Letters, 2002, 366(1/2): 67-72. [2] BALMÉR P. Phosphorus recovery: An overview of potentials and possibilities [J]. Water Science and Technology, 2004, 49(10): 185-190. doi: 10.2166/wst.2004.0640 [3] LU D, XIAO K K, CHEN Y, et al. Transformation of dissolved organic matters produced from alkaline-ultrasonic sludge pretreatment in anaerobic digestion: From macro to micro [J]. Water Research, 2018, 142: 138-146. doi: 10.1016/j.watres.2018.05.044 [4] PERENDECI N A, CIGGIN A S, KÖKDEMIR ÜNŞAR E K, et al. Optimization of alkaline hydrothermal pretreatment of biological sludge for enhanced methane generation under anaerobic conditions [J]. Waste Management (New York, N, Y. ), 2020, 107: 9-19. doi: 10.1016/j.wasman.2020.03.033 [5] ZHANG Y X, ZHANG P Y, ZHANG G M, et al. Sewage sludge disintegration by combined treatment of alkaline+high pressure homogenization [J]. Bioresource Technology, 2012, 123: 514-519. doi: 10.1016/j.biortech.2012.07.078 [6] MUDHOO A, SHARMA S K. Microwave irradiation technology in waste sludge and wastewater treatment research [J]. Critical Reviews in Environmental Science and Technology, 2011, 41(11): 999-1066. doi: 10.1080/10643380903392767 [7] TAO W D, FATTAH K P, HUCHZERMEIER M P. Struvite recovery from anaerobically digested dairy manure: A review of application potential and hindrances [J]. Journal of Environmental Management, 2016, 169: 46-57. [8] 王雅珍, 张雪泽, 狄语韬. 近年硅烷偶联剂在聚合物改性中的研究进展及应用 [J]. 化工新型材料, 2018, 46(11): 5-7,12. WANG Y Z, ZHANG X Z, DI Y T. Research progress and application of silane coupling agent in polymer modification [J]. New Chemical Materials, 2018, 46(11): 5-7,12(in Chinese).
[9] ZHOU T, HUANG S, NIU D J, et al. Efficient separation of water-soluble humic acid using (3-aminopropyl)triethoxysilane (APTES) for carbon resource recovery from wastewater [J]. ACS Sustainable Chemistry & Engineering, 2018, 6(5): 5981-5989. [10] 刘丹凤. 合成甲基三乙酰氧基硅烷的研究 [J]. 化学工程师, 2002, 16(6): 63-64. doi: 10.3969/j.issn.1002-1124.2002.06.030 LIU D F. Study on synthesis of methyltriacetaloxidesilane [J]. Chemical Engineer, 2002, 16(6): 63-64(in Chinese). doi: 10.3969/j.issn.1002-1124.2002.06.030
[11] GRABITZ E, REICH M, OLSSON O, et al. Using structure biodegradability relationships for environmentally benign design of organosilicons-An experimental comparison of organosilicons and their carbon analogues [J]. Sustainable Chemistry and Pharmacy, 2020, 18: 100331. doi: 10.1016/j.scp.2020.100331 [12] GILCREAS F W. Standard methods for the examination of water and waste water [J]. Sensors (Basel, Switzerland), 1966, 56(3): 387-388. [13] DUBOIS M, GILLES K A, HAMILTON J K, et al. Colorimetric method for determination of sugars and related substances [J]. Analytical Chemistry, 1956, 28(3): 350-356. doi: 10.1021/ac60111a017 [14] FRØLUND B, PALMGREN R, KEIDING K, et al. Extraction of extracellular polymers from activated sludge using a cation exchange resin [J]. Water Research, 1996, 30(8): 1749-1758. doi: 10.1016/0043-1354(95)00323-1 [15] LI H, JIN Y Y, MAHAR R, et al. Effects and model of alkaline waste activated sludge treatment [J]. Bioresource Technology, 2008, 99(11): 5140-5144. doi: 10.1016/j.biortech.2007.09.019 [16] NEYENS E, BAEYENS J, CREEMERS C. Alkaline thermal sludge hydrolysis [J]. Journal of Hazardous Materials, 2003, 97(1/2/3): 295-314. [17] XIAO B Y, LIU C, LIU J X, et al. Evaluation of the microbial cell structure damages in alkaline pretreatment of waste activated sludge [J]. Bioresource Technology, 2015, 196: 109-115. doi: 10.1016/j.biortech.2015.07.056 [18] APPELS L, HOUTMEYERS S, DEGRÈVE J, et al. Influence of microwave pre-treatment on sludge solubilization and pilot scale semi-continuous anaerobic digestion [J]. Bioresource Technology, 2013, 128: 598-603. doi: 10.1016/j.biortech.2012.11.007 [19] ESKICIOGLU C, TERZIAN N, KENNEDY K J, et al. Athermal microwave effects for enhancing digestibility of waste activated sludge [J]. Water Research, 2007, 41(11): 2457-2466. doi: 10.1016/j.watres.2007.03.008 [20] DOĞAN I, SANIN F D. Alkaline solubilization and microwave irradiation as a combined sludge disintegration and minimization method [J]. Water Research, 2009, 43(8): 2139-2148. doi: 10.1016/j.watres.2009.02.023 [21] HONG S M, PARK J K, LEE Y O. Mechanisms of microwave irradiation involved in the destruction of fecal coliforms from biosolids [J]. Water Research, 2004, 38(6): 1615-1625. doi: 10.1016/j.watres.2003.12.011 [22] van B M A. Kinetic aspects of the Maillard reaction: A critical review [J]. Die Nahrung, 2001, 45(3): 150-159. doi: 10.1002/1521-3803(20010601)45:3<150::AID-FOOD150>3.0.CO;2-9 [23] FANG W, ZHANG P Y, ZHANG G M, et al. Effect of alkaline addition on anaerobic sludge digestion with combined pretreatment of alkaline and high pressure homogenization [J]. Bioresource Technology, 2014, 168: 167-172. doi: 10.1016/j.biortech.2014.03.050 [24] ZHANG C, TAN X J, YANG X, et al. Acid treatment enhances phosphorus release and recovery from waste activated sludge: Performances and related mechanisms [J]. Science of the Total Environment, 2021, 763: 142947. doi: 10.1016/j.scitotenv.2020.142947 [25] BI W, LI Y Y, HU Y Y. Recovery of phosphorus and nitrogen from alkaline hydrolysis supernatant of excess sludge by magnesium ammonium phosphate [J]. Bioresource Technology, 2014, 166: 1-8. doi: 10.1016/j.biortech.2014.04.092 [26] YAN Y X, QIN L, GAO J L, et al. Protein extraction and sludge dewatering performance of ultrasound-assisted enzymatic hydrolysis of excess sludge [J]. Environmental Science and Pollution Research International, 2020, 27(15): 18317-18328. doi: 10.1007/s11356-020-08208-2 [27] GAO J L, WANG Y C, YAN Y X, et al. Extraction of protein from excess sludge by thermal pretreatment assisted enzymatic hydrolysis [J]. {IOP} Conference Series:Earth and Environmental Science, 2019, 344(1): 012084. doi: 10.1088/1755-1315/344/1/012084 [28] 肖本益, 刘俊新. 污水处理系统剩余污泥碱处理融胞效果研究 [J]. 环境科学, 2006, 27(2): 319-323. doi: 10.3321/j.issn:0250-3301.2006.02.024 XIAO B Y, LIU J X. Study on treatment of excess sludge under alkaline condition [J]. Environmental Science, 2006, 27(2): 319-323(in Chinese). doi: 10.3321/j.issn:0250-3301.2006.02.024
[29] ZHANG R L, LU X Q, TAN Y J, et al. Disordered mesoporous carbon activated peroxydisulfate pretreatment facilitates disintegration of extracellular polymeric substances and anaerobic bioconversion of waste activated sludge [J]. Bioresource Technology, 2021, 339: 125547. doi: 10.1016/j.biortech.2021.125547 [30] 刘博文, 金若菲, 兰兵兵, 等. 热碱-EDTA耦合法强化污泥破解及效果分析 [J]. 环境工程学报, 2020, 14(1): 217-223. doi: 10.12030/j.cjee.201902110 LIU B W, JIN R F, LAN B B, et al. Strengthening sludge disintegration by thermal alkali-EDTA coupling method and its effect analysis [J]. Chinese Journal of Environmental Engineering, 2020, 14(1): 217-223(in Chinese). doi: 10.12030/j.cjee.201902110
[31] SOROCEANU A, STIUBIANU G T. Siloxane matrix molecular weight influences the properties of nanocomposites based on metal complexes and dielectric elastomer [J]. Materials (Basel, Switzerland), 2021, 14(12): 3352. doi: 10.3390/ma14123352 [32] SCHMITT J, FLEMMING H C. FTIR-spectroscopy in microbial and material analysis [J]. International Biodeterioration & Biodegradation, 1998, 41(1): 1-11. [33] SCHUSTER K C, MERTENS F, GAPES J R. FTIR spectroscopy applied to bacterial cells as a novel method for monitoring complex biotechnological processes [J]. Vibrational Spectroscopy, 1999, 19(2): 467-477. doi: 10.1016/S0924-2031(98)00058-7 [34] GLASSFORD S E, BYRNE B, KAZARIAN S G. Recent applications of ATR FTIR spectroscopy and imaging to proteins [J]. Biochimica et Biophysica Acta(BBA)-Proteins and Proteomics, 2013, 1834(12): 2849-2858. doi: 10.1016/j.bbapap.2013.07.015 [35] CASTILLO G A, WILSON L, EFIMENKO K, et al. Amidation of polyesters is slow in nonaqueous solvents: Efficient amidation of poly(ethylene terephthalate) with 3-aminopropyltriethoxysilane in water for generating multifunctional surfaces [J]. ACS Applied Materials & Interfaces, 2016, 8(51): 35641-35649. [36] BELE A, CAZACU M, STIUBIANU G, et al. Polydimethylsiloxane–Barium titanate composites: Preparation and evaluation of the morphology, moisture, thermal, mechanical and dielectric behavior [J]. Composites Part B:Engineering, 2015, 68: 237-245. doi: 10.1016/j.compositesb.2014.08.050 -



 下载:
下载: