-
新污染物正逐步成为当前制约大气、水、土壤环境质量持续深入改善的新难点. 近年来,我国高度重视新污染物治理,自2022年起,新污染物治理连续三年被写入我国政府工作报告. 新污染物在生产、加工和消费的全过程均可能存在环境排放,而常规的污染物管控措施无法有效控制其环境风险[1]. 作为一类新污染物,硅氧烷因其生产使用量大、环境分布广引发了广泛的关注,截至目前已有不少研究在多种环境介质如大气、地表水、灰尘、沉积物甚至人体组织中不同程度的检出了硅氧烷的存在[2]. 数十年来,甲基硅氧烷已广泛用于工业过程和日用品,2023年其全球年产量达到900万t[3]. 随着其在日常生活和工业领域的大量使用,这些化合物的某些低聚物,尤其是环状挥发性甲基硅氧烷(cVMS,如D4、D5和D6)会不可避免地释放到周围环境中[4 − 6]. 苯基甲基硅氧烷是指甲基硅氧烷中最多有一半甲基被苯基取代的硅氧烷化合物,由于其热稳定、抗氧化和抗辐射等性能比二甲基硅氧烷更优越,因此被广泛用于各行业中[7 − 8]. 石油作为主要能源和工业原料,在人类活动中占据重要地位. 原油生产涉及三次采油过程,前两次采油过程相对容易,而第三次采油需要通过注入驱油剂(例如硅氧烷聚合物和表面活性剂)来提高采油率[9]. 近年来,聚二甲基硅氧烷(PDMS)已广泛用作原油生产中的乳化剂和消泡剂[10],Xu等[11]在胜利油田的采油废水样品中发现了较高浓度(12.5—34.3 µg·L−1)的环形甲基硅氧烷(D4-D6). 聚苯基甲基硅氧烷的表面张力和疏水性等性质均比PDMS优越,因此聚苯基甲基硅氧烷或许也可以作为消泡剂应用在采油过程中[12],而小分子苯基硅氧烷(P3、P4等)则可能作为杂质释放到油田周围环境中. 研究发现甲基硅氧烷对动物的免疫、神经和生殖系统产生一定的毒性作用,且具有潜在内分泌的干扰效应,表现出致突变性和致癌性[13]. 此外由于苯基比甲基具有更高的亲脂性,苯基甲基硅氧烷潜在的生物持久性比母体甲基硅氧烷更强,尤其是由于苯基的亲脂性较高,生物体中苯基甲基硅氧烷的浓度可能大于其母体甲基硅氧烷的浓度. 苯基的引入使得硅氧烷产生一些新性质,但目前对于苯基硅氧烷的环境存在、迁移转化以及暴露评价和毒性效应的研究数据还比较缺乏. 截至目前还没有研究关注油田中苯基甲基硅氧烷的产生及其在周围水环境中的归趋.
本研究的主要目的是:1)阐明采油废水处理站污泥中苯基甲基硅氧烷的浓度水平及污染特征;2)考察油田周边水体中苯基甲基硅氧烷污染分布情况;3)研究淡水贻贝中苯基甲基硅氧烷的浓度水平和生物累积.
-
甲基硅氧烷(D4、D5和D6)和苯基甲基硅氧烷(P3和P4)的标准品(纯度>98%)均购自美国Sigma-Aldrich公司,13C标记的D4,D5和D6分别从Moravek Biochemicals(美国)和Cambridge Isotope Laboratories(美国)购买. 色谱级乙酸乙酯、正己烷以及丙酮购自美国Fisher Scientific公司.
-
胜利油田主要位于山东省东营市,是中国第二大油田. 该油田2018年原油产量约为
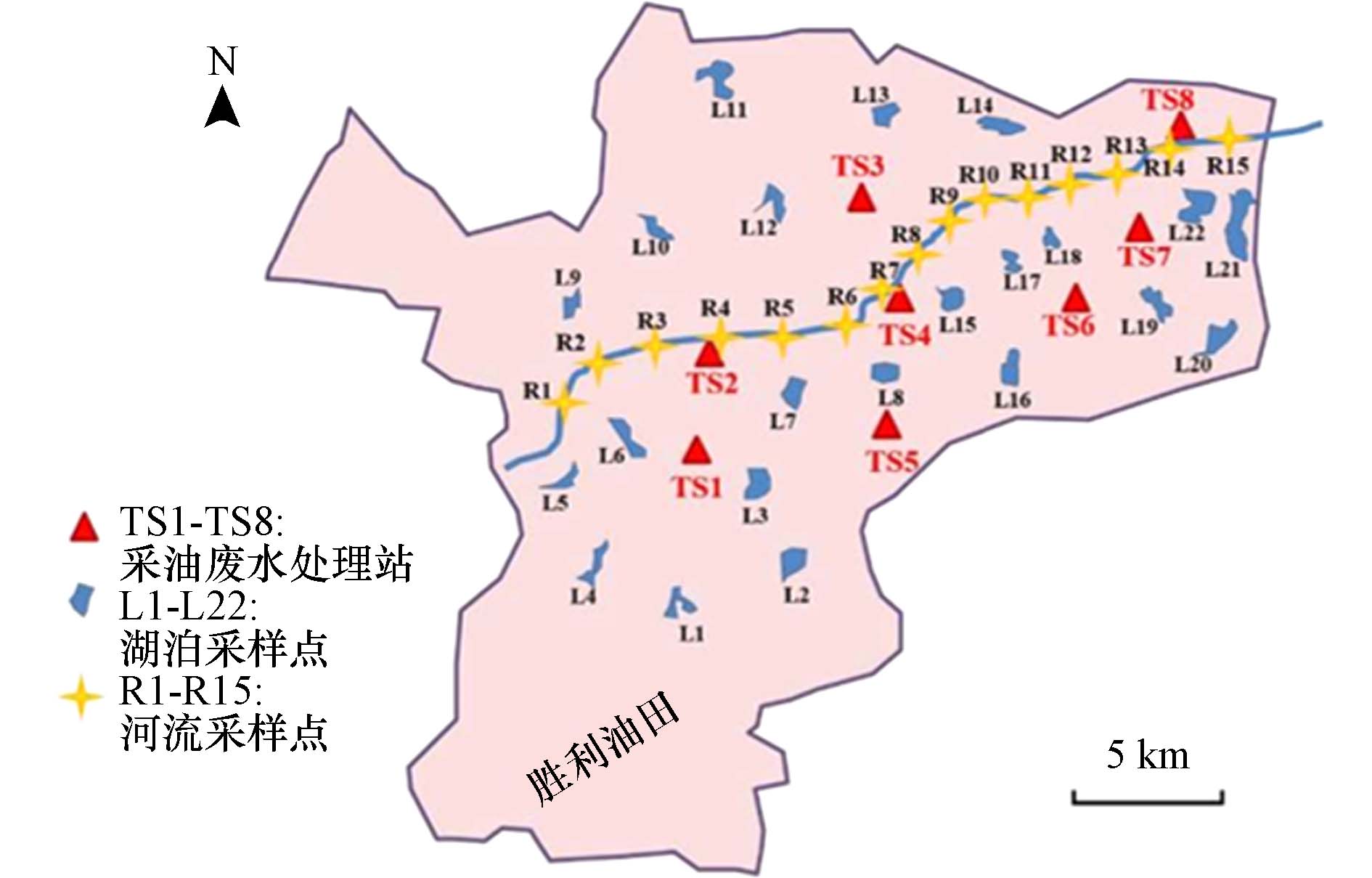
2380 万t. 在2015—2020年期间,从胜利油田的8个处理站(TS1—TS8)收集了脱水污泥样品(n=44)、不同水域沉积物样品(n=37)和淡水贻贝(n=35). 具体来说:6年期间每年从不同油田废水处理站采集7—8个脱水污泥样品;在2020年,用不锈钢铲分别从位于油田附近的22个湖泊和贯穿胜利油田的河流中采集了37个沉积物样品(图1),且在远离石化工业区255 km的沿海区域采集了5个淡水沉积物作为对照;2020年,从3个湖泊和河流中采集了35个淡水贻贝样品(Anodonta woodiana和Corbicula fluminea). -
污泥和沉积物样品中的硅氧烷采用固-液萃取法进行提取. 具体为称取干重1.0 g污泥/沉积物加入100 μL用丙酮配制的1 mg·L−1 13C-D4,13C-D5和13C-D6,然后加入8 mL正己烷/乙酸乙酯(体积比为1:1)涡旋20 min后,将混合物以
12000 r·min−1离心10 min,然后取上清液. 将样品重复萃取两次,将总萃取液过1.0 g无水硫酸钠小柱(Bond Elut,安捷伦科技公司,美国)脱水净化,最后氮吹浓缩定容至1 mL待测. 生物样品(淡水贻贝)中两种硅氧烷的前处理方法:冷冻干燥生物组织,粉碎后用电分散器进行均质化处理,与固体样品相同的方法进行萃取,称取样品重量为0.5 g(干重),前两次萃取方法完全相同,第3次萃取时间为6 h. -
甲基硅氧烷和苯基甲基硅氧烷均使用Agilent 7890A气相色谱仪5975C质谱检测器的选择离子模式(SIM)定性定量分析,目标化合物的MS参数见表1. 使用HP-5MS色谱柱(30 m×0.25 mm×0.25 µm)对其进行分离,质谱离子源为电子电离(EI)源,MS的电离能为70 eV,离子源和四极杆温度分别为230 ℃和150 ℃,传输线温度为250 ℃.
-
为减少样品污染,实验过程中应注意以下问题:1)实验人员避免使用洗手液或其他含有硅油成分的化妆品;2)每个玻璃管/漏斗在使用前用20—50 mL正己烷清洗并于400 ℃烘箱中烘干4 h待用;3)氮气浓缩过程使用钢管替代硅胶管;4)采用现场空白和程序空白评估周围潜在的硅氧烷污染,每6个样本设置1个程序空白. 由于在所有现场或程序空白中均未发现苯基甲基硅氧烷及其异构体,因此将加标(污泥、沉积物为10.0 ng·g−1干重)的现场空白样品(n=6)中目标化合物信号标准偏差的3倍和10倍作为苯基甲基硅氧烷的检测限LOD和定量限LOQ.
D4—D6的平均现场空白在污泥中为3.7—5.2 ng·g−1 dw(干重),沉积物为3.2—4.1 ng·g−1 dw,贻贝中为2.6—4.6 ng·g−1 dw,而D4-D6的平均程序空白在污泥为2.6—4.1 ng·g−1 dw,沉积物为2.3—3.4 ng·g−1 dw 和贻贝中为1.9—3.7 ng·g−1 dw. 这些cVMS的检测限(LOD)和定量限(LOQ)分别确定为现场空白样品(n=7)信号标准偏差的3倍和10倍(见表2). 在污泥、沉积物及贻贝组织中的回收率分别为82%—96%,83%—97%和79%—96%.
-
苯基甲基硅氧烷的生物-沉积物累积因子BSAFs通过公式1计算[14]:
其中,Cm为淡水贻贝中硅氧烷的浓度(ng·g−1 dw),Cs为沉积物中硅氧烷的浓度(ng·g−1 dw);flipid(%)是淡水贻贝的平均脂质含量(其中,Corbicula fluminea和Anodonta woodiana分别为4.4%和3.8%),foc(%)是沉积物中总有机碳含量,测得点位L6、L8、L15、R4和R14沉积物对应的foc分别为4.4%、4.5%、4.6%、4.2%和4.0%.
-
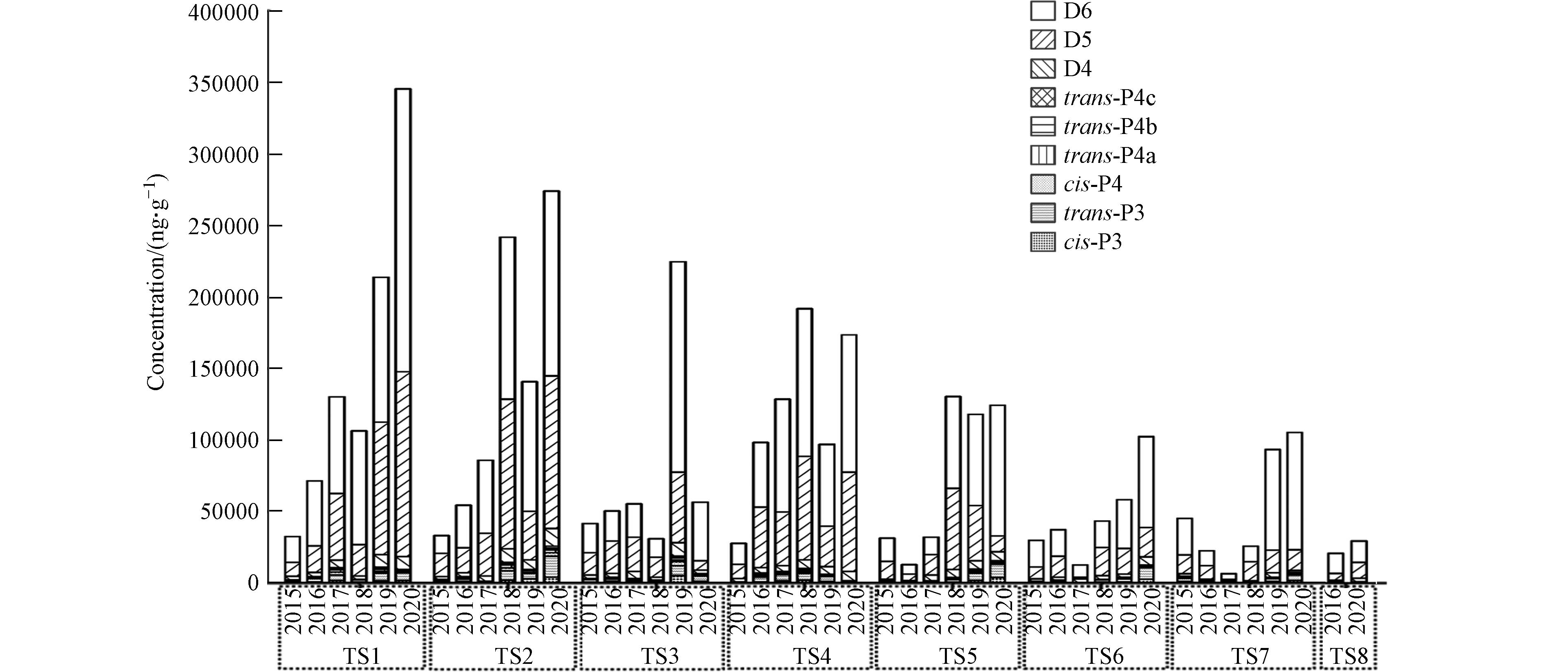
2015—2020年在胜利油田的8个废水处理站(TS1-TS8)收集了44个污泥样品. 在所有油田污泥样品中均检测到环形甲基硅氧烷(D4、D5、D6)及6种苯基甲基硅氧烷异构体(cis-P3、transP3、cis-P4、trans-P4a、trans-P4b和trans-P4c),其中环形甲基硅氧烷总浓度(ΣcVMS,D4—D6)为6.21×103—2.28×104 ng·g−1,苯基甲基硅氧烷总浓度Σ(P4+P3)为58.0—1.54×104 ng·g−1. 油田废水处理站污泥中D4、D5、D6浓度范围分别为:689—1.24×104、1.03×103—1.30×105、4.04×103—1.80×105 ng·g−1,苯基甲基硅氧烷cis-P3、trans-P3、cis-P4、trans-P4a、trans-P4b、trans-P4c浓度范围分别为:23.0—3.75×103、24.0—1.47×104、5.96—2.75×103、3.18—2.26×103、2.80—1.61×103、2.47—1.32×103 ng·g−1,连续6年的硅氧烷平均浓度变化见图2.
由图2可见,环形甲基硅氧烷占主导地位(占总硅氧烷浓度平均比例为94.1%),其次为P3(占总硅氧烷浓度平均比例为4.04%),P3比P4的浓度(占总硅氧烷浓度平均比例为1.83%)平均高2.3倍,这或许跟硅氧烷的市场消耗比例. 据报道,2016年中国聚苯硅氧烷的年消费量约为5.29万吨,比二甲基硅氧烷(104.9万吨)的消费量低约20倍[11]. 环形硅氧烷中D4、D5、D6占比分别为:4%—6%、3%—40%和55%—64%,推测可能是因为D5、D6挥发性比D4弱,而亲脂性更强,大量的D5、D6更易被污泥吸附,也或者是原油开采过程中应用的添加剂中D5和D6占主导. P3中cis-P3、trans-P3占比分别为23%—30%和70%—77%,P4中trans-P4a、trans-P4b、trans-P4c占比分别为31%—36%、28.5%—34%、15.5%—21%、16%—18%,以上表明P3、P4中均是反式异构体占主导地位. Xu等[11]在普通市政污水厂污泥中检测到了6种苯基甲基硅氧烷异构体浓度范围为<LOQ—188 ng·g−1 dw,检出率范围为20.7%—96.6%. 本研究油田废水处理站污泥中甲基硅氧烷和苯基甲基硅氧烷浓度水平比普通市政污泥中的高1—2个数量级. 高浓度苯基甲基硅氧烷在油田废水处理站污泥中的存在证明在油田开采过程中广泛使用了此类化合物. 在2015—2020年6年中,TS1-TS8污泥中总硅氧烷(甲基硅氧烷和苯基甲基硅氧烷之和)浓度较高的是TS1、TS2和TS4,分别为9.00×105、8.29×105、7.16×105 ng·g−1 dw,其余废水处理站的浓度范围为5.0×105—4.58×105 ng·g−1 dw,这可能是由于不同油田区域开采过程中使用的乳化剂或消泡剂的消耗量不同. 整体而言,8个废水处理站污泥中总硅氧烷浓度随着时间变化而明显增加,其中苯基硅氧烷6年的平均增长速率为1.38,环形甲基硅氧烷为1.36. 6种苯基甲基硅氧烷的年平均增长速率均高于3种环形甲基硅氧烷,其中P3的浓度增长速率最大(6年增长速率范围为每年1.1—1.8倍,见图3),推测在石油开采过程中,苯基甲基硅氧烷因其性质稳定使用量也在逐年增加.
-
2020年在胜利油田附近的22个湖泊和一条河流中共采集了37个沉积物样品,在这些样品中均能检测出环形甲基硅氧烷(D4—D6),其浓度范围分别为:3.91—67.7、85.1—670、45.1—501 ng·g−1 dw,除个别点位外,本研究调查区域沉积物中的浓度略高于Zhang等[15]在洞庭湖沉积物中发现的硅氧烷浓度,其范围分别为D4(3.98—360),D5(13.6—305)和D6(4.63—332 ng·g−1 dw). 高于Kierkegaard等[16]在英国亨伯河口的沉积物中检出的D5和D6,其浓度范围分别为60.0—260 ng·g−1 dw和30.0—95.0 ng·g−1 dw. 油田周围水系沉积物中苯基甲基硅氧烷cis-P3、trans-P3、cis-P4、transP4a、trans-P4b和trans-P4c浓度范围分别为:<LOD—108、<LOD—182、<LOD—101、<LOD—92.5、<LOD—67.6和<LOD—60.3 ng·g−1(见表3).
油田周围L3、L6、L8、L15和L22这4个湖泊沉积物中总硅氧烷浓度较高,而部分湖泊沉积物(如L1,L5,L11和L14)中没有检测出苯基甲基硅氧烷,推测与湖泊和污水处理站距离有关,如果湖泊距离油田废水处理站较近,或受影响较大(图4). 同样的现象在河流沉积物中也有体现,如点位R4,R7,R14和R15浓度明显高于其他点位,推测也是因为分别受TS2,TS4,TS8这几个污水处理站影响. 在对照区域沉积物中总硅氧烷的浓度范围为<LOD—242,本研究中湖泊和河流中沉积物平均浓度比对照区域高出2.33倍.
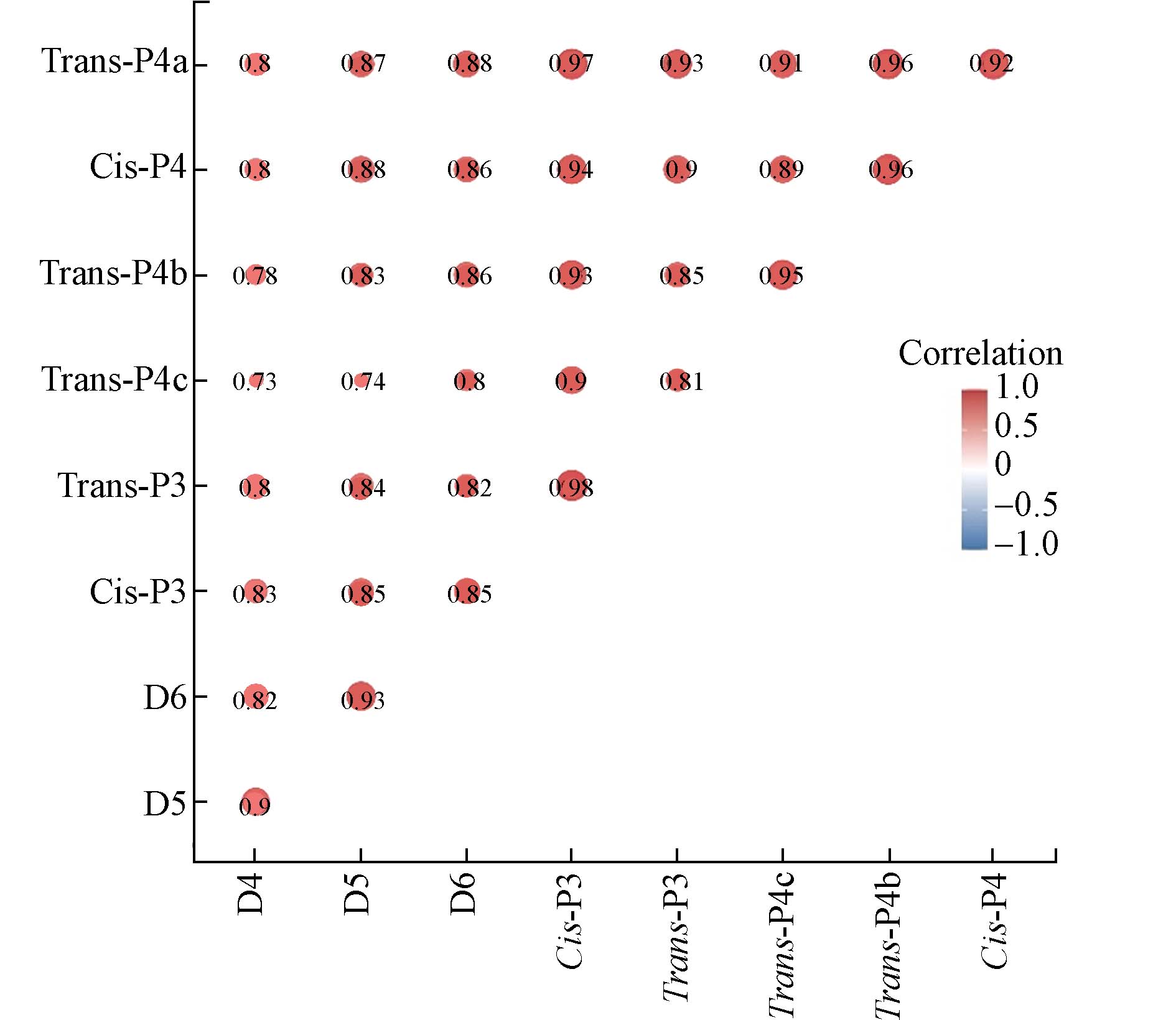
图5显示了用皮尔逊相关系数量化的湖泊和河流沉积物中6种苯基甲基硅氧烷和3种环形甲基硅氧烷之间的关系,9种硅氧烷之间呈现高度正相关(r>0.5;P<0.05),相关系数在0.73—0.98之间,表明该地区水体中各类硅氧烷的来源基本一致,例如油田废水处理站可能是周边地表水中硅氧烷的主要污染源之一.
湖泊和河流沉积物中硅氧烷组成分布如图6所示,不同点位之间的组成分布类似,甲基硅氧烷占比最大,而苯基甲基硅氧烷仅占很小一部分. 总体而言,湖泊和河流沉积物中硅氧烷组成分布与油田污水处理站油泥中类似,以甲基硅氧烷为主,占总硅氧烷的比例分别为79.2%和80.4%,这表明污泥是湖泊和河流沉积物中甲基硅氧烷的主要来源. 油田废水处理厂通常会对污泥进行脱水、焚烧或填埋处理[17 − 18],在污泥处置过程中,硅氧烷可能会通过挥发或者吸附于扬尘进入周围环境中.
-
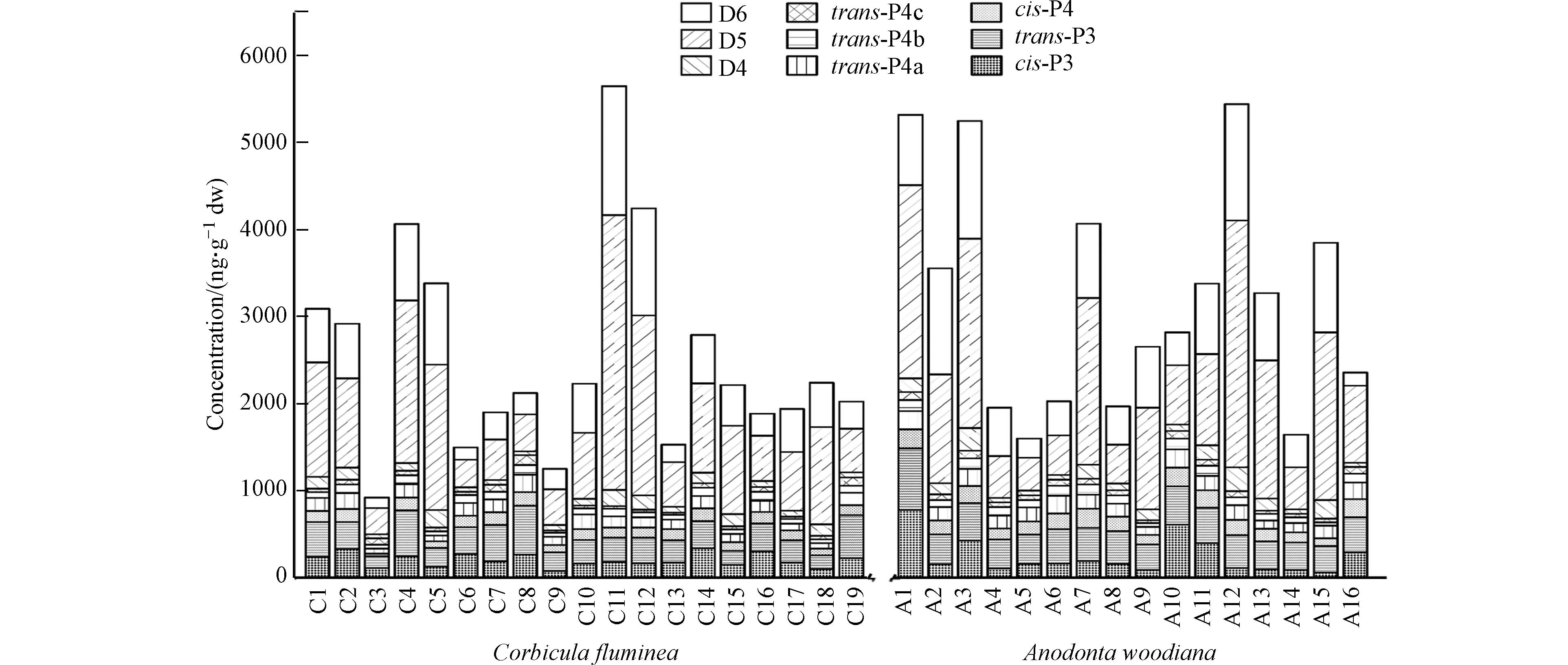
河流和湖泊沉积物中检测到一定浓度水平的甲基硅氧烷和苯基甲基硅氧烷,表明大概率会被一些以沉积物为食的生物(如淡水贻贝)摄取吸收. 在研究区,苯基甲基硅氧烷在距离TS1、TS2、TS4、TS5和TS8的3个湖泊和河流中采集的淡水贻贝(Anodonta woodiana和Corbicula fluminea)中被检测到(图7).
在Anodonta woodiana中检测到的D4—D6的浓度范围分别为47.4—277、380—2.85×103、150—1.36×103 ng·g−1 dw,6种苯基甲基硅氧烷cis-P3、trans-P3、cis-P4、transP4a、trans-P4b和trans-P4c的浓度范围分别为61.4—782、303—709、89.5—219、91.2—211、39.3—128、43.7—92.1 ng·g−1 dw(df均为100%),在Corbicula fluminea中的D4-D6的浓度范围分别91.2—211、302—3.17×103 、123—1.48×103 ng·g−1 dw,苯基甲基硅氧烷的浓度范围分别为77.9—338、139—566、29.6—154、58.3—200、42.1—111、89.5—113,39.3—128、43.7—92.1 ng·g−1 dw(df均为100%),总体来说,淡水贻贝中甲基硅氧烷的平均浓度比苯基甲基硅氧烷的高可达20倍.
根据公式(1)计算得到6种苯基甲基硅氧烷在Corbicula fluminea中的平均BSAF为2.45—3.18,在Anodonta woodiana中的平均BSAF为2.13—2.48(见表4),除Cis-P4外,其他5种苯基甲基硅氧烷比母体cVMS在淡水贻贝中的平均BSAF高1.02—1.40倍(D4-D6在Anodonta woodiana中的平均BSAF分别为2.14、2.41和2.21;在Corbicula fluminea中的平均BSAF为1.92、2.21和1.78). 有文献报道[19],3种氯代甲基硅氧烷D3D(CH2Cl)、D4D(CH2Cl)和D5D(CH2Cl)在Corbicula fluminea中的平均BSAF为2.6、2.3和2.1,在Anodonta woodiana中的平均BSAF为3.0、2.7和2.5,比母体甲基硅氧烷的平均BSAF大1.1—1.5倍. 结合本研究结果发现,苯基或氯代等取代基都比母体甲基类硅氧烷的生物积累性增加,后续研究者应再深入考察改性硅氧烷的毒理学效应,推测或高于母体甲基硅氧烷.
-
本研究持续监测了油田污水处理站污泥中甲基硅氧烷和苯基甲基硅氧烷的污染特征,并考察了周边河流湖泊沉积物中两类污染物的环境赋存情况,进一步研究了其在淡水贻贝中的生物积累性. 发现了原油开采及污水处理站污泥中存在较高浓度的苯基甲基硅氧烷且整体呈现上升趋势,且能在周边水系沉积物中发现了甲基和苯基甲基硅氧烷的存在,证实了原油开采活动不但能带来甲基硅氧烷的污染,同时苯基甲基硅氧烷也有明显排放且存在环境外溢的现象. 进一步,在淡水贻贝中也检测到了两类硅氧烷,经与母体甲基硅氧烷进行比较研究,苯基甲基硅氧烷在淡水贻贝中表现出更强的生物积累性. 上述结果表明苯基甲基硅氧烷在石油生产和其他工业领域的环境归趋和潜在生态影响值得进一步研究和关注.
胜利油田废水处理站污泥及其周边水体苯基甲基硅氧烷的时空分布与生物富集
Spatio-temporal distribution and bioconcentration of phenylmethylsiloxanes in sludge from Shengli Oilfield wastewater treatment station and its surrounding waters
-
摘要: 近年来,聚二甲基硅氧烷和聚苯基甲基硅氧烷常作为乳化剂和消泡剂广泛应用于原油生产中. 本研究考察了胜利油田区域甲基和苯基甲基硅氧烷的环境分布特征. 首先于2015—2020年对油田废水处理站污泥样品进行持续监测,发现了环形甲基硅氧烷(D4、D5、D6)及6种苯基甲基硅氧烷异构体(cis-P3、trans-P3、cis-P4、trans-P4a、trans-P4b、trans-P4c),其中环形甲基硅氧烷总浓度(∑cVMS,D4—D6)为6.21—228 μg·g−1 dw(干重),苯基甲基硅氧烷总浓度(∑(P4+P3))为58.0—1.54×103 ng·g−1 dw. 总体上,两类硅氧烷的浓度逐年增长,且苯基甲基硅氧烷浓度水平低于环形甲基硅氧烷. 结合其他文献可知,原油开采不但能带来较为严重的甲基硅氧烷污染,同时苯基甲基硅氧烷也有明显排放. 另外,在油田周围23个湖泊和河流的沉积物中同样发现了两类硅氧烷,其中总浓度范围分别为:151—1.87×103 ng·g−1 dw和318—1.13×103 ng·g−1 dw,其总硅氧烷平均浓度比对照区域的浓度高2.33倍,以上情况说明原油开采过程中苯基甲基硅氧烷存在环境外溢现象. 本研究进一步在淡水贻贝中发现两类硅氧烷,其中环形甲基硅氧烷总浓度为472—4.84×103 ng·g−1 dw,苯基甲基硅氧烷总浓度为451—2.14×103 ng·g−1 dw,且6种苯基甲基硅氧烷的平均生物-沉积物积累因子(2.13—3.18)比母体甲基硅氧烷大1.02—1.40倍,说明苯基甲基硅氧烷在沉积物中的持久性和在淡水贻贝中的生物累积性更强,其环境分布和生态风险值得关注. 以上工作证实了油田开采过程可导致甲基和苯基甲基硅氧烷的环境排放及后续带来一定的生态风险.Abstract: In recent years, polydimethylsiloxane and polyphenylmethylsiloxane have been widely used as emulsifiers and defoamers in crude oil production. Firstly, continuous monitoring in sludge samples from oilfield wastewater treatment plants from 2015 to 2020 revealed cyclic methyl siloxanes (D4, D5, D6) and six phenylmethylsiloxane isomers (cis-P3, trans-P3, cis-P4, trans-P4a, trans-P4b, and trans-P4c), with the concentrations of total cyclic methyl siloxanes (∑cVMS, D4—D6) and phenylmethylsiloxanes (∑(P3+P4)) being 6.21—228 μg·g−1 dw and 58.0—1.54×103 ng·g−1 dw, respectively. Overall, the concentrations of both two types of siloxanes have increased over the years, and the concentrations of phenylmethylsiloxanes were lower than those of cVMS. Refer to other literature, it can be seen that crude oil extraction can result not only in more serious methyl siloxane pollution, but also in significant emissions of phenyl methyl siloxanes. In addition, two types of siloxanes were also found in the sediments of 23 lakes and rivers around the oilfield, in which the total concentration ranged from 151—1.87×103 ng·g−1 dw and 318—1.13×103 ng·g−1 dw, respectively. The average concentration of total siloxanes was 2.33 times higher than that in the control area, indicating environmental overflow of phenyl methyl siloxanes during crude oil exploration process. Two types of siloxanes were further found in freshwater mussels, with total concentrations of cyclic methylsiloxanes ranging from 472—4.84×103 ng·g−1 dw and total concentrations of phenylmethylsiloxanes ranging from 451—2.14×103 ng·g−1 dw, and the average bio-sediment accumulation factors of the 6 phenylmethylsiloxanes (2.13—3.18) were 1.02—1.40 times greater than those of methylsiloxanes, indicating that phenylmethylsiloxanes are more persistent in sediment and bioaccumulative in freshwater mussels, and their environmental distribution and ecological risk are of concern. The above work confirms that the oilfield extraction process can lead to the release of methyl and phenyl methyl siloxanes into the environment and subsequent ecological risks.
-
Key words:
- phenylmethyl siloxanes /
- oil sludge /
- sediment /
- bioaccumulation
-

-
表 1 化合物的SIM参数
Table 1. MS parameters of compounds
化合物
Compounds内标
Interior label定性离子
Quantization ion(m/z)定量离子
Characterized ions(m/z)D4 13C-D4 281 133, 265, 281 D5 13C-D5 267 73, 267, 355 D6 13C-D6 429 73, 341, 429 cis-P3 13C-D6 315 315, 393 trans-P3 13C-D6 315 315, 393 cis-P4 13C-D6 451 373, 451, 529 trans-P4a 13C-D6 451 373, 451, 529 trans-P4b 13C-D6 451 373, 451, 529 trans-P4c 13C-D6 451 373, 451, 529 13C-D4 — 288 288, 305, 333 13C-D5 — 272 76, 272, 364 13C-D6 — 440 348, 440, 459 表 2 不同样品方法的空白、LOQ和回收率
Table 2. Blank, LOQ, and recovery of different method for samples
化合物Compounds 现场空白/(ng·g−1)
Field blank程序空白/(ng·g−1)Procedural blank LOQ LOD 回收率/%
Recovery100 ng·g−1 500 ng·g−1 2000 ng·g−1 污泥 D4 5.2 4.1 3.3 1.0 96±4 91±5 94±3 D5 4.1 2.6 2.8 0.8 90±4 82±4 89±3 D6 3.7 3.2 2.6 0.8 94±3 92±3 94±4 沉积物 D4 4.1 3.4 2.2 0.7 91±3 94±4 93±3 D5 3.2 2.0 1.8 0.5 83±4 88±3 90±4 D6 2.5 2.3 1.7 0.5 93±2 97±3 94±3 贻贝 D4 4.6 3.7 2.3 0.7 88±5 83±4 85±3 D5 4.1 2.4 4.1 1.2 79±4 85±6 84±4 D6 2.6 1.9 3.4 1.0 96±5 89±4 94±4 表 3 本研究河流和湖泊中硅氧烷浓度(ng·g−1 dw)
Table 3. Concentrations of siloxanes in sediment from the studied lakes and rivers lakes
Sample Cis-P3 Trans-P3 ΣP3 Cis-P4 Trans-P4a Trans-P4b Trans-P4c P4 ΣP3+P4 D4 D5 D6 ΣcvMSs Σsiloxanes L1 <LOD <LOD <LOD <LOD <LOD <LOD <LOD <LOD <LOD 13.6 132 65.4 211 211 L2 9.17 25.6 34.8 <LOD <LOD <LOD <LOD <LOD 34.8 18.5 167 65.6 251 286 湖泊
LakeL3 43.2 87.0 130 31.2 35.9 9.79 5.53 82.4 213 23.8 490 384 898 1.11×103 L4 18.4 53.3 71.7 <LOD <LOD <LOD <LOD <LOD 71.7 9.80 219 135 364 436 L5 <LOD <LOD <LOD <LOD <LOD <LOD <LOD <LOD <LOD 3.91 119 76.0 199 199 L6 138 182 320 101 92.5 67.6 60.3 321 641 66.2 664 501 1.23×103 1.87×103 L7 25.3 55.3 80.6 12.4 6.73 <LOD <LOD 19.1 99.8 19.6 296 112 428 527 L8 86.7 151 237 79.4 56.5 34.8 14.8 185 423 72.1 720 368 1.16×103 1.58×103 L9 2.91 9.44 12.4 2.92 2.57 <LOD <LOD 5.49 17.8 21.8 250 107 379 397 L10 <LOD 2.63 2.63 2.27 0.98 <LOD <LOD 3.25 5.88 10.5 248 111 370 375 L11 <LOD <LOD <LOD <LOD <LOD <LOD <LOD <LOD <LOD 9.50 96.3 45.1 151 151 L12 22.6 66.7 89.3 5.05 5.47 <LOD 3.87 14.4 104 9.10 221 146 376 480 L13 36.6 61.8 98.4 17.8 11.9 7.98 4.90 42.6 141 12.5 195 176 384 525 L14 <LOD <LOD <LOD <LOD <LOD <LOD <LOD <LOD <LOD 7.50 85.1 61.7 154 154 L15 80.3 124 204 38.5 48.7 30.5 23.3 141 345 76.2 670 485 1.23×103 1.58×103 L16 8.49 30.3 38.7 2.33 2.53 4.43 <LOD 9.29 48.0 5.90 141 109 256 304 L17 38.9 54.5 93.4 10.9 11.1 4.23 5.25 31.5 125 31.1 244 147 422 547 L18 30.3 63.3 93.6 6.06 10.2 <LOD <LOD 16.3 110 33.5 274 144 452 562 L19 2.83 7.62 10.5 2.84 <LOD <LOD <LOD 2.84 13.29 9.70 179 79.6 268 282 L20 5.32 20.6 25.9 7.26 7.44 <LOD <LOD 14.7 40.6 14.1 205 91.9 311 352 L21 29.7 47.2 47.2 7.56 11.5 6.3 3.74 29.1 76.3 20.0 175 160 355 431 L22 72.6 102 175 45.5 39.4 24.2 32.6 142 317 67.7 525 331 924 1.24×103 mean 29.6 52.0 80.3 17.0 15.6 8.60 7.00 48.2 129 25.3 287 177 489 618 河流River R1 25.4 58.3 83.7 17.0 11.0 8.00 4.66 40.7 124 50.1 358 172 580 704 R2 4.21 11.7 15.9 <LOD <LOD <LOD <LOD <LOD 15.9 22.1 152 129 303 319 R3 3.47 6.53 10.0 <LOD <LOD <LOD <LOD <LOD 10.0 14.8 171 136 322 332 R4 108 182 290 52.3 64.6 28.2 29.4 175 464 51.2 395 224 670 1.13×103 R5 25.7 53.2 78.8 10.9 12.6 7.96 5.10 36.6 115 33.8 304 175 513 628 R6 28.7 51.1 79.7 13.4 13.7 7.45 3.85 38.4 118 34.1 314 177 525 643 R7 20.9 43.0 63.9 14.7 16.0 5.48 3.74 39.9 104 35.9 389 177 602 706 R8 23.6 42.6 66.2 10.2 10.2 6.71 4.45 31.5 97.8 26.0 297 145 468 566 R9 23.8 38.4 62.1 8.82 12.1 4.79 3.37 29.1 91.2 30.8 283 160 474 565 R10 7.12 15.5 22.7 3.95 2.51 <LOD <LOD 6.46 29.1 25.4 267 133 425 455 R11 13.0 30.0 42.8 4.89 4.04 <LOD <LOD 8.93 51.7 25.1 261 152 438 490 R12 18.7 35.5 54.2 11.9 7.73 3.55 3.92 27.1 81.4 29.8 260 142 432 513 R13 2.35 1.93 4.28 2.79 <LOD <LOD <LOD 2.79 7.07 30.0 199 138 367 374 R14 70.4 122 193 42.2 41.8 14.5 9.94 108 301 48.1 407 219 674 975 R15 46.3 95.9 142 15.8 12.8 6.42 5.18 40.2 182 45.8 308 192 546 728 mean 28.1 52.5 80.6 13.9 13.9 6.20 4.90 39.0 120 33.5 291 165 490 610 表 4 胜利油田周围河流湖泊淡水贻贝中硅氧烷BSAF值
Table 4. Concentrations of siloxanes in sediments from Surrounding aqueous systems of Shengli Oilfield
Mussels Sample Cis-P3 Trans-P3 Cis-P4 Trans-P4a Trans-P4b Trans-P4c D4 D5 D6 Anodonta woodiana 1 7.32 5.04 2.81 2.95 2.44 1.97 3.07 4.34 2.08 2 1.47 2.47 2.03 2.16 1.54 1.42 2.53 2.46 3.18 3 5.02 2.93 2.53 3.55 3.62 5.90 3.69 3.09 3.76 4 0.90 2.11 1.42 1.82 1.75 1.04 0.89 0.83 1.28 5 1.73 2.15 1.84 2.73 2.26 3.66 0.71 0.50 0.57 6 1.60 2.27 1.96 3.13 2.83 3.98 0.65 0.54 0.92 7 1.89 2.14 2.34 2.47 2.82 3.82 1.92 2.26 1.97 8 1.58 2.14 1.76 2.27 2.41 3.43 0.91 0.53 1.03 9 1.57 1.94 1.67 2.47 2.04 3.32 0.64 0.46 0.52 10 1.67 3.53 4.37 2.80 2.09 2.23 2.41 2.61 2.17 11 7.12 4.69 7.57 4.84 5.55 4.35 3.04 2.25 2.39 12 1.30 2.58 4.23 3.25 4.16 2.90 6.75 8.99 7.48 13 0.71 1.41 2.14 1.16 2.23 0.94 2.14 3.19 2.74 14 0.69 1.44 1.83 1.36 1.94 1.14 0.86 1.01 1.38 15 0.61 1.73 1.48 2.44 1.90 3.07 3.07 3.32 3.30 16 4.10 3.27 4.90 4.53 6.94 7.71 0.98 2.16 0.68 mean 2.45 2.62 2.80 2.75 2.91 3.18 2.14 2.41 2.21 Corbicula fluminea 1 2.64 3.37 1.98 2.50 1.48 1.03 3.16 3.04 1.89 2 3.45 4.39 2.58 3.26 1.92 1.34 4.12 3.96 2.47 3 1.25 1.20 0.46 0.99 0.98 1.91 1.14 0.71 0.39 4 2.35 3.79 1.91 2.13 2.02 1.13 1.70 3.68 2.30 5 1.47 1.49 0.98 1.21 1.35 3.03 2.86 2.38 2.61 6 3.54 2.32 1.86 2.96 2.93 2.77 0.81 0.50 0.43 7 2.65 3.37 2.28 3.18 3.07 6.73 0.94 0.79 1.03 8 2.49 3.04 1.56 2.86 2.58 6.18 0.49 0.48 0.54 10 1.69 1.63 1.40 2.70 1.79 2.17 0.98 0.95 1.39 11 4.54 4.56 6.22 5.33 5.80 2.80 4.92 9.56 6.19 12 1.69 1.98 2.47 2.00 1.61 1.05 1.78 2.56 2.10 13 2.05 1.82 3.16 2.16 2.50 1.17 1.67 1.67 1.16 14 2.96 1.63 2.67 2.08 3.17 1.72 2.23 2.46 2.35 15 1.43 0.91 1.99 1.50 1.93 1.30 2.80 2.68 2.18 16 2.38 1.50 2.11 1.69 3.03 1.56 1.20 1.11 0.95 17 2.62 2.22 2.83 1.97 3.89 3.05 1.49 1.75 2.39 18 1.20 1.08 1.55 1.22 2.59 3.54 2.25 2.31 1.94 19 0.47 0.59 0.39 0.49 0.80 1.45 0.17 0.18 0.21 mean 2.25 2.30 2.13 2.29 2.44 2.48 1.92 2.21 1.78 -
[1] 陈雅婷, 赵昕宇, 李艳红, 等. 我国污染场地中新污染物的环境行为和修复进展[J]. 环境工程, 2024, 42(1): 166-176. CHEN Y T, ZHAO X Y, LI Y H, et al. Environmental behavior and restoration progress of emerging contaminants in contaminated sites in China[J]. Environmental Engineering, 2024, 42(1): 166-176 (in Chinese).
[2] 周川琪, 袁涛. 挥发性甲基硅氧烷的环境分布与行为归趋研究进展[J]. 环境化学, 2014, 33(3): 386-396. ZHOU C Q, YUAN T. The environmental occurrences and behaviors of volatile methylsiloxanes: A review[J]. Environmental Chemistry, 2014, 33(3): 386-396 (in Chinese).
[3] STATISTA RESEARCH. Department. Silicon mining worldwide - statistics & facts [EB/OL]. [2024-1-11]. [4] LEI Y D, WANIA F, MATHERS D. Temperature-dependent vapor pressure of selected cyclic and linear polydimethylsiloxane oligomers[J]. Journal of Chemical & Engineering Data, 2010, 55(12): 5868-5873. [5] TANG X C, MISZTAL P K, NAZAROFF W W, et al. Siloxanes are the most abundant volatile organic compound emitted from engineering students in a classroom[J]. Environmental Science & Technology Letters, 2015, 2(11): 303-307. [6] WANG D G, NORWOOD W, ALAEE M, et al. Review of recent advances in research on the toxicity, detection, occurrence and fate of cyclic volatile methyl siloxanes in the environment[J]. Chemosphere, 2013, 93(5): 711-725. doi: 10.1016/j.chemosphere.2012.10.041 [7] 伍川, 金晶, 蒋剑雄, 等. 甲基二苯基封端硅油的制备及其热性能研究[J]. 有机硅材料, 2007, 21(5): 258-262,309. WU C, JIN J, JIANG J X, et al. Preparation of methyldiphenyl-terminated silicone oil and study on its thermal stabilities[J]. Silicone Material, 2007, 21(5): 258-262,309 (in Chinese).
[8] 冯圣玉, 张洁, 李美江, 等. 有机硅高分子及其应用[M]. 北京: 化学工业出版社, 2004: 611. FENG S Y, ZHANG J, LI M J, et al. Silicone polymer and its application[M]. Beijing: Chemical Industry Press, 2004: 61 (in Chinese).
[9] AL-AZANI K, ABU-KHAMSIN S, AL-ABDRABALNABI R, et al. Oil recovery performance by surfactant flooding: A perspective on multiscale evaluation methods[J]. Energy & Fuels, 2022, 36(22): 13451-13478. [10] CHEN J P, HUANG X J, HE L M, et al. Foaming of oils: Effect of poly(dimethylsiloxanes) and silica nanoparticles[J]. ACS Omega, 2019, 4(4): 6502-6510. doi: 10.1021/acsomega.9b00347 [11] XU L, XU S H, ZHANG Q L, et al. Sources and fate of cyclic phenylmethylsiloxanes in one municipal wastewater treatment plant and biosolids-amended soil[J]. Environmental Science & Technology, 2018, 52(17): 9835-9844. [12] BERGERON V, COOPER P, FISCHER C, et al. Polydimethylsiloxane (PDMS)-based antifoams[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 1997, 122(1/2): 103-120. [13] 封棣, 张喜荣, 戚冬雷. 甲基硅氧烷对人体暴露途径的研究进展[J]. 环境化学, 2018, 37(5): 1022-1036. FENG D, ZHANG X R, QI D L. Human exposure pathways of methylsiloxanes: A review of recent studies[J]. Environmental Chemistry, 2018, 37(5): 1022-1036 (in Chinese).
[14] BURKHARD L P, COOK P M, LUKASEWYCZ M T. Direct application of biota-sediment accumulation factors[J]. Environmental Toxicology and Chemistry, 2010, 29(1): 230-236. doi: 10.1002/etc.25 [15] ZHANG Y X, SHEN M C, TIAN Y, et al. Cyclic volatile methylsiloxanes in sediment, soil, and surface water from Dongting Lake, China[J]. Journal of Soils and Sediments, 2018, 18(5): 2063-2071. doi: 10.1007/s11368-018-1948-9 [16] KIERKEGAARD A, MCLACHLAN M S. Determination of decamethylcyclopentasiloxane in air using commercial solid phase extraction cartridges[J]. Journal of Chromatography A, 2010, 1217(21): 3557-3560. doi: 10.1016/j.chroma.2010.03.045 [17] STEGER M T, MEIßNER W. Drying and low temperature conversion - a process combination to treat sewage sludge obtained from oil refineries[J]. Water Science and Technology, 1996, 34(10): 133-139. doi: 10.2166/wst.1996.0249 [18] KACPRZAK M, NECZAJ E, FIJAŁKOWSKI K, et al. Sewage sludge disposal strategies for sustainable development[J]. Environmental Research, 2017, 156: 39-46. doi: 10.1016/j.envres.2017.03.010 [19] OPPERHUIZEN A, DAMEN H W J, ASYEE G M, et al. Uptake and elimination by fish of polydimethylsiloxanes (silicones) after dietary and aqueous exposure[J]. Toxicological & Environmental Chemistry, 1987, 13(3/4): 265-285. -



 下载:
下载: