-
近年来,我国污水排放总量不断增加,大量的污染物排放到水环境中将给水环境造成严重影响,城市污水处理是关系国计民生的重要问题。城市污水处理厂作为城市重要的基础设施之一,在水环境污染防治和生态文明建设方面发挥重要作用。活性污泥法因其高效、经济、环保等优点,成为我国乃至世界上大部分城市污水处理厂普遍采用的工艺[1]。活性污泥作为活性污泥工艺的主体,含有高度复杂的微生物群落,构成一种独特的微生物生态系统,并依靠这些微生物降解有机物、营养物质等,从而实现活性污泥系统稳定运行和良好处理性能[2-3]。马切切等[4]对活性污泥微生物群落结构及与环境因素响应关系研究发现,温度与Nitrospira、Aquihabitans、Terrimonas和Dechloromona等多种关键的脱氮微生物呈负相关,当温度低于15 ℃时,污水处理厂对TN和NH4+-N的去除率仅有49.67%和63.19%;Zoogloea、Arcobacter、Acidovorax和Acinetobacter等优势功能性菌属相对丰度越高,污染物的去除率也越高。因此,污水处理厂的稳定运行在很大程度上依赖于系统微生物群落的特征,特别是一些功能菌的多样性、丰度。深入分析、研究污水处理厂系统中微生物群落组成、功能菌的生理特性,从而选择性调控微生物群落,对于提高污水处理厂活性污泥处理能力具有至关重要的意义。
群体感应(quorum sensing,QS)是微生物间通过自发产生、释放并接收特定化学信号而建立起来的一种通讯机制,所依赖的化学信号分子就是他们的“通讯语言”[5]。近年来,群体感应在有机物降解、生物脱氮等废水生物处理过程中的调控作用受到越来越多的关注[6-8]。LI等[6]在不同乙酸/油酸比条件下对序批式反应器(sequencing batch reactor,SBR)进行了研究,发现N酰化高丝氨酸内脂(N-acyl homoserine lactones,AHLs)介导的群体感应对化学需氧量(COD)和总氮(TN)去除、污泥沉降性等均具有显著的调控作用。WANG等[8]总结了AHLs介导的群体感应在废水生物反应器氮代谢效率、颗粒聚集和生物膜的形成等方面的调控作用。大量研究[9-10]表明,群体感应在废水生物处理中发挥重要作用。因此,本研究对天津市某城市污水处理厂进行了为期1 a的监测研究,重点分析了其微生物群落结构特征和群体感应信号分子变化以探索污水处理厂活性污泥系统的群体感应调控作用,以期为提升污水处理厂处理能力及稳定性提供参考。
-
对天津市某城市污水处理厂的曝气池活性污泥进行样本采集,该城市污水处理厂主体采用A/O处理工艺,并辅以化学法去除尾水中余磷。采样时间为2019年1月、3月、5月、7月、9月和11月中旬,分别命名为S1、S3、S5、S7、S9和S11。样品采集后于−80 ℃保存,待所有样品收集完毕后进行测序。每月的5、15、25日取活性污泥混合液用于群体感应信号分子的提取和检测。
-
AHLs类信号分子采用Bond Elut ENV固相萃取柱(500 mg,6 mL,Agilent)进行固相萃取,具体操作步骤如下:用0.45 μm滤膜过滤水样,分别用5 mL甲醇(Fisher Scientific,LC-MS级)和5 mL纯水活化Bond Elut ENV固相萃取柱,然后以5~10 mL·min−1的速度将过滤后的水样载入固相萃取柱,之后用5mL 5%甲醇水溶液淋洗,待固相萃取柱抽干后用10 mL甲醇(Fisher Scientific,LC-MS级)洗脱萃取的AHLs信号分子,并收集洗脱液。将洗脱液用旋转蒸发仪脱溶后,使用初始流动相定容至2 mL,采用高效液相色谱(Agilent 1290 Infinity II)-质谱(Agilent 6470)联用仪参考LI等[11]采用的方法对AHLs进行定量分析。
-
待所有活性污泥样本收集完毕后送往苏州金唯智生物科技有限公司进行DNA提取。使用Magen Hipure Soil DNA Kit从污泥样品中提取DNA,并使用Qubit® dsDNA HS Assay Kit 检测DNA样品浓度。采用金唯智设计的包含“CCTACGGRRBGCASCAGKVRVGAAT”序列的上游引物和包含“GGACTACNVGGGTWTCTAATCC”序列的下游引物对V3和V4这2个高度可变区进行扩增。对扩增纯化后的DNA通过Illumina MiSeq测序平台进行2×250bp双端测序。
-
对序列进行质量过滤、去除嵌合体后采用VSEARCH(1.9.6)进行OTU聚类(97%相似度),利用RDP classifier贝叶斯算法对OTU进行分类学注释,参考数据库为Silva 132。根据OTU结果进行α多样性指数分析,通过主坐标分析(PCoA)比较各样本间微生物群落差异,利用Tax4Fun进行功能预测分析[12]。
-
本研究中城市污水处理厂不同活性污泥样本微生物α多样性指数如表1所示。由表1可知,所有活性污泥样本的覆盖率均不低于99.8%。这表明样本中的绝大部分微生物均被检测到,测序结果可以反映样本的真实情况。S5样本的ACE指数和Chao指数是所有样本中最低的,表明5月份微生物群落的丰富度较其他时期较低。这是由于此时处于污泥膨胀恢复期,样本内微生物的种类较少。Shannon指数和Simpson指数均反映样本的多样性,Shannon指数可以反映物种均匀度,其值越大表示物种均匀性更高,Simpson指数越大,其多样性越大。而9月份污泥样本的Shannon指数和Simpson指数比其他时期内污泥样品低,表明9月份样品中微生物群落的均匀度和多样性最低。这可能是由于9月份系统运行温度及运行条件适宜某些功能微生物生长,其相对丰度较高,从而使整个系统微生物群落的均匀度降低(Shannon指数低),同时部分微生物无法适应该运行条件而被演替使整个系统微生物多样性降低(Simpson指数降低)。
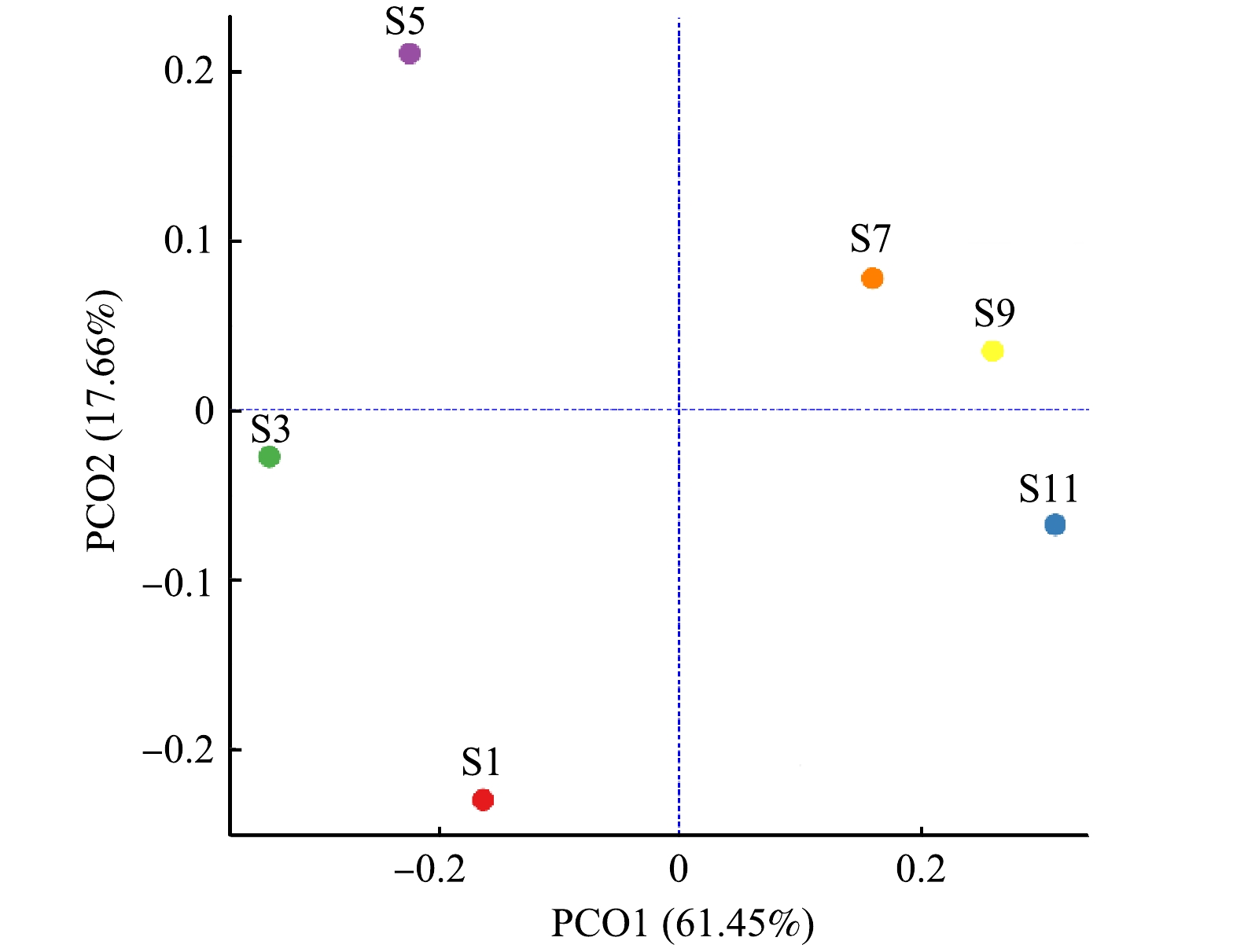
为分析不同样本间群落组成的差异性,基于Bray-Curtis距离算法,采用PCoA分析衡量样本间物种多样性差异,结果如图1所示。由图1可知,PCO1与PCO2分别解释方差为61.45%和17.66%,累计解释能力达79.11%,PCO1将样本S1、S3、S5的OTU与S7、S9和S11明显区分开,样本S1、S3、S5的污泥处于污泥膨胀状态和污泥膨胀恢复状态,样本相似性高;而S7、S9和S11均处于污泥正常状态,故具有高度相似性。同时,注意到S1、S3和S5之间明显分离,而S7、S9和S11之间虽然存在分离,但距离较小,表明在1—5月份污水处理厂由于发生污泥膨胀,微生物群落发生较大的变化,而7—11月份污水处理厂微生物群落差异变化不大,系统比较稳定。
-
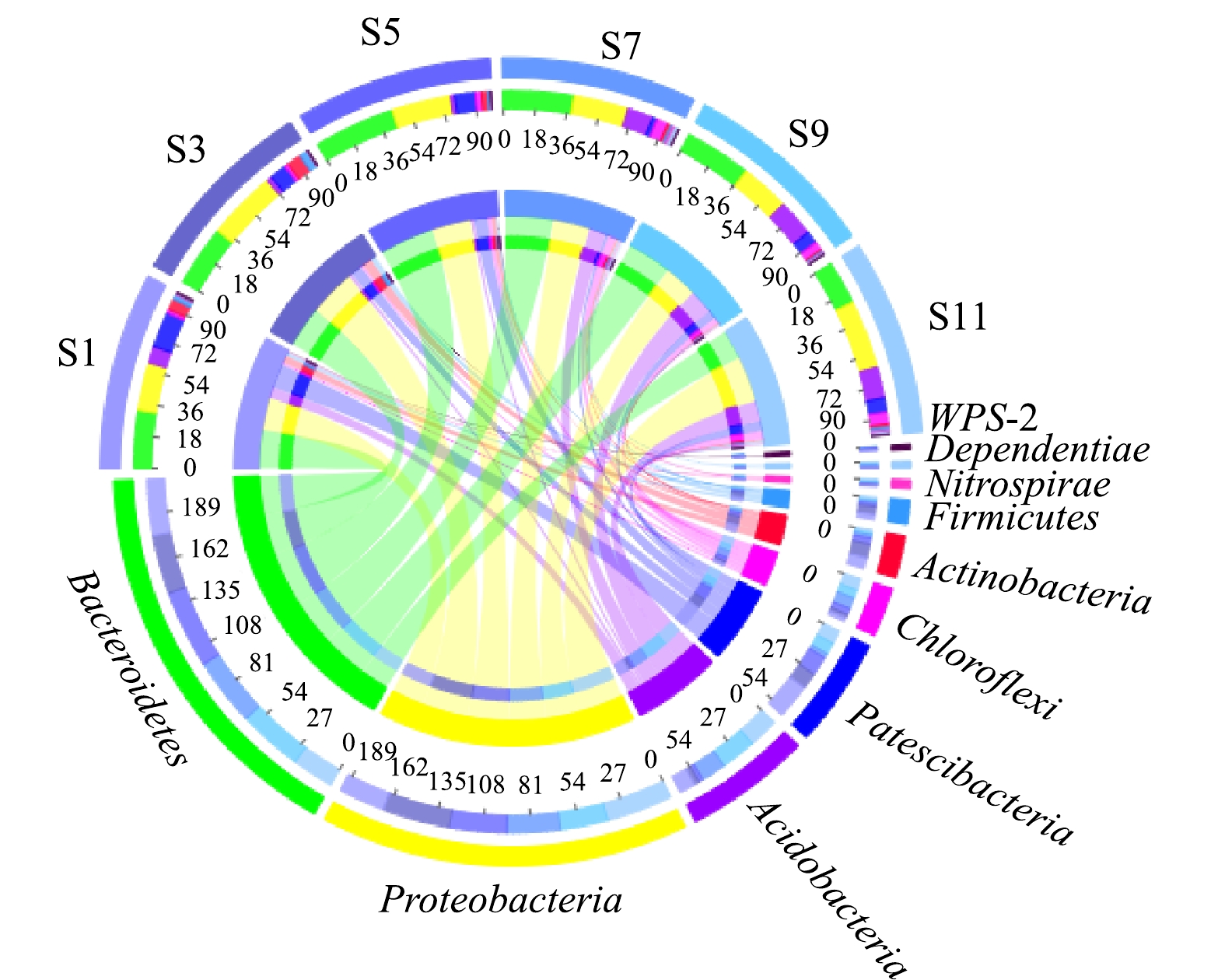
1)门水平上微生物群落结构分析。在门水平上,所有样本均检测到18~26个菌门,其中S3样本仅18个菌门,而S9和S11样本检测到26个菌门,相对丰度在前10的菌门见图2。由图2可见,S1、S3、S5样本中相对丰度较高的菌门为Bacteroidetes、Proteobacteria和Patescibacteria;而S7、S9和S11中主要优势菌门为Bacteroidetes、Proteobacteria和Acidobacteria。在活性污泥系统中,Proteobacteria和Bacteroidetes作为优势菌门已被多次报道[13-14]。在废水生物处理系统中,绝大部分具有去除有机物和脱氮除磷等功能的微生物属于Proteobacteria和Bacteroidetes菌门[14],其相对较高的丰度可保证该污水处理厂污染物的稳定去除。
同时值得注意的是,不同样本的菌门相对丰度存在较大的差异,如Actinobacteria和Chloroflexi,这可能主要是由于污水处理厂进水水质差异以及不同时间段环境温度差异所致。有研究表明,Actinobacteria和Chloroflexi是活性污泥中的主要丝状菌门,其中属于Actinobacteria的丝状菌如Candidatus Microthrix常常引发污泥膨胀,而隶属Chloroflexi的丝状菌通常充当菌胶团骨架[15]。因此,由图2可以看到,在污水处理厂发生污泥膨胀的S1和S3样本中Actinobacteria相对丰度高于其他样本,而在其他样本中Chloroflexi相对丰度比在S1和S3样本中的相对丰度高。
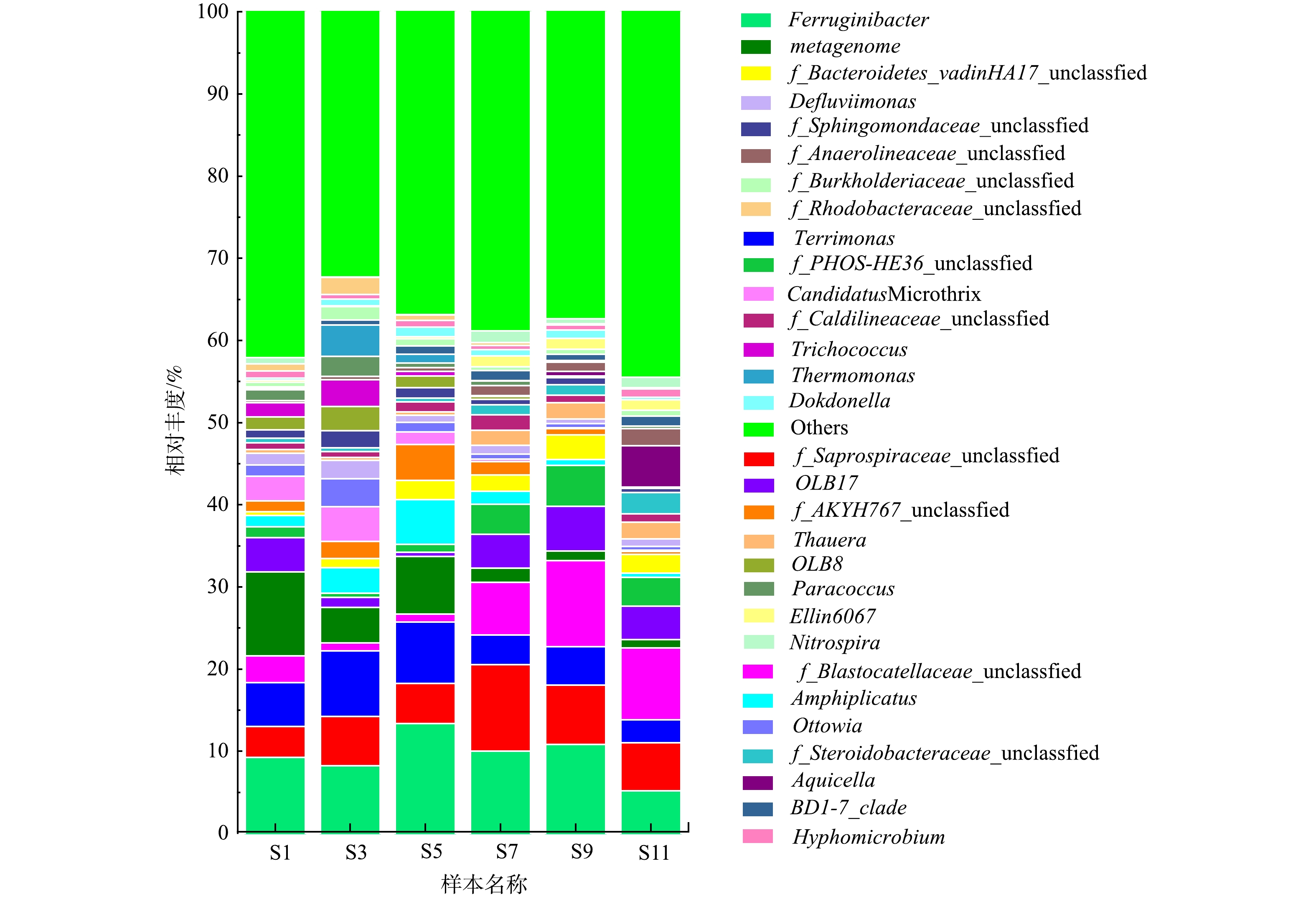
2)属水平微生物群落结构。属水平上微生物群落结构分析更有助于理解系统微生物群落的组成和演替,6个污水处理厂活性污泥样本中相对丰度前30的细菌属见图3。由图3可以看出,该污水处理厂活性污泥中主要菌属有Ferruginibacter、f_Saprospiraceae_unclassified、Terrimonas、f_Blastocatellaceae_unclassified和metagenome,相对丰度分别为5.19%~13.36%、3.73%~10.56%、2.79%~8.01%、0.96%~10.47%、1.06%~10.22%。贺赟等[16]对不同季节城市污水处理厂微生物群落研究也发现Ferruginibacter和Blastocatellaceae是污水处理厂的主要优势菌属。Ferruginibacter具有将复杂有机物分解为小分子有机物的能力[17],Blastocatellaceae能够降解复杂有机物同时可以完全还原NO- 3-N[18]。Saprospiraceae是活性污泥系统中的核心菌属,其不仅能够降解有机物和蛋白质,还具有反硝化除磷能力[19]。Terrimonas是一种典型的反硝化菌[20]。综上所述,这些优势菌属均为能够去除污染物的功能菌,其较高的相对丰度保证了污水处理厂的稳定运行。
同时可以注意到,经常报道能够引发活性污泥膨胀的一种丝状菌属Candidatus Microthrix [21]有被检测到。由图3可以看到,污水处理厂S1和S3样本中Candidatus Microthrix相对丰度较高,分别为3.03%和4.24%,在S5和S7样本中其相对丰度降低至1.49%和0.28%,并在S9和S11中相对丰度进一步降低。在1—3月份,该污水处理厂发生污泥膨胀,污泥SVI均在150 mL·g−1以上,自3月下旬开始其逐渐降低,污泥沉降性能逐渐恢复。由此可以推断,该污水处理厂污泥沉降性能的恶化主要是由于Candidatus Microthrix过度生长所导致,这与春季低温条件利于Candidatus Microthrix的生长有关[21]。故Candidatus Microthrix是1—3月份引发污泥膨胀的主要菌属。这与WANG等[22]对北方城市污水处理厂研究发现是冬春季节引发污泥膨胀的主要菌属是Candidatus Microthrix的研究结果是一致的。
3)功能菌群分析。功能菌群对污水处理厂的稳定运行具有重要作用,活性污泥系统中目前已报道的主要功能菌群有聚糖菌(GAO)、聚磷菌(PAO)、氨氧化菌(AOB)、亚硝酸盐氧化菌(NOB)、反硝化菌(DNB)、反硝化聚磷菌(DPB)、胞外聚合物(EPS)分泌菌等。根据对所研究污水处理厂样本在属水平上检测到的功能菌群进行分类,结果如表2所示。
典型聚糖菌Candidatus Competibacter在该污水处理厂样本内检测到,其相对丰度(0.17%~1.5%)高于典型聚磷菌Candidatus Accumulibacter的相对丰度(0.02%~0.29%),较低丰度的Candidatus Accumulibacter则会影响系统的除磷效果。Candidatus Accumulibacter与Candidatus Competibacter间的竞争关系已被多次报道,系统中Candidatus Competibacter相对丰度较高,则会抑制Candidatus Accumulibacter,使系统除磷效果较差。此外,另一种具有除磷功能的聚磷菌Tetrasphaera[23]在该污水处理厂样品中检出,且其相对丰度(0.02%~1.32%)也显著高于Candidatus Accumulibacter。Tetrasphaera也是一种引起污泥膨胀的丝状菌属,该属的丝状菌能够利用疏水性的长链脂肪酸等,使其在低温条件下占据优势生态位[34]。可以注意到,在污水处理厂发生污泥膨胀期间(1月和3月)Tetrasphaera的相对丰度较高,而非膨胀期间(9月和11月)其相对丰度较低,故该污水处理厂中检测到的Tetrasphaera可能主要是引发污泥膨胀的丝状菌。
此外,2种具有反硝化除磷功能的菌属f_Saprospiraceae_unclassified和Paracoccus也在该污水处理厂样品中检测到。对全球污水处理厂的调查研究表明,Saprospiraceae是活性污泥中的核心菌属[2],其具有代谢葡萄糖、半乳糖、特定蛋白质等能力[33]。同时,Saprospiraceae能够将亚硝酸盐氮作为电子受体,是反硝化除磷系统中的优势菌[19]。Paracoccus在缺氧条件下能够以亚硝酸盐氮为电子受体氧化厌氧条件下合成的聚β-羟基丁酸盐(PHB)以产生能量用于吸磷[24]。2种反硝化除磷功能菌的存在表明系统中存在反硝化除磷现象,且f_Saprospiraceae_unclassified和Paracoccus的相对丰度(3.73%~10.56%和0.15%~2.39%)明显高于聚磷菌Candidatus Accumulibacter的相对丰度,故该污水处理厂可能以反硝化除磷为主。
Nitrosomonas和Nitrospira分别是活性污泥中经常出现的AOB和NOB,在该污水处理厂中其相对丰度分别为0.03%~0.95%和0.04%~1.42%。在3月份和5月份的污泥样品中,Nitrosomonas和Nitrospira的相对丰度均为最低,表明Nitrosomonas和Nitrospira受污泥膨胀影响较大,污泥膨胀发生期间,丝状菌的过度生长抑制了Nitrosomonas和Nitrospira的生长。
此外,该污水处理厂污泥样品中还检测到了多种DNB菌属,丰度相对较高的是Ferruginibacter (5.19%~13.36%)、Terrimonas(2.79%~8.01%)、f_Blastocatellaceae_unclassified (0.96%~10.47%)、Amphiplicatus (0.48%~5.46%)、Ottowia (0.46%~3.41%)等。这些相对丰度较高的反硝化菌是系统实现脱氮的保证。Ferruginibacter菌属能够水解尿素、明胶等有机物,具备将大分子有机物分解为小分子的能力[17],同时也具有反硝化能力[25]。1—9月的样品中Ferruginibacter均为优势反硝化菌,11月样品中优势反硝化菌却为f_Blastocatellaceae_unclassified,故Ferruginibacter对该污水处理厂有机物的降解和脱氮具有重要作用。f_Blastocatellaceae_unclassified能够代谢复杂有机聚合物,同时它也可以利用聚羟基脂肪酸酯(PHA)完全还原硝酸盐氮[18]。故1—9月Ferruginibacter与11月f_Blastocatellaceae_unclassified优势反硝化菌转变的主要原因可能是进水水质差异(如有机物种类、含量等)所致。可以注意到,在整个研究周期内活性污泥样品中f_Blastocatellaceae_unclassified相对丰度变化比较大,污泥膨胀发生期间(3月和5月)f_Blastocatellaceae_unclassified的相对丰度较其他月份显著降低,表明其受污泥膨胀影响较大。据报道,Terrimonas是一种好氧反硝化菌属,能够还原硝酸盐氮,是改良两级A/O和传统两级A/O工艺中的优势菌属[26]。Amphiplicatus是严格好氧型细菌,具备反硝化脱氮性能,却不能水解纤维素、果胶、酪蛋白等基质[27]。Ottowia不仅报道与反硝化作用有关,还是一种重要的具有水解功能细菌,所以能够同时发挥脱氮和有机物降解的作用[28]。此外,经常报道的优势反硝化菌如Thauera等,在该污水厂中相对丰度并不高,且可以注意到在1—5月其相对丰度较低,表明其受低温影响较大。这些反硝化菌的存在保证该污水处理厂脱氮性能的稳定。
能够分泌EPS的絮凝菌也是活性污泥微生物的重要组成部分。有报道称,Terrimonas通过分泌EPS在微生物聚集体中起促进絮凝和聚集的重要作用[32]。HE等[30]总结了不同操作条件下能够产生EPS的关键功能菌,其中Thauera和Devosia能够分泌EPS并进行反硝化。这些EPS产生菌有助于维持活性污泥的聚集和稳定以及对部分营养物质的去除。
-
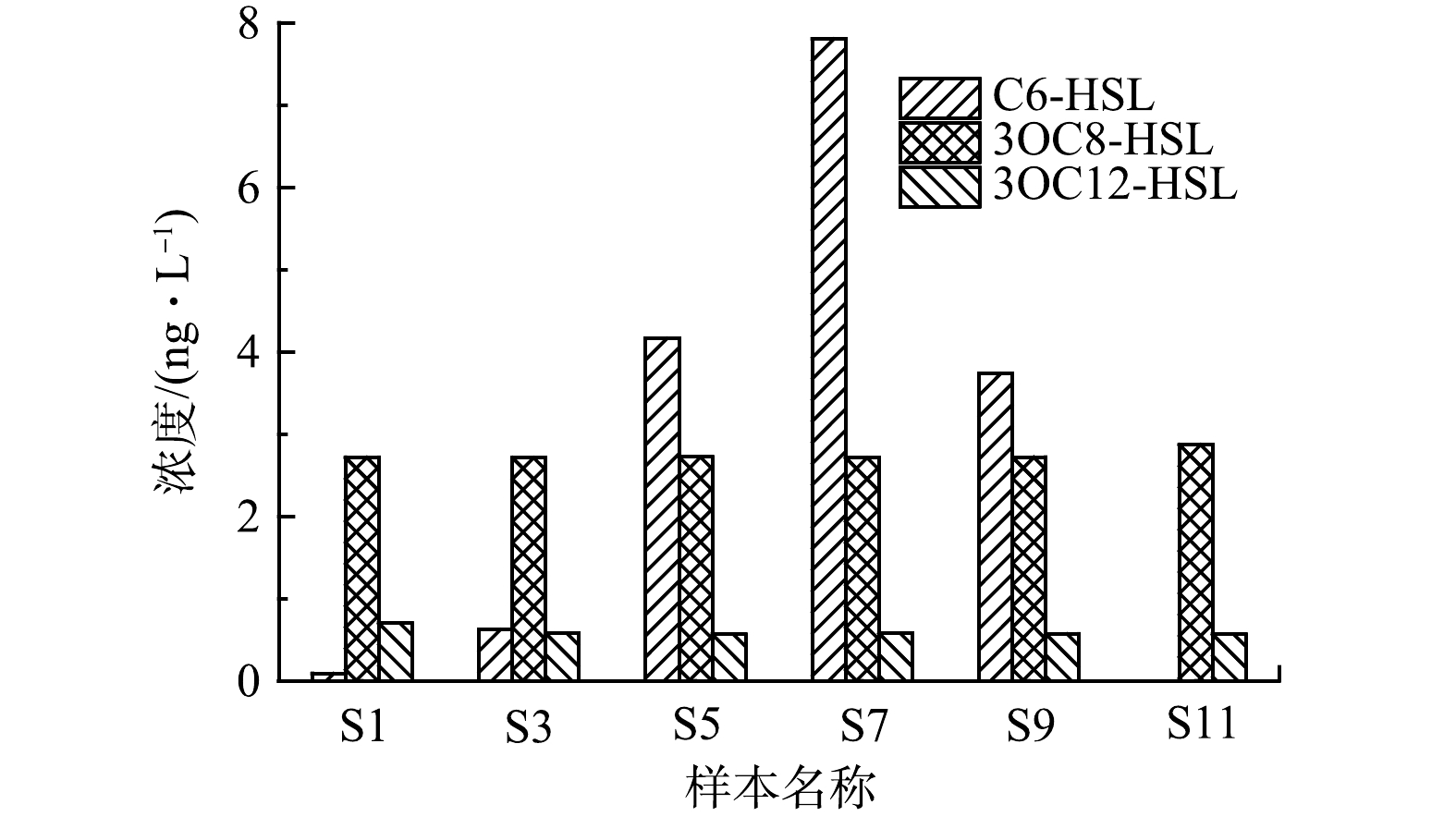
1)群体感应信号分子。在该污水处理厂样品中检测到N-己酰高丝氨酸环内酯(C6-HSL)、3-羰基辛酰基高丝氨酸内酯(3OC8-HSL)和3-羰基十二酰基高丝氨酸内酯(3OC12-HSL)共3种AHLs,其每月平均浓度变化如图4所示。由图4可知,3OC8-HSL和3OC12-HSL的质量浓度相对比较稳定,分别维持在2.7 ng·L−1和0.6 ng·L−1(略有浮动)。而C6-HSL变化较大,1—7月其质量浓度逐渐由0.09 ng·L−1升高至7.8 ng·L−1,此后又降低至3.7 ng·L−1,而在11月份样品中未检出。可以注意到,较低气温下C6-HSL浓度也较低,而较高温度下其浓度也比较高,表明C6-HSL的产生可能与温度呈现一定的相关性。另外,污泥膨胀期间,C6-HSL浓度较低,而非膨胀期间,其浓度相对比较高,故C6-HSL可能与污泥膨胀或丝状菌生长存在调控关系。
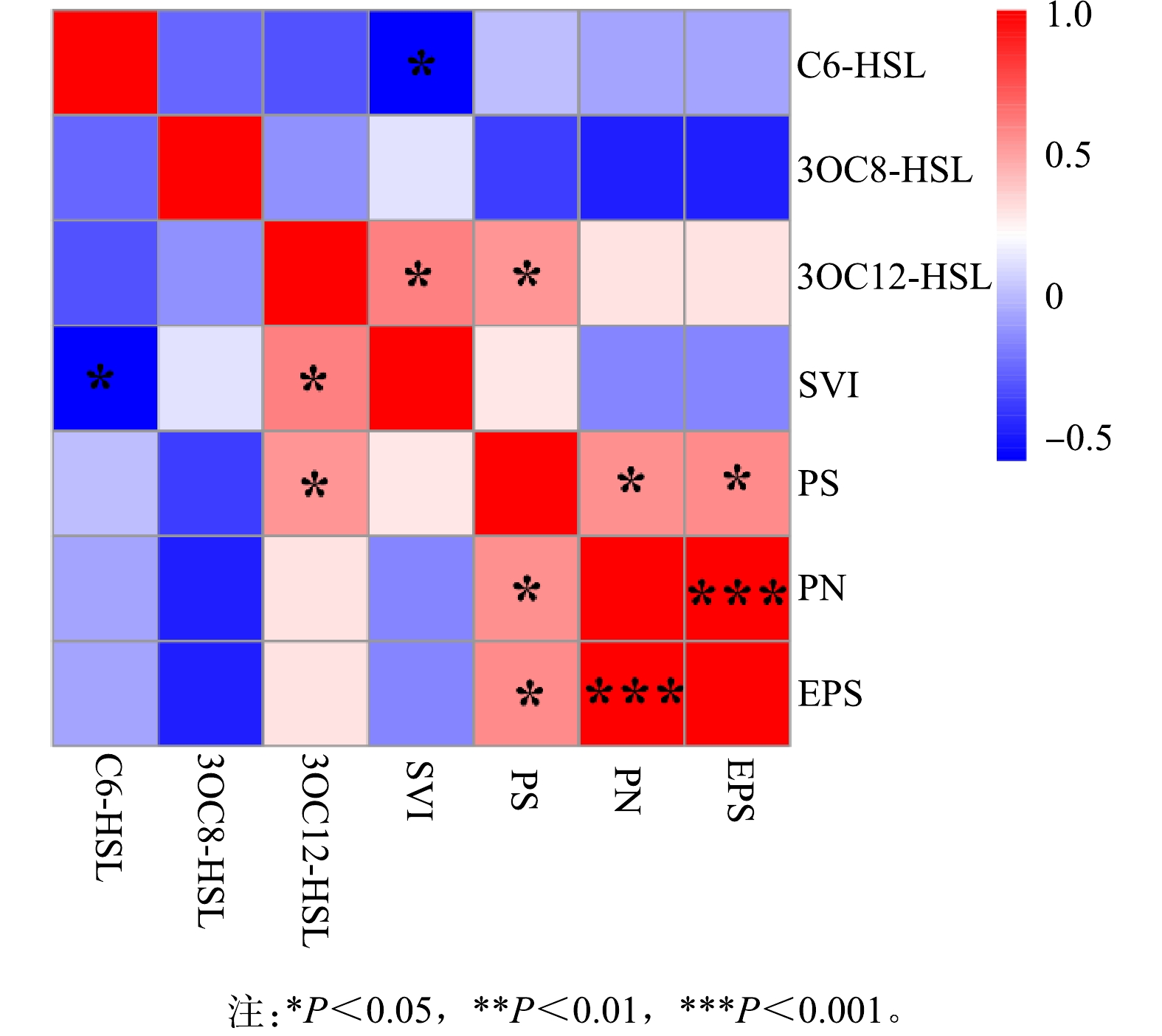
2)群体感应与污泥沉降性。为研究群体感应调控作用,进行Person相关性分析结果如图5所示。可见污泥容积指数(SVI)与C6-HSL呈显著负相关(P<0.05),与3OC12-HSL呈显著正相关(P<0.05),则C6-HSL、3OC12-HSL均与污泥沉降性有关。其中,C6-HSL能够调控抑制系统污泥膨胀的发生,使系统污泥沉降性能良好,而3OC12-HSL能够调控引发系统污泥膨胀的发生,使系统污泥沉降性能恶化。C6-HSL与污泥膨胀之间的调控作用与之前LI等[6]的研究结果是一致的,故鉴于C6-HSL对污泥膨胀的调控作用可以向发生污泥膨胀的系统中投加C6-HSL或者促进C6-HSL信号分子的产生以控制污泥膨胀。此外,3OC12-HSL与多糖(PS)含量呈显著正相关(P<0.05),表明3OC12-HSL主要调控多糖的产生。群体感应对EPS产生的调控作用在不同反应器和城市污水处理厂中均有报道,但在本研究中并没有观察到,这可能主要是工艺、运行条件等的差异[35]。
3)群体感应与微生物群落调控作用。为分析群体感应与微生物群落间的调控作用,将相对丰度前50的菌属与AHLs进行Person相关分析,与AHLs信号分子具有显著相关的细菌属只有f_Saprospiraceae_unclassified、f_Bacteroidetes_vadinHA17_unclassified、SWB02、OLB12、f_Caldilineaceae_unclassified(图6)。f_Saprospiraceae_unclassified、f_Caldilineaceae_unclassified、SWB02与C6-HSL呈显著正相关,其相关系数分别为0.913、0.864、0.904,OLB12与C6-HSL呈极显著正相关,其相关系数为0.982,表明f_Saprospiraceae_unclassified、f_Caldilineaceae_unclassified、SWB02、OLB12是主要的C6-HSL产生菌。而f_Bacteroidetes_vadinHA17_unclassified与3OC12-HSL呈显著负相关,相关系数为−0.819,表明f_Bacteroidetes_vadinHA17_unclassified是3OC12-HSL的群体淬灭菌。
-
为进一步分析该污水处理厂微生物群落的关键功能基因表达情况,采用Tax4Fun基于该污水处理厂污泥样品高通量测序进行KEGG功能基因预测,分析结果见表3。氨基酸代谢(amino acid metabolism)、碳水化合物代谢(carbohydrate metabolism)、膜转运(membrane transport)、能量代谢(energy metabolism)和辅酶因子和维生素代谢(metabolism of cofactors and vitamins)为该污水处理厂中相对丰度较高的代谢功能。氨基酸代谢(amino acid metabolism)、碳水化合物代谢(carbohydrate metabolism)、能量代谢(energy metabolism)和辅酶因子和维生素代谢(metabolism of cofactors and vitamins)均属于新陈代谢(metabolism)功能模块,而膜转运(membrane transport)属于环境信息处理(environmental information processing)功能模块。碳水化合物代谢(carbohydrate metabolism)途径可以将大分子碳水化合物分解、稳定为小分子物质,氨基酸代谢(amino acid metabolism)过程可为反硝化脱氮提供电子,能量代谢(energy metabolism)途径在ATP代谢、电子传输等能量运输中起着关键作用[36],膜转运(membrane transport)在物质运输、群体感应调控方面发挥重要作用[30],这些代谢功能保证了该污水处理厂的正常运行。可以发现一些代谢功能的相对丰度在不同样品中差异较大,可能是由进水水质、运行条件等差异所导致,从而影响污水处理厂有机物的降解、脱氮除磷等性能。
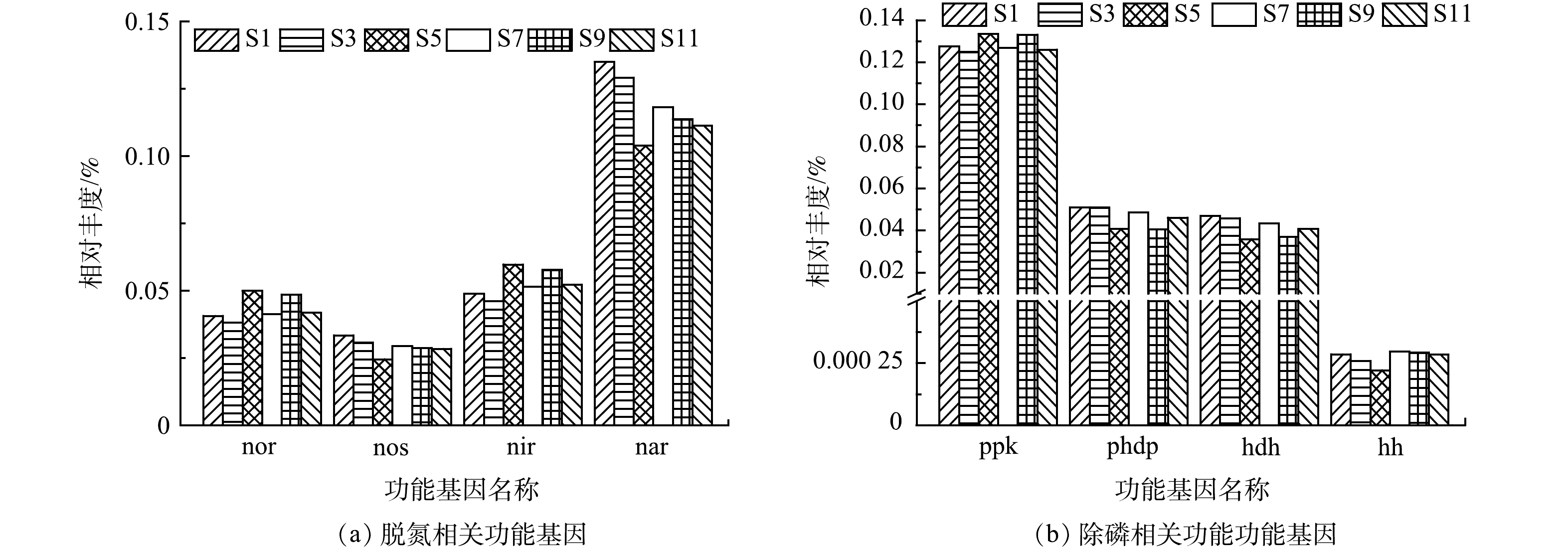
此外,通过深入分析脱氮除磷过程中相关基因的相对丰度表达情况,发现4种参与反硝化过程的nor(一氧化氮还原酶)、nos(一氧化二氮还原酶)、nir(亚硝酸盐还原酶)和nar(硝酸盐还原酶)[37],其中在硝酸盐氮还原为亚硝酸盐氮过程中起重要作用的nar(硝酸盐还原酶)相对丰度(0.104%~0.135%)明显高于其他还原酶((图7(a))。硝酸盐氮的还原是反硝化过程的第一步,是影响脱氮性能的关键过程,因此nar(硝酸盐还原酶)是影响脱氮性能的重要基因,对脱氮性能具有重要决定作用。S5样品的nar(硝酸盐还原酶)相对丰度是所有样品中最低的,同时该样品中nos(一氧化二氮还原酶)相对丰度也是最低的,表明5月份污水处理厂的脱氮性能较其他月份较差。
发现4种参与除磷相关的功能基因,其中ppk(聚磷酸盐激酶)的相对丰度(0.125%~0.133%)明显高于phdp(聚-β-羟基丁酸解聚酶,相对丰度0.041%~0.051%)、hdh(羟丁酸脱氢酶,相对丰度0.036%~0.047%)和hh(羟基丁酸二聚体水解酶,相对丰度0.000 221%~0.000 297%)。ppk(聚磷酸盐激酶)与Poly-P形成相关,而其他3种均与聚-β-羟基丁酸降解有关[37],虽然具有较高的Poly-P形成能力,但受限于较低的聚-β-羟基丁酸降解能力,导致系统的除磷能力较低,故仍需借助化学除磷实现磷的去除。S5样品中与聚-β-羟基丁酸降解有关的3种功能基因相对丰度在所有样品中最低,表明5月份污水处理厂的磷去除能力略逊于其他月份。
-
1)在1—3月污水处理厂发生污泥膨胀为微生物多样性和微生物群落结构存在差异的主要原因,Candidatus Microthrix过量生长是引发污泥膨胀的主要原因。
2) Bacteroidetes、Proteobacteria和Acidobacteria为该污水处理厂的主要优势菌门,Ferruginibacter、f_Saprospiraceae_unclassified、Terrimonas、f_Blastocatellaceae_unclassified和metagenome为该污水处理厂中主要优势菌属。Candidatus Accumulibacter、Nitrosomonas、Nitrospira、Ferruginibacter、Terrimonas等相关功能菌的存在使系统维持相对稳定运行。
3)污水处理厂中检测到C6-HSL、3OC8-HSL和3OC12-HSL3种AHLs,C6-HSL主要调控抑制系统污泥膨胀的发生,3OC12-HSL主要调控多糖的产生。群体感应与微生物群落间的调控作用分析表明f_Saprospiraceae_unclassified、f_Caldilineaceae_unclassified、SWB02、OLB12是主要的C6-HSL产生菌,f_Bacteroidetes_vadinHA17_unclassified是3OC12-HSL的群体淬灭菌。
4)功能预测分析结果表明,5月份样品中nar(硝酸盐还原酶)、nos(一氧化二氮还原酶)、phdp(聚-β-羟基丁酸解聚酶)、hdh(羟丁酸脱氢酶)和hh(羟基丁酸二聚体水解酶)相对丰度均较其他样品低,故其脱氮除磷性能均略逊于其他月份。
城市污水处理厂微生物群落特征与群体感应调控
Microbial community characteristics and their quorum sensing regulation in municipal wastewater treatment plants
-
摘要: 微生物群落在活性污泥中发挥有重要作用,为了解采用活性污泥法的城市污水处理厂微生物群落特征和群体感应调控作用,采集天津市某城市污水处理厂活性污泥样品,采用高通量测序对其微生物群落特征进行解析,并分析其群体感应调控作用。结果表明,该污水处理厂一年间活性污泥样品的微生物多样性和微生物群落结构存在一定差异性,主要是由于冬春季节发生了污泥膨胀。Ferruginibacter、f_Saprospiraceae_unclassified、Terrimonas、f_Blastocatellaceae_unclassified和metagenome等是该污水处理厂中主要优势菌属,冬春季节引发污泥膨胀的主要菌属是Candidatus Microthrix。群体感应调控作用分析表明C6-HSL能够抑制污泥膨胀,3OC12-HSL能够调控促进多糖的产生,f_Saprospiraceae_unclassified、f_Caldilineaceae_unclassified、SWB02、OLB12是主要的C6-HSL产生菌,f_Bacteroidetes_vadinHA17_unclassified是3OC12-HSL的群体淬灭菌。基于高通量测序的Tax4fun功能预测分析表明5月份污水处理厂的脱氮除磷性能均略逊于其他月份。Abstract: Microbial community plays an important role in activated sludge. To understand the microbial community characteristics and quorum sensing regulation in municipal wastewater treatment plant (WWTP) using the activated sludge process, the activated sludge samples from a municipal WWTP in Tianjin were collected, the microbial community characteristics were analysed by high-throughput sequencing, and their quorum sensing regulation was also analysed. The results showed that there were some differences in the microbial diversity and community structure of activated sludge samples during the year, which was mainly caused by sludge bulking in winter and spring. Ferruginibacter, f_Saprospiraceae_unclassified, Terrimonas, f_Blastocatellaceae_unclassified and metagenome were the dominant genera in the municipal WWTP, and Candidatus Microthrix was the main bacterium causing sludge bulking in winter and spring. Analysis of quorum sensing regulation showed that C6-HSL could inhibit sludge bulking, and 3OC12-HSL could promote the production of polysaccharides. f_Saprospiraceae_unclassified, f_Caldilineaceae_unclassified, SWB02 and OLB12 were the main C6-HSL producing bacteria, and f_Bacteroidetes_vadinHA17_unclassified was a quorum quenching bacterium of 3OC12-HSL. The functional prediction analysis by Tax4fun based on high-throughput sequencing showed that the nitrogen and phosphorus removal performance of WWTP in May was slightly inferior to that of other months.
-

-
表 1 样品中微生物多样性指数
Table 1. Microbial diversity index in samples
样品 ACE Chao1 Shannon Simpson 覆盖率/% S1 613.16 613.50 7.015 0.983 99.8 S3 588.12 600.84 6.920 0.983 99.8 S5 576.22 577.28 7.009 0.978 99.9 S7 646.34 644.04 7.167 0.982 99.8 S9 643.03 644.96 6.826 0.974 99.8 S11 647.57 650.17 7.118 0.982 99.9 表 2 功能菌属相对丰度
Table 2. Relative abundance of functional bacteria %
功能菌分类 功能菌属 相对丰度 参考文献 S1 S3 S5 S7 S9 S11 GAO Candidatus Competibacter 0.17 0.32 0.5 0.47 0.48 1.50 [3] PAO Tetrasphaera 0.87 1.32 0.48 0.19 0.03 0.02 [3, 23] Candidatus_Accumulibacter 0.02 0.04 0.29 0.11 0.05 0.11 [3] DPB f_Saprospiraceae_unclassified 3.73 5.99 4.9 10.56 7.23 5.82 [19] Paracoccus 1.35 2.39 0.57 0.58 0.15 0.27 [24] AOB Nitrosomonas 0.18 0.03 0.04 0.95 0.93 0.61 [3] NOB Nitrospira 0.76 0.1 0.04 1.42 0.63 1.25 [3] DNB Ferruginibacter 9.26 8.22 13.36 9.99 10.81 5.19 [25] Terrimonas 5.35 8.01 7.48 3.60 4.69 2.79 [26] f_Blastocatellaceae_unclassified 3.27 0.97 0.96 6.39 10.47 8.74 [18] Amphiplicatus 1.36 3.13 5.46 1.61 0.71 0.48 [27] Ottowia 1.38 3.41 1.19 0.59 0.49 0.46 [28] Defluviimonas 1.40 2.22 0.87 1.07 0.60 0.91 [29] Thauera 0.48 0.37 0.39 1.84 1.95 2.03 [3] Dokdonella 0.24 0.79 1.2 0.76 1.03 0.33 [11] Hyphomicrobium 0.86 0.56 0.79 0.54 0.61 0.99 [30] f_Rhodobacteraceae_unclassified 0.87 2.07 0.68 0.33 0.14 0.19 [30] Rhodobacter 0.84 1.85 0.61 0.20 0.09 0.06 [3] Novosphingobium 0.36 0.7 0.51 0.22 0.16 0.18 [30] Devosia 0.62 0.72 0.28 0.17 0.1 0.12 [30] Thiobacillus 1.28 0.28 0.29 0.03 0.01 0.02 [31] EPS分泌菌 Terrimonas 5.35 8.01 7.48 3.60 4.69 2.79 [32] Thauera 0.48 0.37 0.39 1.84 1.95 2.03 [30] Devosia 0.62 0.72 0.28 0.17 0.1 0.12 [30] 水解菌 Ferruginibacter 9.26 8.22 13.36 9.99 10.81 5.19 [17] f_Saprospiraceae_unclassified 3.73 5.99 4.9 10.56 7.23 5.82 [33] Ottowia 1.38 3.41 1.19 0.59 0.49 0.46 [28] 表 3 功能基因相对丰度
Table 3. Relative abundance of functional gene %
代谢功能 基因相对丰度 S1 S3 S5 S7 S9 S11 氨基酸代谢 13.94 13.88 12.82 13.63 12.96 13.52 碳水化合物代谢 12.58 12.66 11.77 12.33 11.87 12.26 膜转运 12.42 12.04 11.07 12.01 11.58 11.79 辅酶因子和维生素代谢 7.37 7.35 7.19 7.33 7.27 7.34 能量代谢 7.35 7.30 7.32 7.37 7.43 7.45 信号转导 6.62 6.74 7.47 6.94 7.38 7.05 核苷酸代谢 5.44 5.45 5.64 5.54 5.62 5.61 转译 4.34 4.45 4.69 4.44 4.57 4.52 外来生物的生物降解和代谢 4.68 4.61 4.33 4.56 4.34 4.45 复制和修复 3.80 3.88 4.48 4.01 4.33 4.10 脂质代谢 3.69 3.69 3.72 3.67 3.63 3.61 其他氨基酸代谢 2.98 2.97 2.95 2.95 2.90 2.89 萜类和多酮类化合物代谢 2.57 2.57 2.40 2.50 2.38 2.44 折叠、分类和降解 2.24 2.26 2.34 2.28 2.33 2.31 细胞运动 2.03 2.00 2.64 2.21 2.58 2.29 聚糖的生物合成和代谢 2.02 2.11 2.55 2.15 2.41 2.23 细胞生长和死亡 1.66 1.62 1.92 1.74 1.93 1.79 其他次生代谢物生物合成 0.91 0.92 0.90 0.89 0.87 0.88 运输和分解代谢 0.35 0.36 0.36 0.35 0.34 0.34 细胞群落—原核生物 0.32 0.32 0.36 0.32 0.35 0.33 转录 0.19 0.19 0.26 0.21 0.24 0.21 信号分子和相互作用 0.002 0.001 0.02 0.007 0.016 0.009 -
[1] SHEIK A R, MULLER E E L, WILMES P. A hundred years of activated sludge: time for a rethink[J]. Frontiers in Microbiology, 2014, 5: 47. [2] WU L, NING D, ZHANG B, et al. Global diversity and biogeography of bacterial communities in wastewater treatment plants[J]. Nature Microbiology, 2019, 4(7): 1183-1195. doi: 10.1038/s41564-019-0426-5 [3] 鞠峰, 张彤. 活性污泥微生物群落宏组学研究进展[J]. 微生物学通报, 2019, 46(8): 2038-2052. [4] 马切切, 袁林江, 牛泽栋, 等. 活性污泥微生物群落结构及与环境因素响应关系分析[J]. 环境科学, 2021, 42(8): 3886-3893. [5] 程珂珂, 曾艳华, 蔡中华, 等. 微生物的交流信号[J]. 生物化学与生物物理进展, 2022, 49(6): 960-974. [6] LI S, FEI X, CHI Y, et al. Impact of the acetate/oleic acid ratio on the performance, quorum sensing, and microbial community of sequencing batch reactor system[J]. Bioresource Technology, 2020, 296: 122279. doi: 10.1016/j.biortech.2019.122279 [7] HU H, LIU Y, LUO F, et al. Stable and rapid partial nitrification achieved by boron stimulating autoinducer-2 mediated quorum sensing at room & low temperature[J]. Chemosphere, 2022, 304: 135327. doi: 10.1016/j.chemosphere.2022.135327 [8] WANG N, GAO J, LIU Y, et al. Realizing the role of N-acyl-homoserine lactone-mediated quorum sensing in nitrification and denitrification: A review[J]. Chemosphere, 2021, 274: 129970. doi: 10.1016/j.chemosphere.2021.129970 [9] LIU Q, FENG X, SHENG Z, et al. Enhanced wastewater treatment performance by understanding the interaction between algae and bacteria based on quorum sensing[J]. Bioresource Technology, 2022, 354: 127161. doi: 10.1016/j.biortech.2022.127161 [10] MADDELA N R, SHENG B, YUAN S, et al. Roles of quorum sensing in biological wastewater treatment: A critical review[J]. Chemosphere, 2019, 221: 616-629. doi: 10.1016/j.chemosphere.2019.01.064 [11] LI S, FEI X, CAO L, et al. Insights into the effects of carbon source on sequencing batch reactors: Performance, quorum sensing and microbial community[J]. Science of the Total Environment, 2019, 691: 799-809. doi: 10.1016/j.scitotenv.2019.07.191 [12] AßHAUER K P, WEMHEUER B, DANIEL R, et al. Tax4Fun: predicting functional profiles from metagenomic 16S rRNA data[J]. Bioinformatics, 2015, 31(17): 2882-2884. doi: 10.1093/bioinformatics/btv287 [13] CHU H, LIU X, MA J, et al. Two-stage anoxic-oxic (A/O) system for the treatment of coking wastewater: Full-scale performance and microbial community analysis[J]. Chemical Engineering Journal, 2021, 417: 129204. doi: 10.1016/j.cej.2021.129204 [14] FENG Z, LI T, LIN Y, et al. Microbial communities and interactions in full-scale A2/O and MBR wastewater treatment plants[J]. Journal of Water Process Engineering, 2022, 46: 102660. doi: 10.1016/j.jwpe.2022.102660 [15] WANG P, YU Z, QI R, et al. Detailed comparison of bacterial communities during seasonal sludge bulking in a municipal wastewater treatment plant[J]. Water Research, 2016, 105: 157-166. doi: 10.1016/j.watres.2016.08.050 [16] 贺赟, 李魁晓, 王佳伟, 等. 不同季节城市污水处理厂微生物群落特性[J]. 环境科学, 2021, 42(3): 1488-1495. doi: 10.13227/j.hjkx.202007015 [17] 黎镛, 袁辉洲, 柯水洲, 等. 微生物载体对MBBR工艺性能及微生物群落结构的影响[J]. 环境工程, 2021, 39(12): 100-106. doi: 10.13205/j.hjgc.202112015 [18] ZHANG L, HAO S, WANG Y, et al. Rapid start-up strategy of partial denitrification and microbially driven mechanism of nitrite accumulation mediated by dissolved organic matter[J]. Bioresource Technology, 2021, 340: 125663. doi: 10.1016/j.biortech.2021.125663 [19] 顾晓丹, 黄勇, 丁永伟, 等. 改良型UNITANK工艺冬季运行特性及微生物群落分析[J]. 环境工程学报, 2021, 15(7): 2480-2487. doi: 10.12030/j.cjee.202102134 [20] 尚越飞, 王申, 宗倪, 等. 污水生物处理工艺低温下微生物种群结构[J]. 环境科学, 2020, 41(10): 4636-4643. doi: 10.13227/j.hjkx.202004116 [21] FAN N, QI R, HUANG B, et al. Factors influencing Candidatus Microthrix parvicella growth and specific filamentous bulking control: A review[J]. Chemosphere, 2020, 244: 125371. doi: 10.1016/j.chemosphere.2019.125371 [22] WANG J, QI R, LIU M, et al. The potential role of ‘Candidatus Microthrix parvicella’ in phosphorus removal during sludge bulking in two full-scale enhanced biological phosphorus removal plants[J]. Water Science and Technology, 2014, 70(2): 367-375. doi: 10.2166/wst.2014.216 [23] LIU H, ZENG W, MENG Q, et al. Phosphorus removal performance, intracellular metabolites and clade-level community structure of Tetrasphaera-dominated polyphosphate accumulating organisms at different temperatures[J]. Science of the Total Environment, 2022, 842: 156913. doi: 10.1016/j.scitotenv.2022.156913 [24] 叶丽红, 李冬, 张杰, 等. 亚硝化-反硝化除磷技术研究进展[J]. 北京工业大学学报, 2016, 42(4): 585-593. doi: 10.11936/bjutxb2015070009 [25] 赖永恒, 刘敏. A/O-MBBR工艺处理生活污水性能及菌群结构[J]. 中国环境科学, 2022, 42(5): 2120-2128. doi: 10.3969/j.issn.1000-6923.2022.05.016 [26] CHEN X, XU P, YANG C, et al. Study of enhanced nitrogen removal efficiency and microbial characteristics of an improved two-stage A/O process[J]. Environmental Technology, 2021, 42(27): 4306-4316. doi: 10.1080/09593330.2020.1754924 [27] 张晶晶, 杨翠春, 丁鹏霖, 等. MBBR工艺用于唐山某污水厂提标改造效能分析[J]. 中国给水排水, 2020, 36(15): 78-85. [28] LI J, DU Q, PENG H, et al. Optimization of biochemical oxygen demand to total nitrogen ratio for treating landfill leachate in a single-stage partial nitrification-denitrification system[J]. Journal of Cleaner Production, 2020, 266: 121809. doi: 10.1016/j.jclepro.2020.121809 [29] WANG L, ZHAN H, WU G, et al. Effect of operational strategies on the rapid start-up of nitrogen removal aerobic granular system with dewatered sludge as inoculant[J]. Bioresource Technology, 2020, 315: 123816. doi: 10.1016/j.biortech.2020.123816 [30] HE Q, CHEN L, ZHANG S, et al. Hydrodynamic shear force shaped the microbial community and function in the aerobic granular sequencing batch reactors for low carbon to nitrogen (C/N) municipal wastewater treatment[J]. Bioresource Technology, 2019, 271: 48-58. doi: 10.1016/j.biortech.2018.09.102 [31] ZHANG R, CHEN C, XU X, et al. The interaction between Pseudomonas C27 and Thiobacillus denitrificans in the integrated autotrophic and heterotrophic denitrification process[J]. Science of the Total Environment, 2022, 811: 152360. doi: 10.1016/j.scitotenv.2021.152360 [32] ZHAO Y, JIANG B, TANG X, et al. Metagenomic insights into functional traits variation and coupling effects on the anammox community during reactor start-up[J]. Science of the Total Environment, 2019, 687: 50-60. doi: 10.1016/j.scitotenv.2019.05.491 [33] 郑向阳, 罗晓, 袁立霞, 等. AO工艺处理淀粉污水效能及微生物群落解析[J]. 环境工程学报, 2018, 12(3): 804-814. doi: 10.12030/j.cjee.201708047 [34] 王萍, 余志晟. 污水处理厂污泥膨胀和污泥发泡的比较分析[J]. 微生物学通报, 2019, 46(8): 1971-1981. [35] HUANG J, SHI Y, ZENG G, et al. Acyl-homoserine lactone-based quorum sensing and quorum quenching hold promise to determine the performance of biological wastewater treatments: An overview[J]. Chemosphere, 2016, 157: 137-151. doi: 10.1016/j.chemosphere.2016.05.032 [36] 罗景阳, 张乐, 张腾, 等. 不同工艺对污水处理效能及细菌代谢功能的影响[J]. 中国给水排水, 2021, 37(23): 61-67. doi: 10.19853/j.zgjsps.1000-4602.2021.23.011 [37] FANG D, ZHAO G, XU X, et al. Microbial community structures and functions of wastewater treatment systems in plateau and cold regions[J]. Bioresource Technology, 2018, 249: 684-693. doi: 10.1016/j.biortech.2017.10.063 -



 下载:
下载: