-
有机固体废弃物经厌氧发酵处理后可产生生物质能源,是未来固废处理处置技术碳减排的主要发展方向之一。餐厨垃圾和城市污泥都属于有机固体废物。截至2018年,我国餐厨垃圾的年产量超过了1.0×108 t[1],餐厨垃圾中富含淀粉、脂类、蛋白质及纤维素等有机物,对其进行生物转化后再利用已成为其主要处理方式。城市污泥是城镇污水处理厂的副产物,随着污水处理率的提高,城市污泥产生量亦随之逐年递增[2]。因此,被逐渐淘汰的填埋处理方式和综合成本较高的焚烧处理处置方式,已不能满足对城市污泥处理处置的节能减排要求[3]。在碳中和背景下,将这些有机固废进行厌氧发酵以获取生物质能源,符合节能降耗及资源回收的目标[4]。
氢气是清洁能源,可利用范围很广。氢气产于厌氧发酵的初级阶段,但通常产氢效率不高。为提高产氢率,相对早期的研究集中在污泥不同方式的预处理方面[5-7]。目前,已有采用添加铁刨花促进厌氧发酵产氢的报道[8]。近年来,有关铁系物对厌氧发酵产甲烷影响的研究越来越得到关注,相关报道分别集中在零价铁或三价、二价铁方面,这主要是铁元素在系统中的多重作用导致[9-16]。截至目前,这些研究已取得较理想的效果[8,17-18]。因为甲烷是从厌氧发酵第二阶段的产氢产乙酸转化而来,因此,提高第二阶段的产氢产酸量,才能有助于提高甲烷产量。然而,上述研究仅针对厌氧产沼气方面,而对产氢的效果和机理研究较少[18-19]。此外,目前还尚无多价态铁复合材料对厌氧发酵产氢的研究报道。
为提高有机固废发酵产氢效率,基于前期研究基础[20-22],本实验利用机械加工厂的废弃铁刨花制备了一种新型复合铁材料(FE/FEO),探讨FE/FEO材料对城市污泥与餐厨垃圾混合固废的厌氧发酵产氢作用;并考察其厌氧发酵的产氢效果,分析厌氧发酵过程中各种指标的变化,并对制备的FE/FEO材料的形貌、成分进行了测试,最终对其厌氧发酵的作用进行了阐述。本研究拟为提高厌氧发酵产氢方面提供新技术和数据积累。
-
1) 供试混合有机固体废物。本实验所用有机固废是餐厨垃圾和城市污泥的混合物。餐厨垃圾来自于某学校食堂,主要成分为蔬菜和米饭,粉碎后备用。城市污泥取自常州市某城镇污水处理厂,去除其中的大颗粒物和毛发后,调其含固率至3.12%,然后进行碱解预处理30 min[23]。最后,将上述预处理好的餐厨垃圾和城市污泥按照体积比1∶1[22]比例混合均匀后备用。上述各物料的理化指标见表1。
2) FE/FEO的制备。从机械加工厂取废铁刨花,经清洁、氧化、烘干、破碎等步骤,制成0.10~0.50 cm的多孔状颗粒物FE/FEO,再于100 ℃烘箱烘干,反复若干次,直至成型,备用。
-
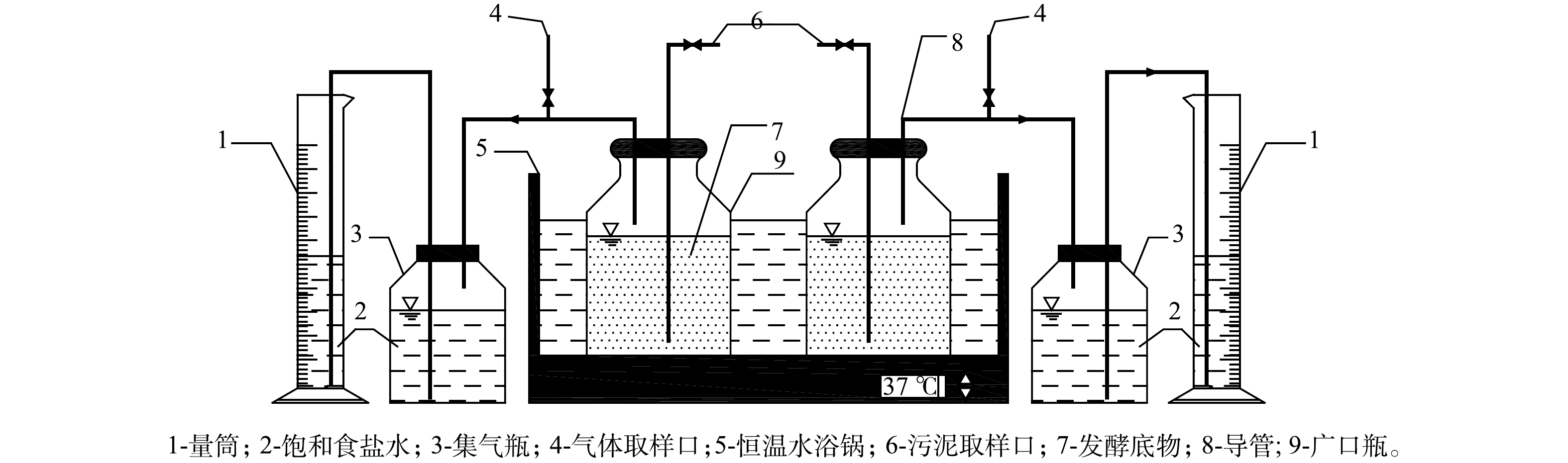
将混合好的有机固废放入有效体积为750 mL的玻璃反应器中,投加20 g·L−1FE/FEO后,混合均匀,置于恒温水浴锅中进行高温厌氧消化(55 ℃)以启动实验。经过若干批次,直至产气稳定后,取1/3体积的混合物作为接种物,采用上述物料,进入正式实验,厌氧发酵产氢24 h。每4 h取气样和发酵液进行测试。同时,与对照组进行比较。因FE/FEO材料可以多次使用,故过量投加,反应后可回收使用。实验搭建的厌氧消化反应装置如图1所示。
-
复合铁材料FE/FEO中除零价铁外的其他成分,分别用傅里叶变换红外光谱仪(IR200型)和同步热分析仪(STA25000型)对其官能团进行定性分析和热重测试。
分析项目包括:产气量和气体成分;厌氧系统中混合底物的pH;发酵液的挥发性脂肪酸VFA质量浓度、溶解性化学需氧量SCOD质量浓度和亚铁离子质量浓度。以上指标每4 h测定1次。发酵液取自厌氧反应器中的混合物,在6 000 r·min-1转速条件下离心5 min后,取上清液经45 μm孔径的滤纸过滤后得到。厌氧反应结束后,取发酵底物进行微生物菌群形貌测试。
厌氧产气的各成分采用岛津GC-2014型气相色谱仪进行测定,色谱柱(1 m×6 mm,5A分子筛)进样口温度100 ℃,热导检测器温度100 ℃,载气采用氩气,柱温50 ℃,恒温分析10 min。pH采用pHS-3C型精密酸度计测定。VFA测定方法按照文献[24]。SCOD质量浓度用连华水质快速测定仪(5B-6C型)测定。亚铁离子用邻菲罗啉分光光度法测定。微生物菌群形貌用扫描电镜(S-3400N型)观察。
-
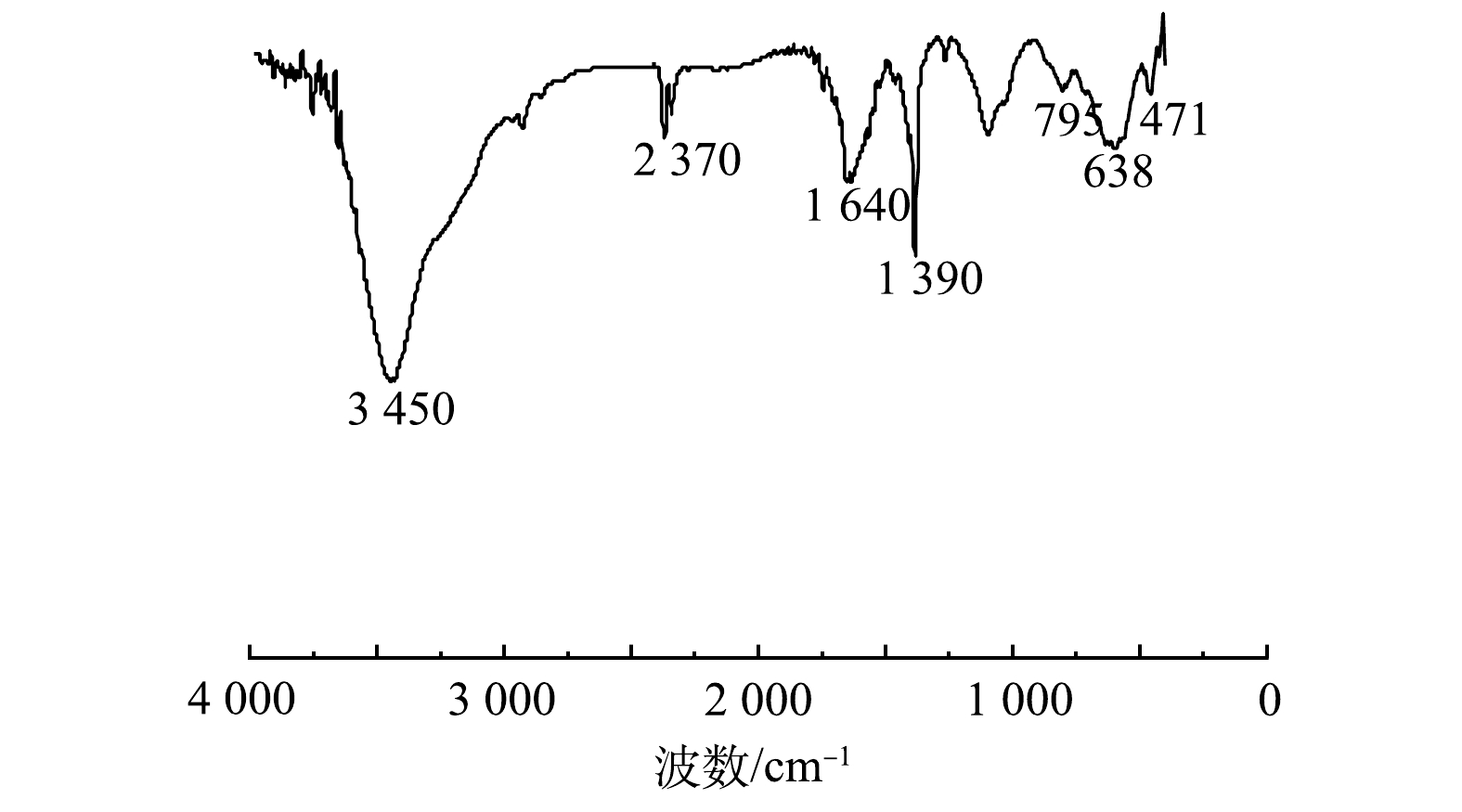
1)红外光谱(IR)分析。图2显示了FE/FEO材料除零价铁外其他成分的红外光谱图。由图可知,在3 450 cm−1出现了-OH的伸缩振动吸收峰,在1 640和1 390 cm−1处分别出现了H-O-H的变形振动吸收峰。这2处峰表明FE/FEO中含有结合水[25]。红外光谱图出现在638和795 cm−1的峰是α-FeOOH的特征吸收峰。这与徐轶群等[26]的研究结果一致。铁-氧键的特征吸收峰处于471 cm−1,是Fe2O3特征吸收峰[24]。由红外分析结果可知,FE/FEO中含有α-FeOOH、Fe2O3和结合水。
2)热重(TG)分析。通过对FE/FEO材料除零价铁外其他成分进行红外分析,发现其主要是由α-FeOOH和Fe2O3组成。由于Fe2O3具有稳定的化学性质,而在200~400 ℃的条件下,带有羟基的FeOOH会发生化学反应式(1)的反应,导致羟基断裂[27]。
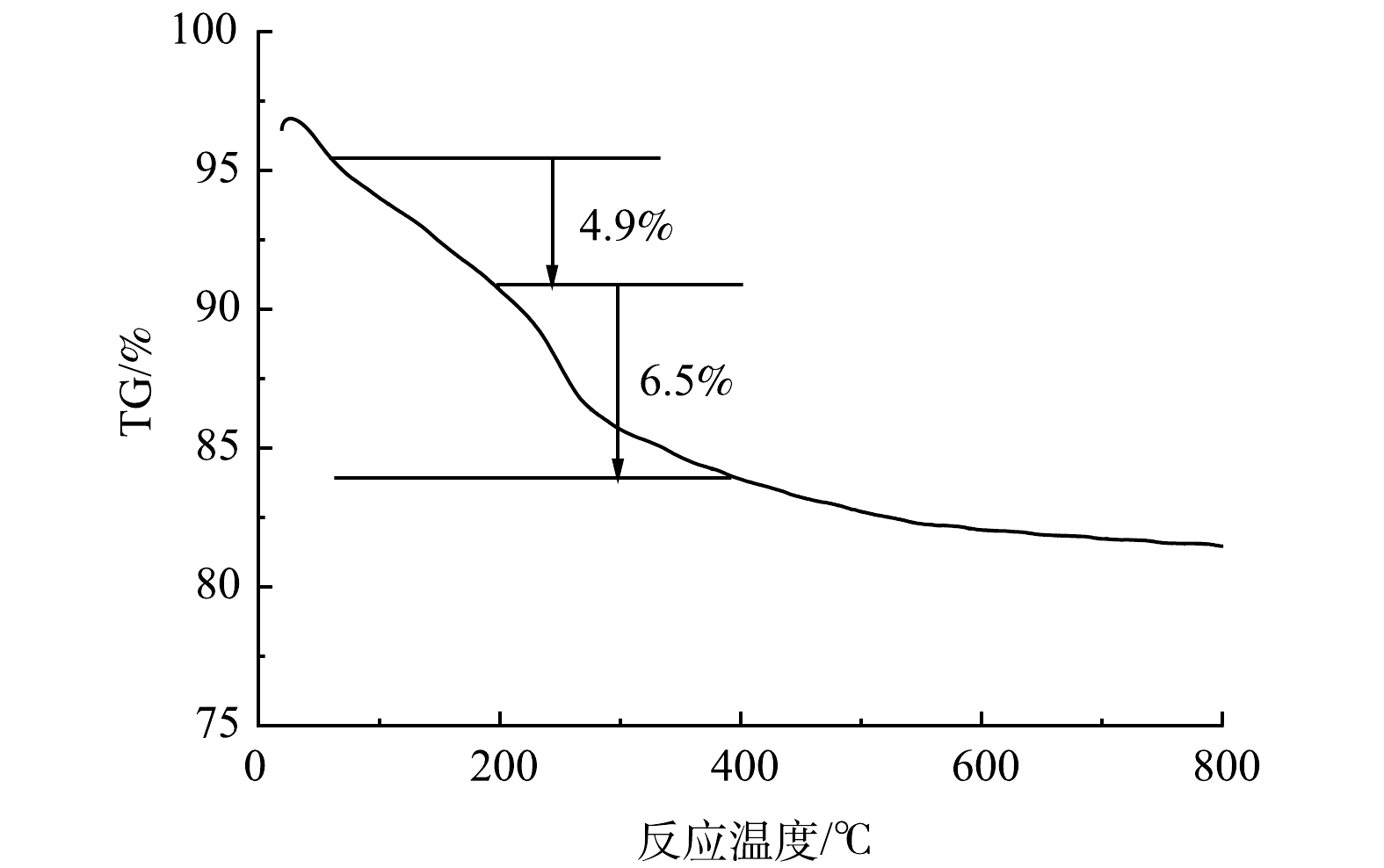
图3是FE/FEO材料除零价铁外其他成分的TG图。由图3可看出,曲线上有2段明显的重量损失。在80~200 ℃,FE/FEO样品的出现重量损失,此时,样品中的结合水随着温度的升高而脱去,样品质量损失了4.9%。在200~400 ℃,α-FeOOH因温度升高会发生式(1)的反应,导致羟基断裂脱去,从而导致样品质量再次损失,此时,样品质量损失了6.5%。
进行热重分析实验的样品总质量为8.80 mg,样品中的结合水脱去后质量损失了4.90%,可推算出结合水为0.43 mg。而根据FeOOH的化学反应式(1),此时损失的水分为0.57 mg。根据质量守恒定律,可计算出,α-FeOOH为5.63 mg,占63.97%。FE/FEO中的Fe2O3为2.74 mg,占31.13%。
铁是铁氧还原蛋白的重要组成成分,产氢的主要途径是丙酮酸脱羧产氢和辅酶Ⅰ的氧化与还原产氢[27],故产氢需要氢化酶中的电子载体铁氧还蛋白 (ferredoxin)的参与,可见铁对产氢过程的作用不可忽视。有研究表明,氢化酶的活性随着铁离子的损耗而降低[28]。
上述实验结果表明,投加了含零价铁、羟基铁和氧化铁组成的FE/FEO材料,能够提高混合菌群的产氢能力。与投加单一的Fe2+或Fe2+或零价铁的研究结果相比,FE/FEO材料能同时提供生物产氢过程所需的多价态铁,这些对发酵菌群产氢会起到促进作用。
3)FE/FEO电镜观察。如图4所示,FE/FEO材料呈现松散、蓬松的结构,由大量针状物错落堆积构成,导致各类大小不一的疏松小孔。从红外光谱和热重分析结果可知,FE/FEO中不仅有零价铁和氧化铁,还有63.9%的α-FeOOH。铁羟基氧化物微观即为褐色针状物,具有较大的比表面积,接近纳米级的零价铁ZVI的比表面积,一般生锈的单质铁中均存在。这是因铁表面在空气中被氧化腐蚀导致。这种疏松结构导致比表面积增加,提高了其吸附能力。而且,这种松散结构容易使铁表面形成大量微电池,引发腐蚀反应,并会向系统中缓慢释放氢气。同时,铁的外源电子在氢酶的中介作用下,将更多的质子转化为氢,从而推动整个还原平衡向产氢的方向发展[8],有利于氢气增产。
-
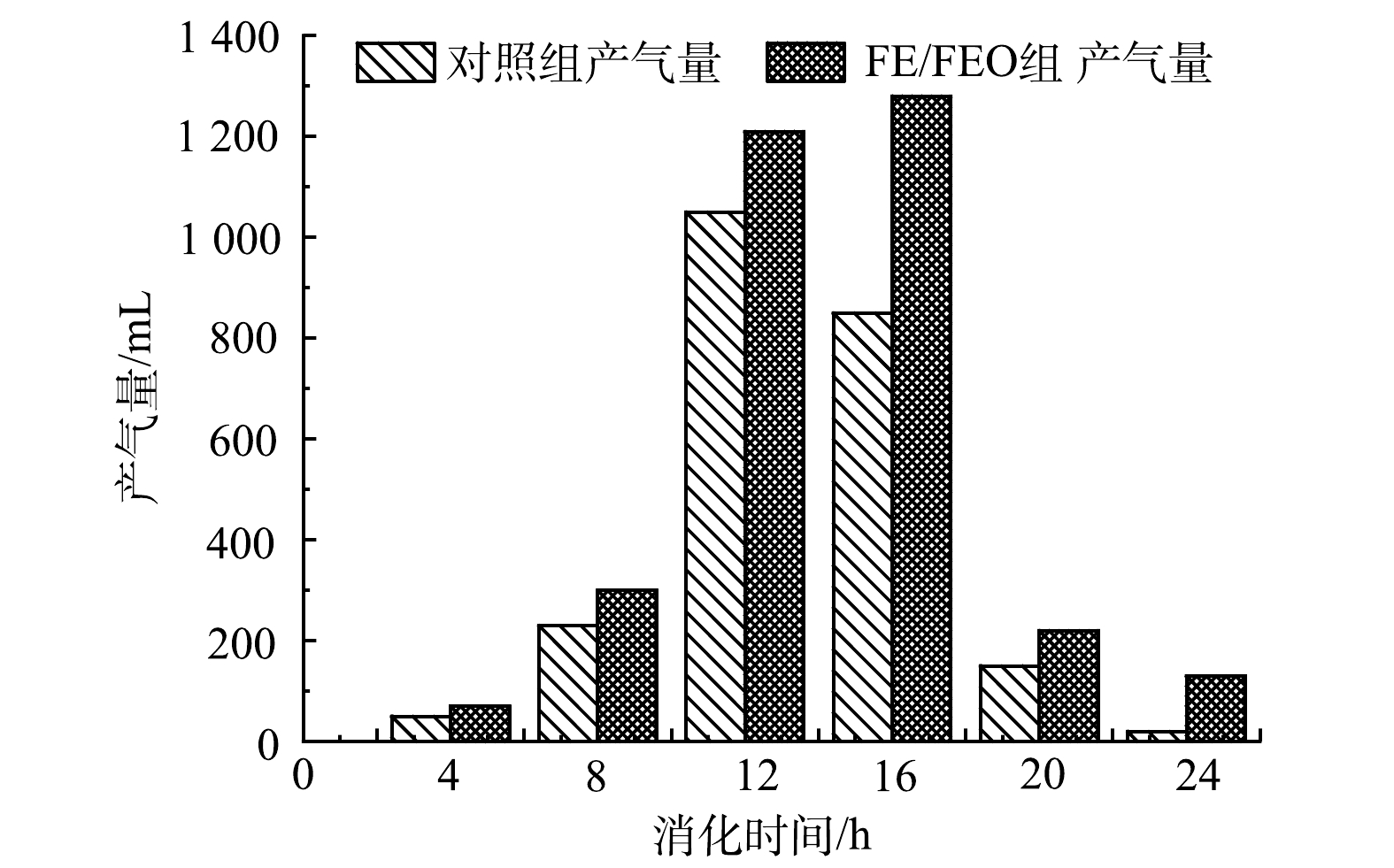
1) 总产气量。实验中考察了FE/FEO组厌氧发酵24 h的产气量,并与对照组进行了比较,其结果见图5。从图5可看出,两组均在厌氧反应的第12~16 h出现产气高峰。FE/FEO组最大值是在第12 h,而对照组是在第16 h。此时,FE/FEO组的产气量为1 280 mL,比对照组的产气量提高了22%。这表明,加入FE/FEO后有助于产气量的提高。在发酵前期,由于系统内的微生物在调整适应新环境,导致产气较少。在产气高峰后,VFA的产生速率远大于微生物对VFA的消耗速率,从而导致系统中出现酸累积现象[29](从第2.3节中可看出),抑制微生物的生长,从而产气量下降。
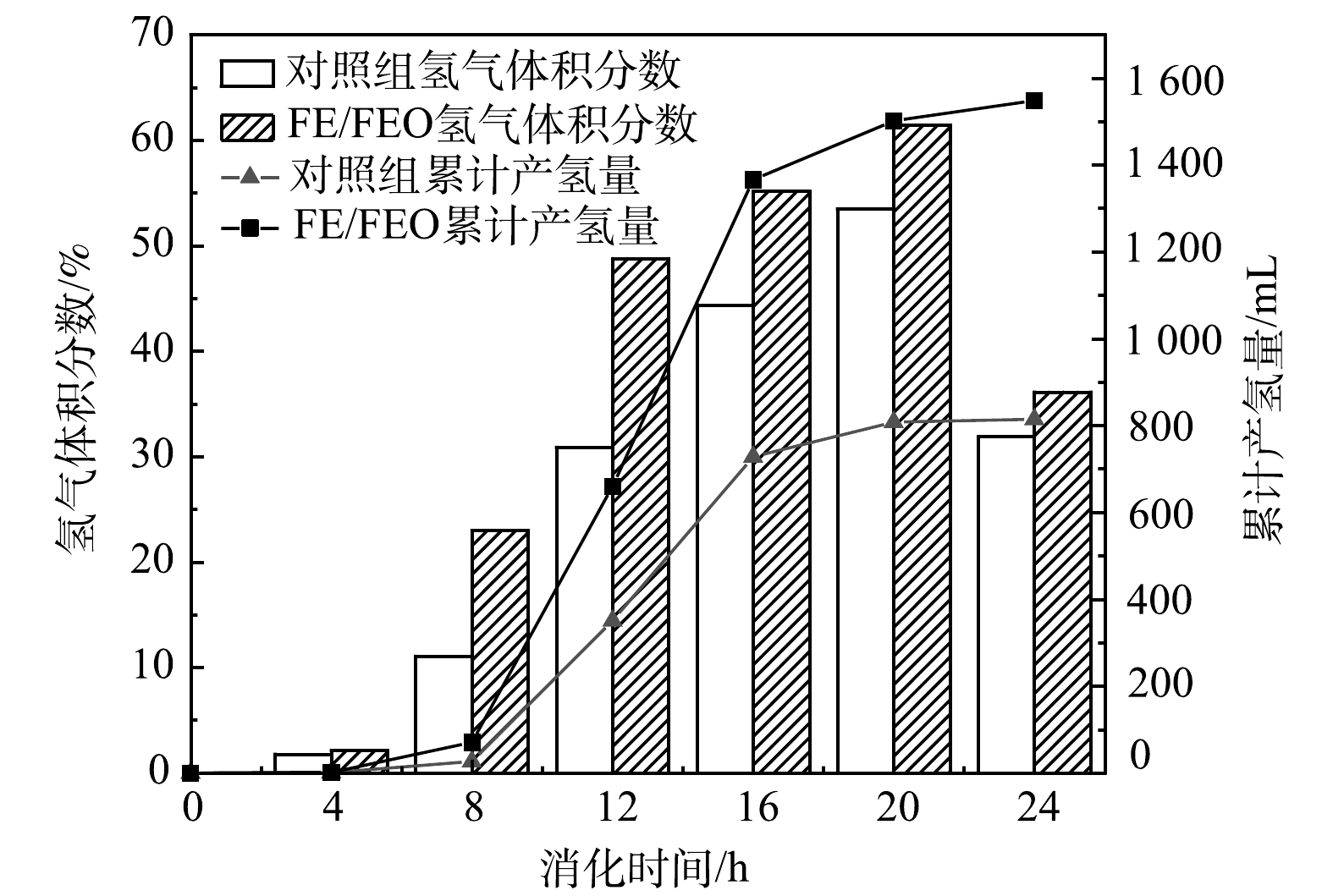
2) 产氢量。由图6可知,两组氢气体积分数均呈现先逐渐增加后下降趋势。第20 h时,两组的氢气体积分数均达到最大,此时,FE/FEO组的氢气体积分数为61.42%,较对照组提高了14.85%。从累积氢气产量看,FE/FEO组为1 548 mL,比对照组提高了56.32%。由图7可知,两组均在第16 h产氢率达到峰值,FE/FEO组的产氢率为22.67 L·kg−1(以1 kg挥发性有机固体VS计),比对照组增加了59.87%。相比在常温(pH=6.5)条件下对污泥进行厌氧发酵的产氢率6.88 mL·g−1[30],本实验结果高出了230%。因此,在55 ℃高温厌氧发酵条件下,FE/FEO材料在提高厌氧产氢和产气方面起到明显的促进作用。
-
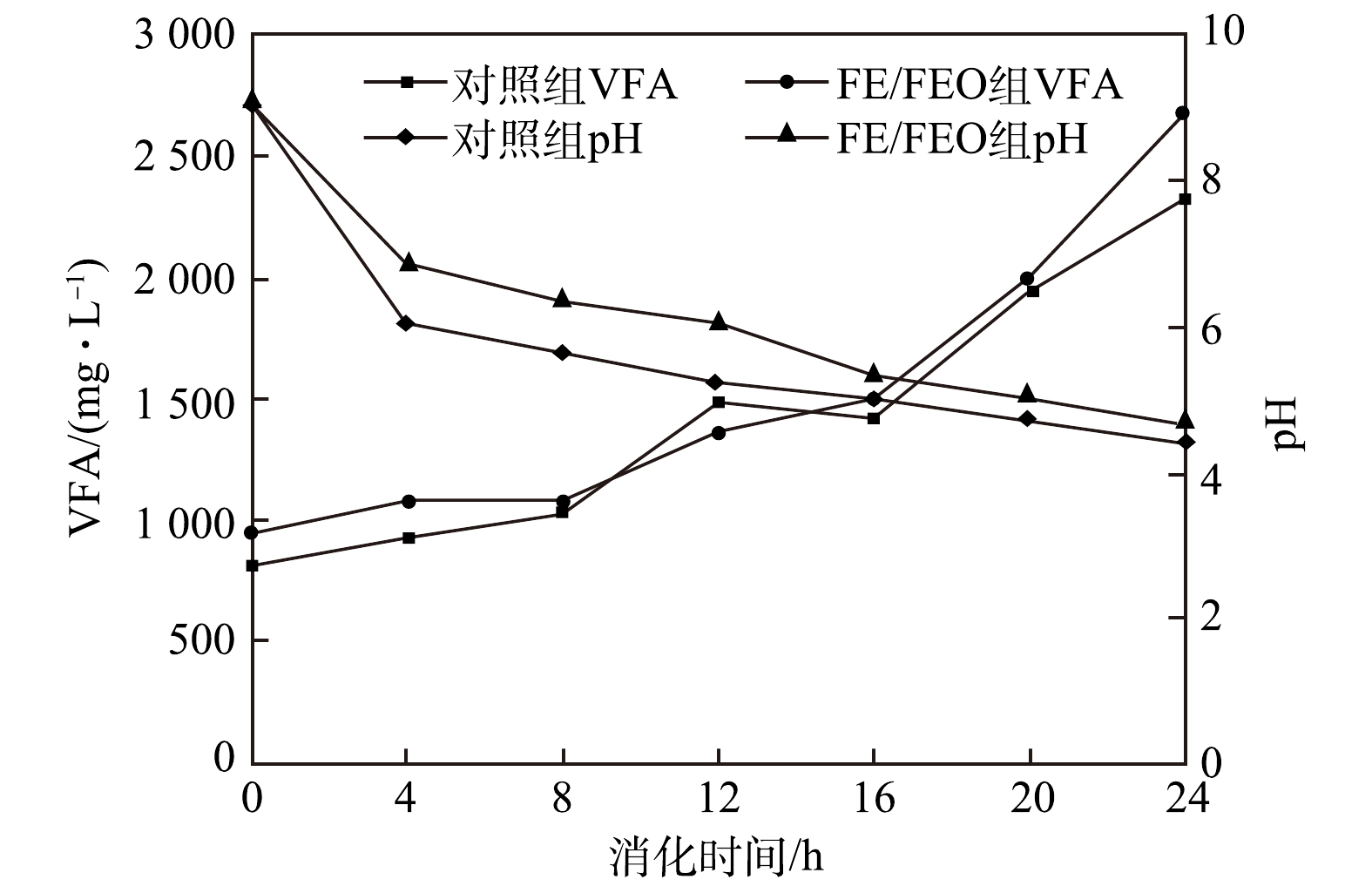
1) 挥发性有机酸(VFA)和pH。由图8可看出,两组反应器的VFA质量浓度随着消化时间逐渐增加。在第24 h,FE/FEO组的挥发性有机酸为2 675 mg·L−1,比对照组提高了16%,这表明复合铁材料FE/FEO能适当提高发酵液中的VFA产量。CAO等[31]发现,在添加零价铁的餐厨垃圾厌氧发酵系统中,第10天,VFAs的最大质量浓度增加到8 245 mg·L−1,比对照组有了显著提高。这是因为,铁是微生物所需的微量元素,可增强微生物代谢能力、提高有机物的降解率,从而也提高了有机酸产量[32]。此外,零价铁也能通过电化学腐蚀产氢[8],因此,复合FE/FEO通过增强厌氧细菌的活性来提高底物的基因代谢效率,从而提高厌氧细菌的产氢性能[8]。
由图8还可看出,随着厌氧消化时间的延长,两组反应器的pH呈逐渐下降趋势。至第24 h,FE/FEO组和对照组pH分别降低到了4.4和4.3。这主要是由于系统中挥发性有机酸的产酸速率快而导致的积累,从而使得pH下降。与对照组相比,FE/FEO组的pH相对较高。这是因为,外加铁元素会在酸性条件下与水发生反应,同时会发生副反应,产生羟基离子,从而提高溶液的总碱度[33]。有研究者[8]发现,厌氧系统中维持pH呈适当酸性状态有利于厌氧产氢。一般乙酸和丁酸的产生与产氢有关,保持有利的产乙酸和产丁酸的环境条件,可促进厌氧发酵产氢。由以上结果可知,FE/FEO的添加能促进厌氧产酸,并导致pH不同程度的下降。与空白相比,FE/FEO组的氢气产量有所增加。
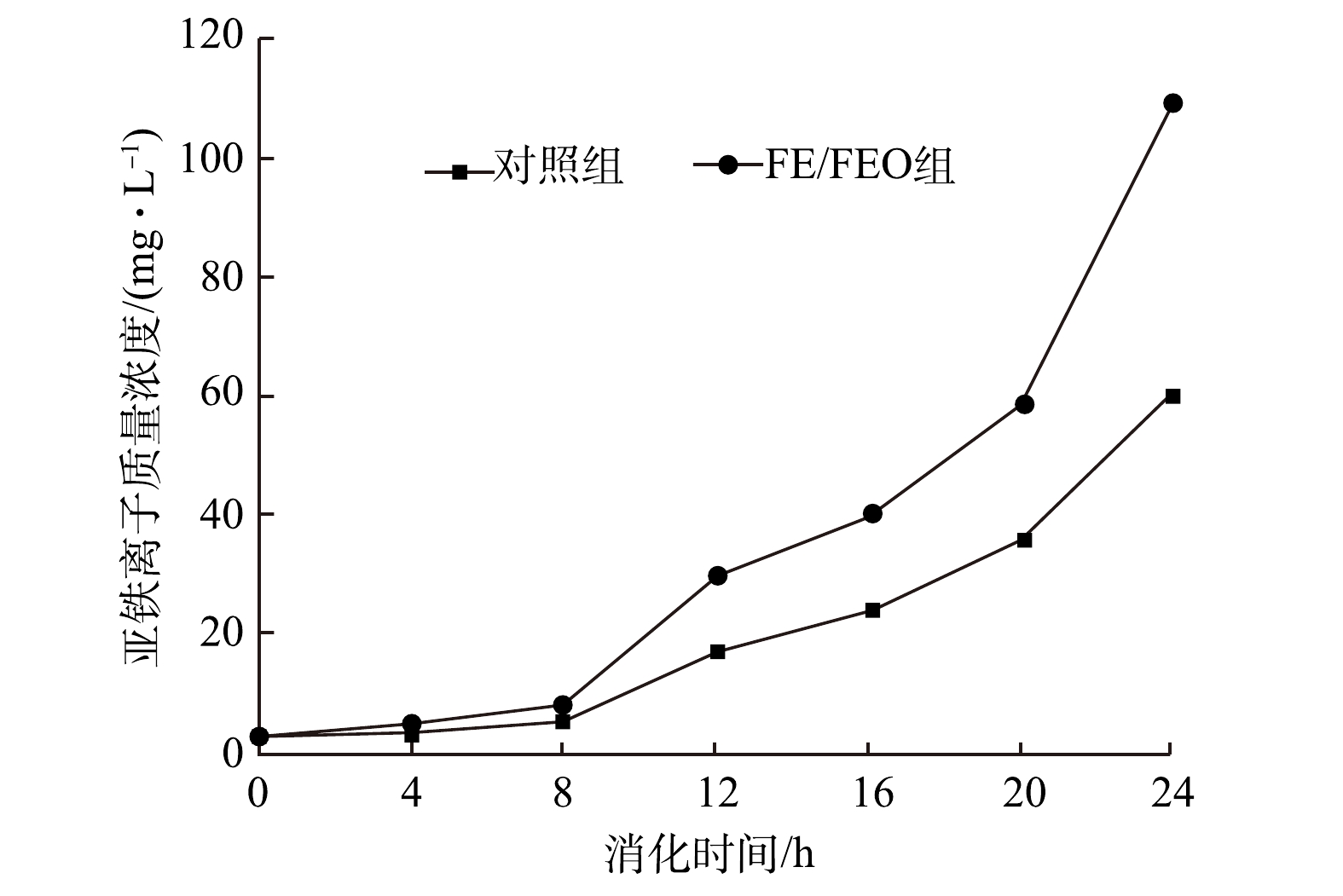
2) 亚铁离子质量浓度。由图9可知,在反应的前8 h,两组反应器的发酵液中亚铁离子无明显变化;从第10 h开始,发酵液中亚铁离子明显增加。相比对照组,FE/FEO组明显提高了发酵液中亚铁离子质量浓度,反应结束时,亚铁离子质量浓度为109.75 mg·L−1,是对照组的1.82倍。这表明,加入的FE/FEO粉末能在厌氧体系中发生相关反应,从而提高厌氧体系中亚铁离子质量浓度,对厌氧发酵产生作用。有研究表明,投加Fe和Fe2+后,都能不同程度提高产氢量和最大比产氢速率[34],但过多投加Fe2+(质量浓度高于200 mg·L−1时),则产氢量随投加Fe2+质量浓度的增加而有减小趋势。这表明,投加Fe2+虽然容易直接被利用,但投加量不宜过多。在本实验中,FE/FEO为铁的复合材料,呈现松散多孔状,不同于直接投加Fe2+,FE/FEO中有效铁元素成分可在厌氧反应过程中逐渐释放。而且,反应结束后可回收利用。本实验结果表明,20 g·L−1的投加量未对系统产生不利影响。
3) 厌氧系统内微生物菌群形貌。从图10中可看出,FE/FEO组(图10(b)和图10(C))的微生物比对照组(图10(a))丰富,显示大量不同菌种的细菌存在于污泥中。图中呈现了球菌、杆菌、弧状菌和丝状菌等;3张图中均观察到杆菌,大小约为1~5 μm。这些细菌都有较完整的形态结构,表面较光滑,菌群数量丰富,菌种之间空隙很小,互相结合紧密。除了微生物外,在图10(c)中,还可观察到FE/FEO组中具有其它物质,如胞外多聚物(EPS)、有机物和无机盐等。在对照组中,大块颗粒物相对较多,且比较紧实,而FE/FEO组不仅体现丝状菌群,还展现了较多絮状松散结构物质;铁羟基氧化物α-FeOOH其多孔性会导致污泥絮体的松散,其与细菌互相交联、包裹,能够提供骨架支撑作用[35],从而可促进微生物与环境中营养物质的良好接触,对其生长代谢起促进作用。
-
1)FE/FEO组的产气峰值、氢气体积分数和产氢率均高于对照组。这表明FE/FEO材料在提高厌氧产氢率和产气量方面能起到明显的促进作用。
2)在厌氧发酵产氢阶段,FE/FEO组的挥发性有机酸质量浓度和亚铁离子质量浓度均比对照组有所增加。这表明FE/FEO能适当提高发酵液有机酸产量并维持系统的总碱度。
3) FE/FEO主要由α-FeOOH(63.9%)和Fe2O3(31.2%)组成,呈现松散、蓬松结构,具有较大的比表面积和吸附能力,其多孔性会导致污泥絮体变得松散,为微生物提供良好的骨架支撑作用,并促进其生长代谢。
复合铁添加物对混合有机固废厌氧产氢的影响
Effects of iron filings additives on anaerobic hydrogen production from mixed organic solid wastes
-
摘要: 将城镇污水处理厂的城市污泥与餐厨垃圾混合后,经厌氧消化处理后可产生能源气体氢气,从而达到资源化利用的目的。废铁屑是机械加工厂的固体废弃物,将其处理后可得到一种新型复合铁材料(FE/FEO)。将城市污泥和餐厨垃圾预处理后按体积比1∶1比例混合,分别等分放入2个反应器中,一个投加FE/FEO粉末作为为FE/FEO组,另一个不加FE/FEO作为对照组,考察了FE/FEO对上述混合有机固废厌氧产氢的影响。结果表明,在厌氧反应的24 h内,FE/FEO组的最大氢气体积分数为61.4%,比不加FE/FEO的对照组增加了15%;FE/FEO组的累积产氢率和最大产氢率分别为49.0和22.7 L·kg−1(以1 kg挥发性有机固体所能产生的氢气体积计),比对照组分别增加了56 %和59%。FE/FEO组的亚铁离子质量浓度在第24 h达到最大,即109.8 mg·L−1。FE/FEO组产生的挥发性有机酸为2 675 mg·L−1,比对照组提高了15%。FE/FEO粉末中不仅含有零价铁、氧化亚铁,还有针孔状α-FeOOH,其结构松散、比表面积大,可对厌氧发酵系统中的微生物菌群起到支撑骨架作用。本研究结果可为提高有机固废厌氧发酵产氢效率提供参考。Abstract: Mixed wastes of municipal sludge from urban wastewater treatment plant (WWTPs) and kitchen waste from catering industry could be utilized to produce biomass energy gas hydrogen by anaerobic digestion process. Iron scraps, solid waste from mechanical processing plants, was treated to iron-containing FE/FEO powder in this paper. After pretreatment, mixing municipal sludge mixed with the same amount of kitchen waste (by the ratio of 1∶1), and then equally divided into two reactors. FE/FEO material was added to one of the anaerobic reactors as FE/FEO group while the other one without FE/FEO as the control group. The effect of FE/FEO on the rate of yield hydrogen by anaerobic fermentation process for the mixed organic solid waste was investigated. The results showed that the maximum hydrogen volume fraction of FE/FEO group was 61.4%, which was 15% higher than that of the control group, while cumulative hydrogen yield and the maximum yield of daily hydrogen of FE/FEO group were 49. 0 and 22.7 L·kg−1 (based on the volume of hydrogen produced by 1 kg volatile organic solid) within 24 hours, respectively, which were 56% and 59% higher that of the control group, respectively. The content of Fe2+ in the FE/FEO group reached a maximum value of 109.8 mg·L−1 at the 24th hour; while the content of volatile organic acid by 2 675 mg·L−1 was 15% higher than that of the control group during 24 h. It is found that FE/FEO powder not only contains elemental Fe and ferrous oxide, but also pinhole α-FeOOH, which increases the specific surface area and plays an important role as the loose structure frame of the microbes in the anaerobic system. Therefore, the addition of FE/FEO plays a promoting role in hydrogen production by anaerobic fermentation process. The study can provide a reference for improving the hydrogen production by anaerobic fermentation process for organic solid wastes.
-
Key words:
- iron scraps /
- anaerobic digestion /
- production of hydrogen /
- municipal sludge /
- food waste
-

-
表 1 混合有机固废及其物料的理化指标
Table 1. Physical and chemical indexes of each material
供试材料 pH 含固率/% VS/(g·L−1) TS/(g·L−1) 餐厨垃圾 6.03 22.97 219.10 228.00 城市污泥 11.45 3.05 23.91 32.75 混合有机固废 9.06 4.34 31.57 39.36 -
[1] WANG Y, ZANG B, LI G, et al. Evaluation the anaerobic hydrolysis acidification stage of kitchen waste by pH regulation[J]. Waste Management, 2016, 53(7): 62-67. [2] LI J, LI C, ZHAO L, et al. The application status, development and future trend of nano-iron materials in anaerobic digestion system[J]. Chemosphere, 2021, 269: 129389-129403. doi: 10.1016/j.chemosphere.2020.129389 [3] GIROTTO F, ALIBARDI L, COSSU R. Food waste generation and industrial uses: A review[J]. Waste Management, 2015, 45: 32-41. doi: 10.1016/j.wasman.2015.06.008 [4] 戴晓虎, 张辰, 章林伟, 等. 碳中和背景下污泥处理处置与资源化发展方向思考[J]. 给水排水, 2021, 57(3): 1-5. [5] ANBAZHAGAN S, CHELLIAH A, GALAVILA R T, et al. Enhancing hydrogen production through anaerobic co-digestion of fruit waste with biosolids[J]. Journal of Environmental Science and Health, Part A, 2019, 54(6): 553-559. [6] 傅木星, 张砺彦, 苏泱洲, 等. 不同预处理方法对剩余污泥厌氧发酵产氢的影响[J]. 安全与环境学报, 2015, 15(1): 273-276. [7] 潘维, 莫创荣, 李小明, 等. 外加淀粉酶预处理污泥厌氧发酵产氢研究[J]. 环境科学学报, 2011, 31(4): 785-790. [8] ZHU H, SETO P, PARKER W J. Enhanced dark fermentative hydrogen production under the effect of zero-valent iron shavings[J]. International Journal of Hydrogen Energy, 2014, 39(33): 19331-19336. doi: 10.1016/j.ijhydene.2014.06.055 [9] HWANG Y, SIVAGURUNATHAN P, LEE M, et al. Enhanced hydrogen fermentation by zero valent iron addition[J]. International Journal of Hydrogen Energy, 2019, 44(6): 3387-3394. doi: 10.1016/j.ijhydene.2018.06.015 [10] HONETSCHLAGEROVA L, LUCIANO V, MARTINEC M, et al. Interactions of nanoscale zero valent iron and iron reducing bacteria in remediation of trichloroethene[J]. International Biodeterioration & Biodegradation, 2018, 127: 241-246. [11] FENG Y, ZHANG Y, QUAN X, et al. Enhanced anaerobic digestion of waste activated sludge digestion by the addition of zero valent iron[J]. Water Research, 2014, 52: 242-250. doi: 10.1016/j.watres.2013.10.072 [12] BAEK G, KIM J, CHO K, et al. The biostimulation of anaerobic digestion with (semi)conductive ferric oxides: Their potential for enhanced biomethanation[J]. Applied Microbiology and Biotechnology, 2015, 99(23): 10355-10366. doi: 10.1007/s00253-015-6900-y [13] YU B, ZHANG D, SHAN A, et al. Methane-rich biogas production from waste-activated sludge with the addition of ferric chloride under a thermophilic anaerobic digestion system[J]. RSC Advances, 2015, 5(48): 38538-38546. doi: 10.1039/C5RA02362A [14] BAEK G, KIM J, LEE C. Influence of ferric oxyhydroxide addition on biomethanation of waste activated sludge in a continuous reactor[J]. Bioresource Technology, 2014, 166: 596-601. doi: 10.1016/j.biortech.2014.05.052 [15] ZHAO Z, ZHANG Y, WOODARD T L, et al. Enhancing syntrophic metabolism in up-flow anaerobic sludge blanket reactors with conductive carbon materials[J]. Bioresource Technology, 2015, 191: 140-145. doi: 10.1016/j.biortech.2015.05.007 [16] ZHU L, GAO K, JIN J, et al. Analysis of ZVI corrosion products and their functions in the combined ZVI and anaerobic sludge system[J]. Environmental Science and Pollution Research International, 2014, 21(22): 12747-12756. [17] ZHOU J, YOU X, NIU B, et al. Enhancement of methanogenic activity in anaerobic digestion of high solids sludge by nano zero-valent iron[J]. Science of the Total Environment, 2020, 703: 135532-135542. doi: 10.1016/j.scitotenv.2019.135532 [18] FAISAL S, SALAMA E, MALIK K, et al. Anaerobic digestion of cabbage and cauliflower biowaste: Impact of iron oxide nanoparticles (IONPs) on biomethane and microbial communities alteration[J]. Bioresource Technology Reports, 2020, 12: 100567-100595. doi: 10.1016/j.biteb.2020.100567 [19] ENGLIMAN N S, ABDUL P M, WU S, et al. Influence of iron (II) oxide nanoparticle on biohydrogen production in thermophilic mixed fermentation[J]. International Journal of Hydrogen Energy, 2017, 42(45): 27482-27493. doi: 10.1016/j.ijhydene.2017.05.224 [20] 朱铖, 程洁红. 铁刨花投量对餐厨垃圾和污泥协同厌氧消化的影响[J]. 中国给水排水, 2018, 34(23): 8-13. [21] CHENG J H, ZHU C, ZHU J, et al. Effects of waste rusted iron shavings on enhancing anaerobic digestion of food wastes and municipal sludge[J]. Journal of Cleaner Production, 2020, 242: 118195-118205. doi: 10.1016/j.jclepro.2019.118195 [22] 经雪, 程洁红, 孔峰, 等. 外加铁对城市污泥厌氧消化产甲烷的作用[J]. 环境工程, 2021, 39(2): 125-130. [23] 付志敏, 陶兰兰, 徐静, 等. 中温碱解预处理促进剩余污泥厌氧产甲烷的研究[J]. 环境工程, 2016, 34(1): 91-95. [24] 王华, 卢培利, 艾海男, 等. 挥发性脂肪酸的滴定测量方法进展[J]. 环境科学与技术, 2008, 31(2): 47-50. doi: 10.3969/j.issn.1003-6504.2008.02.013 [25] 白沙沙, 王欢, 陈玉静, 等. 消除溶剂水吸收峰干扰的红外光谱测量新方法[J]. 光谱学与光谱分析, 2015, 35(4): 894-898. doi: 10.3964/j.issn.1000-0593(2015)04-0894-05 [26] 徐轶群, 杨明, 何成达, 等. 铁的氢氧化合物稳定相α, β-FeOOH的表征及光谱分析[J]. 光谱学与光谱分析, 2013, 33(12): 3330-3333. doi: 10.3964/j.issn.1000-0593(2013)12-3330-04 [27] 任南琪, 王宝贞, 李建政. 有机废水发酵法生物制氢技术中试研究[M]. 哈尔滨: 黑龙江科学技术出版社, 2006. [28] JUNELLES A, JANATI-IDRISSI R, PETITDEMANGE H, et al. Iron effect on acetone-butanol fermentation[J]. Current Microbiology, 1988, 17(5): 299-303. doi: 10.1007/BF01571332 [29] REN N Q, CHUA H, CHAN S Y, et al. Assessing optimal fermentation type for bio-hydrogen production in continuous-flow acidogenic reactors[J]. Bioresource Technology, 2007, 98(9): 1774-1780. doi: 10.1016/j.biortech.2006.07.026 [30] 代东梁, 韩相奎, 李广, 等. 污泥厌氧发酵产氢产酸的影响因素分析[J]. 中国给水排水, 2014, 30(15): 11-13. [31] CAO J, ZHANG Q, WU S, et al. Enhancing the anaerobic bioconversion of complex organics in food wastes for volatile fatty acids production by zero-valent iron and persulfate stimulation[J]. Science of the Total Environment, 2019, 669: 540-546. doi: 10.1016/j.scitotenv.2019.03.136 [32] HU Y, HAO X, ZHAO D, et al. Enhancing the CH4 yield of anaerobic digestion via endogenous CO2 fixation by exogenous H2[J]. Chemosphere, 2015, 140: 34-39. doi: 10.1016/j.chemosphere.2014.10.022 [33] YUHOON H, PERIYASAMY S, MO-KWON L, et al. Enhanced hydrogen fermentation by zero valent iron addition[J]. International Journal of Hydrogen Energy, 2018, 44(6): 3387-3394. [34] 丁杰, 任南琪, 刘敏, 等. Fe和Fe2+对混合细菌产氢发酵的影响[J]. 环境科学, 2004, 25(4): 48-53. doi: 10.3321/j.issn:0250-3301.2004.04.010 [35] DEEPAK K P, GAJENDRA K P, PARIDA K M, et al. Facile fabrication of Gd(OH)3 nanorod/RGO composite: Synthesis, characterisation and photocatalytic reduction of Cr(VI)[J]. Chemical Engineering Journal, 2014, 255: 77-78. -



 下载:
下载: