-
有机污染土壤因其对生态环境和人类健康的危害一直是国内外关注的热点。化学氧化作为一种修复效率高、修复周期短、修复成本低的技术[1],常用于修复有机污染土壤。其中,基于过硫酸盐 (persulfate,PS) 的化学氧化技术具有氧化效率高、化学性质稳定、反应条件温和等优点[2],被广泛用于有机污染土壤的氧化修复。PS通过催化可以产生具有强氧化性的自由基,如硫酸根自由基 (SO4−·) 、羟基自由基 (·OH) 以及超氧自由基 (·O2−) [3]。其中,SO4−·的氧化还原电位高 (2.6~3.1 V) ,且半衰期 (t1/2=30~40 μs) 比·OH更长 (t1/2≤ 1 μs) [4],使其更易与有机污染物接触反应。催化PS还能够生成非自由基物种,如单线态氧 (1O2) [5]。此外,PS还能够通过电子转移直接降解有机污染物[6]。PS的活化方法可分为两大类:均相活化 (如热活化、碱活化、过渡金属离子活化等[7-9]) 和非均相活化 (如三氧化二铁、钴氧化铁等) 。然而,均相活化在实际应用中通常具有局限性 (需要额外持续提供能量、pH工作区间窄等[10]) ,因此,研发高效、低成本的非均相催化剂是目前基于PS化学氧化技术的研究重点和热点。
生物质 (如:玉米秸秆、稻壳、厨余垃圾等) 热解生成的生物炭 (biochar,BC) ,是一种新兴的PS非均相催化材料,具有原料来源广泛、催化效果好、制备工艺简单及环境友好等优点[11]。生物炭含有许多含氧基团 (如羧基、羟基等) ,有研究表明,这些含氧基团有助于生物炭催化PS生成自由基降解有机污染物[12]。然而,仅通过生物质热解产生的生物炭,对PS的催化效果并不尽如人意。研究发现,将过渡金属 (如:Fe(Ⅱ)、Mn(Ⅱ)、Cu(Ⅱ)等) 负载在生物炭上,不仅能大幅提高生物炭对PS的催化能力,还能减少金属离子的浸出[13]。LI等[10]通过制备FeMn@BC催化PS降解土壤中的噻虫啉,结果表明,FeMn@BC通过自由基途径对噻虫啉的去除率为92.5%,且土壤中微生物的酶活性也有所提高。ZHAO等[14]制备了CuFeO@Biochar用于催化PS降解土壤中的邻硝基氯苯,发现超氧自由基 (·O2−) 能够促进Cu(I)/Cu(Ⅱ)和Fe(Ⅱ)/Fe(Ⅲ)循环,从而激活PS生成SO4−·和·OH降解邻硝基氯苯。然而,过渡金属基生物炭在应用中仍存在以下问题:1) 过渡金属 (如:Mn、Cu等) 不可避免地会进入土壤,过渡金属在土壤中积累到一定浓度会对动植物和人类健康造成危害;2) 过渡金属基生物炭的催化效率易受环境因素影响,如在碱性土壤中使用铁基催化剂会使铁物种沉淀,进而导致生物炭的催化活性降低[15]。上述问题使过渡金属基生物炭在实际应用中受到限制,因此,研发一种高效、环境友好型的金属-生物炭复合催化剂活化过硫酸盐修复有机污染土壤具有重要意义。
综上所述,本研究将富含K+、Mg2+的天然矿物光卤石 (carnallite,CA) 负载在生物炭上制备复合催化剂CA-CS。光卤石本身无法有效活化过硫酸盐,将其负载在生物炭上是提高生物炭催化性能的关键。在土柱实验中,以具有高毒性、强挥发性和低生物降解性的苯酚作为污染物,以CA-CS作为催化剂高效催化氧化剂PS修复苯酚污染土壤。还探究了CA-CS添加量、PS浓度、反应时间对土柱中苯酚降解效果的影响,以及CA-CS催化PS对土壤理化性质的影响。此外,还对CA-CS催化PS降解土壤中苯酚的机理进行了探究。
-
1) 实验原料。玉米秸秆取自天津市边某农村地区,光卤石购自兰州市某地,实验过程中所用水均为去离子水 (电阻率≥18.2 MΩ·cm) ,玉米秸秆热解所用N2和CO2纯度均为99.9%,实验所用药品有过硫酸钠 (Na2S2O8) 、苯酚 (C6H6O) 、甲醇 (CH3OH) 、L-组氨酸 (C6H9N3O2) 、碘化钾 (KI) 、碳酸氢钠 (NaHCO3) ,均为分析纯;甲醇 (CH3OH) 为色谱级。
2) 供试土壤。供试土壤取自天津市某地,采集深度为20~30 cm,去除石块、动植物残体与杂物后,将土壤置于冻干机中真空风干、研磨、过60目筛保存待用。以苯酚作为污染物,将200 mg苯酚溶于0.8 L甲醇中,其浓度为250 mg·L−1。将苯酚溶液加入到1 kg上述空白土壤中 (液固比为1∶0.6,w/v) ,将其放置在室温下每小时手动搅拌,持续12 h,使苯酚分散均匀。之后将染毒土壤置于通风橱中使甲醇完全挥发,收集土壤样品并在4 ℃下储存,土壤中苯酚的理论浓度为200 mg·kg−1。在不同位置取样测定染毒土壤中苯酚的平均浓度为170 mg·kg−1。土壤理化性质如表1所示。
-
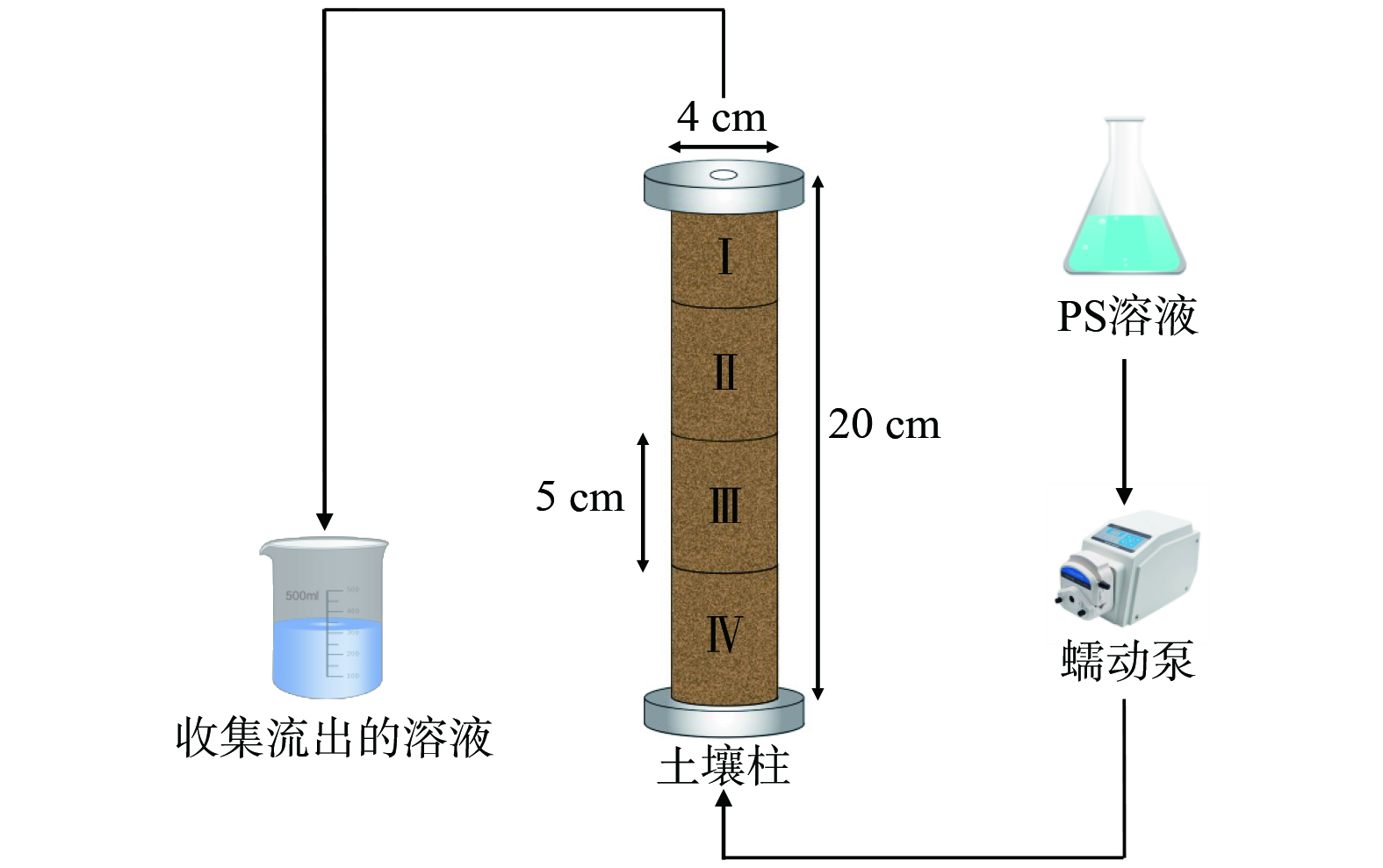
1) 实验装置。定制内径为4 cm,高20 cm的亚克力柱,每5 cm处分段便于取样,从上到下依次为分段Ⅰ、分段Ⅱ、分段Ⅲ、分段Ⅳ。用蠕动泵从柱子下端注入PS溶液,从最上端收集流出的溶液。土柱实验能够更好地模拟修复有机污染土壤,并为实际工程应用提供更准确的数据,例如污染物的迁移和分布、土质变化以及实际应用中的参数条件。实验装置示意图如图1所示。
2) CA-CS制备。将玉米秸秆 (corn stalk,CS) 清洗风干后,于烘箱中105 ℃干燥,再用粉碎机粉碎并过80目筛备用。将光卤石和玉米秸秆按1∶9的质量比加入100 mL去离子水中,于室温下搅拌6 h,之后转移到烘箱中105 ℃烘至水分完全蒸发。将混合物料置于管式炉中程序升温热解,先将热解气氛设为N2,以10 ℃·min−1升温至800 ℃,然后切换热解气氛为CO2在800 ℃下保持1 h,最后在N2气氛下冷却至室温。其中,N2与CO2流量均为100 mL·min−1。所得生物炭材料记为CA-CS,研磨过100目筛备用。制备未掺杂光卤石的生物炭材料作为对照,制备条件同上,记为BC。
3) 土壤渗透性测定。将亚克力柱组装好并保持竖直状态,并在柱子底部装入足量的石英砂防止土流失,向柱子中加入200 g苯酚污染土壤并将其夯实,经测试装填深度为13.5 cm。将10 mmoL·L−1的PS溶液加入柱子中,使液面高度达到5 cm,之后持续将置于天平上的PS溶液加入土柱中,使液体深度始终保持5 cm,按一定的时间间隔读取剩余液体质量,计算每分钟向土柱中加入的液体质量,由此计算出渗透系数k。采用公式(1)进行计算。
式中:m为每分钟加入的液体的质量 (g·min−1) ,ρ为加入液体的密度 (g·cm−3) ,s为亚克力柱内部的横截面积 (cm2) 。经测定,PS溶液在苯酚污染土壤中的渗透系数为1.64×10−4 cm·s−1,属于低渗透性土壤 (图1) 。
4) 土柱实验。将不同质量的CA-CS与300 g苯酚污染土壤混合均匀待用。将苯酚污染土壤加入亚克力柱中,在柱子上下层铺设2 cm石英砂,以保证水流的均匀分布,防止土流失。用蠕动泵从最柱子最下端注入PS溶液,液体流速为1 mL·min−1,从最上端收集流出的PS溶液,于3、4、8、12、24 h取样测定出水中苯酚含量。反应结束后将土壤分段,土样冷冻干燥后提取测定每段中剩余苯酚含量。选用无水甲醇提取土壤中的苯酚,在100 mL锥形瓶中将甲醇与苯酚污染土壤混合 (液固比为6∶1,v/w) ,以封口膜封口,用恒温振荡器25 ℃震荡15 min,速率为200 r·min−1,过0.22 μm有机滤膜待测。其中,计算公式如式(2)、(3)、(4)所示。
-
选用高效液相色谱仪 (Agilent
1260 Ⅱ,美国安捷伦科技有限公司) 测定苯酚浓度,色谱柱型号为C18柱 (4.6 mm×150 mm,4 μm) 。苯酚测试条件:进样量10 μL,流动相为甲醇∶水=60∶40,流速为0.3 mL·min−1,柱温保持在40 ℃,检测器为紫外可见吸收检测器,检测波长270 nm。选用激光粒度仪 (Mastersizer 2000,英国马尔文公司) 对土壤粒径进行测试。具体的过程包括:开机预热15~20 min,开启气体系统,设置sop测试程序,在样品池中添加样品,运行sop测试程序进行测试。sop程序已经预先设置了测试条件 (如折射率、测试时间等) 。测试结束后,获得土壤样品在0.01~1 000 μm范围内不同子区间的体积百分比。
选用分光光度计 (UV-1801,北京市北分瑞利分析仪器公司) 测定反应过程中PS溶液的浓度变化。取1 mL待测液,加入1 mL A液 (5 g·L−1的NaHCO3溶液) 和1 mL B液 (100 g·L−1的KI溶液) ,再向其中加入2 mL去离子水定容至5 mL待测,检测波长为400 nm。
选用扫描电子显微镜 (JSM-7610F,日本电子株式会社公司) 对生物炭材料及土壤形貌进行分析。测试电压为3.0 kV,样品在表征之前喷金处理60 s,再进行检测。
选用总有机碳分析仪 (Shimadzu TOC-L,岛津企业管理 (中国) 有限公司) 对土壤中总有机碳含量进行测定。
选用X射线光电子能谱仪 (K-Alpha,美国Thermo Scientific公司) 对生物炭材料及土壤中元素进行分析。取适量样品压片后,贴于样品盘上,将样品放进样品室中,在样品室的压力小于2.0×10−7 mbar时,将样品送入分析室,光斑大小为400 μm,工作电压12 kV,灯丝电流6 mA;全谱扫描通能为150 eV,步长1 eV;窄谱扫描通能为50 eV,步长0.1 eV。
选用ANSYS Workbench 2 021软件对土壤柱中PS溶液的迁移进行仿真模拟,研究PS溶液在土柱中的压力变化。选用Space Claim构建物理模型,模型与反应装置几何相似。用Meshing对模型进行网格处理,并对进出口以及壁面命名。设置流体温度T =25 ℃,湍流强度I =1,实际速度v =0.1 m·s−1。以速度-入口、压力-出口作为边界条件,选择VOF两相流模型和标准k-epsilon湍流模型模拟PS溶液与空气在土壤柱中的混合流动过程,基于连续性方程和N-S方程建立了流动模型。
-
1) SEM结果分析。SEM图像直观地显示了新型CA-CS复合催化剂的形貌变化,结果如图2所示。观察图2(a)可知,BC的表面光滑平整,孔隙结构较少。在BC上负载光卤石后 (图2(b)) ,CA-CS表面的孔隙结构和粗糙程度明显增加,有利于CA-CS吸附降解土壤中的有机污染物。
2) XPS结果分析。利用XPS能够有效分析新型CA-CS复合催化剂的化学成分组成,结果如图3所示。从图3(a)可以看出,K和Mg成功负载在CA-CS上,表明负载光卤石能够有效提高生物炭中K和Mg的含量。CA-CS的C 1s光谱图3(b)主要有两类峰,在284.9 eV处对应的是石墨化碳 (sp2杂化,C=C) 以及碳缺陷结构 (sp3杂化,C-C) ,在285.3 eV处对应的是C-O-C,石墨化程度提高有利于增强CA-CS的电子转移能力。由图3(c)可知,CA-CS中的K主要以KCl的形式存在。此外,CA-CS的Mg 1s光谱图3(d)表明负载在CA-CS上的Mg主要以MgO (1 303.9 eV) 和Mg(OH)2 (1 305.8 eV) 的形式存在。
-
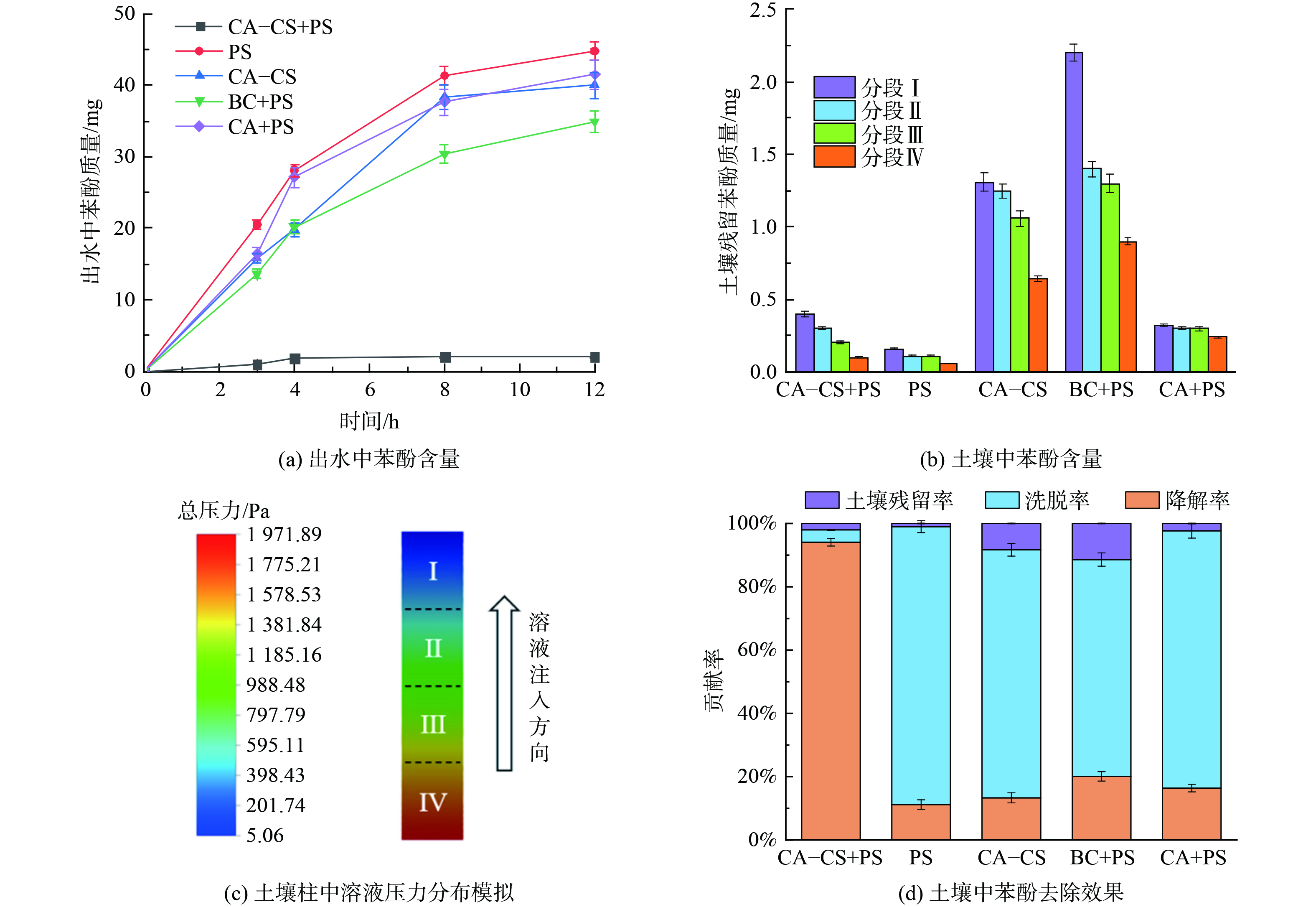
设置实验组 (1) CA-CS+PS; (2) PS; (3) CA-CS+去离子水; (4) BC+PS; (5) CA+PS,研究CA-CS复合催化剂在降解土柱中苯酚的作用,实验结果如图4所示。图4(a)中,当CA-CS和PS共同加入时浸出的苯酚含量最低,仅为2 mg,而其他对照组浸出苯酚含量为35~44 mg,表明加入CA-CS能有效降低苯酚的浸出。在图4(b)中,从分段Ⅰ到分段Ⅳ,土壤中残留的苯酚含量逐渐减少。结合CFD模拟结果 (图4(c)) ,可以直观地看到PS溶液在土柱中的压力从分段Ⅳ到分段Ⅰ逐渐降低,较高的压力可以强化PS与土壤中CA-CS复合催化剂之间的传质速率,进而提高对苯酚的降解效果。因此,苯酚在土柱中的质量分布与PS溶液在土柱中的压力分布结果相一致。此外,仅加入PS溶液土壤中残留的苯酚含量最低,而加入CA-CS和PS时土壤中残留的苯酚含量仅略高于只加入PS。由于生物炭材料会吸附土壤中的苯酚,导致实验组(3)和(4)中土壤残留的苯酚含量升高。分析图4(d)可知,只加入PS溶液土柱中苯酚的降解率仅为11.2%,表明土壤中的矿物组分和有机质无法有效活化PS。并且只加入CA-CS和去离子水对土壤中苯酚的降解率也很低 (13.3%) ,表明吸附并非CA-CS去除苯酚的主要途径。然而,当CA-CS和PS溶液同时加入时,土壤中苯酚的降解率达到94.1%,与上述对照组相比苯酚的降解率大幅提高,证明CA-CS催化PS氧化苯酚是去除土壤中苯酚的主要途径。此外,在生物炭上负载光卤石是提高生物炭催化性能的关键,原因在于CA+PS和BC+PS对土壤中苯酚的降解率分别只有16.4%和20.1%,可知CA和BC对PS的催化效果并不理想。
-
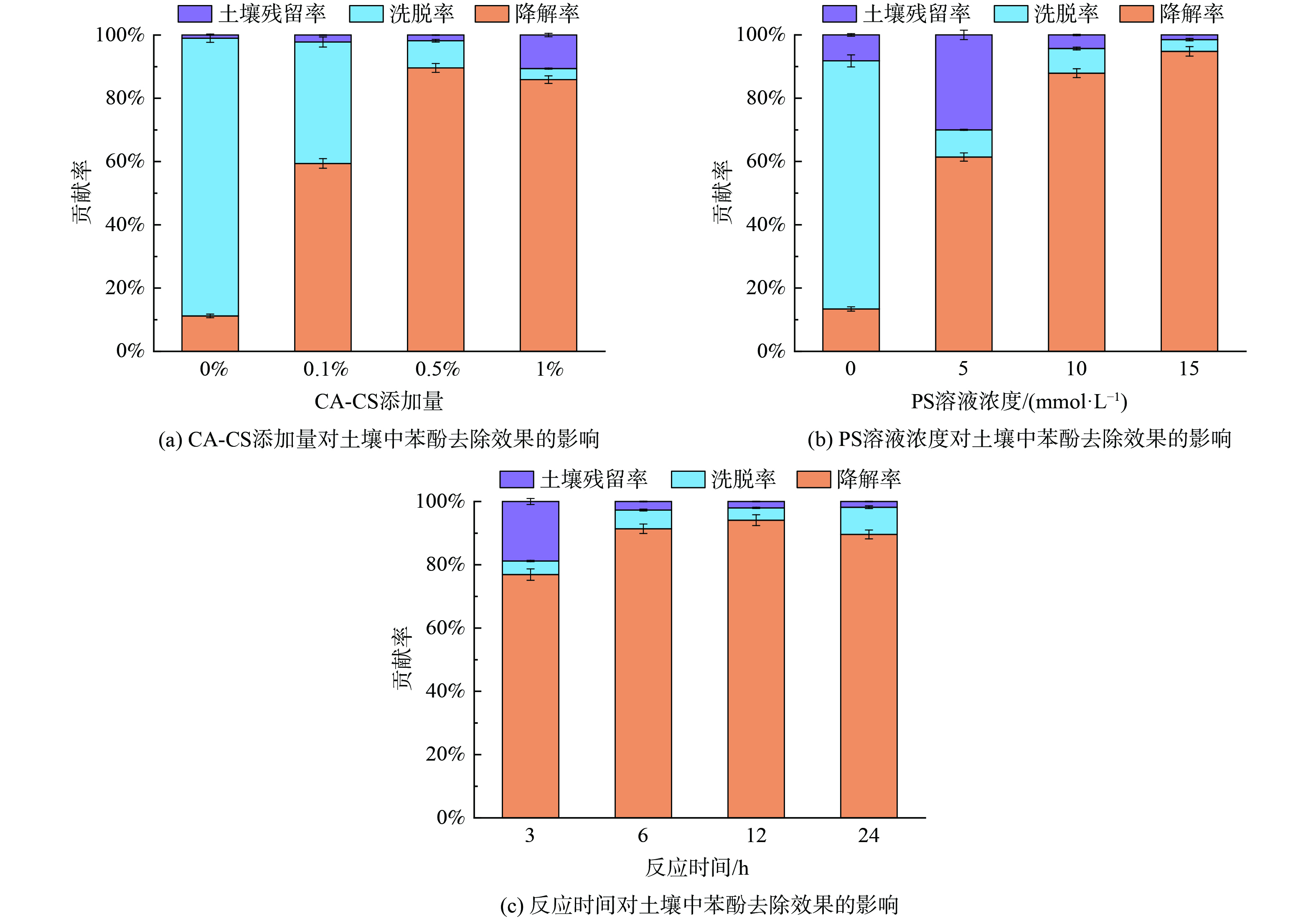
1) CA-CS添加量对降解苯酚的影响。CA-CS添加量对出水和土壤中苯酚含量的影响结果如图5(a)所示。随着CA-CS添加量从0增加到1%,出水中苯酚的总含量逐渐降低,说明添加CA-CS能够有效降解出水中的苯酚含量。土壤中残留的微量苯酚也能支撑这一结论,当CA-CS添加量为1%时,土壤中残留的苯酚含量较高,可能的原因是土壤中的苯酚吸附在过量的CA-CS上,使苯酚残留量提高。随着CA-CS添加量提高,通过氧化降解途径去除的苯酚含量逐渐升高,当CA-CS添加量为0.5%,PS溶液浓度为10 mmol·L−1,反应时间为24 h时,苯酚的降解率达到89.6%。但当CA-CS添加量增加至0.5%以上时,无法进一步提高苯酚的降解去除率。因此,综合考虑成本及去除效果,确定最佳CA-CS添加量为相当于土壤质量的0.5%。
2) PS浓度对降解苯酚的影响。PS浓度对去除土壤中苯酚的影响结果如图5(b)所示。随着PS浓度从0提高到15 mmol·L−1,出水中苯酚的总含量呈先减小后增大的趋势,在PS浓度为5 mmol·L−1时出水中的苯酚含量最低,为1.9 mg 。然而,PS浓度为5 mmol·L−1时土壤中残留的苯酚含量最高,当PS浓度进一步提高后,土壤中残留的苯酚含量显著降低,此时出水中的苯酚含量仅略微升高。当PS浓度为10 mmol·L−1时,苯酚的降解率已达87.1%,而进一步提高PS浓度苯酚的降解率无明显提高。因此,综合考虑成本和去除效果确定最佳PS浓度为10 mmol·L−1。
3) 反应时间对降解苯酚的影响。不同反应时间对去除土壤中苯酚的影响结果如图5(c)所示。当反应时间为3 h时土壤中残留的苯酚为9.6 mg,进一步延长反应时间为6 h时土壤中残留的苯酚含量大幅降低,仅为1.4 mg,表明延长反应时间能够有效减少土壤中的苯酚。随着反应时间的增加,苯酚的降解率先升高后降低,在12 h时苯酚的降解率达到最大值,为94.1%。进一步延长反应时间至24 h,土壤中苯酚的降解率略有下降,可能是由于部分吸附在CA-CS上的苯酚解吸使出水中的苯酚含量增加,导致降解率降低。因此,确定最佳反应时间为12 h。
-
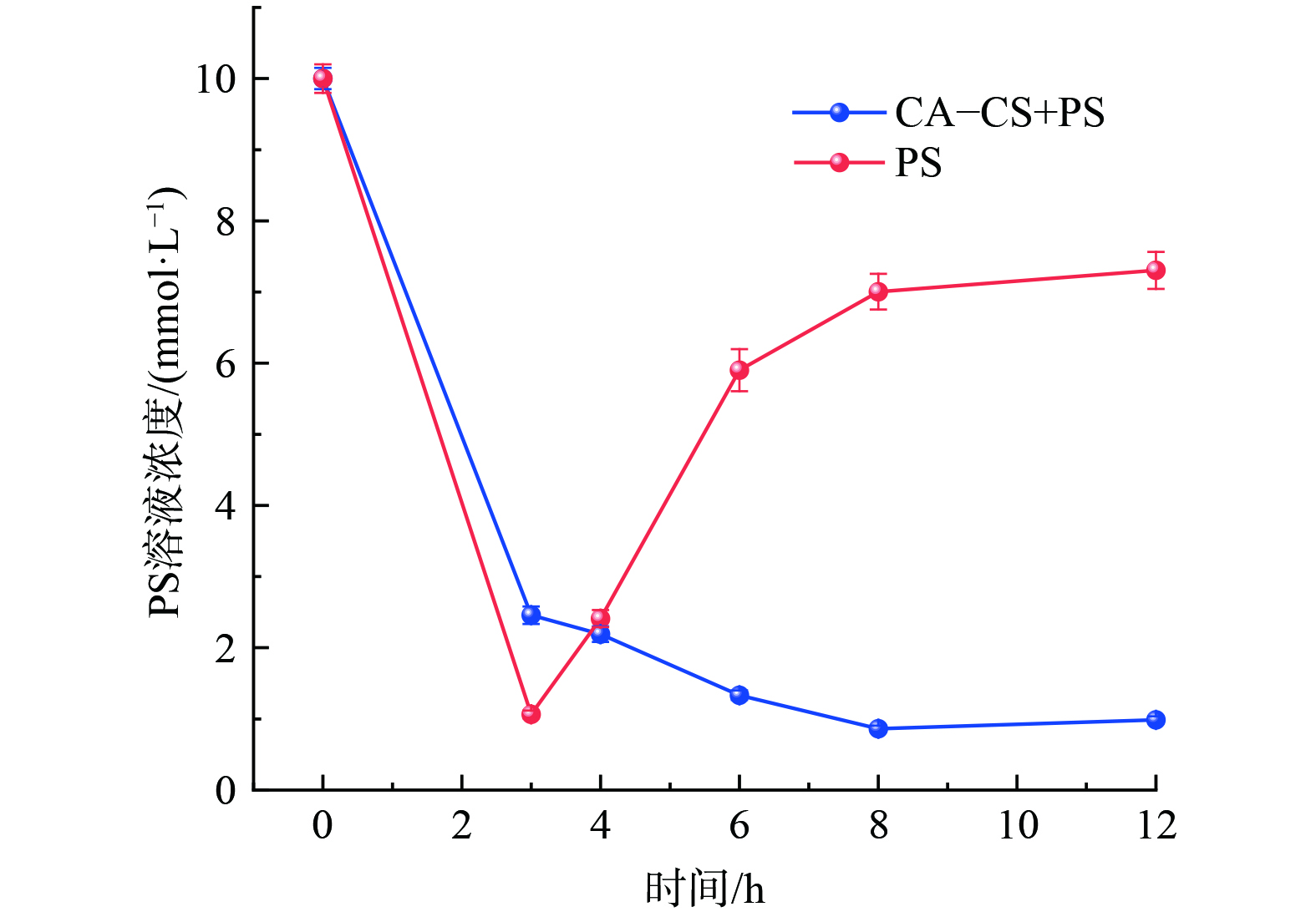
测定出水中PS随时间的浓度变化,实验结果如图6所示。分析可知,两组实验中PS溶液的浓度都随着反应时间的增加呈现先减小后增大的趋势。不同之处在于,只加入PS在3 h时PS溶液的浓度即达最小值,为1.06 mmol·L−1,之后持续增加至7.30 mmol·L−1,表明土壤中的有机质能够消耗部分PS降解苯酚[16];而CA-CS和PS共同添加时,在5~12 h内PS溶液的浓度大幅降低,在8 h时PS溶液的浓度才达到最小值,为0.86 mmol·L−1,在12 h时增加到0.99 mmol·L−1,表明CA-CS能够有效利用PS降解土壤中的苯酚。
-
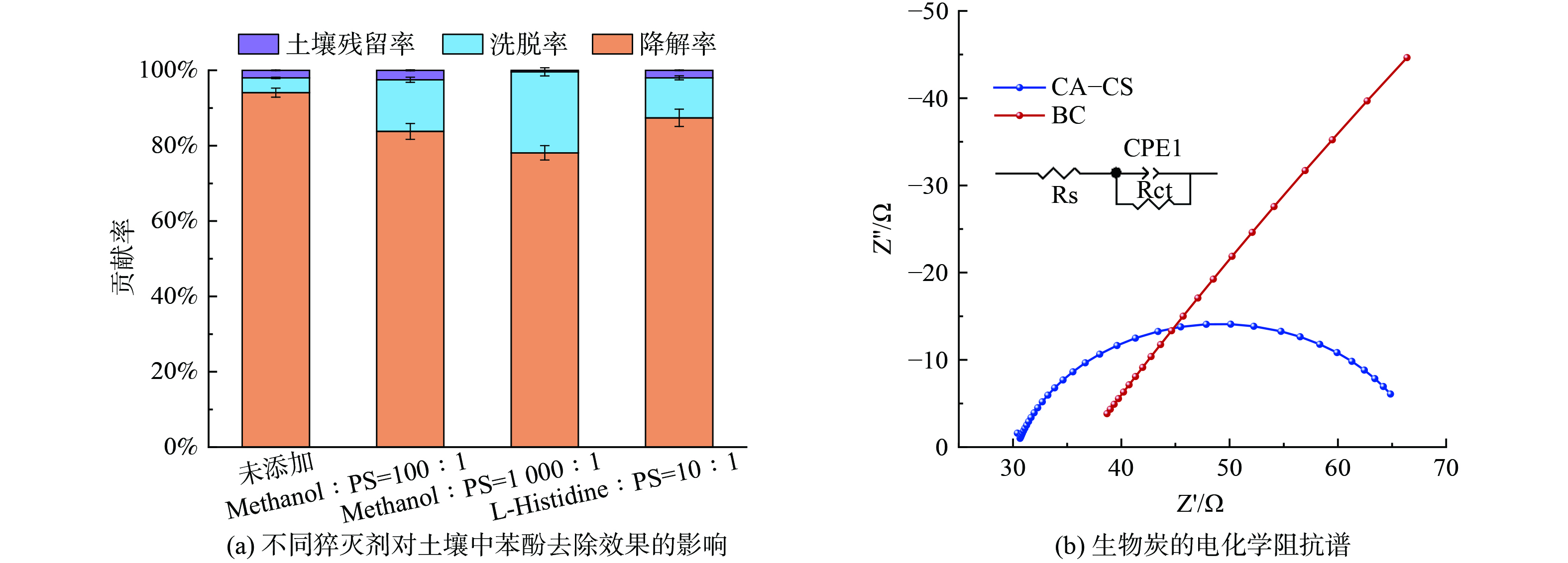
通过猝灭实验探究CA-CS催化PS氧化苯酚的机理,甲醇用于检测·OH和SO4−·,L-组氨酸用于检测1O2。甲醇与PS的摩尔比为0、100∶1、1 000∶1,L-组氨酸与PS的摩尔比为10∶1,其余实验过程与1.6催化实验相同,实验结果如图7(a)所示。分析可知,相比于未添加猝灭剂的实验,甲醇与PS的摩尔比为100∶1时苯酚的降解率降低了10.3%,将甲醇与PS的摩尔比提高至1 000∶1时苯酚的降解率降低了16%。表明·OH和SO4−·在降解苯酚的过程中不占据主导地位。此外,相比于未添加猝灭剂的实验,L-组氨酸与PS的摩尔比为10∶1时苯酚的降解率仅降低6.7%,说明1O2也并非降解土壤苯酚的主要途径。
电化学阻抗 (EIS) 测试用于表征材料的电子转移性能,使用三电极体系对CA-CS复合催化剂进行测试,并用Zview软件对EIS测试结果进行拟合,结果如图7(b)所示。图中半圆的直径表示电荷转移电阻的大小,半圆直径越小材料电荷转移电阻越小,电子转移能力越强[17]。由此可知,CA-CS的电子转移能力强于BC,并且CA-CS和BC的溶液电阻 (Rs) 分别为30.34 Ω和36.35 Ω,在生物炭上掺杂光卤石使其Rs值降低了16.5%。此外,CA-CS的电荷转移电阻 (Rct) 为37.5 Ω,相比于BC (904.3 Ω) 降低了24.1倍。CA-CS电子转移能力的增强有利于其通过电子转移途径降解土壤中的苯酚。结合猝灭实验结果,电子转移应为CA-CS催化PS降解土柱中苯酚的主要途径,其中CA-CS作为电子转移的桥梁,苯酚直接提供电子给PS,进而使苯酚被降解。
-
氧化前后的土壤分别用激光粒度仪进行了测试,测试结果如表2所示。氧化前土壤的平均粒径为88.7 μm。其中,黏粒 (<2 μm) 占2.2%,粉粒 (2~50 μm) 占37.5%,砂粒 (50~2 000 μm) 占60.3%。根据粒径分布,氧化前土壤属于典型的中砂土。氧化后土壤的平均粒径为63.6 μm。其中,黏粒 (<2 μm) 占5.4%,粉粒 (2~50 μm) 占45.2%,砂粒 (50~2 000 μm) 占49.4%,根据粒径分布,氧化后土壤属于粉砂质壤土[18]。氧化后土壤的平均粒径减小,黏粒和粉粒的占比显著增加。
从图8可知,经过修复后的土壤柱中,从上至下较大粒径 (>20 μm) 的土壤颗粒数量占比不断下降,较小粒径 (<20 μm) 的土壤颗粒数量占比上升,并且土壤颗粒的比表面积随之增加。原因为经过CA-CS催化PS氧化后,土壤中的苯酚被氧化去除,土壤颗粒分散程度增加,导致土壤粒径减小及比表面积增大。较细颗粒含量和比表面积的增加可以有效提高土壤对水以及其他营养物质 (氮、磷、钾等) 的保蓄性,进而增强土壤肥力[19]。同时,土壤粒径减小使土壤中的有机质不易流失,有利于修复后土壤中农作物和其他植物的生长[20]。
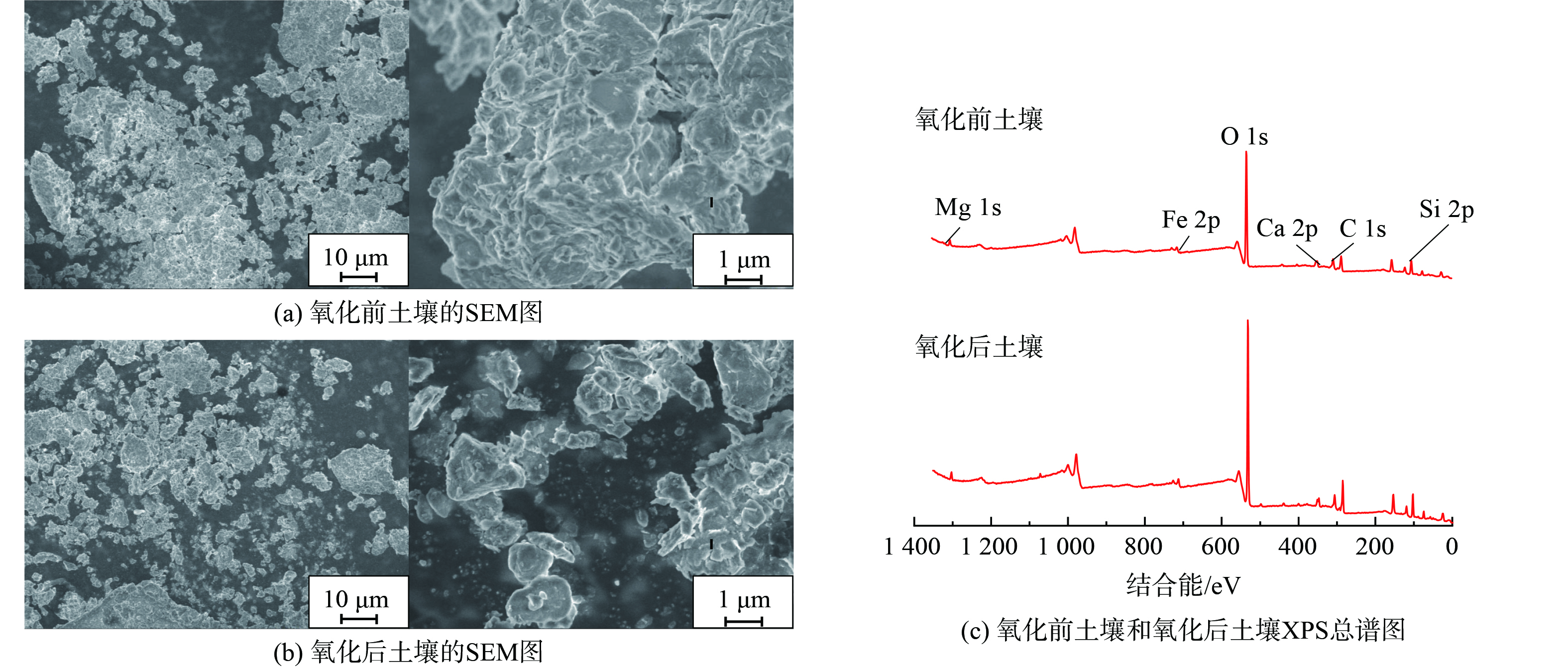
对反应前后土壤的形貌及元素组成进行分析,结果如图9所示。分析可知,氧化前的土壤颗粒团聚,而氧化后土壤颗粒分散程度增大,且土壤中的苯酚被氧化去除,导致土壤颗粒的粒径减小,与土壤粒径分析结果相同。而图9(b)中氧化前后土壤中的元素组成无明显变化,说明CA-CS催化PS降解土壤中苯酚未改变土壤的矿物成分。此外,氧化前土壤的TOC值为21.8 g·kg−1,氧化后土壤的TOC值为14.1 g·kg−1,降低了35.6%,表明土壤中的苯酚部分矿化为CO2和H2O。
-
1) 本研究首次制备出富含K+、Mg2+的光卤石修饰生物炭复合催化剂CA-CS活化PS降解土壤中的苯酚,实验结果表明,负载光卤石是提高生物炭催化性能的关键。在CA-CS添加量相当于土壤质量0.5%、PS浓度为10 mmol·L−1、反应时间为12 h时,土壤中苯酚的降解率达到94.1%。
2) CA-CS催化PS修复苯酚污染土壤的机理为CA-CS作为电子转移的桥梁,加速电子从苯酚转移到PS,最终使苯酚被降解。
3) 修复后苯酚污染土壤的平均粒径从88.7 μm降低到63.6 μm,土壤TOC值降低了35.6%,土壤的比表面积增大了38.1%。此外,修复后土壤颗粒的分散程度增大,并且修复前后土壤的化学组成未发生明显变化。
光卤石修饰生物炭活化过硫酸盐修复有机污染土壤
Activation of persulfate with carnallite-modified biochar for remediation of organic-contaminated soil
-
摘要: 过硫酸盐 (PS) 氧化技术被广泛应用于有机污染物土壤的修复,其中高效、环境友好型非均相催化剂的研发一直是PS氧化技术研究的热点和难点。天然矿物光卤石 (CA) 本身无法有效活化PS,但将其负载在生物炭上制备的复合催化剂CA-CS能够大幅提高生物炭的催化性能。研究结果表明,CA-CS的最佳添加量为土壤质量的0.5%,最佳PS浓度以及反应时间分别为10 mmol·L−1和12 h,该条件下对土壤中苯酚的降解率为94.1%。猝灭实验和电化学表征表明,苯酚、CA-CS、PS构成一个电子供体-电子介导体-电子受体的三元络合体系,在CA-CS催化作用下,PS可以更快地从苯酚提取电子,通过电子转移路径对苯酚进行降解。此外,氧化后土壤的粒径显著降低,且土壤的化学组成未发生明显变化。本研究旨在为实际工程应用中修复有机污染土壤提供一种高效、绿色的非均相催化剂。Abstract: The development of efficient and environmentally friendly heterogeneous catalysts has been a challenging and hot topic in the research of persulfate (PS) oxidation technology, widely applied for the remediation of soil contaminated with organic pollutants. The natural mineral carnallite (CA) alone cannot effectively activate PS, but when loaded onto biochar to form the composite catalyst CA-CS, it significantly enhanced the catalytic performance of biochar. The research findings indicated that the optimal addition amount of CA-CS was equivalent to 0.5% of the soil mass, with the best PS concentration at 10 mmol·L−1 and reaction time for 12 h, resulting in a degradation rate of 94.1% for phenol in soil under these conditions. Quenching experiments and electrochemical characterization demonstrated that phenol, CA-CS, and PS formed a ternary complex system of electron donor-electron mediator-electron acceptor. Under the catalytic action of CA-CS, PS could more efficiently extract electrons from phenol and degrade it through an electron transfer pathway. Additionally, the particle size of the soil significantly decreased after oxidation, while the chemical composition of remained soil relatively unchanged. It aims to provide an efficient and environmentally friendly heterogeneous catalyst for the remediation of organic polluted soil in practical engineering applications.
-
Key words:
- organic-contaminated soil /
- soil column experiment /
- persulfate /
- biochar /
- electron transfer
-

-
表 1 土壤理化性质
Table 1. Soil physical and chemical properties
参数 数值 单位 TOC 21.8 g·kg−1 pH (水土比=2.5∶1) 7.62 — 平均粒径 88.7 μm 比表面积 0.396 m3·g−1 硅 12.19 g·100g−1 氧 39.06 g·100g−1 镁 1.10 g·100g−1 铝 5.06 g·100g−1 钾 1.42 g·100g−1 钙 4.48 g·100g−1 铁 3.35 g·100g−1 表 2 氧化前后土壤粒径对比
Table 2. Comparison of soil particle size before and after oxidation
土壤
样品平均
粒径/μm比表面积/
(m3·g−1)颗粒组成/% 砂粒
(2~0.05 mm)粉粒
(0.05~0.002 mm)黏粒
(<0.002 mm)氧化前 88.7 0.396 60.3 37.5 2.2 氧化后 63.6 0.547 49.4 45.2 5.4 -
[1] WEI K H, MA J, XI B D, et al. Recent progress on in-situ chemical oxidation for the remediation of petroleum contaminated soil and groundwater[J]. Journal of Hazardous Materials, 2022, 432: 128738. doi: 10.1016/j.jhazmat.2022.128738 [2] XIA T, MA M, HUISMAN J A, et al. Monitoring of in-situ chemical oxidation for remediation of diesel-contaminated soil with electrical resistivity tomography[J]. Journal of Contaminant Hydrology, 2023, 256: 104170. doi: 10.1016/j.jconhyd.2023.104170 [3] CUI B, TIAN T, DUAN L, et al. Towards advanced removal of organics in persulfate solution by heterogeneous iron-based catalyst: A review[J]. Journal of Environmental Sciences, 2023, 146: 163-175. doi: 10.1016/j.jes.2023.06.035 [4] XIAO J, HE D, YE Y, et al. Recent progress in persulfate to improve waste activated sludge treatment: Principles, challenges and perspectives[J]. Chemical Engineering Journal, 2023, 469: 143956. doi: 10.1016/j.cej.2023.143956 [5] LIU Z, REN X, DUAN X, et al. Remediation of environmentally persistent organic pollutants (POPs) by persulfates oxidation system (PS): A review[J]. Science of the Total Environment, 2023, 863: 160818. doi: 10.1016/j.scitotenv.2022.160818 [6] REN G B, LI R X, ZHAO M C, et al. Membrane electrodes for electrochemical advanced oxidation processes: Preparation, self-cleaning mechanisms and prospects[J]. Chemical Engineering Journal, 2023, 451: 138907. doi: 10.1016/j.cej.2022.138907 [7] XU Q, ZHOU F, YU Q, et al. Aniline degradation and As (III) oxidation and immobilization by thermally activated persulfate[J]. Chemosphere, 2023, 338: 139573. doi: 10.1016/j.chemosphere.2023.139573 [8] YANG J, LI X, WEI M, et al. Base-activated persulfate strategy for ceramic membrane cleaning after treatment of natural surface water[J]. Chemical Engineering Research and Design, 2023, 194: 245-255. doi: 10.1016/j.cherd.2023.04.063 [9] LI X, SHEN J, SUN Z, et al. Insights into the impacts of chloride ions on the oxidation of 2, 4-dinitrotoluene using ferrous activated persulfate: Removal efficiency, reaction mechanism, transformation pathway, and toxicity assessment[J]. Chemosphere, 2023, 317: 137887. doi: 10.1016/j.chemosphere.2023.137887 [10] LI J, GUO Z, CUI K, et al. Remediating thiacloprid-contaminated soil utilizing straw biochar-loaded iron and manganese oxides activated persulfate: Removal effects and soil environment changes[J]. Journal of Hazardous Materials, 2023, 459: 132066. doi: 10.1016/j.jhazmat.2023.132066 [11] LIU T, YAO B, LUO Z, et al. Applications and influencing factors of the biochar-persulfate based advanced oxidation processes for the remediation of groundwater and soil contaminated with organic compounds[J]. Science of the Total Environment, 2022, 836: 155421. doi: 10.1016/j.scitotenv.2022.155421 [12] DAI C, ZHANG J B, GAO M T, et al. Effects of functional group loss on biochar activated persulfate in-situ remediation of phenol pollution in groundwater and its countermeasures[J]. Journal of Environmental Management, 2023, 341: 118076. doi: 10.1016/j.jenvman.2023.118076 [13] XIONG Y H, PEI D S. A review on efficient removal of phthalic acid esters via biochars and transition metals-activated persulfate systems[J]. Chemosphere, 2021, 277: 130256. doi: 10.1016/j.chemosphere.2021.130256 [14] ZHAO Y, SONG M, CAO Q, et al. The superoxide radicals’ production via persulfate activated with CuFe2O4@biochar composites to promote the redox pairs cycling for efficient degradation of o-nitrochlorobenzene in soil[J]. Journal of Hazardous Materials, 2020, 400: 122887. doi: 10.1016/j.jhazmat.2020.122887 [15] LIU R, YANG J Y. Enhanced removal of sulfamethoxazole in soil by ball-milled Fe0-FeS@BC activated persulfate process[J]. Journal of Environmental Chemical Engineering, 2023, 11: 110747. doi: 10.1016/j.jece.2023.110747 [16] FANG G, CHEN X, WU W, et al. Mechanisms of interaction between persulfate and soil constituents: Activation, free radical formation, conversion, and identification[J]. Environmental Science & Technology, 2018, 52: 14352-14361. doi: 10.1021/acs.est.8b04766 [17] LI C, XU B, JIN M, et al. Sulfur and nitrogen co-doped biochar activated persulfate to degrade phenolic wastewater: Changes in impedance[J]. Journal of Molecular Structure, 2023, 1294: 136344. doi: 10.1016/j.molstruc.2023.136344 [18] 何海龙, 齐雁冰, 吕佳珑, 等. 中国土壤质地分类系统的发展与建议修订方案[J]. 农业资源与环境学报, 2023, 40: 501-510. doi: 10.13254/j.jare.2022.0854 [19] ZOU Q, WEI H, CHEN Z, et al. Soil particle size fractions affect arsenic (As) release and speciation: Insights into dissolved organic matter and functional genes[J]. Journal of Hazardous Materials, 2023, 443: 130100. doi: 10.1016/j.jhazmat.2022.130100 [20] HEMKEMEYER M, CHRISTENSEN B T, MARTENS R, et al. Soil particle size fractions harbour distinct microbial communities and differ in potential for microbial mineralisation of organic pollutants[J]. Soil Biology and Biochemistry, 2015, 90: 255-265. doi: 10.1016/j.soilbio.2015.08.018 -



 下载:
下载: