-
工业废水的水处理问题是我国面临的主要环境问题之一。电催化氧化净水技术具有高效、适应性强、反应条件温和,在工业废水处理上具有极大的优势,电催化氧化过程通常分为直接氧化过程和间接氧化过程[1]。在阳极发生的直接氧化作用是指污染物颗粒吸附在阳极材料表面,通过阳极上电子的转移实现的污染物降解[2],但是通常对污染物的降解作用较小。间接氧化过程是通过阳极表面产生的活性中间物质(如·OH、OCl、O3)或具有高氧化性的高价态金属氧化物来氧化降解水中有机污染物,是污染物降解的最主要形式[3]。值得注意的是,工业废水中通常含有大量的氯离子,氯离子可以在(光)电化学催化氧化下形成强氧化性的氯自由基和活性氯物种(·Cl、·ClO−、Cl2)[4-5],这些含氯氧化剂可与羟基自由基(·OH)共同氧化降解很多有机污染物[6]。然而,对于含盐废水中有机污染物的降解,间接氧化产生的氯活性物种的利用率受限于传质效率,尤其是针对于大分子难降解有机物,较难实现污染物的完全矿化,因此提升氯活性物种的产生和利用效率则有望极大促进含盐废水中有机污染物的降解[7]。
在光电协同降解污染物的体系中,传质效率和提升光的利用率是提升含盐废水中有机污染物的降解效果的重要途径。已有大量研究表明,通过外力作用使含污染物的废水强制性通过多孔极板的穿透式电极构型可以数量级提升传质效率和电子转移效率,从而提升净水性能[8-9]。ISRAEL等[10]通过穿透式和传统的浸没式电极反应器对水中阿莫西林电化学氧化实验对比发现,穿透式构型可以带来更高的电化学氧化效率和更低的能耗,相比于浸没式电极,穿透式反应器运行下对阿莫西林的去除效率提升了70%,降解速率和传质速率分别提升了3.46和10.74倍,强氧化性的中间活性物质·OH的生成量高了5.64倍,每单元能耗降低了19.89倍。WANG等[11]通过TiO2/Ti多孔膜对甲基蓝(MB)降解中发现,在相同的水力停留时间下,穿透式构型中MB去除率可达99.5%,浸没式构型仅为21.0%,强制对流促进的高传质效率是提升污染物降解的关键因素。合理搭建穿透式电极反应器,减少传质距离,多极板串联,可以有效提升传质效率和净水性能。相比于单独的电化学催化,光的引入可以进一步提升氯活性物种的产生量,研究发现,光催化产氯的主要波段在254 nm[12]。然而常规的将光源引入会存在两个问题,一是光源的能量不足以高效将氯离子向氯活性物质激发转化,二是利用光催化处理废水时,光在水中穿透性有限,光能的有效利用率不足。基于此,我们考虑到在实验中引入具有瞬间高强度光能释放的脉冲灯管作为光源,脉冲光是将相同的能量以高峰值形式瞬间释放,在水中具有很好的穿透性,同时在反应过程中可以保持低温,无需像汞灯一样依赖一定的温度对汞进行汽化,两个脉冲之间也有足够的冷却时间,因而在实际应用过程中,比常规的紫外灯有更广的适用范围。现有的研究主要集中于电化学氧化作用提高污染物的降解效率,对于光电协同直接将废水中的氯离子利用并转化为高氧化性的活性氯物质的研究尚不充足,而提高传质并协同提升光利用效率是促进含盐废水中有机物被高效降解的关键。此外,穿透式电极常受限于电极材料的尺寸,以往研究中基本是采用较小体积的过滤器构型反应器,单次穿透时水停留时间很短[13]。因此构建处理水量达到数十升级的较大规模单个反应器,延长水力停留时间,使单次处理出水即可达标,实现连续运行具有更好的实际应用价值。
本研究选用了4-硝基酚(4-np)作为目标污染物,4-硝基酚作为重要的工业原料,广泛应用于医药、农药、染料和防腐等行业。在实际生产加工过程中,这些行业常常会有大量的4-硝基酚排放[14]。构建了具有大体积的光电协同的穿透式电极反应器,将3层多孔电极进行套管式排布,中心放置具有高强度的脉冲光源,通过脉冲光电协同作用,将废水中的氯离子转化为具有氧化活性的氯活性物质(reactive chlorine species,RCS),实现水中有机污染物的快速降解和高效矿化。实验比较了脉冲光和常规紫外光源在污染物降解上的差异性,并考察了流量、施加电压、含盐量、pH值等因素对污染物降解速率的影响,分析了污染物降解的主导因素,确定反应器长期稳定运行的最佳工作条件。本研究为脉冲光电协同反应器在实际工程中的应用奠定了基础并构建了一种高效的含盐废水中有机污染物去除的水处理技术。
-
实验中所用化学试剂4-硝基酚、氯化钠、硫酸钠、硫酸、氢氧化钠、硫代硫酸钠、磷酸、硝酸等均为国药沪试分析纯,DPD粉包为美国哈希(型号
2105569 )。 -
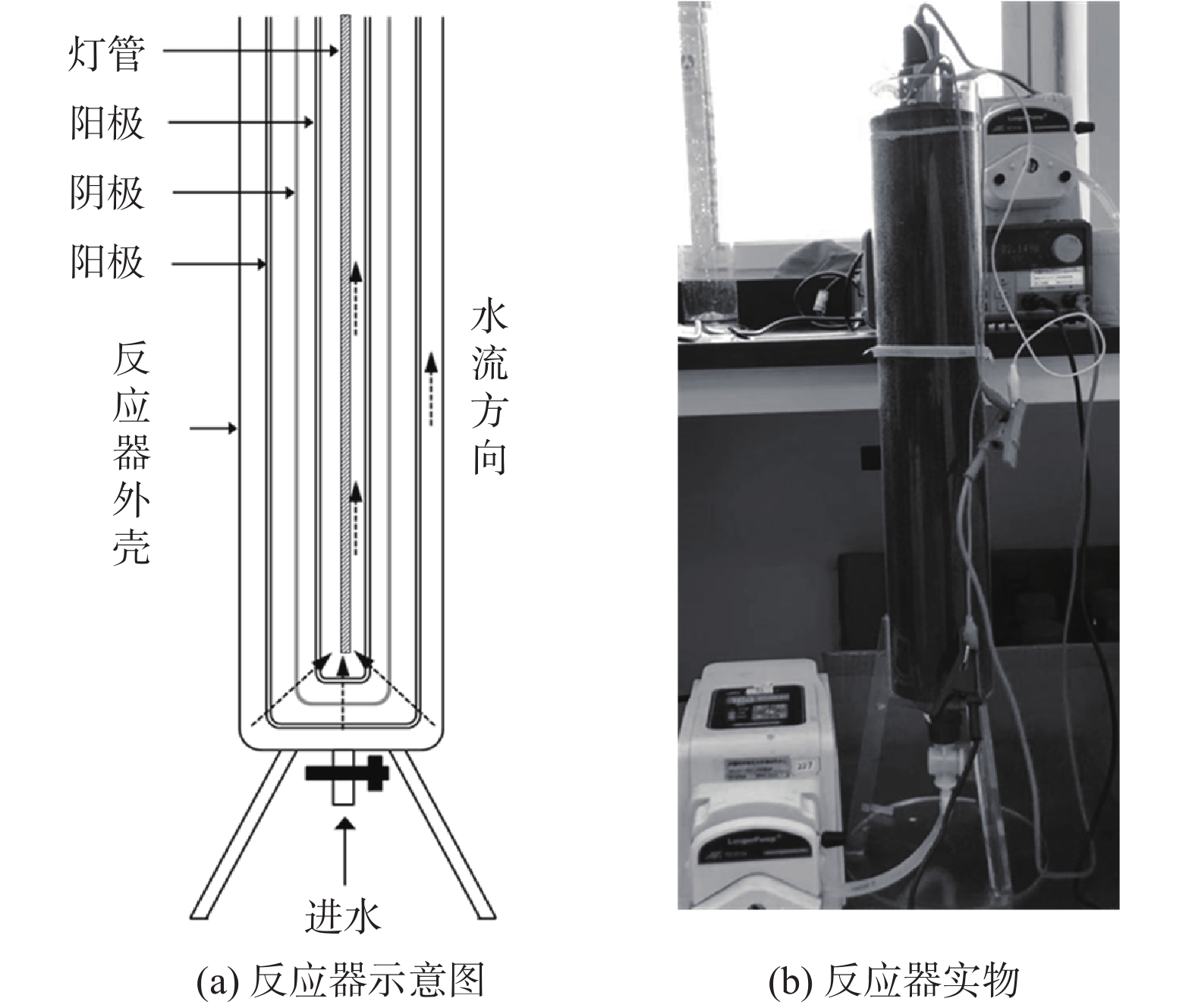
实验采用升流式光电协同穿透式电极反应器,反应器设计如图1(a)所示。反应器主体部分由3层套管电极构成,由外向内为阳极-阴极-阳极;阴极为泡沫钛,平均孔径为50 μm,厚度为2 mm;阳极选用的为相同材质的泡沫钛上喷涂金属钌。3个套管电极的尺寸分别为 Φ65 mm×500 mm、Φ50 mm×490 mm、Φ35 mm×480 mm,电极管上部边缘焊接1 cm×2 cm的钛片以连接电源,该孔径下的3个电极,水流均可无外加压力渗透透过。3层套管中间用硅胶垫片隔离开,以避免短路,极板间距为2 m。反应器外壳为聚四氟乙烯(PTFE)材质作为支撑,腔室下部中间为进水口;反应器上部中心开孔为抽水孔,以便于溢流抽水,反应器顶盖侧面开槽,以便于连接电源线。反应器中心放置灯管光源,光源分别选用定制的脉冲强光灯(IPL)和相等功率的紫外光源(入射波长λ=254 nm,15 W)。脉冲灯管外包裹保护层石英管,光谱透过率大于 90%以上,灯管有效寿命为 5 000 h,脉冲强光的光电能转换率为45%~50%,紫外线能量占约38%,脉冲灯管的能量10 J,功率为15 W。实验中,水流为升流式,水流从底部进水,穿透3层电极后,从反应器顶部抽出,反应器的有效容积为1.9 L。反应器的实物图如图1(b)所示。
-
实验选取4-硝基酚(4-np)为目标污染物进行光电协同降解实验。实验中用直流电源(AMERLLDS302A,大华,中国)进行供电,在未加光照的对照中,灯管仍然放置于电极套管内,以保证平行实验中反应器有效容积的一致性,降解实验分为循环流实验和单次穿透两种模式,实验中,在蠕动泵的作用下从底部进水时刻连接电源,并开启光源,当水流充满反应器,溢流出水时刻开始计时,此时开启蠕动泵在顶端进行溢流排水。循环流实验中间隔一定时长取5 mL水样进行后续分析测试;单次穿透实验中,待反应器稳定运行30 min后每隔10 min取5 mL出水进行分析。水样经过0.45 μm滤膜过滤后,转移到离心管中,加入硫代硫酸钠进行淬灭反应和保存,以测试4-硝基酚的浓度,并测试水样中的活性氯和总有机碳(TOC)。污染物降解实验中,初始4-硝基酚浓度设置为1 mmol·L−1(139.1 mg·L−1);不同流量的实验中,分别设置了200、100、80、50 mL·min−1,计算获得的水力停留时间如表1所示。
不同盐浓度实验中,氯化钠浓度设置为25、50、171、256、512 mmol·L−1;用0.1 mol·L−1硫酸和1 mol·L−1氢氧化钠调节溶液pH,pH值设置为2.0、4.0、6.0、8.00和10.00。不同电压对污染物去除的影响中,施加电压设置为0、1、2、3 V;实验中使用两种光源时均在上述各种条件下进行。污染物降解效果η根据式(1)进行计算。
式中:C0和C分别为4-硝基酚初始浓度(初始总有机碳值)(mg·L−1)和t时刻(min)溶液中的4-硝基酚浓度(t时刻总有机碳值)(mg·L−1)。
-
通过高效液相色谱(Agilent
1260 ,美国)测量样品中 4-硝基酚的浓度,Agilent C18柱(250 mm×4.6 mm, 5 μm)和紫外检测器,柱温35 ℃,进样量50 μL,流动相为10 mM 磷酸和超纯水(50∶50,v/v),流速1 mL·min−1,紫外检测器的检测波长为318 nm;通过N, N-二乙基对苯二胺(DPD)分光光度法(Hitachi,美国)测试样品中活性氯的浓度,每次测试时取1 mL水样,将样品稀释定容到10 mL,加入DPD粉包试剂,晃动20 s,显色3 min后进行读数(Hitachi UV-3100 ,美国);4-硝基酚的矿化程度通过总有机碳(TOC)(Shimadz TOC-L,日本)测定,通过电感协同等离子体发射光谱仪(ICP-OES,Agilent 710,美国)分析测定水中金属钛和钌的浓度,表征是否有钌从电极上剥落,以衡量电极的稳定使用情况实验使用蠕动泵将水从反应器底部泵入,上端溢流出水并收集,以确保液位恒定。测试样品预先用2%硝酸酸化,过0.45 μm滤膜后进行测试。矿化效率一般通过总有机碳(TOC)或化学需氧量(CODCr)衡量,本研究中以TOC为指标,衡量4-硝基酚的矿化率,见式(2)。式中:TOC0和TOCt分别代表初始时刻和t时刻的TOC(mg·L-1)。
本光电反应器的单位能耗的计算根据式(3)。
式中:Ec为单位能耗(kWh·m−3);U为反应时电压值(V);I为反应时电流值(A);t为反应时长(h);V为处理溶液体积(m3)。
-
为了考察相同能耗的光源对污染物的降解能力和本装置的可行性,实验通过循环流模式分别用紫外光(UV)和脉冲光作为光源,对低浓度的4-硝基酚(10 mg·L−1)进行了降解实验。实验采用恒电流模式,施加电流为0.1 A,电解质为50 mmol·L−1氯化钠,实验结果如图2所示。在仅有光照的条件下,污染物降解效率极有限,120 min内4-硝基酚的降解效率分别为15.9%(紫外光源)和14.9%(脉冲光源);电催化性能优于光催化性能,在仅有电的作用下,30 min内4-硝基酚去除效率可达40.0%,60 min时,去除效率达到了98.7%。在同时施加电压和光照的情况下,45 min后4-硝基酚降解效果分别达到了96.6%和91.8%,60 min后溶液中几乎检测不到4-硝基酚。因此,该反应器可用于运行降解4-硝基酚,光电协同效果远优于单独的光/电催化氧化过程。
-
相比于循环流模式,单次穿透更适合于工程化应用,满足实际处理废水的情况,实验在不同的光电条件下进行了单次穿透实验,并考察了流量对于4-硝基酚降解性能的影响。在穿透式电极反应中,流量会直接影响水流和电极的接触时间,不同的水力停留时间会影响传质过程,从而导致降解性能的不同。在反应器稳定运行的条件下,研究了不同流量下不同光电处理中出水4-硝基酚的降解性能,外加电压为3 V,结果如图3所示。实验发现,在仅加电、加电协同紫外光以及加电协同脉冲光3种处理下,随着流量的减少,停留时间的增加,单次穿透后的出水浓度均有明显的下降。更长的停留时间可以使得污染物与电极充分反应,在3种处理模式下,50 mL·min−1流量都足以使污染物完全被降解,在200 mL·min−1的处理中,由于流量较大,停留时间很短,使得出水浓度并不稳定。更大的流量被认为可以促进离子的对流传质和扩散传质,促进反应速率[15],但是更长的停留时间更利于污染物的降解。
实验横向对比了相同流量下,不同光电处理的降解效果,如图4所示。在低流量50 mL·min−1的处理中,3种光电协同处理下的4-硝基酚降解没有明显的区别,出水的降解效果均在99%以上,说明在足够长的停留时间中,电催化直接氧化占了主导地位,可以直接将污染物降解。而在较高流量的处理中(80 mL·min−1 和100 mL·min−1),以脉冲灯为光源的光电协同处理下,污染物降解效率仍能保持在90%以上,而紫外灯为光源的光电协同单元,降解效率下降到80%~85%,这表明在相同的能耗下,强脉冲灯可以带来更好的光电协同效率,这很可能是因为脉冲灯的高光强和脉冲属性,让光在溶液中有更好的穿透性,使得溶液中更多的HOCl和OCl−接触到了光,被激发活化形成了强氧化性的氯自由基,从而促进了污染物的降解。在高流量200 mL·min−1时,3者处理下的差异并不是很大,降解效率下降到75%~80%左右,且出水状态并不稳定。实验表明,HRT在19~24 min(80~100 mL·min−1 )时达到最优的出水效果。同时,出水通过ICP-OES检测在反应过程中是否有电极的溶出,结果表明,出水中钛和钌离子浓度均在检测线以下,说明此穿透式电极反应器能够适应大流量的实际操作条件,并不会带来电极的损坏。
-
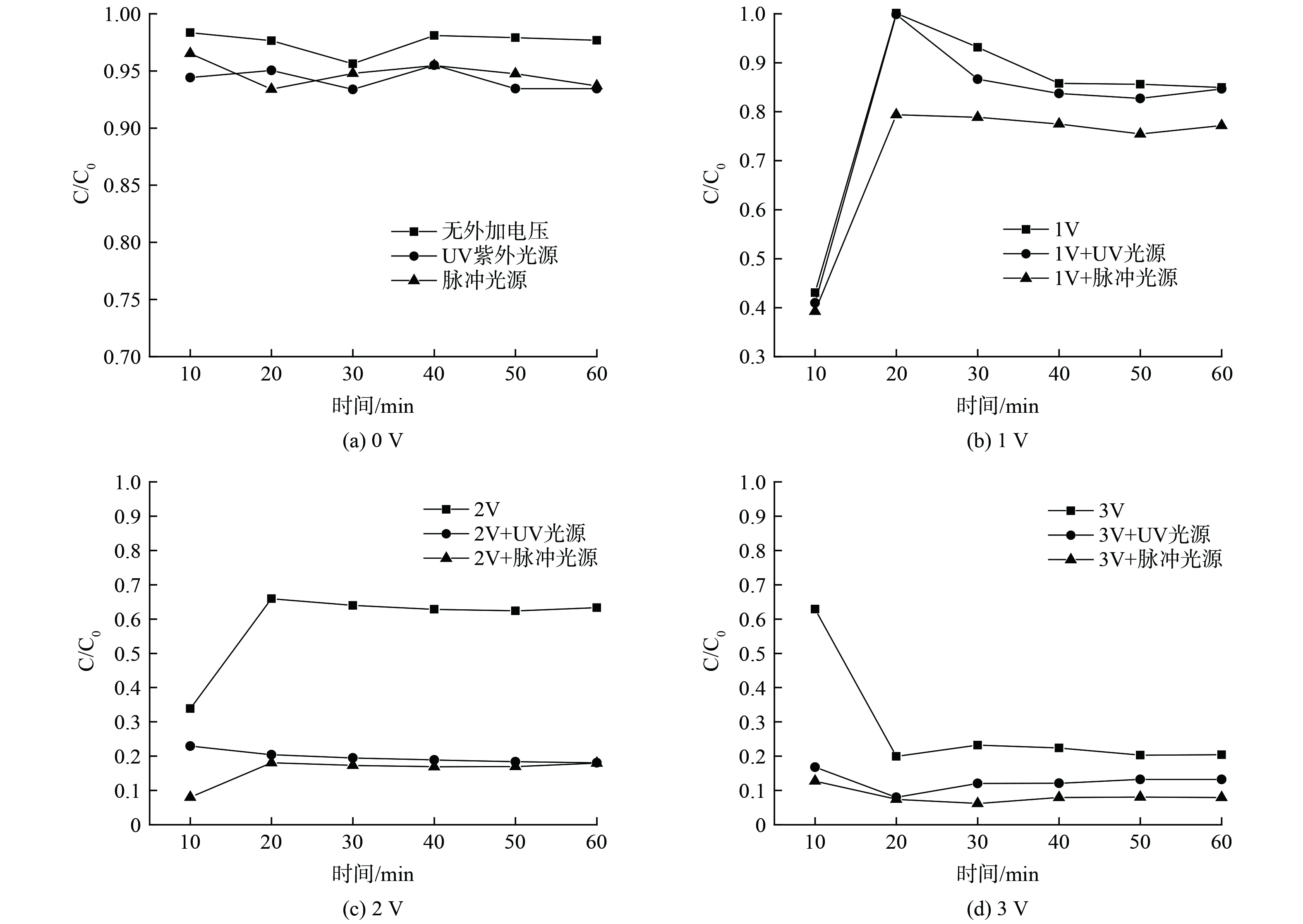
通常而言,外加电压的不同,会导致电化学过程反应速率的不同,同时直接影响了反应器的能耗。由上述实验结果也发现,本反应器体系中电催化对4-硝基酚的降解贡献明显,实验选取反应器运行性能较好的流量为100 mL·min−1时,研究0~3 V电压范围对4-硝基酚降解的影响。实验结果如图5所示,在0 V电压时,仅有光催化的作用,污染物的降解效果为5%~7%,2种光源没有表现出明显的差异,污染物降解几乎难以发生;在电压从1 V提升到3 V的3种处理中,电压和4-硝基酚降解性能呈现正相关。在施加电压下,3种电压的不同光电处理的差别较为明显,脉冲光的效果明显优于紫外。脉冲光源的光电协同处理下,2 V时,单次穿透降解污染物的效果可以达到83.1%,3 V时,降解效果可达92.1%左右。随着电压的升高,4-硝基酚被快速的降解,反应前后的溶液可以观测到明显的脱色变化。较高的电压,会促进体系中产生羟基自由基,利于间接电氧化速率,同时促进了电极表面的电子转移速率,可以有效提升污染物的直接氧化效率[16]。更为重要的是,在光电协同中,会促进HOCl的产量,而HOCl被认为是主要的去除有机污染物的活性物质[17],从而促进电化学过程的降解。然而,实验发现,在过高的电压和过长的HRT的实验中,会有少部分的钌(Ru)脱落,电压值过高会加速阳极极化并且导致大量析氧副反应的发生,降低电极效率并损坏电极,因此后续的实验中选取2 V和流量100 mL·min−1进行实验。
-
在光电协同的系统中,氯离子的含量会直接影响参与反应的活性氯物种,从而影响污染物的降解性能,实验通过改变氯化钠投加量来提升水中氯离子的浓度,并考察了溶液中氯离子浓度和pH对4-硝基酚降解性能的影响,实验结果如图6所示。通常而言,氯化钠浓度为1%以上的溶液被认为是高盐废水,基于此,实验配置了氯化钠浓度设置为25 mmol·L−1、50 mmol·L−1、171 mmol·L−1(1%)、256 mmol·L−1(1.5%)、512 mmol·L−1(3%)研究不同氯离子浓度对污染物降解的影响。如图6所示,在紫外光和脉冲光光电协同体系中,污染物降解浓度和氯离子浓度增加表现出相同的影响趋势,当氯离子浓度从25 mmol·L−1提升到50 mmol·L−1时,随着氯离子浓度的增加,污染物降解性能略有提升,出水的4-硝基酚浓度降低,降解效率分别从77.9%和79.9%提升到81.0%和83.9%;然而随着氯离子浓度的进一步增高,降解效率呈现下降的趋势。在512 mmol·L−1的处理中,降解效率分别为52.2%和59.1%。前期报道认为,当有更多的氯离子时,会大量的生产氯自由基和羟基自由基(初级自由基),同时原位电生成的Cl2可水解生成次氯酸(HOCl)和次氯酸盐离子(OCl−),增加氯离子浓度会促进一系列活性物质的产生,增加降解效率和动力学常数[18-19]。反应生成的活性氯(Cl2、HOCl和ClO−)是去除污染物的主要氧化剂,在阳极的氧化下具有较强的氧化能力,增加间接氧化效率。同时,氯离子的增加可以提高溶液中的电导率,加快电极表面的电子转移效率,提升有机物的直接氧化效果,也利于体系中产生大量羟基自由基[20]。然而,高氯化物浓度会导致大量的氯离子吸附在阳极表面,阻止了阳极上污染物的吸附和传质,从而影响了降解效率;且高浓度的氯离子可能会带来更多的副反应的发生。
溶液初始pH值会影响水中活性氯(Cl2、HOCl、ClO−)的存在形式,从而对4-硝基酚的降解有较大的影响。实验进一步研究了溶液初始pH值对污染物降解的影响,如图6所示,在pH 2~10的范围内,4-硝基酚均能够被降解去除,随着pH的增加,污染物的去除效率逐渐降低。在pH为2的极酸性条件下,污染物的降解效率最高,分别87.1%和88.8%(紫外光源和脉冲光源);在pH近似中性时,4-硝基酚的降解效率有轻微的下降,在pH为6时,降解效率分别为80.1%和83.0%;当溶液为碱性时,4-硝基酚的降解速率有大幅度的下降,分别为33.9%和36.0%。在所有的处理中,以脉冲光为光源的体系比以紫外光为光源的有略高一些的污染物降解去除率。尽管二者在污染物降解率方面差异不是很显著,但以脉冲光为光源的体系比以紫外光为光源的体系还是更具优势。因为脉冲灯光源能瞬间释放高强度光能,具有更大的穿透性(大于90%),在面向透光性较差的有色、有悬浮物的废水优势明显;其次,脉冲光是相同的能量以高峰值形式瞬间释放,同时在反应过程中,能够保持低温,两个脉冲之间也有足够的冷却时间,而紫外光主要是以热能的形式,因此光源使用寿命更长。脉冲光的间歇式发光相比于紫外光源的连续发光,如果以实际发光时间计算,对于污染物的降解和矿化性能则有显著差异。
有研究认为,不同pH下,活性中间物质活性氯的存在形式不同,从而表现出不同的降解能力,在pH>7.5时,OCl−占主导;在pH<2时,Cl2为主要的存在形式;在pH 3~7的范围内,HOCl为主要的存在形式[21]。此外,溶液pH的降解能够抑制阳极析氧副反应的产生,在酸性条件下,析氧电位较高,析氧发生更困难,从而可以减少对4-硝基酚降解的竞争作用,表现出更高的降解效率。实验表明,这种穿透式光电协同反应器适用于较广的pH范围,在酸性条件下降解效果更好。
-
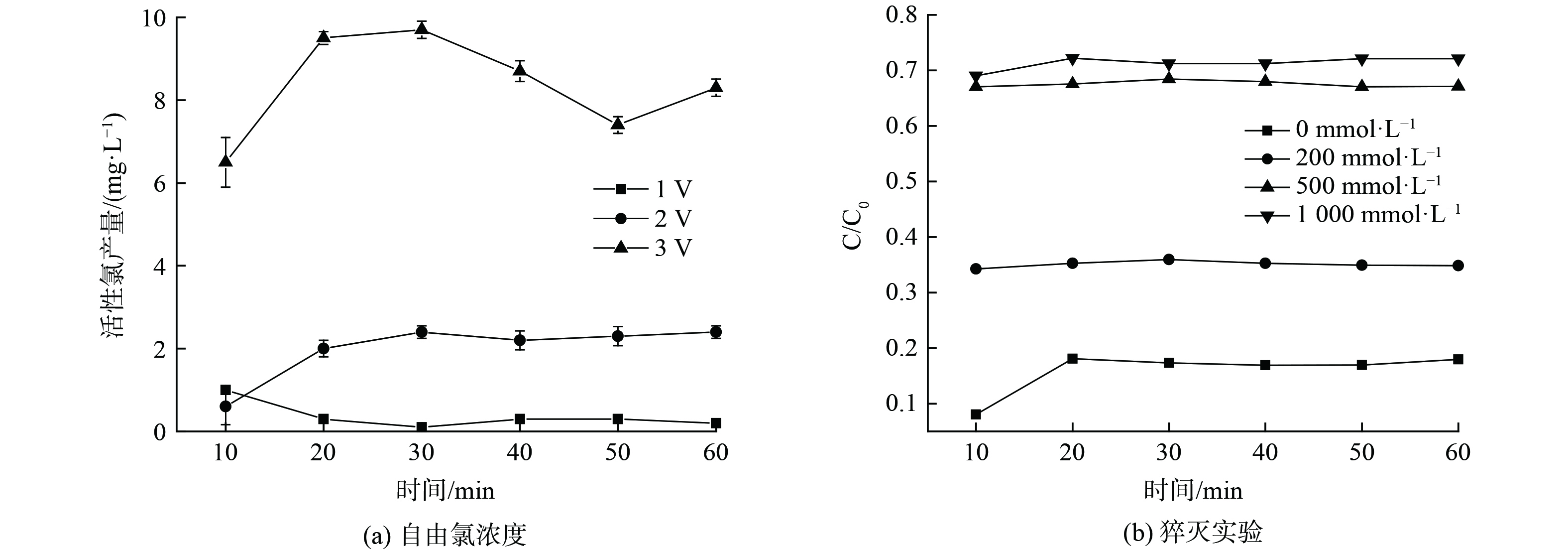
由上述实验发现,脉冲光为光源的光电协同体系对污染物具有更好的降解能力,实验通过DPD法和猝灭实验测定了该体系反应过程中的氯活性物种产生,如图7所示。对于自由氯的测试发现,在低电压下,自由氯产生量较少,大约为2~3 mg·L−1,此时电直接氧化占主导,随着电压的升高,会有更多自由氯的产生,在3 V电压时,自由氯产生量大概为6~10 mg·L−1,促进污染物的降解,随着自由氯浓度的提升,DPD分光光度法测试中的显色反应也更为明显。实验通过猝灭实验研究了氯活性物种对于4-硝基酚的降解贡献,叔丁醇(TBA)被认为可以猝灭体系中的·OH、Cl·、Cl2−和ClO·[22-23]。实验发现,500 mmol L−1的猝灭剂基本可以淬灭体系中的氯活性物质,此时出水的4-硝基酚降解性能下降,约有70%的4-硝基酚未被降解。在脉冲光电协同的体系中,间接氧化反应,会产生大量的活性氯物质(·Cl、ClO−、Cl2),是去除污染物的主要氧化剂[24],进一步在脉冲光的激发下,会生成氯自由基,并通过链式反应生成很多可参与反应的氯活性物种(·ClO、·Cl2−、·ClO2),提升反应速率。通过活性氯和猝灭实验证实在光电脉冲协同体系中,氯活性物种起到了主导作用。
-
实验研究了污染物的矿化情况,如表2所示。有机物的去除率主要是指目标污染物被降解为其他的一些中间产物(包括最终产物CO2和H2O)的比例。有机物完全矿化前,会转变为一些低毒或无毒的小分子,和大量的中间产物。因此有机物的去除率高,并不完全代表目标污染物被完全转化为了CO2和H2O等无机物。矿化效率一般通过总有机碳(TOC)或化学需氧量(CODCr)衡量,本研究中以TOC为指标,衡量4-硝基酚的矿化率。如表2所示,施加不同的电压,脉冲光协同体系均表现出最好的矿化效果。在仅光照的情况下,污染物的降解性能较弱,几乎难以发生矿化,随着电压的提升,矿化效率随着提升,和污染物降解性能提升的趋势相吻合。在1 V电压时,脉冲光电协同系统矿化效率可达到45%,3 V时,矿化效率可达71%,由于脉冲光具有瞬间高强度光能释放的特点,不仅利于污染物的更快速降解,对于促进污染物深度矿化具有更明显的优势。研究认为,4-np的转化路径为4-np首先脱去有色基团亚硝基(-NO2),进而在被·Cl攻击发生亲电取代,在有羟基产生的情况下,·OH继而亲核取代或者消除·Cl,生成领苯二酚和对苯二酚,进而被氧化成苯醌。进一步在溶液中活性氯的作用下,发生开环反应,生成丁烯二酸,最后被完全矿化,生成CO2和H2O[25]。
-
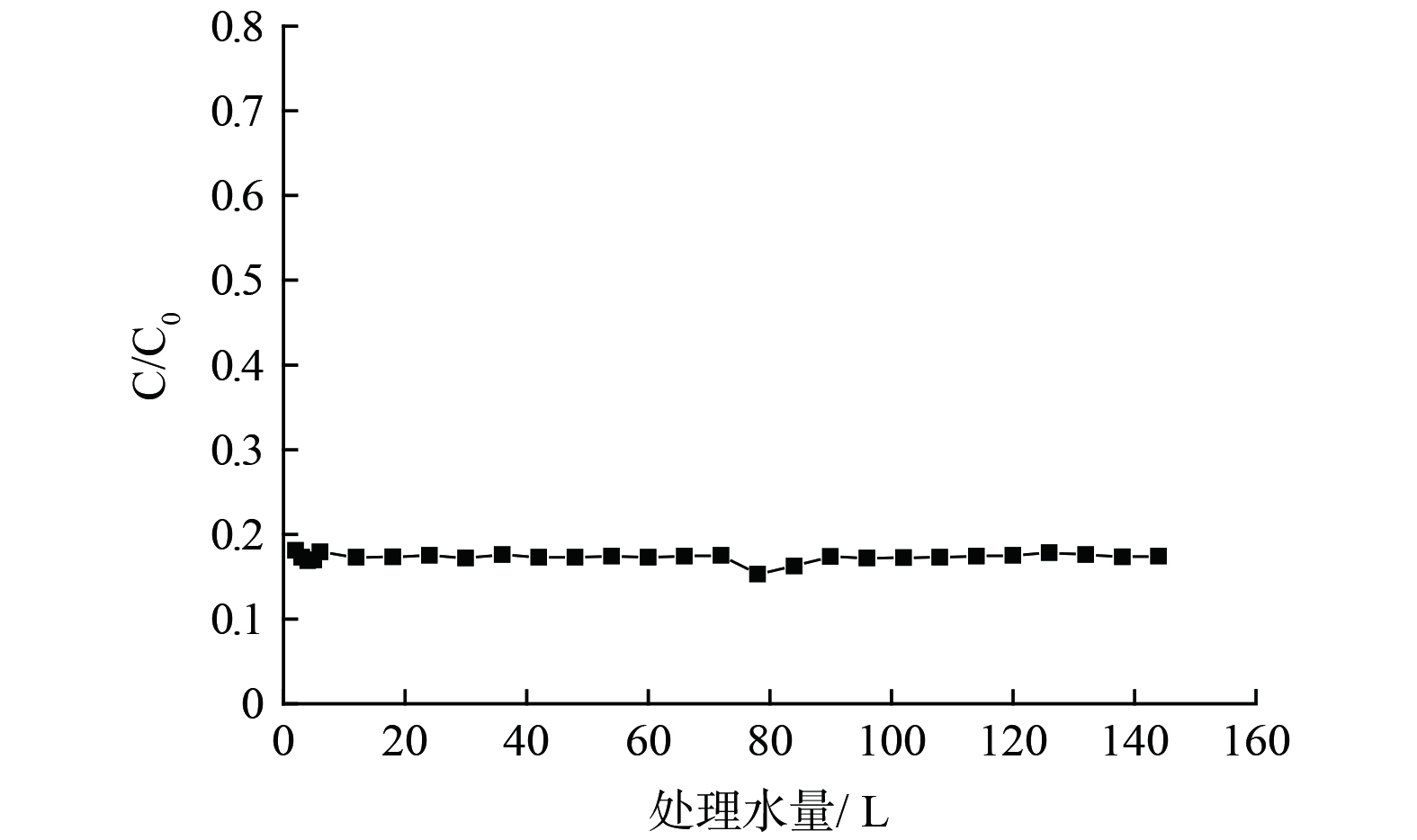
实验对反应器的长期运行稳定性和能耗进行了考察。在最优的反应条件脉冲电压作为光源, 2 V外加电压、50 mmol·L−1氯化钠浓度、19 min的停留时间下以单次穿透进行了连续运行实验。在连续运行48 h,处理水量达144 L的实验中,对污染物的去除效率有轻微波动,但仍能保持在83%以上4-硝基酚降解效率,没有明显的衰减(图8)。同时,出水中的钛和钌离子浓度均在检测线以下,没有明显的溶出,说明该反应器在较长时间的连续运行中有较好的稳定性。本研究体系中总能耗为电能耗和光能耗的总和,该反应体系的运行能耗为3.16 kwh·m−3,以平均电费0.05元·h−1计算,本体系对废水的处理成本约为0.158元·m−3,具有较好的经济性。
-
本研究构建了光电协同穿透式电极反应器,以镀钌泡沫钛作活性阳极,泡沫钛作为阴极,以4-硝基酚作为模型污染物,研究了光电协同穿透式反应器降解污染物的效果,得出的结论如下。
1)光电协同穿透式反应器可实现4-硝基酚的高效降解。在3 V的电压和19~24 min的停留时间下,目标污染物4-硝基酚在单次穿透时即可降解90%以上。
2)溶液的pH、停留时间、外加电压、氯离子浓度都会直接影响污染物的降解效率。在以强脉冲灯(IPL)为光源,2 V外加电压、50 mmol·L−1氯化钠浓度、19 min的停留时间为本研究得到的最优参数。
3)脉冲光电协同对于污染物的降解和深度矿化性能(71%)更优,在污染物降解过程中,氯活性物种占主导作用。该脉冲光电协同体系可实现长时间稳定的连续运行。
脉冲光-电协同去除含盐废水中有机污染物的研究
Removal of organic pollutants from saline wastewater by intense pulsed light (IPL)-electro reactor
-
摘要: 工业废水中本身往往含有大量的氯离子,可以在光电化学催化氧化下形成强氧化性的氯活性物种,达到净水目的。为了改进含盐废水中有机污染物在实际处理中传质效率低、光穿透性差导致的光利用效率低等问题,本研究开发了脉冲光电协同的穿透式电极反应器,并分析了其对有机污染物4-硝基酚的降解性能。研究通过脉冲光源和相同功率的常规紫外光源对比发现,强脉冲光协同电氧化对4-硝基酚的降解效率和矿化效率更高;在3 V电压协同脉冲光源,19~24 min的停留时间下,单次穿透出水可降解90%以上。反应器运行的最佳参数为脉冲光协同2 V电压,50 mmol·L−1的氯化钠浓度和19 min的水力停留时间。溶液的pH、氯离子浓度、停留时间和外加电压都会直接影响4-硝基酚的降解效能。在光电协同下,大量氯活性物质产生,对4-硝基酚降解起到了主导作用。此研究结果为含盐废水中有机污染物的去除提供了新的解决方案。Abstract: Industrial wastewater often contains a large number of chloride ions, which can form strong oxidizing reactive chlorine species (RCS) under photo-electric catalytic process for wastewater purification. In order to improve the shortcomings such as low mass transfer efficiency and poor light penetration in the practical wastewater treatment of saline organic wastewater, this study developed an intense pulsed light coupled with flow-through electrode and analyzed its degradation performance of organic pollutants 4-nitrophenol. By comparing the light source with the conventional ultraviolet light source of the same power, it was found that the degradation efficiency and mineralization efficiency of 4-nitrophenol were higher than that of intense pulse light. Under the 3 V voltage cooperative pulse light source, 19~24 min hydraulic retention time (HRT), 4-nitrophenol removal efficiency could reach up to 90% in single pass The optimum parameters for reactor operation were intense pulsed light with 2 V voltage, 50 mmol·L−1 sodium chloride concentration and HRT of 19 min. The solution pH, chloride ion concentration, HRT and applied voltage could directly affect the degradation efficiency of 4-nitrophenol. Under the photo-electric synergistic effect, reactive chlorine species were greatly produced which played a major role in the degradation of 4-nitrophenol. The results of this study provide a new solution for the removal of organic pollutants in saline wastewater.
-

-
表 1 不同流量对应的水力停留时间(HRT)
Table 1. Summary of HRT in different flow rates
编号 流量/(mL·min−1) 水力停留时间/min 1 200 9.5 2 100 19 3 80 24 4 50 38 表 2 不同光电处理的TOC去除率
Table 2. Summary of TOC removal efficiency under different photo-electric condition
处理/电压 0 V 1 V 2 V 3 V 仅加电 1% 9% 15% 27% 紫外光+电压 2% 34% 59% 68% 脉冲光+电压 3% 45% 65% 71% -
[1] 曲久辉, 刘会娟. 水处理科学与技术: 水处理电化学原理与技术[M]. 北京: 北京科学出版社, 2007. [2] CHIANG L C, CHANG J E, WEN T C. Indirect oxidation effect in electrochemical oxidation treatment of landfill leachate[J]. Water Research, 1995, 29(2): 671-678. doi: 10.1016/0043-1354(94)00146-X [3] COMNINELLIS C, NERINI A. Anodic oxidation of phenol in the presence of NaCl for wastewater treatment[J]. Journal of Applied Electrochemistry, 1995, 25(1): 23-28. [4] RIBORDY P, PULGARIN C, KIWI J, et al. Electrochemical versus photochemical pretreatment of industrial wastewaters[J]. Water Science Techonology, 1997, 35(4): 293-302. doi: 10.2166/wst.1997.0141 [5] YUAN J, LI Y, CHEN X, et al. One electron oxidation-induced degradation of brominated flame retardants in electroactive membrane filtration system: Vital role of dichlorine radical-mediated process[J]. Journal of Hazardous Materials, 2024, 471: 134318. doi: 10.1016/j.jhazmat.2024.134318 [6] WANG Z W, ALMATRAFI E, WANG H, et al. Cobalt single atoms anchored on oxygen-doped tubular carbon nitride for efficient peroxymonosulfate activation: simultaneous coordination structure and morphology modulation[J]. Angewandte Chemie International Edition, 2022, 61(20): 202202338. [7] YANG S Q, LIU Z Q, CUI Y H, et al. Organics abatement and recovery from wastewater by a polymerization-based electrochemically assisted persulfate process: Promotion effect of chloride ion and its mechanism[J]. Journal of Hazardous Materials, 2023, 446: 130658. doi: 10.1016/j.jhazmat.2022.130658 [8] ZHOU Y J, JI Q H, LIU H J, et al. Pore structure-dependent mass transport in flow-through electrodes for water remediation[J]. Environment Science & Technology, 2018, 52(13): 7477-7485. [9] WANG S L, PEI S Z, ZHANG J N, et al. Flow-through electrochemical removal of benzotriazole by electroactive ceramic membrane[J]. Water Research, 2022, 218: 118454. doi: 10.1016/j.watres.2022.118454 [10] HAKIZIMANA I, ZHAO X, WANG C, et al. Efficient multi-stage electrochemical flow-through system for refractory organic pollutant treatment: Kinetics, mass transfer, and thermodynamic analysis[J]. Chemosphere, 2023, 344: 140405. doi: 10.1016/j.chemosphere.2023.140405 [11] WANG L L, WANG L, SHI Y W, et al. Blue TiO2 nanotube electrocatalytic membrane electrode for efficient electrochemical degradation of organic pollutants[J]. Chemosphere, 2022, 306: 135628. doi: 10.1016/j.chemosphere.2022.135628 [12] 李曈. 光化学反应中光生电子及共生自由基的调控与利用研究[D]. 北京: 中国科学院大学, 2018. [13] NATHALIE E G L, PHEBE H V L, JOHAN T P, et al. 20-fold increased limiting currents in oxygen reduction with Cu-tmpa by replacing flow-by with flow-through electrodes[J]. ACS Sustainable Chemistry & Engineering, 2024, 12: 12909-12918. [14] 刘春前. 稀土La掺杂Ti/Sb-SnO2电极电催化氧化对硝基苯酚[D]. 杭州: 浙江工业大学, 2010. [15] LIU H, VECITIS C D. Reactive transport mechanism for organic oxidation during electrochemical filtration: mass-transfer, physical adsorption, and electron-transfer[J]. The Journal of Physical Chemistry C, 2012, 116(1): 374-383. doi: 10.1021/jp209390b [16] WANG Y T, XUE Y D, ZHANG C H. Generation and application of reactive chlorine species by electrochemical process combined with UV irradiation: Synergistic mechanism for enhanced degradation performance[J]. Science of the Total Environment, 2020, 712: 136501. doi: 10.1016/j.scitotenv.2020.136501 [17] ZHANG Y, TANG W J, BAI JING, et al. Highly efficient removal of total nitrogen and dissolved organic compound in waste reverse osmosis concentrate mediated by chlorine radical on 3D Co3O4 nanowires anode[J]. Journal of Hazardous Materials, 2022, 424: 127662. doi: 10.1016/j.jhazmat.2021.127662 [18] XIANG Y Y, FANG J Y, SHANG C. Kinetics and pathways of ibuprofen degradation by the UV/chlorine advanced oxidation process[J]. Water Research, 2015, 90: 301-308. [19] YANG Y, JIEUM S, JUSTIN T J, et al. Multilayer heterojunction anodes for saline wastewater treatment: design strategies and reactive species generation mechanisms[J]. Environmental Science & Technology, 2016, 50(16): 8780-8787. [20] ZHANG J, ZHOU Y Y, YAO B, et al. Current progress in electrochemical anodic-oxidation of pharmaceuticals: Mechanisms, influencing factors, and new technique[J]. Journal of Hazardous Materials, 2021(418): 126313. [21] LI T, JIAGN Y, AN X Q, et al. Transformation of humic acid and halogenated byproduct formation in UV-chlorine processes[J]. Water Research, 2016, 102(10): 421-427. [22] WANG Z Y, LI K L, GUO J J, et al. Elimination of pesticide from high salinity wastewater by electrochlorination process: Active chlorine species and scale-up performance[J]. Separation and Purification Technology, 2023, 306: 122572. doi: 10.1016/j.seppur.2022.122572 [23] PAN Y H, CHENG S S, YANG X, et al. UV/chlorine treatment of carbamazepine: Transformation products and their formation kinetics[J]. Water Research, 2017, 116: 254-265. doi: 10.1016/j.watres.2017.03.033 [24] YANG Z C, QIAN J S, SHAN C, et al. Toward selective oxidation of contaminants in aqueous systems[J]. Environment Science & Technology, 2021(55): 14494-14514. [25] MARIE D, URS V G. Reactions of chlorine with inorganic and organic compounds during water treatment-kinetics and mechanisms: A critical review[J]. Water Research, 2008, 42: 13-51. doi: 10.1016/j.watres.2007.07.025 -



 下载:
下载: