-
随着工业化程度的提高,哮喘、过敏性鼻炎、湿疹等过敏性疾病在全世界范围内呈逐年增高的趋势[1-2],世界卫生组织(WHO)已经把过敏性疾病列为“21世纪重点研究和预防的疾病”。目前全球已有大量研究证实了尘螨与过敏性哮喘、过敏性鼻炎、湿疹等过敏性疾病密切相关[3-4]。尘螨在全世界各个国家都有分布,全世界范围内最为常见的尘螨种类是屋尘螨(Dermatophagoides pteronyssinus)和粉尘螨(Dermatophagoides farinae)[5]。尘螨中的某些蛋白质被认为是导致过敏的主要成分。免疫学研究证明,I类过敏原蛋白是引发尘螨过敏性疾病的主要因素,超过80%的尘螨过敏患者对I类过敏原蛋白(粉尘螨I类过敏原蛋白Der f1 和屋尘螨I类过敏原蛋白 Der p1)的皮肤针刺试验和血清IgE检测呈阳性[6].
有研究表明,O3浓度水平的升高和NOx的存在会引起过敏原蛋白的硝化,从而提高过敏原蛋白的致敏性[7-8],使得人体罹患过敏性疾病的风险增加。蛋白质的硝化主要是指蛋白质中酪氨酸残基被硝化成3-硝基酪氨酸(3-nitrotyrosine,3-NT)的过程。空气污染是当前我国面临的主要环境问题之一。尽管经过近几年的强力治理,PM10、PM2.5、SO2等典型大气污染物已经得到初步的控制,但O3的浓度却在逐年升高[9],这使得过敏原蛋白被硝化的可能性大大增强,给人们的健康增添极大的隐患。因此,环境中过敏原蛋白和硝化过敏原蛋白的存在及含量状况亟需得到大家的重视。
目前最常使用的检测过敏原的分析方法是基于抗体的酶联免疫吸附测定(ELISA)方法和基于DNA的聚合酶链式反应(PCR)方法。ELISA方法灵敏度高,检测时间短[10],但目前市面上大部分试剂盒都是针对单一过敏原设计的,无法对多种过敏原同时进行检测,检测通量较低,并可能存在结构类似物的交叉反应[11];PCR方法虽然可以实现多种目标物同步检测,但它通过测定RNA来间接定量致敏蛋白,易受过敏原蛋白质的浓度、物种、生长条件和DNA水平等限制[12],且容易出现假阳性结果。两种方法都难以适用于当今环境中过敏原的高通量及痕量检测[13]。酶联免疫吸附法(ELISA)也可以用于硝化蛋白质的测定,但ELISA方法以硝化牛血清蛋白为对象制作标准曲线,而所检测的样品中硝化蛋白与抗体的结合能力可能与硝化牛血清蛋白不同,因此ELISA方法只是半定量检测硝化蛋白的方法[14],而且抗体也并非目标硝化蛋白质的特应性抗体。
相比于PCR和ELISA检测,高效液相色谱-质谱联用技术(HPLC-MS/MS)利用测序级胰蛋白酶将目标蛋白酶切成相对分子质量较小的多肽混合物,利用一级质谱(MS)或串联质谱(MS/MS)技术检测多肽混合物中各多肽的相对分子质量或碎片离子信息,找到响应好且能够特异性代替目标蛋白的目标多肽。在质谱多反应监测模式(MRM)下,只对目标多肽进行定量分析,从而反算目标蛋白质的含量。高效液相色谱-质谱联用技术不仅能直接对目标过敏原进行鉴定,还可以同时分析不同亚型和修饰状况,方法的选择性、准确度和通量均有很大提高,目前已被广泛应用于食物过敏原蛋白质的研究中[15]。但目前对于利用HPLC-MS/MS检测环境样品中的尘螨过敏原蛋白质及其硝化产物的研究还鲜见报道。
本研究利用高效液相色谱-质谱联用技术,选择尘螨主要过敏原蛋白Der f 1和Der p 1及其硝化产物nitrated Der f 1和nitrated Der p 1为研究对象,建立能够同时测定环境中两种尘螨主要过敏原蛋白含量及其硝化产物的定量检测方法。并应用该方法检测环境样本中两种尘螨过敏原蛋白及其硝化产物,通过定量检测环境中的尘螨过敏原蛋白的含量水平为进一步揭示环境中尘螨过敏性疾病的健康风险以及有效预防和避免尘螨过敏提供可靠依据。
全文HTML
-
超高效液相色谱-电喷雾电离-三重四极杆串联质谱仪(UPLC/ESI-MS/MS,Xevo TQ-S;Waters,美国);色谱柱Waters BEH C18柱(2.1 mm × 50 mm × 1.7 µm);保护柱VanGuardTM(C18柱,2.1 mm × 5 mm × 1.7 µm);可见分光光度计(HACH DR3900,美国);高速离心机(Centrifuge 5417R, Eppendorf,德国);真空离心浓缩仪(RVC 2-18, Christ,德国);DHZ-D全温振荡培养箱;LoBind低蛋白吸附管(Eppendorf,德国);QL-901涡旋振荡器(Waters,美国);电子天平(220 g / 0.1 mg,ME204, Mettler Toledo,瑞士);所有实验用水由Milli-Q纯水仪(Millipore,美国)制得。
Der f 1蛋白标准品(Recombinant Protein,纯度95%),Der p 1蛋白标准品(Recombinant Protein,纯度95%)购自MyBioSource;胰酶(modified trypsin,sequencing grade)购自美国Promega公司;普通多肽和同位素标记多肽由苏州强耀生物科技有限公司(苏州,中国)商业化合成;BCA试剂盒,Tween-20均购自美国Sigma-Aldrich公司;LC-MS级乙腈购自美国Sigma公司。牛血清蛋白(Bovine serum albumin,BSA,Molecular Biology Grade,分析纯)购自生物工程(上海)股份有限公司;二硫苏糖醇(DL-1,4-Dithiothreitol,DTT,分析纯),三-(2-羰基乙基)膦盐酸盐(Tris(2-carboxyethyl)phosphine hydrochloride,TCEP,分析纯),碘代乙酰胺(Iodoacetamide,IAA,分析纯),甲酸(Formic acid,FA,纯度99%)均购自北京J&K科技公司。
-
尘螨过敏原标准蛋白(Der f 1和Der p 1)按照已有的方法进行酶解[16]。取10 µg的标准蛋白溶液于1.5 mL低蛋白吸附管中,加入20 μL乙腈、20 μL 50 m mol·L−1 NH4HCO3缓冲溶液,37 ℃下放置15 min;加入5 μL还原溶液(45 m mol·L−1 DTT和20 m mol·L−1 TCEP 溶剂于50 m mol·L−1 NH4HCO3缓冲液),37 ℃下放置30 min;加入5 µL 100 m mol·L−1 IAA溶液,暗处37 ℃下混匀放置30 min;加入5.5 μL的90 m mol·L−1 DTT储备液猝灭残留的IAA;加入134.5 μL的超纯水;加入5 μL胰酶(20 ng·μL−1,HCl稀释)使得酶/底物为1∶100(W/W)。在37 ℃下孵育24 h后加入2 μL 10%甲酸(1∶100,V/V),涡旋混匀后室温下放置10 min;用真空离心浓缩仪使溶剂蒸发,并用200 μL 5%乙腈重新溶解。随后4 ℃下14000 r·min−1离心30 min,上清液过0.22 μm水系滤膜,滤液转移至含衬管的进样瓶中,−20 ℃下保存待分析。
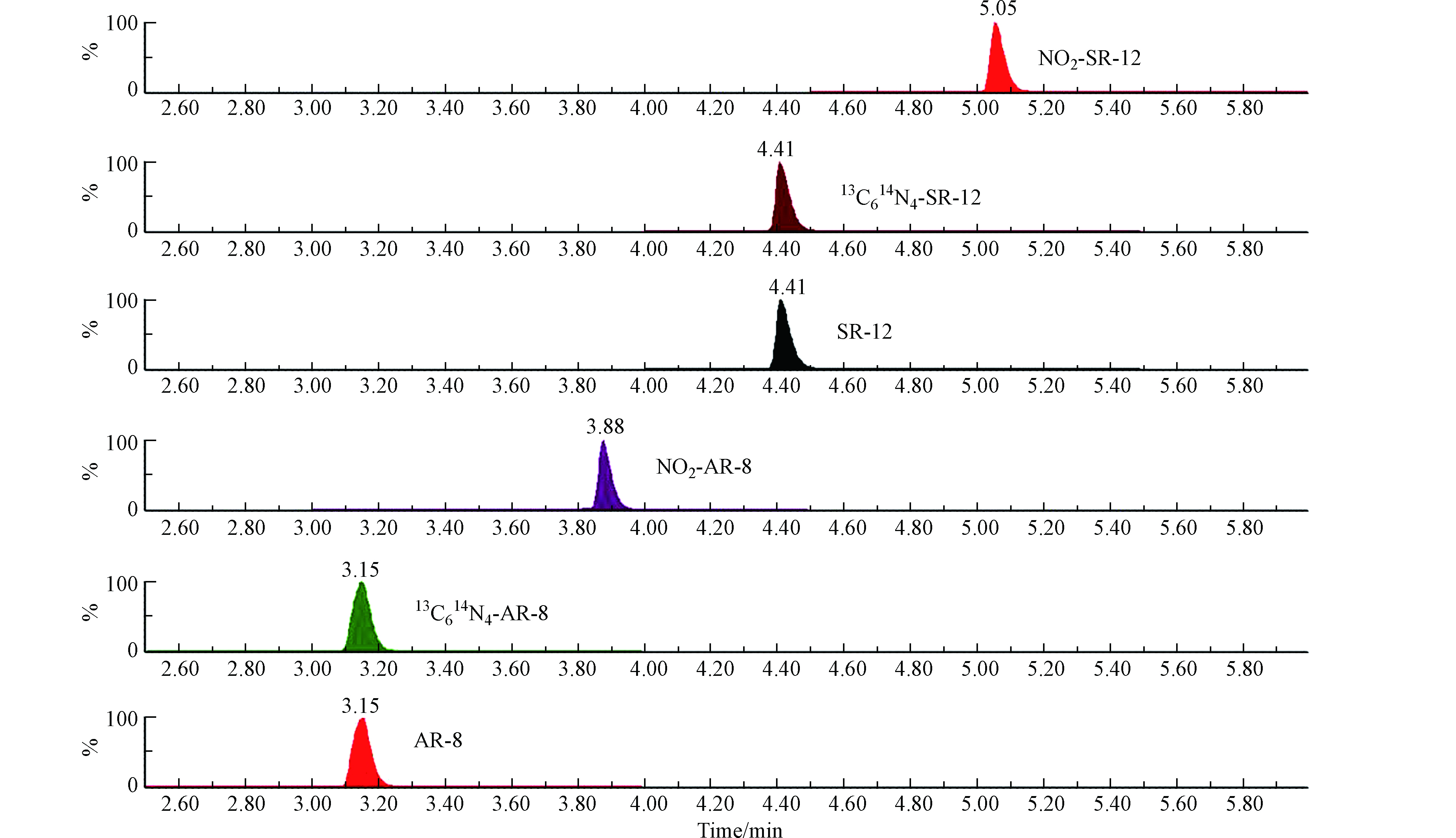
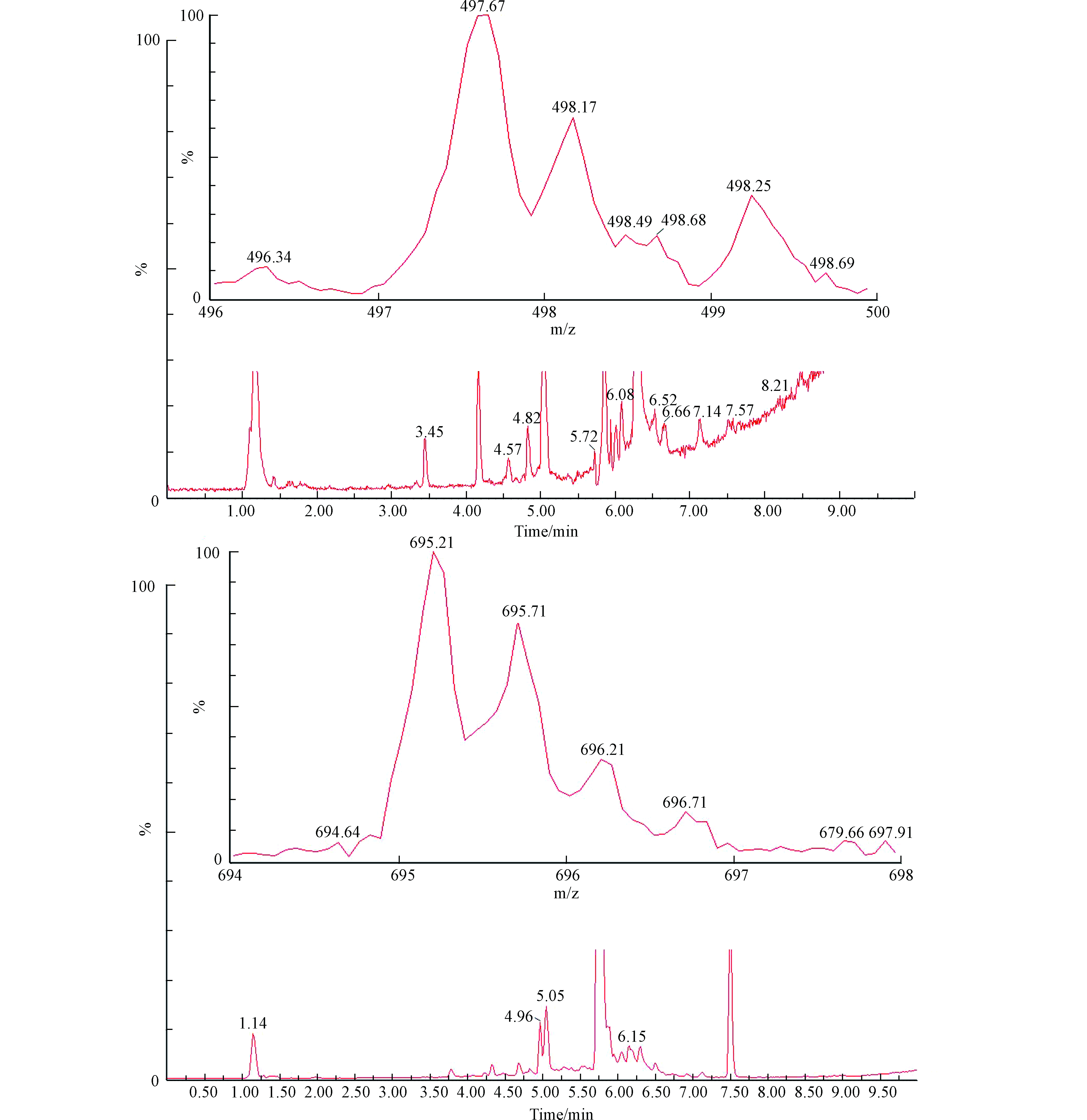
使用UPLC/ESI-MS/MS对尘螨过敏原标准蛋白的酶解液进行分析。采用全扫描模式在m/z 200.0—2000.0的范围内进行扫描,标准蛋白酶解液中丰度最高的多肽离子峰与尘螨过敏原蛋白Der f 1和Der p 1(文本1)胰酶消化的理论肽段对比,最终确定Der f 1的特征多肽AFQHYDGR(AR-8)和Der p 1的特征多肽SYATFEDEEAAR(SR-12)(图1),两条特征多肽中均含有酪氨酸残基。之后商业合成特征多肽(AR-8和SR-12)、同位素标记特征多肽(13C614N4-AR-8和13C614N4-SR-12)和硝化特征多肽(NO2-AR-8和NO2-SR-12)。
-
采集我国东部某城市办公室的办公桌及座位下瓷砖地面上的灰尘样本,由于灰尘分布不均匀,用硬纸板和毛刷小心收拢后用锡箔纸包好装入自封袋带回实验室,用普通筛子先粗略筛去肉眼可见的较大颗粒后,用镊子小心夹取纸屑和毛发等物后弃掉,处理后的灰尘样本在-20 ℃保存。取0.7 g左右灰尘样品,按照1:10(W/V)的比例加入含1%BSA和0.05% Tween-20的磷酸盐缓冲液(1%BSA-PBST)。室温下超声粉碎(200 V)2 h,然后在恒温振荡器中(4 ℃,100 r·min−1)振荡过夜,取上清液在4 ℃,6000 r·min−1条件下离心15 min,离心后取上清液过0.22 μm水系滤膜,−20 ℃下保存备用。
使用BCA蛋白定量试剂盒测定灰尘样品提取液中的总蛋白含量。根据实际测得的灰尘样品中所含的总蛋白质含量,取含400 µg总蛋白的灰尘样品提取液,根据比例按照尘螨过敏原标准蛋白的酶解步骤对样品进行酶解处理,酶/底物选为1∶100(W/W),溶液保存至−20 ℃待分析。
-
使用UPLC/ESI-MS/MS进行分析。柱温设置为40 ℃,进样体积为10 μL,色谱分离的流动相A为0.1%甲酸/乙腈(V/V),B为 0.1%甲酸/水(V/V);流速为0.2 mL·min−1,梯度洗脱的条件为:0 min,5%A;4 min,25%A;5 min,95%A;5.5 min,95%A;6 min,5%A;7 min,5%A。
质谱运行模式为正电离和MRM模式,利用特征多肽(AR-8,SR-12和NO2-AR-8,NO2-SR-12)及其同位素多肽(13C614N4-AR-8和13C614N4-SR-12)的最佳质谱参数对样品中的尘螨过敏原蛋白进行定性定量分析。
-
为验证和评估方法的可靠性,本文对方法检测限、相对回收率和基质效应等参数进行了测定。
仪器检测限(instrument detection limit, IDL):采用EPA[17]推荐的方法计算:浓度为0.1、1、10、100 ng·mL−1的特征多肽标准混合溶液按照每个浓度连续进样5针的规则,计算仪器响应的平均值(mean peak area,M)和相对标准偏差(standard deviation,SD),代入公式(1)计算。
方法检测限(method detection limit,MDL);对于多肽(AR-8,NO2-AR-8,SR-12,NO2-SR-12)将仪器检测限IDL和相对回收率Rr代入公式(2)计算获得MDL。对于过敏原蛋白(Der f1,Nitrated Der f1,Der p1,Nitrated Der p1),MDL由仪器检测限IDL,酶解效率 η 、回收率 Rr以及相对分子质量之比Mr代入公式(3)计算获得。
相对回收率(Rr)的测定:20 μL灰尘样品提取液中加入200 μL浓度为5 ng·mL−1和50 ng·mL−1的特征多肽标准混合溶液,按照“1.2”节的步骤进行前处理,真空离心浓缩至近干后,用200 μL 5%乙腈溶液复溶,仪器响应值记为S2;20 μL的灰尘样品提取液按照“1.2”的步骤进行前处理,真空离心浓缩至近干后,用200 μL 5%乙腈溶液复溶,仪器响应值记为S1;S2-S1的数值代入基质匹配标准曲线得到浓度C1后代入公式(4)计算获得。
基质效应(ME)的测定:20 μL的灰尘样品提取液按照“1.2”的步骤进行前处理,真空离心浓缩至近干后,加入200 μL浓度为5、50 ng·mL−1的标准多肽混合溶液进行复溶,仪器响应值记为S3; 不加样品且不加入胰酶情况下按照“1.2”剩余步骤进行前处理,真空离心浓缩至近干后,加入200 μL浓度为5、50 ng·mL−1的标准多肽混合溶液进行复溶,仪器响应值记为S4,代入公式(5)计算获得。
基质匹配标准曲线:20 μL的灰尘样品提取液按照“1.2”的步骤进行前处理,真空离心浓缩至近干后,加入200 μL浓度为0.1、0.5、1、5、10、50、100 ng·mL−1的标准多肽混合溶液进行复溶,仪器响应值记为S5;以横坐标为浓度值,纵坐标为仪器响应值(S5—S1)作标准曲线。
其中,C表示相对应的标准溶液浓度,此实验中为5 ng·mL−1和50 ng·mL−1;a1—a5为连续测定5次同一浓度标准溶液的5个峰面积值。
-
由于两种过敏原蛋白Der f 1 和Der p 1均只找到一条特征多肽,且该特征多肽上仅有一个酪氨酸残基,因此,以此特征多肽上的酪氨酸硝化率指代过敏原蛋白的硝化率NR,代入公式(6)计算获得。
其中,Mb和Ma表示硝化多肽和原型多肽的质量,ng;Mrb和Mra表示硝化多肽和原型多肽的相对分子质量。
-
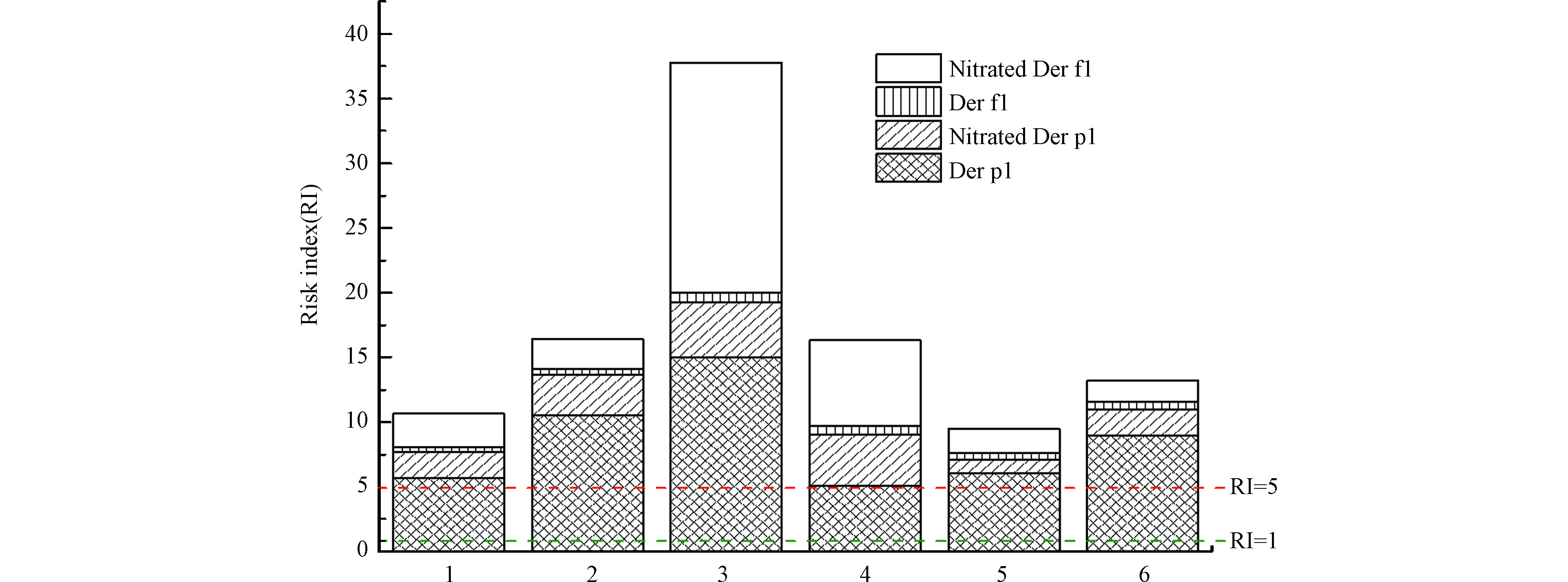
1988年世界卫生组织(WHO)召开的尘螨与哮喘国际研讨会制定了暂行的评价标准[18]:Der p 1含量超过2 µg·g−1足以引起过敏症状,是致敏和哮喘发生的危险因素,Der p 1含量超过10 µg·g−1则足以诱发对尘螨过敏的哮喘病人急性发作或更重的临床病症。为了直观表示尘螨过敏原蛋白的健康风险,我们根据尘螨过敏原蛋白的浓度和WHO建议的风险阈值,计算了各样品的健康风险,并定义了一个风险指数(Risk Index,RI),根据此数值表征尘螨过敏原蛋白的健康风险。
当RI<1时,该环境处于低风险水平,当1≤RI<5时,该环境处于中等风险水平,当RI≥5时,该环境处于高风险水平。RI为1和5时分别对应WHO建议的风险阈值2 µg·g−1和10 µg·g−1。
1.1. 实验材料
1.2. 尘螨过敏原蛋白特征多肽的选择
1.3. 样品采集与前处理
1.4. 仪器分析条件
1.5. 质量控制
1.6. 尘螨过敏原蛋白特征多肽上酪氨酸的硝化率
1.7. 健康风险评价
-
图2是按仪器分析条件得到的100 ng·mL−1的4种特征多肽及2种同位素多肽标准溶液的总离子流色谱图。表1是仪器分析条件下这4种特征多肽及2种同位素内标的反应离子对、保留时间、锥孔电压、碰撞能量和对应内标物等质谱参数。
-
方法学评价中各参数的结果如表2所示,多肽的基质效应为17.3%—45.5%,相对回收率为43%—80%,多肽的方法检测限为0.31—1.75 ng·g−1,过敏原蛋白的方法检测限为0.33—0.57 µg·g−1。
-
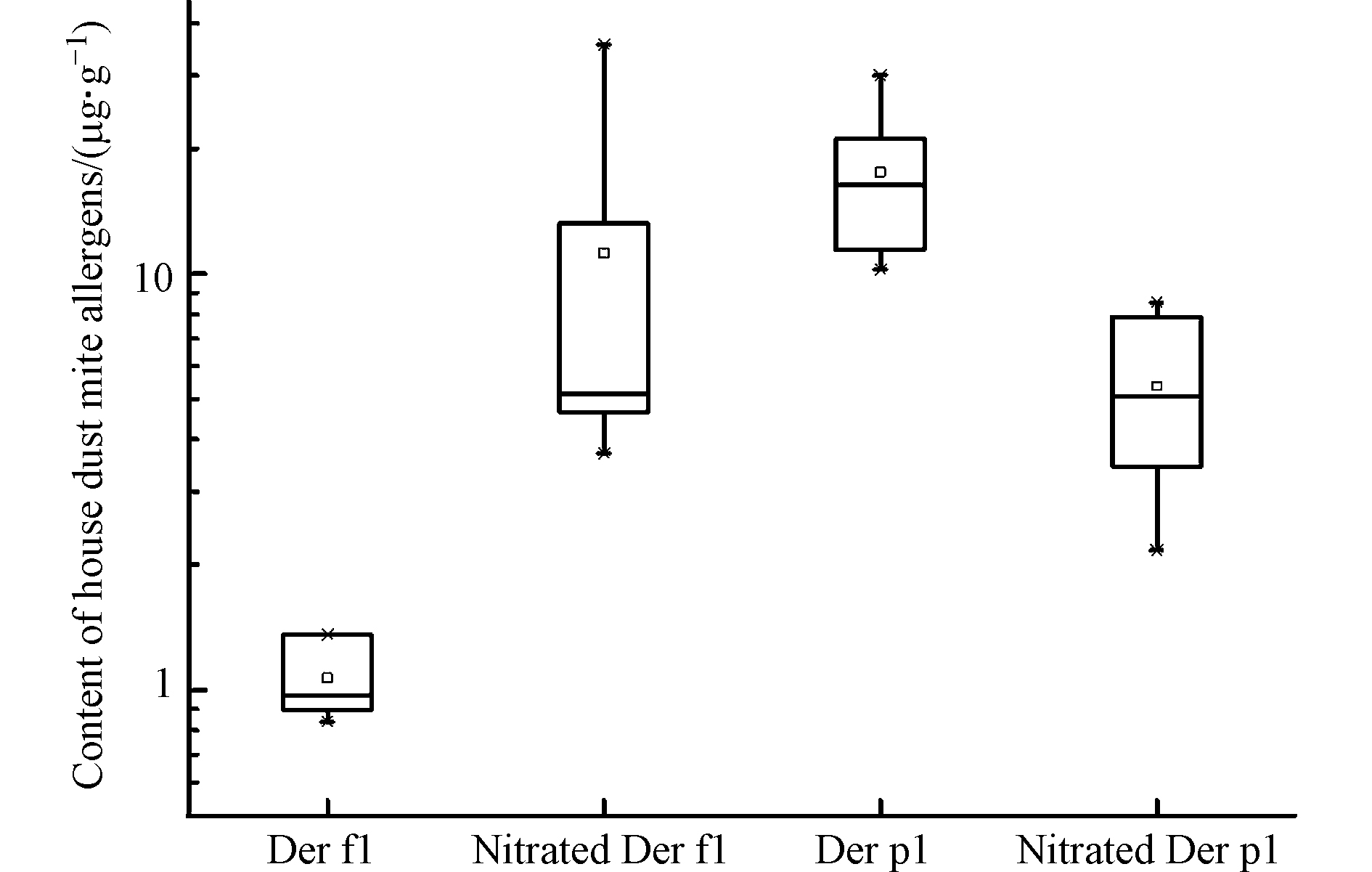
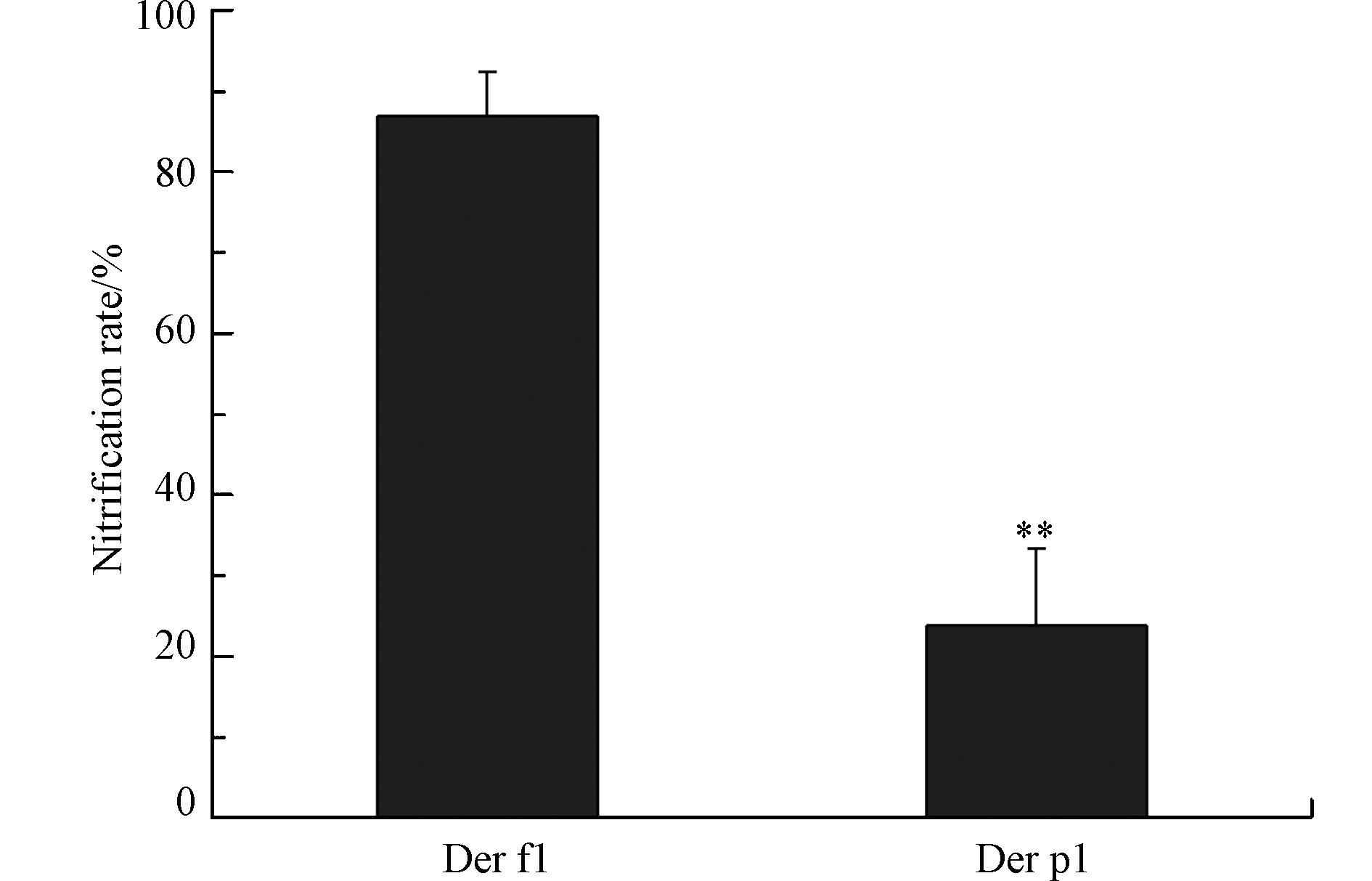
采用本研究开发的基于特征多肽的超高效液相色谱-串联质谱法分析办公室环境样本中的尘螨过敏原蛋白Der f 1,Der p 1及其硝化产物nitrated Der f 1和nitrated Der p 1的含量水平。结果显示,所测6个灰尘样本中Der f 1含量为0.84—1.36 µg·g−1,nitrated Der f 1含量为3.71—35.6 µg·g−1,Der p 1含量为10.3—30.0 µg·g−1,nitrated Der p 1含量为2.16—8.54 µg·g−1(图3)。Der f 1硝化率为80%—96%,Der p 1硝化率为14%—43%(图4)。除此以外,风险评估结果显示所测灰尘样本的风险指数(RI)值为9—38,均处于高风险水平(图5)。
马来西亚办公室灰尘过敏原蛋白含量水平的研究调查显示[19],Der p 1的含量为267—935 ng·g−1,Der f 1的含量为174—1.41×104 ng·g−1,Der f 1的含量会略高于Der p 1,即当地灰尘中粉尘螨数量略多于屋尘螨。本次研究的6个样本中Der f 1含量为0.84—1.36 µg·g−1,Der p 1含量为10.3—30.0 µg·g−1,Der p 1含量高于其他研究报导含量,且Der p 1含量高于Der f 1,这可能与当地环境有关,我国螨类调查研究也显示,在我国东部地区,屋尘螨为优势螨种[20]。目前硝化尘螨过敏原蛋白暂无其他相关报导,从研究结果来看,硝化尘螨过敏原蛋白在环境中的含量与原型尘螨过敏原蛋白含量接近,因此也是人类健康风险的重要威胁。
除此以外,从风险指数上来看,仅Der p 1一种过敏原蛋白的RI值就已达到高风险水平,而已有的研究表明,硝化后的过敏原蛋白其致敏性会增强,导致过敏原蛋白的风险大大增加,另外,由于本次研究只选择了其中一条含有酪氨酸残基的目标多肽进行研究,Der f 1和Der p 1中还有很多含有酪氨酸残基的肽段未进行分析检测,因此,本次研究中硝化过敏原蛋白的硝化效率和健康风险可能会被低估。且由于目前暂无硝化过敏原蛋白的致敏风险的评价标准,以原型过敏原蛋白的致敏风险评价标准进行评估,也可能会导致硝化过敏原蛋白健康风险被低估。因此,实际环境的健康风险可能会高于计算结果。
2.1. LC-MS/MS检测方法
2.2. 方法学评价
2.3. 灰尘样品测定
-
本文建立了一种基于特征多肽的超高效液相色谱-串联质谱分析方法,可同时检测环境中两种尘螨过敏原蛋白及其硝化产物。该方法具有较好的选择性以及高准确度和高分析通量的特点,并已成功应用于实际灰尘样本中尘螨过敏原蛋白及其硝化产物的定性和定量。本方法通过分析实际样品中尘螨过敏原蛋白及其硝化产物的含量水平,有助于揭示环境的健康风险,为今后降低尘螨暴露风险和提出可行性措施打下良好的基础。



 下载:
下载: