-
FeⅢTA纳米复合薄膜,属于金属有机骨架结构材料(metal organic framework, MOF),一般定义为经过自组装方式由配位于单宁酸的铁离子组成的超分子网络结构[1]。在众多MOF材料中,FeⅢTA纳米薄膜具有绿色环保、比表面积高、金属活性位点丰富、循环利用性强、结构多样化、表面易修饰的优点,在光学、生物学、环境学的应用中极具竞争力。其中FeⅢTA纳米薄膜将金属铁离子赋予的特殊性能与单宁酸表面强粘附性结合在一起,在光化学催化、药物运输、疾病诊断治疗,能源存储、废水处理等领域具有广泛的应用前景[2-5]。
传统的MOF材料因自身局限性限制了应用领域,如ZIF系列骨架材料(zeolitie imidazalate framework)制备方法复杂、制备成本相对偏高、适用范围小;CPL系列骨架材(coordiation pillared-layer)循环使用率低、稳定性差且含有毒物质。近年来新型MOF材料FeⅢTA纳米薄膜因对环境友好、比表面积高、制备工艺简单等特点成为研究焦点。但这种研究目前还处于起步阶段。
本文归纳了以单宁酸(Tannic Acid)和铁离子(FeⅢ)作为原材料制备金属有机骨架材料的相关研究。简述了以单宁酸和金属铁离子作为研究对象,FeⅢTA纳米薄膜形成的装配途径和制备方法,以及在生物学和环境领域上FeⅢTA薄膜的具体应用;最后对FeⅢTA薄膜的发展前景进行展望,指出了FeⅢTA薄膜在今后应用中应着重解决的问题。
-
天然材料来源丰富,价格低廉,绿色环保。使用天然化合物的优势在于可以构建各种减轻环境负荷的新材料。其中酚类成分是自然环境中种类最多的重要次生代谢产物,在环境中分布广泛[6]。
单宁酸(一种从植物中提取的多酚,也称之为鞣质、鞣酸)是多元酚类高分子化合物,具有高亲和力,静电相互作用、还原性以及对各种金属离子的强螯合能力,在动植物生长过程中具有促生长作用[7]。选择其为原料主要有以下几个方面:(1)作为一种酚类配体,TA可以与金属离子螯合,其邻近羟基为金属离子提供螯合位点,且TA上的邻苯三酚基团有助于驱动配位交联,从而形成三维稳定的金属多酚网络结构。(2)单宁酸属于天然化合物多酚中的一种,由它作为原材料制备FeⅢTA薄膜可以为制造先进的功能材料提供一种新的绿色路线。(3)多巴胺[7]分子结构中含有的儿茶酚,使其不仅具有粘附在各种材料表面的能力[8],且可以将金属离子还原为金属纳米颗粒[9]。单宁酸分子结构上也存在大量的儿茶酚,但比多巴胺成本低廉。(4)单宁酸分子结构中的邻苯三酚羟基基团具有高亲和力、氢键、疏水相互作用和静电相互作用。(5)单宁酸具有独特的还原性,是一种温和的还原剂。
铁离子广泛存在于自然界且价格低廉,其在化学催化、生物领域以及各种疾病检测和治疗中举足轻重。且FeⅢTA薄膜性质由铁离子决定,允许其控制膜厚度、拆卸特性和荧光行为[10]。
Ejima等[2]首次提出通过TA和FeⅢ之间的配位络合,在多种基底表面包覆多层膜的制备方法,成功涂覆各种平面和颗粒基板并制备出多功能薄膜。国内外一系列研究表明单宁酸和金属铁形成的聚合物是通过邻苯三酚基团与铁离子之间的强螯合作用形成,并且在室温下,聚合反应仍可快速进行[11-12]。
-
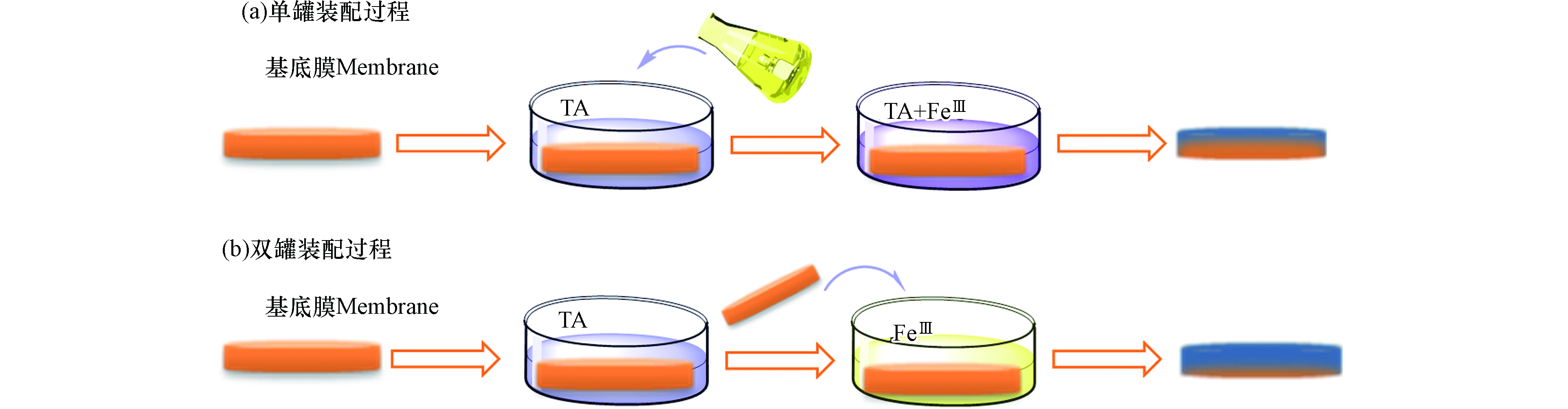
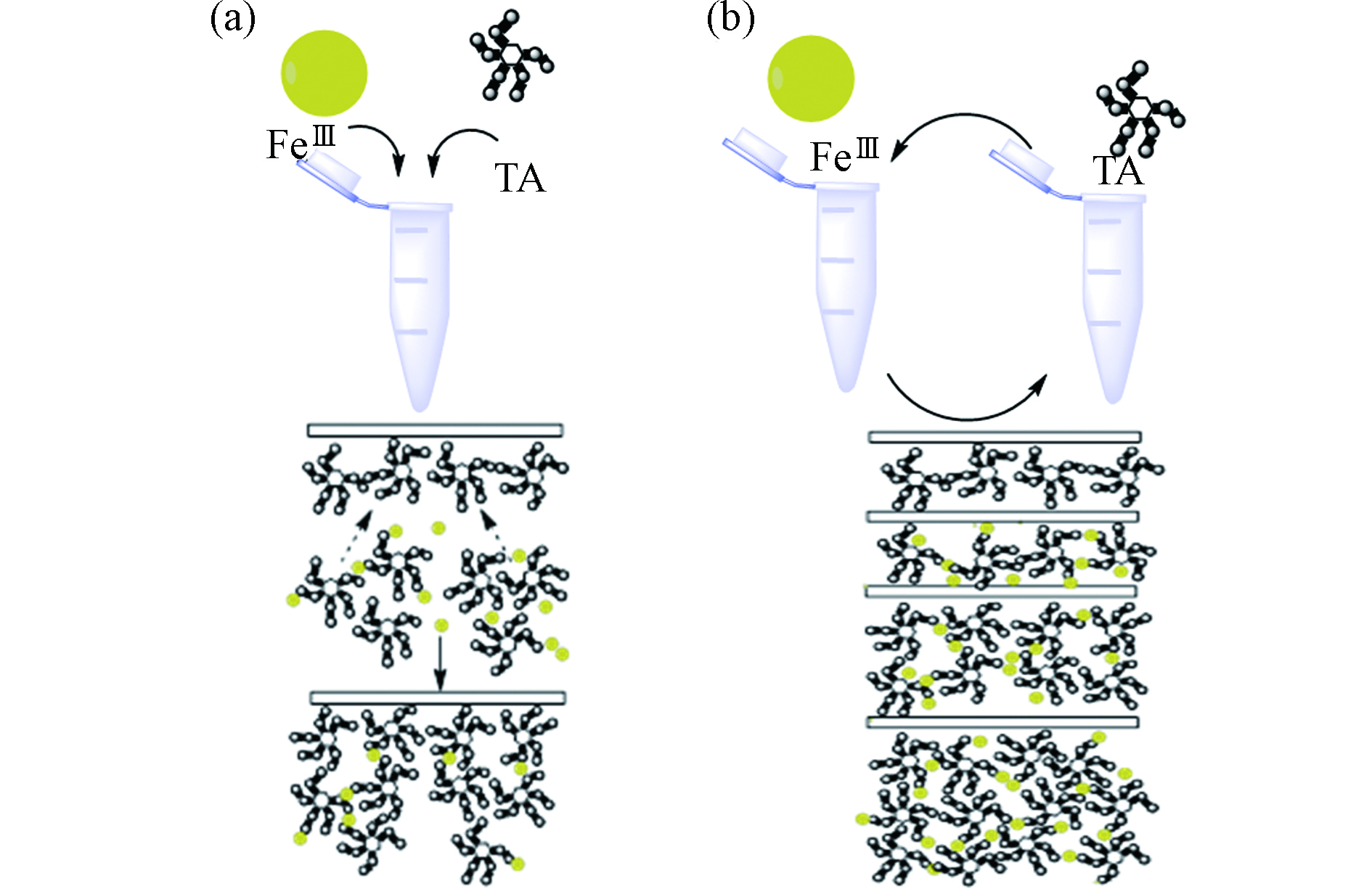
FeⅢTA 自组装途径始于单宁酸分子的吸附作用,由单宁酸和铁离子形成配位键介导,最终在模板表面快速自组装。FeⅢTA薄膜的组装途径一般分为两种: “一步自组装”(图1a)和“多步自组装”(图1b)。一步自组装是将FeⅢ和TA置于同一容器中混合,多步自组装则是将基质交替浸入TA和FeⅢ溶液中,两者都会在基质表面上形成涂层。
-
如图1a所示,将TA和FeⅢ同时加入离心管中,形成的TA-FeⅢ复合物,除在底物上吸附自由的单宁酸之外,还会与基底表面结合,得到厚度为10 nm的膜[13]。傅氏转换红外线光谱分析仪(FT-IR)和Raman光谱[15]确定了FeⅢTA薄膜的形成,X射线光电子能谱显示,与三价铁离子螯合后,TA的HO-C基团结合能升高,说明TA向FeⅢ的转移电子。通过改变TA和FeⅢ的初始浓度值,可以改变薄膜厚度.
-
多步自组装(图1b),底物分别在过量TA和FeⅢ的溶液中反应,获得独特的表面涂层性能[14]。未被吸附的TA或FeⅢ在多次洗涤步骤中得以去除。因此,该方法可以避免在溶液中形成微小的TA-FeⅢ团聚体。通过紫外可见分光光度法和石英晶体微天平(QCM)监测到薄膜的形成。其中,TA中邻苯三酚基团的螯合位点在组装过程中主要被FeⅢ占据,由于底物表面的TA含量远小于溶液中FeⅢ的含量,导致TA螯合位点的FeⅢ含量达到饱和。而对于一步组装来说,TA和FeⅢ同时混合,在溶液中形成小络合物吸附到表面,因此TA的螯合位点未被占据。虽然多步组装法制备的薄膜FeⅢ含量(摩尔分数50%)高于一步组装法制备的FeⅢ含量(摩尔分数25%),但多步组装MPNs的杨氏模量较低[16]。这是由于交联的单宁酸分子的百分比较低,因此在多步组装过程中,三价铁离子的存在有利于薄膜的稳定。
经分析,在络合性质和表面涂层的理化特性(例如渗透性和刚度)方面,一步和多步自组装制备的薄膜差异明显。这些结果为组装机理提供了一些理论基础,即使用相同材料成分,不同的组装途径形成的薄膜具有不同的功能性质,因此实验过程中需要根据实际情况选择特定的组装方法。
-
目前国内外制备FeⅢTA薄膜的方法有很多,不同的制备方法,产出的薄膜性能、形貌、厚度都大不相同。现阶段较常见的FeⅢTA薄膜制备方法主要有在颗粒基质上的成膜、在平面基底上的成膜、球磨方式成膜等[17-18]。
在颗粒基质上成膜是指将单宁酸、三价铁化合物、纳米颗粒混溶于水溶液中,经离心过滤、洗涤、干燥等步骤纯化,使用四氢呋喃溶解颗粒物质得到空心薄膜。成膜后混合物的pH值会有所改变[19]。在平面基底上的成膜与颗粒物质成膜标准规程相同,只是被包裹的物质和处理方式有所差别。相比较于基底成膜,球磨方式作为一种有效稳健的方法制备FeⅢTA薄膜,因无需溶剂、可控薄膜厚度、耗时时间短等特点被广泛应用。Dai等首次使用干燥原料制备可溶性多孔配位膜并通过球磨组件进行调节 [20]。Kaupp[21]将球磨机理描述为3个过程:(1)反应物的扩散[22];(2)产核的形成和生长;(3)生成新的反应物表面[23]。Junk等[24]和Baytekin等 [25]提出:快速剪切力提供足够的能量使化学键断裂产生活性基团。单宁酸活性部分通过摩擦触发,与金属铁离子或含铁氧化物表面结合[26-27] ,且单宁酸中的耦合基团可能会形成低聚物,通过氢键或π-π键堆积相互作用。正是机械和化学效应的共同作用,最终薄膜形成。各种制备方法的优缺点见表1。
-
FeⅢTA薄膜的自组装受pH值影响。大量实验数据表明铁离子与单宁酸分子上的邻苯三酚基团的螯和具有pH依赖性。如图2所示, FeⅢ与TA的配位以及悬浮液的颜色依赖于pH值大小。pH值小于2时,悬浮液呈现无色状态,TA和FeⅢ主要以单齿配体结构存在;pH值在3到6之间(包含3和6),悬浮液颜色呈现蓝色,TA和FeⅢ主要以二齿配体结构存在;pH值大于7时,悬浮液呈红色,TA和 FeⅢ 主要以三齿配体形结构存在。悬浮液颜色变化与三价铁离子和邻苯三酚基团的复合物观察结果一致[28-29]。这归因于TA分子上的邻苯三酚基团与FeⅢ配位键的络合,溶液中游离的TA和小的FeⅢTA复合物吸附在模板表面上,随后通过络合作用与铁离子形成薄膜。但在低pH条件下,单宁酸分子结构中的大多数羟基基团被质子化,形成的质子氢会同铁离子形成竞争关系与单宁酸螯和,导致薄膜不稳定甚至解体。因此铁离子和单宁酸自组装得到的表面薄膜稳定性依赖于pH值[2,30-31]
-
Park [32]等以FeⅢTA薄膜包裹3种不同类型的单个哺乳动物细胞:海拉细胞(HeLa)、小鼠胚胎成纤维细胞(NIH3T3)和急性T细胞白血病细胞(Jurkat)。HeLa、NIH3T3和Jurkat在确保细胞活力的细胞相容性条件下,被FeⅢTA薄膜包裹。FeⅢTA纳米薄膜增强了单个哺乳细胞的结构稳定性,使被包覆的细胞具备抵抗有害应力的能力,能有效地保护哺乳动物细胞免受UV-C照射和有毒化合物侵害。分析表明,细胞增殖是由FeⅢTA纳米外壳程序化形成和降解控制的,细胞生长和增殖过程可被FeⅢTA纳米薄膜暂时抑制,通过可控FeⅢTA纳米薄膜降解得以恢复,模拟了自然界中产孢和萌发过程。
-
FeⅢTA纳米薄膜可用于药物运输[33]。使用FeⅢTA薄膜包裹药物,随着pH值的改变,薄膜会逐渐分解。因此药物可以通过pH值的变化使薄膜分解从而逐渐释放到特定器官, FeⅢ决定薄膜溶解的pH值大小。因为肿瘤的局部pH值比健康组织低,即在肿瘤组织的酸性条件下FeⅢTA薄膜会逐渐降解从而释放出药物,因此FeⅢTA薄膜在抗癌治疗中具有应用潜力。结果表明,FeⅢTA薄膜不仅可以应用于药物运输而且能提高药物载物量,Shen等[31]使用FeⅢTA薄膜覆盖在紫杉醇纳米粒子表面,使得药物载药量大幅度提高。
-
单宁酸和铁离子的超分子金属-有机配合物的抗菌喷雾纳米涂层在受控的方式下可喷涂在水果等商品上。如图3所示,喷涂后的橘子和草莓存储时间延长,这表明FeⅢTA薄膜在易腐产品的可食用涂层方面具有实用潜力。
-
Zheng等[34]用FeⅢTA薄膜包覆聚乙烯亚胺(PEI)和人体抑癌基因(p53基因)形成的复合纳米颗粒。首先,p53质粒与PEI通过静电相互作用,形成PEI/p53复合物, 然后依次在PEI/p53溶液中加入氯化铁和单宁酸,制备FeⅢTA-p53。实验证明FeⅢTA -p53通过铁死亡和凋亡混合途径杀死癌细胞,其中铁死亡在调节细胞死亡中起主导作用。详细的机制研究表明,纳米颗粒能极大地抑制谷胱甘肽合成途径,产生大量的过氧化物脂质,从而导致氧化应激引发铁死亡。且FeⅢTA-p53介导旁观者效应,使细胞对FeⅢTA-p53诱导的铁蛋白作用更加敏感。一项长期的抗癌实验表明,FeⅢTA-p53治疗不仅抑制了肿瘤的生长,而且延长了荷瘤小鼠的寿命。在这一探索下,具有诱导铁坏死能力的纳米材料可能会绕过传统抗肿瘤药物的耐药性,为传统治疗失败后的肿瘤治疗提供新的临床视角。
-
氧化石墨烯(GO)是一种新型的多孔碳纳米材料,具有高比表面积、大量微-介孔结构等优点。由于其表面富含的负电性含氧官能团,GO纳米薄片很容易被FeⅢTA薄膜包覆。涂覆后,GO的Zeta电位从−36 mV变为−44 mV,薄膜包覆的GO在水中仍具有高度分散性和稳定性,易于进一步操作。动态光散射测量显示,包覆后GO水动力直径较小,表明FeⅢTA薄膜的存在减少了GO的聚集。用原子力、扫描电子和透射电子显微镜测量包裹后GO薄片的表面形貌,结果表明,覆盖FeⅢTA薄膜的GO薄片被化学还原,却不会导致包裹的FeⅢTA/ GO纳米骨架结构坍塌。这使得将其放置在微电极阵列上进行电导率测量可应用于超级电容器和电子设备中。
-
FeⅢTA薄膜在废水处理中起着非常重要的作用。基于孔径大小来过滤不同污染物的防污膜已广泛应用废水处理。由于防污膜表面与污染物之间的非特异性相互作用、实际应用条件以及复杂的分离系统,常造成严重的膜污染[35-39]。因此防污膜表面改性成为研究焦点。
Lee等[40]通过单罐组装工艺将FeⅢTA薄膜涂覆在聚醚砜超滤膜表面(图4a), FeⅢTA薄膜具有高亲水性,且具有良好的防污性能(与原始膜相比,蛋白质、油脂和微生物溶液过滤的通量下降50%)。FeⅢTA膜与带负电荷的污染物的相互作用极低,通过原子力显微镜的力曲线未检测到粘附力。
Song等[41]通过双罐组装工艺将FeⅢTA薄膜涂覆在聚丙烯微滤(PPMF)膜表面(图4b),双罐组装形成的FeⅢTA薄膜与TA-FeⅢ配位络合物均匀分布在微滤膜和通道表面,这有利于提高防污膜的超亲水性、高导磁率、膜的水下超疏油性和优异的抗油污性能。
在单罐法组装中,TA和FeⅢ混合时发生络合,TA在溶液中的强金属螯合作用限制了FeⅢ在膜孔中的扩散,因此FeⅢTA配位络合物主要沉积在膜外表面,在膜表面形成TA-FeⅢ复合层,使膜孔径变小,实现表面改性。双罐组装时,TA被预吸附在膜表面和孔表面,随着FeⅢ在膜表面或膜孔中扩散,TA与FeⅢ发生络合。FeⅢTA薄膜沿整个膜骨架涂覆,有利于提高膜的渗透和防污能力。分析表明,膜表面的FeⅢTA配位络合物还可以作为前体或界面层,利用其邻苯三酚基团和儿茶酚基团的多重相互作用,进一步实现防污膜的功能化[42-,44]
FeⅢTA薄膜制备的多功能过滤膜还可去除多种物质[45-46]:FeⅢTA涂覆的聚醚砜膜显示出高通水量以及对油的分离性能,体现出在FeⅢTA薄膜在水净化方面中水油分离的应用潜能[47]。由于邻苯二酚与FeⅢ的高结合亲和力,邻苯二酚涂层基底也可用于环境修复,去除重金属[48]和有机污染物。嵌入了PDA改性纳米颗粒的FeⅢTA薄膜可以用于二氧化碳分离[49]。
-
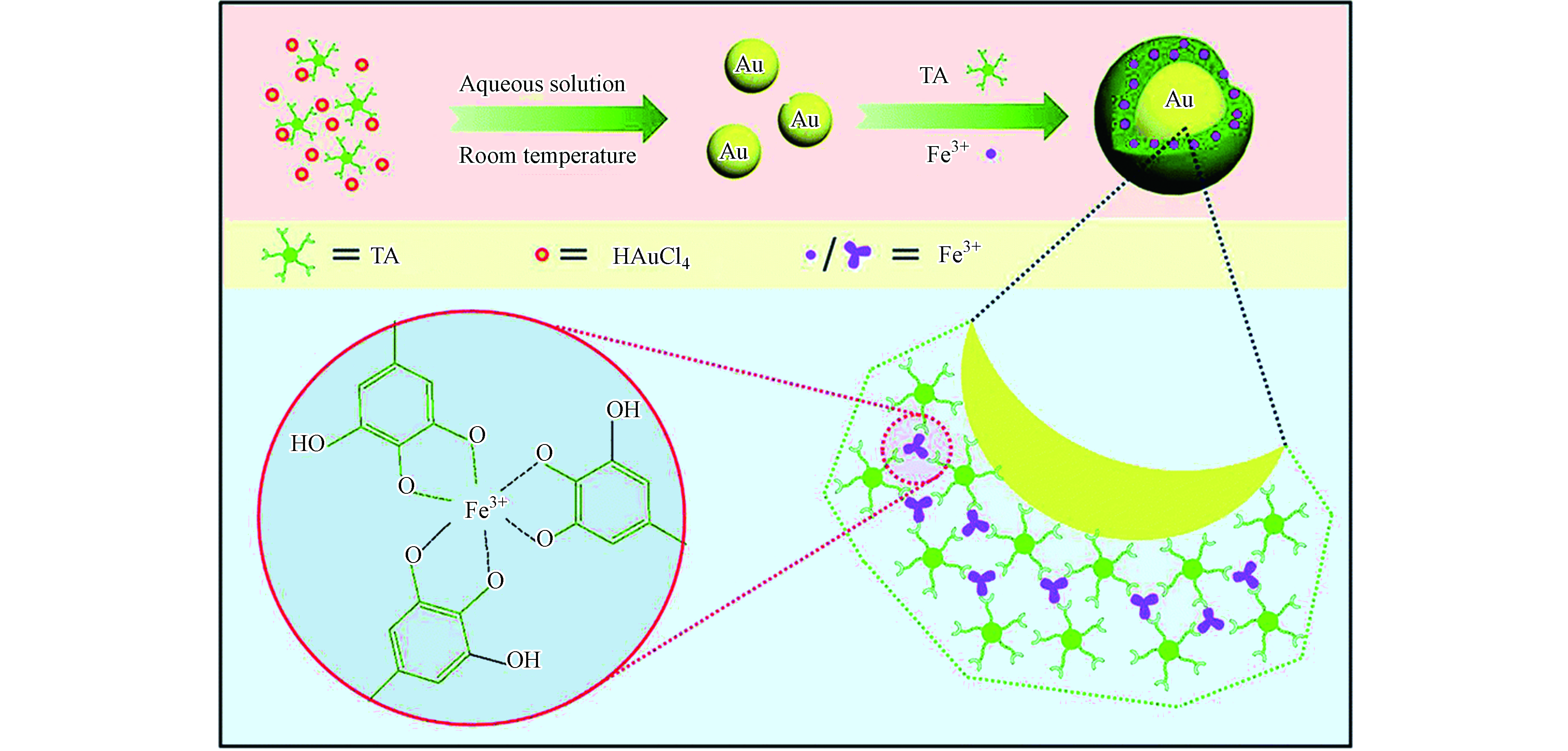
金纳米颗粒因聚集倾向较强导致其失去初始活性的缺点限制了其在催化领域的应用[50-52]。因此有研究者提出以金纳米颗粒作为核的核壳结构观点。研究发现,以金纳米颗粒作为核的核壳结构有以下优点:(a)FeⅢTA薄膜会阻止核与核之间的聚合。(b) FeⅢTA薄膜所具有的独特性能以及薄膜和核之间的交互反应可以实现显著的催化活性。如图5所示,Xu等[9]利用TA对HAuCl4良好的还原能力在室温下形成金纳米颗粒,随后TA和FeⅢ络合在金纳米颗粒表面形成超分子外壳。在这过程中,TA作为有机配体,FeⅢ作为无机交联剂,几个TA分子的邻苯三酚基团螯合一个FeⅢ离子形成稳定的八面体络合物,从而形成交联的FeⅢTA超分子薄膜。再加上TA表面高亲合力,使得该薄膜很容易被涂覆到金纳米颗粒表面上。制备这种催化剂不需要热处理、有机溶剂、特殊仪器和添加剂,这大大降低了成本并防止了可能的污染。与未包覆金纳米颗粒相比,FeⅢTA薄膜包覆的金纳米颗粒催化性能提升,对4-硝基苯酚的降解能力增强,并提高了其可循环利用性。在π-π健的作用下,TA中丰富的芳香环浓缩了对硝基苯酚从而导致局部高浓度的对硝基苯酚, 因此使其具有更高的催化活性。被包覆的金纳米颗粒可以通过离心从反应混合物中分离出来,循环使用率高。TEM图像证实经过多次催化循环后FeⅢTA包覆的金纳米颗粒的形态没有改变。
-
因FeⅢTA薄膜无毒无害,制备简单,材料易获得,在环境领域上会有很大的应用前景。因此对FeⅢTA薄膜还可以从以下几方面深入研究:
(1)被广泛认为是一种全球性环境威胁的纳塑料污染,由于粒径小、密度低,在纳米尺度范围内很难被检测到,却可以通过空气、土壤和水进行迁移。而FeⅢTA薄膜通过吸附和疏水相互作用可以覆盖到纳米塑料颗粒表面,这增加了塑料颗粒之间的空间和静电排斥,从而提供了稳定作用使纳米塑料逐渐聚集,达到去除效果。
(2)过氧化氢和二价铁离子的混合溶液称为芬顿试剂,具有强氧化性,在废水处理中应用普遍。随着芬顿反应的进行,FeII 逐渐转变成 FeⅢ 从而限制了芬顿反应的速率[53],单宁酸的存在可以将FeⅢ还原成芬顿反应活性更高的FeII,提升废水处理效果。将FeⅢTA薄膜同芬顿试剂结合起来用于废水处理能大幅度提升
(3)FeⅢTA薄膜包覆磁性纳米材料可具备双重性能,如包覆磁性三氧化二铁,可具备催化和吸附功能,且复合材料又具有磁性,极易回收重复使用,在废弃染料处理中应用前景广。
从低成本、工艺制备简单、绿色环保、稳定性好、用量少、循环利用等方面考虑,FeⅢTA薄膜无疑成为最具优势之一的新型材料。
单宁酸-铁离子纳米薄膜的合成及应用现状
Synthesis and application of tannic acid - iron ion nano films
-
摘要: 单宁酸-铁离子纳米薄膜(FeIIITA薄膜)是由自然界中分布广泛的铁离子和单宁酸快速自组装形成的新型纳米材料,属于金属有机骨架结构材料(Metal Organic Framework ,MOF)。该类材料具有绿色环保、比表面积高、孔径大、制备过程简单、成本低、金属活性位点丰富、黏附性强等特点。与其他MOF材料相比,FeIIITA薄膜的绿色制备和降解过程使其在生物学、能源与环保领域显现出巨大的应用潜力。本文从FeIIITA薄膜的合成、组装途径、在生物学和环境领域的应用等方面综述了FeIIITA薄膜的研究进展。针对目前FeIIITA薄膜应用的不足提出研究建议,并对其在环境领域的发展趋势进行展望。
-
关键词:
- 单宁酸 /
- 表面涂层 /
- 金属有机骨架结构材料 /
- 纳米薄膜 /
- 环境领域
Abstract: Tannic acid - iron nano films (FeIIITA films) self-assembled of iron ions and tannic acid is a new type of Metal Organic Framework (MOF) materials with high specific surface area, large pore size, simple preparation process, low cost, rich active sites, strong adhesion and so on. Compared with other MOF materials, due to its green environment-friendly preparation and degradation process, FeIIITA thin films have found important applications in the fields of photocatalysis ,biology, environmental protection, and etc. In this article review, we have summarized the research progress of FeIIITA thin films in terms of its synthesis and assembly pathways, as well as its current applications in biological and environmental fields. Based on the current research status, the research suggestions are put forward.-
Key words:
- tannic acid /
- surface coating /
- metal organic framework(MOF) /
- nano films /
- environmental application
-

-
表 1 FeⅢTA薄膜的制备方法对比
Table 1. Comparison of preparation methods of FeⅢTA films
制备方法
Preparation methods缺点
Disadvantages优点
Advantages颗粒基质成膜 耗时长、合成量少 工艺成熟、反应条件温和 平面基底成膜 耗时长、需大量溶剂、原材料单一 无污染、反应条件温和 球磨方式成膜 需高机械能、成本高 无溶剂、产量高、简单快捷 -
[1] DAI Y, CHENG S, WANG Z, et al. Hypochlorous acid promoted platinum drug chemotherapy by myeloperoxidase-encapsulated therapeutic metal phenolic nanoparticles [J]. ACS Nano, 2018, 12(1): 455-463. doi: 10.1021/acsnano.7b06852 [2] EJIMA H, RICHARDSON J J, LIANG K, et al. One-step assembly of coordination complexes for versatile film and particle engineering [J]. Science, 2013, 341(6142): 154-157. doi: 10.1126/science.1237265 [3] CHEETHAM A K, RAO C N R, FELLER R K. Structural diversity and chemical trends in hybrid inorganic-organic framework materials [J]. Chem Commun, 2006, 46: 4780-4795. [4] NGUYEN T T, FURUKAWA H, FELIPE G, et al. Back cover: selective capture of carbon dioxide under humid conditions by hydrophobic chabazite-type zeolitic imidazolate frameworks [J]. Angewandte Chemie International Edition, 2014, 53(40): 10645-10648. doi: 10.1002/anie.201403980 [5] DAS P, YURAN S, YAN J, et al. Sticky tubes and magnetic hydrogels co-assembled by a short peptide and melanin-like nanoparticles [J]. Chem Commun, 2015, 51(25): 5432-5435. doi: 10.1039/C4CC07671K [6] 兰欣, 汪东风, 徐莹, 张旭鹏. 食品中酚类成分及其与其它成分相互作用研究进展[J]. 食品与机械2012, 28(3): 250-254. LAN X, WANG F F, XU Y, ZHANG X P. Advances in studies on phenolic compounds in food and their interactions with other compounds [J]. Food and Machinery 2012, (3): 250-254(in Chinese).
[7] 付伟, 吴子龙, 耿霄, 张浩. 单宁酸生物学功能及其应用前景 [J]. 饲料研究, 2019, 42(11): 108-111. FU W, WU Z L, GENG X, ZHANG H. biological function and application prospect of tannic acid [J]. Feed research, 2019, 42(11): 108-111(in Chinese).
[8] MAIER G P, RAPP M V, WAITE J H, et al. Adaptive synergy between catechol and lysine promotes wet adhesion by surface salt displacement [J]. Science, 2015, 349(6248): 628-632. doi: 10.1126/science.aab0556 [9] XIE Y, YAN B, XU H, et al. Highly Regenerable Mussel-Inspired Fe3O4@Polydopamine-Ag Core-Shell Microspheres as Catalyst and Adsorbent for Methylene Blue Removal [J]. Acs Applied Materials & Interfaces, 2014, 6(11): 8845-8852. [10] GUO J, PING Y, EJIMA H, et al. Engineering multifunctional capsules through the assembly of metal-phenolic networks [J]. Angewandte Chemie, 2014, 53(22): 5546‐5551. [11] GEISLER S, BARRANTES A, TENGVALL P, et al. Deposition kinetics of bioinspired phenolic coatings on titanium surfaces. [J]. Langmuir, 2016, 32(32): 8050-8060. doi: 10.1021/acs.langmuir.6b01959 [12] SHEN Y, DU C, ZHOU J, et al. Application of nano FeIII-tannic acid complexes in modifying aqueous acrylic latex for controlled-release coated urea [J]. Journal of Agricultural & Food Chemistry, 2017, 65(5): 1030-1036. [13] YANG L, HAN L, REN J, et al. Coating process and stability of metal-polyphenol film [J]. Colloids & Surfaces A Physicochemical & Engineering Aspects, 2015, 484: 197-205. [14] PARK J H, KIM K, LEE J, et al. A cytoprotective and degradable metal-polyphenol nanoshell for single-cell encapsulation [J]. Angewandte Chemie, 2014, 126(46): 12628-12633. doi: 10.1002/ange.201405905 [15] OZAWA H, HAGA M A. Soft nano-wrapping on graphene oxide by using metal–organic network films composed of tannic acid and Fe ions [J]. Physical Chemistry Chemical Physics, 2015, 17(14): 8609-8613. doi: 10.1039/C5CP00264H [16] EJIMA H, RICHARDSON J J, CARUSO F, et al. Metal-phenolic networks as a versatile platform to engineer nanomaterials and biointerfaces [J]. Nano Today, 2017: 136-148. [17] SUNGUR S, UZAR A. Investigation of complexes tannic acid and myricetin with Fe(III). [J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2008, 69(1): 225-229. doi: 10.1016/j.saa.2007.03.038 [18] BRAY K, PREVIDI R, GIBSON B C, et al. Enhanced photoluminescence from single nitrogen-vacancy defects in nanodiamonds coated with phenol-ionic complexes [J]. Nanoscale, 2015, 7(11): 4869-4874. doi: 10.1039/C4NR07510B [19] RAHIM M A, KEMPE K, MULLNER M, et al. Surface-confined amorphous films from metal-coordinated simple phenolic ligands [J]. Chemistry of Materials, 2015, 27(16): 5825-5832. doi: 10.1021/acs.chemmater.5b02790 [20] ZHANG P, LI H, VEITH G M, et al. Soluble porous coordination polymers by mechanochemistry:From metal-containing films/membranes to active catalysts for aerobic oxidation [J]. Advanced Materials, 2015, 27(2): 234-239. doi: 10.1002/adma.201403299 [21] KAUPP G. Solid-state molecular syntheses: complete reactions without auxiliaries based on the new solid-state mechanism [J]. CrystEngComm, 2003, 5(23): 117-133. doi: 10.1039/b303432a [22] LEMMERER A, BERNSTEIN J, KAHLENBERG V. Hydrogen bonding patterns of the co-crystal containing the pharmaceutically active ingredient isoniazid and terephthalic acid [J]. Journal of Chemical Crystallography, 2011, 41(7): 991-997. doi: 10.1007/s10870-011-0031-9 [23] FRISCIC T, HALASZ I, BELDON P J, et al. Real-time and in situ monitoring of mechanochemical milling reactions [J]. Nature Chemistry, 2013, 5(1): 66-73. doi: 10.1038/nchem.1505 [24] PITENIS A A, HARRIS K L, JUNK C P, et al. Ultralow wear PTFE and alumina composites: It is all about tribochemistry [J]. Tribology Letters, 2015, 57(1): 3735-3739. [25] BAYTEKIN H T, BAYTEKIN B, HUDA S, et al. Mechanochemical activation and patterning of an adhesive surface toward nanoparticle deposition [J]. Journal of the American Chemical Society, 2015, 137(5): 1726-1729. doi: 10.1021/ja507983x [26] HARRIS K L, PITENIS A A, SAWYER W G, et al. PTFE tribology and the role of mechanochemistry in the development of protective surface films [J]. Macromolecules, 2015, 48(11): 3739-3745. doi: 10.1021/acs.macromol.5b00452 [27] KANG J, BAI G, MA S, et al. On‐Site Surface coordination complexation via mechanochemistry for versatile metal–phenolic networks films[J]. Advanced Materials Interfaces, 2019, 6(5): 1801789. [28] FUJIE T, KAWAMOTO Y, HANIUDA H, et al. Selective molecular permeability induced by glass transition dynamics of semicrystalline polymer ultrathin films [J]. Macromolecules, 2013, 46(2): 395-402. doi: 10.1021/ma302081e [29] HOLTENANDERSEN N, HARRINGTON M J, BIRKEDAL H, et al. pH-induced metal-ligand cross-links inspired by mussel yield self-healing polymer networks with near-covalent elastic moduli [J]. Proceedings of the National Academy of Sciences of the United States of America, 2011, 108(7): 2651-2655. doi: 10.1073/pnas.1015862108 [30] FU Z , CHEN R . Study of Complexes of tannic acid with Fe(III) and Fe(II)[J]. Journal of Analytical Methods in Chemistry, 2019,3: 3894571. [31] SHEN G, XING R, ZHANG N, et al. Interfacial cohesion and assembly of bioadhesive molecules for design of long-term stable hydrophobic nanodrugs toward effective anticancer therapy [J]. ACS Nano, 2016, 10(6): 5720-5729. doi: 10.1021/acsnano.5b07276 [32] HONG D, PARK M, YANG S H, et al. Artificial spores: Cytoprotective nanoencapsulation of living cells [J]. Trends in Biotechnology, 2013, 31(8): 442-447. doi: 10.1016/j.tibtech.2013.05.009 [33] POPESCU M, MOURTAS S, PAMPALAKIS G, et al. pH-responsive hydrogel/liposome soft nanocomposites for tuning drug release [J]. Biomacromolecules, 2011, 12(8): 3023-3030. doi: 10.1021/bm2006483 [34] ZHENG D, LEI Q, ZHU J, et al. Switching apoptosis to ferroptosis: metal-organic network for high-efficiency anticancer therapy. [J]. Nano Letters, 2017, 17(1): 284-291. doi: 10.1021/acs.nanolett.6b04060 [35] ZHU Y, WANG D, JIANG L, et al. Recent progress in developing advanced membranes for emulsified oil/water separation [J]. NPG Asia Materials, 2014, 6(5): e101. doi: 10.1038/am.2014.23 [36] MOHAMMAD A W, TEOW Y H, ANG W L, et al. Nanofiltration membranes review: Recent advances and future prospects [J]. Desalination, 2015, 356: 226-254. doi: 10.1016/j.desal.2014.10.043 [37] MATIN A, KHAN Z, ZAIDI S M, et al. Biofouling in reverse osmosis membranes for seawater desalination: phenomena and prevention [J]. Desalination, 2011, 281(281): 1-16. [38] RANA D, MATSUURA T. Surface modifications for antifouling membranes [J]. Chemical Reviews, 2010, 110(4): 2448-2471. doi: 10.1021/cr800208y [39] YANG Q, MI B. Nanomaterials for membrane fouling control: accomplishments and challenges [J]. Advances in Chronic Kidney Disease, 2013, 20(6): 536-555. doi: 10.1053/j.ackd.2013.08.005 [40] KIM H J, KIM D, YOON H, et al. Polyphenol/FeIII complex coated membranes having multifunctional properties prepared by a one‐step fast assembly [J]. Advanced Materials Interfaces, 2015, 2(14): 1500298. doi: 10.1002/admi.201500298 [41] SONG Y, KONG X, YIN X, et al. Tannin-inspired superhydrophilic and underwater superoleophobic polypropylene membrane for effective oil/water emulsions separation [J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2017, 522: 585-592. doi: 10.1016/j.colsurfa.2017.03.023 [42] WU J, WANG Z, YAN W, et al. Improving the hydrophilicity and fouling resistance of RO membranes by surface immobilization of PVP based on a metal-polyphenol precursor layer [J]. Journal of Membrane Science, 2015, 496: 58-69. doi: 10.1016/j.memsci.2015.08.044 [43] DONG C, WANG Z, WU J, et al. A green strategy to immobilize silver nanoparticles onto reverse osmosis membrane for enhanced anti-biofouling property [J]. Desalination, 2017, 401: 32-41. doi: 10.1016/j.desal.2016.06.034 [44] ZHAO X, ZHANG R, LIU Y, et al. Antifouling membrane surface construction: Chemistry plays a critical role [J]. Journal of Membrane Science, 2018, 551: 145-171. doi: 10.1016/j.memsci.2018.01.039 [45] DING X, ZHANG B, PEI Q, et al. Triptolide induces apoptotic cell death of human cholangiocarcinoma cells through inhibition of myeloid cell leukemia-1 [J]. BMC Cancer, 2014, 14(1): 271. doi: 10.1186/1471-2407-14-271 [46] KIM Y I , YOON T H , LEE S , et al. Integrated optical isolator using multi-mode interference structure.:US10955980[P]. [2005-05-05] [47] YOON H M, KIM Y, LEE J H, et al. Robot-assisted total gastrectomy is comparable with laparoscopically assisted total gastrectomy for early gastric cancer [J]. Surgical Endoscopy and Other Interventional Techniques, 2012, 26(5): 1377-1381. doi: 10.1007/s00464-011-2043-0 [48] TAN Q R, WANG X Z, WANG C Y, et al. Differential effects of classical and atypical antipsychotic drugs on rotenone-induced neurotoxicity in PC12 cells [J]. European Neuropsychopharmacology, 2007, 17(12): 768-773. doi: 10.1016/j.euroneuro.2007.03.003 [49] GURR P A, SCOFIELD J M P, KIM J, et al. Polyimide polydimethylsiloxane triblock copolymers for thin film composite gas separation membranes [J]. Journal of Polymer Science Part A Polymer Chemistry, 2014, 52(23): 3372-3382. doi: 10.1002/pola.27401 [50] BALANTA A, GODARD C, CLAVER C, et al. Pd nanoparticles for C–C coupling reactions [J]. Chemical Society Reviews, 2011, 40(10): 4973-4985. doi: 10.1039/c1cs15195a [51] GARG N, MOHANTY A, LAZARUS N, et al. Robust gold nanoparticles stabilized by trithiol for application in chemiresistive sensors [J]. Nanotechnology, 2010, 49: 4962-4966. [52] XIAO Y, SHLYAHOVSKY B, POPOV I, et al. Shape and color of au nanoparticles follow biocatalytic processes. [J]. Langmuir, 2005, 21(13): 5659-5662. doi: 10.1021/la050308+ [53] BOLOBAJEV J, TRAPIDO M, GOI A. Interaction of tannic acid with ferric iron to assist 2, 4, 6-trichlorophenol catalytic decomposition and reuse of ferric sludge as a source of iron catalyst in Fenton-based treatment [J]. Applied Catalysis B, 2016, 187: 75-82. doi: 10.1016/j.apcatb.2016.01.015 -



 下载:
下载: