-
城市森林生态系统是受人为活动影响较多的森林生态系统,快速的工业化和城市化缩小了城市森林的生存环境[1]。但城市森林是城市生态系统中最重要的组成部分,具有重要的生态服务功能[1-2],例如缓解雨水径流[3]、减小噪音[4]、降低热岛效应[1]和增强城市审美价值[5],另外城市森林可以通过吸附痕量金属缓解局部污染[6]。这些痕量金属污染物中,汞作为一种全球性的污染物,可以通过水生和陆生食物链富集,从而对人体健康造成威胁[7]。汞在大气中有3种不同的形态:气态单质汞(Hg0)、活性气态汞(Hg(II))和颗粒态汞(Hg(p))。其中气态单质汞占总汞的95%,能够进行全球性传输,可以通过大气从城市和工业地区传输并沉降到偏远地区[8-9],因此大气汞的沉降是全球性的环境问题。当地的燃煤、燃烧化石燃料和使用农药都会加剧城市汞污染[10-12]。大气汞沉降到森林生态系统中包括干沉降和湿沉降两种途径[13-14],其中干沉降是大气汞沉降到森林中的主要途径,占总沉降的70%—85%[15]。有研究表明75%左右的干沉降是通过凋落物汞的方式沉降到森林生态系统中[16],因此凋落物是进入森林生态系统土壤的最大汞通量[17]。现有大量研究表明树叶组织中几乎所有的汞来自于大气,并且主要通过气孔吸收大气气态单质汞[18-20],叶片汞浓度和大气汞浓度之间的正相关关系[19,21-22]使叶片凋落物中汞浓度的空间分布一定程度上代表大气汞浓度的空间分布[23]。因此,有必要研究叶片凋落物在大气汞循环中的作用。我国已有一些学者在西南地区的亚热带森林调查过森林汞浓度和汞通量[24-25],但大部分研究主要集中在自然森林生态系统中。目前,我国对城市森林的研究处于起步阶段,对城市森林生态系统中汞浓度和汞通量的研究数据还十分欠缺。
近几十年北京经济持续增长且城市急速扩张,为了调查城市森林凋落物汞分布规律,本研究选取北京城市森林,(1)比较不同树种叶片凋落物中汞浓度;(2)对比北京市公园、街道和居民点的3种不同土地利用区同一种树种叶凋落物汞浓度,对比北京市区和郊区叶凋落物汞浓度差异;(3)量化北京市不同区叶凋落物汞沉降通量,为进一步理解和评估城市森林生态系统对全球汞生物地球化学循环中的作用提供基础支撑。
-
北京(39°56'N,116°20' E)地处中国北部,为暖温带半湿润半干旱季风气候,全年降水80%在夏季,无霜期180—200 d。北京市地带性植被类型是暖温带落叶阔叶林并间有温性针叶林分布。市区里树种单一,受人为活动影响很大。本研究选取了北京市区西北至东南对角线上的公园、街道和居民点的3种土地利用地区,采集了29个采样点上的主要绿化树种的叶片凋落物。具体采样点见图1。
-
2020年10月,在北京市区西北至东南对角线上的公园、街道和居民区每个点采集5个左右主要树种的叶凋落物。采集叶片凋落物的主要绿化树种分别是白蜡(Fraxinus excelsior)、刺槐(Robinia pseudoacacia L)、国槐(Sophora japonica Linn)、银杏(Ginkgo biloba L.)、柳树(Salix matsudana koidz.)、杨树(Populus tomentos)、圆柏(Sabina chinensis(L.)Ant.)和油松(Pinus tabuliformis Carr.)。在每个采样点每个树种选3棵树重复收集树下叶凋落物。收集的叶凋落物装在密封袋中带到实验室.样品带回实验室以后先在65 °C烘箱中烘干。在分析之前,用高速万能粉碎机FW100(公司名称)把样品粉碎供测定分析。
利用直接测汞仪DMA80(Milestone DMA-80,美国)测定叶凋落物样品汞浓度。该仪器使用纳米级金汞齐富集技术,配合高解析速率,充分保证吸收峰型,以获得优异的准确度和精密度,仪器总汞检测限为0.34 ng·g−1。测定过程中的质量控制和质量保证采用随机重复和标准物质测定来控制。利用柑橘叶(GBW10020,(150±20)ng·g−1)进行标准曲线测定,其覆盖样品测定值范围且相关性达0.999。每个样品测两次,且平行样品汞浓度差异<10%,否则重新测量。每6个样品加入1个标准参考物质测量, 保证校正因子F在0.9—1.1区间,所有样品称取0.01—0.1 g最佳。数据以平均值±标准差的形式表示,使用Spss25.0软件进行单因素方差分析(ANOVA),当P<0.05时,表明有显著性差异。
-
北京城市森林平均叶凋落物汞浓度为(35.98±14.90) ng·g−1,高于我国各地郊区落叶阔叶林平均叶凋落物汞浓度(25.80±10.10)ng·g−1,低于我国各地郊区常绿阔叶林的平均叶凋落物汞浓度(50.80±39.40) ng·g−1,这可能与北京的主要绿化树种是落叶阔叶树有关,其叶片生长期短于常绿阔叶林[17]。与美国佛蒙特州和新罕布什尔州郊区树叶汞浓度(35.00±9.40)ng·g−1[26],明尼苏达州市区树叶汞浓度(30.75±10.30)ng·g−1相似[27];高于Obrist等报道的纽约郊区及全美国14个地区树叶平均汞浓度(24.71±11.29)ng·g−1[28]。
北京城市森林生态系统主要绿化树种汞浓度见图2。不同树种叶凋落物之间汞浓度各不相同,单因素方差分析结果显示,不同树种叶片凋落物汞浓度具有显著性差异(P<0.05)。以往的研究表明,针叶树种由于叶片生长期长,比阔叶树种叶片汞浓度高[29-32]。但本研究中发现白蜡叶凋落物中的平均汞浓度(50.14±31.10) ng·g−1在所有调查树种叶凋落物汞浓度中最高,显著高于杨树(14.79±9.29)ng·g−1和油松(12.58±8.69)ng·g−1(P<0.05),这可能与白蜡叶片表面多深沟槽有关[33]。比较叶汞浓度中值发现, 槐树叶汞中值在8个树种中最高,这可能跟槐树叶片被毛能吸收更多的汞有关[33]。值得注意的是,云杉(Picea asperata Mast.)叶凋落物平均汞浓度最高(92.33±104.70)ng·g−1,但本次调查中仅在两个地点(海淀公园和官园公园)采集到云杉(Picea asperata Mast.)叶凋落物,因此不包括在统计分析中。相反,油松叶凋落物平均汞浓度(12.58±8.69) ng·g−1在所有调查树种叶凋落物平均汞浓度中最低,显著低于白蜡(50.14±31.10)ng·g−1、刺槐(47.59±12.05) ng·g−1、国槐(49.88±18.52) ng·g−1、圆柏(39.23±52.29) ng·g−1和银杏(38.63±65.41) ng·g−1(P<0.05)。总体而言,阔叶树种叶片凋落物汞浓度高于针叶树种叶片凋落物汞浓度,这种与美国佛蒙特州[34]、新罕布什尔州[26]和纽约州[35]研究结果一致。因此,除了不同植被对大气汞的吸收有差异以外,不同树种树叶之间的生理差异,比如气孔数量与形状、叶片粗糙度和叶面积指数等会影响叶片对大气汞的吸收[17,26,30]。
已有大量研究报道,叶片中的汞浓度会随着暴露时间的延长而逐渐增加[19,27,36-37]。但叶片中的汞浓度不仅随季节变化,还随不同年份变化[35-37]。本文与牛振川等[17]报道的十年前北京城市地区主要绿化树种叶凋落物中汞浓度相比,除银杏和槐树没有显著性差异(P>0.05)以外,近十年杨树和油松叶凋落物中汞浓度显著下降(P<0.05),这与北京市区大气汞浓度逐年降低有关,从2002年的7.9—34.9 ng·m−3 [38] 到2015年的4.61 ng·m−3,再到2018年的2.72 ng·m−3[39]。在全球汞观测中,中国观测到的大气汞下降趋势是最显著的[40-42],这就意味着有必要重新评估当前大气汞浓度下森林植被在汞循环中的作用。
-
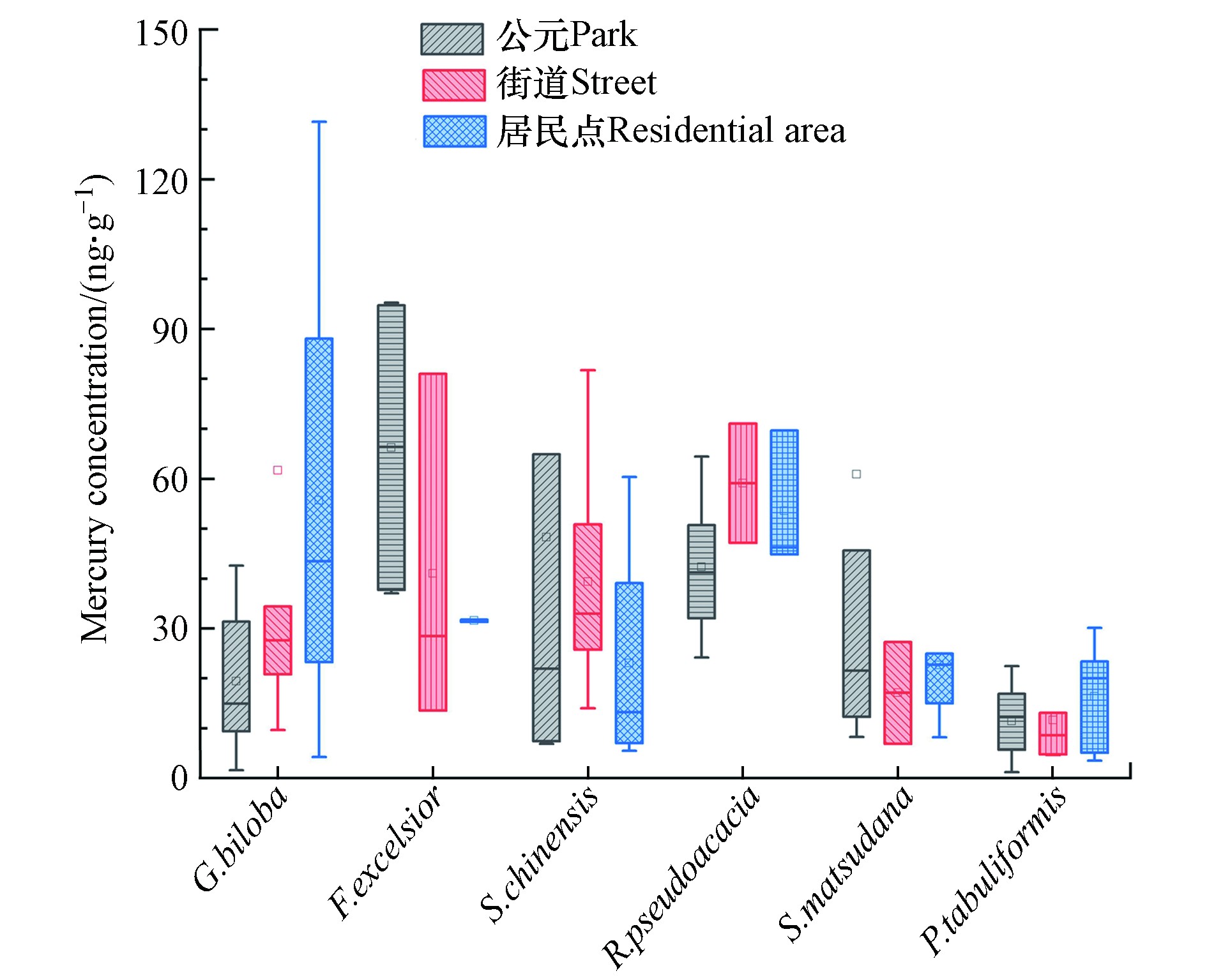
根据实地观察、卫星和地面图像在每个采样点选取公园、街道和居民区的3个土地利用类型收集凋落物。北京市主要绿化树种在3种不同土地利用类型中平均叶凋落物汞浓度见图3。公园、街道和居民点的银杏叶凋落物平均汞浓度分别是(19.46±14.85)、(61.69±86.69) 、(55.67±53.85) ng·g−1;刺槐叶凋落物平均汞浓度分别是(42.32±14.89 )、(59.10±16.88)、(53.58±13.91) ng·g−1。银杏和刺槐叶凋落物在街道平均汞浓度比居民点和公园高。油松叶片凋落物平均汞浓度在居民点最高(16.42±11.66)ng·g−1,在公园和街道分别是(11.42±7.06)ng·g−1、(11.66±9.68) ng·g−1。公园、街道和居民点的柳树叶凋落物平均汞浓度分别是(60.89±96.48)、(17.11±14.43)、(22.69±12.92) ng·g−1,白蜡叶凋落物平均汞浓度分别是(66.26±32.92)、(41.03±35.41)、(31.57±0.32) ng·g−1,圆柏叶凋落物平均汞浓度分别是(48.32±61.82)、(41.61±22.18)、(23.08±25.41)ng·g−1。白蜡、柳树和圆柏叶凋落物平均汞浓度在公园最高,这与北二环官园公园柳树叶片凋落物中汞浓度(高达256 ng·g−1)和市中心景山公园圆柏叶片凋落物在汞浓度(高达179.81 ng·g−1)远远高于其它采样点有关。另一方面,从凋落物汞浓度中值来看,银杏、柳树和油松在居民点最高,圆柏和刺槐在街道最高,仅白蜡在公园最高。总体来看,各树种凋落物汞在公园、街道和居民点没有显著性差异(P>0.05),这可能与北京市区同一个区域内不同土地利用类型下大气汞浓度差异不明显有关。
-
北京城市地区叶凋落物汞浓度空间分布见图4。从图4可知,所有树种的平均叶凋落物汞浓度在北京市中心和北二环显示最高,分别是(39.75±46.01)ng·g−1和(79.56±84.74)ng·g−1。北京市区北部叶凋落物中的汞浓度相比南部较高,这跟10年前的调查结果相似[17]。随着逐渐远离市中心,叶凋落物中的平均汞浓度明显呈下降趋势,五环以外叶凋落物中的汞浓度达到最低。北京市北部郊区鹫峰山国家森林公园叶片凋落物平均汞浓度是(19.04±12.75) ng·g−1,北京市南边郊区马驹桥湿地公园叶凋落物平均汞浓度是(13.80±9.83)ng·g−1。这与已有监测显示北京市中心大气汞浓度高于北京郊区的大气汞浓度[38,43]的结果一致,说明大气汞浓度是凋落物汞累积的关键因素。
-
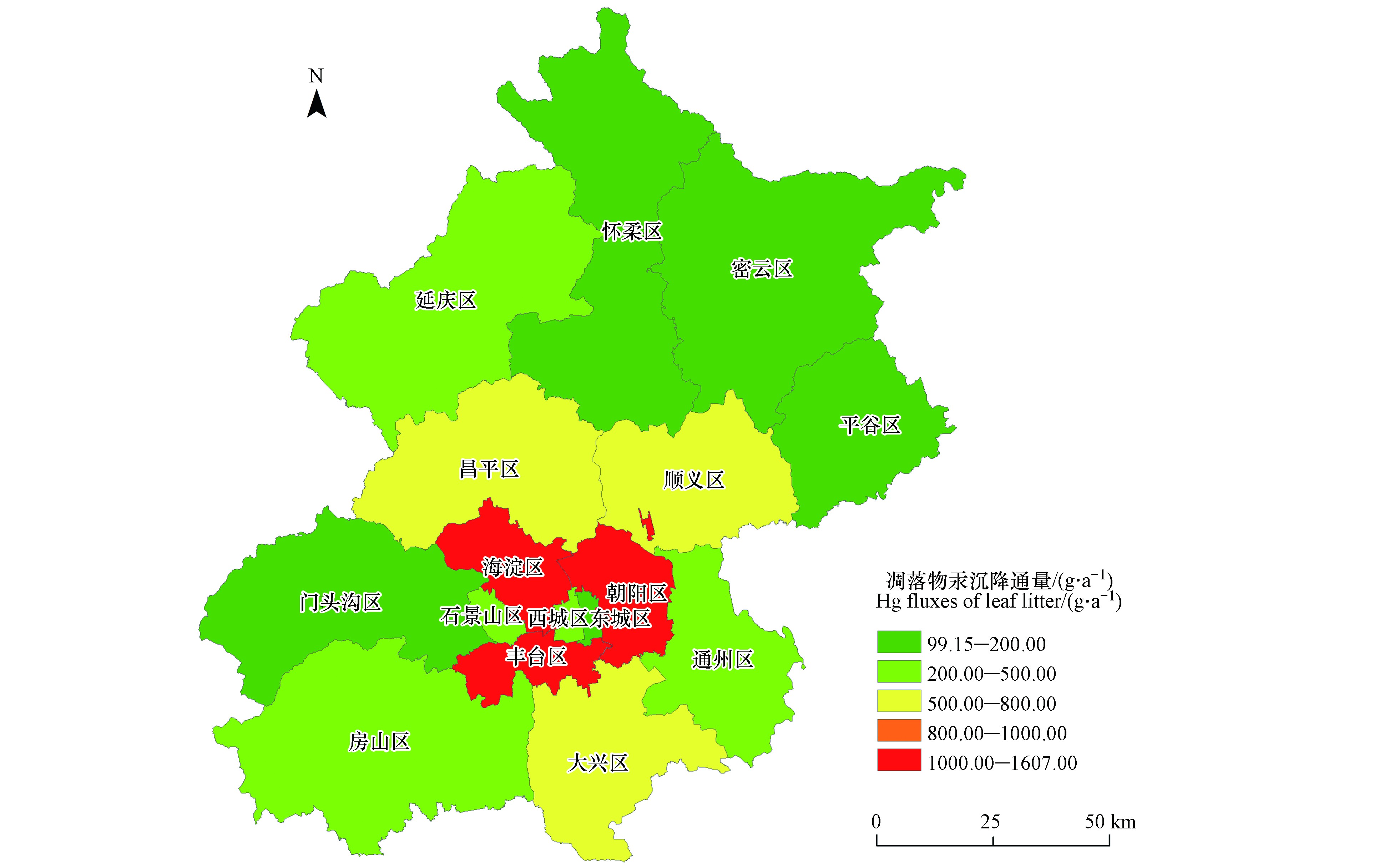
本研究通过凋落物的汞浓度乘以凋落物生物量的方式估算北京城市森林凋落物汞沉降通量[14,44-45],年凋落物生物量数据引自章志琴等[46]。城区没采样地区凋落物汞通量通过本调查中城区所有样品平均汞浓度计算获得,怀柔区、密云区和平谷区等没采样的北京郊区市辖区凋落物汞通量通过本调查中郊区采样点样品平均汞浓度获得。北京市区森林凋落物汞沉降通量范围是(196.29—438.08)mg·(ha·a)−1,北京郊区森林凋落物汞沉降通量范围是(105.98—153.52)mg·(ha·a)−1,北京城市森林凋落物汞沉降通量是其降水汞沉降通量的5—10倍[47],北京城市森林生态系统中凋落物汞通量高于北京自然森林生态系统东灵山森林凋落物汞通量[48],表明城市森林生态系统是大气汞重要的汇,值得关注。在此基础上,结合2019年北京市城市绿化资源数据库[49]中的北京市公园、街道和居民区树木面积,分别估算了北京市16个市辖区城市森林凋落物汞沉降通量(见图5)。
北京市总的凋落物汞沉降量是8.28 kg·a−1,其中城六区凋落物的汞沉降量是4.85 kg·a−1,占总沉降量的58.57%;北京郊区的10个区凋落物汞沉降量是3.43 kg·a−1,占总沉降量的41.43%。总体上北京城市中心市辖区的森林凋落物汞通量高于北京郊区市辖区森林凋落物汞通量。城市森林是重要的森林类型,与人类生活密切相关,但城市森林凋落物生物量与对污染物的吸收方面的研究还极少。本研究获得的北京市森林汞浓度和汞沉降通量数据为进一步深入评估城市森林生态系统在大气汞循环中的作用提供了基础支撑。
-
本研究选取北京市区西北至东南对角线上的公园、街道和居民区的3种土地利用类型,收集了29个采样点主要绿化树种的凋落物并分析其汞浓度。北京市8个主要绿化树种平均叶凋落物汞浓度是(35.98±14.90)ng·g−1,其中白蜡凋落物中汞浓度最高(50.14±31.10)ng·g−1,油松凋落物中汞浓度最低(12.58±8.69)ng·g−1,大部分树种凋落物叶汞浓度间存在显著性差异。每个树种在公园、街道和居民点的3个不同土地利用区叶片凋落物汞浓度没有显著性差异。北京市叶凋落物汞浓度从市中心到郊区总体呈下降趋势。北京市区森林凋落物汞沉降通量范围是(196.29—438.08)mg·(ha·a)−1,北京郊区森林凋落物汞沉降通量范围是(105.98—153.52) mg·(ha·a)−1,高于同地区自然森林生态系统汞沉降通量,说明北京城市森林生态系统受人为活动影响强烈。
北京城市森林生态系统凋落物汞分布特征及沉降通量
Mercury distribution characteristics and deposition flux of leaf litter in Beijing urban forest ecosystem
-
摘要: 大气汞沉降是全球性的环境问题,因其可从城市和工业地区进行远距离传输沉降到偏远地区,并通过食物链富集危害到人类和野生动植物的健康。为了揭示城市森林生态系统中凋落物汞分布特征及沉降通量,本研究选取北京市西北至东南对角线上的公园、街道和居民区3种土地利用类型,收集了29个采样点主要绿化树种的凋落物。结果表明,北京市平均叶凋落物汞浓度为(35.98±14.90)ng·g−1;在8个主要绿化树种中,白蜡凋落物汞浓度最高(50.14±31.10)ng·g−1,油松凋落物汞浓度最低(12.58±8.69 )ng·g−1,大部分树种之间存在显著性差异;同一树种在不同土地利用类型中没有显著性差异,但所有树种的平均叶凋落物汞浓度呈现从市中心到郊区下降趋势,说明北京城市森林生态系统中的汞分布受到人为活动影响明显。北京市区森林凋落物汞沉降通量范围是(196.29—438.08)mg·(ha·a)−1,北京郊区森林凋落物汞沉降通量范围是(105.98—153.52)mg·(ha·a)−1,这些结果为进一步深入评估城市森林生态系统在大气汞循环中的作用提供了基础支撑。Abstract: The deposition of atmospheric mercury(Hg) is a global problem, because it can be transported from cities and industrial areas to remote areas through long-distance transportation and endanger the health of humans, wild animals and plants through food chain enrichment. In order to reveal the mercury distribution characteristics and deposition flux of leaf litter in the urban forest ecosystem, this study collected leaf litter samples from 29 sites in parks, streets, and residential areas on the diagonal from northwest to southeast of Beijing. The results showed that the average mercury concentration of leaf litter in Beijing was (35.98±14.90) ng·g−1. Among the eight main greening tree species, the highest mercury concentration of leaf litter was (50.14±31.10) ng·g−1 from the Fraxinus excelsior , and the mercury concentration of leaf litter in the Pinus tabuliformis Carr. was the lowest ((12.58±8.69) ng·g−1). There are significant differences among most tree species and no significant difference was found in the same tree species from different land use. The average mercury concentration in leaf litter showed a downward trend from the city center to the suburbs, indicating that the mercury distribution in Beijing's urban forest ecosystem is significantly affected by human activities. The leaf litter mercury deposition flux in Beijing urban forests are (196.29—438.08) mg·(ha·a)−1, and (105.98—153.52) mg·(ha·a)−1 for Beijing suburban forests . These results will benefit to the further evaluation of the role of urban forest ecosystems in the atmospheric mercury cycle.
-
Key words:
- city /
- forest /
- mercury concentration /
- mercury flux /
- Beijing
-

-
-
[1] 李晓曼, 康文星. 广州市城市森林生态系统碳汇功能研究 [J]. 中南林业科技大学学报, 2008, 28(1): 8-13. doi: 10.3969/j.issn.1673-923X.2008.01.014 LI X M, KANG W X. Function of carbon sink of forest ecosystem in Guangzhou [J]. Journal of Central South University of Forestry & Technology, 2008, 28(1): 8-13(in Chinese). doi: 10.3969/j.issn.1673-923X.2008.01.014
[2] 李锋, 刘旭升, 王如松. 城市森林研究进展与发展战略 [J]. 生态学杂志, 2003, 22(4): 55-59. doi: 10.3321/j.issn:1000-4890.2003.04.011 LI F, LIU X S, WANG R S. Advances in urban forest and its development strategies research [J]. Chinese Journal of Ecology, 2003, 22(4): 55-59(in Chinese). doi: 10.3321/j.issn:1000-4890.2003.04.011
[3] BERLAND A, SHIFLETT S A, SHUSTER W D, et al. The role of trees in urban stormwater management [J]. Landscape and Urban Planning, 2017, 162: 167-177. doi: 10.1016/j.landurbplan.2017.02.017 [4] ISLAM M N, RAHMAN K S, BAHAR M M, et al. Pollution attenuation by roadside greenbelt in and around urban areas [J]. Urban Forestry & Urban Greening, 2012, 11(4): 460-464. [5] NOWAK D J. Institutionalizing urban forestry as a “biotechnology” to improve environmental quality [J]. Urban Forestry & Urban Greening, 2006, 5(2): 93-100. [6] LIVESLEY S J, MCPHERSON G M, CALFAPIETRA C. The urban forest and ecosystem services: Impacts on urban water, heat, and pollution cycles at the tree, street, and city scale [J]. Journal of Environmental Quality, 2016, 45(1): 119-124. doi: 10.2134/jeq2015.11.0567 [7] WHEATLEY B, WHEATLEY M A. Methylmercury and the health of indigenous peoples: A risk management challenge for physical and social sciences and for public health policy [J]. Science of the Total Environment, 2000, 259(1/2/3): 23-29. [8] FU X W, ZHANG H, YU B, et al. Observations of atmospheric mercury in China: A critical review [J]. Atmospheric Chemistry and Physics, 2015, 15(16): 9455-9476. doi: 10.5194/acp-15-9455-2015 [9] DRISCOLL C T, MASON R P, CHAN H M, et al. Mercury as a global pollutant: Sources, pathways, and effects [J]. Environmental Science & Technology, 2013, 47(10): 4967-4983. [10] HASHEMI S A, TABIBIAN S. Application of Mulberry nigra to absorb heavy metal, mercury, from the environment of green space city [J]. Toxicology Reports, 2018, 5: 644-646. doi: 10.1016/j.toxrep.2018.05.006 [11] DRISCOLL C T, HAN Y J, CHEN C Y, et al. Mercury contamination in forest and freshwater ecosystems in the northeastern United States [J]. BioScience, 2007, 57(1): 17-28. doi: 10.1641/B570106 [12] STREETS D G, HOROWITZ H M, LU Z F, et al. Global and regional trends in mercury emissions and concentrations, 2010—2015 [J]. Atmospheric Environment, 2019, 201: 417-427. doi: 10.1016/j.atmosenv.2018.12.031 [13] JOHNSON D W, LINDBERG S E. The biogeochemical cycling of Hg in forests: Alternative methods for quantifying total deposition and soil emission [J]. Water, Air, and Soil Pollution, 1995, 80(1/2/3/4): 1069-1077. [14] REA A W, KEELER G J, SCHERBATSKOY T. The deposition of mercury in throughfall and litterfall in the lake Champlain watershed: A short-term study [J]. Atmospheric Environment, 1996, 30(19): 3257-3263. doi: 10.1016/1352-2310(96)00087-8 [15] WANG X, BAO Z D, LIN C J, et al. Assessment of global mercury deposition through litterfall [J]. Environmental Science & Technology, 2016, 50(16): 8548-8557. [16] 王训, 袁巍, 冯新斌. 森林生态系统汞的生物地球化学过程 [J]. 化学进展, 2017, 29(9): 970-980. doi: 10.7536/PC170343 WANG X, YUAN W, FENG X B. Global review of mercury biogeochemical processes in forest ecosystems [J]. Progress in Chemistry, 2017, 29(9): 970-980(in Chinese). doi: 10.7536/PC170343
[17] NIU Z C, ZHANG X S, WANG Z W, et al. Mercury in leaf litter in typical suburban and urban broadleaf forests in China [J]. Journal of Environmental Sciences, 2011, 23(12): 2042-2048. doi: 10.1016/S1001-0742(10)60669-9 [18] FLECK J A, GRIGAL D F, NATER E A. Mercury uptake by trees: An observational experiment [J]. Water, Air, and Soil Pollution, 1999, 115(1/2/3/4): 513-523. [19] ASSAD M, PARELLE J, CAZAUX D, et al. Mercury uptake into poplar leaves [J]. Chemosphere, 2016, 146: 1-7. doi: 10.1016/j.chemosphere.2015.11.103 [20] ERICKSEN J A, GUSTIN M S, SCHORRAN D E, et al. Accumulation of atmospheric mercury in forest foliage [J]. Atmospheric Environment, 2003, 37(12): 1613-1622. doi: 10.1016/S1352-2310(03)00008-6 [21] ERICKSEN J A, GUSTIN M S. Foliar exchange of mercury as a function of soil and air mercury concentrations [J]. Science of the Total Environment, 2004, 324(1/2/3): 271-279. [22] FRESCHOLTZ T E, GUSTIN M S, SCHORRAN D E, et al. Assessing the source of mercury in foliar tissue of quaking aspen [J]. Environmental Toxicology and Chemistry, 2003, 22(9): 2114-2119. doi: 10.1002/etc.5620220922 [23] MÉLIÈRES M A, POURCHET M, CHARLES-DOMINIQUE P, et al. Mercury in canopy leaves of French Guiana in remote areas [J]. Science of the Total Environment, 2003, 311(1/2/3): 261-267. [24] WANG Z W, ZHANG X S, XIAO J S, et al. Mercury fluxes and pools in three subtropical forested catchments, southwest China [J]. Environmental Pollution, 2009, 157(3): 801-808. doi: 10.1016/j.envpol.2008.11.018 [25] ZHOU J, WANG Z W, ZHANG X S. Deposition and fate of mercury in litterfall, litter, and soil in coniferous and broad-leaved forests [J]. Journal of Geophysical Research:Biogeosciences, 2018, 123(8): 2590-2603. doi: 10.1029/2018JG004415 [26] RICHARDSON J B, FRIEDLAND A J. Mercury in coniferous and deciduous upland forests in northern New England, USA: Implications of climate change [J]. Biogeosciences, 2015, 12(22): 6737-6749. doi: 10.5194/bg-12-6737-2015 [27] LAACOURI A, NATER E A, KOLKA R K. Distribution and uptake dynamics of mercury in leaves of common deciduous tree species in Minnesota, USA [J]. Environmental Science & Technology, 2013, 47(18): 10462-10470. [28] OBRIST D, JOHNSON D W, LINDBERG S E, et al. Mercury distribution across 14 US forests. part I: Spatial patterns of concentrations in biomass, litter, and soils [J]. Environmental Science & Technology, 2011, 45(9): 3974-3981. [29] RASMUSSEN P E, MIERLE G, NRIAGU J O. The analysis of vegetation for total mercury [J]. Water Air & Soil Pollution, 1991, 56(1): 379-390. [30] OBRIST D, JOHNSON D W, EDMONDS R L. Effects of vegetation type on mercury concentrations and pools in two adjacent coniferous and deciduous forests [J]. Journal of Plant Nutrition and Soil Science, 2012, 175(1): 68-77. doi: 10.1002/jpln.201000415 [31] YANG Y, YANAI R D, DRISCOLL C T, et al. Concentrations and content of mercury in bark, wood, and leaves in hardwoods and conifers in four forested sites in the northeastern USA [J]. PLoS One, 2018, 13(4): e0196293. doi: 10.1371/journal.pone.0196293 [32] HALL B D, ST LOUIS V L. Methylmercury and total mercury in plant litter decomposing in upland forests and flooded landscapes [J]. Environmental Science & Technology, 2004, 38(19): 5010-5021. [33] 杨佳, 王会霞, 谢滨泽, 等. 北京9个树种叶片滞尘量及叶面微形态解释 [J]. 环境科学研究, 2015, 28(3): 384-392. YANG J, WANG H X, XIE B Z, et al. Accumulation of particulate matter on leaves of nine urban greening plant species with different micromorphological structures in Beijing [J]. Research of Environmental Sciences, 2015, 28(3): 384-392(in Chinese).
[34] JUILLERAT J I, ROSS D S, BANK M S. Mercury in litterfall and upper soil horizons in forested ecosystems in Vermont, USA [J]. Environmental Toxicology and Chemistry, 2012, 31(8): 1720-1729. doi: 10.1002/etc.1896 [35] BLACKWELL B D, DRISCOLL C T. Deposition of mercury in forests along a montane elevation gradient [J]. Environmental Science & Technology, 2015, 49(9): 5363-5370. [36] REA A W, LINDBERG S E, SCHERBATSKOY T, et al. Mercury accumulation in foliage over time in two northern mixed-hardwood forests [J]. Water, Air, and Soil Pollution, 2002, 133(1/2/3/4): 49-67. [37] BUSHEY J T, NALLANA A G, MONTESDEOCA M R, et al. Mercury dynamics of a northern hardwood canopy [J]. Atmospheric Environment, 2008, 42(29): 6905-6914. doi: 10.1016/j.atmosenv.2008.05.043 [38] LIU S L, NADIM F, PERKINS C, et al. Atmospheric mercury monitoring survey in Beijing, China [J]. Chemosphere, 2002, 48(1): 97-107. doi: 10.1016/S0045-6535(02)00026-7 [39] WU Q R, TANG Y, WANG S X, et al. Developing a statistical model to explain the observed decline of atmospheric mercury [J]. Atmospheric Environment, 2020, 243: 117868. doi: 10.1016/j.atmosenv.2020.117868 [40] NGUYEN L S P, SHEU G R, LIN D W, et al. Temporal changes in atmospheric mercury concentrations at a background mountain site downwind of the East Asia continent in 2006-2016 [J]. Science of the Total Environment, 2019, 686: 1049-1056. doi: 10.1016/j.scitotenv.2019.05.425 [41] KIM K H, BROWN R J C, KWON E, et al. Atmospheric mercury at an urban station in Korea across three decades [J]. Atmospheric Environment, 2016, 131: 124-132. doi: 10.1016/j.atmosenv.2016.01.051 [42] TANG Y, WANG S X, WU Q R, et al. Recent decrease trend of atmospheric mercury concentrations in East China: The influence of anthropogenic emissions [J]. Atmospheric Chemistry and Physics, 2018, 18(11): 8279-8291. doi: 10.5194/acp-18-8279-2018 [43] ZHANG W, TONG Y D, HU D, et al. Characterization of atmospheric mercury concentrations along an urban-rural gradient using a newly developed passive sampler [J]. Atmospheric Environment, 2012, 47: 26-32. doi: 10.1016/j.atmosenv.2011.11.046 [44] SHEEHAN K D, FERNANDEZ I J, KAHL J S, et al. Litterfall mercury in two forested watersheds at Acadia National Park, Maine, USA [J]. Water, Air, and Soil Pollution, 2006, 170(1/2/3/4): 249-265. [45] SILVA-FILHO E V, MACHADO W, OLIVEIRA R R, et al. Mercury deposition through litterfall in an Atlantic forest at ilha grande, southeast Brazil [J]. Chemosphere, 2006, 65(11): 2477-2484. doi: 10.1016/j.chemosphere.2006.04.053 [46] 章志琴, 朱亚男, 杨晓荣, 等. 无锡城市绿地凋落物存留特征及处理方式分析 [J]. 林业勘察设计, 2019, 39(4): 14-17. ZHANG Z Q, ZHU Y N, YANG X R, et al. Characteristics and treatment mode on litter decomposition in Wuxi City [J]. Forestry Prospect and Design, 2019, 39(4): 14-17(in Chinese).
[47] 张欢. 北京城市大气中汞的形态及气粒分配[D]. 北京: 中国科学院生态环境研究中心, 2019. ZHANG H. Speciation and gas-particle partitioning of mercury in Beijing urban atmosphere [D]. Beijing: Research Center for Eco-Environmental Sciences, Chinese Academy of Science, 2019(in Chinese)
[48] ZHOU J, WANG Z W, ZHANG X S, et al. Mercury concentrations and pools in four adjacent coniferous and deciduous upland forests in Beijing, China [J]. Journal of Geophysical Research:Biogeosciences, 2017, 122(5): 1260-1274. doi: 10.1002/2017JG003776 [49] 北京市园林绿化局. 2019年北京市城市绿化资源情况[EB/OL]. [2020-4-23]. 北京市园林绿化局, Beijing Gardening and Greening Bureau. Urban greening resources in Beijing in 2019[EB]. [2020-4-23]. (in Chinese).
-




 下载:
下载: