-
多相催化臭氧氧化技术是一种新型的在常温常压下将那些难以用臭氧单独氧化的有机污染物降解的方法 [1-3]. 一直以来,高效、廉价和稳定的催化剂研制是催化臭氧氧化技术应用的关键. 大量的金属氧化物或复合金属氧化物被合成用于有效的催化臭氧氧化水中的有机物,但存在比表面积小,活性组分价格昂贵等情况[4-6]. 由于不同催化剂的性质差异较大,催化臭氧氧化的机理也不尽相同,目前多相催化臭氧氧化技术尚未大规模应用[7].
根据报道,Al2O3催化剂上的Lewis酸性位是促进臭氧有效分解的活性位点,在气态条件下,臭氧在Al2O3表面分解为活性原子氧,但Al2O3的比表面积有限[8-9]. 铁具有多价态,在自然界广泛存在,有利于臭氧有效分解[10]. 本研究通过水热法合成SBA-15作为载体,将铁、铝双金属负载于SBA-15表面制备Fe-Al2O3/SBA-15催化剂,用于催化臭氧氧化水中医药污染物布洛芬的研究,通过不同初始pH对催化反应的影响和电子自旋共振实验,研究催化反应机理. 布洛芬(IBU)是一种抗炎药,估计全球年产量为数千吨,在地表水和废水中检测到的浓度范围为ng·L−1至低μg·L−1水平,IBU是一种持久性污染物,一些研究人员认为,IBU可能会改变淡水环境中无尾类动物的胚胎发育. 因此,选择IBU来评价催化剂的活性和性能[11].
-
三嵌段共聚物EO20PO70EO20(P123,MW 5800,分析纯,Sigma-Aldrich),布洛芬(分析纯,东京化成工业株式会社),结晶氯化铝(AlCl3·6H2O)、结晶氯化铁(FeCl3·6H2O)、正硅酸四乙酯(分析纯,国药集团化学试剂北京有限公司),自由基捕捉剂BMPO(分析纯,东仁化学科技(上海)有限公司). 超纯水(电阻率为18.2 MΩ·cm)由Milli-Q超纯水仪制得. 溶液的pH用2 mol·L−1盐酸和2 mol·L−1氢氧化钠溶液调节.
-
SBA-15制备[12]. 以P123为模板剂,正硅酸四乙酯为硅源,在强酸条件下合成SBA-15. 具体方法:称取4 g P123放入烧杯中,加入125 mL 2 mol· L−1 盐酸,40 ℃恒温条件下搅拌直至完全溶解,然后缓慢滴加9.63 mL正硅酸四乙酯,并继续搅拌24 h. 将白色溶胶装入反应釜中,在100 ℃水热条件下晶化48 h,所得白色固体洗涤至中性,在鼓风干燥箱80 ℃干燥10 h后,用马弗炉在空气气氛下550 ℃焙烧6 h,得到SBA-15.
Al2O3/SBA-15制备. 称取0.89 g AlCl3·6H2O溶于10 mL水中,溶解后加入2 g SBA-15,搅拌1 h,然后85 ℃烘干10 h;以上过程再重复2次,然后用马弗炉在空气气氛下550 ℃焙烧6 h得到Al2O3/SBA-15.
Fe-Al2O3/SBA-15制备. 将适量FeCl3·6H2O溶于4 mL水中,溶解后加入2 g Al2O3/SBA-15,超声1 h,85 ℃烘干,然后用马弗炉在空气气氛下300 ℃焙烧30 min,得到Fe-Al2O3/SBA-15催化剂. Fe/SBA-15催化剂的制备和上述类似,以SBA-15作为载体.
-
用X射线粉末衍射仪(XRD)对催化剂晶型结构进行表征,测试条件:操作电压为40 kV,操作电流为100 mA,用Cu Kα(λ=0.154059 nm)辐射为激发源. 催化剂的形貌及粒度分布在日本JEOL-2010型场发射透射电子显微镜(TEM)上进行分析. 以无水乙醇为溶剂,对样品进行超声波振荡,使其颗粒分散良好后,制样、拍摄照片,加速电压为200 kV. 催化剂的比表面积和孔径、孔容分布采用美国Micromeritics公司的ASAP-2020比表面积仪测定. 孔径、孔容分布用氮气吸附-脱附等温线和Barrett-Joyner-Halenda(BJH)方法分析. 催化剂表面零电荷点(pHpzc)采用马尔文Nano-ZS90型Zeta电位仪测定[10].
-
催化臭氧氧化实验在鼓泡式玻璃反应器中进行,反应器容积1.2 L. 称取1.5g催化剂加到装有1L浓度为10 mg·L−1布洛芬溶液的反应器中,用盐酸和氢氧化钠调节pH值到7.0. 臭氧由高纯氧气经过3S-A5型臭氧发生器(北京同林科技有限公司)产生,30 mg·L−1的臭氧/氧气混合气体经微孔砂心布气头进入反应器,混合气体的流速控制为200 mL·min−1,尾气用KI溶液吸收. 所有样品取出后立刻加入几滴0.1 mol·L−1硫代硫酸钠终止溶液中剩余的臭氧,并用0.45 μm醋酸纤维滤膜过滤.
水中布洛芬浓度采用高效液相色谱(HPLC,1200 series;Agilent,Santa Clara,CA)测定,色谱柱为Eclipse XDB-C18 column(5 μm,4.6 mm×150 mm;Agilent). 分析条件为:流动相为60:40(V/V)乙腈:磷酸盐缓冲液(20 mmol·L−1,pH = 2.5),柱温40 ℃,进样量20 μL,流量为1 mL·min−1,紫外检测波长220 nm. 总有机碳(TOC)采用岛津TOC-VCPH型总有机碳分析仪测定. 电子顺磁共振分析使用德国布鲁克公司ESP300E型电子顺磁共振波谱仪,用自由基捕捉剂BMPO自旋捕捉方法直接测定反应溶液中的活性氧物种. 仪器中心场强3480 G,微波频率为9.79 GHz,功率为5.05 mW.
-
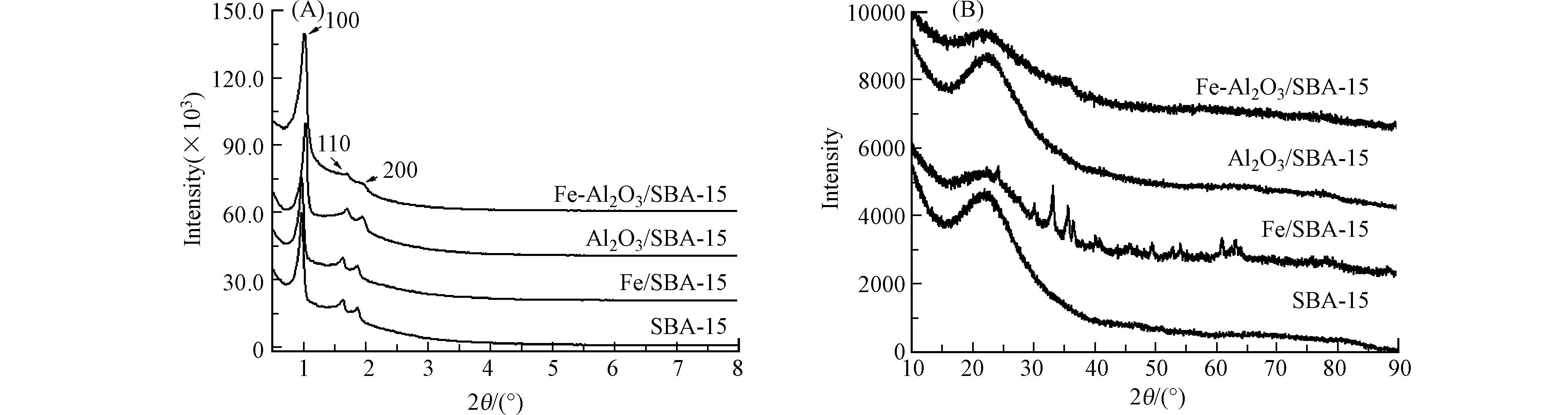
图1是不同催化剂的小角和广角XRD图,所有样品在1°(100晶面)附近出现强的衍射峰,且在1.6°附近出现两个弱的衍射峰(分别为110和200晶面),说明催化剂经过负载改性后保持了SBA-15高度有序的六方孔道结构[13]. Al2O3/SBA-15和Fe-Al2O3/SBA-15催化剂没有出现氧化铝晶相衍射峰,说明氧化铝均匀涂覆在SBA-15的孔壁上. Fe/SBA-15出现几个典型的α-Fe2O3(JCPDS卡片01-073-2234)衍射峰[14],说明α-Fe2O3在SBA-15表面发生聚集. 而Fe-Al2O3/SBA-15催化剂没有出现铁氧化物的晶相衍射峰,说明铁氧化物高度分散在Al2O3/SBA-15表面. 这些结果表明氧化铝均匀涂覆在SBA-15的孔壁上有利于铁的分散.
不同样品的TEM照片进一步证实了上面的结论(图2). 所有的催化剂显示出高度有序的六角孔道结构,氧化铝高度分散在Al2O3/SBA-15和Fe-Al2O3/SBA-15表面,α-Fe2O3颗粒在Fe/SBA-15表面发生聚集,而铁氧化物高分散于Fe-Al2O3/SBA-15表面.
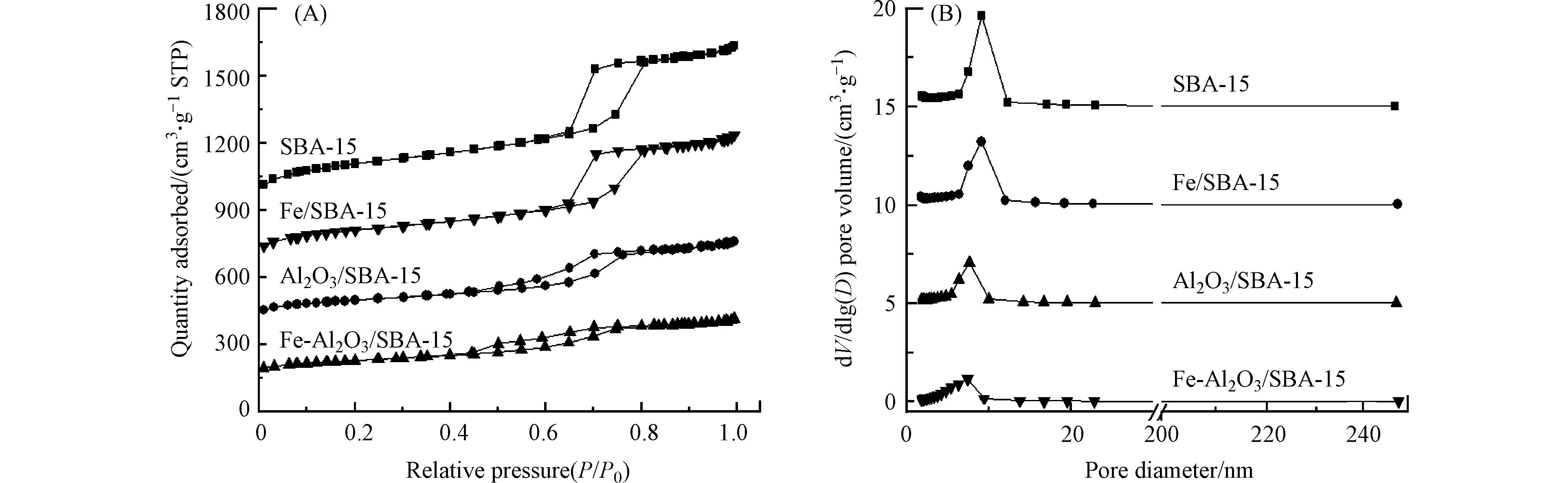
图3是不同催化剂的氮气吸附脱附等温线和孔径、孔容分布图. 所有样品的氮气吸附脱附等温线都符合第Ⅳ类吸附等温线特征,表现出集中的孔径分布. 这说明这4种催化剂都有介孔结构[15]. 另外,从表1可以看出,与SBA-15相比,铁、铝负载于SBA-15表面后,比表面积、孔径、孔容减少,孔壁厚度增大,说明铁、铝成功负载于SBA-15表面.
-
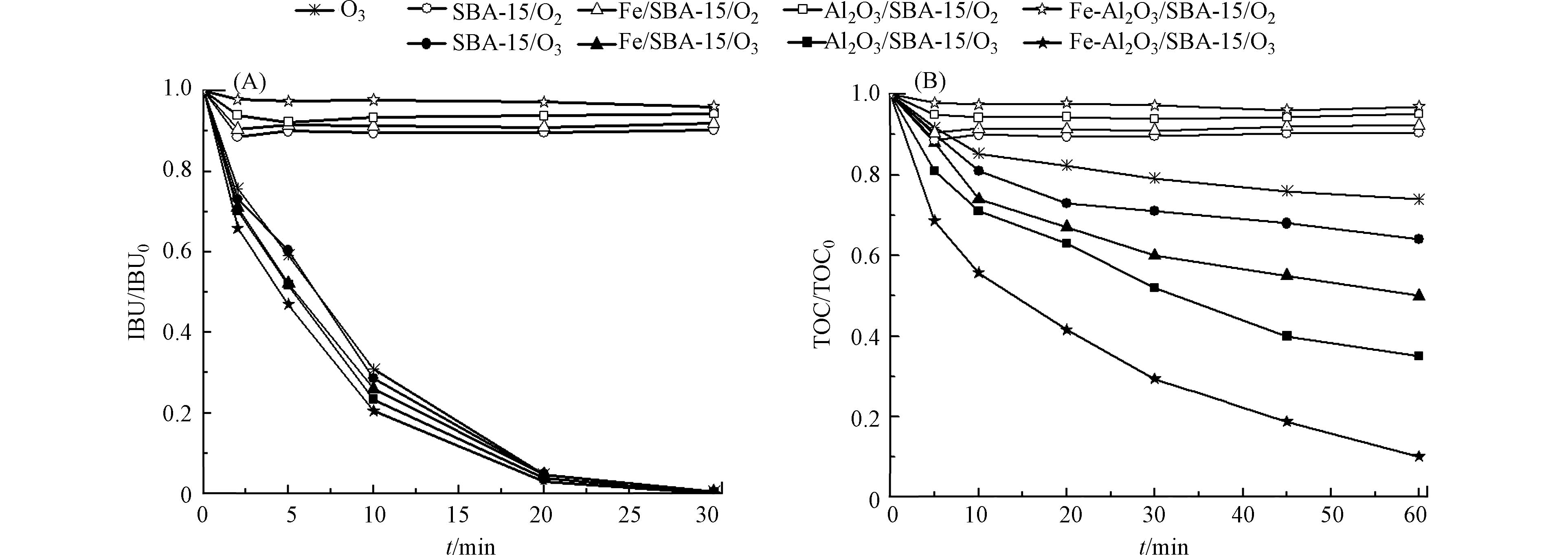
图4是不同工艺对布洛芬、TOC去除率效果图. Fe-Al2O3/SBA-15、Al2O3/SBA-15、Fe/SBA-15和SBA-15对布洛芬的吸附去除率分别为2.8%、5.7%、8.0%和9.7%. 与单独臭氧氧化工艺相比,催化臭氧氧化工艺对布洛芬的去除率有所增加,但显著提高TOC去除率,在反应60 min,单独臭氧氧化工艺TOC去除率仅有26%,而Fe-Al2O3/SBA-15、Al2O3/SBA-15、Fe2O3/SBA-15和SBA-15催化臭氧氧化工艺的TOC去除率分别为90%、65%、50%和36%. 这些结果表明,催化臭氧氧化有利用布洛芬的矿化,铁、铝氧化物的负载显著提高SBA-15催化臭氧氧化水中布洛芬的活性,并且铁、铝具有协同作用,Fe-Al2O3/SBA-15具有最佳的催化活性.
-
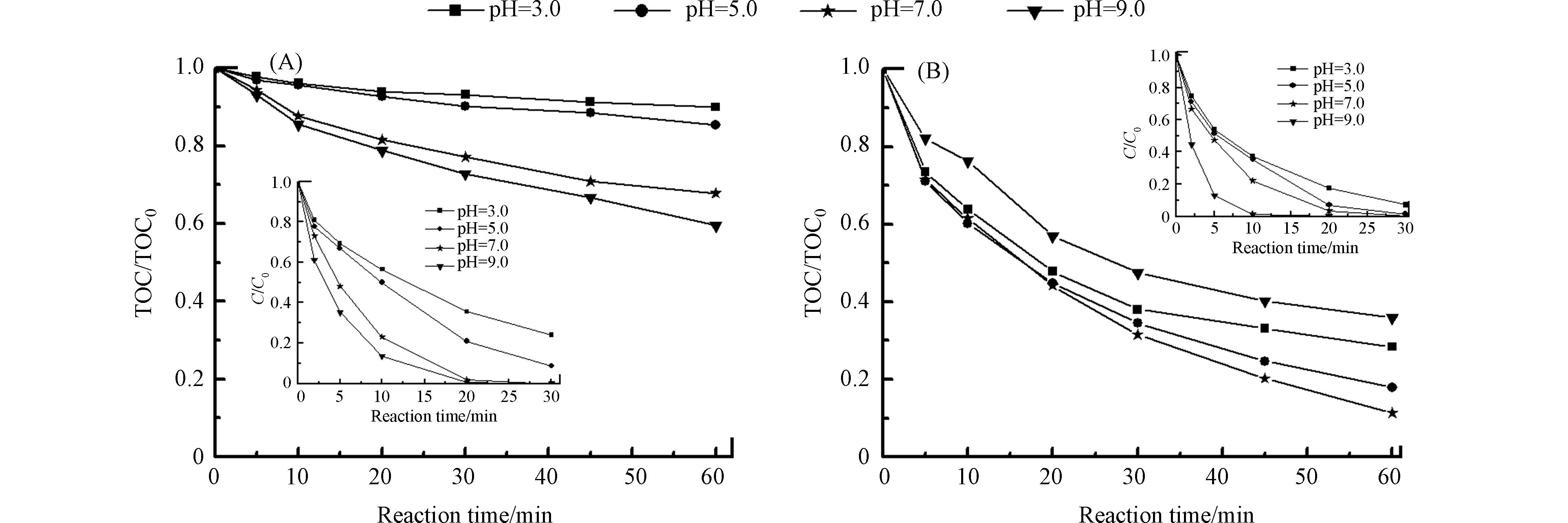
图5是初始pH对单独臭氧氧化和Fe-Al2O3/SBA-15催化臭氧氧化IBU和TOC去除的影响. 单独臭氧氧化过程,随着pH的增加, IBU和TOC的去除率都增大. Fe-Al2O3/SBA-15催化臭氧氧化过程,随着pH的增加,IBU去除率增大,TOC去除率先增大后显著减小. 由于Fe-Al2O3/SBA-15的pHpzc是7.25,在pH<7.25时,催化剂的表面带正电荷,IBU和小分子有机酸可通过静电引力吸附在催化剂表面; 在pH>7.25时,催化剂表面带负电荷,由于电荷排斥作用,催化剂几乎不会对小分子有机酸有吸附. 结果表明,小分子有机酸的降解主要发生在催化剂表面,催化剂表面有更多的活性氧物种生成.
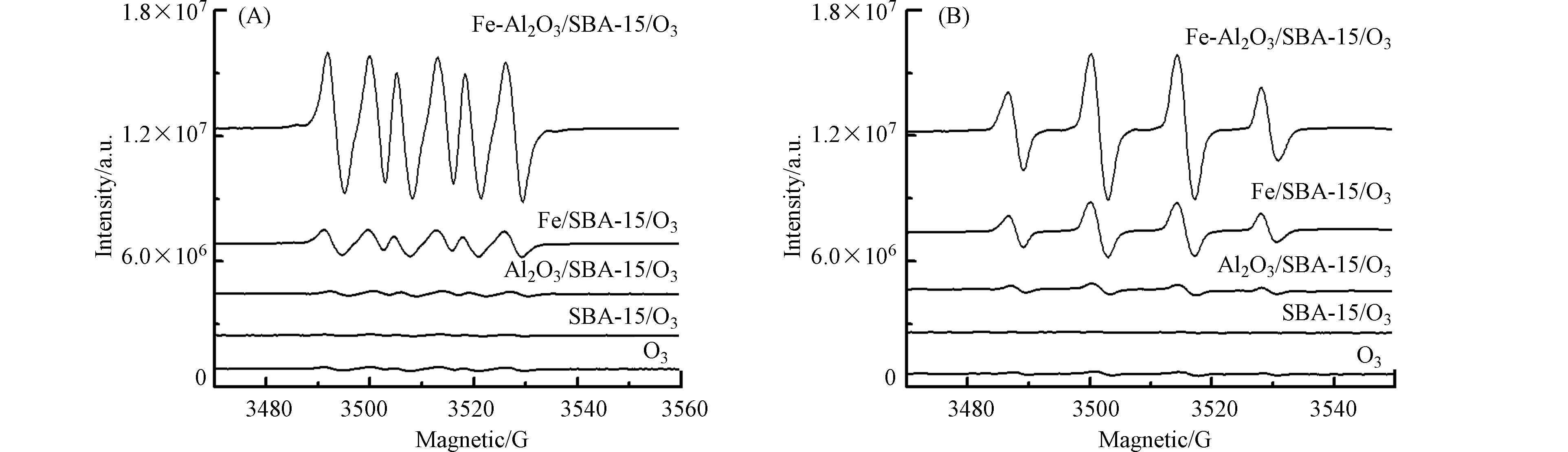
电子顺磁共振波谱进一步分析不同工艺过程产生的活性氧物种. 图6是不同催化剂饱和臭氧水悬浮液以BMPO为捕获剂的ESR图. 从图6中可以看出,在SBA-15的悬浮液中没有检测到超氧自由基(O2•−)和羟基自由基(•OH)的信号,这表明SBA-15表面物理吸附的臭氧不分解. 在Al2O3/SBA-15,Fe/SBA-15和Fe-Al2O3/SBA-15悬浮液观察到BMPO-•OH和BMPO-O2•−的特征峰,并且峰强度按照Al2O3/SBA-15、Fe/SBA-15、Fe-Al2O3/SBA-15的顺序增加. 这些结果说明,铁的负载能够显著地促进臭氧分解产生超氧自由基和羟基自由基,说明Fe2+/Fe3+的电子循环对臭氧的有效分解起重要作用. 另外,从图4可以看出,与Fe/SBA-15相比,Al2O3/SBA-15催化臭氧氧化过程对布洛芬和TOC具有更高的催化活性,而在不同催化剂饱和臭氧水悬浮液中Fe/SBA-15比Al2O3/SBA-15产生更多的超氧自由基和羟基自由基(图6),这说明Al2O3/SBA-15催化臭氧氧化过程有活性原子氧生成,活性原子氧是主要的活性氧物种[16]. Fe-Al2O3/SBA-15催化臭氧氧化布洛芬具有最佳的催化活性,说明Fe、Al双金属的协同作用进一步强化了臭氧分解产生羟基自由基、超氧自由基和活性原子氧,从而具有最高的催化活性.
-
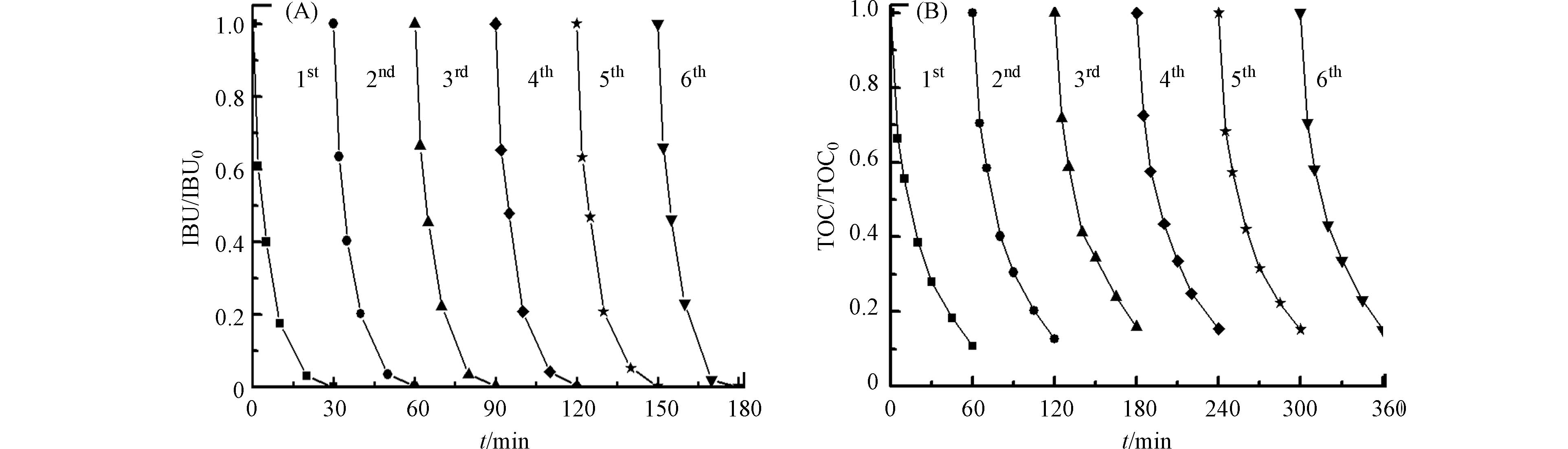
图7是Fe-Al2O3/SBA-15催化剂的活性与稳定性实验. 催化剂重复使用6次后,布洛芬的降解速率几乎不变,TOC的去除率重复3次后就基本稳定,仅下降5%,并且反应后溶液中未检测到Fe、Al的溶出,这说明Fe-Al2O3/SBA-15催化剂具有很好的活性和稳定性.
-
成功制备了铁、铝双金属负载SBA-15介孔分子筛催化剂. XRD、TEM、氮气吸附脱附表征结果表明,该催化剂具有大的比表面积,铁、铝氧化物在SBA-15表面高度分散. Fe-Al2O3/SBA-15催化臭氧氧化布洛芬结果表明,该催化剂有很好的催化活性和稳定性,反应60 min时,TOC去除率达到90%,而单独臭氧氧化过程TOC去除率只有26%. 不同初始pH、电子顺磁共振实验结果表明,布洛芬和小分子有机酸吸附于Fe-Al2O3/SBA-15催化剂表面,铁、铝双金属的协同作用促进臭氧有效分解产生超氧自由基、羟基自由基和活性原子氧,有利于有机物的矿化,从而表现出最高的催化活性. Fe-Al2O3/SBA-15是一种有前景的臭氧化催化剂.
Fe-Al2O3/SBA-15催化臭氧氧化水中布洛芬
Catalytic ozonation of ibuprofen by Fe-Al2O3/SBA-15 in water
-
摘要: 以嵌段共聚物为模板剂,在酸性条件下水热合成SBA-15. 将铁、铝负载于SBA-15表面制备Fe-Al2O3/SBA-15介孔分子筛催化剂,并将其用于催化臭氧氧化水中布洛芬(IBU). 透射电子显微镜、X射线衍射、氮气吸附-脱附表征结果表明,铁、铝均匀负载于SBA-15表面,保持SBA-15有序的介孔结构,具有较大的比表面积. 不同催化剂活性评价结果表明,铁、铝的负载显著提高SBA-15催化臭氧氧化水中布洛芬的活性,反应60 min后,Fe-Al2O3/SBA-15的TOC去除率为90%,而Al2O3/SBA-15、Fe/SBA-15和SBA-15的TOC去除率分别为65%、50%和36%,单独臭氧氧化仅为26%. 实验结果表明,铁、铝的协同作用有利于臭氧分解为羟基自由基、超氧自由基和活性原子氧,布洛芬和小分子有机酸吸附于催化剂表面从而有利于有机物的矿化. 催化剂重复利用6次后仍保持较高的催化活性和稳定性.
-
关键词:
- Fe-Al2O3/SBA-15 /
- 催化臭氧氧化 /
- 布洛芬 /
- 活性氧.
Abstract: SBA-15 was synthesized hydrothermally in acidic conditions using block copolymer as template. Fe-Al2O3/SBA-15 mesoporous molecular sieve catalyst was prepared by loading iron and aluminum on the surface of SBA-15, and it was used for catalytic ozonation of ibuprofen in water. The characterization results of transmission electron microscope, X-ray diffraction and nitrogen adsorption desorption showed that iron and aluminum were uniformly loaded on the surface of SBA-15, maintaining the ordered mesoporous structure of SBA-15, and having a large specific surface area. The activity evaluation results of different catalysts showed that the loading of iron and aluminum significantly improved the catalytic activity of SBA-15 for ozonation of ibuprofen in water, and iron and aluminum had a synergistic effect. After 60 min of reaction, the TOC removal rate of Fe-Al2O3/SBA-15 was 90%, while that of Al2O3/SBA-15, Fe/SBA-15 and SBA-15 were 65%, 50% and 36%, respectively, and that of ozonation alone was only 26%. The experimental results showed that the synergistic effect of iron and aluminum was beneficial to the decomposition of ozone into hydroxyl radicals, superoxide radicals and active atomic oxygen. Ibuprofen and small molecule organic acid were adsorbed on the surface of the catalyst, which was conducive to the mineralization of organic matter. The catalyst remains high catalytic activity and stability after being reused for 6 times.-
Key words:
- Fe-Al2O3/SBA-15 /
- catalytic ozonation /
- ibuprofen /
- active oxygen.
-

-
表 1 不同催化剂的比表面、孔径、孔容和孔壁
Table 1. Surface area, pore diameter, pore volume and pore wall of different catalysts
催化剂
Catalyst硅铝物质的量比
Si/Al ratio铁含量/% wt
Fe content比表面积/ (m2·g−1)
S BET孔径/ nm
Pore diameter孔容/(cm3 g−1)
Pore volume孔壁/ nm
Pore wallSBA-15 — — 726.8 6.34 1.12 4.33 Fe/SBA-15 — 12% 564.1 6.29 0.91 4.46 Al2O3/SBA-15 3 — 424.2 6.01 0.56 4.90 Fe-Al2O3/SBA-15 3 12% 359.1 5.36 0.43 4.98 -
[1] LEGUBE B, LEITNER N K V. Catalytic ozonation: A promising advanced oxidation technology for water treatment [J]. Catalysis Today, 1999, 53(1): 61-72. doi: 10.1016/S0920-5861(99)00103-0 [2] KASPRZYK-HORDERN B, ZIÓŁEK M, NAWROCKI J. Catalytic ozonation and methods of enhancing molecular ozone reactions in water treatment [J]. Applied Catalysis B:Environmental, 2003, 46(4): 639-669. doi: 10.1016/S0926-3373(03)00326-6 [3] WANG J L, CHEN H. Catalytic ozonation for water and wastewater treatment: Recent advances and perspective [J]. Science of the Total Environment, 2020, 704: 135249. doi: 10.1016/j.scitotenv.2019.135249 [4] ISSAKA E, AMU-DARKO J N O, YAKUBU S, et al. Advanced catalytic ozonation for degradation of pharmaceutical pollutants―A review [J]. Chemosphere, 2022, 289: 133208. doi: 10.1016/j.chemosphere.2021.133208 [5] JIN X G, WU C Y, FU L Y, et al. Development, dilemma and potential strategies for the application of nanocatalysts in wastewater catalytic ozonation: A review [J]. Journal of Environmental Sciences, 2023, 124: 330-349. doi: 10.1016/j.jes.2021.09.041 [6] CAI C, DUAN X D, XIE X J, et al. Efficient degradation of clofibric acid by heterogeneous catalytic ozonation using CoFe2O4 catalyst in water [J]. Journal of Hazardous Materials, 2021, 410: 124604. doi: 10.1016/j.jhazmat.2020.124604 [7] NAWROCKI J. Catalytic ozonation in water: Controversies and questions [J]. Applied Catalysis B:Environmental, 2013, 142/143: 465-471. doi: 10.1016/j.apcatb.2013.05.061 [8] ROY S, MPOURMPAKIS G, HONG D Y, et al. Mechanistic study of alcohol dehydration on γ-Al2O3[J]. ACS Catalysis 2012, 2: 1846-1853. [9] TRUEBA M, TRASATTI S P. γ-alumina as a support for catalysts: A review of fundamental aspects [J]. ChemInform, 2005, 36(44): 3393-3403. [10] HUANG R H, YAN H H, LI L S, et al. Catalytic activity of Fe/SBA-15 for ozonation of dimethyl phthalate in aqueous solution [J]. Applied Catalysis B:Environmental, 2011, 106(1/2): 264-271. [11] VELDHOEN N, SKIRROW R C, BROWN L L, et al. Effects of acute exposure to the non-steroidal anti-inflammatory drug ibuprofen on the developing North American Bullfrog (Rana catesbeiana) tadpole [J]. Environmental Science & Technology, 2014, 48(17): 10439-10447. [12] ZHAO D, FENG J, HUO Q, et al. Triblock copolymer syntheses of mesoporous silica with periodic 50 to 300 angstrom pores [J]. Science, 1998, 279(5350): 548-552. doi: 10.1126/science.279.5350.548 [13] SUN Q Q, WANG Y, LI L S, et al. Mechanism for enhanced degradation of clofibric acid in aqueous by catalytic ozonation over MnOx/SBA-15 [J]. Journal of Hazardous Materials, 2015, 286: 276-284. doi: 10.1016/j.jhazmat.2014.12.050 [14] SHU Z, CHEN Y, HUANG W M, et al. Room-temperature catalytic removal of low-concentration NO over mesoporous Fe-Mn binary oxide synthesized using a template-free approach [J]. Applied Catalysis B:Environmental, 2013, 140/141: 42-50. doi: 10.1016/j.apcatb.2013.03.030 [15] GHUGE S P, SAROHA A K. Ozonation of Reactive Orange 4 dye aqueous solution using mesoporous Cu/SBA-15 catalytic material [J]. Journal of Water Process Engineering, 2018, 23: 217-229. doi: 10.1016/j.jwpe.2018.04.009 [16] BING J S, HU C, ZHANG L L. Enhanced mineralization of pharmaceuticals by surface oxidation over mesoporous γ-Ti-Al2O3 suspension with ozone [J]. Applied Catalysis B:Environmental, 2017, 202: 118-126. doi: 10.1016/j.apcatb.2016.09.019 -



 下载:
下载: