-
二十世纪中叶以来,重(类)金属与抗生素复合污染已是环境领域的研究热点,其主要原因是全球人口持续增长以及工农业、医疗业、畜牧和水产养殖业的发展[1 − 2]. 我国由于农民耕作方式以及土壤地质特征、面源污染等,地表水和土壤受到多种污染物的交互影响,大量的类金属砷(As)、四环素类抗生素(Tetracyclines, TCs)进入水土环境[3- 4]. 据统计,我国约80%的水体受到不同程度的As污染,其中长江和珠江流域最为严重[5],其主河流中溶解态As的均值为3.1×10−3 mg·L−1,远高于其世界平均值1.0×10−4 mg·L−1. 2014年水利部报告指出,我国至少3亿人次饮用水不达标,约
1000 万人口饮用As超标水[6]. 此外,我国是抗生素生产和使用大国,其在我国的人均消耗量是英美等西方国家的六倍[7]. 研究发现,TCs在多种环境介质中频繁检出,其在污水处理厂出水、地表径流、地下水中常以ng·L−1或μg·L−1级别;由于TCs吸附性强,其在土壤和沉积物中检出浓度通常为μg·kg−1和mg·kg-1[8 − 10]. 而且,抗生素的大量使用,会进一步导致耐药性问题. 砷与四环素复合污染日趋严重,对人体健康及生态系统安全构成重大威胁.研发环境中砷与四环素复合污染的去除新技术是当前环境科学领域的研究热点. 近年来,介孔碳因具有独特的结构和性能优势,被广泛用于修复水土环境中砷与四环素的污染修复. 关于使用介孔碳修复砷或四环素单一污染体系的研究有较多的报道,而砷与四环素复合污染仍相对较少. 有研究表明,砷与四环素存在络合作用[11],导致污染物赋存形态更具复杂性和不确定性,去除难度更大. 因此,厘清砷与四环素的相互作用对介孔碳效能的影响关系,是实现高效去除或固定环境中的砷和四环素的研究重点和难点. 本文综述了近年来使用介孔碳修复水土环境砷与四环素污染的研究,重点讨论了介孔碳在不同制备方法的微结构特征、影响介孔碳效能的关键影响因子、作用机理及在污染物去除的应用,归纳了现阶段研究不足,并对砷与四环素复合污染的未来研究方向进行展望.
-
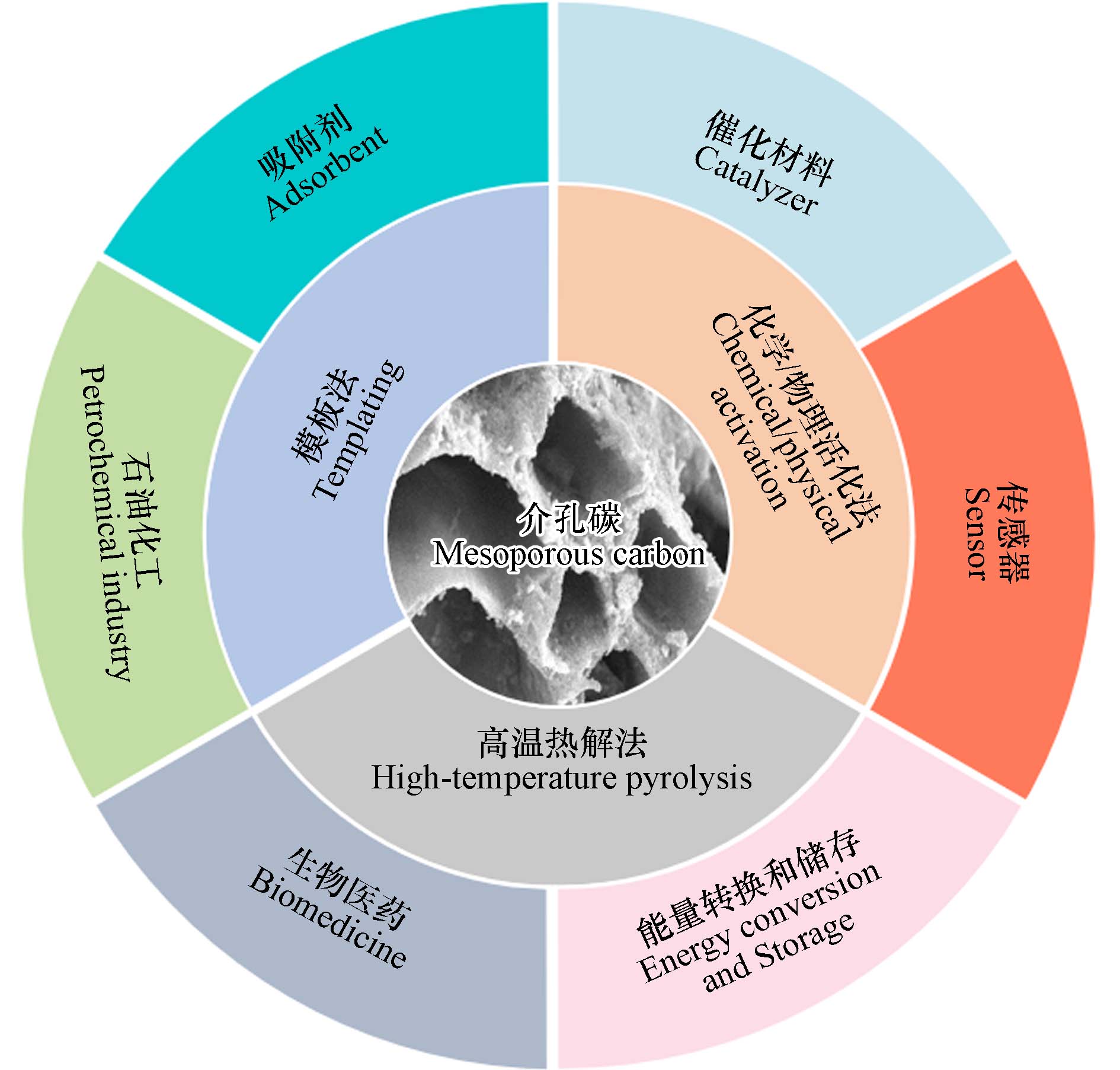
近几十年,多孔碳材料因独特的物理化学性质而成为环境、化学和材料科学等关注的焦点. 根据IUPAC定义,多孔材料按照孔径可分为微孔材料、介孔材料及大孔材料[12]. 介孔碳是一类新型非硅基材料,孔径在2—50 nm,具有较大的比表面积和孔体积,热稳定性高、化学性能好、多孔结构均匀可控、易于功能化等特点(见图1示意图),被广泛用作催化材料、吸附剂、能量转换和储存、石油化工、传感器和生物医药等领域,具有广泛的应用前景[13 − 15].
介孔碳之所以具有吸引力,是因为介孔碳的孔隙结构支持在多孔通道内或其表面掺入新的功能剂(有机或无机组分),从而改善其整体使用性能;另一方面,介孔碳较大的比表面积和孔径弥补了传统活性炭的局限性. 从几何结构角度来看,介孔碳既具有2D材料的高活性,又具有3D网络结构作为有效催化剂的强大稳定性,防止反应位点聚集退化;高度可接近的表面位点由于其高不饱和配位而表现出高活性. 离散的空隙不仅使亚稳反应中间体能够被捕获在反应位点上以进一步反应,而且还通过选择性相互作用浓缩反应物;均匀的通道/孔结构实现迅速的传质和尺寸筛分. 此外,可以通过表面修饰和封装手段,将具有明确和空间分离位置的多反应类型位点整合到一个颗粒上[16 − 17],以引入新的功能并完成复杂的反应. 因此,这些独特的结构特征使介孔碳材料成为合理设计高效环境功能材料的有前途的候选者.
-
介孔碳具有丰富的多孔结构和活性位点,能有效去除环境中的污染物. 常见的制备方法主要有模板法、化学/物理活化法和高温热解法(如图2所示).
(1)模板法
模板法是以模板为主要结构,通过控制尺寸诱导材料定向生长的合成方法,是目前最为常用的制备方法. 根据模板的类型不同可以分为硬模板法和软模板法.
①硬模板法
硬模板法制备主要分为四步[18]. 首先,制备硬模板,如选用胶态晶体、分子筛、天然矿物等在表面活性剂作用下合成模板. 然后,填充碳源,将前驱体填充至硬模板孔隙中. 随后,转化碳源,将前驱体在孔隙中聚合碳化形成碳-模板前驱体. 最后,去除硬模板,用HF或NaOH去除无机模板. RYOO等[19]采用硬模板法,首次以MCM48为硬模板,蔗糖为碳源,合成介孔碳. LIU等[20]利用纳米SiO2为模板,将纳米SiO2静电吸附十六烷基三甲基溴化铵,并通过乳液聚合制备不同纳米SiO2含量的聚丙烯腈/纳米SiO2复合材料,然后将颗粒高温碳化和蚀刻,得到高纯度介孔碳. 硬模板法制备的介孔碳虽形貌可控,但操作步骤复杂,模板材料昂贵,同时需消耗大量强酸强碱而耗费较大成本.
②软模板法
软模板法能有效克服硬模板法的缺点,其制备主要步骤有三步. 首先,自组装,将有机碳源与软模板通过库仑力、氢键作用、亲水/疏水作用等进行自组装. 然后,将模板剂去除,通过去除表面活性剂获得介孔聚合物材料. 最后,高温碳化,在惰性气体下高温碳化介孔聚合物,从而得到介孔碳. 赵东元等人[19]使用EISA法,以酚醛树脂为碳源,F127为导向剂,通过蒸发诱导自组装工艺制得F127-酚醛树脂复合物,并在N2保护下煅烧去除F127,使其炭化,最终得到介孔碳. 赵宝龙等人[21]以红薯粉为碳源,F127为模板剂,制备红薯粉介孔碳. 软模板法不仅步骤简单、易于调控,而且成本低、无需去除模板,但可选模板剂少、易造成二次污染、副产物较多、反应难以控制.
(2)化学/物理活化法
化学活化法指活化剂(KOH、ZnCl2、NaOH或H3PO4)与原材料按一定比例混合,在惰性气体下进行碳化和活化,进而获得介孔结构. UNER团队[22]以西瓜皮为原料,采用ZnCl2一步化学活化法制备介孔碳,在碳化温度为700 ℃时所得介孔碳比表面积为
1156 m2·g−1,总孔体积为1.41 cm3·g−1. 此外,该方法的活化剂用量可以控制介孔碳的比表面积,并且活化剂有效加快原材料中O和H结合生成水并脱离分解,有效降低碳化温度. 但活化剂在产物中仍有残留,副产物可能造成设备腐蚀. 物理活化法是以空气、CO2、水蒸气或它们的混合气体为活化剂,并于原料中的碳原子发生气化脱离碳表面,疏通碳材料被堵的孔或由逃逸通道形成新孔,进而形成介孔材料. GHOUMA等人[23]以橄榄核为原料,在750℃下经蒸汽物理活化制备介孔炭,其表面展现出含量高且不均匀的宏观孔隙度. 化学/物理活化法中活化剂的强氧化性以及难以控制的温度对孔隙的影响较大,而且碳的利用率低,生产成本高,因此在工业生产中并不常使用.(3)高温热解法
高温热解法是将生物质在无氧或低氧环境下高温加热,使生物质原料转化为生物质油、可燃气体和生物炭[24, 25]. 该方法中,首先将干燥的生物质原料放入马弗炉中. 然后用真空泵将炉内的空气抽出以形成热解条件,以一定的速率将炉子加热到一定温度,最后将氮气注入炉中. 具有介孔结构的生物炭也称为介孔生物炭. 高温热解可提高生物炭的比表面积及孔隙率,从而提高介孔生物炭的性能[26]. 该方法根据反应时间的不同分为慢速热解、中速热解和快速热解. 三种工艺的成炭率、气体与生物质油的比例等基本性质见下表1. 三种热解法产物的比例随加热温度和加热速率的变化而变化. 温度和加热速率需控制在较低水平方可提高生物炭的产出率. 但温度过低将造成碳化不完全,时间过长则影响成炭率. 快速热解因升温速率快使有机质分解较快,气体因停留时间短而挥发逸出,造成生物油产量高、成炭率低. 此外,生物炭内部因热解过快易形成大孔造成结构不稳定、比表面积小. 与其相比,慢速热解因升温速率低、停留时间长,生物炭产率可以最大化,性能更好.
(4)其它
除以上制备介孔碳的方法,还有乳液法[27]、溶胶-凝胶法[28]、水热法[17]、气化技术[24, 29]、微波热解技术[24, 29]、闪蒸炭化技术[29]等. 这些新兴技术可以有效调控介孔碳中其它元素的含量以及孔隙结构,近年来得到快速的发展.
-
水体As的去除方法主要有:混凝沉淀法、离子交换法和吸附法等,其中吸附法因成本低、效果优良和绿色环保而被广泛使用. 江湛如等[30]以海藻酸钠为前驱体,通过高温热解制备磁性海藻酸铁介孔碳,并重点研究pH值、投加量、时间、污染物初始浓度对介孔碳吸附As3+和As5+的影响. 结果显示,介孔碳可以较好的吸附As3+和As5+,且对As3+的吸附效果更为显著;当5<pH<7时,介孔碳对As3+和As5+的吸附性能最好. 冯彦房等[31]以玉米秸秆为原料制备载镧介孔生物炭吸附水中的As5+. 结果显示,负载后的介孔生物炭可较好的吸附As5+,此外,中性和酸性条件有利于砷酸根的吸附.
梁欣冉等[32]通过吸附实验和土壤培养实验,分析铁改性介孔生物炭对土壤As的吸附和钝化能力. 研究表明,共沉淀法制备的铁改性介孔生物炭可有效促进非专性吸附态砷转化为残渣态砷,对砷的去除率为21.40%—34.14%. 钱子研等[33]通过盆栽实验研究不同As污染程度下,施加铁改性介孔生物炭对土壤-水稻系统中砷的有效性和迁移性的影响. 结果表明,施加铁改性介孔生物炭能有效降低土壤中砷的浓度,当土壤砷的浓度为120 mg·kg−1时,施加1%铁改性介孔生物炭后,As浓度降低了30.56%.
-
由于抗生素的亲水性、持久性,使得其极易在水环境中残留. LI等[34]将木材经800 ℃的高温热解制备介孔生物炭,对水体中抗生素的吸附量最大可达163 mg·g−1. 马峰峰等[35]以猪粪、β-环糊精为原料制备改性猪粪生物炭,结果显示,酸性条件下更有助于四环素的吸附;与猪粪生物炭相比,改性猪粪生物炭对四环素的吸附效果更显著,最大吸附量为53.51 mg·g−1. 徐晋等[36]使用KOH对小麦秸秆进行活化,所制备的生物炭具有介孔结构,可用于对水体四环素的吸附. 结果显示,该改性生物炭对四环素的最大吸附量为491.19 mg·g−1.
介孔碳因其较大的比表面积和丰富的官能团,可有效吸附/催化降解抗生素. 李文斌等[37]按1%质量比将介孔生物炭添加至嘉陵江流域采集的供试土样中,结果显示,添加生物炭后,该土壤对四环素的吸附量提高了15.41%—167.47%. 此外,土样在40℃、离子强度为0.1 mol·L−1、pH=3的条件下对四环素的吸附量最大. 李慧君等[38]以甘蔗渣制备介孔生物炭,探究其不同剂量(1%、2%、3%)对四环素的修复效果. 结果显示,添加生物炭后显著提高了四环素的降解,其中添加2%生物炭的去除率为79.50%,并有效提高了土壤pH值、有机质和腐殖质的含量.
-
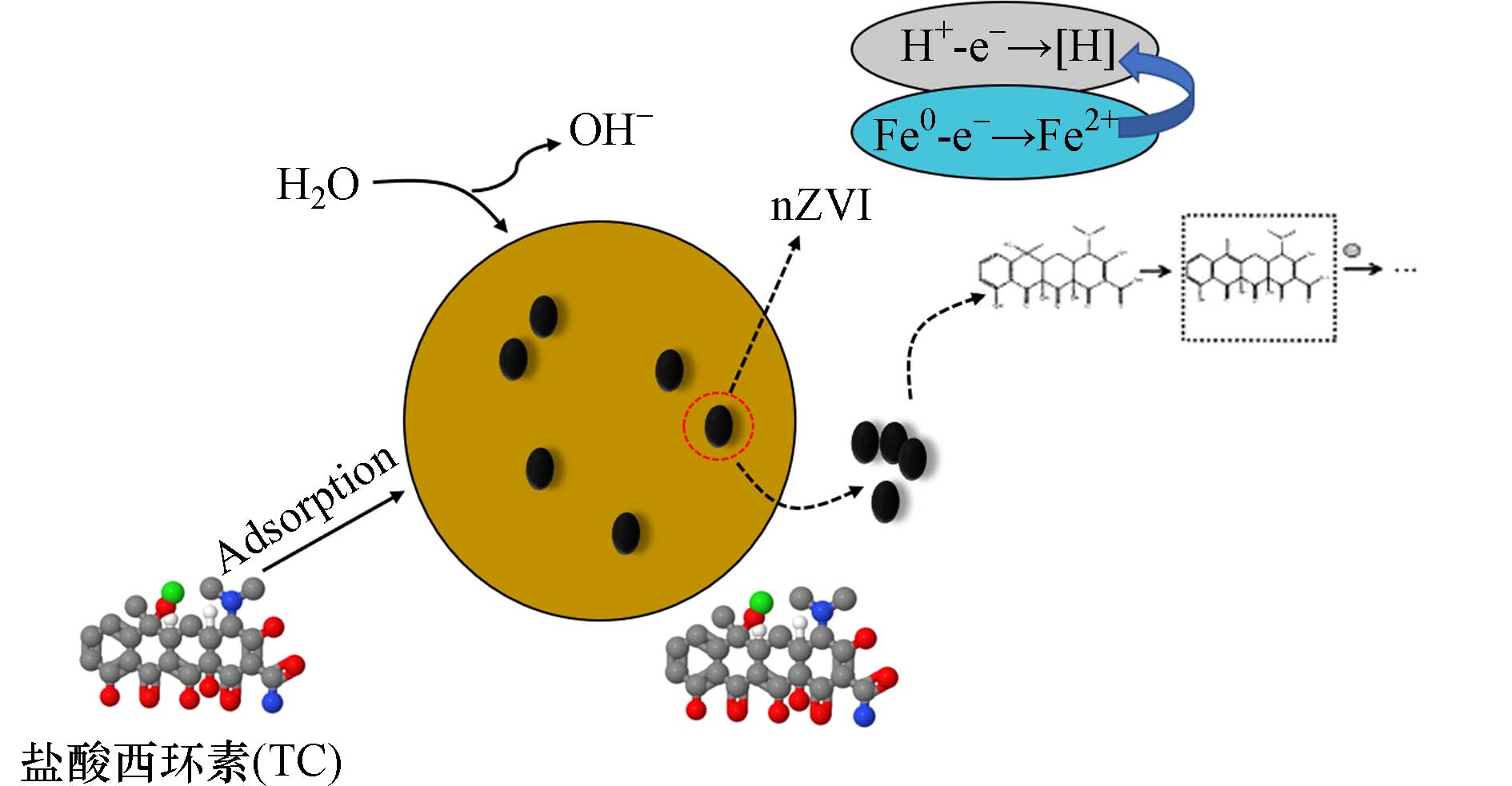
环境污染往往表现为多污染物复合污染,目前,介孔碳去除As与四环素复合污染的研究相对较少. 刘子璇等[39]以葡萄籽提取液为还原剂制备风车草生物炭负载纳米零价铁(CBC-nZVI),研究CBC-nZVI去除水体中As与四环素的机制(如图3所示). CBC-nZVI投加量为0.5 g、溶液初始浓度500 mg·L−1、pH 8.0、温度45℃、反应时间120 min时,对As3+的去除量最大,为103.78 mg·g−1;对四环素的最佳去除条件为投加量0.8 g、溶液初始浓度500 mg·L−1、pH 7.0、温度65 ℃、反应时间120 min时,最大去除量为102.52 mg·g−1. CBC-nZVI对As的去除机理,一方面是生物炭表面的FeOOH将As3+部分氧化为As5+,另一方面Fe2+/Fe3+发生复杂的转化反应,生成铁(氢)氧化物,实现对As3+/As5+的共沉淀;而CBC-nZVI对四环素的去除是通过阳离子交换与静电作用. 四环素与CBC结合,再由Fe0与CBC形成了原电池效应,通过阴极上CBC表面的电子传输,将氢离子转化形成原子氢促进四环素的降解. CBC-nZVI对四环素和As3+的去除量与投加量、离子浓度、pH呈正相关.
刘文贵等[40]用微波热解技术和药剂稳定化/微波固定联用技术分别研究稻壳鸡粪中残留的四环素和As. 研究表明,FeSO4·7H2O可显著提高稻床养鸡固废对微波吸收作用,升稻壳鸡粪中四环素的微波热解效果,并对砷具有更强的稳定/固定化作用,其中FeSO4·7H2O同时起到了共沉淀稳定剂和微波敏化剂的关键作用. 当FeSO4·7H2O含量为10%,微波条件为560W、20 min下,四环素的消减率高于95%. 当FeSO4·7H2O添加量为5%,700 W、20 min的微波条件下,稻壳鸡粪中砷的稳定/固化率达到了96.1%.
-
物理作用主要为物理吸附,即介孔碳利用其大的孔隙率和比表面积,使重(类)金属或有机物吸附在其表面,吸附能力与孔隙结构呈正相关. 当介孔碳表面含有碱性矿物、带负电荷的官能团时,其吸附性能进一步提高[29]. ZHANG等人[41]通过球磨生物炭而改变生物炭的表面结构,使更多吸附位点得以暴露,从而提高四环素的吸附量,拟合的吸附动力学和等温式模型也证实了其主要机制为孔隙填充的物理吸附.
-
(1)离子交换
介孔碳表面的羟基、羧基等官能团,可与水溶液的阳离子或阴离子发生离子交换,反应如下:
生物质含有大量K、Na、Mg等矿物元素,在制备介孔碳时难免残留在内. 这些矿物元素在水体中溶出,并与水体中的重金属或质子化酸性官能团发生离子交换作用,从而可使重金属去除. MERODIO等[42]通过改性生物炭吸附五价砷,结果显示砷离子的吸附机理包括静电吸引和羟基的离子交换作用. FTIR对吸附剂表面官能团的定性分析表明对五价砷吸附过程中以离子交换为主.
(2)静电吸引
静电吸引是介孔碳吸附金属离子和可电离有机物的主要机制,吸附剂与吸附质带异种电荷时发生静电吸引反应,反之发生静电排斥反应. 介孔碳表面的含氧官能团(酚羟基和羧基等)在溶液中去质子化后带负电,可通过静电引力与金属阳离子发生反应. AGRAFIOTI等[43]研究发现改性生物炭作为吸附剂对水溶液中As5+的去除的主要机制是静电相互作用.
(3)沉淀反应
介孔碳对重金属的沉淀反应主要有两种途径[29]:介孔碳的加入增加了原有环境的pH值,使重金属离子析出,从而降低重金属的迁移能力;介孔碳中的PO43−、CO32−等无机/改性组分与重金属离子发生反应形成沉淀,如纳米零价铁改性介孔碳释放的铁氧化物与As作用生成FeAsO4·2H2O沉淀[44].
(4)络合反应
络合反应是电子给体和电子受体相互作用形成配合物的过程. 电子给体是电子对的提供者,而受体是金属离子或有机化合物. 分子或离子与金属离子相互结合形成非常稳定的新离子的过程称为络合反应或配位反应. WANG等[45]研究了生物炭负载零价铁纳米复合材料对水溶液中砷酸盐的吸附机理,表面络合可能是去除As5+的主要机制.
(5)氧化还原反应
介孔碳首先将污染物吸附于表面并作为电子供体或受体诱导污染物发生氧化还原,改变污染物的价态,进而降低污染物毒性或迁移性. 砷在土壤中的主要存在形式为As3+和As5+,As3+毒性远大于As5+,由此降低砷危害的关键是将As3+转化为As5+. 据VITHANAGE等研究[46],介孔生物炭表面的氧化铁可将As3+转化为低毒的As5+,反应过程如下表示:
(6)催化反应
据研究,介孔碳可以通过光催化、电催化和化学催化等去除抗生素. 由于材料介孔结构提高吸光率的同时又能防止颗粒聚集,因此介孔碳在抗生素吸附/降解研究中发挥重要作用[47]. 此外,介孔碳表面丰富的官能团使其具有良好的氧化还原特性及接受/提供电子的能力.
-
介孔碳的施用不仅增加水土环境中的有机质含量,而且能影响水土环境中微生物的活性、丰度、群落结构等. 然而,不同制备来源的介孔碳对微生物具有不同的影响,介孔碳可通过促进或抑制某些特定微生物群落达到去除污染物的目的. 研究证实,介孔碳可为微生物提供养分和附着点等适宜的生存条件,使其活性增强,进而提高其对污染物的降解能力[48]. 尤其是当介孔碳表面负载功能菌,可通过新陈代谢固定/降解水土环境中污染物,从而起到修复效果. JI等[49]研究玉米秸秆介孔生物炭与混合菌联用修复土壤As污染,微生物可促进PbAs2O6和Cd3(AsO4)2沉淀的生成,而使重金属砷的固定效率远高于原始生物炭. 然而,也有研究发现介孔碳的施用可能会对某些微生物产生负面影响. 赵远超等[50]研究发现, 土壤加入生物炭后降低了携带四环素抗性基因的大肠杆菌的数量.
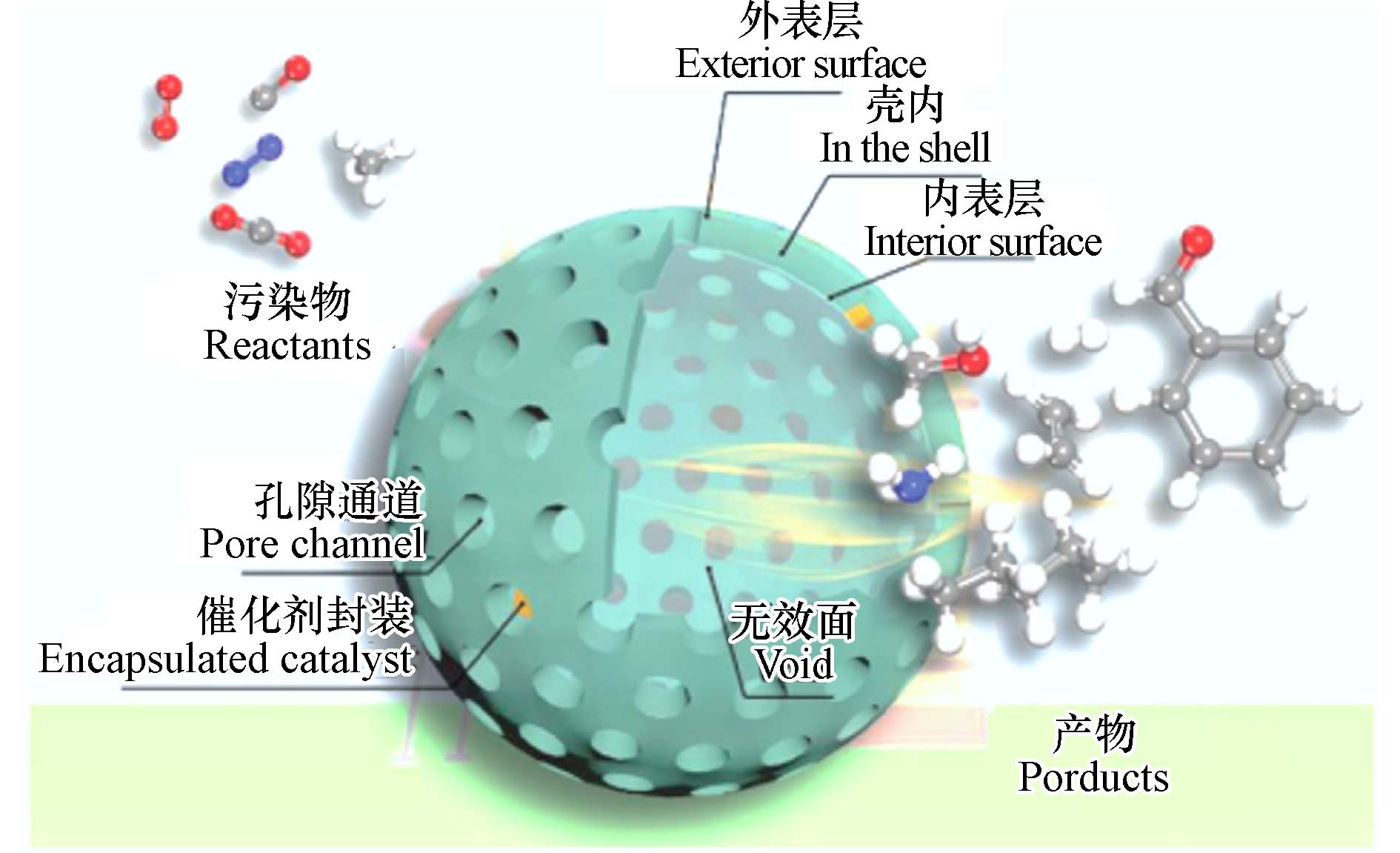
实际上,介孔碳对污染物的作用过程并非单一,而往往是多种反应机理同时进行(如图4所示). 介孔碳对污染物的主要作用机理取决于其孔径、比表面积、官能团种类及周围环境,本质上与原料性质、制备/改性方法密切相关. 不同制备方法的介孔碳去除污染物的主要作用机制展示如表2.
-
介孔碳的吸附能力受到多种环境因素的影响. pH、温度、共存离子干扰物、溶解性有机碳、微生物等均会影响介孔碳的吸附效果. 一般地,环境影响因素的扰动会显著改变介孔碳的吸附效果,但本质上介孔碳的吸附能力由其自身性质决定.
-
环境中的pH值影响污染物赋存形态,同时也影响介孔碳的表面电荷密度,进而影响介孔碳对污染物的吸附效果[63]. 当环境pH值<表面电荷零点(pHPZC),介孔碳表面的官能团因发生质子化而使其表面带正电,与带正电的金属离子相斥,限制了其对重金属的吸附作用. 反之,当pH > pHPZC,介孔碳表面带负电,则有利于吸附阳离子. 此外,pH较高时,金属离子易发生沉淀而难以被生物炭吸附. 一般而言,介孔炭去除四环素在酸性条件下更佳,因为在酸性条件下静电相互作用、π-π电子供体-受体作用和氢键的作用会增加,随着pH值的升高,四环素类抗生素的吸附速率降低[64].
-
温度影响介孔碳的理化性质和结构特性. 介孔碳的高吸附能力取决于高比表面积,而比表面积受温度影响[65]. 低温可获得较高的生物炭产量,高温可获得更大的孔隙度[66]. 如低温(200—400 ℃)制备的生物炭含有羧基和酚羟基,O/C摩尔比更高,更适合去除污染物. 此外,污染物因温度的升高而具有更多能量,从而提高其扩散速率而到达吸附位点,增强污染物、氧化剂和催化剂之间的接触;离子交换过程也需要吸收热量,高温可促进离子交换[67]. JOHANSSON等[68]研究发现两种藻类衍生铁基生物炭的吸附效率随热解温度的升高而降低,通过300 ℃热解制备最佳生物炭,其吸附量为80.7 mg·g−1. HU等[69]以竹笋壳所制备的介孔碳发现,高温可促进Cr(Ⅵ)的吸附,而抑制Cu(Ⅱ)的吸附. HU和CHEN等[70]在百香果壳改性生物炭中活化过氧一硫酸盐降解盐酸四环素,结果表明,随着温度从20 °C升至40 °C,四环素的降解率从82%提高到93%. 较高的温度可以活化过硫酸盐生成更多的活性物种,并促进催化剂与过硫酸盐之间的电子转移,有利于有机污染物的降解.
-
环境中的共存离子(Na+、K+、Ca2+、PO43−、SO42−)可与环境中的污染物竞争吸附位点,或与重金属发生离子交换,从而限制了介孔碳对污染物的去除. 不同的离子对介孔炭吸附污染物的影响不同. 阴离子对介孔炭吸附影响不大,阳离子能不同程度地促进或抑制介孔炭的吸附[71]. PAN等[72]研究表示,当Na+和Ca2+存在于溶液中,表面官能团会与这些离子反应,从而减少介孔炭对四环素的吸附. 共存磷酸盐阴离子与砷具有类似的化学性质,通过竞争吸附增强As从土壤中的解吸. BAIG等[69]研究发现PO43−显著降低生物炭对As5+的吸附,因为PO43−和AsO43−具有相似的离子结构,可以竞争相同的吸附位点.
-
DOC是介孔碳修复As污染土壤的关键因素,因为它影响As的迁移,而不受土壤类型的影响[73]. DOC不仅是土壤中最具流动性的有机配体,而且DOC可以通过竞争吸附增强As的解吸[74]. DOC和As在土壤表面对吸附位点的竞争会导致水中As浓度的增加. 此外,在有机碳含量高的土壤中,DOC会与As发生络合而影响介孔碳对其吸附[56]. 土壤DOC由于带负电,与四环素通过静电吸引结合,提高对四环素的吸附量.
-
介孔碳的多孔结构和灰分可为微生物的生长提供空间和营养,微生物因此成功附着于介孔碳,从而使得污染物转移到具有降解或固定功能的微生物群落. 功能微生物通过代谢作用、免疫调节等分解或固定污染物. 目前已分离出可耐受砷镉重金属的功能微生物有氧化亚铁硫杆菌、富养产碱菌、假单胞菌属等[75].
-
水土环境中砷和四环素复合污染对生态环境构成了重大威胁,尤其是我国长江流域和珠江流域等沿海地区. 介孔碳可能是治理砷与四环素复合污染的理想材料. 尽管研究学者已经发表了一些学术论文,但仍处于起步阶段,为此我们应重点关注以下几个研究方向:
(1)单一污染的研究较多,但复合污染的研究仍相对较少. 应更准确、更有效地评估介孔碳对多污染体系的机制研究,从分子水平揭示材料与目标污染物反应的构效关系.
(2)砷存在有机砷物种,比如甲基砷和硫代砷,在使用介孔碳催化降解抗生素与砷复合污染研究中,很少关注到有机砷物种及其对抗生素降解转化的影响.
(3)微生物对重金属和抗生素的影响应该进一步考虑,大多数研究只考虑改性介孔碳对土壤重金属或抗生素去除效应,但土壤中微生物类型很多,施用介孔碳后,微生物必然发生变化,从而间接影响重金属或抗生素在微生物群落间的迁移转化.
(4)实际水和土壤基质比仅含单污染物的纯水实验要复杂,应该更多的使用不同场景的污水、农田土壤、富含砷和四环素的土壤综合评估材料的效果.
介孔碳对水土环境中砷与四环素复合污染修复的研究进展
Research progress on the remediation of arsenic and tetracycline combined pollution in soil and water environment by mesoporous carbon
-
摘要: 水土环境中砷与四环素复合污染已是环境领域的研究热点. 介孔碳因具有独特的微观结构和性能优势,在吸附和催化氧化等方面对污染物具有优异的去除效果而备受关注. 然而,研究者们集中关注于砷与抗生素复合污染的毒理效应,对其相互作用及影响过程研究尚少. 本文通过总结介孔碳的制备方法、关键影响因子及其作用机理,综述了介孔碳对砷与抗生素修复应用的研究与发展现状,归纳了现阶段研究不足,同时对介孔碳在砷与抗生素复合污染的研究趋势进行了展望.Abstract: The combined pollution of arsenic and tetracycline in soil and water environment has become a research hotspot in the field of environment. Mesoporous carbon has attracted much attention due to its unique microstructure and performance advantages, which have excellent removal effects on pollutants in adsorption and catalytic oxidation. However, researchers have focused on the toxicological effects of arsenic combined with antibiotic contamination, and there is still little research on their interactions and influencing processes. This article summarizes the preparation methods, key influencing factors, and mechanism of action of mesoporous carbon, summarizes the research and development status of its application in arsenic and antibiotic remediation, summarizes the current research shortcomings, and looks forward to the research trend of mesoporous carbon in arsenic and antibiotic composite pollution.
-
Key words:
- mesoporous carbon /
- arsenic /
- tetracycline /
- interaction /
- mechanism
-

-
表 1 三种工艺类型的反应条件及产物比列[26]
Table 1. Reaction conditions and product ratios for three types of processes[26]
工艺类型
Process type温度/℃
Temperature反应时间
Reaction time加热速率/(℃·s−1)
Heating rate生物油比例/%
Biooil ratio气体比例/%
Gas ratio成炭率/%
Charcoal formation rate慢速热解 300—550 5—30 min 0.1—0.8 20—50 15—20 25—35 中速热解 300—450 10—20 min 3—5 35—50 20—30 25—40 快速热解 300- 1000 <2 s 10— 1000 50—70 15—20 10—30 表 2 不同制备方法的介孔碳去除污染物的主要作用机制
Table 2. The main mechanism of pollutants removal by mesoporous carbon with different preparation methods
制备方法
Preparation
method改性方法
Modification
method污染物
Pollution吸附量/(mg·g−1)
Adsorption
capacity去除率/%
Removal rate主要作用机制
Main mechanism参考文献
References高温裂解 Fe As(Ⅲ)/As(Ⅴ) 82.97/50.52 — 物理吸附、化学吸附 [30] 热解法 La3+ As(Ⅴ) — 89.74 静电吸引 [31] 热解法 Fe As(Ⅲ) — 29.61 静电吸引、离子交换、沉淀或络合反应 [32] 热解法 富含Ca As(Ⅲ) 69.03 — 络合作用、沉淀作用、氧化作用、静电吸引 [51] 模板法 Fe3O4 As(Ⅲ)/As(Ⅴ) 121.35/188.75 — 化学吸附、静电吸引、络合作用 [52] 热解法 小麦秸秆源 总As — 60.25 物理吸附、化学吸附、离子交换、扩散吸附 [53] 热解法 虾壳源 As(Ⅲ)/As(Ⅴ) 7.71/8.40 — 物理吸附、静电吸引、络合作用 [54] 热解法 针铁矿 As(Ⅲ) 149.63 88.9—94.2 络合作用、离子交换、沉淀作用 [55] 热解法 鸡粪源 As(Ⅲ) — 98 静电吸引、离子交换 [56] 热解法 Fe、Mn As(Ⅲ) 4.1 — 物理吸附、氢键、静电吸引 [57] 热解法 β-环糊精 Tc 53.5 — 静电反应、氢键、π-π相互作用 [35] 化学活化法 小麦秸秆源 Tc 491.19 — 孔隙填充、π-π相互作用、氢键、络合作用 [36] 热解后活化 鸡血藤渣 Tc 78.32 — 孔隙填充、π-π相互作用、氢键 [58] 活化法 木薯乙醇污泥 Tc 154.45 — 静电吸引、氢键、孔隙填充、π-π相互作用 [59] 水热法 微藻 Tc 142.4 — 孔隙填充、π-π相互作用、氢键作用 [60] 软模板法 F127 Tc 238.7 — 孔隙填充、氢键作用、π-π相互作用 [61] 热解法 核桃壳 Tc 607.0±31.87 — 孔隙填充、氢键作用、π-π相互作用、氢键 [62] 热解法 虾壳源 Tc 800.6 — 孔隙填充、络合作用、氢键、静电吸引 [63] -
[1] 卫承芳, 李佳乐, 孙占学, 等. 水-土壤环境中抗生素污染现状及吸附行为研究进展[J]. 生态毒理学报, 2022, 17(3): 385-399. WEI C F, LI J L, SUN Z X, et al. Research progress of antibiotic pollution and adsorption behavior in water-soil environment[J]. Asian Journal of Ecotoxicology, 2022, 17(3): 385-399 (in Chinese).
[2] ZHANG Q Q, YING G G, PAN C G, et al. Comprehensive evaluation of antibiotics emission and fate in the river basins of China: Source analysis, multimedia modeling, and linkage to bacterial resistance[J]. Environmental Science & Technology, 2015, 49(11): 6772-6782. [3] 杨惠程, 崔小燕, 孙千鸿. 环境中四环素类抗生素污染处理技术研究进展[J]. 清洗世界, 2022, 38(9): 81-83. YANG H C, CUI X Y, SUN Q H. Research progress on treatment technology of tetracycline antibiotics pollution in the environment[J]. Cleaning World, 2022, 38(9): 81-83 (in Chinese).
[4] YU H Y, WANG X Q, LI F B, et al. Arsenic mobility and bioavailability in paddy soil under iron compound amendments at different growth stages of rice[J]. Environmental Pollution, 2017, 224: 136-147. doi: 10.1016/j.envpol.2017.01.072 [5] 罗明科. 生物炭接枝和负载改性及其对重金属砷、镉吸附去除性能[D]. 北京: 北京科技大学, 2020. Luo M. Grafting and loading modification of biochar and its adsorption and removal performance for heavy metals arsenic and cadmium[D]. Beijing: Beijing University of Science and Technology, 2020.
[6] 吕倩, 魏洁云. 中国地下水污染现状及治理[J]. 生态经济, 2016, 32(10): 10-13. LYU Q, WEI J Y. Current situation and treatment of groundwater pollution in China[J]. Ecological Economy, 2016, 32(10): 10-13 (in Chinese).
[7] TANG J P, WANG S, TAI Y P, et al. Evaluation of factors influencing annual occurrence, bioaccumulation, and biomagnification of antibiotics in planktonic food webs of a large subtropical river in South China[J]. Water Research, 2020, 170: 115302. doi: 10.1016/j.watres.2019.115302 [8] 王娜, 郭欣妍, 单正军, 等. 农田土壤抗生素污染管控建议[J]. 中国工程科学, 2021, 23(1): 167-173. doi: 10.15302/J-SSCAE-2021.01.023 WANG N, GUO X Y, SHAN Z J, et al. Suggestions for management and control of antibiotics in farmland soil in China[J]. Strategic Study of CAE, 2021, 23(1): 167-173 (in Chinese). doi: 10.15302/J-SSCAE-2021.01.023
[9] 朱冬, 陈青林, 丁晶, 等. 土壤生态系统中抗生素抗性基因与星球健康: 进展与展望[J]. 中国科学:生命科学, 2019, 49(12): 1652-1663. doi: 10.1360/SSV-2019-0267 ZHU D, CHEN Q L, DING J, et al. Antibiotic resistance genes in the soil ecosystem and planetary health: Progress and prospect[J]. Scientia Sinica (Vitae), 2019, 49(12): 1652-1663 (in Chinese). doi: 10.1360/SSV-2019-0267
[10] SUN J T, ZENG Q T, TSANG D C W, et al. Antibiotics in the agricultural soils from the Yangtze River Delta, China[J]. Chemosphere, 2017, 189: 301-308. doi: 10.1016/j.chemosphere.2017.09.040 [11] 乔娜. 高铁酸钾控制水体典型抗生素与重金属复合污染的研究[D]. 南京: 东南大学, 2021. QIAO N. Study on potassium ferrate to control the combined pollution of typical antibiotics and heavy metals in water body[D]. Nanjing: Southeast University, 2021 (in Chinese).
[12] ZHU W, CHEN Z, PAN Y, et al. Functionalization of hollow nanomaterials for catalytic applications: Nanoreactor construction[J]. Advanced Materials, 2019, 31(38): 1800426. doi: 10.1002/adma.201800426 [13] SHAHRAM M, ELHAM A. Mesoporous carbon-based materials: A review of synthesis, modification, and applications[J]. Catalysts, 2022, 13(1): 2. doi: 10.3390/catal13010002 [14] BENZIGAR M R, TALAPANENI S N, JOSEPH S, et al. Recent advances in functionalized micro and mesoporous carbon materials: Synthesis and applications[J]. Chemical Society Reviews, 2018, 47(8): 2680-2721. doi: 10.1039/C7CS00787F [15] LINARES N, SILVESTRE-ALBERO A M, SERRANO E, et al. Mesoporous materials for clean energy technologies[J]. Chemical Society Reviews, 2014, 43(22): 7681-7717. doi: 10.1039/C3CS60435G [16] 张巧利, 徐强, 张媛媛, 等. 磁性介孔碳的制备及对水体中染料的吸附去除[J]. 环境化学, 2018, 37(11): 2548-2554. doi: 10.7524/j.issn.0254-6108.2018020503 ZHANG Q L, XU Q, ZHANG Y Y, et al. Preparation of magnetic mesoporous carbon and its application for dyes removal from water[J]. Environmental Chemistry, 2018, 37(11): 2548-2554 (in Chinese). doi: 10.7524/j.issn.0254-6108.2018020503
[17] QIAO Z A, ZHANG P F, CHAI S H, et al. Lab-in-a-shell: Encapsulating metal clusters for size sieving catalysis[J]. Journal of the American Chemical Society, 2014, 136(32): 11260-11263. doi: 10.1021/ja505903r [18] 屈佳, 李美兰, 黄宏普, 等. 有序介孔碳的模板化构筑及其水处理应用研究[J]. 精细化工, 2020, 37(12): 2435-2446. QU J, LI M L, HUANG H P, et al. Template construction of ordered mesoporous carbon materials and their applications in water treatment[J]. Fine Chemicals, 2020, 37(12): 2435-2446 (in Chinese).
[19] 田喜强, 赵宏吉, 董艳萍, 等. 介孔碳的合成及水处理的研究进展[J]. 化学工程师, 2019, 33(1): 49-52. TIAN X Q, ZHAO H J, DONG Y P, et al. Research progress in synthesis of mesoporous carbon and water treatment[J]. Chemical Engineer, 2019, 33(1): 49-52 (in Chinese).
[20] XI J G, LI H, XI J M, et al. Preparation of high porosity biochar materials by template method: A review[J]. Environmental Science and Pollution Research, 2020, 27(17): 20675-20684. doi: 10.1007/s11356-020-08593-8 [21] 赵宝龙. 生物质源多孔炭材料的制备及对四环素的吸附性能研究[D]. 郑州: 华北水利水电大学, 2021. ZHAO B L. Preparation of biomass-derived porous carbon materials and study on its adsorption performance for tetracycline[D]. Zhengzhou: North China University of Water Resources and Electric Power, 2021 (in Chinese).
[22] ÜNER O, GEÇGEL Ü, BAYRAK Y. Preparation and characterization of mesoporous activated carbons from waste watermelon rind by using the chemical activation method with zinc chloride[J]. Arabian Journal of Chemistry, 2019, 12(8): 3621-3627. doi: 10.1016/j.arabjc.2015.12.004 [23] GHOUMA I, JEGUIRIM M, DORGE S, et al. Activated carbon prepared by physical activation of olive stones for the removal of NO2 at ambient temperature[J]. Comptes Rendus Chimie, 2015, 18(1): 63-74. [24] 汪佳玥, 凌茜, 张雲豪, 等. 生物炭制备方法及其在环境污染治理中的应用研究[J]. 南通大学学报(自然科学版), 2022, 21(4): 1-14. WANG J Y, LING (Q /X), ZHANG Y H, et al. Study on preparation method of biochar and its application in environmental pollution control[J]. Journal of Nantong University (Natural Science Edition), 2022, 21(4): 1-14 (in Chinese).
[25] ZHANG H Y, YUE X P, LI F, et al. Preparation of rice straw-derived biochar for efficient cadmium removal by modification of oxygen-containing functional groups[J]. Science of the Total Environment, 2018, 631/632: 795-802. doi: 10.1016/j.scitotenv.2018.03.071 [26] HAO M J, QIU M Q, YANG H, et al. Recent advances on preparation and environmental applications of MOF-derived carbons in catalysis[J]. Science of the Total Environment, 2021, 760: 143333. doi: 10.1016/j.scitotenv.2020.143333 [27] 赵筱茜, 王聪, 田勇, 等. 微乳液法制备介孔碳材料[J]. 化学进展, 2022, 34(10): 2316-2328. ZHAO X (Q /X), WANG C, TIAN Y, et al. Preparation of mesoporous carbon materials by microemulsion method[J]. Progress in Chemistry, 2022, 34(10): 2316-2328 (in Chinese).
[28] 王旭阳, 汪颖军, 所艳华, 等. MCM-48介孔材料的制备及其催化应用的研究进展[J]. 化学与粘合, 2020, 42(5): 383-387. WANG X Y, WANG Y J, SUO Y H, et al. Research progress in preparation and catalytic application of MCM-48 mesoporous materials[J]. Chemistry and Adhesion, 2020, 42(5): 383-387 (in Chinese).
[29] LIANG M N, LU L, HE H J, et al. Applications of biochar and modified biochar in heavy metal contaminated soil: A descriptive review[J]. Sustainability, 2021, 13(24): 14041. doi: 10.3390/su132414041 [30] 江湛如, 汤媛媛, 李冰玉, 等. 磁性海藻酸铁介孔碳微球的合成及对水体中砷的去除[J]. 环境科学学报, 2018, 38(6): 2382-2392. JIANG Z R, TANG Y Y, LI B Y, et al. Synthesis of magnetic alginate mesoporous carbon for the removal of As from water solution[J]. Acta Scientiae Circumstantiae, 2018, 38(6): 2382-2392 (in Chinese).
[31] 冯彦房, 薛利红, 杨梖, 等. 载镧生物炭的优化制备及其对水体中砷的吸附[J]. 中国环境科学, 2015, 35(8): 2433-2441. FENG Y F, XUE L H, YANG B, et al. Optimized preparation of lanthanum uploaded biochar and its application in adsorbing pentavalent arsenic ions from aqueous solution[J]. China Environmental Science, 2015, 35(8): 2433-2441 (in Chinese).
[32] 梁欣冉, 何丹, 郑曌华, 等. 两种铁改性生物炭对微碱性砷镉污染土壤的修复效果[J]. 环境科学, 2023, 44(7): 4100-4108. LIANG X R, HE D, ZHENG Z H, et al. Remediation effect of two iron-modified biochars on slightly alkaline arsenic and cadmium contaminated soil[J]. Environmental Science, 2023, 44(7): 4100-4108 (in Chinese).
[33] QIAN Z Y, XUE S G, CUI M Q, et al. Arsenic availability and transportation in soil-rice system affected by iron-modified biochar[J]. Journal of Central South University, 2021, 28(6): 1901-1918. doi: 10.1007/s11771-021-4738-2 [34] LI C Y, ZHU X X, HE H L, et al. Adsorption of two antibiotics on biochar prepared in air-containing atmosphere: Influence of biochar porosity and molecular size of antibiotics[J]. Journal of Molecular Liquids, 2019, 274: 353-361. doi: 10.1016/j.molliq.2018.10.142 [35] 马锋锋, 张建, 赵保卫, 等. β-环糊精改性猪粪生物炭对水中四环素的吸附特性及机制[J]. 环境工程学报, 2022, 16(8): 2480-2489. MA F F, ZHANG J, ZHAO B W, et al. Adsorption characteristics and mechanism of tetracycline in water by swine manure biochar modified with β-cyclodextrin[J]. Chinese Journal of Environmental Engineering, 2022, 16(8): 2480-2489 (in Chinese).
[36] 徐晋, 马一凡, 姚国庆, 等. KOH活化小麦秸秆生物炭对废水中四环素的高效去除[J]. 环境科学, 2022, 43(12): 5635-5646. XU J, MA Y F, YAO G Q, et al. Efficient removal of tetracycline from wastewater by KOH activated wheat straw biochar[J]. Environmental Science, 2022, 43(12): 5635-5646 (in Chinese).
[37] 李文斌, 陈芯怡, 邓红艳, 等. 外源生物炭对嘉陵江流域川渝段沿岸土壤四环素吸附特征的影响[J]. 土壤通报, 2020, 51(2): 487-495. LI W B, CHEN X Y, DENG H Y, et al. Effects of exogenous biochar on tetracycline adsorption by different riverbank soils from Sichuan and Chongqing section of Jialing River[J]. Chinese Journal of Soil Science, 2020, 51(2): 487-495 (in Chinese).
[38] 李慧君, 卫婷, 黄枫城, 等. 生物炭对四环素污染土壤微生物群落结构的影响及环境因子关联的剂量效应分析[J]. 农业环境科学学报, 2023, 42(1): 101-111. LI H J, WEI T, HUANG F C, et al. Effect of biochar on microbial community structure in tetracycline contaminated soil and dose-effect analysis of environmental factors[J]. Journal of Agro-Environment Science, 2023, 42(1): 101-111 (in Chinese).
[39] 刘子璇. 风车草生物炭负载纳米铁对水体中Cd、As、四环素的去除效应研究[D]. 长沙: 中南林业科技大学, 2021. LIU Z X. Study on the removal effect of Cd, As and tetracycline in water by nano-iron loaded on Cyperus alterniflora biochar[D]. Changsha: Central South University of Forestry & Technology, 2021 (in Chinese).
[40] 刘文贵. 稻床养鸡固废中残留抗生素和砷的微波处理研究[D]. 武汉: 华中科技大学, 2015. LIU W G. Study on microwave treatment of residual antibiotics and arsenic in rice bed chicken solid waste[D]. Wuhan: Huazhong University of Science and Technology, 2015 (in Chinese).
[41] ZHANG D W, HE Q Q, HU X L, et al. Enhanced adsorption for the removal of tetracycline hydrochloride (TC) using ball-milled biochar derived from crayfish shell[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2021, 615: 126254. doi: 10.1016/j.colsurfa.2021.126254 [42] MERODIO-MORALES E E, REYNEL-ÁVILA H E, MENDOZA-CASTILLO D I, et al. Lanthanum- and cerium-based functionalization of chars and activated carbons for the adsorption of fluoride and arsenic ions[J]. International Journal of Environmental Science and Technology, 2020, 17(1): 115-128. doi: 10.1007/s13762-019-02437-w [43] LI X P, WANG C B, ZHANG J G, et al. Preparation and application of magnetic biochar in water treatment: A critical review[J]. Science of the Total Environment, 2020, 711: 134847. doi: 10.1016/j.scitotenv.2019.134847 [44] 阮华珍, 高章龙, 陈玉婷, 等. 共存钙离子对镧铝改性稻壳生物炭除磷性能的影响[J]. 环境化学, 2020, 39(5): 1279-1289. doi: 10.7524/j.issn.0254-6108.2019070802 RUAN H Z, GAO Z L, CHEN Y T, et al. Effect of coexisting calcium ions on phosphate removal performance of lanthanum and aluminum modified rice husk biochar[J]. Environmental Chemistry, 2020, 39(5): 1279-1289 (in Chinese). doi: 10.7524/j.issn.0254-6108.2019070802
[45] WANG Z R, CAI X W, XIE X Y, et al. Visible-LED-light-driven photocatalytic degradation of ofloxacin and ciprofloxacin by magnetic biochar modified flower-like Bi2WO6: The synergistic effects, mechanism insights and degradation pathways[J]. Science of the Total Environment, 2021, 764: 142879. doi: 10.1016/j.scitotenv.2020.142879 [46] 许亚琼, 王雪佳, 李荣华, 等. 纳米零价铁改性生物炭对污染土壤中Cd稳定化效果及作用机制研究[J]. 农业环境科学学报, 2022, 41(11): 2478-2487. XU Y Q, WANG X J, LI R H, et al. Study on the stabilization effect and mechanism of nano-zero-valent iron modified biochar on Cd in polluted soil[J]. Journal of Agro-Environment Science, 2022, 41(11): 2478-2487 (in Chinese).
[47] VITHANAGE M, HERATH I, JOSEPH S, et al. Interaction of arsenic with biochar in soil and water: A critical review[J]. Carbon, 2017, 113: 219-230. doi: 10.1016/j.carbon.2016.11.032 [48] 汤冬梅, 武俊梅, 黄永炳, 等. 生物炭添加对土壤中抗生素和抗性基因的环境行为影响研究进展[J]. 环境化学, 2022, 41(6): 1957-1966. doi: 10.7524/j.issn.0254-6108.2021022201 TANG D M, WU J M, HUANG Y B, et al. Research advances in the effect of biochar amendment on environmental behaviors of antibiotics and antibiotic resistance genes in soils[J]. Environmental Chemistry, 2022, 41(6): 1957-1966 (in Chinese). doi: 10.7524/j.issn.0254-6108.2021022201
[49] JI X W, WAN J, WANG X D, et al. Mixed bacteria-loaded biochar for the immobilization of arsenic, lead, and cadmium in a polluted soil system: Effects and mechanisms[J]. Science of the Total Environment, 2022, 811: 152112. doi: 10.1016/j.scitotenv.2021.152112 [50] 王玉洁, 唐宇嘉, 张亚平, 等. 生物炭对土壤中抗生素抗性基因的阻控潜力及机制研究进展[J]. 应用生态学报, 2022, 33(11): 3116-3126. WANG Y J, TANG Y J, ZHANG Y P, et al. Retarding potential of biochar on antibiotic resistance genes in soil and the mechanisms: A review[J]. Chinese Journal of Applied Ecology, 2022, 33(11): 3116-3126 (in Chinese).
[51] LIU J X, ZHANG W J, MEI M, et al. A Ca-rich biochar derived from food waste digestate with exceptional adsorption capacity for arsenic (III) removal via a cooperative mechanism[J]. Separation and Purification Technology, 2022, 295: 121359. doi: 10.1016/j.seppur.2022.121359 [52] ZHAO Y L, SHI H, TANG X, et al. Performance and mechanism of As(III/V) removal from aqueous solution by Fe3O4-sunflower straw biochar[J]. Toxics, 2022, 10(9): 534. doi: 10.3390/toxics10090534 [53] KUMAR A, BHATTACHARYA T. Removal of arsenic by wheat straw biochar from soil[J]. Bulletin of Environmental Contamination and Toxicology, 2022, 108(3): 415-422. doi: 10.1007/s00128-020-03095-2 [54] SUN T, PEI P G, SUN Y B, et al. Performance and mechanism of As(III/Ⅴ) removal from aqueous solution by novel positively charged animal-derived biochar[J]. Separation and Purification Technology, 2022, 290: 120836. doi: 10.1016/j.seppur.2022.120836 [55] ZHAO Z L, HUANG F, LIU Z T, et al. Quantification adsorption mechanisms of arsenic by goethite-modified biochar in aqueous solution[J]. Environmental Science and Pollution Research, 2023, 30(30): 74791-74807. doi: 10.1007/s11356-023-27585-y [56] BABAEI K, SALIMI S, MAHMOUDABADI Z S, et al. Synthesis and application of chicken manure biochar as an effective nanoporous adsorbent for removal of arsenic from wastewater: A cost-effective approach[J]. Journal of the Iranian Chemical Society, 2023, 20(3): 541-550. doi: 10.1007/s13738-022-02686-6 [57] CHEN C K, CHEN J J, NGUYEN N T, et al. Specifically designed magnetic biochar from waste wood for arsenic removal[J]. Sustainable Environment Research, 2021, 31(1): 1-16. doi: 10.1186/s42834-020-00075-3 [58] FAN Z, FANG J E, ZHANG G L, et al. Improved adsorption of tetracycline in water by a modified Caulis spatholobi residue biochar[J]. ACS Omega, 2022, 7(34): 30543-30553. doi: 10.1021/acsomega.2c04033 [59] ZHANG Z L, LI Y, DING L, et al. Novel sodium bicarbonate activation of cassava ethanol sludge derived biochar for removing tetracycline from aqueous solution: Performance assessment and mechanism insight[J]. Bioresource Technology, 2021, 330: 124949. doi: 10.1016/j.biortech.2021.124949 [60] NIE Y, ZHAO C W, ZHOU Z Y, et al. Hydrochloric acid-modified fungi-microalgae biochar for adsorption of tetracycline hydrochloride: Performance and mechanism[J]. Bioresource Technology, 2023, 383: 129224. doi: 10.1016/j.biortech.2023.129224 [61] ZHENG Z H, ZHAO B L, GUO Y P, et al. Preparation of mesoporous batatas biochar via soft-template method for high efficiency removal of tetracycline[J]. Science of the Total Environment, 2021, 787: 147397. doi: 10.1016/j.scitotenv.2021.147397 [62] SHI Q Y, WANG W B, ZHANG H M, et al. Porous biochar derived from walnut shell as an efficient adsorbent for tetracycline removal[J]. Bioresource Technology, 2023, 383: 129213. doi: 10.1016/j.biortech.2023.129213 [63] LI H Y, YE X X, GENG Z G, et al. The influence of biochar type on long-term stabilization for Cd and Cu in contaminated paddy soils[J]. Journal of Hazardous Materials, 2016, 304: 40-48. doi: 10.1016/j.jhazmat.2015.10.048 [64] ZOROUFCHI BENIS K, SOLTAN J, McPHEDRAN K N. Electrochemically modified adsorbents for treatment of aqueous arsenic: Pore diffusion in modified biomass vs. biochar[J]. Chemical Engineering Journal, 2021, 423: 130061. doi: 10.1016/j.cej.2021.130061 [65] PAN X Q, GU Z P, CHEN W M, et al. Preparation of biochar and biochar composites and their application in a Fenton-like process for wastewater decontamination: A review[J]. Science of the Total Environment, 2021, 754: 142104. doi: 10.1016/j.scitotenv.2020.142104 [66] NIAZI N K, BIBI I, SHAHID M, et al. Arsenic removal by perilla leaf biochar in aqueous solutions and groundwater: An integrated spectroscopic and microscopic examination[J]. Environmental Pollution, 2018, 232: 31-41. doi: 10.1016/j.envpol.2017.09.051 [67] LIN H, HAN S K, DONG Y B, et al. The surface characteristics of hyperbranched polyamide modified corncob and its adsorption property for Cr(VI)[J]. Applied Surface Science, 2017, 412: 152-159. doi: 10.1016/j.apsusc.2017.03.061 [68] ZHANG W, CHO Y, VITHANAGE M, et al. Arsenic removal from water and soils using pristine and modified biochars[J]. Biochar, 2022, 4(1): 55. doi: 10.1007/s42773-022-00181-y [69] HU H, ZHANG J Y, WANG T, et al. Adsorption of toxic metal ion in agricultural wastewater by torrefaction biochar from bamboo shoot shell[J]. Journal of Cleaner Production, 2022, 338: 130558. doi: 10.1016/j.jclepro.2022.130558 [70] HU Y, CHEN D Z, ZHANG R, et al. Singlet oxygen-dominated activation of peroxymonosulfate by passion fruit shell derived biochar for catalytic degradation of tetracycline through a non-radical oxidation pathway[J]. Journal of Hazardous Materials, 2021, 419: 126495. doi: 10.1016/j.jhazmat.2021.126495 [71] SHIRANI Z, SONG H, BHATNAGAR A. Efficient removal of diclofenac and cephalexin from aqueous solution using Anthriscus sylvestris-derived activated biochar[J]. Science of the Total Environment, 2020, 745: 140789. doi: 10.1016/j.scitotenv.2020.140789 [72] PAN J Y, BAI X T, LI Y Y, et al. HKUST-1 derived carbon adsorbents for tetracycline removal with excellent adsorption performance[J]. Environmental Research, 2022, 205: 112425. doi: 10.1016/j.envres.2021.112425 [73] KIM H B, KIM S H, JEON E K, et al. Effect of dissolved organic carbon from sludge, Rice straw and spent coffee ground biochar on the mobility of arsenic in soil[J]. Science of the Total Environment, 2018, 636: 1241-1248. doi: 10.1016/j.scitotenv.2018.04.406 [74] JEON E K, RYU S, PARK S W, et al. Enhanced adsorption of arsenic onto alum sludge modified by calcination[J]. Journal of Cleaner Production, 2018, 176: 54-62. doi: 10.1016/j.jclepro.2017.12.153 [75] WU C, LI F, YI S W, et al. Genetically engineered microbial remediation of soils co-contaminated by heavy metals and polycyclic aromatic hydrocarbons: Advances and ecological risk assessment[J]. Journal of Environmental Management, 2021, 296: 113185. doi: 10.1016/j.jenvman.2021.113185 -



 下载:
下载: