-
全氟与多氟化合物(per- and polyfluoroalkyl substances, PFAS)是一类脂肪链上的氢原子被氟原子全部或部分取代的人工合成有机物,因其出众的热稳定性、化学稳定性和表面活性被广泛应用于金属电镀、纺织、农药、消防、涂层等多个领域[1 − 3]. 而后续的研究则证明PFAS具有极强的持久性,其在人体中的半衰期长达2.6—7.7年,在天然水体中半衰期长达数十年[4 − 5]. 因此全氟辛烷磺酸(PFOS)和全氟辛酸(PFOA)等典型PFAS先后被列入斯德哥尔摩公约中的持久性有机污染物名单并受到国际的广泛关注[6 − 7]. 释放入环境中的PFAS能够稳定存在于地表水、土壤以及地下水等多种环境介质并在各介质间发生迁移[8 − 10]. 此前的研究表明,PFAS会首先在浅层土壤中累积,并通过淋溶、吸附、络合等作用向土壤深处迁移[11]. Houtz等发现,污染场地周边深层土壤(深度5—6 m)中均能检出高浓度PFAS,且深层土壤全氟己烷磺酸(PFHxS)浓度显著高于表层土壤(150 ng·g−1干重 vs. 66 ng·g−1干重)[12],说明较短链的PFAS具有更强的迁移性[13]. 相似地,一项在挪威污染场地周边展开的调查发现在0—4 m深的土壤中均能检出较高浓度的PFOS[14],也说明PFAS能够在土壤中垂直向下迁移,进而导致地下水的污染. 然而,这些研究主要通过简单的几个土壤剖面开展研究,无法深入理解PFAS在土柱中垂直迁移的行为和影响因素.
胶体是广泛存在于土壤中的粒径在1—
1000 nm范围内的颗粒,其内部微粒核由有机物、无机物或有机物-无机物复合体构成,而外部由双电层(即决定电位离子层和补偿离子层)构成[15]. 胶体由于其较强的异质性、较大的比表面积、较高的阳离子交换量、较复杂的表面官能团组成等理化性质能够对污染物在土壤中的迁移行为造成影响[16]. 例如,土壤胶体能够与Cd2+、Pb2+、Cu2+和As3+等(类)金属离子之间发生包括物理吸附、静电吸附以及专性吸附在内的多种吸附行为,从而促进这些金属离子在土壤中的垂直向下迁移[16 − 18]. 有机污染物可通过吸附位点结合的方式,或通过水溶液与土壤有机质之间的分配作用进行结合[19 − 20],例如胶体能够与诺氟沙星和四环素等抗生素发生吸附结合,而胶体的迁移性低于水溶液,因此吸附在胶体上的抗生素被保留在较浅层的土壤中,其迁移性降低[16, 21]. 目前针对有机污染物随胶体迁移的研究主要是针对疏水性较强的物质(如多环芳烃、多氯联苯、多溴联苯醚、有机农药和抗生素等),而忽略了胶体对PFAS等离子型表面活性剂的迁移载带作用.本研究在中国山东省某氟化工业园区(FIP)附件采集了深度为20.3 m的土柱样品,对分析土壤及胶体中各PFAS浓度与占比随深度的变化趋势,对比土壤与胶体PFAS的浓度特征与运移特征,明确结构对PFAS在两相分配中的影响,计算PFAS随胶体的运移量并确定胶体运移对PFAS土壤总赋存的贡献,为科学描述PFAS在土壤中的迁移行为提供理论依据.
-
HPLC级甲醇购自Fisher(美国),氢氧化钠、氨水、乙酸铵和盐酸购自阿拉丁(中国). PFAS标准品及其内标购自Wellington Laboratories(中国),标准品包含全氟丁酸(PFBA)、全氟戊酸(PFPeA)、全氟己酸(PFHxA)、全氟庚酸(PFHpA)、全氟辛酸(PFOA)、全氟壬酸(PFNA)、全氟癸酸(PFDA)、全氟十一酸(PFUdA)、全氟十二酸(PFDoA)、全氟丁烷磺酸(PFBS)、全氟己烷磺酸(PFHxS)、全氟辛烷磺酸(PFOS)、六氟环氧丙烷二聚酸(HFPO-DA)、六氟环氧丙烷三聚酸(HFPO-TA)、6:2多氟烷基醚磺酸(6:2 Cl-PFESA,商品名6:2 F-53B)和8:2多氟烷基醚磺酸(8:2 Cl-PFESA,商品名8:2 F-53B).
-
在距山东省某FIP仅50 m的位置设置钻井采样点. 0—0.5 m的样品采用手动采样,每隔0.1 m采集1个样品,使用甲醇清洗干净的铲子采集,装在写有标记的真空袋中. 0.5—21 m则采用专用钻井进行土柱样品采集,钻头为直径30 cm的空心圆柱性铁柱,每次提取土柱的深度为5 m,钻井的初见水位为9 m,地下水位为20.5 m,土柱总深度为20.3 m. 0.5—9.5 m每隔0.3 m采集1个样品,9.5—21 m每隔0.6 m采集1个样品,共采集土柱样品53个.
-
称取60 ℃烘干的土壤1 g到 50 mL PP离心管中,并加入1 ng内标平衡过夜. 将 6 mL 100 mmol·L−1的NaOH甲醇溶液(8:2,甲醇:水)加入PP管,再加入15 mL 纯甲醇,超声30 min. 将混合物以250 r·min−1的速度恒温振荡15 min. 然后将其以
8000 r·min−1的速度离心5 min,将上清液转移到新的PP管中. 重复提取过程3次,合并上清液,用 2 mL 600 mmol·L−1 HCl 酸化,并用水稀释至1 L,过PEP固相萃取小柱(艾杰尔,中国)进行富集与除杂. -
将预处理过的土壤配成土壤悬液,置于槽型超声波清液槽中,超声分散20 min后稀释成3%悬液进行沉降分离. 粒径小于2.0 μm和2.0—5.0 μm的胶体悬浊液分别于沉降1.06 min和6.53 min后获取. 悬浊液在60 ℃下放置约1周烘干,而后进行PFAS的提取,提取过程与2.3节中的描述一致.
-
胶体中PFAS对土柱中总PFAS贡献度按下式(1)进行计算:
式中,CColloid和CSoil分别表示胶体和土柱中PFAS的浓度,mColloid和mSoil分别表示对应土柱中胶体质量和土柱质量.
-
本实验中PFAS由超高效液相色谱(Vanquish,Thermo Fisher Scientific, USA)串联三重四极杆质谱(TSQ ALTIS,Thermo Fisher Scientific, USA)测定,色谱柱选用柱长为50 mm的BEHC18(Waters,USA),具体仪器分析方法见Chen等[22].
-
采样时设置现场空白,以此来监测和校正采样过程中的污染;在样品前处理时设置过程空白,监测实验前处理过程中的污染;仪器分析时没10次进样设置1个溶剂空白,用以监测仪器背景值. 定量分析由内标校正的标准曲线计算获得(浓度梯度为0、0.5、1、2、5、8、10、50、100、200 ng·mL−1,R2> 0.99). PFAS的加标回收率(加标浓度5 ng·g−1)在61%到105%之间,方法检出限在<0.01 ng·g−1到3.65 ng·g−1之间.
-
t检验用于分析PFAS浓度的正态性,Spearman分析用于分析PFAS之间的相关性,最小偏二乘分析(PLS-DA)用于分析土壤与土壤胶体之间的组成差异以及不同土壤(与土壤胶体)深度PFAS组成差异. 所有统计分析均在RStudio中完成(版本4.0.3).
-
PFAS在土柱不同深度的土壤样品中均有检出,其中短碳链PFAS(PFBA和PFPeA)检出率低于15%,6:2 F-53B、PFBS和PFHxS等磺酸类PFAS检出率也较低,分别为5.7%、62.2%和62.2%. PFAS平均总浓度为(309.5±177.1)ng·g−1,该结果与之前针对同一地区的报道结果一致[7, 23],但比非污染场地PFAS浓度高1—2个数量级[8, 24]. 其中PFOA浓度最高,为244.3 ng·g−1(占比77.8%),其次为HFPO-TA(39.6 ng·g−1,占比11.6%)、PFHxA(8.38 ng·g−1,占比3.6%)、PFHpA(5.76 ng·g−1,占比2.0%)和HFPO-DA(4.8 ng·g−1,占比1.9%)(图1(A)).
从空间分布上看,随土壤深度增加,长碳链PFAS占比降低,例如PFOA在表层土壤中占比超过80%,而在较深层的土壤(> 10 m)中占比仅为70%左右(图1(B)). 此外,PFOA浓度与土壤深度存在显著的负相关关系(r =−0.72,P < 0.001),说明深层土壤中PFOA主要来自于表层土壤的垂直迁移. 相似地,HFPO-TA在表层土壤中占比超过了20%,而在较深层的土壤中占比仅不到10%. 与此相反,链长较短的PFAS,如PFHxA和HFPO-DA,其在表层土壤的占比相对较低,均为1%,而在较深层土壤中占比分别超过了3%和5%. 这些结果说明短链PFAS较长链物质在土壤中具有更强的垂直迁移能力. 这与之前一项分层土壤的研究结果一致,即短碳链PFAS在各层土壤中检出浓度基本相当,主要是由于短碳链PFAS亲水性较强,容易随淋溶作用而向下迁移;而长碳链PFAS的浓度随深度增加浓度明显下降,可能和它们与土壤中有机质较强的作用有关[10, 25 − 26]. 在本研究中,土壤总有机碳(TOC)含量随土壤深度增加而减少,而长碳链PFAS(如PFOA和HFPO-TA)浓度与TOC含量显著正相关(P< 0.01). 这说明长碳链PFAS由于其较强的疏水作用,通过与浅层土壤中有机质结合,限制其垂直迁移,导致其浓度随深度增加而降低[27 − 28]. 先前的研究表明,虽然该地区地表水中PFAS主要以PFOA为主,但地下水中短碳链PFAS(如C4-7全氟羧酸(PFCAs))占比与PFOA相当甚至超过PFOA成为最主要的PFAS[9, 26],这些研究结果都说明短碳链PFAS比长链PFAS具有更强的垂直迁移性.
-
土壤胶体被认为是有机污染物在土壤中运移的重要途径,因此本实验对土壤胶体中的PFAS进行了分析测定. 如图2(A)所示,土壤胶体中PFAS总浓度为(542.3±313.5)ng·g−1,高于土壤中PFAS总浓度. 与土壤中的趋势相似,PFOA的占比仍然最高(87.5%),其次为PFBA(2.2%)、PFHxA(2.1%)和PFPeA(1.2%)等短碳链PFAS,且长碳链PFAS占比随深度增加逐渐降低,短碳链PFAS则呈现相反趋势(图2(B)). 相关性分析表明土壤中PFOA、PFNA和HFPO-TA等长碳链PFAS浓度与它们在胶体中对应浓度之间存在显著正相关关系(P < 0.001). 这说明长碳链PFAS可通过疏水、静电、配体交换等作用较强吸附在土壤胶体上,并随胶体运移至深层土壤中[19 − 20, 29]. 此外,长碳链PFAS(如HFPOs)浓度与土壤胶体粒径显著负相关(P < 0.05),进一步说明胶体因其较大的比表面积,对长链PFAS具有较强的吸附能力,对其在土柱中的运移具有一定的贡献[5]. 与土壤中PFAS组成特征不同的是,短碳链PFAS(如PFBA和PFPeA)在所有胶体样品中均有检出,检出率与检出浓度均显著高于土壤(P < 0.001),说明短碳链PFAS也可通过静电、配体交换等吸附在胶体上[29],并随胶体向下迁移. 先前的研究已表明PFAS在土壤中的分配行为与土壤性质、PFAS官能团以及链长均有显著关联,长碳链PFAS被证实能够与土壤中含有羟基官能团的组分结合,并形成大而聚集的簇,从而限制其迁移[30 − 31]. 值得一提的是,两种新型PFAS(HFPO-TA与HFPO-DA)在土壤胶体中的浓度仅为0.61 ng·g−1和0.43 ng·g−1(占比< 0.1%),显著低于其土壤浓度(P < 0.01),说明这两种新型PFAS在胶体上的吸附相对较弱. 然而它们在土壤中无论浓度与占比都相对较高,推测其主要通过随水的淋溶作用向下迁移.
PFOA在胶体中浓度显著高于土壤,但其浓度随深度逐渐降低,在较深层处接近土壤浓度(图3(A)). 本文计算了胶体中PFOA在各层土壤胶体中的平均浓度,结果表明表层(深度0.1—0.8 m)土壤胶体中PFOA平均浓度达到
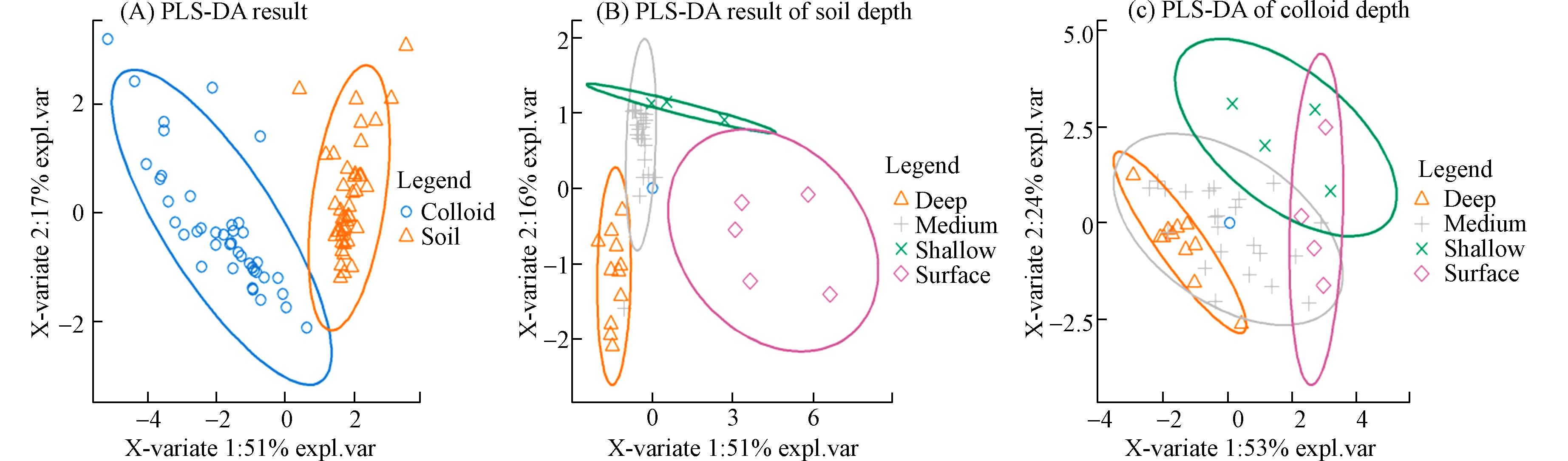
1109 ng·g−1,在浅层(深度1.1—2.6 m)土壤胶体中PFOA浓度为888.9 ng·g−1,较表层土壤下降19.9%,而在中层(深度2.9—9.5 m)和深层(10.1—20.3 m)土壤胶体中PFOA浓度分别为401.6 ng·g−1和524.3 ng·g−1,降幅达到63.8%和77.1%. 随深度增加,土壤胶体中PFOA浓度降幅增大,这说明长碳链PFAS较难随土壤胶体向下迁移 [32]. 与PFOA相似,胶体中短碳链PFCA(4—7碳)浓度也显著高于土壤,但其随深度变化不大,主要呈现波动式变化(图3(B)). 短碳链PFCA在浅层土壤胶体中的浓度相较于表层土壤中下降了24.4%—45.2%,虽然在中层和深层土壤胶体中浓度依然有所下降,但降幅有限(例如PFBA在深层土壤胶体中浓度降幅仅比浅层土壤胶体高3.4%),且明显低于PFOA的变化率,说明短碳链PFAS更容易随土壤胶体迁移至更深处土壤. 与PFOA和短链PFAS相反,HFPO-DA与HFPO-TA在胶体中浓度低于土壤,且其浓度较为稳定,不随土壤深度变化而变化,进一步说明这两种PFAS在胶体上的吸附能力较弱. 与PFAS类似,多溴联苯醚、多环芳烃和有机氯农药等强疏水性有机污染物在胶体中的浓度高于土壤浓度,但与PFAS随胶体向下运移趋势不同的是,强疏水性物质在胶体中的浓度通常不随深度增加而变化,说明强疏水性有机污染物主要通过与胶体结合的方式向土壤深处运移[20],而PFAS等离子型表面活性剂除随胶体运移外,还可通过随水等其他途径向土壤深处运移.进一步通过PLS-DA分析发现土壤与土壤胶体被明显分成两组(图4(A)),说明两者在组成上有明显差异,不同链长和不同官能团的PFAS在胶体上具有显著不同的吸附能力. 此外,不同深度土壤的组成特征也有明显差别(图4(B)).
随着深度的增加,短碳链PFAS(如PFBA、PFPeA和PFHxA)浓度与占比逐渐升高,而长碳链PFAS(如PFOA和PFNA)浓度与占比均逐渐降低,且两类PFAS变化相对较大,导致各层土壤PFAS特征不重叠. 与之相反的是,土壤胶体中PFAS的组成特征随深度变化相对较小(图4(C)),虽然胶体中PFAS总体变化趋势与土壤相似,但其变化相对平缓连贯,上层土壤胶体与其下一层土壤胶体特征具有一定重合性,且中层土壤胶体与下层土壤胶体特征完全重合. 以上结果表明,PFAS通过土壤的运移具有深度依赖性,由于各层土壤性质的差异(如TOC、孔隙度、含水率、比表面积等)较大,导致上层土壤吸附的PFAS较多,而下层吸附较少[19, 33];相反地,不同深度土壤胶体由于相对较低的异质性,使其吸附的PFAS相当,因而不同层之间的PFAS特征具有一定的相似性.
-
土壤胶体在上层(0.1—2.6 m,即上文所述表层和浅层土壤之和)与下层(2.9—20.3 m,即上文所述中层和深层土壤之和)土壤中的浓度分别为63.4(占比6.3%)和15.4 mg·g−1(占比1.5%),浓度具有显著差异(P < 0.001). 基于从土壤中所提取的胶体质量以及胶体中的PFAS浓度,本文对胶体负载的PFAS量进行了计算. 与土壤胶体浓度趋势类似,上层胶体中PFAS总量显著高于下层(982.0 ng vs. 146.0 ng,P< 0.001). PFOA的胶体负载量最高,在上层和下层土壤胶体中分别为925.2 ng和128.0 ng(图5(A)),其次为PFBA(上层和下层土壤胶体中负载量分别为15.8 ng和5.3 ng)、PFHxA(上层和下层土壤胶体中负载量分别为14.1 ng和5.2 ng)和PFHpA(上层和下层土壤胶体中负载量分别为13.9 ng和4.0 ng)等短碳链PFAS. 进一步地,通过对PFAS在胶体中载量对土壤PFAS总量贡献的估算发现,上层土壤胶体中PFPeA、PFHxA、PFHpA和PFOA对其各自的土壤总量的相对贡献分别为26.6%、16.6%、12.6%和15.9%;下层土壤胶体中的相对贡献度分别为6.4%、4.2%、2.7%和2.9%,基本上符合随碳链增加其贡献度减小的趋势(图5(B)).
短碳链PFAS通常具有较大的电离常数因而更可能与胶体双电层发生吸附作用[34],导致胶体中短碳链PFAS对其土壤总量的贡献高于长碳链. 同时,由于短碳链PFAS与土壤胶体之间较强的吸附作用,使其更可能随胶体向土壤下层迁移. 此外,各PFAS的胶体负载量与其土壤总量的贡献度之间存在显著正相关关系(P < 0.001). 以上结果表明,在2.6 m以上的土壤中,土壤中PFAS以较高的比例分配于土壤胶体中,而随着深度加深,受土壤及土壤胶体理化性质的改变以及地下水的影响,土壤中的PFAS以更少的比例分配至胶体相中,即在上层土壤中PFAS除随水向下迁移外,也可通过胶体载带作用向下迁移. 随着深度增加,土壤胶体浓度降低,其载带作用减弱.
-
本研究通过对工业园区周边0—20.3 m土柱样品及胶体中PFAS随深度变化趋势进行分析,证明PFAS具有较强的垂直迁移能力,即使在深度为20.3 m的土层中也能检出较高浓度PFAS. 通过对比土壤及胶体中PFAS的组成特征,发现胶体中短碳链PFAS的占比要显著高于土壤,长碳链PFAS及新型醚羧酸类PFAS(HFPO-DA和HFPO-TA)则相反. 进一步的定量分析发现,胶体中PFBA对其土壤总量的贡献超过26%,而随碳链长度增加,胶体中PFAS对土壤总量的贡献逐渐下降,PFOA的胶体贡献度仅为15.9%,证明短碳链PFAS具有更强的随胶体迁移能力. 本文结果与先前发现的该地区地下水中存在较高浓度PFAS的结果相一致,说明PFAS能够通过随水和胶体在土壤中垂直迁移至地下水中,导致地下水PFAS污染和潜在健康风险. 本研究对深入理解PFAS在土壤(尤其是深层土壤)中的垂直迁移行为具有重要意义.
全氟与多氟化合物在场地土壤中的垂直迁移行为
Vertical transportation behavior of per- and polyfluoroalkyl substances (PFAS) in soil column around a fluorochemical industrial park
-
摘要: 全氟与多氟化合物(per- and polyfluoroalkyl substances,PFAS)因其极强的环境持久性而受到广泛关注,然而其在土壤中的垂直运移行为尚不清楚. 本研究在我国某氟化工业园区附近采集了深度为20.3 m的土柱,对其进行分层并提取土壤中的胶体. 定量分析不同深度土壤和胶体中18种常见PFAS. 结果表明,土壤和胶体中PFAS平均总浓度分别达到了309.5 ng·g−1干重和542.3 ng·g−1干重,全氟辛酸PFOA为最主要的物质,占比均超过77%. 随深度增加,长碳链PFAS在土壤与胶体中占比不断下降而短碳链PFAS则上升,说明短碳链PFAS具有更强的迁移能力. 土壤与胶体在PFAS组成上具有明显差异:土壤中新型醚羧酸类PFAS占比显著高于胶体,而胶体中短碳链PFAS占比更高,说明PFAS的化学结构对其在胶体上的吸附具有较大影响. 进一步的计算表明,相比于下层土壤,PFAS在上层土壤(0.1—2.6 m)胶体上具有较高的负载量(982.0 ng vs. 146.0 ng),表明上层土壤中胶体载带对PFAS的垂直迁移具有一定贡献,特别是对短链羧酸垂直迁移的贡献要大于PFOA. 本研究证明PFAS(尤其是短碳链PFAS)能够随胶体垂直运移至深层土壤并对地下水安全造成潜在威胁.Abstract: Per- and polyfluoroalkyl substances (PFAS) have attracted global concern due to their high environmental persistence, yet their vertical transport mechanisms in soil is far beyond well understood. In this investigation, a 20.3 m soil column was procured in the vicinity of a fluorochemical industrial park in China, which was sectioned at various depths, and the soil colloids were extracted from each section. Then, 18 prevalent PFAS were analyzed in both the soil sections and colloids. Results indicated that the average total concentration of PFAS in the bulk soil and colloid samples were 309.5 ng·g−1dw and 542.3 ng·g−1dw, with perfluorooctanoic acid (PFOA) being the predominant species (over 77% contribution). It was observed that the proportion of long chain PFAS in the total PFAS decreased as soil depth increased, while a contrast trend was observed for the short chain PFAS, highlighting the greater mobility of short chain PFAS. The PFAS composition profiles exhibited remarkable difference between the bulk soil and colloid: the novel PFAS with ether bond exhibited much higher proportions in the bulk soil than in colloid, which on the other hand favored a higher proportion of short-chain PFAS. This indicates that the chemical structure of PFAS significantly influences their adsorption on colloid. Further calculation suggested that the colloid in the upper soil layers (0.1—2.6 m) carried more PFAS than deeper layers (982.0 ng versus 146.0 ng), underscoring the substantial role of colloid in facilitating the vertical transport of PFAS, particularly accentuating the migration of short-chain PFAS over PFOA. This study provides crucial insights into the contribution of colloid in promoting vertical transportation of PFAS in soil, especially the short chained PFAS, highlighting a potential threat to the safety of groundwater.
-
Key words:
- PFAS /
- soil column /
- colloid /
- vertical transportation.
-

-
-
[1] WANG Z Y, DeWITT J C, HIGGINS C P, et al. A never-ending story of per- and polyfluoroalkyl substances (PFASs)?[J]. Environmental Science & Technology, 2017, 51(5): 2508-2518. [2] SUNDERLAND E M, HU X C, DASSUNCAO C, et al. A review of the pathways of human exposure to poly- and perfluoroalkyl substances (PFASs) and present understanding of health effects[J]. Journal of Exposure Science & Environmental Epidemiology, 2019, 29(2): 131-147. [3] 张美, 楼巧婷, 邵倩文, 等. 全氟化合物污染现状及风险评估的研究进展[J]. 生态毒理学报, 2019, 14(3): 30-53. ZHANG M, LOU Q T, SHAO Q W, et al. Research progress of perfluorinated compounds pollution status and risk assessment[J]. Asian Journal of Ecotoxicology, 2019, 14(3): 30-53 (in Chinese).
[4] ZHANG Y F, BEESOON S, ZHU L Y, et al. Biomonitoring of perfluoroalkyl acids in human urine and estimates of biological half-life[J]. Environmental Science & Technology, 2013, 47(18): 10619-10627. [5] LI Y, FENG X M, ZHOU J, et al. Occurrence and source apportionment of novel and legacy poly/perfluoroalkyl substances in Hai River Basin in China using receptor models and isomeric fingerprints[J]. Water Research, 2020, 168: 115145. doi: 10.1016/j.watres.2019.115145 [6] XU Y Y, FLETCHER T, PINEDA D, et al. Serum half-lives for short- and long-chain perfluoroalkyl acids after ceasing exposure from drinking water contaminated by firefighting foam[J]. Environmental Health Perspectives, 2020, 128(7): 77004. doi: 10.1289/EHP6785 [7] FENG X M, YI S J, SHAN G Q, et al. Occurrence of perfluoroalkyl substances in the environment compartments near a mega fluorochemical industry: Implication of specific behaviors and emission estimation[J]. Journal of Hazardous Materials, 2023, 445: 130473. doi: 10.1016/j.jhazmat.2022.130473 [8] SCHULZ K, SILVA M R, KLAPER R. Distribution and effects of branched versus linear isomers of PFOA, PFOS, and PFHxS: A review of recent literature[J]. The Science of the Total Environment, 2020, 733: 139186. doi: 10.1016/j.scitotenv.2020.139186 [9] LIU Z Y, LU Y L, SHI Y J, et al. Crop bioaccumulation and human exposure of perfluoroalkyl acids through multi-media transport from a mega fluorochemical industrial park, China[J]. Environment International, 2017, 106: 37-47. doi: 10.1016/j.envint.2017.05.014 [10] CHEN H, YAO Y M, ZHAO Z, et al. Multimedia distribution and transfer of per- and polyfluoroalkyl substances (PFASs) surrounding two fluorochemical manufacturing facilities in Fuxin, China[J]. Environmental Science & Technology, 2018, 52(15): 8263-8271. [11] BAO J, YU W J, LIU Y, et al. Perfluoroalkyl substances in groundwater and home-produced vegetables and eggs around a fluorochemical industrial park in China[J]. Ecotoxicology and Environmental Safety, 2019, 171: 199-205. doi: 10.1016/j.ecoenv.2018.12.086 [12] HOUTZ E F, HIGGINS C P, FIELD J A, et al. Persistence of perfluoroalkyl acid precursors in AFFF-impacted groundwater and soil[J]. Environmental Science & Technology, 2013, 47(15): 8187-8195. [13] 黄柳青, 王雯冉, 张浴曈, 等. 地表水中全氟及多氟烷基化合物(PFASs)的污染现状研究进展[J]. 环境化学, 2024, 43(3): 693-710. doi: 10.7524/j.issn.0254-6108.2022090901 HUANG L Q, WANG W R, ZHANG Y T, et al. Research progress on the pollution status of per-and polyfluoroalkyl substances(PFASs) in surface water: A review[J]. Environmental Chemistry, 2024, 43(3): 693-710 (in Chinese) . doi: 10.7524/j.issn.0254-6108.2022090901
[14] HALE S E, ARP H P H, SLINDE G A, et al. Sorbent amendment as a remediation strategy to reduce PFAS mobility and leaching in a contaminated sandy soil from a Norwegian firefighting training facility[J]. Chemosphere, 2017, 171: 9-18. doi: 10.1016/j.chemosphere.2016.12.057 [15] 杨悦锁, 王园园, 宋晓明, 等. 土壤和地下水环境中胶体与污染物共迁移研究进展[J]. 化工学报, 2017, 68(1): 23-36. YANG Y S, WANG Y Y, SONG X M, et al. Co-transport of colloids and facilitated contaminants in subsurface environment[J]. CIESC Journal, 2017, 68(1): 23-36 (in Chinese).
[16] 刘胜, 梁媛, 王思雨. 土壤胶体迁移行为及其介导污染物迁移模拟与研究进展[J]. 化学通报, 2023, 86(7): 824-832. LIU S, LIANG Y, WANG S Y. Research progress in soil colloid transport behavior and its mediated pollutant migration[J]. Chemistry, 2023, 86(7): 824-832 (in Chinese).
[17] XIE B Y, JIANG Y J, ZHANG Z, et al. Co-transport of Pb (Ⅱ) and Cd (Ⅱ) in saturated porous media: Effects of colloids, flow rate and grain size[J]. Chemical Speciation & Bioavailability, 2018, 30(1): 135-143. [18] LI X Y, CAO Z Y, DU Y P, et al. Multi-metal contaminant mobilizations by natural colloids and nanoparticles in paddy soils during reduction and reoxidation[J]. Journal of Hazardous Materials, 2024, 461: 132684. doi: 10.1016/j.jhazmat.2023.132684 [19] DUAN L, YING Y Q, ZHONG J Y, et al. Key factors controlling colloids-bulk soil distribution of polybrominated diphenyl ethers (PBDEs) at an e-waste recycling site: Implications for PBDE mobility in subsurface environment[J]. The Science of the Total Environment, 2022, 819: 153080. doi: 10.1016/j.scitotenv.2022.153080 [20] DUAN L, ZHONG J Y, YING Y Q, et al. Preferential association of polycyclic aromatic hydrocarbons (PAHs) with soil colloids at an e-waste recycling site: Implications for risk of PAH migration to subsurface environment[J]. The Science of the Total Environment, 2023, 889: 164222. doi: 10.1016/j.scitotenv.2023.164222 [21] XING Y N, CHEN X J, CHEN X, et al. Colloid-mediated transport of pharmaceutical and personal care products through porous media[J]. Scientific Reports, 2016, 6: 35407. doi: 10.1038/srep35407 [22] CHEN X, FENG X M, SUN X, et al. Quantifying indirect contribution from precursors to human body burden of legacy PFASs based on paired blood and one-week duplicate diet[J]. Environmental Science & Technology, 2022, 56(9): 5632-5640. [23] LIU Z Y, LU Y L, SONG X, et al. Multiple crop bioaccumulation and human exposure of perfluoroalkyl substances around a mega fluorochemical industrial park, China: Implication for planting optimization and food safety[J]. Environment International, 2019, 127: 671-684. doi: 10.1016/j.envint.2019.04.008 [24] LAN Z H, YAO Y M, XU J Y, et al. Novel and legacy per- and polyfluoroalkyl substances (PFASs) in a farmland environment: Soil distribution and biomonitoring with plant leaves and locusts[J]. Environmental Pollution, 2020, 263(Pt A): 114487. [25] BAO J, LI C L, LIU Y, et al. Bioaccumulation of perfluoroalkyl substances in greenhouse vegetables with long-term groundwater irrigation near fluorochemical plants in Fuxin, China[J]. Environmental Research, 2020, 188: 109751. doi: 10.1016/j.envres.2020.109751 [26] XU B T, QIU W H, DU J, et al. Translocation, bioaccumulation, and distribution of perfluoroalkyl and polyfluoroalkyl substances (PFASs) in plants[J]. iScience, 2022, 25(4): 104061. doi: 10.1016/j.isci.2022.104061 [27] CHEN X W, ZHU L Y, PAN X Y, et al. Isomeric specific partitioning behaviors of perfluoroalkyl substances in water dissolved phase, suspended particulate matters and sediments in Liao River Basin and Taihu Lake, China[J]. Water Research, 2015, 80: 235-244. doi: 10.1016/j.watres.2015.04.032 [28] MILINOVIC J, LACORTE S, VIDAL M, et al. Sorption behaviour of perfluoroalkyl substances in soils[J]. The Science of the Total Environment, 2015, 511: 63-71. doi: 10.1016/j.scitotenv.2014.12.017 [29] BORTHAKUR A, CRANMER B K, DOOLEY G P, et al. Release of soil colloids during flow interruption increases the pore-water PFAS concentration in saturated soil[J]. Environmental Pollution, 2021, 286: 117297. doi: 10.1016/j.envpol.2021.117297 [30] LOGANATHAN N, WILSON A K. Adsorption, structure, and dynamics of short- and long-chain PFAS molecules in kaolinite: Molecular-level insights[J]. Environmental Science & Technology, 2022, 56(12): 8043-8052. [31] CAMPOS-PEREIRA H, KLEJA D B, AHRENS L, et al. Effect of pH, surface charge and soil properties on the solid-solution partitioning of perfluoroalkyl substances (PFASs) in a wide range of temperate soils[J]. Chemosphere, 2023, 321: 138133. doi: 10.1016/j.chemosphere.2023.138133 [32] COSTELLO M C S, LEE L S. Sources, fate, and plant uptake in agricultural systems of per- and polyfluoroalkyl substances[J]. Current Pollution Reports, 2020,DOI:10.1007/s40726-020-00168-y. [33] 胡桂林, 吕兆媛, 苗育, 等. 全氟辛酸在腐殖酸上的吸附平衡[J]. 环境化学, 2019, 38(4): 943-949. doi: 10.7524/j.issn.0254-6108.2018053005 HU G L, LYU Z Y, MIAO Y, et al. Adsorption of perfluorooctanoic acid on humic acid[J]. Environmental Chemistry, 2019, 38(4): 943-949 (in Chinese). doi: 10.7524/j.issn.0254-6108.2018053005
[34] LAMPIC A, PARNIS J M. Property estimation of per- and polyfluoroalkyl substances: A comparative assessment of estimation methods[J]. Environmental Toxicology and Chemistry, 2020, 39(4): 775-786. doi: 10.1002/etc.4681 -




 下载:
下载: