-
挥发性有机化合物(VOCs)作为O3和PM2.5的前体物质,会导致光化学烟雾与城市雾霾等复合污染的发生,引发区域性大气污染问题[1-2]。TiO2光催化技术能够在室温(20 °C)下将VOCs分解为CO2和H2O,具有绿色环保、成本低廉和氧化性强等优点[2-4],是目前最具应用前景的VOCs治理技术之一。
光催化反应体系中的相对湿度会对材料的活性产生显著影响[5-6]。Zhong等[7]发现当体系中的相对湿度增加,乙醇、丙酮、己烷和甲苯等VOCs的光催化降解反应会受到明显的抑制。Cedillo等[8]将TiO2自净建筑材料暴露在高湿度环境中,发现水分子阻碍了污染物在TiO2活性位点上的吸附并导致TiO2涂层的光催化性能降低。VOCs排放时往往伴随着大量水汽,相对湿度对于TiO2光催化的不利影响会限制其在实际工程中的应用。因此,提高TiO2在湿度条件下的光催化效率至关重要。TiO2的光催化活性与光生载流子的行为密切相关[5],在早期的工作中发现,由于水分子与TiO2表面之间的电荷传输较弱,导致湿度条件下光生载流子的复合机率大,TiO2的光催化性能相较干空气中更低[9-10]。而SnO2纳米材料与水分子间存在强相互作用,作为气体传感器时对于湿度十分敏感[11-12]。Zhang等[13]制备的介孔SnO2-石墨烯传感器具有超高的灵敏度,在11%—98%的相对湿度范围内均能作出快速响应。Li等[14]的实验表明,紫外光照射可以促进SnO2表面电子的生成,使得表面氧化过程加强,吸附水变多,从而提高传感器的湿度灵敏度。综上所述,有望通过Sn掺杂构建水分子的强作用位点,改善水分子和TiO2表面的电荷传输,同时抑制电子和空穴复合,促进光生载流子的迁移,来提高TiO2在湿度气氛下的光催化活性。
为提高湿度条件下的光催化性能,本研究采用水热法制备了Sn掺杂TiO2,在TiO2表面构建了水分子的强作用位点。探究材料在湿度气氛下对甲苯的紫外光催化效率,并通过透射电镜(TEM)、X射线衍射(XRD)、X射线电子能谱(XPS)和气氛表面光电压谱(SPV)等方法表征了材料的微观形貌、物理性质以及化学组成,讨论了Sn掺杂对于湿度条件下光生载流子的分离以及表面电荷分布的影响。
-
将SnCl4·5H2O加入含有1 mmol·L−1十二胺的120 mL无水乙醇中,搅拌使得固体溶解。接着加入3.45 mL钛酸四丁酯,搅拌0.5 h,使充分混合。再将10 mL超纯水逐滴滴加到钛酸四丁酯-无水乙醇溶液中,继续搅拌2 h。所得混合溶液置于反应釜中150 °C加热24 h,得到的白色沉淀物。沉淀经离心、洗涤、烘干后在500 °C煅烧4 h,最后再用研钵磨成粉末,得到Sn掺杂TiO2。不同材料中加入Sn的物质的量占总物质量的2%、5%和10%,分别命名为2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2。空白TiO2纳米颗粒的制备过程中不添加SnCl4·5H2O,其它步骤不变。
-
使用透射电子显微镜Tecnai F20(Philips-FEI,荷兰)观察材料的微观形貌。材料的晶相结构采用D8 Advance型X-射线衍射仪进行检测(Bruker,德国)。材料中掺杂元素的含量通过Agilent 720ES型(HITACHI,日本)电感耦合等离子光谱仪(ICP-OES)进行测试。材料的比表面积由BELSORP-max全自动比表面及孔径分析仪(MicrotracBEL,日本)测得。材料的吸光特性在U-3900型紫外-可见分光光度计(HITACHI,日本)上进行检测。NH3-程序升温脱附曲线(NH3-TPD)通过配有TCD检测器的BELCAT-Ⅱ全自动化学吸附仪(MicrotracBEL,日本)进行测试。气氛SPV的测试具体实验方法可以参考以前的工作[10]。使用LifeSpec II型超快荧光寿命光谱仪(爱丁堡,英国)记录材料的荧光衰减光谱,并计算平均荧光寿命。材料的XPS由Scientific K-Alpha型X-射线电子能谱仪(Thermo,美国)测得。
-
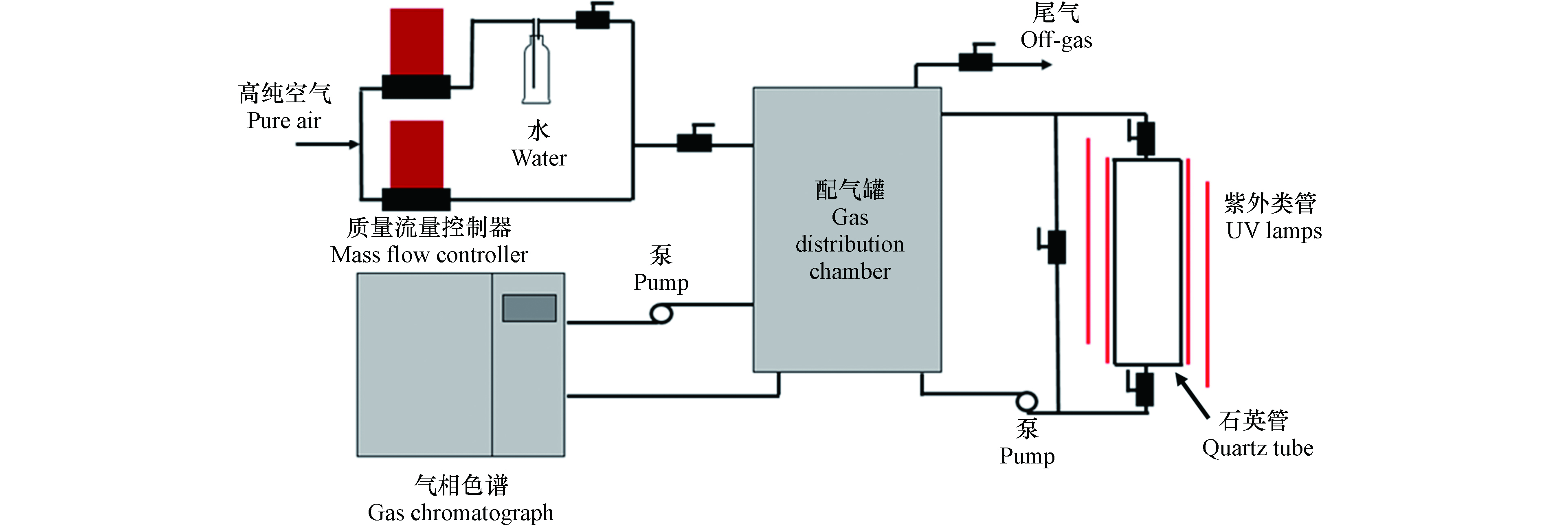
将甲苯作为代表性VOCs进行吸附以及光催化降解实验。测试系统如图1所示,主要由配气罐、光催化反应室和气相检测器三大部分组成。配气罐总体积为21.195 L,光催化反应室由石英管和紫外灯管组成,石英管内光催化材料的负载量为10 mg,并在四周设置了4根功率为8 W的紫外灯管。气相检测器主要由气相色谱仪(FID 9790II)和六通阀组成,用于测定反应系统中甲苯及CO2的浓度。测试前通过装有水的洗瓶通入相对湿度为50%的空气,使得测试体系中的相对湿度达到50%。接着向系统内注射甲苯蒸汽,控制甲苯初始浓度为20 mg·m−3,气相测定每8 min时间间隔下甲苯的浓度。吸附实验在不开灯的条件下进行,吸附至平衡后打开紫外灯,开始进行光催化实验。测定材料的光催化活性时,每种材料重复实验3次,并取平均值。
甲苯矿化效率(φ, %)的计算公式如下:
式中,Cc和Cs分别表示生成CO2浓度(mg·m−3)和甲苯的初始浓度(mg·m−3)。
-
通过TEM表征了样品的微观形态。图2A-D分别为TiO2、2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2的TEM图。TiO2主要由较为规则的纳米颗粒组成。当TiO2中掺杂Sn,颗粒的棱角逐渐圆润,颗粒的形状更趋向于球形。TiO2、2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2的颗粒平均粒径分别为(18.9±4.7)nm、(12.9±3.1)nm、(10.8±2.0)nm和(10.3±1.9) nm,颗粒粒径随着Sn掺杂浓度的增加逐渐减小。这可能是由于Sn4+的存在影响了水热过程中TiO2的结晶过程。图2E和图2F分别为TiO2和5%Sn-TiO2的高分辨透射电镜图(HR-TEM)。图2E中宽度为0.352 nm的晶格条纹代表锐钛矿TiO2的(101)晶面,而图2F中测量得到的晶格条纹宽度有0.352 nm和0.357 nm。若掺杂金属离子的电负性和离子半径与氧化物中晶格金属离子的电负性和离子半径相匹配,则掺杂金属离子会在掺杂反应过程中代替晶格金属离子[15]。Sn4+的电负性和半径相比Ti4+略大[16],因此Sn4+会参与钛酸四丁酯的水解缩合反应并取代TiO2的晶格中的Ti4+。在5%Sn-TiO2的HRTEM中测得0.357 nm的晶格条纹,相比正常锐钛矿TiO2(101)晶面的晶格条纹更宽,证明Sn掺入TiO2晶格中,使得晶格发生膨胀。
-
采用XRD表征了材料的晶相结构,见图3。各材料在25.3°、37.9°、48.1°、54.0°、55.1°、62.8°、68.9°、70.3°和75.2°附近均有衍射峰,分别代表锐钛矿TiO2的(101)、(004)、(200)、(105)、(211)、(204)、(116)、(220)和(215)晶面(JCPDS No.21-1272)。这说明所有材料中的TiO2均为锐钛矿型,而没有明显的SnO2晶相存在(JCPDS No.41-1445)。与TiO2相比,2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2在25.3°左右的衍射峰分别向低角度偏移0.15°、0.15°和0.24°,由此可以推断Sn已掺杂到TiO2的晶格中,引起晶格畸变。随着Sn掺杂比例的增加,各样品的衍射峰强度逐渐降低,表明Sn掺杂使得TiO2的结晶度降低。同时,XRD衍射峰半峰宽逐渐变宽。根据谢乐公式计算得TiO2、2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2的晶粒尺寸分别为14.4、10.2、8.8、8.3 nm,晶粒尺寸逐渐减小。这与TEM测量得到的各样品颗粒尺寸变化规律一致。
如表1所示,TiO2、2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2中Sn元素的理论含量分别为0、2%、5%和10%,通过ICP-OES测得实际材料体相中Sn元素含量分别为0、1.99%、4.82%和8.57%,与理论Sn元素的含量基本符合。
-
通过氮气等温吸附脱附曲线可得到材料的总比表面积和内、外比表面积,如表2所示。Sn掺杂后,材料的总比表面积和内、外比表面积均有明显增加。其中5%Sn-TiO2的总比表面积及内、外比表面积最大。结合材料的晶粒以及颗粒尺寸来看,比表面积与材料的尺寸大小有一定的相关性,其变化呈现相反的趋势,即材料尺寸越小,比表面积越大。Sn掺杂带来了更大的比表面积,同时也引入了更多的反应位点,有利于光催化反应的进行。
-
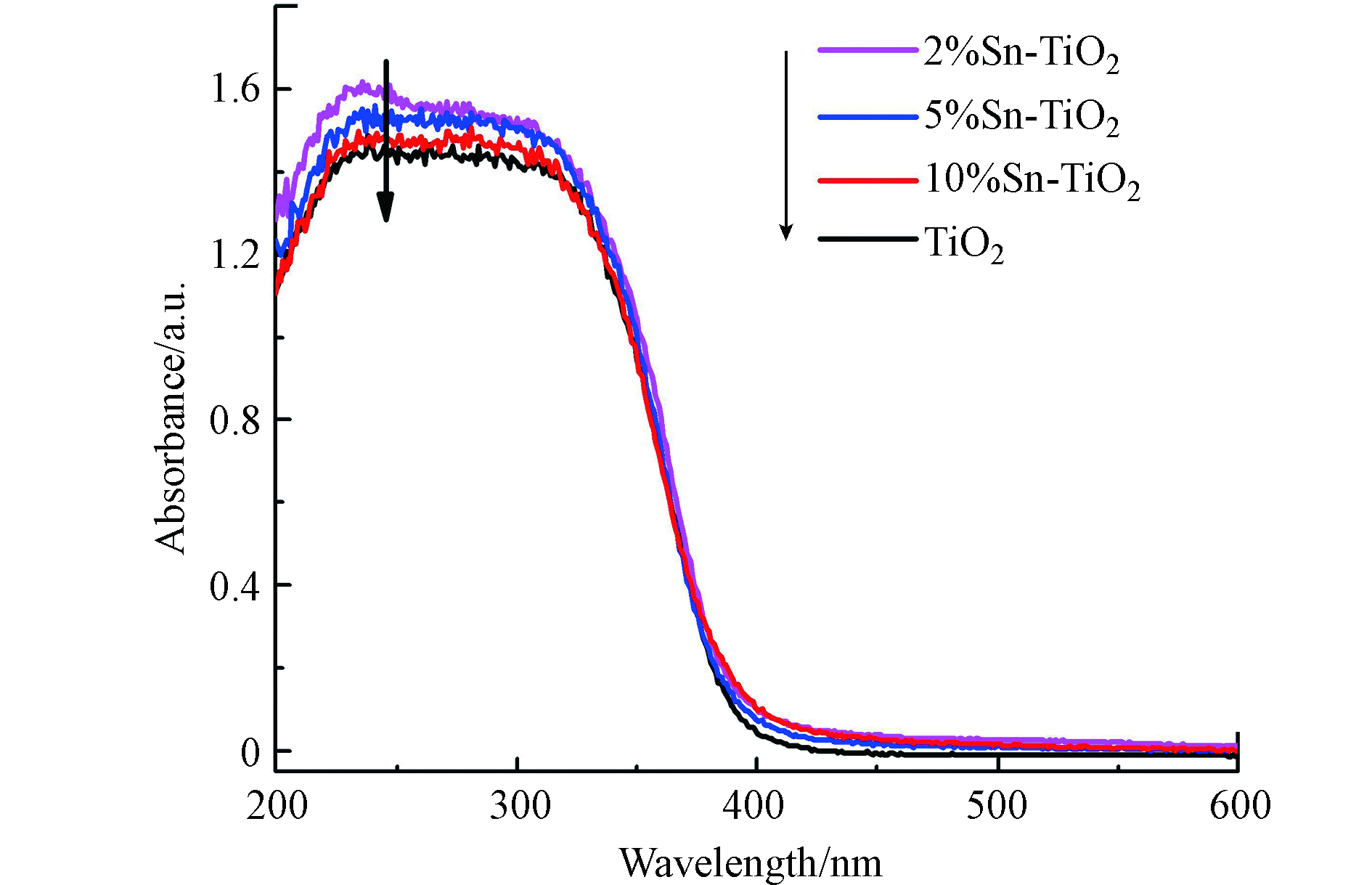
材料的紫外-可见漫反射光谱(UV-vis DRS)如图4所示。Sn掺杂后,材料在紫外区域的吸光度略有提升。对谱线400 nm前后的线性部分分别做切线,通过两切线交点的横坐标可以计算对应的禁带宽度。TiO2、2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2的禁带宽度分别为3.19、3.16、3.18、3.13 eV。材料的禁带宽度变化可能是由于Sn掺杂后产生了杂质能级,降低了电子迁跃所需的能量[17]。
-
选取甲苯作为典型VOCs,研究Sn掺杂前后材料在湿度条件下的光催化降解速率和矿化能力。相对湿度为50%时材料吸附和光催化反应过程中甲苯、CO2的浓度变化曲线以及反应动力学拟合曲线如图5所示。在没有材料负载的情况下,系统中的甲苯浓度没有明显下降,并且基本没有CO2生成。由图5A可知,TiO2、2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2在50%湿度气氛中对甲苯的吸附量相似,分别为2.97、2.37、2.33、2.16 mg·g−1。水和甲苯发生了竞争吸附,水分子占据了材料表面的吸附位点[18],使得各材料对于甲苯的吸附量较少。开灯64 min后,5%Sn-TiO2已将甲苯完全去除,而TiO2在开灯144 min时才将甲苯完全去除。对各材料的反应速率进行拟合,如图5C所示,可以发现各材料对甲苯的降解过程能够较好地满足零级反应动力学模型。TiO2、2%Sn-TiO2、5%Sn-TiO2和10%Sn-TiO2的反应速率常数k0分别为0.14、0.17、0.32、0.25 mg·m−3·min−1,5%Sn-TiO2的反应速率常数约为TiO2的2.3倍。由图5B可知,开灯72 min后,5%Sn-TiO2光催化降解甲苯产生的CO2浓度趋于平稳,说明已基本完成矿化。此时5%Sn-TiO2的矿化率是91.5%,是TiO2的2.0倍。另外,在表3中将Sn掺杂TiO2材料与前期制备的各类TiO2光催化材料进行比较,Sn掺杂TiO2在50%湿度条件下表现出优异的光催化矿化甲苯能力。以上结果说明Sn掺杂增强了TiO2的活性,有利于在湿度条件下光催化降解甲苯及其矿化,其中最佳Sn掺杂浓度是5%。排除吸附和光吸收的影响,甲苯的降解效率与载流子分离和迁移的效率密切相关。
-
甲苯分子中离域的π键是一个给电子基团,这使得甲苯容易在催化剂表面的酸性位点上被活化成苄基,然后与表面活性物种反应生成CO2和H2O[20]。为了探究Sn掺杂对于催化剂表面酸性位点的影响,进行了NH3-TPD测试。由图6可知,Sn掺杂后NH3的脱附峰强度增加,证明其表面酸性位点含量增加。另外,TiO2和5%Sn-TiO2的总酸度分别为0.97 mmol·g−1和1.20 mmol·g−1,5%Sn-TiO2的总酸度是TiO2的1.2倍。Sn掺杂后TiO2的比表面积扩大,进而提高了催化剂的表面酸性[21-22],增强了甲苯与材料表面的有效接触,有利于甲苯分子的活化和降解。
-
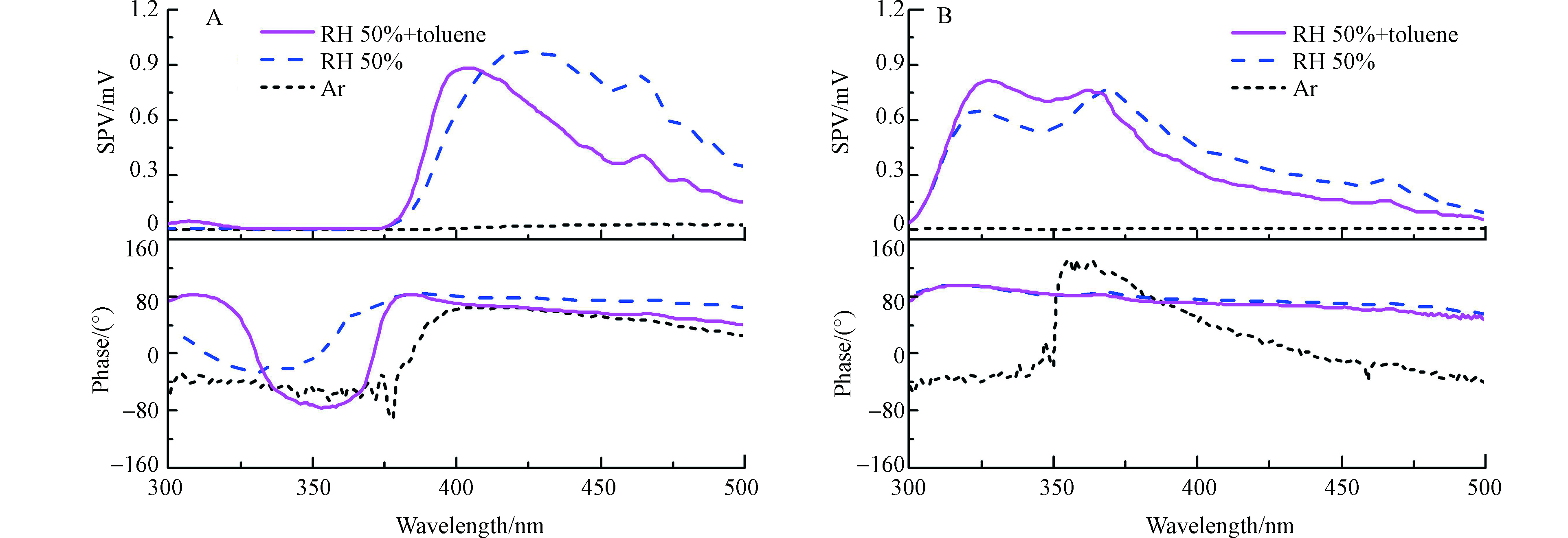
通过气氛SPV研究不同气氛下材料的电荷分离行为。图7A和7B分别测试了TiO2和5%Sn-TiO2在Ar、50%相对湿度以及50%相对湿度+甲苯气氛下的SPV。在Ar气氛下,两种材料的SPV信号均较低。这是由于惰性气体与表面光生载流子之间不会发生相互作用。380 nm在TiO2禁带宽度对应的波长附近,波长小于380 nm区域的SPV信号指示带带跃迁载流子的信息,大于380 nm区域的信号反映表面态跃迁载流子的信息[9]。在50%相对湿度条件下,TiO2在300—380 nm无明显的SPV信号,相位出现向0°偏移的趋势,这是由于水分子在TiO2表面捕获空穴。而在380—500 nm产生SPV信号,说明水分子能够促进TiO2表面态跃迁产生的光生载流子分离。不同于TiO2,5%Sn-TiO2在300—350 nm和350—500 nm分别产生SPV信号,相位抬升并维持在90°左右。该结果表明水分子能够同时促进5%Sn-TiO2带带跃迁和表面态跃迁产生的光生载流子分离。结合相位的变化,推测水分子在5%Sn-TiO2表面能够捕获光生电子。通入甲苯后,TiO2在300—380 nm的相位向0°偏移的趋势增加,这是由于甲苯对光生空穴的捕获有一定的促进作用。5%Sn-TiO2在300—380 nm的SPV升高,而相位不发生变化。水和甲苯作为空穴受体,在材料表面竞争捕获空穴[18]。当甲苯参与捕获空穴,水分子对空穴的捕获能力相应减弱,而对电子的捕获能力增加,从而使得空穴和电子的捕获同步增加。因此SPV信号提升,而相位不变。此时5%Sn-TiO2在紫外区域的SPV约为TiO2的16.2倍,表明在混合气氛下,其带带跃迁产生的载流子分离效率显著高于TiO2。
总的来说,Sn掺杂改善了水分子与5%Sn-TiO2表面间的电荷传递,水分子在5%Sn-TiO2表面能够捕获光生电子,从而促进带带跃迁产生的光生载流子分离。当水与甲苯共存时,两者可以分别捕获光生电子和空穴,发生的协同作用进一步提高光生载流子的分离效率。与TiO2不同,水和甲苯在5%Sn-TiO2表面对光生空穴的竞争捕获减弱,甲苯对空穴的捕获增加,促进了甲苯和空穴的直接作用,使得5%Sn-TiO2在湿度条件下的光催化能力得到提高。
-
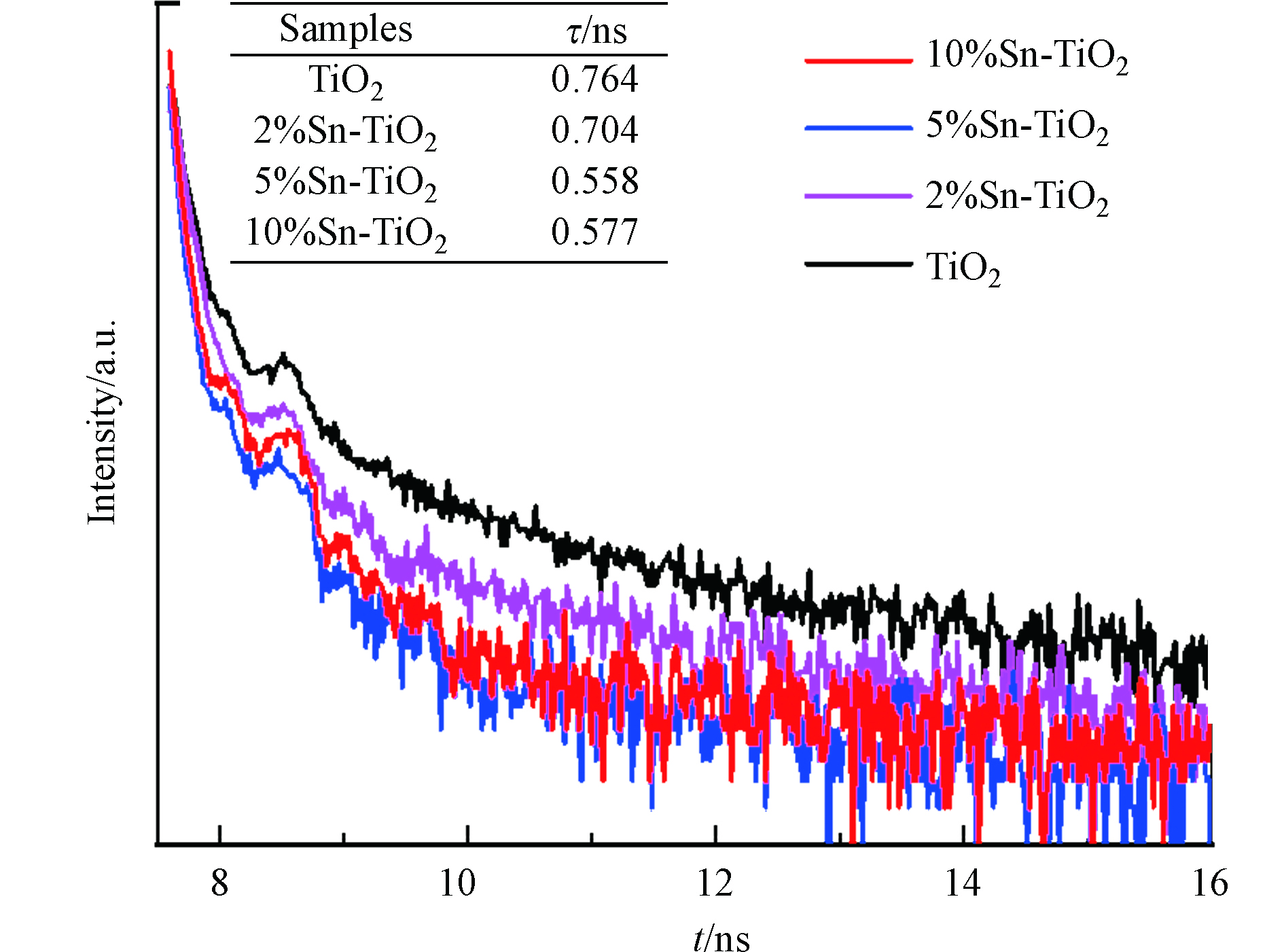
为了确定Sn掺杂TiO2后载流子迁移行为的变化,测试了材料的时间分辨光致发光光谱。如图8所示,各材料的荧光强度随时间以指数级形式衰减。通过对其衰减曲线的拟合,得到TiO2,2%Sn-TiO2,5%Sn-TiO2和10%Sn-TiO2的平均荧光寿命分别为0.764、0.704、0.558、0.577 ns。各材料平均荧光寿命从大到小依次为TiO2>2%Sn-TiO2>10%Sn-TiO2>5%Sn-TiO2,Sn掺杂后材料的平均荧光寿命减小,荧光衰减更迅速。平均荧光寿命减小,意味着光生载流子的转移速度更快,而复合几率减少[23]。材料载流子迁移效率的大小规律与平均荧光寿命相反,并与降解结果相符。5%Sn-TiO2的平均荧光寿命最短,说明在此掺杂比例下,载流子的迁移效率最高,光催化活性提升最为明显。
-
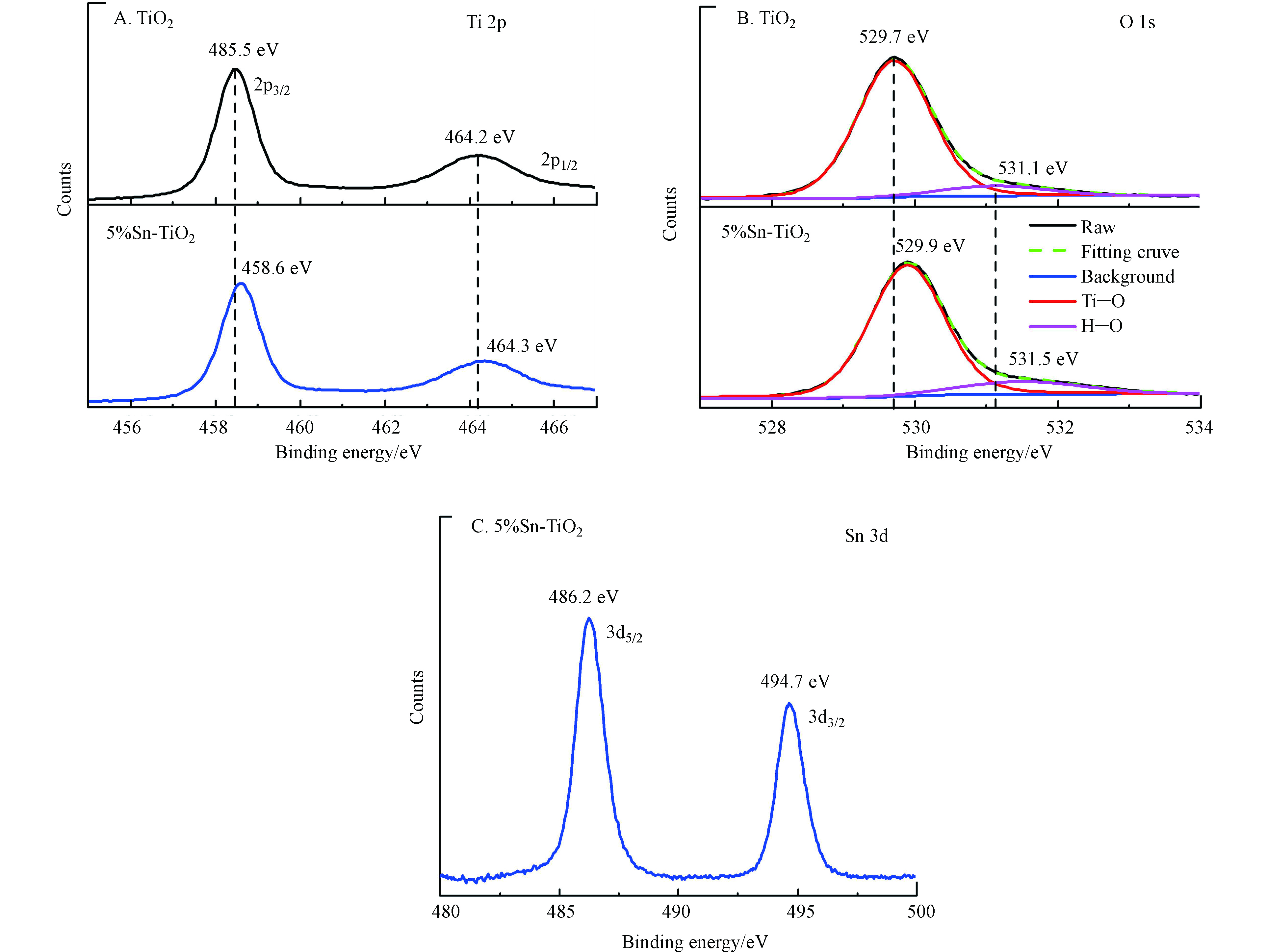
采用XPS对TiO2和5%Sn-TiO2的电子结构特征和表面化学性质进行了探测。图9A为TiO2和5%Sn-TiO2在Ti2p轨道的XPS谱图。Sn掺杂后,Ti2p的峰值位置向更高的结合能方向移动了0.1 eV。图9B为TiO2和5%Sn-TiO2的O1s的XPS谱图。TiO2在529.7 eV和531.1 eV处的拟合峰分别代表晶格氧(Ti—O—Ti)和表面羟基氧(H—O—Ti)[24]。5%Sn-TiO2中晶格氧所对应的峰向更高的结合能移动了0.2 eV。图9C显示5%Sn-TiO2在486.2 eV和494.6 eV附近检测到明显的XPS信号峰,分别代表Sn3d5/2和Sn3d3/2轨道。与文献中SnO2的Sn3d轨道结合能对比[25],5%Sn-TiO2中Sn3d轨道向低结合能偏移了0.20 eV。结合能降低说明相应电子轨道中电子的数量增加[26]。上述结合能的位移说明Sn掺杂后TiO2表面Ti和O轨道周围的电子减少,而Sn轨道周围电子增加。结合TEM和XRD的数据,证明Sn4+进入TiO2的晶格中,形成了Ti—O—Sn键,表面电荷发生了重新分配。由于Sn4+的电负性为1.96,而Ti4+的电负性为1.54[16, 27],Sn4+的电负性更强,电子从Ti向Sn转移。Sn轨道周围的电子更多,光激发产生的光生空穴更容易向Sn4+迁移,从而阻碍电子和空穴的复合,有利于光催化反应的进行。
-
(1)通过水热法合成了Sn掺杂TiO2纳米颗粒。随着Sn的加入,TiO2颗粒粒径变小,比表面积增大,表面酸性位点增加,并出现晶格膨胀的现象。
(2)Sn掺杂TiO2能够有效提高材料的抗湿性能,5%Sn-TiO2在湿度条件下对于甲苯的降解反应速率常数和矿化效率最大,分别达到TiO2的2.3倍和2.0倍。
(3)5%Sn-TiO2在湿度条件下具有良好的光催化性能,主要是由于Sn掺杂改善了TiO2表面的电荷传输。当水与甲苯共存时,两者在5%Sn-TiO2表面分别捕获光生电子和空穴,强化了甲苯和光生空穴之间的直接作用,有效提高了光生载流子分离、迁移和利用的效率。
Sn掺杂强化TiO2在湿空气中光催化降解甲苯的性能
Sn doping enhanced the photocatalytic degradation of toluene by TiO2 in humid air
-
摘要: 为了提高湿度条件下的光催化性能,通过Sn掺杂在TiO2表面构建了水分子的强作用位点。采用TEM、XRD、XPS以及气氛SPV等方法表征了材料的物化性质及光生载流子分离行为,并考察了材料的光催化性能。结果表明,Sn掺杂有效提高了湿空气中TiO2光催化降解甲苯的活性,Sn的最佳掺杂浓度为5%,5%Sn-TiO2的反应速率常数和矿化效率分别达到TiO2的2.3倍和2.0倍。Sn掺入TiO2晶格中,增加了TiO2的比表面积,提供了丰富的酸性位点。此外,Sn掺杂使得TiO2表面电荷发生重排,促进了水分子对光生电子的捕获,强化了甲苯和光生空穴的直接作用,有效提高了光生载流子分离、迁移和利用的效率。Abstract: In order to improve the photocatalytic performance under humid conditions, strong reacting sites with water molecules were constructed on the surface of TiO2 by Sn doping. The physicochemical properties of materials and the separation behavior of photogenerated carriers were characterized by XRD, TEM, XPS and atmospheric SPV. The photocatalytic performance of the materials was also investigated. Our results showed that Sn doping effectively improved the photocatalytic degradation of toluene by TiO2 in humid air. When the optimal Sn-doping concentration of 5% was reached, the reaction rate constant and mineralization efficiency of 5%Sn-TiO2 increased by 2.3 times and 2.0 times compared to that of TiO2, respectively. Sn that entered the TiO2 crystal lattice increased the specific surface area and provided abundant acid sites. In addition, Sn doping caused the rearrangement of TiO2 surface charges and enhanced the capture of photogenerated electrons by water molecules. Sn doping might also promote the direct interaction between toluene and photogenerated holes. Overall, Sn doping was shown to effectively improve the separation, migration and utilization of photogenerated carriers.
-
Key words:
- Sn-doped TiO2 /
- VOCs /
- humidity /
- photocatalytic
-

-
表 1 ICP-OES测得材料中Sn元素的含量
Table 1. The content of Sn element of the prepared samples analyzed by ICP-OES
TiO2 2%Sn-TiO2 5%Sn-TiO2 10%Sn-TiO2 理论Sn含量 0 2% 5% 10% 实际Sn含量 低于检出限,为0 1.99% 4.82% 8.57% 表 2 材料的总比表面积、内、外比表面积以及晶粒和颗粒尺寸
Table 2. Total specific surface area, internal, external specific surface area, grain size, and particle size of the prepared samples
材料
Sample总比表面积/(m2·g−1)
Total specific surface area内比表面积/(m2·g−1)
Internal specific surface area外比表面积/(m2·g−1)
External specific surface area晶粒尺寸/nm
Grain size颗粒尺寸/nm
Particle sizeTiO2 78.29 16.12 62.17 14.4 18.9±4.7 2%Sn-TiO2 107.12 25.16 81.96 10.2 12.9±3.1 5%Sn-TiO2 130.19 34.80 95.39 8.8 10.8±2.0 10%Sn-TiO2 123.38 34.38 89.00 8.3 10.3±1.9 表 3 不同催化剂光催化甲苯矿化效率的比较
Table 3. A comparison of the mineralization efficiency of toluene for different catalysts
材料
Samples组成
Components甲苯初始浓度/(mg·m−3)
Initial concentration反应相对湿度
Relative humidity矿化效率/%
Mineralization efficiency参考文献
Ref.TiO2 TiO2 20 50% 45.8 — 2%Sn-TiO2 TiO2 20 50% 63.2 — 5%Sn-TiO2 TiO2 20 50% 91.5 — 10%Sn-TiO2 TiO2 20 50% 84.1 — FTHS TiO2/H2Ti3O7 28 0 91.5 [19] THS TiO2 28 0 61.0 [19] GR-TiO2-5.0% Graphene/TiO2 22 0 40.0 [10] Microporous TiO2 TiO2 22 0 26.5 [10] -
[1] WANG P, CHEN Y, HU J L, et al. Attribution of tropospheric ozone to NOx and VOC emissions: Considering ozone formation in the transition regime [J]. Environmental Science & Technology, 2019, 53(3): 1404-1412. [2] XIE R J, LEI D X, ZHAN Y J, et al. Efficient photocatalytic oxidation of gaseous toluene over F-doped TiO2 in a wet scrubbing process [J]. Chemical Engineering Journal, 2020, 386: 121025. doi: 10.1016/j.cej.2019.02.112 [3] LI M, LU B, KE Q F, et al. Synergetic effect between adsorption and photodegradation on nanostructured TiO2/activated carbon fiber felt porous composites for toluene removal [J]. Journal of Hazardous Materials, 2017, 333(Jul.5): 88-98. [4] CHO Y, KIM S, PARK B, et al. Multiple heterojunction in single titanium dioxide nanoparticles for novel metal-free photocatalysis [J]. Nano Letters, 2018, 18(7): 4257-4262. doi: 10.1021/acs.nanolett.8b01245 [5] SHAYEGAN Z, LEE C S, HAGHIGHAT F. TiO2 photocatalyst for removal of volatile organic compounds in gas phase-A review [J]. Chemical Engineering Journal, 2018, 334: 2408-2439. doi: 10.1016/j.cej.2017.09.153 [6] MAMAGHANI A H, HAGHIGHAT F, LEE C S. Photocatalytic oxidation technology for indoor environment air purification: The state-of-the-art [J]. Applied Catalysis B-Environmental, 2017, 203: 247-269. doi: 10.1016/j.apcatb.2016.10.037 [7] ZHONG L X, HAGHIGHAT F, LEE C S, et al. Performance of ultraviolet photocatalytic oxidation for indoor air applications: Systematic experimental evaluation [J]. Journal of Hazardous Materials, 2013, 261: 130-138. doi: 10.1016/j.jhazmat.2013.07.014 [8] CEDILLO G E I, HERNANDEZ L J M, RUIZ V J J, et al. Self-cleaning TiO2 coatings for building materials: The influence of morphology and humidity in the stain removal performance [J]. Construction and Building Materials, 2020, 237: 117692. doi: 10.1016/j.conbuildmat.2019.117692 [9] GAO J X, LYU J Z, LI J, et al. Localization and stabilization of photogenerated electrons at TiO2 nanoparticle surface by oxygen at ambient temperature [J]. Langmuir, 2018, 34(24): 7034-7041. doi: 10.1021/acs.langmuir.8b01011 [10] ZHOU Z, GAO J X, ZHANG G S, et al. Optimizing graphene-TiO2 interface properties via Fermi level modulation for photocatalytic degradation of volatile organic compounds [J]. Ceramics International, 2020, 46(5): 5887-5893. doi: 10.1016/j.ceramint.2019.11.040 [11] FENG H, LI C, LI T, et al. Three-dimensional hierarchical SnO2 dodecahedral nanocrystals with enhanced humidity sensing properties [J]. Sensors & Actuators B Chemical, 2017, 234: 704-714. [12] MALIK R, TOMER V K, CHAUDHARY V, et al. Correction: An excellent humidity sensor based on In-SnO2 loaded mesoporous graphitic carbon nitride [J]. Journal of Materials Chemistry A, 2020, 8(38): 20187-20188. doi: 10.1039/C9TA90268F [13] ZHANG D, CHANG H, LI P, et al. Fabrication and characterization of an ultrasensitive humidity sensor based on metal oxide/graphene hybrid nanocomposite [J]. Sensors & Actuators B Chemical, 2016, 225: 233-240. [14] LI W, WANG L L, CAI Y, et al. Enhanced humidity sensing response of SnO2/Silicon nanopillar array by UV irradiation [J]. Sensors, 2019, 19(9): 2141. doi: 10.3390/s19092141 [15] SAYILKAN H. Improved photocatalytic activity of Sn4+-doped and undoped TiO2 thin film coated stainless steel under UV- and VIS-irradiation [J]. Applied Catalysis A-General, 2007, 319: 230-236. doi: 10.1016/j.apcata.2006.12.012 [16] SU T S, WEI T C. Co-electrodeposition of Sn-doped TiO2 electron-transporting layer for perovskite solar cells [J]. Physica Status Solidi A-Applications and Materials Science, 2020, 217(1): 1900491. [17] THIRUPPATHI M, SENTHIL KUMAR P, DEVENDRAN P, et al. Ce@TiO2 nanocomposites: An efficient, stable and affordable photocatalyst for the photodegradation of diclofenac sodium [J]. Journal of Alloys and Compounds, 2018, 735: 728-734. doi: 10.1016/j.jallcom.2017.11.139 [18] ZHANG G X, PEYRAVI A, HASHISHO Z, et al. Integrated adsorption and photocatalytic degradation of VOCs using a TiO2/diatomite composite: Effects of relative humidity and reaction atmosphere [J]. Catalysis Science & Technology, 2020, 10(8): 2378-2388. [19] LYU J, ZHOU L, SHAO J, et al. Synthesis of TiO2/H2Ti3O7 composite with nanoscale spiny hollow hierarchical structure for photocatalytic mineralization of VOCs [J]. Chemical Engineering Journal, 2020, 400: 125927. doi: 10.1016/j.cej.2020.125927 [20] MENON U, GALVITA V V, MARIN G B. Reaction network for the total oxidation of toluene over CuO-CeO2/Al2O3 [J]. Journal of Catalysis, 2011, 283(1): 1-9. doi: 10.1016/j.jcat.2011.05.024 [21] ZHANG G, HAN W, ZHAO H, et al. Solvothermal synthesis of well-designed ceria-tin-titanium catalysts with enhanced catalytic performance for wide temperature NH3-SCR reaction [J]. Applied Catalysis B-Environmental, 2018, 226: 117-126. doi: 10.1016/j.apcatb.2017.12.030 [22] GUO Y, LIANG J B, LIU Y, et al. Identifying surface active sites of SnO2: Roles of surface O2-, O22- anions and acidic species played for toluene deep oxidation [J]. Industrial & Engineering Chemistry Research, 2019, 58(40): 18569-18581. [23] WU J, ZHANG Y, ZHOU J, et al. Uniformly assembling n-type metal oxide nanostructures (TiO2 nanoparticles and SnO2 nanowires) onto P doped g-C3N4 nanosheets for efficient photocatalytic water splitting [J]. Applied Catalysis B-Environmental, 2020, 278: 119301. doi: 10.1016/j.apcatb.2020.119301 [24] LU Z X, SHI Y, YAN C F, et al. Investigation on IrO2 supported on hydrogenated TiO2 nanotube array as OER electro-catalyst for water electrolysis [J]. International Journal of Hydrogen Energy, 2017, 42(6): 3572-3578. doi: 10.1016/j.ijhydene.2016.12.098 [25] DUAN Y D, FU N Q, LIU Q P, et al. Sn-doped TiO2 photoanode for dye-sensitized solar cells [J]. The Journal of Physical Chemistry C, 2012, 116(16): 8888-8893. doi: 10.1021/jp212517k [26] FIGUERAS M, SOUSA C, ILLAS F. Effect of electron correlation in the decomposition of core level binding energy shifts into initial and final state contributions [J]. Physical Chemistry Chemical Physics, 2019, 21(18): 9399-9406. doi: 10.1039/C9CP01569H [27] NI S M, GUO F Y, WANG D B, et al. Modification of TiO2 nanowire arrays with Sn doping as photoanode for highly efficient dye-sensitized solar cells [J]. Crystals, 2019, 9(2): 113. doi: 10.3390/cryst9020113 -



 下载:
下载: