-
氯苯类化合物(chlorobenzenes, CBs)是一类人工合成的有机氯化合物,包括一氯苯(monochlorobenzene, MoCB)、二氯苯(dichlorobenzene, DiCB)、三氯苯(trichlorobenzene, TrCB)、四氯苯(tetrachlorobenzene, TeCB)、五氯苯(pentachlorobenzene, PeCB)和六氯苯(hexachlorobenzene, HCB). 这类化合物具有高毒性、难降解性和生物蓄积性,其中PeCB和HCB早已作为持久性有机污染物被列入《关于持久性有机污染物的斯德哥尔摩公约》受控污染物名单中,被禁止商业化生产和使用[1-2]. 而一些CBs仍在被广泛地应用于制药、农药、印刷、染色、皮革和电子制造等工业生产以及相关产品在农业生产、日常生活中的使用[3-6]. 含CBs的工业废水、城市污水和农业排水等排入自然水体,可能造成CBs水污染,直接或间接地危害生态环境和人体健康.
污水处理厂作为收集、集中处理和排放城镇污水的关键设施,也成为了污染物的潜在“二次源”. 目前,关于污水处理厂中CBs的研究主要集中在污泥介质[7-9],而污水中CBs的基础数据仍十分有限. 通过污水处理厂进出水以及各处理单元污水中CBs的含量和组成分布分析,能够了解当地工业废水或生活污水中CBs的赋存情况以及污水处理工艺对CBs的去除效率,并有助于判断排放的CBs是否会对受纳水环境造成生态危害等. 以往若干有关我国污水处理厂污水中CBs的研究[5, 10]仅分析了一部分氯苯物质,对所有同族体的赋存和去除情况缺乏全面性了解,不利于相关污染与风险的精准防控.
纺织印染行业常使用CBs作为染料及助剂的溶剂,导致纺织印染废水中往往含有CBs污染. 我国中山市、东莞市、佛山市和广州市的纺织印染废水处理厂出水中能检测到几百到几千纳克每升的CBs(Cl4-Cl6) [5]. 浙江省地处中国东南沿海、长江三角洲南翼,工业化和城市化程度高,其中纺织印染产业规模更是位列全国第一,然而省内纺织印染发达地区污水处理厂污水中CBs的赋存特征及排放风险尚无报道,亟待展开研究.
本文分析了浙江省纺织印染较发达城市两家污水处理厂污水中CBs(Cl1-Cl6)的浓度水平和组成分布特征,探讨了CBs在不同工艺处理过程中的变化规律与去除效率. 此外,还基于环境影响度和风险熵值计算模型,评估了污水处理厂排放水体中CBs可能产生的生态环境风险,为CBs水污染及风险防治提供了科学依据.
-
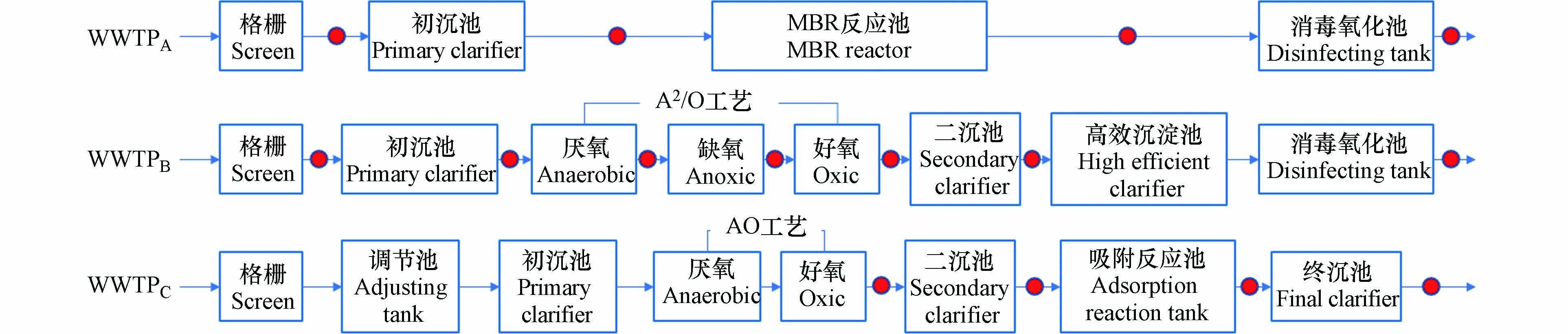
2020年12月,在浙江省嘉兴市两家污水处理厂采集了17个不同工艺单元的水样. 两家污水厂的主要处理工艺流程和采样点如图1所示. 第一家污水处理厂是该市最大的城镇综合污水处理厂,总处理规模为6 × 105 m3·d−1,包括两期工程(以下分别称为“A系统”和“B系统”). 该厂进水水质复杂,进水中工业废水与生活污水比例约为50:50,其中工业废水种类也较为多样化,含有纺织印染、化工、机械加工等多种行业废水. 第二家污水处理厂(以下简称“C系统”)是以印染纺织废水为主的中小型污水处理厂,处理规模为3.3 × 104 m3·d−1,工业废水约占其进水的88%. 使用预先洗净的棕色玻璃瓶采集水样,确保每个采样瓶装满水样,避免顶部空间留有空气. 水样经0.45 μm滤膜过滤后进行样品前处理.
-
正己烷和二氯甲烷均为农残级,购自J.T.Baker(美国). 氯化钠(分析纯)购自国药集团化学试剂有限公司. 无水硫酸钠(分析纯)购自天津市永大化学试剂有限公司. 弗罗里硅土(60—100目)购自Supelco公司(美国). 硅胶(0.063—0.100 mm)从德国Merck公司购得. 使用前,弗罗里硅土在140 ℃下活化7 h;硅胶以及无水硫酸钠在550 ℃下加热6 h,然后装入试剂瓶中并用封口膜封口,保存在干燥器中备用. 石英棉购自Sigma公司(美国).
CBs混合标准液含有MoCB,3种DiCB(1,4-DiCB、1,3-DiCB和1,2-DiCB),3种TrCB(1,3,5-TrCB、1,2,4-TrCB和1,2,3-TrCB),3种TeCB(1,2,3,5-TeCB、1,2,4,5-TeCB和1,2,3,4-TeCB),PeCB以及HCB,各物质浓度为0.1 mg·mL−1,购自AccuStandard公司(美国). 13C同位素标记的六氯苯标准液(0.1 mg·mL−1于壬烷中)作为内标,购自Cambridge公司(美国).
-
采用液液萃取法提取水样中的CBs,具体步骤:首先,量取250 mL水样置于分液漏斗中,并加入5 g 氯化钠、25 mL二氯甲烷和100 ng的13C6-HCB标准,充分振摇6 min,待溶液静置分层后,收集二氯甲烷相. 该萃取过程共重复3次,合并每一次的萃取液. 随后,使用无水硫酸钠对萃取液进行脱水,并在45 ℃条件下利用旋转蒸发仪将萃取液浓缩至2—3 mL. 采用自制层析柱(5 mL玻璃移液管,从上往下依次为 0.5 g无水硫酸钠、0.5 g硅胶和1 g弗罗里硅土)对浓缩后的萃取液进行净化,先用10 mL正己烷预淋洗净化柱,随后上载萃取液,再用20 mL正己烷洗脱目标物. 将上述净化过程收集的洗脱液经旋转蒸发浓缩至2—3 mL,并氮吹浓缩定容至1 mL,密封保存于4 ℃冰箱,待进行仪器分析.
-
采用气相色谱(安捷伦7890A型)和质谱(安捷伦5975型)联用方法进行CBs的定性和定量分析.
气相参数:毛细管气相色谱柱DB-5MS(60 m×0.25 mm×0.25 μm,美国Agilent公司);以1.0 mL·min−1流速的氦气(99.999%)作为载气;进样口温度:250 ℃;程序升温模式:初始温度40 ℃,保持6 min,以10 ℃·min−1升温至60 ℃,保持1 min,以2.5 ℃·min−1升温至100 ℃,以10 ℃·min−1升温至250 ℃,保持3 min,以20 ℃·min−1升温至300 ℃,保持3 min;进样量为1 μL.
质谱参数:电子轰击离子源(EI);离子源温度230 ℃;四极杆温度150 ℃;传输线温度280 ℃;离子源电子能量70 eV;溶剂延迟6 min;采集模式为选择离子扫描(SIM).
-
实验过程保证严格的质量控制,每个水样在进行前处理前加入了13C6-HCB标准指示目标物的回收率. 每7个样品随行1个实验室空白,13C6-HCB的加标回收率为78%—107%. 空白中检出MoCB(平均浓度2.43 ng·L−1)、DiCB(8.12 ng·L−1)、TrCB(1.12 ng·L−1)、TeCB(0.27 ng·L−1)、PeCB(0.47 ng·L−1)和HCB(0.36 ng·L−1),定量结果经空白扣除. 此外,由于所采用的仪器分析方法无法彻底分开1,2,4,5-TeCB和1,2,3,5-TeCB这两种同分异构体,因此在数据分析时对这两种物质进行合并定量. 目标物的检出限(3倍信噪比)范围在0.15—0.80 ng·L−1,定量限(10倍信噪比)范围在0.50—2.67 ng·L−1,低于检出限的目标物浓度用0代替,以便于数据统计分析.
-
环境影响度(ambient severity, AS)是一个用于评估污染物对环境影响程度的指标,即水样中某种化合物的实际浓度(Ci)和其在水体中的环境目标值(CA)的比值. 当采用以对健康影响为依据的排放环境目标值(discharge multimedia environmental goals, DMEGWH)作为CA时,AS可以反映出污染物的生物健康风险,对判断排放的污染物是否会构成人类健康风险具有很大帮助. AS的计算公式如下所示[11-12]:
式中,DMEGWH也叫作最小急性毒性作用排放值,表示生物体与排放流短期接触时排放水体中该化合物的最大允许浓度. 该值可以根据大鼠经口的半数致死量(median lethal dose, LD50)估算获得,本研究所使用的LD50来自先前的毒理学研究[5-6]. ASi值越大,表示排放水体中该化合物的影响越大. 当ASi < 1时,表明排放水体中该化合物不会对人体健康产生不可逆转的有害影响.
本研究暂不考虑各化合物之间的复合作用,并假定AS值大小与潜在危害呈线性关系,并且各化合物的效应是可以加和的. 基于此,可通过计算各组成部分的AS值之和来评估它们对环境的总影响,称为总环境影响度(TAS)[13]:
式中,ASij是指j类化合物中第i个化合物的AS,TASij是指j类化合物的总AS. 评价目标污染物对环境影响程度同样也以1为临界点.
-
风险熵值(risk quotients, RQs)是一种常用的环境健康风险评估指标,用于比较环境中化学物质的暴露水平和健康效应阈值之间的关系,从而来评估人体或生态系统受到的潜在风险. 可以通过计算水环境中污染物的实测浓度(measured environmental concentration, MEC)和预测无效应浓度(predicted no effect concentration, PNEC)的比率来确定RQs[5],计算公式如式(4)所示.
式中,PNEC为半致死浓度(LC50,即暴露96 h后,导致50%的鱼死亡的污染物浓度)除以评估因子1000,LC50参考先前的研究[5, 14-15]. 本研究对每一种单体都进行了RQ评估,每个处理单元污水的总RQs是指所有污染物的RQ之和[14]. RQs < 0.1时,表明生态风险较低;0.1 < RQs <1时,表明存在中等生态风险;RQs > 1时,表明存在高生态风险.
-
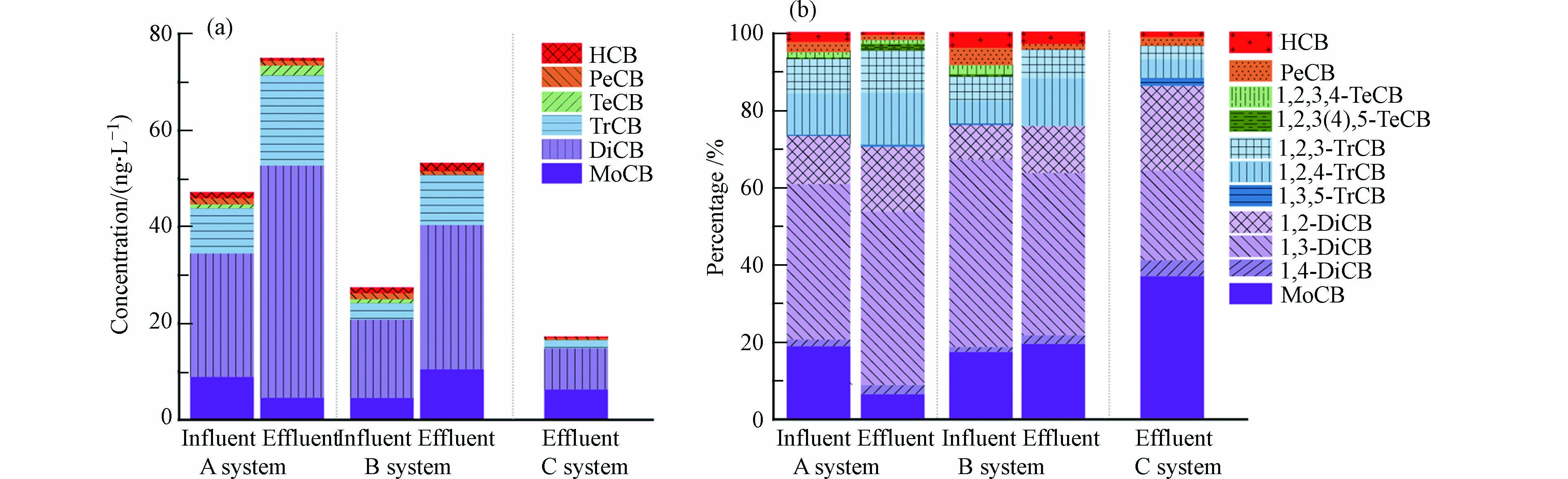
所采集的浙江省两家污水处理厂水样中CBs的检出率为100%,暗示着该地区工业及生活污水中CBs污染普遍存在. 图2(a)显示了污水处理A、B、C系统进出水中CBs的浓度,其中污水处理A系统的进水和出水中CBs总浓度分别为47.0 ng·L−1和75.1 ng·L−1,B系统的进水和出水浓度分别为27.5 ng·L−1和52.9 ng·L−1,C系统缺少进水样品,在此不作分析,其出水中的CBs总浓度为17.4 ng·L−1. 3个污水处理系统排放出水中MoCB和DiCB浓度均远低于我国《城镇污水处理厂污染物排放标准》(GB 18918—2002)[16]规定的排放限值(MoCB 3 × 105 ng·L−1, 1,4-DiCB 4 × 105 ng·L−1, 1,2-DiCB 1 × 106 ng·L−1). 此外,广东省纺织印染废水处理厂出水中CBs浓度最高达678 ng·L-1[5],远高于本研究中数值. 这些结果表明,浙江嘉兴地区工业废水和生活污水中CBs的污染较小. 需要警惕的是,污水处理A系统和B系统出水中CBs的浓度反而高于进水中的浓度,说明该污水处理厂采用的处理工艺未能有效去除水中CBs,甚至可能在处理过程中增大CBs污染. 先前的研究[5]也同样指出了常规污水处理厂难以解决污水中CBs的污染问题.
污水处理A、B、C系统进出水中CBs组成分布情况如图2(b)所示. 污水处理A系统和B系统进水中CBs的组成分布相似,以DiCB为主要污染物,分别占总CBs的54.5%和58.8%. 其次是MoCB(占比为18.7%和17.2%)和TrCB(占比为19.9%和12.5%). 此结果和这几种氯代苯类化合物在纺织印染及工业活动中被广泛用作染料、色基、颜料的中间体和原料、脱脂剂和阻燃剂等[6, 17]有关. TeCB、PeCB、HCB仅占总CBs浓度的很小一部分,可能是因为它们在纺织印染工业中使用相对较少[18],尤其PeCB和HCB已被禁止商业化使用,仅作为杂质或者少量副产物存在,因此相应的排放量也相对较少. 由于两家污水处理厂污水来源和处理工艺不同,出水中CBs的组成有所差异. 在A系统和B系统出水中DiCB仍是主要污染物(占比分别为64.1%和56.5%),PeCB和HCB的占比相比进水中的有所下降,而TrCB的占比显著提高. 这表明这两个系统污水处理过程中可能存在着高氯苯脱氯行为,TrCB是主要的中间产物[19-20]. 在C系统的出水中DiCB也是主要污染物(49.3%),但MoCB比例(36.8%)较A/B系统(17.2%—19.2%)的高.
进一步分析发现,污水处理A和B系统进出水中1,3-DiCB占最高比例(40.3%—48.5%),C系统出水中1,3-DiCB也是主要成分之一(23.2%). 这可能是由于高氯代苯常见的一条脱氯途径为,HCB→PeCB→1,2,3,4-TeCB→1,2,3-TrCB→1,3-DiCB→MoCB [20-21]. 由于苯环上3个氯原子相邻结构不稳定,中间的氯原子结合苯环上碳原子的力最弱,使其最容易脱离[22-23]. 当1,2,3-TrCB脱氯后,形成了稳定的1,3-DiCB结构,脱氯反应难以继续[22, 24].
-
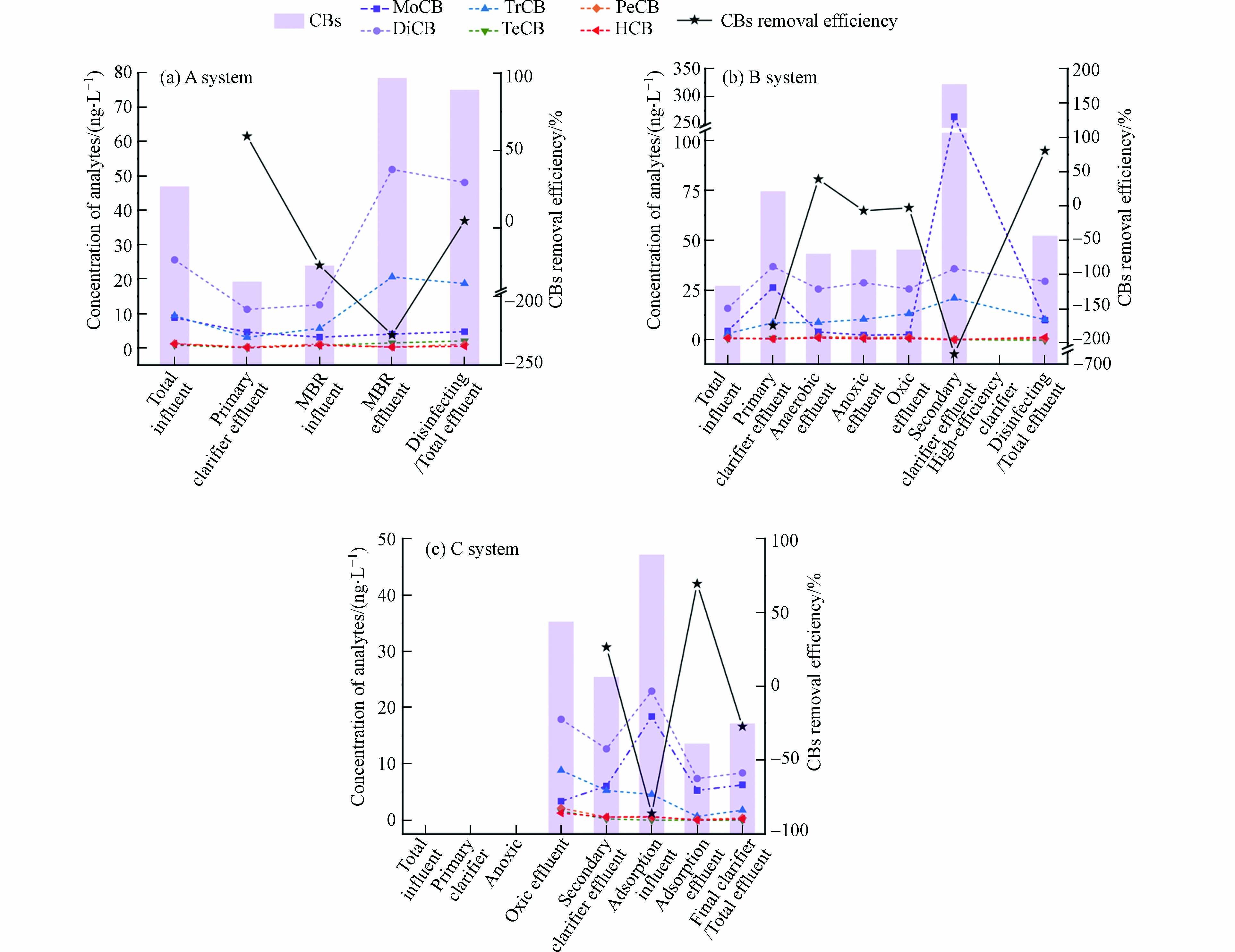
不同污水处理系统各个工艺单元污水中CBs的浓度以及去除效率如图3所示. 污水处理A系统主要采用膜生物反应器工艺(membrane bio-reactor, MBR). 经MBR处理后,A系统污水中的CBs浓度出现了大幅上升,其中DiCB和TrCB的含量分别增长了314%和263%. 说明MBR工艺对CBs并没有去除效果,甚至可能导致其污染加重,其他关于含纺织染色废水中CBs研究也观察到类似的情况[5]. 这可能是由于苯环上的氯原子增强了CBs的吸电子能力,导致膜生物反应器内微生物产生的氧化酶难以从苯环上吸引电子并发生氧化反应[5]. 同时,A系统进水组成复杂,可能含有抑制MBR生物活性、影响生物处理效能的物质[25]. 此外,MBR工艺可能因污水中的颗粒物和有机物等的吸附或者沉积而出现膜堵塞或膜污染问题[26],导致CBs在膜上积累并在MBR运行过程中重新释放.
污水处理B系统主要采用了厌氧-缺氧-好氧工艺(A2/O)和高效沉淀工艺. 在A2/O工艺中,污水中CBs的去除主要发生在厌氧段,缺氧和好氧段对CBs的去除效果不佳. 这可能是由于有机氯化合物在厌氧环境中更容易发生脱氯反应,厌氧脱氯后非氯代或低氯代产物的生物矿化则主要在好氧段中进行[5, 22]. 该系统中污水经过二沉池处理后,水体中MoCB浓度显著上升,表明存在着二次污染的情况,这可能是由于MoCB与污泥结合较弱,在处理过程中被重新释放回到污水中. 其后的高效沉淀池中投加了砂和活性碳以及一些药剂,经该单元处理后MoCB浓度大幅度降低,得到了有效去除.
由于污水处理C系统缺少进水样本,因此研究采用好氧池出水作为进水参照,评估了C系统的总CBs去除率. 结果表明,该系统对CBs有一定的去除效果,且其出水中CBs总浓度是所有污水处理系统中最低的. 这可能与该厂污水处理量较小有关. 吸附反应池中投加了铁盐类混凝剂,能够有效去除CBs,其中不溶性物质对CBs的吸附去除起主要作用.
综上所述,本研究中的3个污水处理系统对污水中CBs的去除效率普遍不高,部分工艺还存在污染再释放问题,难以实现CBs水污染的消减控制.
-
污水处理厂排放水体CBs的环境影响度及相关数据如表1所示. 3个污水处理系统出水中每个目标物的AS值及总CBs的TAS值处于1×10-10到1×10−7级别范围之内,均小于1. 该结果表明,所研究的两家污水处理厂排放水体中的CB单体或CBs整体对人类健康都不会造成显著危害. 其中,1,3-DiCB和1,2-DiCB的健康影响度高于其他氯苯类化合物,其AS值范围分别为5.58×10−9—4.70×10−8和1.12×10−8—3.73×10−8,分别占总健康影响度的20.5%—38.2%和23.7%—41.3%. 而TeCB,PeCB以及HCB对健康的影响极小(AS值均小于1×10−8),对总健康影响度的贡献仅占3.1%—5.1%,可忽略不计.
不同污水处理系统进出水中CBs的RQs及相关数据如表2所示. 所有污水处理系统进出水中CBs的RQs均小于0.1,说明这些水体中存在的CBs对生态环境造成的潜在风险较小. 但是,由于这些污水会持续不断地排入自然水体,而CBs具有生物蓄积性和持久性[2],可能在水生生物中累积并产生一定的生物毒性效应,最终通过食物链危害人类健康,因此仍需警惕污水排放CBs带来的长期性的生态环境风险.
-
本文研究了浙江省两家污水处理厂中CBs的赋存特征、消减规律及排放风险. 研究发现CBs在污水处理厂污水中普遍存在,但污染水平较低,以低氯代苯(如DiCB)为主. CBs在厌氧处理或污泥吸附沉淀处理过程中能够被部分去除,但在MBR工艺、吸附反应、沉淀处理等过程中存在二次污染问题. 所研究污水处理厂排放水体CBs的理论生态风险较小,但仍需警惕持续排放可能带来风险加剧. 所用AS和HQ评估方法涉及的一些假设和简化对风险评估结果也会产生影响,多种氯苯类化合物复合污染导致的毒性效应需进一步研究. 此外,未来也需要加强对污水处理厂污水中其他高毒性有机污染物的研究和风险评估.
浙江省典型污水处理厂中氯苯类化合物的赋存特征及风险评估
Occurrence characteristics and risk assessment of chlorobenzenes in typically wastewater treatment plants from Zhejiang Province
-
摘要: 氯苯类化合物(chlorobenzene,CBs)是一类具有高毒性、难降解和易富集性的有机氯化合物,持续受到广泛关注. 污水处理厂在城市水污染控制中发挥着重要作用,然而,目前关于污水处理厂中的CBs研究十分有限,其消减规律与排放特征仍不清楚. 本研究系统分析了浙江省两家典型污水处理厂中CBs的赋存特征、去除效率及排放潜在风险. 发现CBs在各污水处理厂污水中普遍存在,但污染水平较低,出水中CBs的总浓度范围为17.4—75.1 ng·L−1,远低于我国相关排放标准. 二氯苯是进出水中CBs的主要组成成分,占比49.3%—64.1%. 厌氧处理及污泥吸附沉淀对CBs的去除效果相对较好,但现有污水处理工艺对CBs的总体去除效果不佳,部分处理单元还存在CBs含量上升情况. 基于环境影响度(ambient severity,AS)和风险熵值(risk quotients,RQs)评估结果表明,所研究污水处理厂排放水中CBs对人体健康以及生态风险较小(AS <1,RQs <0.1). 研究结果有助于深入了解CBs在污水处理系统中的环境行为和排放风险,也为优化污水处理工艺、进一步控制和减少CBs水污染提供了基础数据。Abstract: Chlorobenzenes (CBs), a group of chlorinated organic compounds, have been concerned for their high toxicity, poor degradability, and strong ability of accumulation by the public. Wastewater treatment plants (WWTPs) play an important role in controlling the urban water pollution; whereas the research on CBs in WWTPs is extremely limited, reduction trends and emission characteristics of which are still not well-known. This study systematically analyzed the occurrence characteristics, removal efficiency, and potential risks of emission of CBs in different treatment processes of two typical WWTPs in Zhejiang Province. The results showed that CBs presented frequently in the wastewater samples from the WWTPs, but in low pollution levels. Concentrations of CBs in the effluents were in the range 17.4—75.1 ng·L−1, far below the related emission standard of China. Dichlorobenzene was the main component of CBs in the influents and effluents, accounting for 49.3%—64.1% of the total CBs. Anaerobic treatment and sludge adsorption precipitation had relatively good removal efficiency for CBs. However, the existing wastewater treatment processes generally had poor capacities for removing CBs, and some treatment processes were even found an increased effect on CB contents. Based on the evaluation results of ambient severity (AS) and risk quotient (RQ), it was indicated that the human health and ecological environmental impact of CBs in the effluent from the studied WWTPs was relatively low (AS < 1, RQ < 0.1). These findings contribute to a deeper understanding of the environmental behaviors and emission risks of CBs in WWTPs, also provide essential data for optimizing wastewater treatment processes and further controlling and reducing the CBs in wastewater.
-

-
表 1 污水处理厂排放水体CBs的环境影响度及相关数据
Table 1. The ambient severity (AS) of CBs in the effluent from WWTPs and relevant data
污染物
Pollutants a半数致死量/
(mg·kg−1)
LD50[5-6]环境介质阈值/
(μg·L−1)
DMEGWHA系统
A systemB系统
B systemC系统
C system浓度/(ng·L−1)
Concentration环境影响度/
(×10−9)
AS浓度/(ng·L−1)
Concentration环境影响度/
(×10−9)
AS浓度/(ng·L−1)
Concentration环境影响度/
(×10−9)
ASMoCB 2290 1545750 4.72 3.05 10.2 6.60 6.34 4.10 1,4-DiCB 500 337500 1.76 5.21 1.18 3.50 0.71 2.10 1,3-DiCB 1062 716850 33.7 47.0 22.2 31.0 4.00 5.58 1,2-DiCB 500 337500 12.6 37.3 6.48 19.2 3.79 11.2 1,3,5-TrCB 800 540000 0.38 0.70 < 0.61 b < 1.13 0.35 0.65 1,2,4-TrCB 756 510300 10.1 19.8 6.52 12.8 0.84 1.65 1,2,3-TrCB 1830 1235250 8.20 6.64 3.92 3.17 0.60 0.49 1,2,3(4),5-TeCB c 1500 1012500 1.33 1.31 < 0.26 b < 0.26 < 0.26 b < 0.26 1,2,3,4-TeCB 1727 1165725 0.70 0.06 < 0.38 b < 0.33 < 0.38 b < 0.33 PeCB 1167 787725 1.01 1.28 0.80 1.02 0.39 0.50 HCB 1080 729000 0.48 0.66 1.60 2.19 0.22 0.30 TAS — — — < 124 — < 81.1 — < 27.2 a MoCB、DiCB、TrCB、TeCB、PeCB和HCB分别代表一氯苯、二氯苯、三氯苯、四氯苯、五氯苯和六氯苯,TAS为总环境影响度;b该物质未检出,用检出限代替浓度进行计算;c 1,2,3,5-TeCB和1,2,4,5-TeCB无法分峰,合并定量,记为1,2,3(4),5-TeCB.
a MoCB, DiCB, TrCB, TeCB, PeCB and HCB represent monochlorobenzene, dichlorobenzene, trichlorobenzene, tetrachlorobenzene, pentachlorobenzene and hexachlorobenzene, respectively, and TAS is total ambient severity; b This substance was not detected and the concentration was substituted with the limit of detection for the calculation; c 1,2,3,5-TeCB and 1,2,4,5-TeCB could not be separated into single peaks and were combined for quantification, which was recorded as 1,2,3(4),5-TeCB.表 2 不同污水处理系统进出水中CBs的风险熵值及相关数据
Table 2. The Risk quotients (RQs) values and related data of CBs in the influent and effluent of different wastewater treatment systems
污染物
Pollutants a预测无效应浓度/
(μg·L−1) [5, 14, 15]
PNEC风险熵值 RQs A系统
A systemB系统
B systemC系统
C system进水 Influent 出水 Effluent 进水 Influent 出水 Effluent 出水 Effluent MoCB 2.60 0.003 0.002 0.002 0.004 0.002 1,4-DiCB 0.70 0.001 0.003 0.001 0.002 0.001 1,3-DiCB 0.96 0.020 0.035 0.014 0.023 0.004 1,2-DiCB 0.74 0.008 0.017 0.003 0.009 0.005 1,3,5-TrCB —b — — — — — 1,2,4-TrCB 1.32 0.004 0.008 0.001 0.005 0.001 1,2,3-TrCB 2.20 0.002 0.004 0.001 0.002 0.000 1,2,3(4),5-TeCB c 1.55 0.000 0.001 0.000 0.000 0.000 1,2,3,4-TeCB 1.10 0.001 0.001 0.001 0.000 0.000 PeCB 0.25 0.005 0.004 0.005 0.003 0.002 HCB 7.60 0.000 0.000 0.000 0.000 0.000 Total — 0.044 0.074 0.027 0.048 0.015 a MoCB、DiCB、TrCB、TeCB、PeCB和HCB分别代表一氯苯、二氯苯、三氯苯、四氯苯、五氯苯和六氯苯;b数据无法获取;c 1,2,3,5-TeCB和1,2,4,5-TeCB无法分峰,合并定量,记为1,2,3(4),5-TeCB.
a MoCB, DiCB, TrCB, TeCB, PeCB and HCB represent monochlorobenzene, dichlorobenzene, trichlorobenzene, tetrachlorobenzene, pentachlorobenzene and hexachlorobenzene, respectively; b Data not available; c 1,2,3,5-TeCB and 1,2,4,5-TeCB could not be separated into single peaks and were combined for quantification, which was recorded as 1,2,3(4),5-TeCB. -
[1] UNEP. All POPs listed in the Stockholm Convention [DB/OL]. [2023-3-10]. http://chm.pops.int/TheConvention/ThePOPs/ListingofPOPs/tabid/2509/Default.aspx [2] SONG Y, WANG F, BIAN Y R, et al. Chlorobenzenes and organochlorinated pesticides in vegetable soils from an industrial site, China [J]. Journal of Environmental Sciences, 2012, 24(3): 362-368. doi: 10.1016/S1001-0742(11)60720-1 [3] PATEL A, VYAS T K. Chlorobenzene degradation via ortho-cleavage pathway by newly isolated Microbacterium sp. strain TAS1CB from a petrochemical-contaminated site [J]. Soil and Sediment Contamination:an International Journal, 2015, 24(7): 786-795. doi: 10.1080/15320383.2015.1029042 [4] KLEES M, HOMBRECHER K, GLADTKE D. Polychlorinated biphenyls in the surrounding of an e-waste recycling facility in North-Rhine Westphalia: Levels in plants and dusts, spatial distribution, homologue pattern and source identification using the combination of plants and wind direction data [J]. Science of the Total Environment, 2017, 603/604: 606-615. doi: 10.1016/j.scitotenv.2017.06.079 [5] YUAN Y Q, NING X A, ZHANG Y P, et al. Chlorobenzene levels, component distribution, and ambient severity in wastewater from five textile dyeing wastewater treatment plants [J]. Ecotoxicology and Environmental Safety, 2020, 193: 110257. doi: 10.1016/j.ecoenv.2020.110257 [6] WHO. Chlorobenzenes other than hexachlorobenzene: Environmental aspects. [M/OL]. [2023-3-10]. http://inchem.org/documents/cicads/cicads/cicad60.htm [7] ZHANG H Y, WANG Y W, SUN C, et al. Levels and distributions of hexachlorobutadiene and three chlorobenzenes in biosolids from wastewater treatment plants and in soils within and surrounding a chemical plant in China [J]. Environmental Science & Technology, 2014, 48(3): 1525-1531. [8] BYLIŃSKI H, ASZYK J, KUBICA P, et al. Differences between selected volatile aromatic compound concentrations in sludge samples in various steps of wastewater treatment plant operations [J]. Journal of Environmental Management, 2019, 249: 109426. doi: 10.1016/j.jenvman.2019.109426 [9] CAI Q Y, MO C H, WU Q T, et al. Occurrence of organic contaminants in sewage sludges from eleven wastewater treatment plants, China [J]. Chemosphere, 2007, 68(9): 1751-1762. doi: 10.1016/j.chemosphere.2007.03.041 [10] SONG J Y, ZHAO J, YANG C, et al. Integrated estrogenic effects and semi-volatile organic pollutants profile in secondary and tertiary wastewater treatment effluents in North China [J]. Journal of Hazardous Materials, 2022, 435: 128984. doi: 10.1016/j.jhazmat.2022.128984 [11] 邓赐洪. 多介质环境目标值在生物农药建设项目环境影响评价中的应用 [J]. 海峡科学, 2014(3): 21-22. DENG C H. Application of multi-media environmental target value in environmental impact assessment of biopesticide construction project [J]. Straits Science, 2014(3): 21-22(in Chinese).
[12] 高香玉, 崔益斌, 胡长伟, 等. 太湖梅梁湾2008年有机污染物检测及环境影响度 [J]. 中国环境科学, 2009, 29(12): 1296-1300. GAO X Y, CUI Y B, HU C W, et al. Detection and ambient severity evaluation of organic compounds in Meiliang Bay of Taihu Lake in 2008 [J]. China Environmental Science, 2009, 29(12): 1296-1300(in Chinese).
[13] GAO X Y, SHI X R, CUI Y B, et al. Organic pollutants and ambient severity for the drinking water source of western Taihu Lake [J]. Ecotoxicology, 2011, 20(5): 959-967. doi: 10.1007/s10646-011-0681-6 [14] ZHANG K F, CHANG S, FU Q, et al. Occurrence and risk assessment of volatile organic compounds in multiple drinking water sources in the Yangtze River Delta region, China [J]. Ecotoxicology and Environmental Safety, 2021, 225: 112741. doi: 10.1016/j.ecoenv.2021.112741 [15] BOUTONNET J C, THOMPSON R S, de ROOIJ C, et al. 1, 4-dichlorobenzene marine risk assessment with special reference to the osparcom region: North sea [J]. Environmental Monitoring and Assessment, 2004, 97(1): 103-117. [16] 国家环境保护总局, 国家质量监督检验检疫总局. 城镇污水处理厂污染物排放标准GB 18918-2002 [S]. 2002. State Environmental Protection Administrationstate, General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China. Discharge standard of pollutants for municipal wastewater treatment plant GB 18918-2002 [S]. 2002(in Chinese).
[17] 蔡建利, 龙建银, 杨斌, 等. 对二氯苯的生产、技术及市场前景 [J]. 中国氯碱, 2009(7): 1-4. CAI J L, LONG J Y, YANG B, et al. Production, technology and market prospect of p-dichlorobenzene [J]. China Chlor-Alkali, 2009(7): 1-4(in Chinese).
[18] SU F H, ZHANG P. Accurate analysis of trace pentachlorophenol in textiles by isotope dilution liquid chromatography-mass spectrometry [J]. Journal of Separation Science, 2011, 34(5): 495-499. doi: 10.1002/jssc.201000476 [19] LERCHE D, van de PLASSCHE E, SCHWEGLER A, et al. Selecting chemical substances for the UN-ECE POP Protocol [J]. Chemosphere, 2002, 47(6): 617-630. doi: 10.1016/S0045-6535(02)00028-0 [20] TONG M, YUAN S H. Physiochemical technologies for HCB remediation and disposal: A review [J]. Journal of Hazardous Materials, 2012, 229/230: 1-14. doi: 10.1016/j.jhazmat.2012.05.092 [21] SHIH Y H, HSU C Y, SU Y F. Reduction of hexachlorobenzene by nanoscale zero-valent iron: Kinetics, pH effect, and degradation mechanism [J]. Separation and Purification Technology, 2011, 76(3): 268-274. doi: 10.1016/j.seppur.2010.10.015 [22] BRAHUSHI F, KENGARA F O, SONG Y, et al. Fate processes of chlorobenzenes in soil and potential remediation strategies: A review [J]. Pedosphere, 2017, 27(3): 407-420. doi: 10.1016/S1002-0160(17)60338-2 [23] LIU C Y, JIANG X, WANG F, et al. Hexachlorobenzene dechlorination as affected by nitrogen application in acidic paddy soil [J]. Journal of Hazardous Materials, 2010, 179(1/2/3): 709-714. [24] JIANG L, WANG Q, LIU H, et al. Influence of degradation behavior of coexisting chlorobenzene congeners pentachlorobenzene, 1, 2, 4, 5-tetrachlorobenzene, and 1, 2, 4-trichlorobenzene on the anaerobic reductive dechlorination of hexachlorobenzene in dye plant contaminated soil [J]. Water, Air, & Soil Pollution, 2015, 226(9): 299. [25] LIN H J, PENG W, ZHANG M J, et al. A review on anaerobic membrane bioreactors: Applications, membrane fouling and future perspectives [J]. Desalination, 2013, 314: 169-188. doi: 10.1016/j.desal.2013.01.019 [26] KANG G D, CAO Y M. Development of antifouling reverse osmosis membranes for water treatment: A review [J]. Water Research, 2012, 46(3): 584-600. doi: 10.1016/j.watres.2011.11.041 -



 下载:
下载: