-
电化学电容器是重要的储能设备之一,具有放电容量较大、能量密度较高等优点,已经被广泛应用于混动汽车、军工等新能源领域之中[1,2]. 为了获得优异的充放电性能,研究者开发了多种电极材料,如碳材料[3 − 6]、导电聚合物[7 − 9]、氧化物[10 − 16]及复合材料[17 − 19]. 以氧化物为电极材料,可以获得较高的放电比容量和能量密度,并且制备简单,价格便宜. 因此,氧化物在电容器中备受关注. Yang等以镍钴锰混合氧化物NCM811为活性物质进行充放电,电流密度为1 A·g−1时,放电比容量为208.3 F·g−1,能量密度为26 W·kg−1[11].
电化学电容器的充放电性能不仅与电极材料有关,还与电解液有关. 目前已经有多种电解液被应用于超级电容器之中,如HCl、KOH、Na2SO4等[7,10,12]. 氧化物在不同电解液中产生不同的电化学行为,可以获得不同的充放电性能. 以氧化物为电极材料时,电解液多为KOH溶液. 研究者将颗粒状NiO置于6 mol·L−1 KOH中充放电,通过Ni2+/Ni3+的转变产生赝电容. 电流密度为1 A·g−1时,放电比容量可达254.5 F·g−1[10]. 然而,KOH腐蚀性较强,不利于电容器长时间保存. 以中性溶液为电解液可以解决这一问题. Yang等以α-Fe2O3为活性物质,1 mol·L−1 Na2SO4为电解液,通过Fe2+/Fe3+法拉第反应获得较高的电化学性能. 电流密度为3 A·g−1时,放电比容量可达306.9 F·g−1[12]. 然而,将电流密度增大到10 A·g−1时,容量保持率仅为31.9%. 对电极材料在不同电解液中的电化学行为进行探究,有助于优化电容器并提高充放电性能.
由于NiCo2O4中含有Ni和Co两种过渡金属元素,可能同时参与充放电过程,获得较好的充放电性能[11]. KOH可以提供OH−并与Ni、Co发生氧化还原反应,产生赝电容,提高放电比容量[11-12]. K4Fe(CN)6溶液呈中性,并且在电场作用下可能发生氧化还原反应产生赝电容,提高充放电性能. 为此,本文通过水热合成法制备NiCo2O4,分别选用KOH和K4Fe(CN)6为电解液组装三电极,探究NiCo2O4在KOH和K4Fe(CN)6溶液中的电化学行为和倍率充放电性能.
-
分别以NiCl2·6H2O、CoCl2·6H2O为Ni源、Co源,尿素为沉淀剂,结合水热合成法和高温固相法制备电极材料NiCo2O4,制备原理如方程式①—④所示[11,20-21]. NiCo2O4的具体步骤如下:将1.185 g NiCl2·6H2O和2.38 g CoCl2·6H2O溶于20 mL去离子水中,并将1.4 g尿素溶于20 mL去离子水和20 mL乙醇的混合溶液中. 将尿素溶液逐滴加入至Ni2+和Co2+混合溶液中,搅拌2 h. 将所得溶液转移至高压反应釜中,并于160 ºC水热处理24 h. 将产物冷却,并用去离子水洗涤至中性,并于100 ºC干燥12 h. 将所得产物于350 ℃焙烧2 h(升温速率和降温速率均为2 ℃·min-1),得到产物NiCo2O4.
-
利用XD-6型X-射线衍射仪对NiCo2O4的物相信息进行分析,Cu 靶 Kα1(λ=
0.15406 nm),扫描范围10°—80°. 采用K-Alpha型X-射线光电子能谱仪(XPS)对电极材料结构进行表征. 利用Sigma 300型扫描电子显微镜分析材料形貌. 通过FEI Tecnai F20型透射电子显微镜分析材料精细结构. 结合XPS和能量色散谱(EDS)分析材料组成. 利用ASAP2460 型比表面分析仪测定材料孔结构. -
按照8 : 1 : 1的质量比称取NiCo2O4、超导电碳(SP)和聚偏二氟乙烯(PVDF). 将PVDF溶于8 g N-甲基吡咯烷酮(NMP)之中,再加入SP和NiCo2O4,搅拌4 h. 将所得浆料涂覆在1 cm × 1 cm的泡沫镍表面,并置于80 ℃干燥箱中保持12 h. 涂覆浆料前后,电极片厚度分别为100 μm、105 μm. 泡沫镍表面的活性物质含量约为5 mg. 以NiCo2O4极片为工作电极、Pt片为对电极、HgO/Hg电极为参比电极组装三电极,并将其分别置于6 mol·L−1 KOH和0.5 mol·L−1 K4Fe(CN)6中进行充放电测试,探究NiCo2O4在不同电解液中的电化学行为.
分别利用循环伏安(CV)曲线和恒电流充放电(GCD)曲线分析NiCo2O4在KOH和K4Fe(CN)6中的充放电性能. 放电比容量、能量密度和功率密度. 利用CV曲线和公式(1)、(2)计算三电极体系的伏安放电比容量和平均能量密度,通过GCD曲线和公式(3)、(4)、(5)计算三电极的放电比容量、能量密度和功率密度[11,22 − 24]. 其中:CS为NiCo2O4在KOH和K4Fe(CN)6中的伏安放电比容量(F·g−1)、Cg为NiCo2O4在KOH和K4Fe(CN)6中的恒流放电比容量(F·g−1),Ea、Eg为对应的伏安放电能量密度和恒流放电能量密度(Wh·kg−1),Pg为NiCo2O4在两种电解液中的功率密度(W·kg−1),I为充放电电流(A),V为电压窗口(V),m为活性物质的质量(g),S为扫描速率(V·s−1)、t为放电时间(s),
$ \int_{ }^{ }I\mathrm{d}V $ 为CV曲线包围的面积(A·V),$ \int_{ }^{ }V\mathrm{d}t $ 为GCD曲线中放电曲线包围的面积(V·s). -
图1为NiCo2O4的XRD图. 由图1可知,XRD曲线中的衍射峰与立方相NiCo2O4的PDF#20-0781一致,晶格常数为0.811 nm,因此NiCo2O4制备成功. 衍射角为18.906°、31.148°、32.655°、36.696°、44.622°、59.094°、64.980°处出现(111)、(220)、(311)、(400)、(511)和(440)晶面的衍射峰. 面心立方晶体中,h、k、l全为奇数或偶数时,可分别采用公式(6)计算出立方相晶体的晶面间距. 其中:dhkl为晶面间距,a为晶格常数,h、k、l为晶面指数. 经过计算,(111)、(220)、(311)、(400)、(511)和(440)的晶面间距分别为
0.4682 、0.2867 、0.2445 、0.2028 、0.1561 、0.1434 nm. PDF#20-0781对应NiCo2O4的晶面间距分别为0.4690 、0.2869 、0.2447 、0.2029 、0.1562 、0.1434 nm. 实际晶面间距与标准晶面间距吻合度较高,因此所制备的NiCo2O4为面心立方结构. -
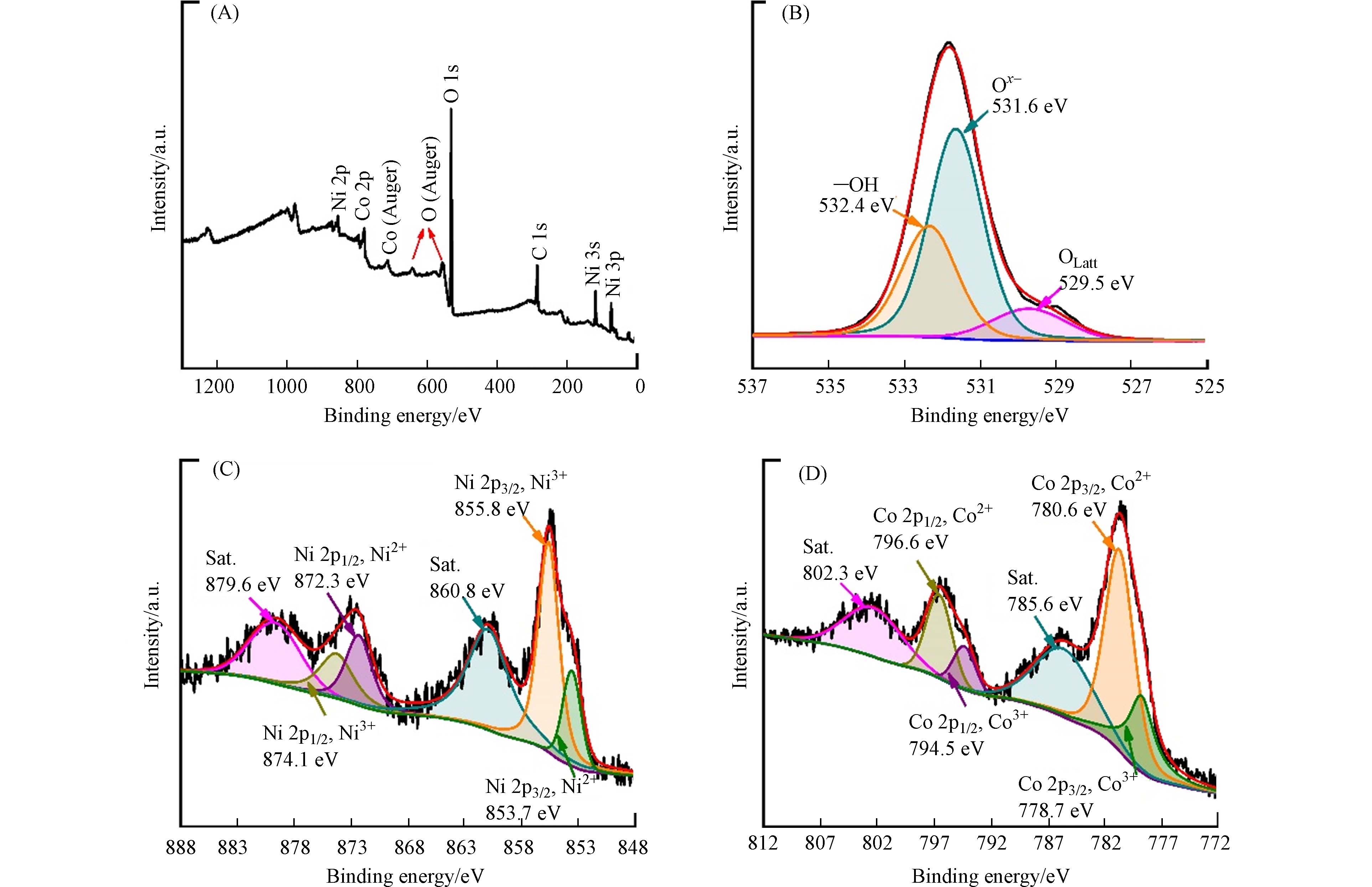
图2为NiCo2O4的XPS图. 由全谱图(图2A)可知,NiCo2O4中含有Ni、Co、O和C元素. 其中,C元素可能是由于吸附在NiCo2O4的孔道内部的CO2未被完全排出所致[24]. NiCo2O4中Ni、Co和O元素占比分别为11.6%、25.56%、50.31%,比值约为1 : 2.2 : 4.3,因此NiCo2O4的化学式可以记为NiCo2.2O4.3. 由O 1s分谱图(图2B)可知,532.4、531.6、529.5 eV处出现3个能级峰,即NiCo2O4中的O元素主要以3种形式存在,分别为NiCo2O4表面—OH、M—O骨架中的Ox-离子(M为Ni或Co)和NiCo2O4晶体中的晶格氧[10,11]. 由Ni 2p、Co 2p分谱图(图2C、图2D)可知, 874.1 、855.8 eV处的谱峰为Ni3+的Ni 2p1/2、Ni 2p3/2自旋轨道分裂峰,872.3、853.7 eV处的谱峰为Ni2+的Ni 2p1/2、Ni 2p3/2自旋轨道分裂峰(图2C)[10,11]. 796.6 eV、780.6 eV处的谱峰为Co2+的Co 2p1/2、Co 2p3/2自旋轨道分裂峰,794.5、778.7 eV处的谱峰为Co3+的Co 2p1/2、Co 2p3/2自旋轨道分裂峰(图2D)[10,11]. 由XPS结果可知,NiCo2O4中Ni、Co元素同时以Ni2+、Ni3+、Co2+、Co3+形式存在.
-
图3为NiCo2O4的SEM、TEM和EDS测试结果. 由图3A可知,NiCo2O4由小颗粒堆积而成,相互堆积的小颗粒之间含有较多小孔. 与SEM结果一致,在TEM图中也可以看到小颗粒和小颗粒之间的空隙(图3B). 由图3B可知,NiCo2O4衍射花样中含有多个亮斑,并且形成同心圆. 此外,由图3C中可以看到(220)和(311)晶面的晶格条纹. 由SEM和TEM结果可知,NiCo2O4为多晶材料. 由NiCo2O4的能谱mapping测试结果可知(图3D),NiCo2O4中含有Ni、Co和O元素,并且Ni、Co、O的原子百分含量分别为13.6%、28.6%、57.8%,即:1 : 2.1 : 4.25,与XPS结果吻合度较高.
-
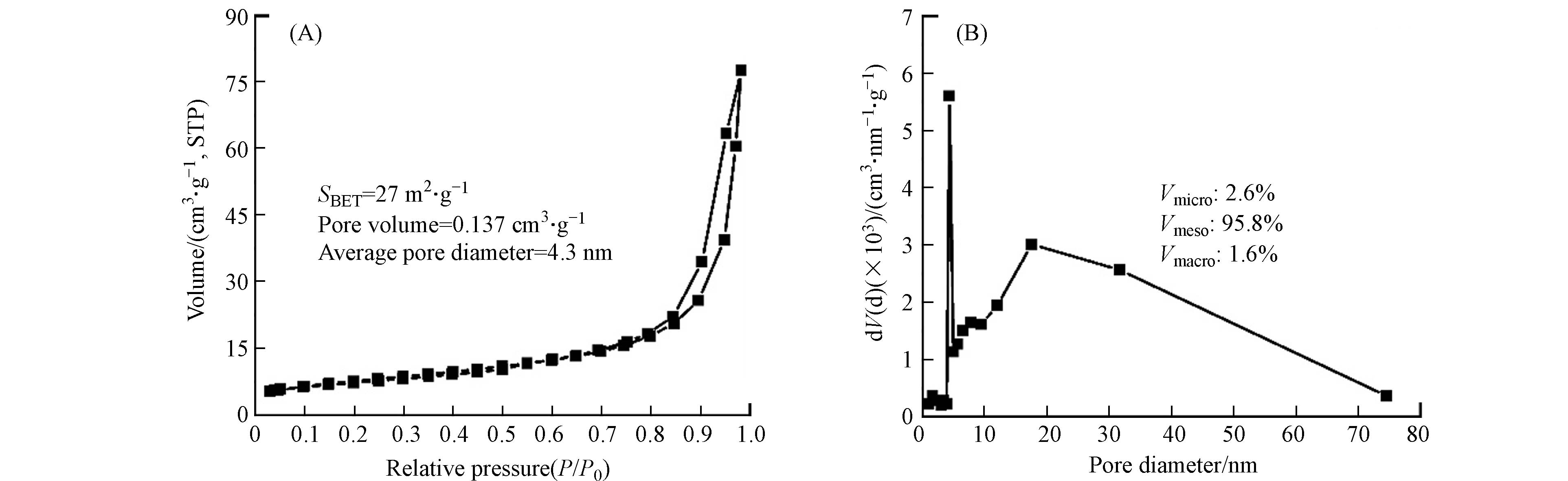
图4是NiCo2O4的N2吸附-脱附曲线图. 由图4A可知,随着相对压力变化,N2吸附量先增大后减少,并且起点与终点重合,即吸附等温线闭合. 等温线形状为第Ⅲ型吸附等温线. 相对压力(P/P0)处于0.8 — 1.0时,产生回滞环,这是由于NiCo2O4表面产生毛细管凝聚效应所致. 由NiCo2O4的孔径分布测试结果可知(图4B),NiCo2O4中微孔、介孔和大孔比例分别为2.6%、95.8%、1.6%,平均孔径为4.3 nm,孔体积为0.137 cm3·g−1. 因此,NiCo2O4以介孔为主.
-
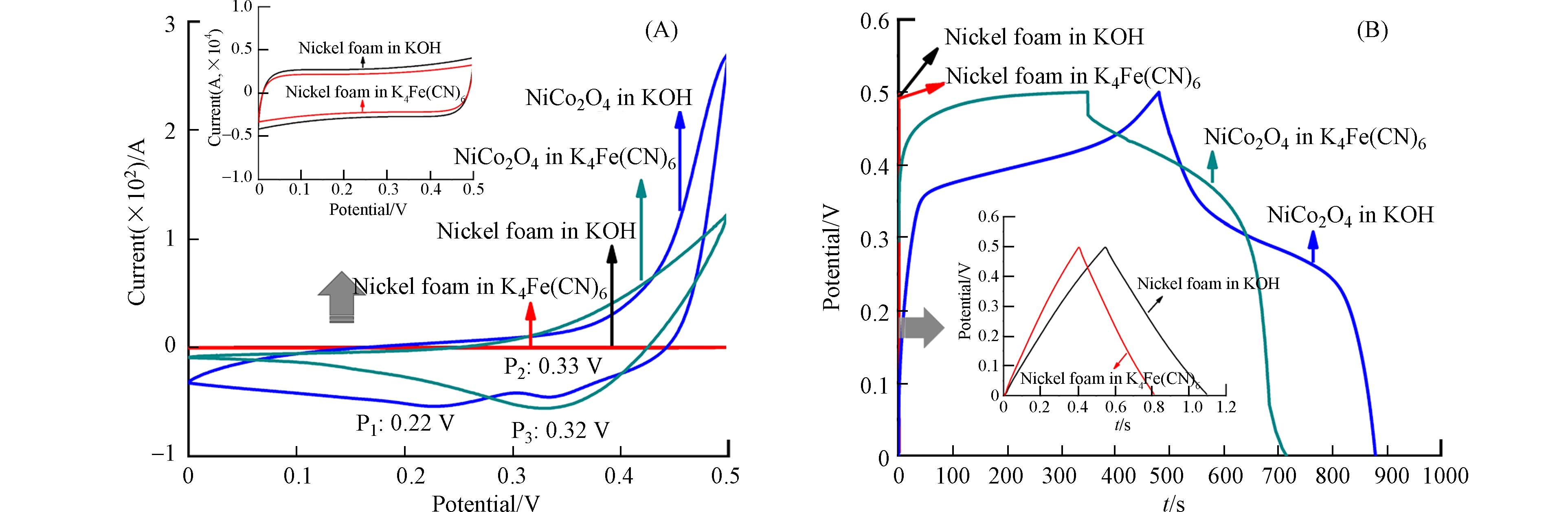
图5是NiCo2O4在KOH和K4Fe(CN)6电解液中的CV测试结果. 根据文献可知[10-11],理想电容器的CV曲线形状接近矩形. 电容器中产生赝电容时,曲线形状偏离矩形. 赝电容行为越明显,偏离程度越大. 由图5A可知,NiCo2O4在KOH溶液中的CV曲线偏离矩形较大. 与文献报道一致[13],电压为0.4 — 0.5 V时,开始产生氧化峰. 由于电压上限较低,氧化峰未显示完全. 电压为0.22、0.33 V时,产生两个还原峰. 由XRD和XPS结果可知,所制备的电极材料为立方相NiCo2O4,并且Ni2+、Ni3+、Co2+和Co3+同时存在于材料之中. 充电过程中,OH−进入到多孔材料NiCo2O4的体相之中并与晶格中的Ni2+、Co2+发生氧化反应(方程式⑤、⑥),产生赝电容,因此在CV曲线上形成氧化还原峰. 放电过程中,NiOOH和CoO2还原为NiCo2O4,并释放OH−. 增大扫描速率,P1和P2处的还原峰电位逐渐减小,但变化幅度较小,说明NiOOH和CoO2较易还原为NiCo2O4. 与以上结果相似,NiCo2O4在K4Fe(CN)6溶液中的CV曲线偏离矩形较大,并且出现明显的还原峰(0.32 V),说明充放电过程中产生氧化还原反应,反应式如方程式⑦所示[25]. 扫描速度为5、10、20、30、50 mV·s−1时,还原峰电位分别为0.29、0.28、0.27、0.26、0.25 V,即还原峰电位逐渐降低,并且变化较大,因此充放电可逆性和倍率充放电性能较差. 由图5C和图5D可知,随着扫描速度增大,NiCo2O4在KOH和K4Fe(CN)6溶液中的伏安放电比容量和平均能量密度均逐渐降低. 根据文献报道[10-11,13],扫描速度增大,电流随之增大,导致三电极体系的极化增大,比电容和能量密度随之降低. 与K4Fe(CN)6相比,NiCo2O4在KOH溶液中具有更好的倍率性能. 扫描速度由5 mV·s−1增大至50 mV·s−1时,KOH和K4Fe(CN)6溶液中的三电极的伏安放电比容量保持率分别为23.7%、17.0%. 增大扫描速度,NiCo2O4在K4Fe(CN)6中的还原电位降低幅度较大,在KOH中还原电位变化较小,即:与
$ {\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{3-}/{\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{4-} $ 的转变相比较,Ni3+/Ni2+和Co3+/Co2+转变更容易实现,因此NiCo2O4在KOH溶液中的倍率性能更好. -
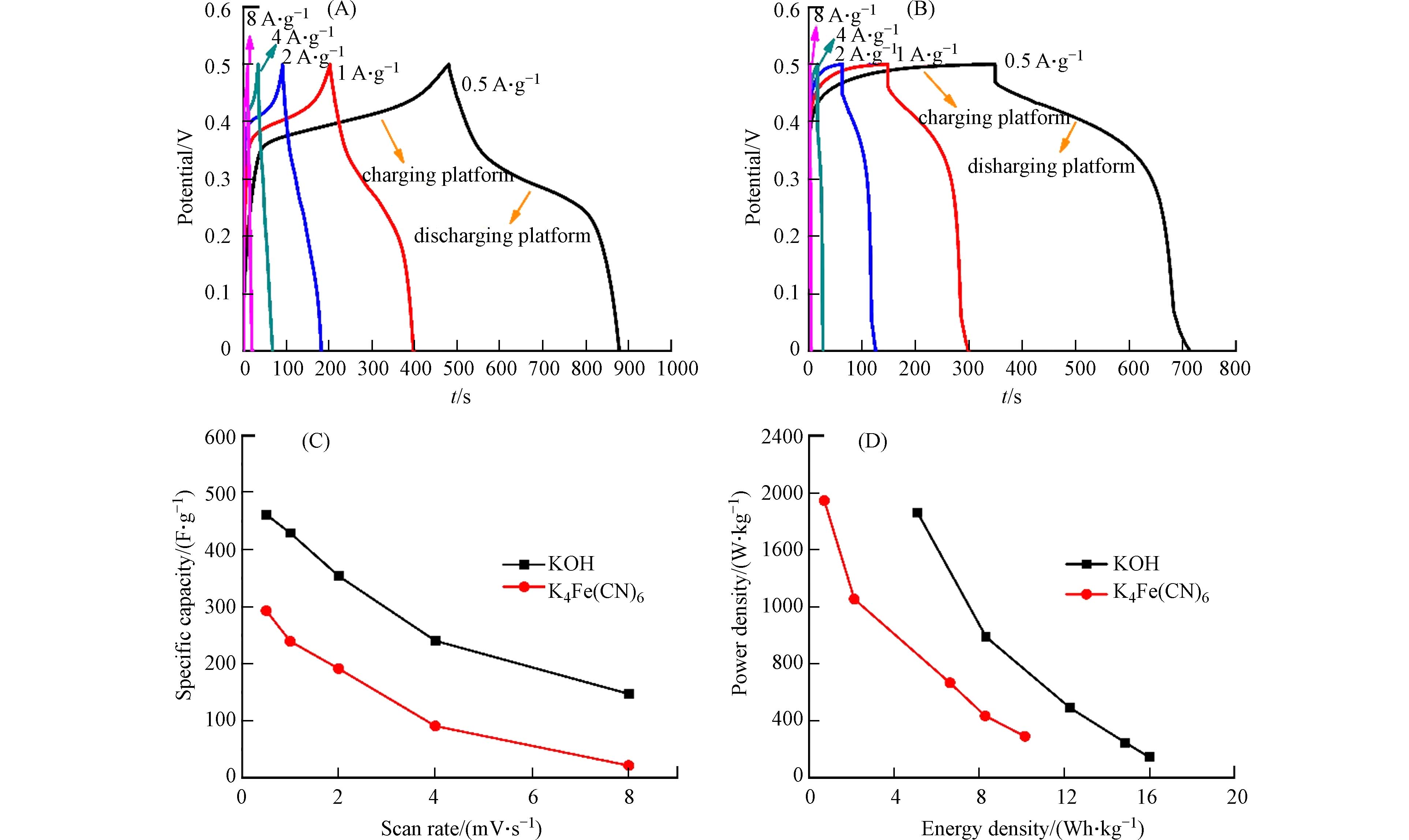
图6 NiCo2O4在KOH和K4Fe(CN)6溶液中的GCD测试结果. 由图可知,NiCo2O4在KOH溶液中的充放电曲线上出现充电平台和放电平台,充电平台电压为0.35 — 0.5 V,放电平台电压为0.2 — 0.35 V(图6A). 此结果与CV测试结果一致,是由于Ni2+/Ni3+和Co2+/Co3+的氧化还原转变所致. 与此相似,由于存在
$ {\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{4-}/{\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{3-} $ 的转变,NiCo2O4在K4Fe(CN)6溶液中的充放电曲线上也出现充电平台(0.4 — 0.5 V)和放电平台(0.3 — 0.45 V)(图6B). 随着电流密度增大,库伦效率($ {C}_{放}\times 100\mathrm{\%}/{C}_{充} $ )逐渐降低. 电流密度为0.5、1、2、4、8 A·g−1时,NiCo2O4在KOH溶液中的库伦效率分别为90.4%、85.3%、77.5%、65.6%、56.1%,在K4Fe(CN)6溶液中的库伦效率分别为87.7%、81.6%、70.4%、51.5%、49.6%. 结合CV和GCD结果可知,电流密度增大时,还原峰电位逐渐降低,Ni3+、Co3+、$ {\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{3-} $ 还原为Ni2+、Co2+和$ {\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{4-} $ 的难度增大,导致库伦效率降低. 然而,NiCo2O4在KOH溶液中的还原峰电位变化较小,因此库伦效率更高. 同时,随着电流密度增大,放电比容量和能量密度逐渐减低. 电流密度为8 A·g−1时,KOH和K4Fe(CN)6溶液中的三电极的放电比容量为147.2、21.6 F·g−1,能量密度分别为5.1 Wh·kg−1、0.7 Wh·kg−1. 根据文献报道[10-11,13],电流密度增大时,电流逐渐增大,导致三电极体系中极化增大,放电比容量和能量密度逐渐降低. 电流密度由0.5 A·g−1增大到8 A·g−1,NiCo2O4在KOH溶液中的比容量保持率是其在K4Fe(CN)6溶液中的4.3倍. 结合CV曲线可知,增大电流密度时,Ni3+/Ni2+和Co3+/Co2+的转变更容易实现. 此外,OH−的半径远小于$ {\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{4-} $ 的半径,更容易进入NiCo2O4的体相,获得更好的倍率放电性能.为了验证实验结果的准确性,以泡沫镍为工作电极、Pt片为对电极、HgO/Hg电极为参比电极组装三电极,并将其置于相同的条件中进行电化学测试. 如图7A所示,泡沫镍在KOH和K4Fe(CN)6电解液中的CV曲线形状均接近矩形,即:不产生赝电容. 扫描速度为5 mV·s−1时,泡沫镍在KOH和K4Fe(CN)6中的伏安放电比容量分别为1 F·g−1、0.7 F·g−1,远小于NiCo2O4的比容量(644.6 F·g−1、361.7 F·g−1),可以忽略不计. 由图7B知,泡沫镍在KOH和K4Fe(CN)6电解液中的充放电曲线为线性直线,放电比容量为0.8 F·g−1、0.5 F·g−1,远低于NiCo2O4的比容量(461.2 F·g−1、292.8 F·g−1),因此也可以忽略不计.
-
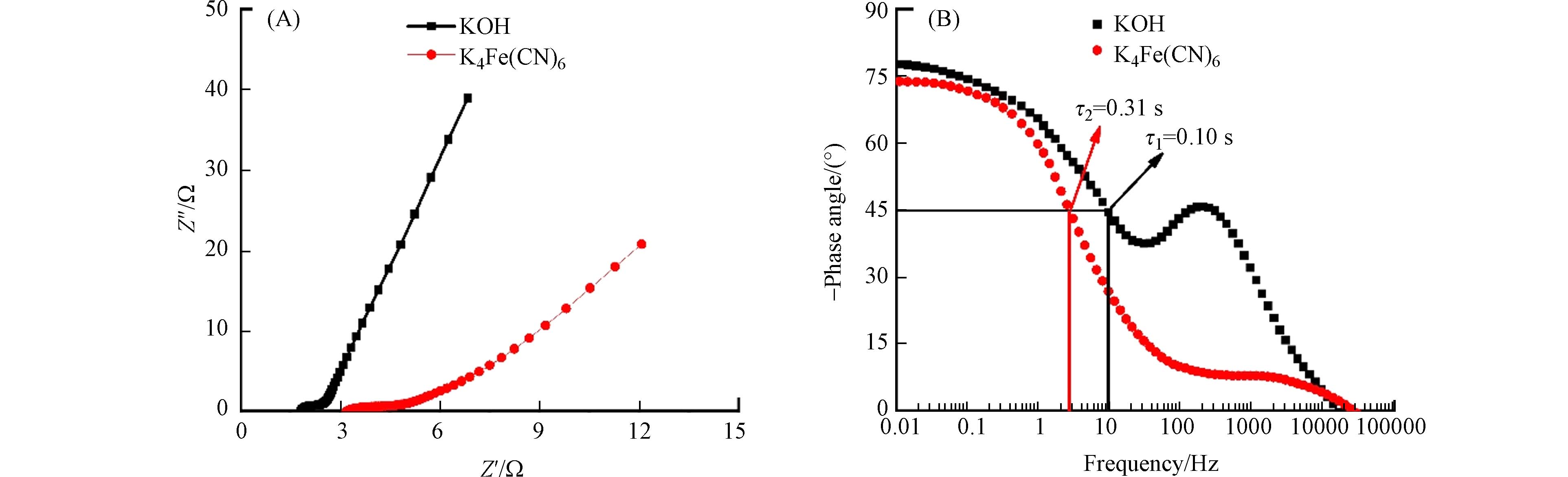
图8为NiCo2O4在KOH和K4Fe(CN)6溶液中的EIS测试结果. 由图8A可知:(1)EIS曲线均由高频区、中频区半圆和低频区直线组成. 高频区表示欧姆阻抗,由正负离子和电子在立方相NiCo2O4、KOH或K4Fe(CN)6电解液、泡沫镍及外部导线上传输过程所产生的电阻组成[10]. 电解液为KOH和K4Fe(CN)6时,欧姆阻抗分别为1.81 Ω、3.22 Ω. (2)中频区半圆表示电化学转移阻抗,由Ni2+/Ni3+、Co2+/Co3+和
$ {\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{4-}/{\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{3-} $ 法拉第反应引起[11,13,25]. 在KOH和K4Fe(CN)6电解液中,电化学转移阻抗分别为0.63 Ω、1.43 Ω. NiCo2O4在KOH电解液中的电化学转移阻抗更小,其充放电可逆性可能更好. (3)低频区直线为Warburg阻抗. 直线斜率偏离垂线程度越大,说明正负离子在NiCo2O4体相中的迁移阻抗越高. 与K4Fe(CN)6相比较,NiCo2O4在KOH电解液中的低频区直线斜率更高(3.4 Vs 8.8),离子迁移速度更快,更有利于实现Ni2+/Ni3+、Co2+/Co3+转变,完成充放电过程.根据文献报道[10,11,26],相位角φ为−45°时,阻抗与容抗相等. 由Bode图(图8B)可知:(1)相位角φ为−45°时,NiCo2O4在KOH和K4Fe(CN)6溶液中的频率f1和f2为10 Hz、3.162 Hz,弛豫时间常数τ1(τ1 = 1/ f1)、τ2(τ2 = 1/ f2)分别为0.10 s、0.31 s. NiCo2O4在KOH溶液中的弛豫时间常数较小,说明倍率充放电性能可能更好. 电流密度由0.5 A·g−1增大至8 A·g−1时,NiCo2O4在KOH溶液中的比电容保持率为31.9%,是其在K4Fe(CN)6中的4.3倍. (2)K4Fe(CN)6电解液中,低频区相位角约为−74.3°,与−90°差值为15.7°,说明该三电极体系中存在一定的界面接触. 电解液为KOH时,低频区相位角更低(−77.6°),与-90°差值更小(12.4°),说明界面接触阻抗更低,更有利于KOH电解液中正负离子进入NiCo2O4体相之中并完成Ni2+/Ni3+、Co2+/Co3+氧化还原转变,获得更好的倍率充放电性能.
-
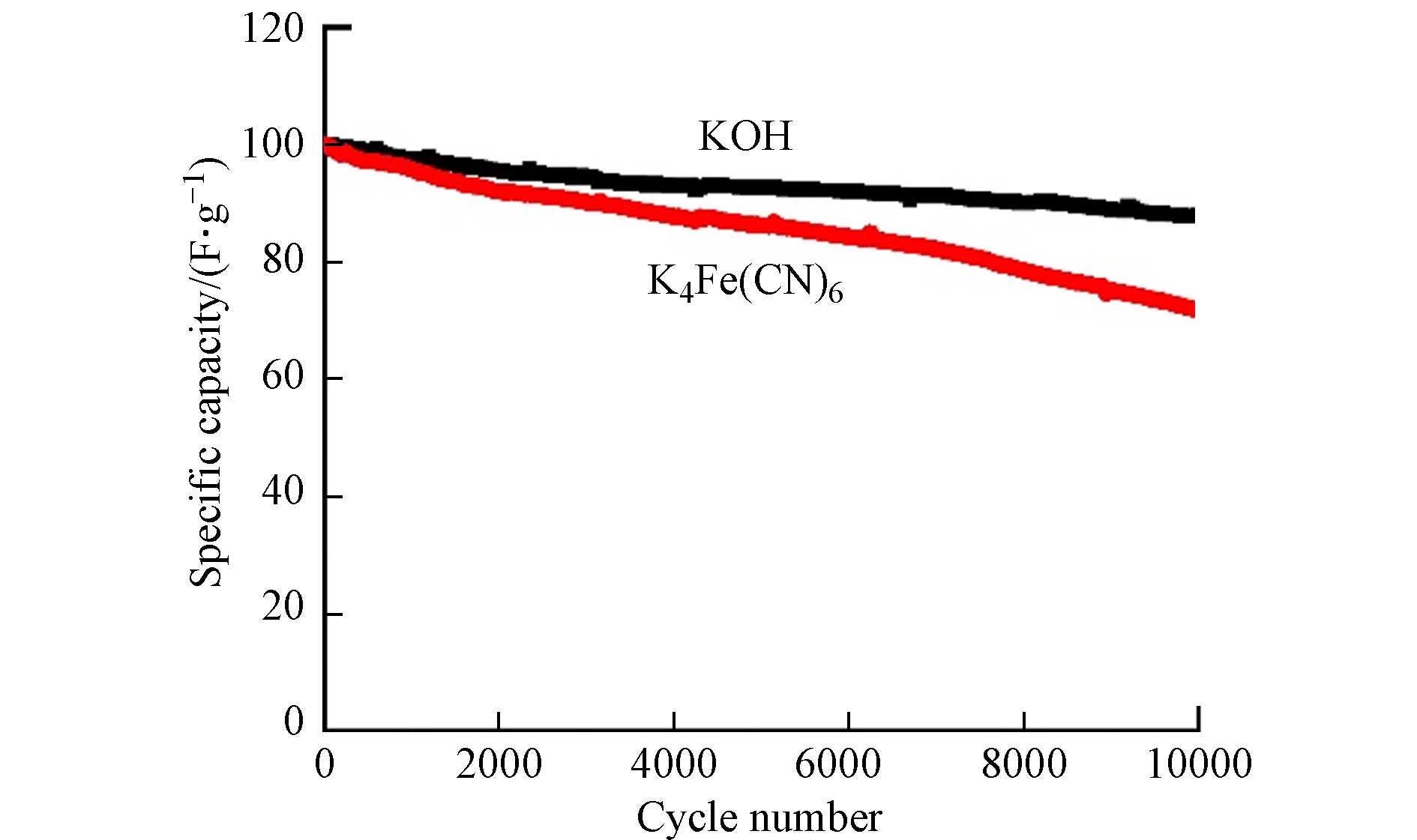
图9是NiCo2O4的循环性能测试结果. 由图9可知,电流密度为0.5 A·g−1,循环
10000 次后,NiCo2O4在KOH和K4Fe(CN)6溶液中的放电比容量保持率分别为87.8%、71.7%. 由CV、GCD和EIS结果可知:(1)与K4Fe(CN)6相比较,NiCo2O4在KOH电解液中的Ni2+/Ni3+、Co2+/Co3+转变更容易实现;(2)NiCo2O4在KOH溶液中充放电时的库伦效率更高(90.4% Vs 87.7%);(3)NiCo2O4在KOH溶液中的阻抗更低. 因此,NiCo2O4在KOH电解液中的充放电可逆性更好,容量保持率更高. -
本文制备了一种立方相颗粒状多孔NiCo2O4电极材料,并对其在KOH和K4Fe(CN)6电解液中的充放电性能进行了测试与分析. NiCo2O4中的Ni和Co分别以Ni2+、Ni3+、Co2+、Co3+形式存在,并且通过Ni2+/Ni3+、Co2+/Co3+的协同转变过程产生赝电容. NiCo2O4在K4Fe(CN)6溶液中通过
$ {\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{4-}/ {\mathrm{F}\mathrm{e}\left(\mathrm{C}\mathrm{N}\right)}_{6}^{3-} $ 的氧化还原反应产生赝电容. 电流密度为0.5 A·g−1、8 A·g−1时,NiCo2O4在KOH电解液中的放电比容量分别是在K4Fe(CN)6溶液中的1.6倍和7倍.
颗粒状NiCo2O4的制备及其在不同电解液中的电化学性能
The preparation of granular NiCo2O4 and the electrochemical performance in different electrolytes
-
摘要: 本文以NiCl2为镍源、CoCl2为钴源,通过静态水热处理合成NiCo2O4,并对其在6 mol·L−1 KOH、0.5 mol·L−1 K4Fe(CN)6溶液中的赝电容行为进行探究. 采用X-射线衍射、X-射线光电子能谱、扫描电子显微镜、透射电子显微镜、能量色散谱和N2吸附-脱附技术对NiCo2O4的物相、组成、形貌和孔结构进行分析. 结果表明,NiCo2O4为立方相多晶材料,并且Ni2+/Ni3+、Co2+/Co3+同时存在于晶格之中. NiCo2O4为颗粒状多孔材料,平均孔径为4.3 nm,孔体积为0.137 cm3·g−1. 与K4Fe(CN)6相比较,NiCo2O4在KOH溶液中具有更好的倍率充放电性能. 扫描速度由5 mV·s−1增大至50 mV·s−1时,NiCo2O4在KOH和K4Fe(CN)6溶液中的伏安放电比容量保持率分别为23.7%、17.0%. 电流密度由0.5 A·g−1增大至8 A·g−1时,NiCo2O4在KOH的放电比容量保持率为31.9%,是其在K4Fe(CN)6溶液中的4.3倍.Abstract: In the present study, NiCo2O4 was prepared by a static hydrothermal treatment using NiCl2 as Ni source and CoCl2 as Co source. Then, the pseudocapacitance behavior of NiCo2O4 was investigated in 6 mol·L−1 of KOH and the 0.5 mol·L−1 of K4Fe(CN)6 solutions. The phase, composition, morphology and pore structure of NiCo2O4 were analyzed using X-ray diffraction, X-ray photoelectron spectroscopy, scanning electron microscope, transmission electron microscope, energy dispersion spectrum and N2 adsorption-desorption techniques. The results show that NiCo2O4 is a cubic phase polycrystalline material and both of Ni2+/Ni3+ and Co2+/Co3+ exist in the crystal lattice. The NiCo2O4 is a granular porous material with an average pore size of 4.3 nm and a pore volume of 0.137 cm3·g−1. Compared with K4Fe(CN)6, NiCo2O4 has a good rate charge/discharge performance in KOH solution. With the rise of scanning rate from 5 mV·s−1 to 50 mV·s−1, the specific volt-ampere discharge capacity retentions of NiCo2O4 are 23.7% and 17.0% in KOH and K4Fe(CN)6 solutions, respectively. When the current density is improved from 0.5 A·g−1 to 8 A·g−1, the specific discharge capacity retention of NiCo2O4 in KOH is 32%, which is 4.3 times higher than that in K4Fe(CN)6 solution.
-
Key words:
- NiCo2O4 /
- KOH /
- K4Fe(CN)6 /
- pseudocapacitance
-

-
-
[1] 展长振, 曾晓婕, 吕瑞涛, 等. 石墨质多孔炭的制备及其双离子电容储能机理[J]. 新型炭材料(中英文), 2023, 38(3): 576-582. doi: 10.1016/S1872-5805(23)60727-9 ZHAN C Z, ZENG X J, LV R T, et al. Preparation of porous graphitic carbon and its dual-ion capacitance energy storage mechanism[J]. New Carbon Materials, 2023, 38(3): 576-582 (in Chinese). doi: 10.1016/S1872-5805(23)60727-9
[2] 郝生阳, 张雨婷, 王晓清. Mo掺杂NiMnSe2的制备及其超级电容器性能[J]. 无机化学学报(中英文), 2023, 39(6): 1091-1102. HAO S Y, ZHANG Y T, WANG X Q. Preparation and supercapacitor performance of Mo-doped NiMnSe2[J]. Chinese Journal of Inorganic Chemistry, 2023, 39(6): 1091-1102 (in Chinese).
[3] LIU C F, LIU Y C, YI T, et al. Carbon materials for high-voltage supercapacitors[J]. Carbon, 2019, 145: 529-548. doi: 10.1016/j.carbon.2018.12.009 [4] CHEN X L, PAUL R, DAI L M. Carbon-based supercapacitors for efficient energy storage[J]. National Science Review, 2017, 4(3): 453-489. doi: 10.1093/nsr/nwx009 [5] JI H X, ZHAO X, QIAO Z H, et al. Capacitance of carbon-based electrical double-layer capacitors[J]. Nature Communications, 2014, 5: 3317. doi: 10.1038/ncomms4317 [6] 魏良, 王健恺, 刘凯歌, 等. 纳米纤维素/还原氧化石墨烯复合材料用于高性能超级电容器[J]. 无机化学学报(中英文), 2023, 39(3): 456-464. WEI L, WANG J K, LIU K G, et al. Nanocellulose/reduced graphene oxide composites for high performance supercapacitors[J]. Chinese Journal of Inorganic Chemistry, 2023, 39(3): 456-464 (in Chinese).
[7] KUTTAN S S, GIRIJA N, DEVAKI S J, et al. Modulating electrochemical performance of interfacially polymerized, MoS2 decorated polyaniline composites for electrochemical capacitor applications[J]. ACS Applied Energy Materials, 2022, 5(7): 8510-8525. doi: 10.1021/acsaem.2c01040 [8] ANANDHU T P, MOHAN R, CHERUSSERI J, et al. High areal capacitance and enhanced cycling stability of binder-free, pristine polyaniline supercapacitor using hydroquinone as a redox additive[J]. Electrochimica Acta, 2022, 425: 140740. doi: 10.1016/j.electacta.2022.140740 [9] HALDAR S, RASE D, SHEKHAR P, et al. Incorporating conducting polypyrrole into a polyimide COF for carbon-free ultra-high energy supercapacitor[J]. Advanced Energy Materials, 2022, 12(34): 2200754. doi: 10.1002/aenm.202200754 [10] 杨泛明, 贺国文. 颗粒状NiO的制备及其电化学性能和CO2吸附性能[J]. 化工进展(中英文), 2023, 42(2): 907-916. YANG F M, HE G W. Preparation of granular NiO for the electrochemical performance and CO2 adsorption performance[J]. Chemical Industry and Engineering Progress, 2023, 42(2): 907-916 (in Chinese).
[11] YANG F M, ZHOU X Y, LI X D, et al. Hollow urchin-shaped NCM811 ternary-structure for high rate charge/discharge capability and efficient CO2 adsorption[J]. Journal of Environmental Chemical Engineering, 2023, 11(2): 109445. doi: 10.1016/j.jece.2023.109445 [12] YANG S H, SONG X F, ZHANG P, et al. Self-assembled α- Fe2O3 mesocrystals/graphene nanohybrid for enhanced electrochemical capacitors[J]. Small, 2014, 10(11): 2270-2279. doi: 10.1002/smll.201303922 [13] LIU X. Y, ZHANG Y Q, XIA X H, et al. Self-assembled porous NiCo2O4 hetero-structure array for electrochemical capacitor[J]. Journal of Power Sources, 2013, 239: 157-163. doi: 10.1016/j.jpowsour.2013.03.106 [14] ZHANG M, CHEN Y, YANG D Y, et al. High performance MnO2 supercapacitor material prepared by modified electrodeposition method with different electrodeposition voltages[J]. Journal of Energy Storage, 2020, 29: 101363. doi: 10.1016/j.est.2020.101363 [15] NUMAN A, RAMESH KUMAR P, KHALID M, et al. Facile sonochemical synthesis of 2D porous Co3O4 nanoflake for supercapattery[J]. Journal of Alloys and Compounds, 2020, 819: 153019. doi: 10.1016/j.jallcom.2019.153019 [16] ADHIKARI H, GHIMIRE M, RANAWEERA C K, et al. Synthesis and electrochemical performance of hydrothermally synthesized Co3O4 nanostructured particles in presence of urea[J]. Journal of Alloys and Compounds 2017, 708: 628-638. [17] XU J, LI L, GAO P, et al. Facile preparation of NiCo2O4 nanobelt/graphene composite for electrochemical capacitor application[J]. Electrochimica Acta, 2015, 166: 206-214. doi: 10.1016/j.electacta.2015.03.093 [18] LIU P B, YANG M Y, ZHOU S H, et al. Hierarchical shell-core structures of concave spherical NiO nanospines@carbon for high performance supercapacitor electrodes[J]. Electrochimica Acta, 2019, 294: 383-390. doi: 10.1016/j.electacta.2018.10.112 [19] ASKARI M B, SALARIZADEH P, BEHESHTI-MARNANI A, et al. NiO-Co3O4 -rGO as an efficient electrode material for supercapacitors and direct alcoholic fuel cells[J]. Advanced Materials Interfaces, 2021, 8(15): 2100149. doi: 10.1002/admi.202100149 [20] MOLLAMAHALE Y B, LIU Z, ZHEN Y D, et al. Simple fabrication of porous NiO nanoflowers: Growth mechanism, shape evolution and their application into Li-ion batteries[J]. International Journal of Hydrogen Energy, 2017, 42: 7202-7211 doi: 10.1016/j.ijhydene.2016.05.193 [21] SREEKANTH T V M, SINDHU R, KUMAR E P, et al. Controllable synthesis of urea-assisted Co3O4 nanostructures as an effective catalyst for urea electrooxidation[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2023, 657: 130576. doi: 10.1016/j.colsurfa.2022.130576 [22] MAI L Q, MINHAS-KHAN A, TIAN X C, et al. Synergistic interaction between redox-active electrolyte and binder-free functionalized carbon for ultrahigh supercapacitor performance[J]. Nature Communications, 2013, 4: 2923. doi: 10.1038/ncomms3923 [23] SUN K J, ZHANG Z G, PENG H, et al. Hybrid symmetric supercapacitor assembled by renewable corn silks based porous carbon and redox-active electrolytes[J]. Materials Chemistry and Physics, 2018, 218: 229-238. doi: 10.1016/j.matchemphys.2018.07.052 [24] YANG P H, MAI W J. Flexible solid-state electrochemical supercapacitors[J]. Nano Energy, 2014, 8: 274-290. doi: 10.1016/j.nanoen.2014.05.022 [25] TIAN Y, YAN J W, XUE R, et al. Capacitive properties of activated carbon in K4Fe(CN)6[J]. Journal of the Electrochemical Society, 2011, 158(7): A818. doi: 10.1149/1.3591061 [26] LIU Z, XIAO K K, GUO H, et al. Nitrogen-doped worm-like graphitized hierarchical porous carbon designed for enhancing area-normalized capacitance of electrical double layer supercapacitors[J]. Carbon, 2017, 117: 163-173. doi: 10.1016/j.carbon.2017.02.087 -




 下载:
下载: