-
垃圾填埋场由于受雨水径流和地表水的冲刷、浸渍,污染物不断渗入渗滤液,导致填埋场渗滤液的污染物往往成分较复杂且浓度较高[1]。渗滤液的成分和性质也会随着填埋场的年龄和位置表现出差异性[2]。通常,垃圾渗滤液表现为棕黑色或深棕色液体,伴随着恶臭气味,其中包含着高浓度的新型污染物,例如磺胺类抗生素、喹诺酮类抗生素、四环素类抗生素以及抗癫痫药物等。在华南的3个垃圾填埋场原始垃圾渗滤液中共检测到了37种新型污染物,其浓度在272~1 780 μg·L−1[3]。垃圾渗滤液中污染物浓度也会随着季节的变动而波动,已检测到渗滤液中药物和个人护理品(pharmaceutical and personal care products,PPCPs)的总浓度在月份间差异较大,为39.0~1 200 μg·L−1,而在8—9月出现峰值浓度,这可能是由于夏季降雨量上升,过量的雨水促进了废弃物中PPCPs的渗出[4]。渗滤液中含有的多种药物类污染物(pharmaceutically active compounds, PhACs)通过地下水和地表水流入周边环境,会严重威胁生态环境和人体健康,因此,需要在排放前高效去除。传统渗滤液处理方法通常包括生物处理、物理处理和化学处理[5],但这些方法在去除PhACs方面研究较少,探索一种高效同步去除渗滤液中多种PhACs的方法,对于控制渗滤液中PhACs的环境风险具有重要意义。
臭氧(ozone, O3)氧化工艺得益于臭氧的强氧化能力,可以降解大分子有机物,在处理渗滤液方面被广泛应用[6]。碳基材料和金属基负载催化剂可强化臭氧氧化[7],如MnCeO/γ-Al2O3催化剂被证明能够活化臭氧提升垃圾渗滤液的处理效率[8]。然而,传统的碳基材料和金属基催化剂往往成本高,且可重复利用性低,因此,需要选择合适的材料来优化臭氧氧化工艺。另一方面,随着污水处理厂剩余污泥产量的不断提升,剩余污泥处理成为制约污水处理厂进一步提质增效的瓶颈问题。目前常见的污泥处理方法主要有填埋和焚烧,但这些方法不仅会对环境造成二次污染,还会增加能源消耗,因此,如何合理且环保的处理污泥成为当前研究的热点。剩余污泥中富含生物质和金属资源(Fe、Al、Cu、Mn等)[9],利用剩余污泥制备生物炭催化剂,不仅能解决固体废物的处置问题,而且还可以进一步回用于污水处理。已有研究表明,热解生物炭在催化、储能和环境保护方面具有巨大潜能[9],其优越的理化性能,如较大的表面积、优良的孔隙结构、丰富的表面含氧官能团等,使生物炭具备良好的吸附和催化性能。有研究[10]表明,污泥生物炭表面的羧酸和内酯官能团能够有效促进臭氧分解产生·OH;负载Mn的污泥基生物炭催化臭氧氧化,实现了对垃圾渗滤液的高效稳定处理[11]。然而,利用污泥基生物炭催化臭氧来处理实际渗滤液中的PhACs罕有报道,由于渗滤液背景基质复杂,其催化氧化PhACs的机理也需进一步探讨。
本研究旨在利用高温热解制备污泥生物炭(sludge biochar, SDBC),用于催化臭氧氧化降解渗滤液中的多种PhACs,表征分析了高温热解下SDBC的形貌和结构特征,评估了热解温度、SDBC投加量、O3浓度及pH条件对污染物降解的影响;同时利用淬灭实验和EPR实验探讨体系中活性物质的存在及其作用机制。
-
渗滤液水样取自上海市老港垃圾填埋场一级处理后出水,样品均不含本文所选的四种目标污染物,在使用前于冰箱4 °C保存。臭氧发生器型号为JY-SY20。磺胺甲噁唑(Sulfamethoxazole, SMX)、四环素(Tetracycline, TTC)、环丙沙星(Ciprofloxacin, CIP)、卡马西平(Carbamazepine, CBZ)、叔丁醇(tert-Butanol, TBA)、L-组氨酸(L-Histidine, L-his)和三氯甲烷(Trichloromethane, CHCl3)购于阿拉丁试剂有限公司。所有试剂均为分析纯,使用时无需进一步提纯。实验用水均为超纯水。
在该垃圾渗滤液中,检测到NaCl的浓度为185.66 mmol·L−1,NaNO3的浓度为0.81 mmol·L−1,NH4+-N为174 mg·L−1,NO3−-N为8.31 mg·L−1,NO2−-N为0.02 mg·L−1,TN为188.29 mg·L−1,TP为1.37 mg·L−1,COD为1 879.3 mg·L−1,pH为7.8。
-
本实验室制备生物炭所需污泥取自上海市松江区的污水处理厂二沉池。污泥经离心处理后,在105 °C烘箱中烘干24 h,烘干后的污泥经研磨后放入管式炉的石英管中,用高纯度氮气以100 mL·min−1的流速通入石英管中,保持10 min,确保石英管内为惰性气体环境。在热解过程中,氮气流速为60 mL·min−1,热解时间为2 h,升温速率为10 °C·min−1,热解温度为800 °C。将制备好的生物炭用去离子水洗涤3~4遍,之后在真空干燥箱60 °C烘干并用研钵磨碎,过100目筛,记为SDBC。此外,污泥分别在400 °C、600 °C下进行热解,根据热解温度不同分别记为SDBC 400、SDBC 600。
-
实验在常温的100 mL玻璃杯内进行,首先加入26 mL的渗滤液,之后依次加入SMX、CBZ、TTC、CIP,确保体系为50 mL溶液,体系中每种污染物浓度均为60 μmol·L−1。同时加入1.6 g·L−1生物炭和通入0.3 mg·L−1臭氧引发反应。若要调节pH,则用1 mmol·L−1 H2SO4和NaOH进行调节。在预定的时间间隔内收集1 mL样品过膜后(孔径0.22 μmol·L−1)进入液相小瓶中,在用高效液相色谱仪分析前保存在4 °C。
-
污染物的测定采用高效液相色谱仪(High Performance Liquid Chromatography, HPLC),电子顺磁共振(electron paramagnetic resonance, EPR)识别体系中活性反应物质,5,5-二甲基-1-吡咯啉-N-氧化物(5,5-Dimethyl-1-pyrroline N-oxide, DMPO)、四甲基哌啶酮(Triacetonamine, TEMP)作为捕获剂。采用扫描电子显微镜、能量分散色谱(scanning electron microscope-energy dispersive spectroscopy, SEM-EDS)对SDBC表面进行成分元素分析并观察SDBC的微观形貌。采用X射线衍射仪(X-ray powder diffractometer, XRD)测量SDBC的晶体结构。采用X射线光电子能谱(X-ray photoelectron spectroscopy, XPS)分析SDBC反应前后的化学状态和元素组成。采用傅里叶变换红外光谱(fourier transform infrared, FTIR)分析热解后SDBC的表面官能团。
-
首先使用SEM对800 °C下制备的SDBC进行形貌表征,如图1所示,SDBC表面呈现出疏松且具多孔的结构,分布着大量微米级颗粒,表明其具有丰富的吸附位点。文献报道指出,污泥生物炭在高温热解过程中容易发生碳化和石墨化,并伴随着气体和挥发性物质的释放,形成裂缝和多孔结构,因此高温热解后的污泥生物炭具有丰富的活性位点和良好的催化活性[12]。EDS图显示了SDBC表面含有大量的C、O、Fe和Al(图2),而Co、Mn和N含量则较少。已有研究表明Fe作为活泼的过渡金属,能有效活化氧化剂并用于处理难降解有机物[13-14],因此该体系也将探讨Fe在活化O3方面的潜在机制。
SDBC热解后的XRD图谱如图3所示,在2θ为23.86°的衍射峰对应C,38.7°的衍射峰对应FeO,42.4°的衍射峰对应Fe2.5C,而在不同的2θ值下则出现Fe2O3、Fe3O4和Fe的衍射峰,这些多种铁价态物质的形成归因于高温热解过程。有研究[15-17]表明,随着热解的进行,高价态铁会逐渐转化为低价态铁,甚至转化为零价铁(Fe2O3→Fe3O4→FeO→Fe0),而零价铁比含铁氧化物表现出更强的催化活性[18],可有效催化臭氧产生Fe2+和活性物质,因此,这些含铁化合物中铁价态的转变使热解后的SDBC具有较高的活性。
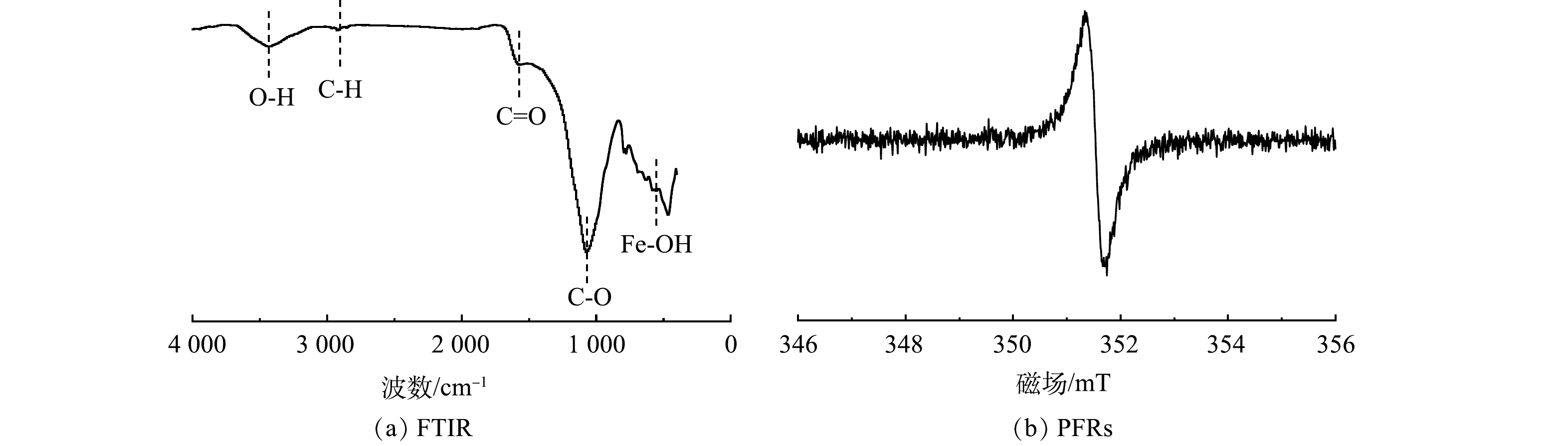
通过FTIR对SDBC表面官能团进行分析,结果如图4(a)所示,3 446 cm−1处的吸收峰归于醇或胺基团的O-H拉伸振动[19],2 922 cm−1的吸收峰归于C-H[13],在1 681 cm−1和1 050 cm−1处的吸收峰归于C-O和C=O[20],此外,在571 cm−1处还观察到了Fe-O峰的存在,推测该吸收峰形成的原因主要是污泥中的铁和氧在高温热解下形成的[21]。热解后的SDBC表面含有含氧基团(如O-H和C=O)已被确定为催化臭氧化的活性位点[22-23],而C-O和C=O基团会促进持久性自由基(persistent free radicals, PFRs)的形成。图4(b)反映了SDBC中PFRs的EPR光谱。说明热解后的生物炭中存在大量的PFRs,该自由基可以作为氧化还原反应的中心,可提供电子给氧化剂,生成强有效的活性物质,实现对污染物的去除[24]。SDBC表面上的含氧官能团可通过静电相互作用和氢键促进吸附亲和力,而π电子作为电子转移介质,促进了污染物和生物炭之间的电子转移[25]。此外,C=O基团也可促进体系中非自由基的生成,因此,该体系也可能有非自由基的参与[26]。
-
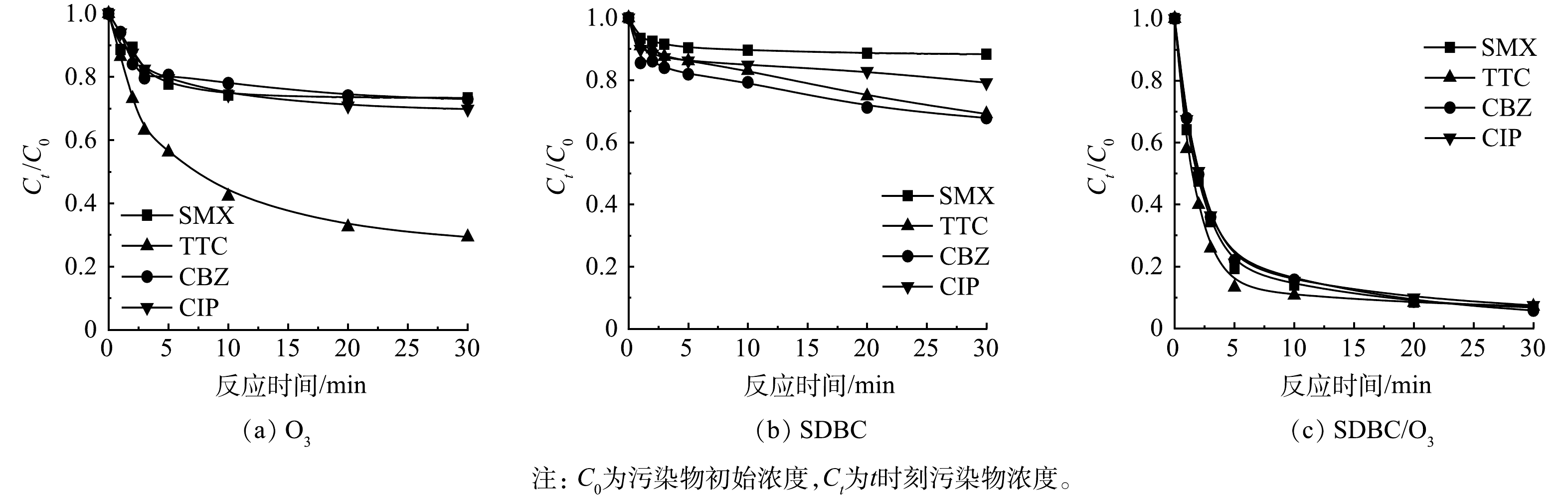
1) 不同体系对多种PhACs的降解效能。图5反映了单独O3、SDBC以及SDBC/O3对渗滤液中PhACs去除效率的影响。单独使用O3对渗滤液中的不同污染物表现出不同的降解速率,SMX、CBZ和CIP在单独使用O3下均降解了约30%(图5(a)),而TTC在30 min内快速降解了70%,TTC的降解速率比SMX、CBZ和CIP都要高,推断可能是在未调pH的条件下(pH=7.8)下,弱碱性环境促进了TTC的矿化以及O3易降解芳香族类有机污染物[27],使得在相同的O3浓度下TTC更容易降解。而单独使用SDBC对污染物仅表现出轻微的吸附作用,其中SMX的去除率最低,为10%,CIP去除率为20%,TTC和CBZ的去除率约为30%(图5(b))。在SDBC/O3体系中,渗滤液中的污染物降解速度显著增加,4种污染物在30 min内均能达到90%的去除率(图5(c)),效果显著优于单独使用O3及SDBC。有研究表明,污泥生物炭催化臭氧可有效促进活性氧物质的产生(·OH、O2•−等),从而有效处理垃圾渗滤液[28]。该体系中O3和SDBC的耦合也表现出较好的去除渗滤液PhACs的效能,说明其产生的活性物质受背景基质影响小,在复杂的渗滤液背景基质中也能达到较好的处理效果。
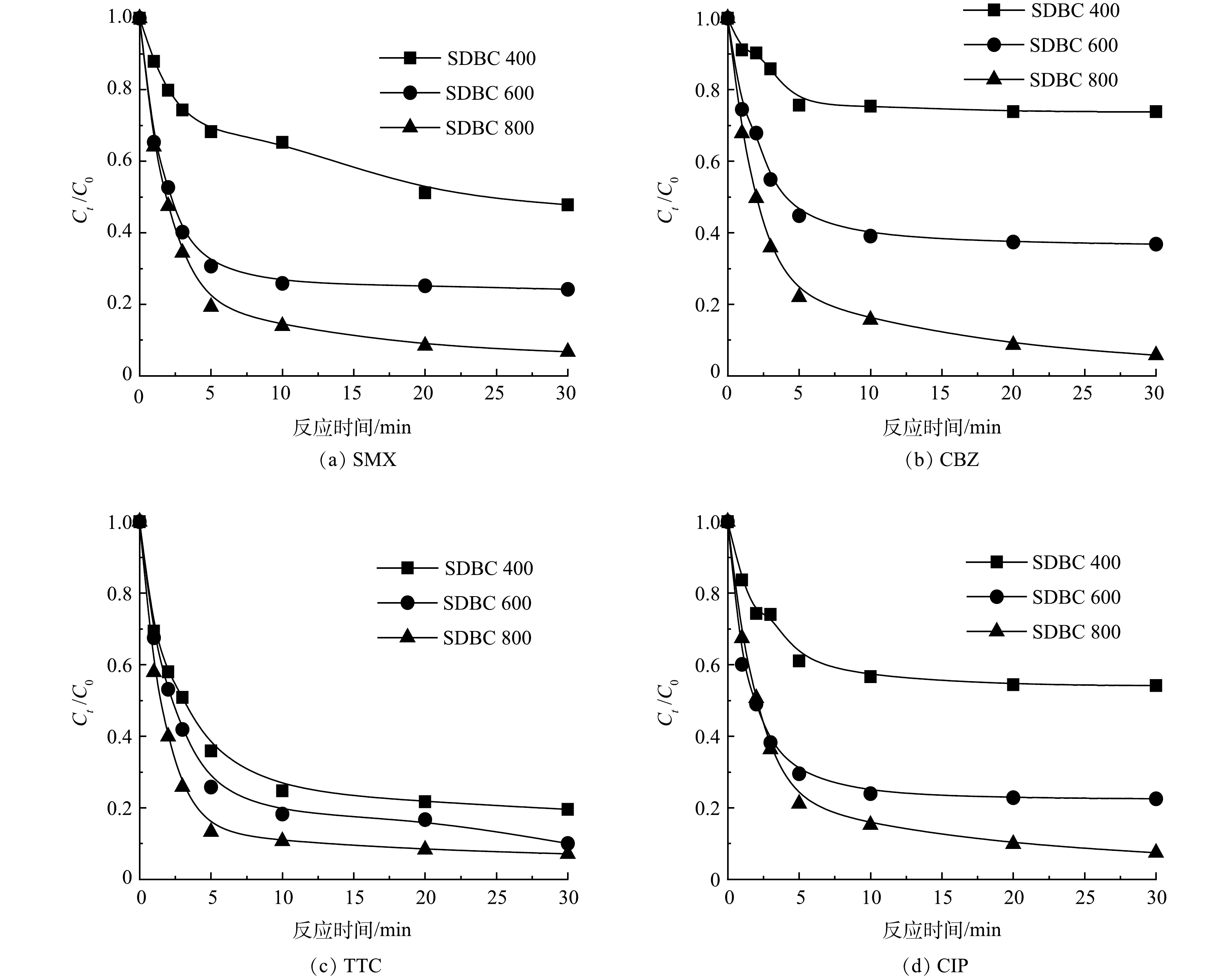
2) 不同热解温度对SDBC/O3去除PhACs的影响。热解温度会显著影响SDBC的形貌及其吸附和催化性能,因此本研究探讨了不同热解温度下SDBC催化O3降解污染物的效能。如图6所示,在400、600和800 °C的热解温度下进行污染物的降解,当热解温度由400 °C升到600 °C再升到800 °C时,渗滤液中4种污染物的去除率均有所提高,SMX的去除率由50%提升到92%,CBZ的去除率由30%提升到93%,TTC的去除率由80%提升到92%,CIP的去除率由50%提升到91%。这表明在较高的热解温度下制备的SDBC更容易活化O3,从而产生更多的活性物质,加速渗滤液中污染物的去除。已有研究表明,随着热解温度的升高,污泥生物炭的亲水性和极性降低,而芳烃含量逐渐增加[29],且热解温度的升高促使大分子有机物分解为小分子有机物,增加了生物炭的比表面积[26],从而确保了更高的碳化和石墨化程度并产生更多的还原金属位点[12]。此外,不同温度热解后SDBC的催化性能不同,800 °C下热解的SDBC会更大程度的芳香化,即sp2杂化结构和共轭π电子之间相互作用可促进溶液中自由基和非自由基的产生,从而快速降解污染物[24,30]。因此,提高生物炭的热解温度可一定程度上增强其吸附性能和活化O3的能力。
进一步,通过XPS分析800 °C下热解SDBC的孔隙结构和官能团特征,反应前和反应后的XPS光谱图如图7所示。SDBC的Fe2p光谱显示出结合能为711.10 eV和712.69 eV处的2个峰,分别对应于Fe2+和Fe3+[31]。将反应后SDBC中不同价态的Fe含量与反应前相比,Fe3+含量由29.31%增加到43.33%,而Fe2+含量由70.69%减少至56.67%,表明在SDBC/O3体系降解污染物过程中,由于热解后的SDBC上含有Fe0,其可和臭氧氧化生成的Fe2+,而Fe2+在臭氧的存在下又进一步转化为Fe3+,同时诱导·OH和O2•−的生成[32],因此,表现出Fe2+含量的下降以及Fe3+含量的上升。·OH和O2•−的降解作用将在2.3节进行讨论。
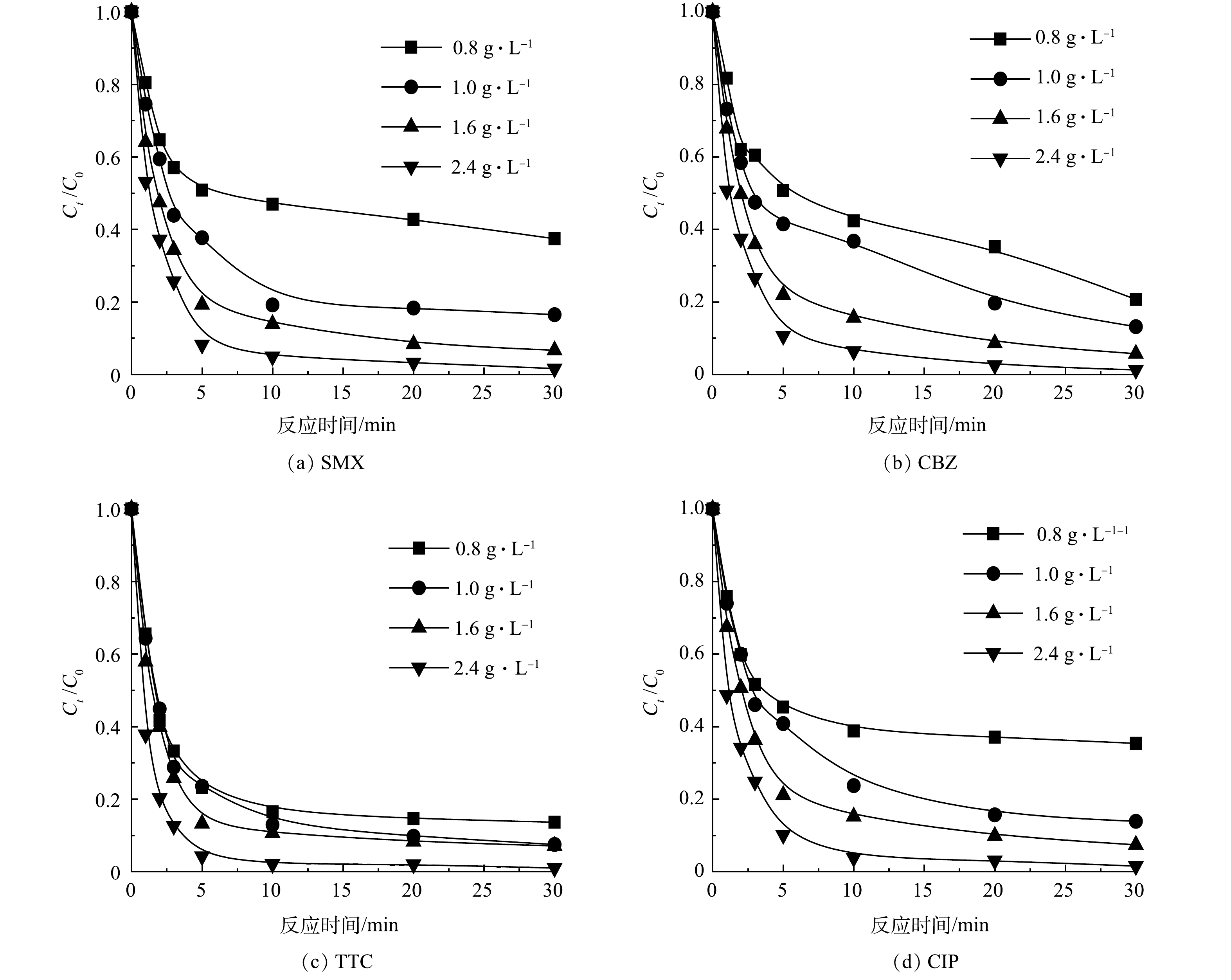
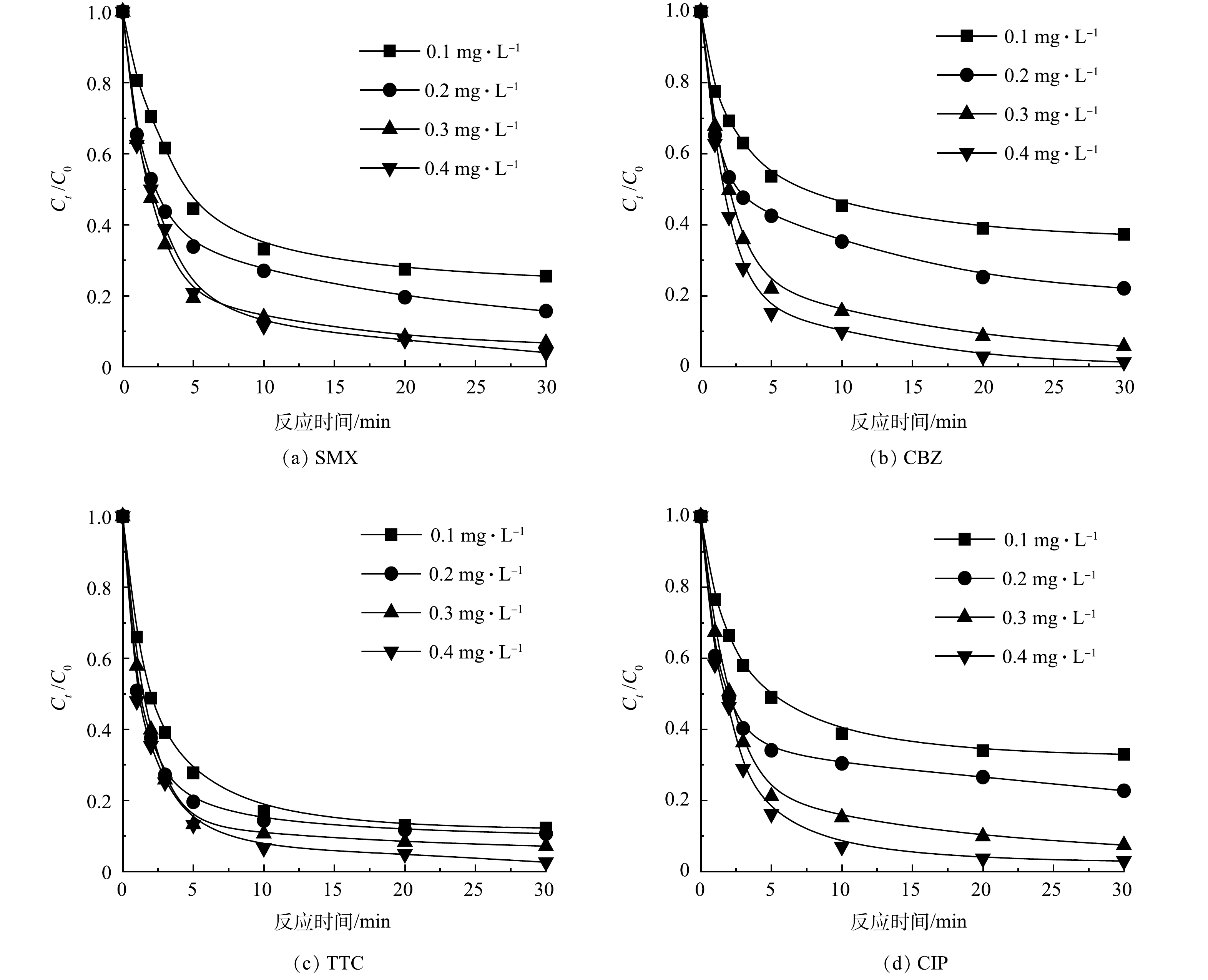
3)不同SDBC投加量以及O3浓度对PhACs去除的影响。为了探究不同的SDBC投加量以及O3浓度对渗滤液中PhACs去除效果的影响,进行了相关实验。如图8所示,在O3浓度为0.3 mg·L−1,初始pH为7.8的条件下,随着SDBC的投加量由0.8 g·L−1增加到2.4 g·L−1时,4种污染物的去除率显著提高,SMX的去除率由60%增加到98%,CBZ的去除率由80%增加到98%,TTC的去除率由83%增加到99%,CIP的去除率由60%增加到98%,这一现象归因于SDBC投加量的增加不仅提高了吸附效率,还提供了更多的活性位点,促进了O3活化,从而生成更多的活性物种来降解污染物。同时,在SDBC为1.6 g·L−1,初始pH为7.8的条件下,随着O3的投加量从0.1 mg·L−1增加到0.4 mg·L−1时,4种污染物的去除率也均有所提高(图9),结果表明,O3浓度的增加可促进生物炭表面吸附臭氧以及增加活性氧自由基和非自由基的数量,从而更快速地降解污染物。综上所述,考虑污染物的去除效率以及降解成本等原因,选定1.6 g·L−1的SDBC和0.3 mg·L−1的O3作为该体系的最佳投加量用于去除渗滤液中60 μmol·L−1的PhACs。
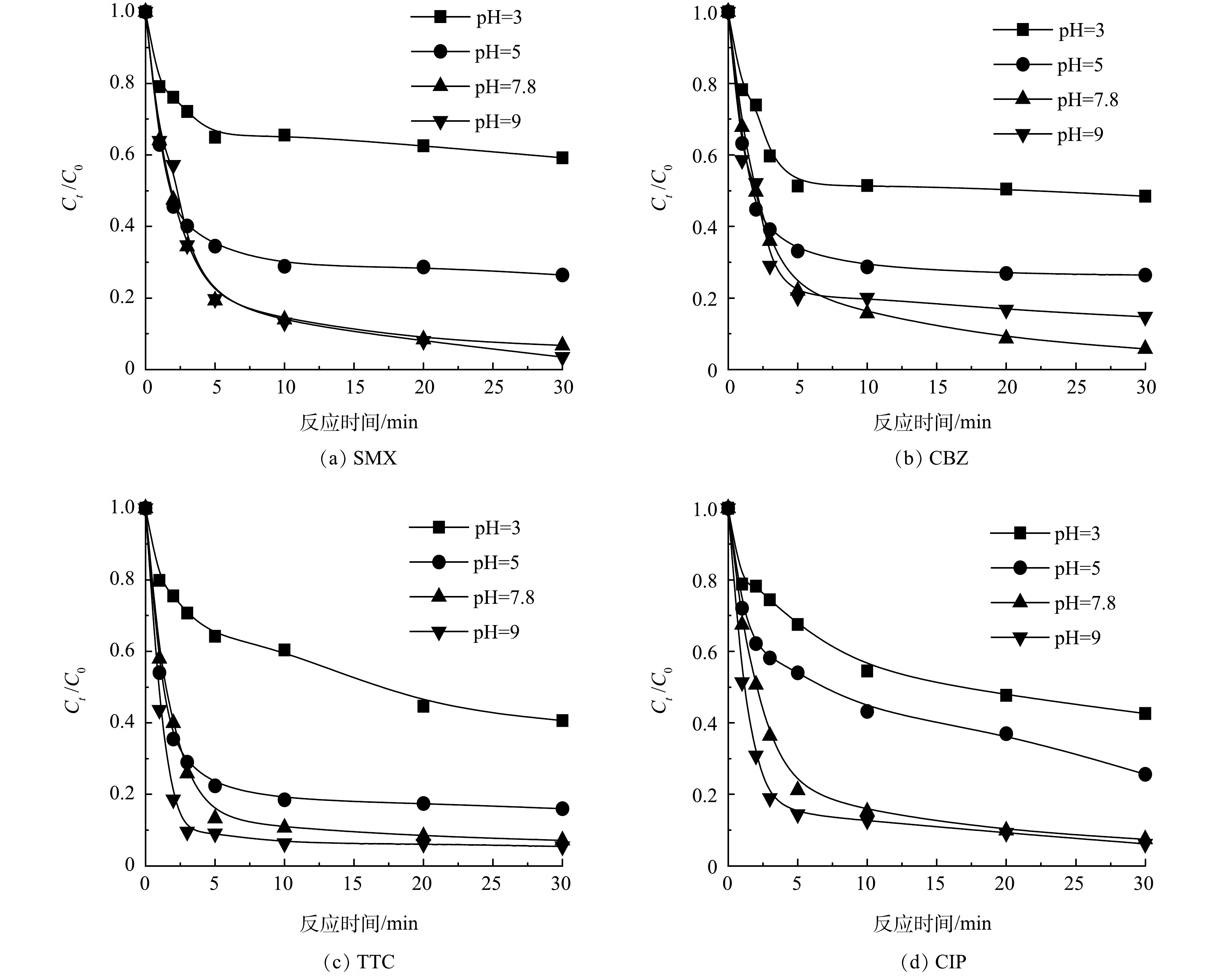
4)不同pH条件对SDBC/O3去除PhACs的影响。溶液的pH对污染物的降解具有显著影响,尤其在催化臭氧化体系中更为重要,因为其初始pH不仅影响臭氧的分解,还影响着活性氧自由基和非自由基的生成。因此,本研究探讨了不同pH条件下SDBC/O3体系对渗滤液中污染物的降解效果。如图10所示,随着溶液pH从3增加到9时,4种污染物的去除率均显著有所提高,SMX的去除率由40%升至98%,CBZ的去除率由45%升至92%,TTC的去除率由60%升至95%,CIP的去除率由60%升至95%。这可能是由于pH在很大程度上影响非均相体系臭氧的分解,在pH为2~6时,活性氧自由基往往难以形成,这就导致了较低的污染物去除率,而在pH>6条件下,污泥生物炭表面会吸附臭氧和原子氧,并在催化剂表面形成游离·OH和其他活性物质,因此,中性或碱性的pH条件下更适合臭氧氧化去除体系中污染物[32-33]。此外,酸性条件下SDBC中丰富的Fe元素容易浸出,导致材料表面的活性位点减少[34],这也是在pH=3时污染物去除率较低的原因之一。另一方面,生物炭存在着大量表面电荷,这些表面电荷的来源被认为是其脂肪族/芳香族表面和官能团(如羧基部分)的解离[35]。因此,生物炭的表面电荷与溶液中的pH息息相关,在pH<5.3时,生物炭的表面电荷带正电(pHpzc=5.3),随着pH的增加,生物炭的表面就会慢慢的带负电荷,从而呈现负电荷的状态。TTC、SMX和CIP在为酸性条件下通常以正电荷的形式存在,CBZ往往以不带电荷的形式存在,随着pH值升高,污染物慢慢以中性或负电荷的形式存在。综上,在酸性条件下,污染物的表面正电荷和生物炭的表面正电荷会产生相斥作用,不利于污染物的降解,只有在中碱性条件下,生物炭表面负电荷增加,有利于和中性的污染物相互作用。
-
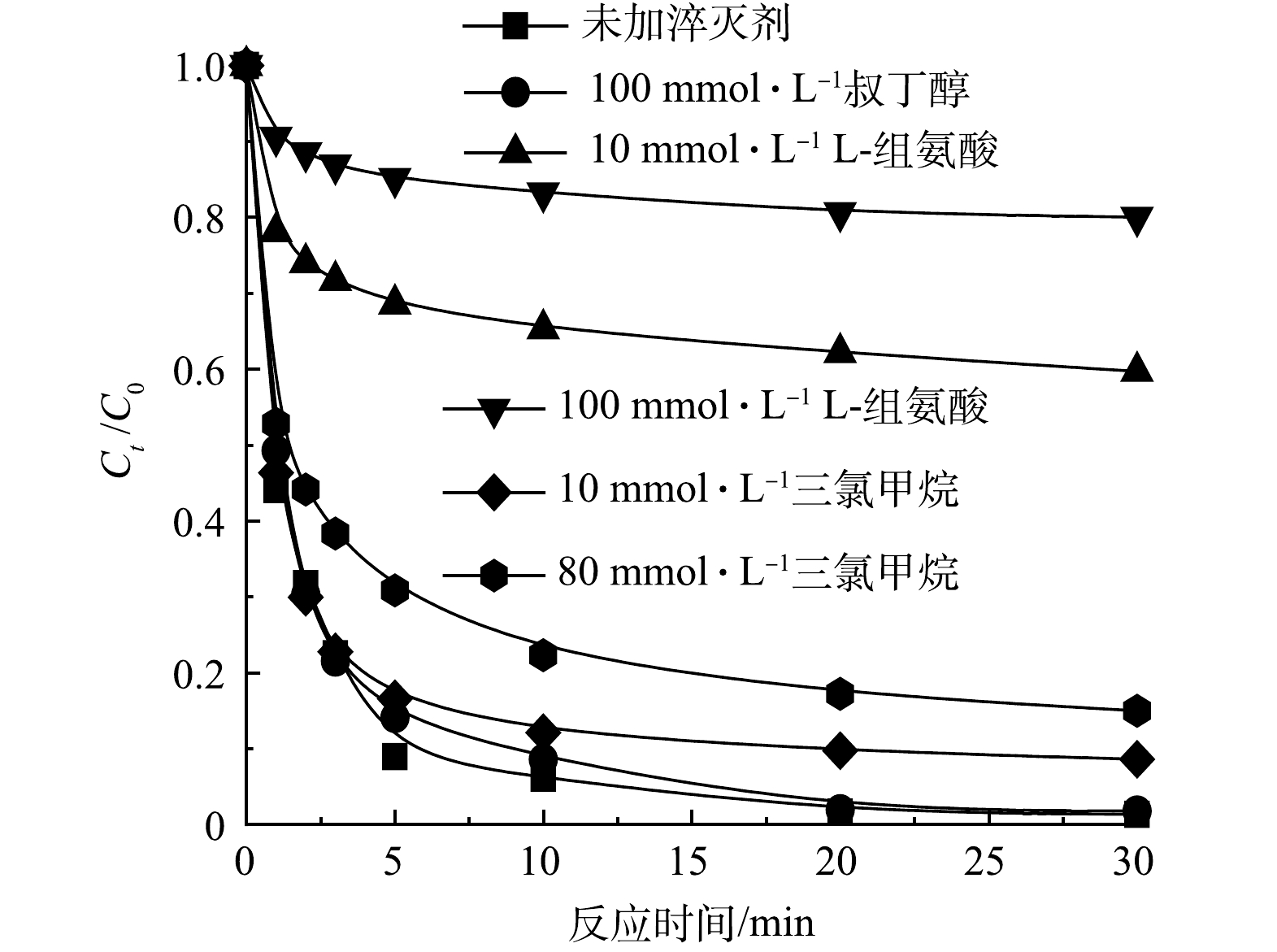
1)活性物质淬灭分析。为探究SDBC/O3体系中产生的活性物质,对单独一种污染物SMX的降解进行了淬灭实验研究。TBA常用作·OH淬灭剂(
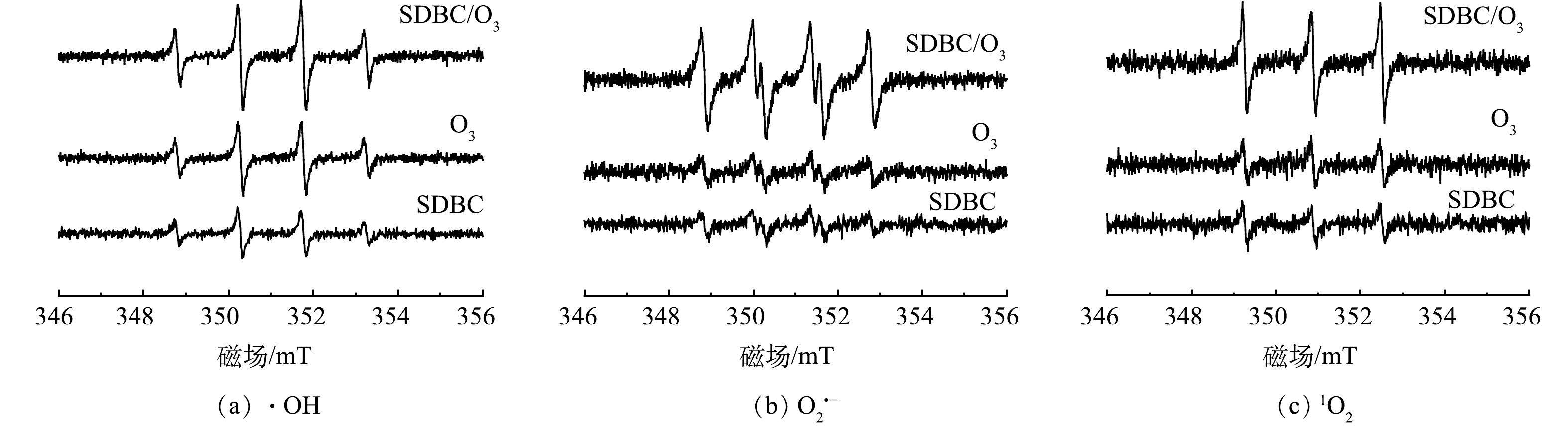
$ {\mathit{k}}_{\mathbf{T}\mathbf{B}\mathbf{A}/·\mathbf{O}\mathbf{H}} $ =6.0×108 L·(mol·s)−1)[36],如图11所示,在体系中加入100 mM的TBA并没有抑制污染物SMX的降解,说明在SDBC/O3体系去除污染物的过程中,·OH并不是主要活性物种,对SMX的降解无显著影响。选择CHCl3作为O2•−的淬灭剂$ ({\mathit{k}}_{{\mathrm{CH}}{{\mathrm{Cl}}}_{3}/{{\mathrm{O}}}_{2}^{·-}} $ =3.0×1010 L·(mol·s)−1)[37],发现10 mmol·L−1的CHCl3对体系污染物的降解有轻微抑制作用,而80 mmol·L−1的CHCl3进一步抑制了SMX的降解,去除率由100%降至82%,这表明O2•−在体系中起到了微小的降解作用。L-组氨酸可以作为1O2的淬灭剂[38]。10 mmol·L−1的L-组氨酸可以将污染物的去除率降低至40%,而100 mmol·L−1的L-组氨酸进一步将去除率降低至20%。由此可见,O2•−和1O2在SDBC/O3体系中对降解起主要作用的活性物质,其中1O2起主要作用,O2•−起次要作用。2)EPR分析。为进一步确定SDBC/O3体系中产生的活性物质,使用EPR实验进行活性物质的测定。DMPO作为·OH的捕获剂[39],图12(a)中显示了在SDBC、O3和SDBC/O3体系中均存在着强度比为1∶2∶2∶1的DMPO-·OH的信号峰,与前2个体系相比,SDBC/O3体系的信号峰有所增加,说明该体系生成了·OH。然而,TBA淬灭实验结果表明,·OH对污染物不起降解作用,因此,尽管该体系生成了·OH,但对污染物无去除作用。同时以DMPO作为捕获剂探究O2•−的生成情况,如图12(b)所示,单独使用SDBC和O3体系均出现了微弱的DMPO-O2•−信号峰,而SDBC/O3体系的DMPO-O2•−信号峰显著增强,可见该体系生成了大量O2•−,这与CHCl3的淬灭实验结果相一致,O2•−在该体系起到降解作用。以TEMP为捕获剂进一步探究了1O2的生成情况[40]。在图12(c)的EPR光谱中,检测到了明显的TEMP-1O2信号峰,与单独使用SDBC和O3体系相比,SDBC/O3体系的TEMP-1O2信号峰明显增强。由此可见,该体系生成了大量的1O2,且1O2在污染物降解中起主导作用。SDBC的FTIR谱图表明SDBC表面的C=O基团对于非自由基1O2的产生有一定的促进作用[26]。除此之外,在单独SDBC体系中,检测出了DMPO-O2•−和TEMP-1O2的信号峰,推测这可能与体系中的溶解氧有关,有研究[41]表明,在铁屑/溶解氧的体系中检测到·OH、O2•−和1O2的EPR信号光谱,而通入N2可显著降低体系中的光谱信号,可以佐证溶解氧在生成活性物质过程中的重要作用。因此,在单独SDBC体系也会检测到DMPO-O2•−和TEMP-1O2的信号峰。
-
1)本研究采用800 °C条件下制备的SDBC活化O3,SDBC/O3可高效去除渗滤液中PhACs(SMX、CBZ、TTC、CIP)。在SDBC/O3体系中,随着热解温度的升高,SDBC的吸附催化性能显著提升,这可能归因于生物炭比表面积的增大和活性位点的增多,因此,高热解温度有助于提升SDBC的催化性能。
2)随着溶液pH从3增加到9,PhACs的去除率逐渐增加。对反应前后SDBC的XPS光谱分析,发现Fe2+含量的下降以及Fe3+含量的生成,以及SDBC的FTIR光谱图说明该体系中生物炭表面的Fe2+和C=O基团参与了臭氧的活化过程。
3)在SDBC/O3体系中,O2•−和1O2是主要的活性物种,其中1O2起主要降解作用。综上所述,SDBC/O3体系在处理渗滤液有机微污染物方面具有一定的应用前景。
污泥生物炭耦合臭氧氧化去除渗滤液中多种药物类污染物
The removal of multiple pharmaceuticals from leachates by sludge biochar combined with ozonation
-
摘要: 臭氧(Ozone, O3)作为一种较强的氧化剂,被广泛应用于高级氧化工艺,催化剂的加入能够激活臭氧,产生活性氧物质(如·OH等)从而实现对废水的处理。然而,基于污泥生物炭催化臭氧氧化去除渗滤液中药物类污染物(pharmaceutically active compounds, PhACs)的效能及特性罕有报道。因此本研究通过高温热解法制备污泥生物炭(sludge biochar, SDBC)催化臭氧降解渗滤液中的典型PhACs,包括磺胺类抗生素磺胺甲恶唑(sulfamethoxazole, SMX)、喹诺酮类抗生素环丙沙星(ciprofloxacin, CIP)、四环素类抗生素四环素(tetracycline, TTC)以及抗癫痫药物卡马西平(carbamazepine, CBZ)。研究结果表明,在未调pH的条件下(pH=7.8),SDBC/O3体系能快速去除渗滤液的多种PhACs,在30 min内去除率均超过90%,效果显著优于单独使用O3或SDBC,表明该体系能较好地处理渗滤液中的微污染物。pH实验表明SDBC/O3体系在中性和碱性的条件下降解效果较好,在酸性的条件下效果较差,推测是由于酸性的水环境不利于臭氧分解产生活性物质以及污染物和生物炭之间易产生相斥作用。淬灭实验和电子顺磁共振实验(electron paramagnetic resonance, EPR)显示,体系中主要的活性物质为O2•−和1O2,其中1O2起降解主要作用,O2•−起次要作用。SDBC表面上的C=O基团和Fe2+是臭氧活化的主要活性位点。本研究阐明了SDBC在催化臭氧化方面的主要机制,研究结果可以为渗滤液中有机微污染物的处理提供理论依据和技术支撑。Abstract: Ozone (O3), as an common oxidant, is extensively applied in advanced oxidation processes. Adding catalysts can activate ozone to generate reactive oxygen species (ROS), such as hydroxyl radicals (·OH), thereby enhancing the efficiency of wastewater treatment. However, there is limited researches on the efficiency and mechanism of sludge derived biochar catalyzed ozonation (SDBC/O3) for pharmaceutically active compounds (PhACs) removal from leachates. In this study, SDBC was prepared through high temperature pyrolytic cracking method, and SDBC/O3 was used to remove typical PhACs in leachates, such as sulfonamide antibiotics of sulfamethoxazole (SMX), the quinolone antibiotics of ciprofloxacin (CIP), the tetracycline antibiotics of tetracycline (TTC), and the antiepileptic drugs of carbamazepine (CBZ). The results showed that under unadjusted pH conditions (pH=7.8), all the PhACs could be rapidly removed by SDBC/O3 from leachates, with the removal efficiency exceeding 90% in 30 min, which is significantly higher than O3 or SDBC alone. This indicated that SDBC/O3 could well treat the micropollutants in the leachates. The effect of pH investigation revealed that higher removal efficiency occurred at neutral and alkaline pHs than acidic pHs, likely due to the unfavorable environment for ozone decomposition into reactive oxygen species and easy production of repulsion between pollutants and biochar in acidic water. Quenching experiments and electron paramagnetic resonance (EPR) indicated that the primary reactive species in the system were O2•− and singlet oxygen 1O2, and 1O2 played the major role in removing PhACs. The C=O and Fe2+ on SDBC were the dominant reactive sites for O3 activating. This research elucidates the mechanism of SDBC/O3 removing PhACs in leachates and provides a theoretical and technical support for treating organic micropollutants in leachates.
-
Key words:
- sludge biochar /
- ozone /
- leachate /
- pharmaceuticals
-

-
-
[1] SAXENA V, PADHI S K, DIKSHIT P K, et al. Recent developments in landfill leachate treatment: Aerobic granular reactor and its future prospects[J]. Environmental Nanotechnology, Monitoring & Management, 2022, 18: 100689. [2] ALFAIA R G D S M, COSTA A M, CAMPOS J C. Municipal solid waste in Brazil: A review[J]. Waste Management & Research, 2017, 35(12): 1195-1209. [3] HAN Y, HU L-X, LIU T, et al. Non-target, suspect and target screening of chemicals of emerging concern in landfill leachates and groundwater in Guangzhou, South China[J]. Science of the Total Environment, 2022, 837: 155705. doi: 10.1016/j.scitotenv.2022.155705 [4] YU X, SUI Q, LYU S, et al. Rainfall influences occurrence of pharmaceutical and personal care products in landfill leachates: evidence from seasonal variations and extreme rainfall episodes[J]. Environmental Science & Technology, 2021, 55(8): 4822-4830. [5] TENG C, ZHOU K, PENG C, et al. Characterization and treatment of landfill leachate: A review[J]. Water Research, 2021, 203: 117525. doi: 10.1016/j.watres.2021.117525 [6] GAUTAM P, KUMAR S, LOKHANDWALA S. Advanced oxidation processes for treatment of leachate from hazardous waste landfill: A critical review[J]. Journal of Cleaner Production, 2019, 237: 117639. doi: 10.1016/j.jclepro.2019.117639 [7] NAWROCKI J, KASPRZYK-HORDERN B. The efficiency and mechanisms of catalytic ozonation[J]. Applied Catalysis B: Environmental, 2010, 99(1/2): 27-42. [8] ZHU Y, LUO H, WANG T, et al. Advanced treatment of landfill leachate by catalytic ozonation with MnCeOx/γ-Al2O3 catalyst[J]. Surfaces and Interfaces, 2024: 104113. [9] LIU W-J, JIANG H, YU H-Q. Development of biochar-based functional materials: toward a sustainable platform carbon material[J]. Chemical Reviews, 2015, 115(22): 12251-12285. doi: 10.1021/acs.chemrev.5b00195 [10] WEN G, PAN Z-H, MA J, et al. Reuse of sewage sludge as a catalyst in ozonation–efficiency for the removal of oxalic acid and the control of bromate formation[J]. Journal of Hazardous Materials, 2012, 239: 381-388. [11] GAO B, ZHANG J, LIU J, et al. Excess sludge-based biochar loaded with manganese enhances catalytic ozonation efficiency for landfill leachate treatment[J]. Environmental Pollution, 2024: 123591. [12] WANG R, DUAN X, WANG S, et al. Production, properties, and catalytic applications of sludge derived biochar for environmental remediation[J]. Water Research, 2020, 187: 116390. doi: 10.1016/j.watres.2020.116390 [13] ZHANG X, SUN P, WEI K, et al. Enhanced H2O2 activation and sulfamethoxazole degradation by Fe-impregnated biochar[J]. Chemical Engineering Journal, 2020, 385: 123921. doi: 10.1016/j.cej.2019.123921 [14] TAO S, LIANG S, CHEN Y, et al. Enhanced sludge dewaterability with sludge-derived biochar activating hydrogen peroxide: Synergism of Fe and Al elements in biochar[J]. Water Research, 2020, 182: 115927. doi: 10.1016/j.watres.2020.115927 [15] WANG X, GU L, ZHOU P, et al. Pyrolytic temperature dependent conversion of sewage sludge to carbon catalyst and their performance in persulfate degradation of 2-Naphthol[J]. Chemical Engineering Journal, 2017, 324: 203-215. doi: 10.1016/j.cej.2017.04.101 [16] WANG J, LIAO Z, IFTHIKAR J, et al. Treatment of refractory contaminants by sludge-derived biochar/persulfate system via both adsorption and advanced oxidation process[J]. Chemosphere, 2017, 185: 754-763. doi: 10.1016/j.chemosphere.2017.07.084 [17] COSTA R C, MOURA F C, ARDISSON J, et al. Highly active heterogeneous Fenton-like systems based on Fe0/Fe3O4 composites prepared by controlled reduction of iron oxides[J]. Applied Catalysis B: Environmental, 2008, 83(1/2): 131-139. [18] GAN Q, HOU H, LIANG S, et al. Sludge-derived biochar with multivalent iron as an efficient Fenton catalyst for degradation of 4-Chlorophenol[J]. Science of the Total Environment, 2020, 725: 138299. doi: 10.1016/j.scitotenv.2020.138299 [19] ZHAO L, CAO X, MAŠEK O, et al. Heterogeneity of biochar properties as a function of feedstock sources and production temperatures[J]. Journal of Hazardous Materials, 2013, 256: 1-9. [20] ZHAO Y, SONG M, CAO Q, et al. The superoxide radicals’ production via persulfate activated with CuFe2O4@ Biochar composites to promote the redox pairs cycling for efficient degradation of o-nitrochlorobenzene in soil[J]. Journal of Hazardous Materials, 2020, 400: 122887. doi: 10.1016/j.jhazmat.2020.122887 [21] DAI X-H, FAN H-X, YI C-Y, et al. Solvent-free synthesis of a 2D biochar stabilized nanoscale zerovalent iron composite for the oxidative degradation of organic pollutants[J]. Journal of Materials Chemistry A, 2019, 7(12): 6849-6858. doi: 10.1039/C8TA11661J [22] OULTON R, HAASE J P, KAALBERG S, et al. Hydroxyl radical formation during ozonation of multiwalled carbon nanotubes: performance optimization and demonstration of a reactive CNT filter[J]. Environmental Science & Technology, 2015, 49(6): 3687-3697. [23] ZHANG F, WU K, ZHOU H, et al. Ozonation of aqueous phenol catalyzed by biochar produced from sludge obtained in the treatment of coking wastewater[J]. Journal of Environmental Management, 2018, 224: 376-386. doi: 10.1016/j.jenvman.2018.07.038 [24] LIANG J, XU X, ZAMAN W Q, et al. Different mechanisms between biochar and activated carbon for the persulfate catalytic degradation of sulfamethoxazole: Roles of radicals in solution or solid phase[J]. Chemical Engineering Journal, 2019, 375: 121908. doi: 10.1016/j.cej.2019.121908 [25] DUAN X, SUN H, TADE M, et al. Metal-free activation of persulfate by cubic mesoporous carbons for catalytic oxidation via radical and nonradical processes[J]. Catalysis Today, 2018, 307: 140-146. doi: 10.1016/j.cattod.2017.04.038 [26] LUO J, BO S, QIN Y, et al. Transforming goat manure into surface-loaded cobalt/biochar as PMS activator for highly efficient ciprofloxacin degradation[J]. Chemical Engineering Journal, 2020, 395: 125063. doi: 10.1016/j.cej.2020.125063 [27] WANG C, LIN C-Y, LIAO G-Y. Feasibility study of tetracycline removal by ozonation equipped with an ultrafine-bubble compressor[J]. Water, 2021, 13(8): 1058. doi: 10.3390/w13081058 [28] ZHANG J, LIU J, GAO B, et al. The efficiency and mechanism of excess sludge-based biochar catalyst in catalytic ozonation of landfill leachate[J]. Journal of Hazardous Materials, 2023, 459: 132118. doi: 10.1016/j.jhazmat.2023.132118 [29] ZHAO B, O'CONNOR D, ZHANG J, et al. Effect of pyrolysis temperature, heating rate, and residence time on rapeseed stem derived biochar[J]. Journal of Cleaner Production, 2018, 174: 977-987. doi: 10.1016/j.jclepro.2017.11.013 [30] DUAN X, AO Z, ZHOU L, et al. Occurrence of radical and nonradical pathways from carbocatalysts for aqueous and nonaqueous catalytic oxidation[J]. Applied Catalysis B: Environmental, 2016, 188: 98-105. doi: 10.1016/j.apcatb.2016.01.059 [31] XU L, WANG J. Magnetic nanoscaled Fe3O4/CeO2 composite as an efficient Fenton-like heterogeneous catalyst for degradation of 4-chlorophenol[J]. Environmental Science & Technology, 2012, 46(18): 10145-10153. [32] KASPRZYK-HORDERN B, ZIóŁEK M, NAWROCKI J. Catalytic ozonation and methods of enhancing molecular ozone reactions in water treatment[J]. Applied Catalysis B: Environmental, 2003, 46(4): 639-669. doi: 10.1016/S0926-3373(03)00326-6 [33] GU L, ZHANG X, LEI L. Degradation of aqueous p-nitrophenol by ozonation integrated with activated carbon[J]. Industrial & Engineering Chemistry Research, 2008, 47(18): 6809-6815. [34] RONG X, XIE M, KONG L, et al. The magnetic biochar derived from banana peels as a persulfate activator for organic contaminants degradation[J]. Chemical Engineering Journal, 2019, 372: 294-303. doi: 10.1016/j.cej.2019.04.135 [35] HARVEY O R, HERBERT B E, KUO L-J, et al. Generalized two-dimensional perturbation correlation infrared spectroscopy reveals mechanisms for the development of surface charge and recalcitrance in plant-derived biochars[J]. Environmental Science & Technology, 2012, 46(19): 10641-10650. [36] CHEN J, QIAN Y, LIU H, et al. Oxidative degradation of diclofenac by thermally activated persulfate: implication for ISCO[J]. Environmental Science and Pollution Research, 2016, 23: 3824-3833. doi: 10.1007/s11356-015-5630-0 [37] BUXTON G V, GREENSTOCK C L, HELMAN W P, et al. Critical Review of rate constants for reactions of hydrated electrons, hydrogen atoms and hydroxyl radicals (· OH/· O− in Aqueous Solution[J]. Journal of Physical and Chemical Reference Data, 1988, 17(2): 513-886. doi: 10.1063/1.555805 [38] ZHANG K, YE C, LOU Y, et al. Promoting selective water decontamination via boosting activation of periodate by nanostructured Ru-supported Co3O4 catalysts[J]. Journal of Hazardous Materials, 2023, 442: 130058. doi: 10.1016/j.jhazmat.2022.130058 [39] YU J, TANG L, PANG Y, et al. Magnetic nitrogen-doped sludge-derived biochar catalysts for persulfate activation: Internal electron transfer mechanism[J]. Chemical Engineering Journal, 2019, 364: 146-159. doi: 10.1016/j.cej.2019.01.163 [40] YIN R, GUO W, WANG H, et al. Singlet oxygen-dominated peroxydisulfate activation by sludge-derived biochar for sulfamethoxazole degradation through a nonradical oxidation pathway: Performance and mechanism[J]. Chemical Engineering Journal, 2019, 357: 589-599. doi: 10.1016/j.cej.2018.09.184 [41] XUE G, LIU C, WANG K, et al. Implementing conversion of Sb (III) to Sb (V) and their sequestration by iron shavings simultaneously: Synergistic role of hydroxyl radical and iron (hydr) oxides[J]. Chemical Engineering Journal, 2024, 483: 149140. doi: 10.1016/j.cej.2024.149140 -




 下载:
下载: