-
在厌氧反硝化过程中,细胞内部电子传递主要是由有机物经糖酵解和三羧酸循环产生还原型烟酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide, NADH)为反硝化过程提供电子,电子经复合体Ⅰ(黄素单核苷酸FMN和Fe-S蛋白)传递给醌池,然后一部分电子传递给膜结合的硝酸盐还原酶(NAR)将硝酸盐还原为亚硝酸盐,另一部分电子经复合体Ⅲ传递给周质空间中的细胞色素c,细胞色素c作为电子载体再将电子传递给周质中的亚硝酸盐还原酶(NIR)、一氧化氮还原酶(NOR)和一氧化二氮还原酶(NOS),最终实现将硝酸盐还原为氮气(
$ \mathrm{N}{\mathrm{O}}_{3}^{-}\stackrel{\mathrm{N}\mathrm{A}\mathrm{R}}{\to }\mathrm{N}{\mathrm{O}}_{2}^{-}\stackrel{\mathrm{N}\mathrm{I}\mathrm{R}}{\to } $ NO$ \stackrel{\mathrm{N}\mathrm{O}\mathrm{R}}{\to }{\mathrm{N}}_{2}\mathrm{O}\stackrel{\mathrm{N}\mathrm{O}\mathrm{S}}{\to }{\mathrm{N}}_{2} $ )[1]。生物反硝化过程归根结底是电子的产生与传递,提升电子传递速率是强化反硝化的关键。由于纳米材料独特的物理、化学和电学性质(包括微生物易于粘附和定殖、金属纳米粒子的导电性、比表面积大等),利用纳米材料强化微生物电子传递的研究越来越受关注。在反硝化领域,LIU等[2]综述了零价铁纳米粒子(nZVI)通过生物和非生物协同作用强化反硝化,他们指出虽然nZVI在促进反硝化方面取得了良好的成效,但是,nZVI易产生活性氧物质(ROS),在生物膜表面形成钝化层,限制了nZVI的实际应用。此外,石墨烯[3]、黏土矿物[4]、Mn3O4等[5]在强化生物反硝化过程也发挥了积极的作用。但化学法合成金属纳米粒子的过程需要有毒的化学物质和极端的反应条件,特别是这些金属纳米粒子表面能高,易在水中团聚,进而减少反应的活性位点,降低反应速率。相反,生物法合成纳米颗粒可以在较为温和环境下进行,具有生物相容性、非毒性溶剂和低成本等优点。特别是钯基双金属被报道在选择性催化硝酸盐还原方面表现出较好的对N2的选择性,避免了副产物亚硝酸盐和N2O的过量积累[6]。影响微生物降解污染物的原因除了电子传递效率,还有以群感信号分子为媒介的群体感应(QS)现象,它是微生物通过产生、积累、感应信号分子来调控自身基因表达的一种方式,与生物膜的形成、毒力因子的表达、颗粒污泥的形成和生物酶活性等密切相关。在脱氮方面,目前的研究主要集中于对厌氧氨氧化(Anammox)[7]、异养硝化-好氧反硝化[8]、以及以铜绿假单胞菌为代表的反硝化过程[9],对活性污泥参与的一般厌氧反硝化过程缺乏QS方面的研究。此外,关于纳米粒子对QS的影响目前也只是处于初步研究阶段,例如,LI等[10]研究表明,100 μg·L−1 Ag和氧化石墨烯会显著增加3OC12-HSL信号分子的浓度,促进铜绿假单胞菌(Pseudomonas aeruginosa PAO1)蛋白酶的产生和生物膜的形成,而等量的Fe虽然也刺激了3OC12-HSL的分泌,但并没有导致蛋白酶和生物膜的增加。OUYANG等[11]向恶臭假单胞菌(Pseudomonas putida)生物膜中添加0.5 mg·L−1 ZnO,其促进了QS信号分子c-di-GMP的释放,从而使生物膜有关的基因上调,促进生物膜的形成,而250 mg·L−1 ZnO则表现出相反的抑制作用。
基于上述研究结果,本研究利用取自污水处理厂的活性污泥合成了Bio-Pd0,探究了钯对反硝化酶电子传递的影响,通过三维荧光光谱、生物群落分析和群体感应抑制剂研究了Bio-Pd0对反硝化的影响和群体感应对反硝化效果的调控,本研究结果以期为Bio-Pd0强化反硝化提供参考。
-
主要试剂包括四氯钯酸钠(Na2PdCl4,98%,麦克林)、葡萄糖,以上试剂均为分析纯;反硝化活性污泥取自广东广州某污水处理厂;反硝化培养基(DM培养基)中含有4.2 g·L−1 Na2HPO4、1.5 g·L−1 KH2PO4、0.1 g·L−1 MgSO4、微量元素1 mL,葡萄糖为碳源;微量元素含有5.0 g·L−1 EDTA、2.2 g·L−1 ZnSO4、5.5 g·L−1 CaCl2、5.06 g·L−1 MnCl2·4H2O、5 g·L−1 FeSO4·7H2O、1.57 g·L−1 CuSO4·5H2O、1.1 g·L−1 (NH4)6 Mo7O2·4H2O、1.61 g·L−1 CoCl2·6H2O。
-
将20 mL活性污泥与80 mL DM培养基加入血清瓶(污泥质量浓度为2 g·L−1),然后加入不同量的Na2PdCl4母液(1 g·L−1),以葡萄糖0.94 g·L−1为电子供体,充氮气15 min后立即密封,将其置于恒温摇床(150 r·min−1,(32±1) °C)培养,同时,将高温灭菌后的相同体系做对照。Pd2+浓度为0、5和10 mg·L−1的样品分别定义为Bio-PdNPs-0、Bio-PdNPs-5和Bio-PdNPs-10。用EDS能谱分析污泥中钯在微生物表面的分布情况。
-
在150 mL血清瓶中进行硝酸盐反硝化实验。将负载不同量Bio-PdNPs的活性污泥离心并接种于100 mL DM培养基,葡萄糖1.4 g·L−1,初始NO3−-N质量浓度为(200±2) mg·L−1(污泥浓度为2 g·L−1),此时C/N=7,充氮气10 min后立即密封并置于恒温摇床(150 r·min−1,(31±1) ℃)。通过调节葡萄糖浓度确定不同的C/N比(3、7和10)。每隔一定时间用注射器取样,通过紫外分光光度法测定溶液中的NO3−-N、N-(1-萘基)-乙二铵分光光度法测定NO2−-N、纳氏试剂法测NH4+-N,用铝箔气体采样袋收集产生的气体,通过傅里叶变换红外气体分析仪(MultiGas 2030,MKS,美国)分析NOx气体。基于反硝化速率的反硝化酶电子传递能力分析参考OBEROI等[12]的计算方法。
-
使用3D荧光-分光光度计(HITACHI F7000,China)测定不同溶解性有机物(DOM)的含量。激发波长(Ex)为200~400 nm,狭缝宽度为5 nm;发射波长(Em)为280~500 nm,狭缝宽度为2.36 nm。
-
通过向反硝化体系中添加群体感应抑制剂猪肾酰化酶和香兰素探究群体感应对反硝化的影响,实验内容如下:将香兰素用热水溶解制备1 g·L−1的母液,向Bio-PdNPs-0和Bio-PdNPs-5介导的反硝化体系(NO3−-N = 200 mg·L−1,C/N=7)分别加入香兰素母液使得最终质量浓度为0、0.3、0.6、0.8、1 g·L−1,或向Bio-PdNPs-0和Bio-PdNPs-5中分别加入0.2 g·L−1猪肾酰化酶,测定反硝化产物。
-
采用高通量16S rRNA基因焦磷酸测序技术评价微生物群落结构。分别采集10 mL均质污泥样品(Bio-PdNPs-0、Bio-PdNPs-5),交由百迈克生物科技有限公司测定。经DNA提取后,在Hiseq 2500平台上使用Illumina高通量测序进行PCR扩增、纯化、定量和焦磷酸测序,测序数据及生物信息学分析在Biomarker在线平台上进行。
-
以葡萄糖为电子供体用于微生物还原钯,反应12 h后,Bio-Pd0在微生物表面的分布见图1。随着Pd2+添加量的增加,钯元素响应增强,其元素占比由0.53%增加到1.28%,表明钯成功负载在微生物表面。
-
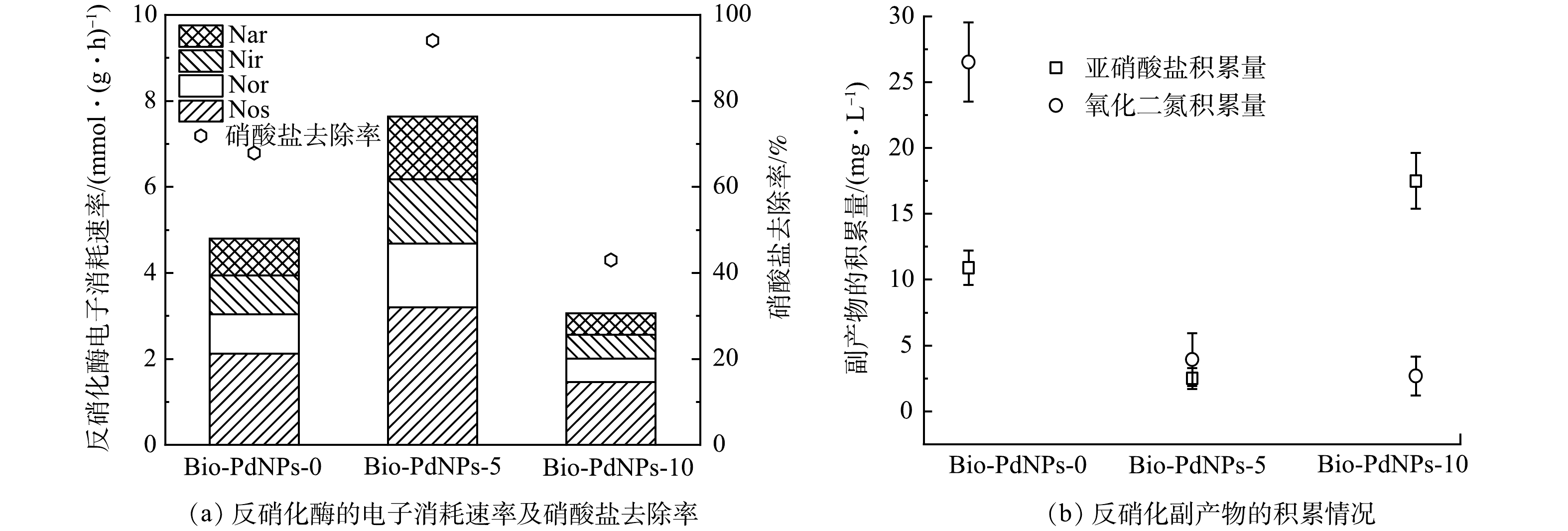
基于反硝化速率的反硝化酶电子利用情况见图2。可见,随着生物钯负载量的增加,反硝化酶电子利用速率呈现先增后减的趋势,说明Bio-PdNPs-5促进了反硝化酶对电子的利用,使得Nar、Nir、Nor、Nos的电子消耗速率(3.20、1.49、1.49、1.46 mmol·(g·h)−1(以VSS计))较Bio-PdNPs-0(2.13、0.91、0.91、0.85 mmol·(g·h)−1))分别提高了50.35%、63.38%、63.38%、70.92%,相应的亚硝酸盐和N2O的积累量分别由Bio-PdNPs-0的10.9 mg·L−1和26.53 mg·L−1降至2.5 mg·L−1和3.93 mg·L−1(Bio-PdNPs-5),这与硝酸盐的去除效果一致。反应5 h后,Bio-PdNPs-5中硝酸盐的去除率由67.85%提高到94.00%,而Bio-PdNPs-10对反硝化酶电子利用(1.47、0.55、0.55、0.50 mmol·(g·h)−1)的抑制率分别高达31.05%、40%、40%、41.41%,并产生17.5 mg·L−1和2.68 mg·L−1的亚硝酸盐和N2O积累,对硝酸盐的去除率也降低到43%。这可能是过量钯对生物的毒性抑制作用。LV等[13]发现大量的钯纳米粒子可以刺激细胞产生ROS,从而对细胞膜和DNA造成内部的氧化损伤,或由于纳米粒子的锋利边缘破坏细胞膜,导致膜透性增加以及膜电位崩溃。
-
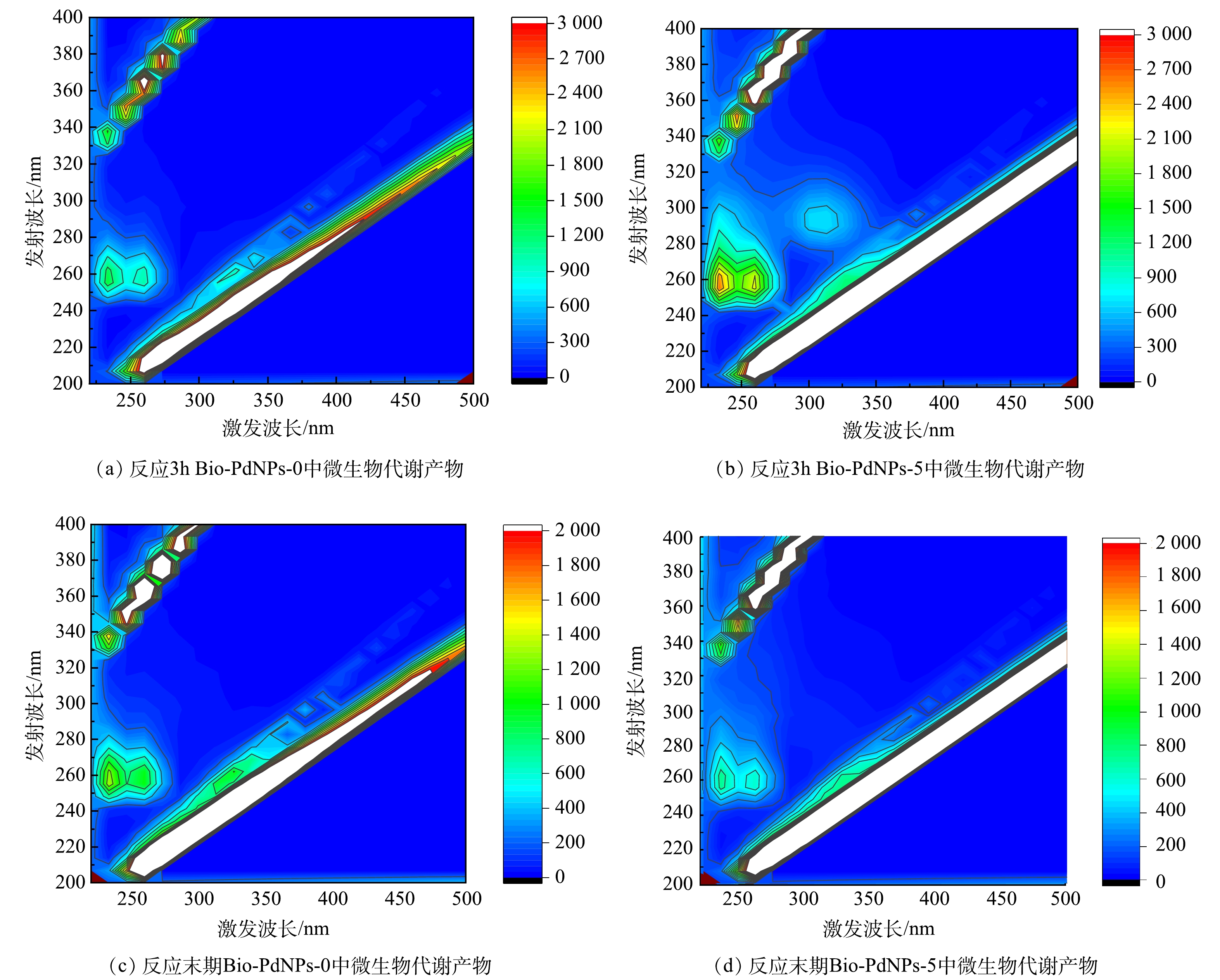
对不同反应时刻反应体系中的DOM进行测定,结果见图3。反应3 h后,在Ex/Em=250~280 nm/220~270 nm处为微生物的代谢产物类蛋白质等物质[14],其中Bio-PdNPs-5中在Ex/Em=280~300 nm/325~350 nm处发现微生物的代谢产物类色氨酸类物质,类色氨酸类物质是构成松散型胞外多聚物(S-EPS)的主要成分[15],S-EPS被认为是微生物机质分解过程和内源呼吸过程的产物,S-EPS逐渐增强,表明负载钯可促进了微生物的代谢作用,这有助于生物同步脱氮除碳。在反应末期,在2个反应体系中均检测到残余类蛋白质物质,且其在负载钯组中的浓度低于对照组,说明负载钯可促进微生物的代谢。
-
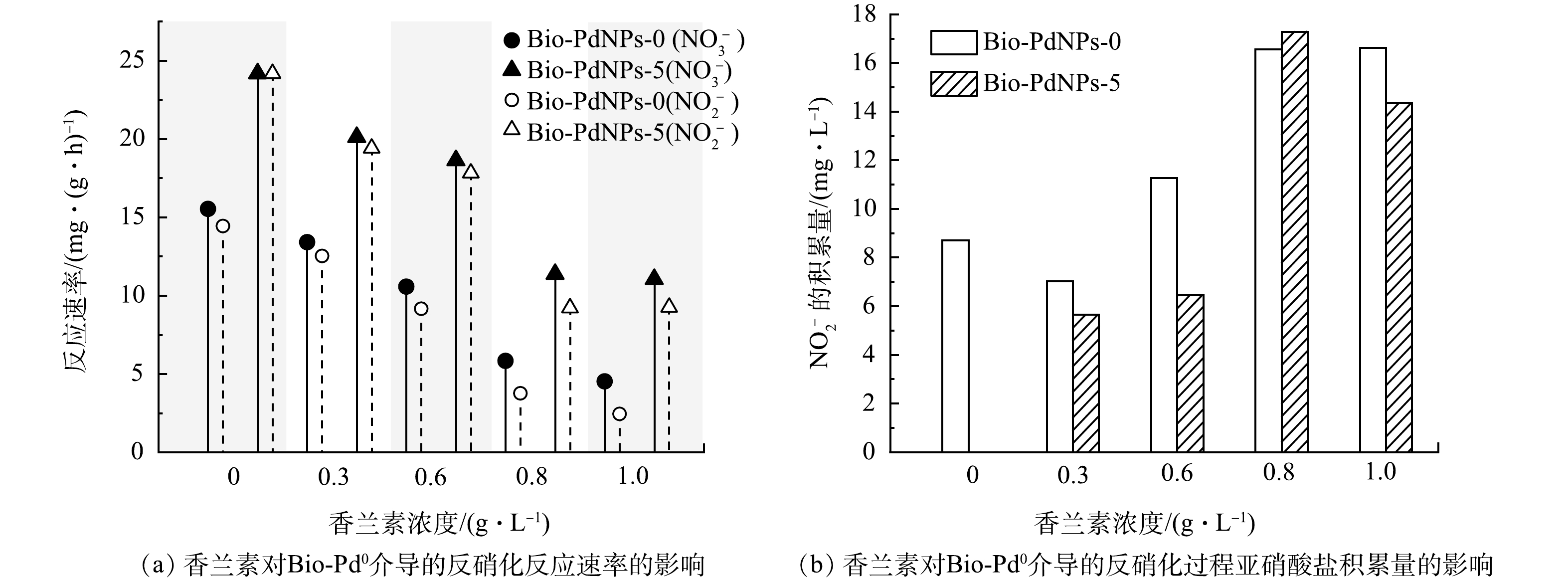
香兰素对Bio-PdNPs介导的反硝化影响情况见图4。可见,随着香兰素浓度的增加,加钯组(Bio-PdNPs-5)和不加钯组(Bio-PdNPs-0)的活性污泥反硝化速率均持续降低,并产生大量亚硝酸盐的积累。这可能是由于香兰素抑制了细胞EPS的合成及其生物活性。SHI等[16]外加0.05 g·L−1的香兰素使活性污泥EPS中蛋白质含量下降了80%。香兰素通过干扰细菌的QS系统来抑制菌落的生长,如枯草芽孢杆菌、大肠杆菌等[17]。值得注意的是,负载钯后(Bio-PdNPs-5),虽然硝酸盐还原速率被香兰素抑制,但是其反硝化速率仍高于相同条件下的Bio-PdNPs-0组,进一步说明Bio-Pd0在该反硝化过程中的重要非生物催化作用。
进一步以典型的群体感应抑制剂猪肾酰化酶对Bio-Pd0介导的反硝化的影响见图5。外加0.2 g·L−1猪肾酰化酶后,不加钯组(Bio-PdNPs-0)的活性污泥NO3−和NO2−反硝化速率分别由15.32、13.96 mg·(g·h)−1(以VSS计)提高到17.52、15.97 mg·(g·h)−1,相应的促进率为14.36%、14.40%。加钯组(Bio-PdNPs-5)的活性污泥中NO3−和NO2−反硝化速率分别由22.50、22.19 mg·(g·h)−1提高到27.72、27.21 mg·(g·h)−1,相应的促进率为23.20%、22.62%,并且没有产生大量亚硝酸盐的积累,说明群体感应淬灭对反硝化有利,同时也说明钯对群体感应调控反硝化过程具有积极的影响。CHENG等[18]向反硝化体系中投加2 μmol·L−1的群体感应信号分子C6-HSL抑制了厌氧反硝化硝酸盐的去除率,并且产生N2O的积累。TOYOFUKU等[19]在铜绿假单胞菌(P. aeruginosa. PAO1)反硝化体系中观察到QS突变体(ΔrhlI和ΔlasI)能够加速硝酸盐的还原,而外加QS信号分子C4-HSL(10 μmol·L−1)和3-oxo-C12-HSL(1 μmol·L−1)后,硝酸盐的还原速率降低至原来的水平,进一步研究[20]表明铜绿假单胞菌的rhl QS系统可以通过调控nark1、nirS、norC和nosR基因的转录影响反硝化作用,las QS系统通过作用于rhl QS系统间接影响反硝化。综上可以得出添加QSI猪肾酰化酶可以在协同Bio-PdNPs化学催化作用的基础上进一步提高生物反硝化效果。
-
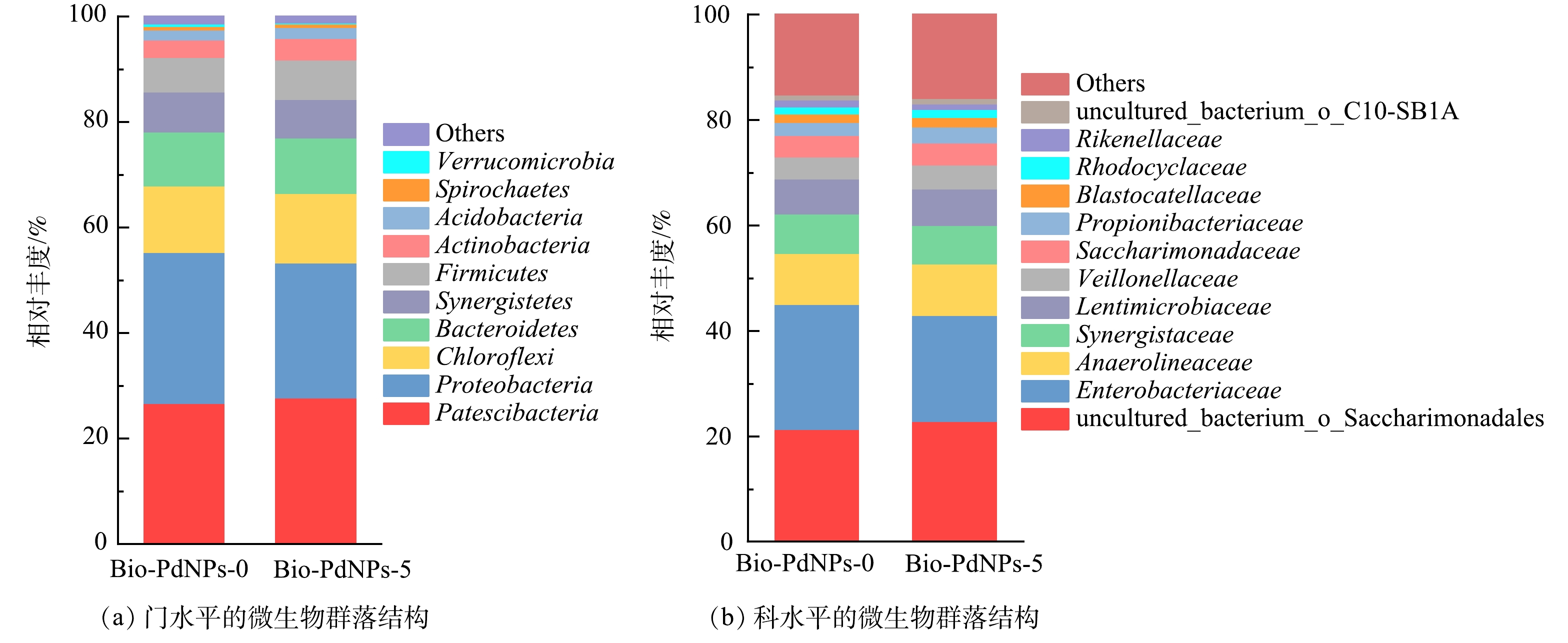
门水平的微生物群落结构见图6。由图6可见,Bio-PdNPs对门水平上的微生物群落结构影响不大,占主要比例的菌门有髌骨细菌门(Patescibacteria)、变形杆菌门(Proteobacteria)、绿弯菌门(Chloroflexi)和拟杆菌门(Bacteroidetes),这些微生物均与反硝化有关[21],负载Bio-PdNPs后上述4种菌门仍然占主导地位。其中,相比较 Bio-PdNPs-0中髌骨细菌门、绿弯菌门、拟杆菌门的相对丰度为26.78%、12.57%、10.20% 这些微生物在Bio-PdNPs-5中的相对丰度分别提高至27.78%、13.23%和10.46%,说明其占比在负载钯后略有提高,而变形杆菌门Bio-PdNPs-0的28.60% 降至Bio-PdNPs-5的25.54%,略有降低。此外,在2反应体系中均检测到互养菌门(Synergistetes),其对蛋白质和氨基酸的降解具有重要的作用,在厌氧消化体系中是种间电子传递的主要菌种之一。厚壁菌门(Firmicutes)和放线菌门(Actinobacteria)也在2反硝化体系中均有检测到,并且其在Bio-PdNPs-5中的占比(7.51%、4.01%)均高于Bio-PdNPs-0(6.55%、3.35%)。有研究[22]表明,厚壁菌门和放线菌门与发酵过程产酸和特定有机物降解有关。
科水平的微生物群落的分析结果表明,Saccharimonadales、肠杆菌科(Enterobacteriaceae)和厌氧绳菌科(Anaerolineaceae)是实验体系中的3种主要的菌科。其中Saccharimonadales与硝酸盐的还原有关[23],厌氧绳菌科在厌氧环境中分解低分子有机物,能够为反硝化菌提供必需的电子,其在Bio-PdNPs-5(22.85%、9.80%)的反硝化体系中的占比均高于Bio-PdNPs-0(21.42%、9.60%)。此外,可以还原钯的红环菌科(Rhodocyclaceae) [24]在2个反应体系中均有检测到,且其在Bio-PdNPs-5(1.52%)中的占比高于Bio-PdNPs-0(1.46%)。具有种间电子传递能力,且负责乙酸氧化、氨基酸发酵功能的互营乙酸氧化菌(Synergistaceae)[25]也在Bio-PdNPs-0(7.53%)和Bio-PdNPs-5(7.30%)中检测到。
值得注意的是,与短链高丝氨酸内酯类(AHL)信号分子相关的肠杆菌科、厌氧绳菌科和互营乙酸氧化菌[26-27]在负载Bio-PdNPs后或者减少或者几乎没有变化,表明某些QS信号分子可能对反硝化产生了负面影响。据TOYOFUKU等[19]研究表明,QS信号分子可以抑制铜绿假单胞菌(Pseudomonas aeruginosa PAO1)反硝化基因(nark1、nirS、norC)的启动子。此外,Bio-PdNPs-5中还检测到其他与QS相关的细菌,如暖绳菌科(Caldilineaceae)、红杆菌科(Rhodobacteraceae),群体感应淬灭(QQ)相关的黄杆菌科(Flavobacteriaceae),尽管他们的比例较低(< 1%),但在生物代谢和种间信息“交流”过程中的作用不容忽视。
-
1)反硝化活性污泥负载Bio-Pd0后,微生物代谢活性提高,反硝化酶Nar、Nir、Nor和Nos对电子的消耗速率分别提高了50.35%、63.38%、63.38%、70.92%,并且Bio-Pd0减少了反硝化副产物如亚硝酸盐和N2O的积累。
2)香兰素对生物反硝化的抑制作用表明Bio-Pd0在该反硝化过程中具有重要的非生物催化作用。
3)负载钯影响了与QS和QQ有关的群落结构,并且通过添加群体感应淬灭剂猪肾酰化酶可以进一步调控生物反硝化能力,这为强化污水脱氮提供新策略和新视角。
生物钯强化反硝化及群体感应调控
Biosynthetic palladium enhancing denitrification and quorum sensing regulation
-
摘要: 水体氮素污染对生态环境和人类健康具有严重的威胁,因此,探索高效的污水脱氮方法成为水处理领域高度关注的焦点。本研究利用厌氧活性污泥原位合成零价钯(Bio-Pd0),探究了钯负载量对反硝化效果的影响。结果显示,负载适量的钯可以加快反硝化酶对电子的利用速率,从而减少亚硝酸盐和N2O的积累,使硝酸盐的去除率提高了38.54%,而过量的钯负载会抑制生物反硝化效率。从微生物代谢和群体感应两方面进行了机理分析,结果表明,负载适量的钯能够促进微生物的代谢,从而提高对有机物的利用效率。并且添加0.2 g·L−1群感抑制剂(QSI)猪肾酰化酶能进一步强化生物反硝化效果。本研究结果对改善污水脱氮效率具有重要的参考价值。Abstract: Nitrogen pollution in waterbody posed a serious threat to eco-environment and human health. Therefore, to explore efficient denitrification methods has become a focus in the field of water treatment. In this study, zero-valent palladium (Bio-Pd0) was in-situ synthesized by anaerobic sludge, and the effect of palladium loading on denitrification was investigated. The results showed that an appropriate amount of palladium loading could accelerate the electron utilization efficiency, reduce the accumulation of nitrite and N2O, and increase the nitrate removal rate by 38.54%, while denitrification was inhibited with excessive palladium. The mechanism was analyzed from the aspects of microbial metabolism and quorum sensing. The results showed that an appropriate amount of palladium loading could promote the metabolic capacity of microorganisms and increase the organic utilization rate. Moreover, the addition of 0.2 g·L−1 group sensing inhibitor (QSI) porcine kidney acylase could further enhance the biological denitrification effect. The results of this study have an important reference for improving the denitrification effect of sewage.
-
Key words:
- biosynthetic palladium /
- denitrification /
- quorum sensing /
- microbial community structure
-

-
-
[1] LIU S, WANG C, HOU J, et al. Effects of Ag and Ag2S nanoparticles on denitrification in sediments[J]. Water Research, 2018, 137: 28-36. doi: 10.1016/j.watres.2018.02.067 [2] LIU Y, WANG J. Reduction of nitrate by zero valent iron (ZVI)-based materials: A review[J]. Science of the Total Environment, 2019, 671: 388-403. doi: 10.1016/j.scitotenv.2019.03.317 [3] LI J, PENG Z, HU R, et al. Micro-graphite particles accelerate denitrification in biological treatment systems[J]. Bioresource Technology, 2020, 308: 122935. doi: 10.1016/j.biortech.2020.122935 [4] ZHANG Y, LU C, ChEN Z, et al. Multifaceted synergistic electron transfer mechanism for enhancing denitrification by clay minerals[J]. Science of the Total Environment, 2021, 812: 152222. [5] CHEN X, FENG Q, CAI Q, et al. Mn3O4 nanozyme coating accelerates nitrate reduction and decreases N2O emission during photoelectrotrophic denitrification by thiobacillus denitrificans-CdS[J]. Environmental Science & Technology, 2020, 54(17): 10820-30. [6] BI S, LIU H, ChEN Y, et al. Promoting interspecies hydrogen/electron transfer in Bio-PdNPs-mediated denitrification with the selectivity towards N2[J]. Biochemical Engineering Journal, 2022, 181: 108395. doi: 10.1016/j.bej.2022.108395 [7] 唐鹏. 基于群体感应效应的 Anammox-AGS 工艺特性及调控研究[D]. 青岛: 青岛大学, 2020. [8] 朱子倩. 群体感应系统调控异养硝化好氧反硝化机制研究[D]. 哈尔滨: 哈尔滨工业大学, 2019. [9] ZHAO Z, XIE G, LIU B, et al. A review of quorum sensing improving partial nitritation-anammox process: Functions, mechanisms and prospects[J]. Science of the Total Environment, 2021, 765: 142703. doi: 10.1016/j.scitotenv.2020.142703 [10] LI N, WANG L, YAN H, et al. Effects of low-level engineered nanoparticles on the quorum sensing of Pseudomonas aeruginosa PAO1[J]. Environmental Science and Pollution Research International, 2018, 25(7): 7049-58. doi: 10.1007/s11356-017-0947-5 [11] OUYANG K, MORTIMER M, HOLDEN P A, et al. Towards a better understanding of Pseudomonas putida biofilm formation in the presence of ZnO nanoparticles (NPs): Role of NP concentration[J]. Environment International, 2020, 137: 105485. doi: 10.1016/j.envint.2020.105485 [12] OBEROI A S, HUANG H, KHANNAL S K, et al. Electron distribution in sulfur-driven autotrophic denitrification under different electron donor and acceptor feeding schemes[J]. Chemical Engineering Journal, 2021: 404. [13] LV Y, LI L, CHEN Y, et al. Effects of glucose and biphenyl on aerobic cometabolism of polybrominated diphenyl ethers by Pseudomonas putida: Kinetics and degradation mechanism[J]. International Biodeterior & Biodegrad, 2016, 108: 76-84. [14] 万鹏亮. 某城市污水厂A~2O工艺沿程水质特征分析与提质增效方案研究[D]. 西安: 西安理工大学, 2021. [15] 王共磊. 异养-自养混合式部分ANAMMOX系统同步脱氮除碳效能研究[D]. 太原: 太原理工大学, 2020. [16] SHI H X, WANG J, LIU S Y, et al. New insight into filamentous sludge bulking: Potential role of AHL-mediated quorum sensing in deteriorating sludge floc stability and structure[J]. Water Research, 2022, 212: 118096. doi: 10.1016/j.watres.2022.118096 [17] SHIN H, PARK C, LEE C K, et al. Mitigating biofouling with a vanillin coating on thin film composite reverse osmosis membranes[J]. Environmental Science And Pollution Research, 2020, 27(2): 1677-85. doi: 10.1007/s11356-019-06653-2 [18] CHENG Y, ZHANG Y, SHEN Q, et al. Effects of exogenous short-chain N-acyl homoserine lactone on denitrifying process of Paracoccus denitrificans[J]. Journal of Environmental Science-China, 2017, 54: 33-9. doi: 10.1016/j.jes.2016.05.019 [19] TOYOFUKU M, NOMURA N, FUJII T, et al. Quorum sensing regulates denitrification in Pseudomonas aeruginosa PAO1[J]. Journal of Bacteriology, 2007, 189(13): 4969-72. doi: 10.1128/JB.00289-07 [20] TOYOFUKU M, NOMURA N, KUNO E, et al. Influence of the Pseudomonas quinolone signal on denitrification in Pseudomonas aeruginosa[J]. Journal of Bacteriology, 2008, 190(24): 7947-56. doi: 10.1128/JB.00968-08 [21] LEI X, JIA Y, CHEN Y, et al. Simultaneous nitrification and denitrification without nitrite accumulation by a novel isolated Ochrobactrum anthropic LJ81[J]. Bioresource Technology, 2019: 272. [22] GUO F, LIU H. Impact of heterotrophic denitrification on BOD detection of the nitrate-containing wastewater using microbial fuel cell-based biosensors[J]. Chemical Engineering Journal, 2020: 394. [23] SHI L, ZHANG P, HE Y, et al. Enantioselective effects of cyflumetofen on microbial community and related nitrogen cycle gene function in acid-soil[J]. Science of the Total Environment, 2021, 771: 144831. doi: 10.1016/j.scitotenv.2020.144831 [24] ZHOU C, Ontiveros-Valencia A, Wang Z, et al. Palladium recovery in a H2-based membrane biofilm reactor: Formation of Pd(0) nanoparticles through enzymatic and autocatalytic reductions[J]. Environmental Science & Technology, 2016, 50(5): 2546-55. [25] ZHU X, CAMPANARO S, TREU L, et al. Novel ecological insights and functional roles during anaerobic digestion of saccharides unveiled by genome-centric metagenomics[J]. Water Research, 2019, 151: 271-9. doi: 10.1016/j.watres.2018.12.041 [26] MADDELA N R, SHENG B, YUAN S, et al. Roles of quorum sensing in biological wastewater treatment: A critical review[J]. Chemosphere, 2019, 221: 616-29. doi: 10.1016/j.chemosphere.2019.01.064 [27] MARTINS M L, PINTO U M, RIEDEL K, et al. Quorum sensing and spoilage potential of psychrotrophic enterobacteriaceae isolated from milk J][J]. Biomed Research International, 2018, 2018: 2723157. -




 下载:
下载: