-
赋存于泥页岩中以自生自储成藏的页岩气资源的大规模开采改变了全球能源结构。我国页岩气资源潜力巨大,开发页岩气对提高能源安全、促进能源结构调整、改善大气环境质量具有重要意义,并在过去十年已经取得巨大进展[1]。水力压裂技术通过将压裂液(组成为90%的水、9%的支撑剂和1%的化学添加剂)注入地层,在高压作用下使岩石产生裂缝,从而增加页岩储集层的渗透性,是页岩气开发的关键技术。但是,这些压裂液随后混合地层水返回到地面形成的页岩气返排水(包括初期返排水和后期采气水)[2]不仅含有压裂液成分,还包含原位地层盐水、页岩-水相互作用中浸出的组分、原位转化反应的产物等[3],有机成分复杂,还含有各种重金属、放射性核素等污染物,对生态环境具有潜在威胁,是页岩气开发行业最受关注的环境问题[4]。
在上述页岩气返排水污染物中,具有高生态环境风险[5]的多环芳烃(PAHs,polycyclic aromatic hydrocarbons)的普遍存在已经被确认。美国Marcellus页岩气田返排水中的PAHs主要以低分子量的萘、菲、苊、蒽和烷基化PAHs为主,也含少量的高分子量的茚、煤油和芘[6]。科罗拉多州Denver–Julesburg盆地页岩气返排水中检测到的PAHs有2-甲基萘、菲、芘,其质量浓度分别为15、3、0.9 μg·L−1[7]。加拿大Calgary页岩气田返排水样品中同样检出了三环和四环的PAHs,大部分为菲和菲的衍生物,总PAHs的最大质量浓度达到112.7 μg·L−1[8]。Duvernay页岩气田返排水中含量最高的PAHs是芴,其次是菲、萘、蒽,总PAHs质量浓度在500~1 000 ng·L−1[9]。在我国重庆涪陵页岩气田的返排水中检出了萘和芘,质量浓度分别为96.4 μg·L−1和2.4 μg·L−1[10]。PAHs是页岩气返排水中普遍存在的污染物,具有显著的生态环境风险和健康隐患。因此,高效地处理PAHs是实现页岩气绿色安全开发的必然要求。
生物处理具有环境友好和低成本优势,也是PAHs去除的重要方法之一。在PAHs好氧生物降解过程中,氧作为最终电子受体,也作为羟基化和氧介导的芳烃环裂解的共底物[11],加氧酶能将氧原子加到C—C键上形成C—O键,随后再通过加氢、脱水等作用使C—C键断裂,裂解苯环[12],最终形成水杨酸、邻苯二甲酸等小分子中间体,然后进入三羧酸循环(TCA Cycle,tricarboxylic acid cycle)。PAHs厌氧生物降解则是微生物利用NO3−、SO42-、Fe3+、Mn4+等作为电子受体降解PAHs[13]。以萘的降解为例,萘通过羧化生成2-萘酸后活化成2-萘酰基辅酶A,通过还原逐步开环裂解[14]。好氧颗粒污泥(AGS,aerobic granular sludge)是近年来受到广泛关注的一项新兴生物处理技术。AGS是微生物通过自凝聚作用形成的聚集体,具有好氧、兼氧和厌氧层的特殊三维结构。这种结构不仅具有较大的生物量和良好的沉降性能,还具备抗冲击负荷、耐毒性和强吸附力等特点,在处理有毒和难降解污染物方面表现出明显的优势[15-18]。由于AGS同时存在着厌氧/好氧的分区,使得其对PAHs的生物降解存在好氧/厌氧两条途径的综合作用,有助于提高对PAHs的去除效果。在本课题组前期的研究中,已经成功培养并驯化了用于处理页岩气返排水的AGS系统[19],其对返排水中的有机物:总有机碳(TOC,total organic carbon)和化学需氧量(COD,chemical oxygen demand)显示出良好的去除效果[20]。但是,关于返排水中的PAHs在该AGS返排水处理系统中的去除效果和过程机制尚不明确,PAHs本身具有较强的生物毒性,其在AGS系统处理过程中所具有的毒性的变化尚不清晰。
本研究从环境健康角度关注废水处理过程的新污染物PAHs,以页岩气返排水中普遍检出的PAHs的典型物种萘和菲为研究对象,考察了AGS对返排水中的典型PAHs萘和菲的去除效果及生物毒性的变化,揭示萘和菲在该处理过程中的行为特征及去除与毒性变化机制,旨在为AGS技术在页岩气返排水处理中的应用与优化,尤其是高风险新污染物的去除,提供理论指导与技术参考。
-
本研究所用的具有返排水处理能力的AGS取自能稳定处理实际页岩气返排水的实验室AGS反应器,COD去除率稳定在78%~82%。污泥表面为浅黄色,呈球形或椭球形,粒径平均在1.5~2 mm,沉降性能良好,污泥体积指数(SVI,sludge volume index)为31 mL·g−1[21],AGS运行装置、形貌如图1所示。
为了更有效地研究AGS系统对页岩气返排水中典型PAHs的去除效果,本实验选取萘和菲作为研究对象,并设置合成废水中PAHs的质量浓度为30 mg·L−1,以便更明显地观察实验结果。另外,基质中添加1‰微量元素(50 mg·L−1 H3BO3、50 mg·L−1 CoCl2·6H2O、30 mg·L−1 CuCl2、50 mg·L−1 AlCl3、30 mg·L−1 KI、50 mg·L−1 MnSO4、60 mg·L−1 Na2MoO4·2H2O、50 mg·L−1 ZnCl2、50 mg·L−1 NiCl2),维持NaCl质量浓度为10 000 mg·L−1 (与AGS页岩气返排水处理系统保持一致)。实验采用与实际返排水处理系统相同的序批式反应器(SBR,sequencing batch reactor)运行,其中进水20 min,曝气210 min,沉淀5 min,出水5 min,出水交换比80%,水力停留时间(hydraulic retention time,HRT)为300 min。实验过程中控制反应器温度始终维持在25 ℃,pH=7~7.5。
-
从处理页岩气返排水的反应器中取适量的AGS,经过3次纯水洗涤后,置于1%叠氮化钠溶液中灭活1 h;将处理后的AGS置于250 mL锥形瓶中,之后进行PAHs的吸附热力学实验。分别加入灭活污泥和不同质量浓度PAHs的自配水置于恒温振荡培养箱中,反应温度为25 ℃,振荡速度为50 r·min−1。在0、20、60、120、180、240、480、720和1 440 min时取样,测定溶液中PAHs质量浓度,并进行吸附动力学和吸附热力学模型的数学拟合。PAHs吸附量根据式(1)计算。为描述吸附过程中的物理和化学机制,评估和解释吸附剂对吸附质的吸附过程,使用Langmuir(式(2))、Freundlich(式(3))、Temkin(式(4))等温吸附模型对实验结果进行拟合。
式中:Q为PAHs的吸附量,mg·g−1;C0为PAHs的初始质量浓度,mg·L−1;Ct为t时刻PAHs的质量浓度,mg·L−1;CMLSS为污泥质量浓度,g·L−1。
式中:Ce为吸附平衡时PAHs质量浓度,mg·L−1;qe为平衡吸附量,mg·g−1;qm为饱和吸附量,mg·g−1;KL为吸附常数,与键合位点的亲和力及吸附能有关,mg·g−1;KF为Freundlich吸附常数,与吸附容量和强度有关,(mg1-nLn)g−1;1/n为是吸附强度或表面异质性的指标;Kt为平衡常数,L·g−1,体现了吸附剂对吸附质的亲和力;F为与吸附热相关的常数,J·mol−1。
为了评估在吸附过程中的扩散和吸附位点的可用性限制,了解控制吸附过程的主要因素,采用准一级动力学(式(5))、准二级动力学(式(6))、颗粒内扩散(式(7))模型进行动力学拟合:
式中:t为吸附时间,min;qe为平衡吸附量,mg·g−1;qt为t时刻吸附量,mg·g−1;k1是准一级吸附速率常数,min−1;k2为准二级吸附速率常数,g·(mg·min)−1;ki为颗粒内部扩散速率常数min0.5·mg·g−1;C为边界层厚度。
-
在研究AGS系统去除PAHs的机制时,主要关注以下三种去除路径:挥发、生物吸附和生物降解。为了量化PAHs的吹脱贡献,设计了无AGS的对照反应器,通过专门实验测定相同浓度下PAHs的吹脱损失。去除途径贡献量按照式(8)进行计算。
式中:D为生物降解量,mg·g−1;R为总去除量,mg·g−1;B为吹脱量,mg·g−1;A为吸附量,mg·g−1。
-
1)多环芳烃含量测定。采用液液萃取高效液相色谱法测定水质中PAHs含量[22]。样品处理步骤为:从反应器取1 mL样品加入1 mL甲醇的离心管中,经20 min涡旋振荡后,通过0.22 μm尼龙滤头过滤至2 mL色谱瓶。使用高效液相色谱仪(Agilent
1260 ,HPLC,America),配SB-C18色谱柱和二极阵列检测器进行测定。测定方法如下:萘:流动相20%水+80%甲醇,流速1 mL·min−1,检测波长223 nm,进样量10 μL,运行5 min。菲:流动相25%水+75%甲醇,流速1 mL·min−1,检测波长254 nm,进样量20 μL,运行13 min。2)傅里叶红外光谱分析.。取吸附PAHs前后的AGS入冷冻干燥箱干燥12 h,将干燥后的污泥样品置于玛瑙研钵中,加入溴化钾粉末研磨,压片后用傅里叶红外光谱仪(Thermo Nicolet iS5,FTIR,America)扫描。
3)生物毒性分析。采用基于发光细菌(Vibrio fischeri)的毒性测试仪(Deltatox II,England)进行毒性测试。发光细菌复苏后,用稀释液(2% NaCl溶液)稀释至40 mL作为测试使用。测试管A加入1 mL水样和100 μL缓冲液(22% NaCl溶液);测试管B加入100 μL发光细菌使用液。读数后,将A中900 μL溶液转至B,反应5 min后再检测,记录抑制度。
4)多环芳烃降解中间产物分析。从反应器中取10 mL样品,用0.22 μm尼龙滤膜过滤,并加入1 M HCl调整pH至2。然后加入等体积的二氯甲烷,充分振荡后分离两相,加入无水硫酸钠去除水分,静置后过滤。通过旋转蒸发仪将样品浓缩至1 mL,并转移至1.5 mL棕色进样瓶中备分析。
样品通过气相色谱-质谱联用仪(Agilent
8860 -5977B,GC-MS,America)分析。在进行生物降解中间产物的检测时,进样口的温度设定为280 °C。色谱柱(HP-5MS,30 m×0.25 mm×0.25 μm)的温度程序从40 °C开始,保持2 min,随后以5°C·min−1的速率升温至300 °C,并在300 °C下保持10 min。MS检测采用电离模式(EI+),电离能设置为70 eV,离子源温度为300 ℃。 -
1)典型多环芳烃的去除效果。为探究具有返排水处理能力的AGS对页岩气返排水中典型PAHs的去除效能,本研究在连续运行的AGS系统内投加典型PAHs萘和菲,其去除结果如图2所示。在反应器进入稳定运行状态后的整个期间内,萘的平均进水质量浓度为29.6 mg·L−1,平均出水质量浓度降至1.8 mg·L−1;菲的平均进水质量浓度为30.2 mg·L−1,平均出水质量浓度为2.6 mg·L−1。萘和菲的平均去除率分别达到了93.8%和91.3%,表明由含有返排水处理能力的AGS处理系统能够稳定有效地从水相中去除所研究的典型PAHs。AGS由于其多孔性结构,拥有极大的内表面积,对PAHs具有高度亲和性[23]。有研究表明,在AGS系统中,PAHs首先被吸附在颗粒表面,通过扩散运输通过空隙,发生生物降解[16],生物降解的能力取决于微生物的组成及其代谢特性[24]。因此,PAHs能够在进入反应器后与颗粒污泥高效接触,通过初始阶段的生物吸附作用表现出从水相中的快速去除,也可能为后续通过生物转化和彻底降解彻底有效去除奠定基础。
2)好氧颗粒污泥对典型多环芳烃的吸附过程。根据已有认识,吸附是AGS系统去除PAHs的首要步骤。为了认识上述具有返排水处理能力的AGS去除典型PHAs的过程特征,本节通过实验专门探究了该AGS在上述反应系统中对萘和菲的吸附特征。
吸附等温线分析可以揭示在一定温度条件下,当吸附到达平衡状态时,吸附质在吸附剂与溶液之间的浓度关系。本研究采用Langmuir、Freundlich和Temkin模型评估具有页岩气返排水处理能力AGS对萘和菲的吸附特性。Langmuir模型假设生物吸附表面是均匀的且各分子互不干扰,理论上来说单分子层吸附可以使吸附位点都达到饱和状态[25]。Freundlich模型描述在非均匀表面上的多层吸附过程,表面存在的官能团可以作为天然配体来源提供结合位点[26]。Temkin模型考虑了在非理想条件下吸附剂和吸附质之间的相互作用,用于描述静电力存在下的化学吸附过程[27]。
通过以上3种吸附等温线模型分别考察该反应系统中的单分子层吸附、多分子层吸附以及在静电力影响下的化学吸附。在污染物初始质量浓度为5、10、15、20、30、50 mg·L−1下的吸附过程及模型拟合结果如表1和图3所示。由表1可见,随着PAHs初始质量浓度的增加,该种特殊的AGS的平衡吸附量也增加,但增速减慢,表明该AGS表面的有效吸附位逐渐接近饱和;在50 mg·L−1的萘和菲质量浓度下,最终平衡吸附量分别为16.7 mg·g−1和19.2 mg·g−1。萘和菲在该AGS上的饱和吸附量分别为21.53 mg·g−1和25.48 mg·g−1。对萘而言,Langmuir、Freundlich和Temkin模型吸附热力学的拟合度分别为0.96、0.97和0.93。因此,本研究中的具有返排水处理能力的AGS可能主要通过单层和双层吸附机制吸附萘,过程中还涉及静电力驱动的化学吸附。Freundlich模型中1/n=0.44(n>1),表明该AGS对萘具有较强亲和力,易于发生吸附。对菲而言,其Langmuir、Freundlich和Temkin模型的拟合度分别为0.96、0.87和0.97,表明该AGS对菲的吸附主要遵循Temkin和Langmuir模型,吸附过程伴随着复杂的能量交换和相互作用,并伴有单分子层吸附。Temkin模型参数Kt=6.0和f=2.72证明了在吸附初期存在强烈的相互作用,随着表面活性位的饱和,该AGS对菲的亲和力降低[28]。综上所述,虽然颗粒污泥,包括本研究中的具有返排水处理能力的AGS在短时间内易于快速吸附PAHs,但由于总体吸附容量有限,存在吸附饱和,难以支撑长期稳定运行的AGS系统中PAHs的稳定有效的彻底去除。
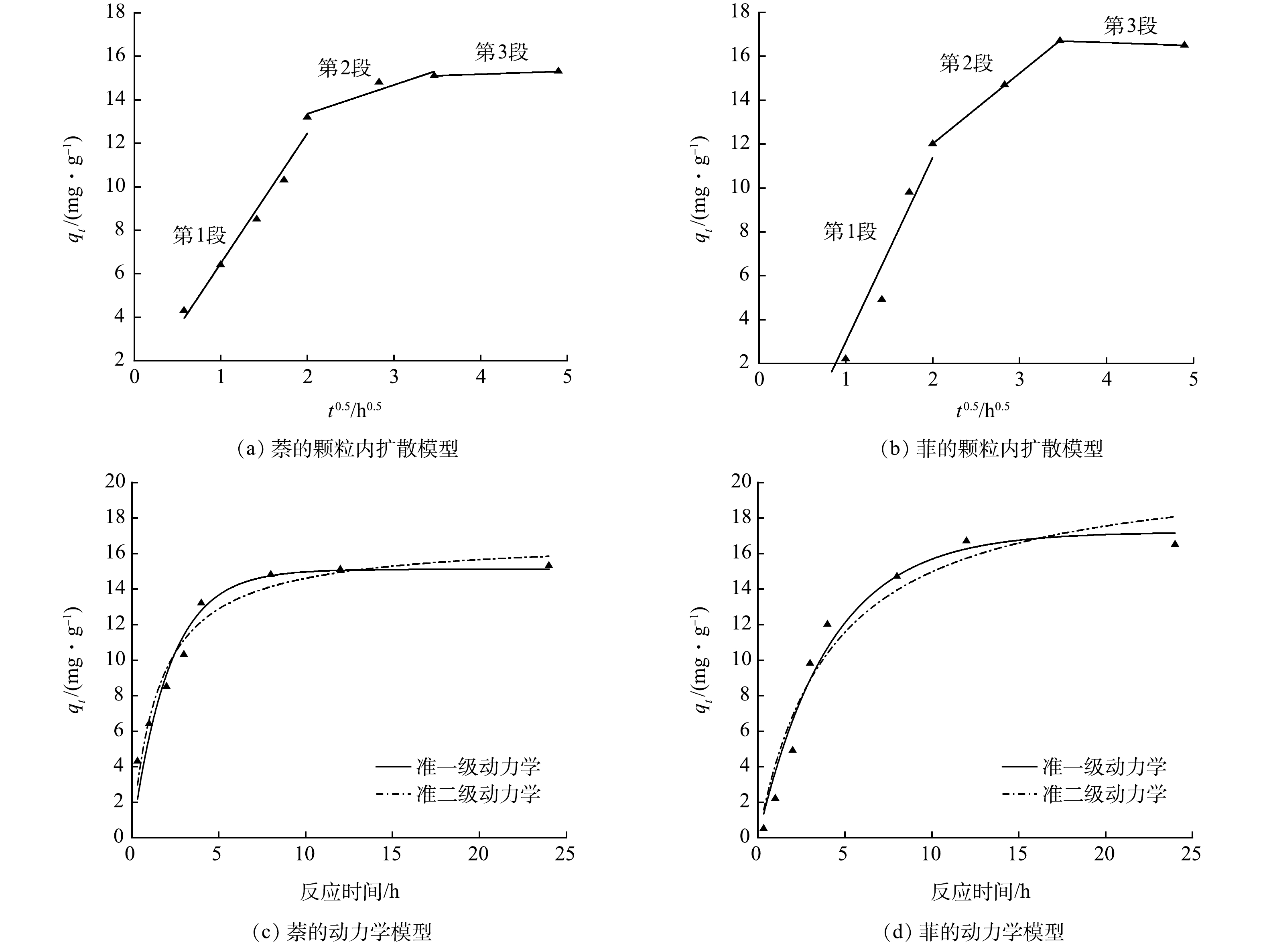
为探究具有返排水处理能力的AGS对PAHs的吸附过程的动力学机理,本研究进一步分别采用颗粒内扩散模型及准一级反应动力学模型、准二级反应动力学模型分析该AGS对萘和菲的吸附行为。颗粒内扩散模型是用于描述颗粒内部传质过程的模型,可用来分析反应中的控制步骤[29]。准一级动力学吸附速率模型是基于表面上存在的活性位点,吸附速率与活性位点的表面浓度成正比,吸附剂与吸附质之间通过物理作用力吸附[30]。准二级动力学模型假设吸附受化学吸附的影响,涉及到吸附剂和吸附之间的电子共享或转移[31]。
拟合结果如图4和表2所示。对萘而言,准一级动力学和准二级动力学模型的R2分别为0.95和0.94,说明该AGS对萘的吸附过程为物理和化学吸附的综合机制。对菲的吸附,准一级动力学和准二级动力学模型的R2分别为0.97和0.94,相较于准二级动力学模型,准一级动力学模型可能能够更准确地描述AGS对菲的吸附过程;菲的吸附过程主要以化学吸附为主,即吸附速率依赖于吸附位点的占据程度以及吸附质在吸附剂表面的浓度。图4(a)和图4(b)分别为萘和菲的颗粒内扩散模型。颗粒内扩散模型主要用于识别吸附过程中的速率控制步骤,包括吸附剂从溶液中移动到吸附剂表面,穿透吸附剂外层,进入其内部孔隙的多阶段运输[32]。在萘和菲的吸附过程中,颗粒内扩散模型均呈三段线性关系,且没有经过原点。这说明在该具有页岩气返排水处理能力的AGS吸附萘和菲的过程中,第一阶段是PAHs通过边界层扩散过水膜,第二阶段是PAHs在AGS内继续扩散,第三阶段是PAHs在颗粒内表面进行吸附,限速吸附步骤同时由膜扩散和颗粒内扩散共同控制。
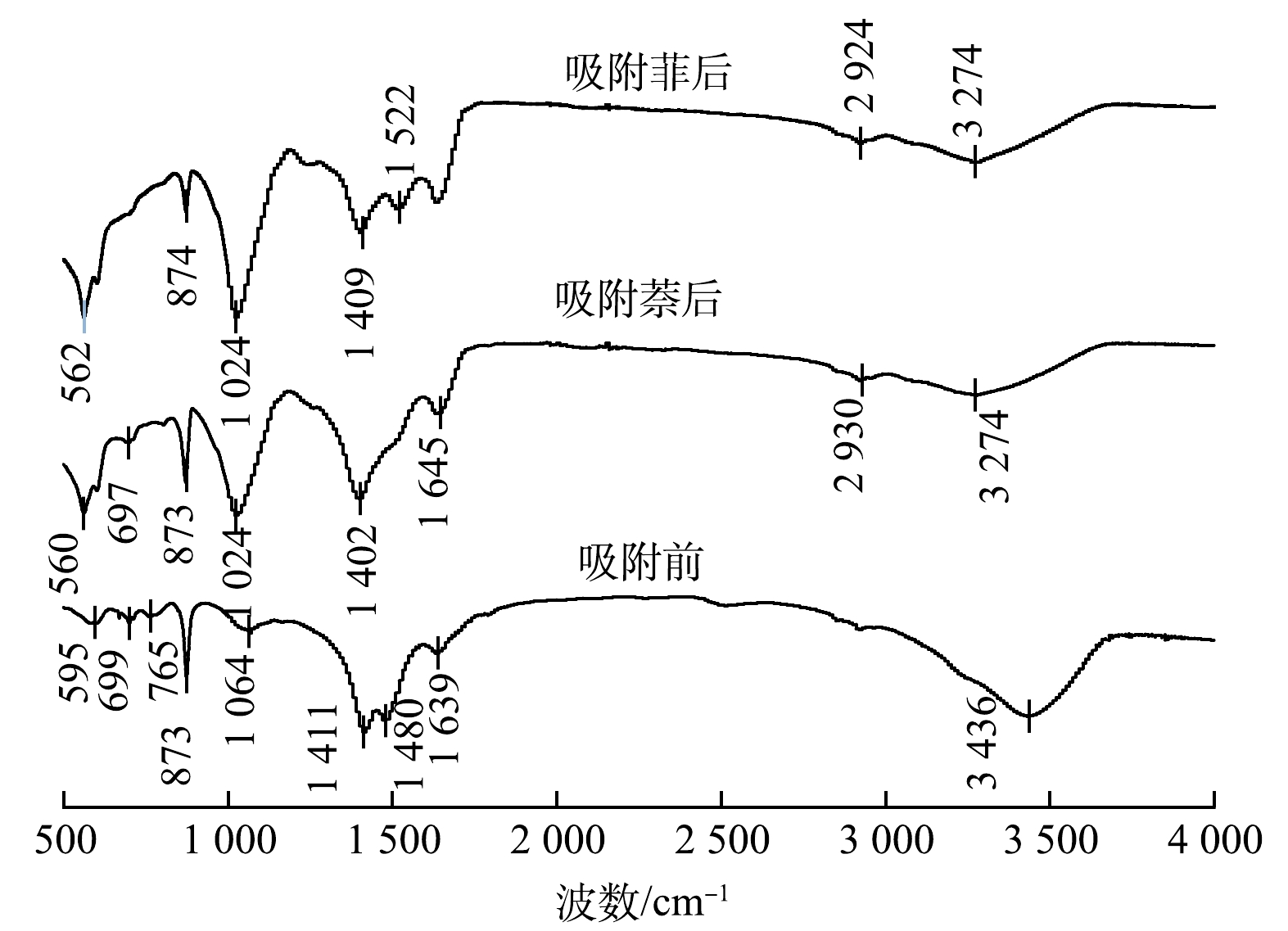
图5反映了AGS吸附典型PAHs萘和菲前后AGS表面官能团的变化。吸附前后AGS表面的各官能团位置和形状均发生明显改变。由图5可见,萘的吸附导致O—H伸缩振动吸收峰由3 236 cm−1移至3 274 cm−1,吸收峰的红移暗示富含—OH的多糖可能在吸附过程中起作用。(酰胺I带)C=O的伸缩振动吸收峰从1 639 cm−1处向高频移动到了1 645 cm−1处,(酰胺Ⅲ带),C—N吸收峰从1 411 cm−1移动到了1 402 cm−1,说明萘的吸附与蛋白质中的C=O键和C—N键相关[33],酰胺键的伸缩振动变化指示了蛋白质分子结构在萘吸附后发生了调整,推测蛋白质与萘分子间形成了非共价相互作用,如氢键或范德华力。C—O伸缩振动峰在1 024 cm−1处的明显增强,因此,多糖中的C—O—C基团可能参与了吸附反应[34]。
比较菲吸附前后的红外谱图,同样观察到3 236 cm−1处的吸收峰移动到了3 274 cm−1处,可能归因于该AGS表面的-OH基团对菲的吸附作用,(酰胺I带)C=O的伸缩振动吸收峰从1 639 cm−1处移动到了1 636 cm−1处,(酰胺Ⅲ带) C-N吸收峰是1 411 cm−1移动到了1 409 cm−1,1 522 cm−1处的吸收峰是(酰胺Ⅱ带) N-H的弯曲振动,相比吸附萘,吸附菲后N-H峰明显增强,可能是由于蛋白质中C=O结合—NH和—CN弯曲振动所引起的,菲的吸附增强了蛋白质分子间的氢键网络。1 024 cm−1处的C-O吸收峰强度明显高于其他两个,说明吸附菲后C-O键增加的最多。胞外聚合物中多糖的C-O-C键在菲的吸附中起重要作用。
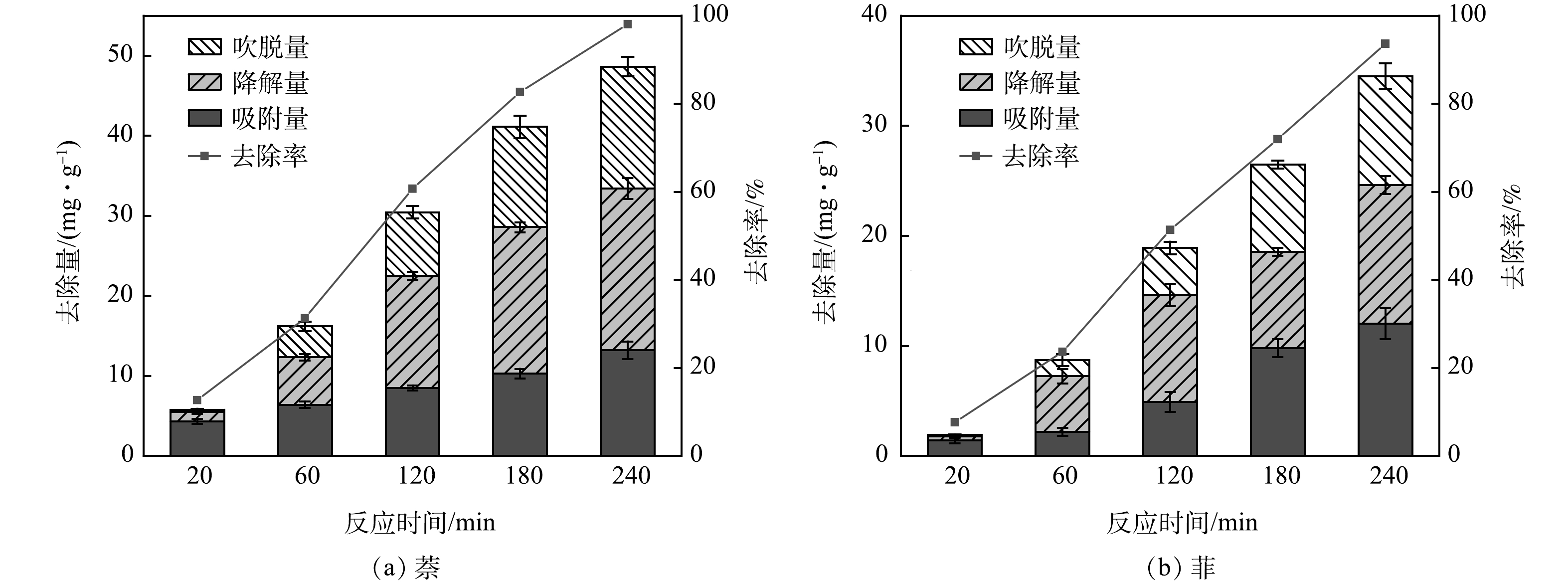
3)不同途径对典型多环芳烃的去除贡献。吸附、降解与吹脱是AGS系统对PAHs的主要去除路径,在单个周期内三种途径的贡献比率如图6所示。在基于具有返排水处理能力的AGS的反应器不同运行阶段,吸附、降解与吹脱在典型PAHs萘和菲的去除中所发挥的作用存在差异。在厌氧进水段,初期吸附为萘和菲主要的去除途径,对厌氧段萘和菲去除量贡献率为76.8%和73.7%,生物降解对萘和菲的去除贡献率分别为23.2%和26.7%。然而,在后续的好氧曝气阶段,该AGS的PAHs去除中吸附贡献率持续降低,生物降解与曝气吹脱的贡献率逐步提升。直至结束时,萘和菲的去除中吸附贡献率降至30.5%和34.8%,而生物降解贡献率则升至46.7%和36.6%,其成为最主要的去除途径。
从对AGS吸附动力学与热力学的拟合结果可以看出,该AGS对于萘和菲的吸附量有限,易达到吸附饱和,而AGS反应器完整运行1个周期的吸附贡献也进一步佐证了这一点。故在1个长期稳定运行的AGS返排水处理系统中,PAHs吸附主要发生在初始的周期内,而在后续的运行过程中,AGS系统对于PAHs的去除主要依赖生物降解。长期运行的基于该AGS的系统中典型PAHs降解与吹脱途径的贡献占比如图7所示。可见,萘和菲的降解去除贡献率分别为64.1%和72.2%,吹脱量去除贡献率分别为35.9%和27.8%,进一步证明了AGS系统中的具有返排水处理能力的AGS中的微生物群落具有较高的生物活性,能够有效地降解PAHs。AGS系统通过吹脱、吸附和生物降解等多重机制共同作用,实现了PAHs的高效去除,其中生物降解作为核心去除机制,对于PAHs的长期彻底去除起到了决定性作用。
-
为探究典型PAHs萘和菲的急性生物毒性特征,本研究采用了发光细菌法进行评估。图8反映了在具有返排水处理能力的AGS处理含萘和菲的合成废水过程中,不同处理时间下废水中萘和菲诱发的急性生物毒性的变化。结果表明,在1个运行处理周期内,含萘和菲的废水毒性总体都呈现出显著的下降趋势。在30 mg·L−1的初始质量浓度下,萘对发光细菌的初始抑制率为76%,并在经历厌氧段后提升至93%,但是在进入好氧段后,萘所诱导的废水生物毒性逐渐降低,直至反应结束,反应器排水对发光细菌的抑制率仅为1%。上述现象可能是因为在厌氧降解的早期阶段产生了比萘本身毒性更强的代谢产物。有研究表明,在降解过程中,会生成PAHs的羟基化衍生物,如酮类化合物。这些羟基化PAHs已经被证明比其母体的毒性更强[35]。因此在本研究的AGS反应器运行初期,可能由于这些毒性中间产物的生成而导致废水生物毒性的上升,随着进入好氧段,这些有毒代谢物被进一步分解乃至矿化,使得最终处理出水的毒性显著下降。对于菲而言,从初始进水至反应系统运行的前120 min内,对发光细菌的抑制率一直接近100%。虽然菲在降解过程中也会产生有毒的中间产物,但由于其本身毒性较高,导致抑制率接近最大值100%,因此在厌氧段未检测到毒性变化。但随着菲及其中间产物在好氧段的进一步转化和矿化,直至160 min时反应器中的废水毒性开始快速下降,至反应结束时的排水的发光抑制率降至16%。以上结果均表明了基于具有返排水处理能力的AGS的废水处理系统对于缓解返排水中典型PAHs萘和菲的生物毒性具有明显的效果,且主要由好氧段发挥作用。
-
为进一步解析本研究中具有页岩气返排水处理能力的AGS系统中萘和菲的代谢路径与生物毒性变化的内在机制,分别对其中间产物进行了测定分析。
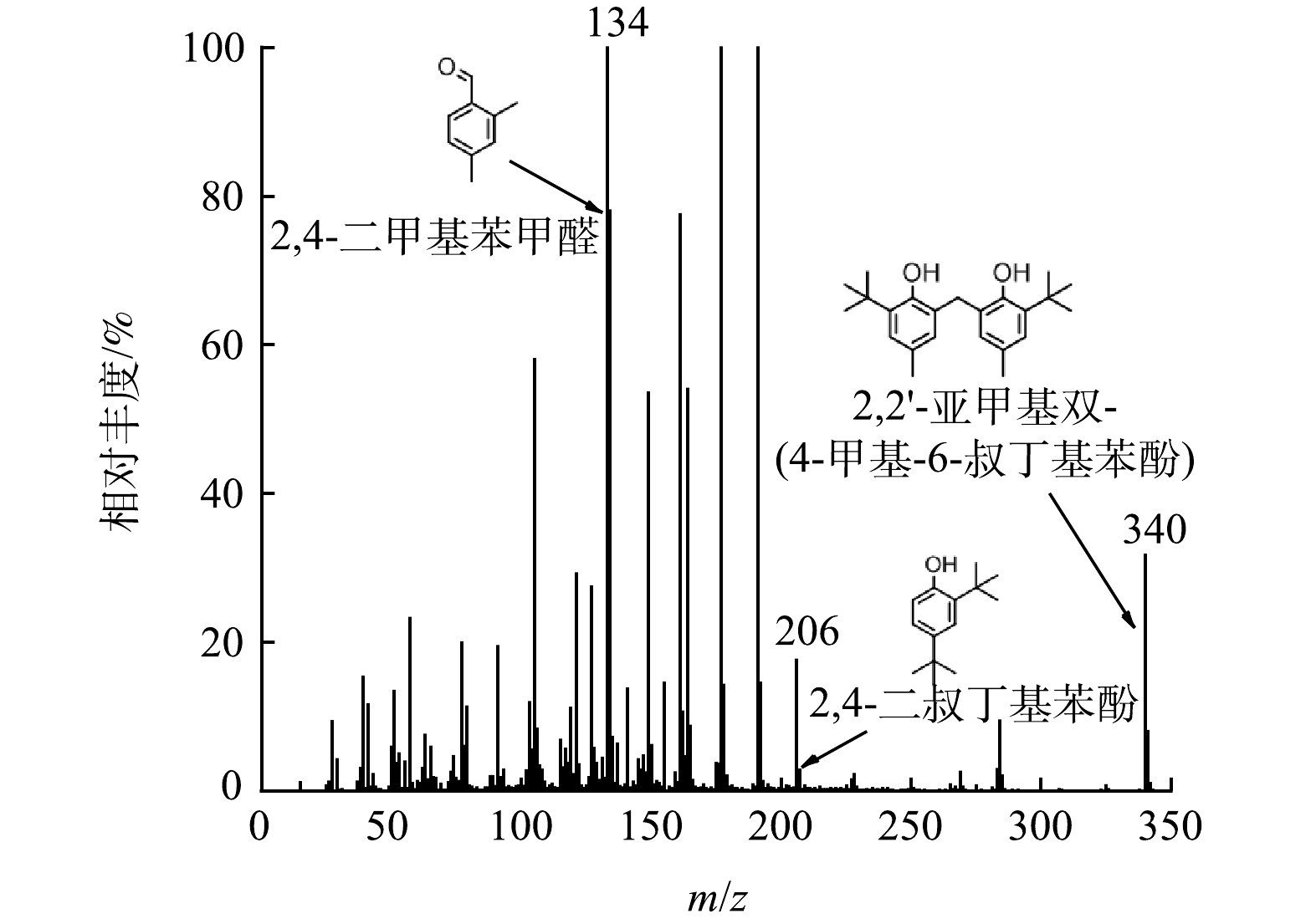
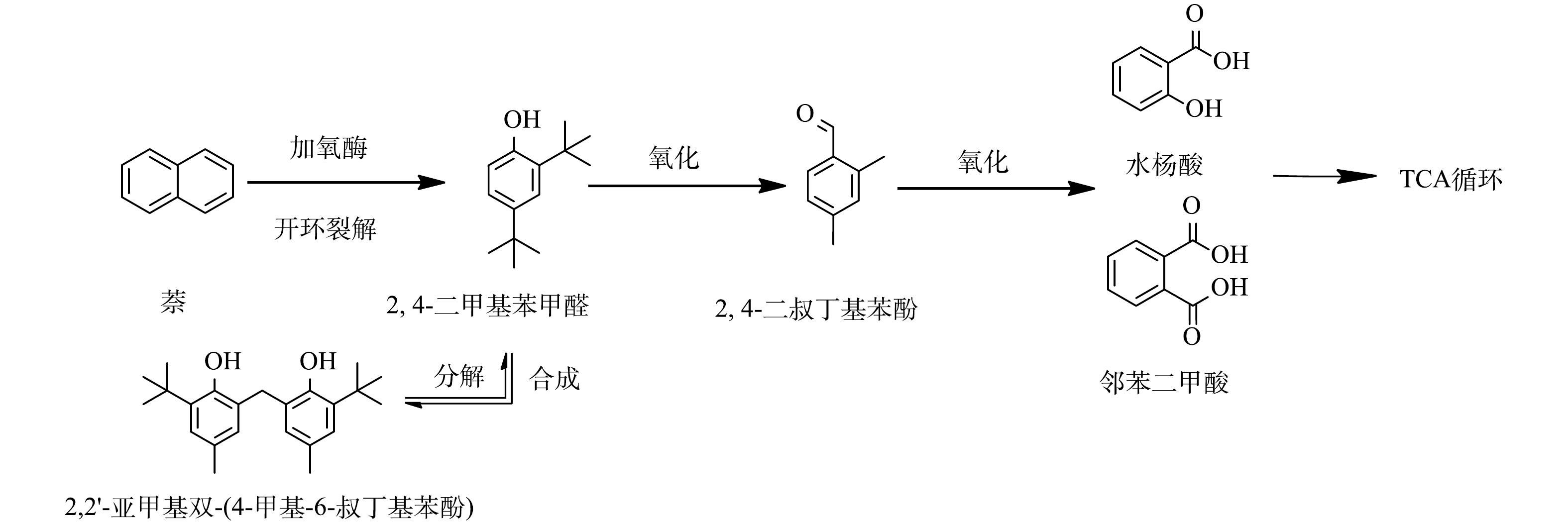
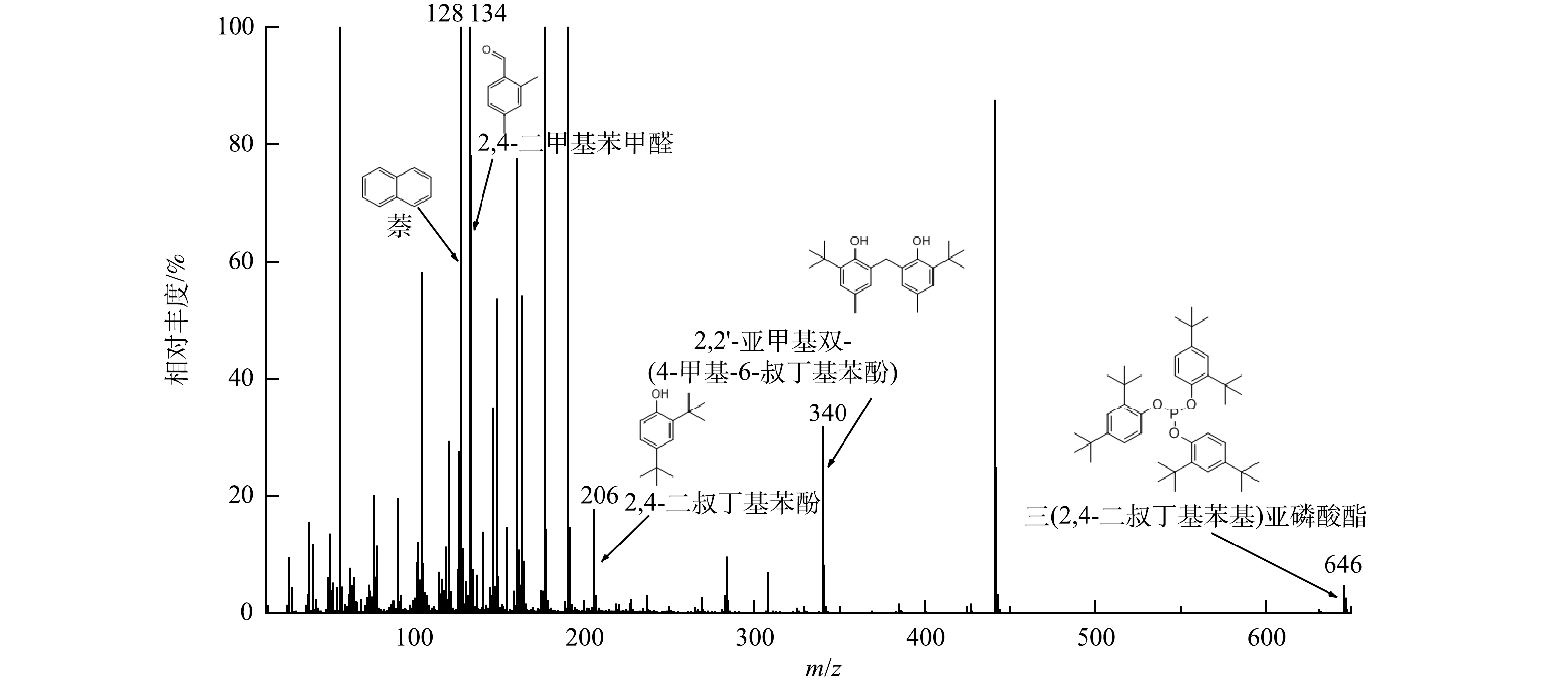
1)萘的降解路径解析。本研究基于GC-MS技术对AGS系统降解萘的中间产物进行了分析,具体质谱图和化学结构表征如图9所示。本研究的中间产物检测结果表明,萘在经历从初始反应至最终转化为水杨酸或邻苯二甲酸进入TCA循环的降解路径中,产生的中间产物有2,4-二甲基苯甲醛(2,4-dimethylbenzaldehyde)、2,4-二叔丁基苯酚(2,4-Di-t-butylphenol)、2,2'-亚甲基双-(4-甲基-6-叔丁基苯酚)(2,2'-Methylenebis(6-tert-butyl-4-methylphenol))。由降解中间产物可以推断出萘的降解路径,首先通过加氧酶催化进行芳环的羟基化反应,随后通过邻位或间位的裂解反应生成单环化合物2,4-二甲基苯甲醛,接着2,4-二甲基苯甲醛被氧化成为2,4-二叔丁基苯酚,最后2,4-二叔丁基苯酚被氧化为水杨酸或邻苯二甲酸,进入三羧酸循环(TCA 循环)[36]被进一步代谢。以往的研究表明,2,4-二叔丁基苯酚可以合成2,2'-亚甲基双-(4-甲基-6-叔丁基苯酚)[37],2,2'-亚甲基双-(4-甲基-6-叔丁基苯酚)又可以被降解为2,4-二叔丁基苯酚[38],最终被微生物完全降解。据此可以推测,萘在本研究的AGS系统中的潜在降解途径如图10所示。2.2中的毒性变化结果显示,在萘的降解过程中,毒性呈现先上升后下降的过程特征,先前的研究已经表明,萘的中间产物2,2'-亚甲基双-(4-甲基-6-叔丁基苯酚)对水蚤的半致死质量浓度(LC50)为4 mg·L−1[39],显著高于萘的毒性,这可能是导致R1中生物毒性在厌氧段上升的主要原因。
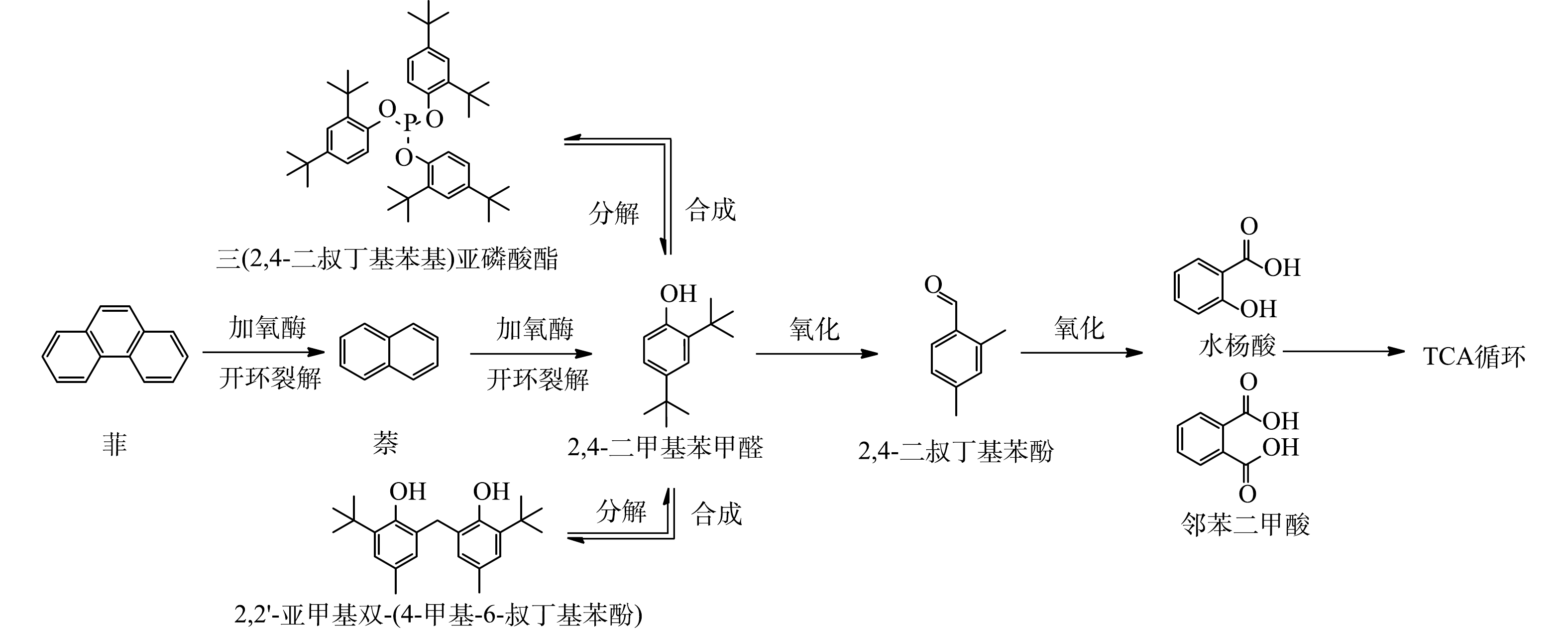
2)菲的降解路径解析。菲在本研究的AGS系统中降解的中间产物如图11所示。结果表明,相较于萘,菲的代谢途径中产物新增了萘(Naphthalene)和三(2,4-二叔丁基苯基)亚磷酸酯(Tris(2,4-ditert-butylphenyl)phosphite),这表明在降解过程中,菲可以转化为萘,萘再进一步被AGS降解,生成与2.3 1) 中类似的中间产物。AGS的结构分为外层的好氧层和内层的缺氧层,内层的缺氧层富集着聚磷菌[40],因此三(2,4-二叔丁基苯基)亚磷酸酯的生成可能是由于聚磷菌厌氧释磷后的磷酸盐与2,4-二叔丁基苯酚发生反应[41]。据此推测的菲的微生物降解路径如图12所示:当菲进入AGS系统后,能够在加氧酶的作用下发生氧化反应开环裂解形成萘,萘继续通过加氧酶氧化成为2,4-二甲基苯甲醛和2,4-二叔丁基苯酚,并合成2,2'-亚甲基双-(4-甲基-6-叔丁基苯酚)和三(2,4-二叔丁基苯基)亚磷酸酯,这些中间产物最终通过代谢途径转化为水杨酸或邻苯二甲酸,并进入TCA循环。
-
1)具有页岩气返排水处理能力的AGS长期运行中对典型PAHs具有高效稳定的去除效果,对萘和菲的去除率分别达到了93.8%和91.3%。由于AGS易达到吸附饱和,因此在长期运行过程中生物降解是主要去除路径,萘和菲的生物降解去除贡献比分别为64.1%和72.2%。伴随着反应器中萘和菲的降解,两者诱发的废水生物毒性亦得到显著缓解,且发生在好氧反应阶段。
2)具有页岩气返排水处理能力的AGS的吸附作用对典型PAHs的去除发挥了初期的短期贡献。萘的吸附遵循Freundlich和Langmuir等温线模型和准二级动力学模型,属于多分子层的化学吸附,菲的吸附遵循Temkin和Langmuir等温线模型和准一级动力学模型,吸附过程为物理吸附和静电力作用下的化学吸附,萘和菲的吸附均遵循颗粒内扩散三段式模型。傅里叶红外光谱显示,该AGS所具有的C=O、-CN、C-O-C等功能性基团可能对萘和菲的吸附发挥了关键作用,-NH基团亦对菲的吸附具有显著影响。
3)在萘和菲的降解过程中通过GC-MS检测到的降解中间产物有2,4-二甲基苯甲醛、2,4-二叔丁基苯酚、2,2'-亚甲基双-(4-甲基-6-叔丁基苯酚)、萘和三(2,4-二叔丁基苯基)亚磷酸酯。萘和菲遵循相似的降解路径:菲通过开环裂解为萘,萘进一步降解生成中间产物,最终转化为水杨酸和邻苯二甲酸,并进入三羧酸循环实现矿化。
好氧颗粒污泥对页岩气返排水中的典型多环芳烃的去除、解毒作用及机制
Performance and mechanism of removal and detoxification of typical polycyclic aromatic hydrocarbons in shale gas flowback water by aerobic granular sludge
-
摘要: 页岩气开发是我国重大能源战略的关键组成部分,返排水的处理是该行业面临的主要挑战。目前,在返排水中普遍存在的多环芳烃由于具有高环境风险而备受关注。本研究采用具有页岩气返排水处理能力的好氧颗粒污泥探究其对典型多环芳烃萘和菲的处理能力及其行为特征,并通过HPLC和GC-MS分析降解过程中的中间产物探究降解路径,及好氧颗粒污泥对多环芳烃毒性的缓解效应。结果显示,该好氧颗粒污泥对萘和菲的去除率达到93.8%和91.3%,并能保持长期稳定。生物降解是该好氧颗粒污泥系统长期稳定去除典型多环芳烃的主要途径,对萘和菲的去除贡献率分别达到64.1%和72.2%。受限于吸附容量,吸附作用仅在初期发挥短期贡献,且具有不同的吸附机制:萘的吸附过程主要表现为多分子层的化学吸附,而菲的吸附表现为物理吸附和静电力作用下的化学吸附。伴随着萘和菲的去除,含萘和菲的废水经该好氧颗粒污泥处理之后生物毒性显著降低,分别降至1%和16%。萘降解生成的中间体包括2,4-二甲基苯甲醛、2,4-二叔丁基苯酚和2,2'-亚甲基双-(4-甲基-6-叔丁基苯酚),而菲的降解中间体则包括萘、三(2,4-二叔丁基苯基)亚磷酸酯、2,4-二甲基苯甲醛、2,4-二叔丁基苯酚和2,2'-亚甲基双-(4-甲基-6-叔丁基苯酚),这些中间体最终转化为水杨酸和邻苯二甲酸,通过三羧酸循环实现矿化并缓解毒性。上述结果暗示处理页岩气返排水的好氧颗粒污泥系统能够对返排水中的多环芳烃进行有效去除进而缓解其毒性效应,为好氧颗粒污泥技术应用于页岩气返排水处理提供了技术支撑。Abstract: Shale gas development is a crucial element of China's significant energy strategy, and managing flowback water presents a substantial challenge for the industry. The presence of PAHs in flowback water has received particularly concerns due to their high environmental risks. This study utilizes aerobic granular sludge, which is capable of treating shale gas flowback water, to explore its effectiveness in processing typical PAHs such as naphthalene and phenanthrene, and examine the behavior of these compounds and their degradation pathways by analyzing the intermediates via HPLC and GC-MS. Additionally, the capacity of aerobic granular sludge to reduce the toxicity associated with PAHs was evaluated, highlighting its potential benefits in environmental remediation. The results showed that the aerobic granular sludge could remove 93.8% of naphthalene and 91.3% of phenanthrene with a sustained efficacy over time. Biodegradation served as the primary pathway for a long-term stable removal of typical PAHs by this AGS system, contributing 64.1% to naphthalene removal and 72.2% to phenanthrene removal. Constrained by adsorption capacity, adsorption only played a fleeting yet crucial role at the initial stage with the distinct pathways: chemisorption for naphthalene in a multimolecular layer and a combination of physisorption and chemisorption influenced by electrostatic forces for phenanthrene. Notably, the treatment significantly reduced the biotoxicity of PAH-laden wastewater to 1% and 16% for naphthalene and phenanthrene, respectively. Degradation intermediates such as 2,4-dimethylbenzaldehyde, 2,4-di-tert-butylphenol, and 2,2'-methylenebis (4-methyl-6-tert-butylphenol) for naphthalene, while those for phenanthrene degradation included naphthalene, tris (2,4-di-tert-butylphenyl) phosphite, 2,4-dimethylbenzaldehyde, 2,4-di-tert-butylphenol, and 2,2'-methylenebis (4-methyl-6-tert-butylphenol) , ultimately transformed into salicylic acid and phthalic acid, facilitating detoxification and mineralization through the tricarboxylic acid cycle. These insights affirmed the potential of aerobic granular sludge systems in efficiently mitigating PAHs toxicity in shale gas flowback water, provides the technical support for the application of this technology to treat the shale gas flowback water.
-
Key words:
- shale gas flowback water /
- aerobic granular sludge /
- PAHs /
- adsorption /
- biodegradation /
- biotoxicity
-

-
表 1 AGS 对萘和菲的吸附等温线模型参数
Table 1. Parameters of the isotherm model for the adsorption of naphthalene and phenanthrene by AGS
污染物 Langmuir Freundlich Temkin qm/(mg·g−1) KL/(L·mg−1) R2 1/n KF/((mg1-n·Ln)g−1) R2 Kt/(L·g−1) F/(J·mol−1) R2 萘 21.53 0.26 0.96 0.44 5.62 0.97 3.98 2.72 0.93 菲 25.48 0.18 0.96 0.46 5.33 0.87 6.01 2.71 0.97 表 2 AGS对萘和菲的吸附动力学模型参数
Table 2. Kinetic modelling parameters for the adsorption of naphthalene and phenanthrene by AGS
污染物 准一级动力学模型 准二级动力学模型 k1/(min−1) qe/(mg·g−1) R2 k2/(g(mg·min)−1) qe/(mg·g−1) R2 萘 0.47 15.1 0.94 0.04 16.8 0.95 菲 0.24 17.1 0.97 0.01 21.2 0.94 -
[1] YU M, WEINTHAL E, PATINO-ECHEVERRI D, et al. Water availability for shale gas development in Sichuan basin, China[J]. Environmental Science & Technology, 2016, 50(6): 2837-2845. [2] FABER A-H, ANNEVELINK M P J A, SCHOT P P, et al. Chemical and bioassay assessment of waters related to hydraulic fracturing at a tight gas production site[J]. Science of the Total Environment, 2019, 690: 636-646. doi: 10.1016/j.scitotenv.2019.06.354 [3] ZHONG C, ZOLFAGHARI A, HOU D, et al. Comparison of the hydraulic fracturing water cycle in China and North America: a critical review[J]. Environmental Science & Technology, 2021, 55(11): 7167-7185. [4] DIGIULIO D C, JACKSON R B. Response to comment on "Impact to underground sources of drinking water and domestic wells from production well stimulation and completion practices in the Pavillion, Wyoming field"[J]. Environmental Science & Technology, 2016, 50(19): 10771-10772. [5] PATEL A B, SHAIKH S, JAIN K R, et al. Polycyclic aromatic hydrocarbons: Sources, toxicity, and remediation approaches[J]. Frontiers in Microbiology, 2020, 11: 562813. doi: 10.3389/fmicb.2020.562813 [6] OREM W, TATU C, VARONKA M, et al. Organic substances in produced and formation water from unconventional natural gas extraction in coal and shale[J]. International Journal of Coal Geology, 2014, 126: 20-31. doi: 10.1016/j.coal.2014.01.003 [7] LESTER Y, FERRER I, THURMAN E M, et al. Characterization of hydraulic fracturing flowback water in Colorado: Implications for water treatment[J]. Science of the Total Environment, 2015, 512: 637-644. [8] FOLKERTS E J, BLEWETT T A, DELOMPRE P, et al. Toxicity in aquatic model species exposed to a temporal series of three different flowback and produced water samples collected from a horizontal hydraulically fractured well[J]. Ecotoxicology and Environmental Safety, 2019, 180: 600-609. doi: 10.1016/j.ecoenv.2019.05.054 [9] HE Y, FLYNN S L, FOLKERTS E J, et al. Chemical and toxicological characterizations of hydraulic fracturing flowback and produced water[J]. Water Research, 2017, 114: 78-87. doi: 10.1016/j.watres.2017.02.027 [10] 王丹, 陈龙利, 何敏, 等. 页岩气采出水水质特性分析[J]. 环境监测管理与技术, 2018, 30(6): 50-53. doi: 10.3969/j.issn.1006-2009.2018.06.012 [11] CHEN B, HUANG J, YUAN K, et al. Direct evidences on bacterial growth pattern regulating pyrene degradation pathway and genotypic dioxygenase expression[J]. Marine Pollution Bulletin, 2016, 105(1): 73-80. doi: 10.1016/j.marpolbul.2016.02.054 [12] GUPTA G, KUMAR V, PAL A K. Biodegradation of polycyclic aromatic hydrocarbons by microbial consortium: A distinctive approach for decontamination of soil[J]. Soil & Sediment Contamination, 2016, 25(6): 597-623. [13] DHAR K, SUBASHCHANDRABOSE S R, VENKATESWARLU K, et al. Anaerobic microbial degradation of polycyclic aromatic hydrocarbons: A comprehensive review[J]. Reviews of Environmental Contamination and Toxicology, 2020, 251: 25-108. [14] ESTELMANN S, BLANK I, FELDMANN A, et al. Two distinct old yellow enzymes are involved in naphthyl ring reduction during anaerobic naphthalene degradation[J]. Molecular Microbiology, 2015, 95(2): 162-172. doi: 10.1111/mmi.12875 [15] CAMPO R, DI BELLA G. Petrochemical slop wastewater treatment by means of aerobic granular sludge: effect of granulation process on bio-adsorption and hydrocarbons removal[J]. Chemical Engineering Journal, 2019, 378: 122083. doi: 10.1016/j.cej.2019.122083 [16] CORSINO S F, CAMPO R, DI BELLA G, et al. Aerobic granular sludge treating shipboard slop: Analysis of total petroleum hydrocarbons loading rates on performances and stability[J]. Process Biochemistry, 2018, 65: 164-171. doi: 10.1016/j.procbio.2017.11.005 [17] DUAN F A, WANG J, ISMAIL S, et al. Hydroxypropyl-beta-cyclodextrin improves the removal of polycyclic aromatic hydrocarbons by aerobic granular sludge[J]. Environmental Technology, 2022, 43(21): 3262-3268. doi: 10.1080/09593330.2021.1921045 [18] YAN L, CHEN W, WANG C, et al. Tetracycline removal in granulation: Influence of extracellular polymers substances, structure, and metabolic function of microbial community[J]. Chemosphere, 2022, 288: 132510. doi: 10.1016/j.chemosphere.2021.132510 [19] 卢培利, 邱哲, 张代钧, 等. 页岩气开采返排废水有机污染物研究进展与展望[J]. 化工进展, 2018, 37(3): 1161-1166. [20] ZHANG X, CHEN A, ZHANG D, et al. The treatment of flowback water in a sequencing batch reactor with aerobic granular sludge: Performance and microbial community structure[J]. Chemosphere, 2018, 211: 1065-1072. doi: 10.1016/j.chemosphere.2018.08.022 [21] 陈翱翔. 好氧颗粒污泥SBR处理页岩气开采水力压裂返排废水的研究[D]. 重庆; 重庆大学, 2017. [22] 中华人民共和国生态环境部, 中国国家标准化管理委员会. 水质 多环芳烃的测定 液液萃取和固相萃取高效液相色谱法: HJ 478—2009[S]. 北京: 中国环境科学出版社, 2009. [23] LIU J J, WANG X C, FAN B. Characteristics of PAHs adsorption on inorganic particles and activated sludge in domestic wastewater treatment[J]. Bioresource Technology, 2011, 102(9): 5305-5311. doi: 10.1016/j.biortech.2010.12.063 [24] FERNáNDEZ-LóPEZ C, POSADA-BAQUERO R, GARCíA J L, et al. Root-mediated bacterial accessibility and cometabolism of pyrene in soil[J]. Science of the Total Environment, 2021, 760: 143408. doi: 10.1016/j.scitotenv.2020.143408 [25] FERREIRA V R A, AMORIM C L, CRAVO S M, et al. Fluoroquinolones biosorption onto microbial biomass: activated sludge and aerobic granular sludge[J]. International Biodeterioration & Biodegradation, 2016, 110: 53-60. [26] ZHU L, LV M L, DAI X, et al. Role and significance of extracellular polymeric substances on the property of aerobic granule[J]. Bioresource Technology, 2012, 107: 46-54. doi: 10.1016/j.biortech.2011.12.008 [27] CHEUNG W H, SZETO Y S, MCKAY G. Intraparticle diffusion processes during acid dye adsorption onto chitosan[J]. Bioresource Technology, 2007, 98(15): 2897-2904. doi: 10.1016/j.biortech.2006.09.045 [28] ZHAO X, WANG H, ZHANG G Z, et al. Characteristics of Cu(II)-modified aerobic granular sludge biocarbon in removal of doxycycline hydroxide[J]. Environmental Science and Pollution Research, 2022, 29(10): 14019-14035. doi: 10.1007/s11356-021-16547-x [29] REDóN L, SUBIRATS X, CHAPEL S, et al. Comprehensive analysis of the effective and intra-particle diffusion of weakly retained compounds in silica hydrophilic interaction liquid chromatography columns[J]. Journal of Chromatography A, 2024, 1713: 464529. doi: 10.1016/j.chroma.2023.464529 [30] DEBNATH S, DAS R. Strong adsorption of CV dye by Ni ferrite nanoparticles for waste water purification: Fits well the pseudo second order kinetic and Freundlich isotherm model[J]. Ceramics International, 2023, 49(10): 16199-16215. doi: 10.1016/j.ceramint.2023.01.218 [31] CHU T P, NGUYEN N T, VU T L, et al. Synthesis, characterization, and modification of alumina nanoparticles for cationic dye removal[J], Soil and Sediment Contamination: An International Journal, 2019, 12(3): 450-465. [32] CHEN Y, MA R, PU X, et al. The characterization of a novel magnetic biochar derived from sulfate-reducing sludge and its application for aqueous Cr(VI) removal through synergistic effects of adsorption and chemical reduction[J]. Chemosphere, 2022, 308: 136258. doi: 10.1016/j.chemosphere.2022.136258 [33] ZHENG L, TIAN Y, DING A-Z, et al. Adsorption of Cd(II), Zn(II) by extracellular polymeric substances extracted from waste activated sludge[J]. Water Science & Technology, 2008, 58(1): 195-200. [34] ADT I, TOUBAS D, PINON J-M, et al. FTIR spectroscopy as a potential tool to analyse structural modifications during morphogenesis of Candida albicans[J]. Archives of Microbiology, 2006, 185(4): 277-285. doi: 10.1007/s00203-006-0094-8 [35] ZHANG Y, HU Q, FU J, et al. Influence of exposure pathways on tissue distribution and health impact of polycyclic aromatic hydrocarbon derivatives[J]. Environment & Health, 2023, 1(3): 150-167. [36] IMAM A, SUMAN S K, KANAUJIA P K, et al. Biological machinery for polycyclic aromatic hydrocarbons degradation: A review[J]. Bioresource Technology, 2022, 343: 126121. doi: 10.1016/j.biortech.2021.126121 [37] 杜飞, 耿旺, 常美荣, 等. 新工艺法合成2, 2′-亚甲基双(4, 6-二叔丁基苯酚)[J]. 精细石油化工, 2010, 27(3): 30-33. doi: 10.3969/j.issn.1003-9384.2010.03.009 [38] 马翠, 刘亚琦, 何争光, 等. 臭氧催化氧化降解2, 2′-亚甲基-双(4-甲基-6-叔丁基苯酚)效能及机制研究[J]. 安全与环境学报, 2022, 22(2): 1045-1051. [39] MA C, JIA S, YUAN P, et al. Catalytic ozonation of 2, 2′-methylenebis (4-methyl-6-tert-butylphenol) over nano-Fe3O4@cow dung ash composites: Optimization, toxicity, and degradation mechanisms[J]. Environmental Pollution, 2020, 265. [40] HE Q, WANG H, CHEN L, et al. Elevated salinity deteriorated enhanced biological phosphorus removal in an aerobic granular sludge sequencing batch reactor performing simultaneous nitrification, denitrification and phosphorus removal[J]. Journal of Hazardous Materials, 2020, 390: 114597. [41] 王磊, 齐涛, 江洋, 等. 一种合成三[2, 4-二叔丁基苯基]亚磷酸酯的方法: CN202010489413.6[P]. 2020-06-02. -




 下载:
下载: