-
氮氧化物(NOx)是大气中直接或间接地危害人类和生态环境的主要污染物之一[1-3]。在去除效率、稳定性和经济性方面,NH3选择性催化还原NOx (selective catalytic reduction,SCR)被称为烟气净化的最佳控制技术[4]。催化剂是SCR技术的核心,其中,V2O5-WO3(MoO3)/TiO2催化剂具有较高的NOx脱除效率、选择性以及优异的抗SO2性能,是目前工业上应用最为普遍的SCR商业催化剂[5-8]。随着十三五期间电力行业完成超低排放改造,我国工业烟气污染治理的主战场从电力行业转移到了工业窑炉等非电力行业。相对于电力行业,这些工业窑炉排烟温度较低、工况不稳定、污染物浓度波动大。玻璃、焦化、垃圾焚烧、水泥等多个行业的工业窑炉其烟气温度一般都在 300 oC 以下(如钢铁行业的焦炉烟气温度为180~300 oC,垃圾焚烧烟气温度仅为180~300 oC)[8]。基于此,极有必要研发适用于中低温(180~300 oC) 烟气条件的SCR脱硝催化剂。氮氧化物和SO2同时存于玻璃、焦化、水泥、垃圾焚烧发电等工业窑炉烟气中[9-11]。因此,针对这些行业的烟气治理,需要同时考虑氮氧化物去除效率以及催化剂抗硫中毒性能。
钒基催化剂在高温下具有较强的抗SO2中毒能力,但在低温下(< 200 oC)依然面临 SO2中毒问题[12]。一些关于钙对催化剂上NO还原的影响的研究已有报道,CHEN等[13]发现,在氧化钙质量分数超过2%时,可导致明显的活性损失。高含量的CaO会极大地抑制表面氧物种和还原性,使得催化剂失活[14]。然而,目前有研究发现烟气中的SO2可以调节碱金属毒化作用,也可通过对载体的硫酸化或负载S物种,来提高催化剂的抗碱金属性能。YU等[15]研究了新鲜和经KNO3浸渍后K中毒的商业V2O5-WO3/TiO2蜂窝催化剂,在添加了0.15% SO2后,转化率由40%增加到70%,脱硝效率提高。同时,PUTLURU等[16]研究表明,相对于商业V2O5-WO3/TiO2催化剂,载体硫酸化后的V2O5/TiO2、V2O5/ZrO2均具有较好的耐碱金属性能。而熊尚超等[17]研究表明,VTi催化剂易发生硫中毒且在碱金属K存在时也易失活,但当K和S共存时,SCR活性恢复到接近新鲜VTi的水平,结果表明,K和S共存时存在类似于以毒攻毒这样的拮抗效应。YANG等[18]研究了CaO掺杂对V2O5- CeO2 /TiO2催化剂的中毒累积效应,结果表明,对于CaO中毒的催化剂,SO2可促进Brønsted酸性位上氨的吸附,在一定程度上抵消了氧化反应,从而提高了NH3-SCR的反应活性。尽管学者们已经对SO2调节碱金属毒化作用有一定的研究,但目前的研究报道主要是SO2对碱金属毒化作用调节的机理研究,鲜有碱金属掺杂调节SO2中毒的研究报道。
基于此,本研究通过等体积浸渍法制备了xCaO-V2O5-MoO3/TiO2,对其进行了脱硝性能评价以及长时间的抗 SO2、H2O 中毒性能测试,并结合物理吸附、BET、H2-TPR 、Raman和 in situ DRIFTS等表征手段对实验结果进行分析,获得了可用于200 oC以下,具有较好SO2、H2O 中毒性能的中低温脱硝催化剂。
-
以锐钛矿型TiO2(安徽迪诺环保新材料科技有限公司,纯度98%)为载体,偏钒酸铵(阿拉丁,纯度 AR 99%)、硝酸钙(AR)、钼酸铵(阿拉丁,纯度 99.95%)分别为CaO、V2O5、MoO3的前驱物,采用等体积浸渍法制备催化剂。具体制备方法如下:分别配制一定量的硝酸钙溶液、偏钒酸铵溶液以及钼酸铵溶液,其中,偏钒酸铵溶液配制过程中添加适量草酸加速其溶解,然后取一定量的硝酸钙溶液加入至 TiO2粉末中,搅拌均匀后,在110 oC下干燥 12 h、600 oC焙烧2 h后获得xCaO/TiO2载体,其中,x为CaO的质量分数。而后将偏钒酸铵溶液和钼酸铵溶液加入到制备好的xCaO/TiO2载体中,60 oC水域条件下,搅拌成泥浆状,在110 oC 下干燥 12 h、500 oC焙烧4 h,获得xCaO-V2O5-MoO3/TiO2催化剂(V2O5、MoO3质量分数分别为3.5%、8%)。xCaO-V2O5-MoO3/TiO2-u表示在180 oC下H2O和SO2氛围中进行NH3-SCR反应65 h后的催化剂。
-
催化剂的NH3-SCR脱硝活性测试评价采用微型常压固定床反应装置。催化剂的用量为0.12 g(40~60目),反应气体组成(体积分数)为:氨气,0.03%;一氧化氮,0.03%;二氧化硫,0.035%(抗水硫测试);一氧化碳,0.4%;二氧化碳,5%;水蒸气,10% ;氧气,16%;N2为载气;气体流量为300 mL·min−1;空速 (GHSV),30 000 h -1;采用FTIR(MKS6030HS)气体分析仪,在线连续监测进出口气体中各气体组分的浓度。NOx转化率和N2选择性根据式(1)和式(2)[7,12]计算。
式中:
$ C $ 为NOx的转化率,%;S为N2选择性,%;$ {C}_{1} $ 为入口气体中NOx的浓度,%$ ;{C}_{2} $ 为出口气体中NOx的浓度,%;$ {C}_{3} $ 为入口气体中NH3的浓度,%;$ {C}_{4} $ 为出口气体中NH3的浓度,%;$ {C}_{5} $ 为出口气体中N2O的浓度,%。 -
比表面积是影响催化剂脱硝性能的一项重要参数,通过物理吸附分析仪(美国Micromeritics ASAP 2460)获得的氮气吸附-脱附曲线,得到了BET比表面积和孔径分布。通过X射线衍射仪(XRD)分析测试样品的晶体结构,本测试采用的是日本Rigaku公司的 SmartLab 9 kW型X射线衍射仪。测试条件为:采用Cu靶辐射射线,管电压40 kV,管电流40 mA,扫描速度10 º·min−1,扫描范围10º~90º。
H2-TPR是用来测试催化剂样品的氧化还原能力强弱一种技术。在此研究过程中采用的是AutoChem 2920 型化学吸附仪。首先在N2气氛下将0.1 g 40~60目的催化剂350 oC预处理1 h,待降到室温后将N2转换为10% H2/N2 (50 mL·min−1)气体,从室温以10 ℃·min−1的速率程序性升温至650 oC,使用热导检测器(TCD)对信号进行采集。
DRIFTS实验采用美国Thermo Fisher Scientific公司Nicolet 6700傅立叶变换红外光谱仪,该仪器带有漫反射原位池(Harrick公司产,KBr窗体)和高灵敏度的MCT检测器,MCT检测器需用液氮冷却至−196 ℃,以降低噪声,扫描次数为64次,分辨率为4 cm−1。催化剂样品选用研磨后的粉末,实验前在400 ℃下用N2预处理1 h。
拉曼光谱分析采用Horiba公司 LabRAM HR Evolution拉曼光谱分析仪,该设备配备532 nm (Ventus LP 532) 激光源和Synapse CCD探测器,以及Linkam CCR1000原位池。累积次数20,累积时间10 s。光谱扫描范围800~1 200 cm−1,激发光源采用532 nm。
-
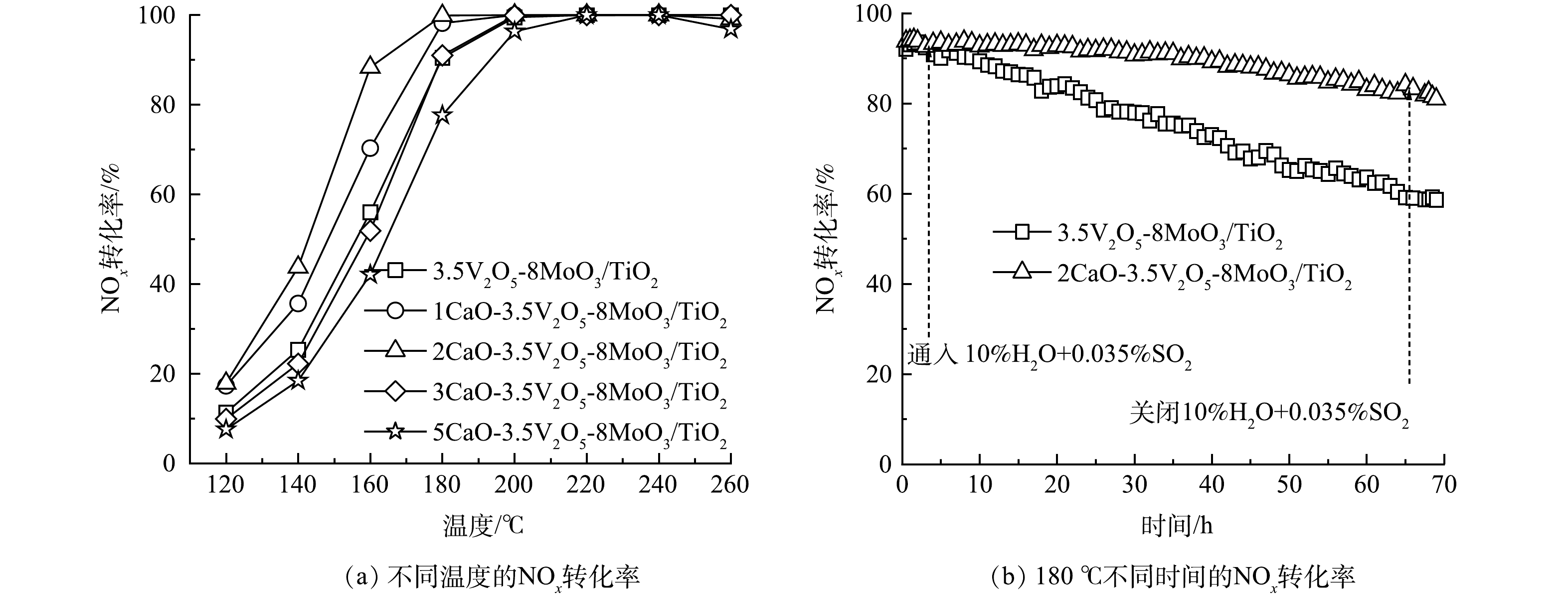
采用浸渍法制备不同CaO含量的xCaO-V2O5-MoO3/TiO2催化剂,催化剂的活性和选择性如图1所示。从图1(a)中可以看出,随着CaO掺杂量的提高,在100~180 oC内 NOx转化率逐渐降低,N2选择性先升高后降低。反应气中加入H2O和SO2对催化剂活性的影响结果如图2(a)所示。由图2(a)可以看出,CaO掺杂量低于或等于2%时,NOx转化率明显高于V2O5-MoO3/TiO2,在H2O和SO2存在时,2CaO-V2O5-MoO3/TiO2催化剂具有最佳的NOx转化率。通过比较图1(a)和图2(b)发现,在反应气中通入H2O和SO2时,尽管xCaO-V2O5-MoO3/TiO2催化剂和V2O5-MoO3/TiO2催化剂的NOx转化率均有一定的降低,但2CaO-V2O5-MoO3/TiO2和1CaO-V2O5-MoO3/TiO2仍表现出比V2O5-MoO3/TiO2更优异的催化性能。
为了进一步研究H2O和SO2对2CaO-V2O5-MoO3/TiO2和V2O5-MoO3/TiO2催化剂活性的影响,在180 oC、H2O和SO2存在条件下进行了稳定性实验,结果见图2(b)。由2(b)可知,V2O5-MoO3/TiO2催化剂经过65 h反应后,NOx转化率显著下降,由93.5%下降至59.1%,2CaO-V2O5-MoO3/TiO2经过65 h反应后,NOx转化率由93.8%降至83.8%,由上述结果可知,与V2O5-MoO3/TiO2催化剂相比,2% CaO的掺杂显著提高了催化剂的抗SO2和H2O中毒性能,使催化剂的失活速率明显减慢。以上结果表明,掺杂CaO掺杂的催化剂对SO2和H2O的耐受性要明显高于V2O5-MoO3/TiO2。
综上所述,通过比较xCaO-V2O5-MoO3/TiO2催化剂的NOx转化率、N2选择性及抗硫抗水性能,2CaO-V2O5-MoO3/TiO2的催化剂具有相对较好的脱硝性能。为了进一步研究CaO掺杂提高抗硫性能的原因,后续实验和研究主要围绕抗硫稳定性实验前后的2CaO-V2O5-MoO3/TiO2和V2O5-MoO3/TiO2展开。
-
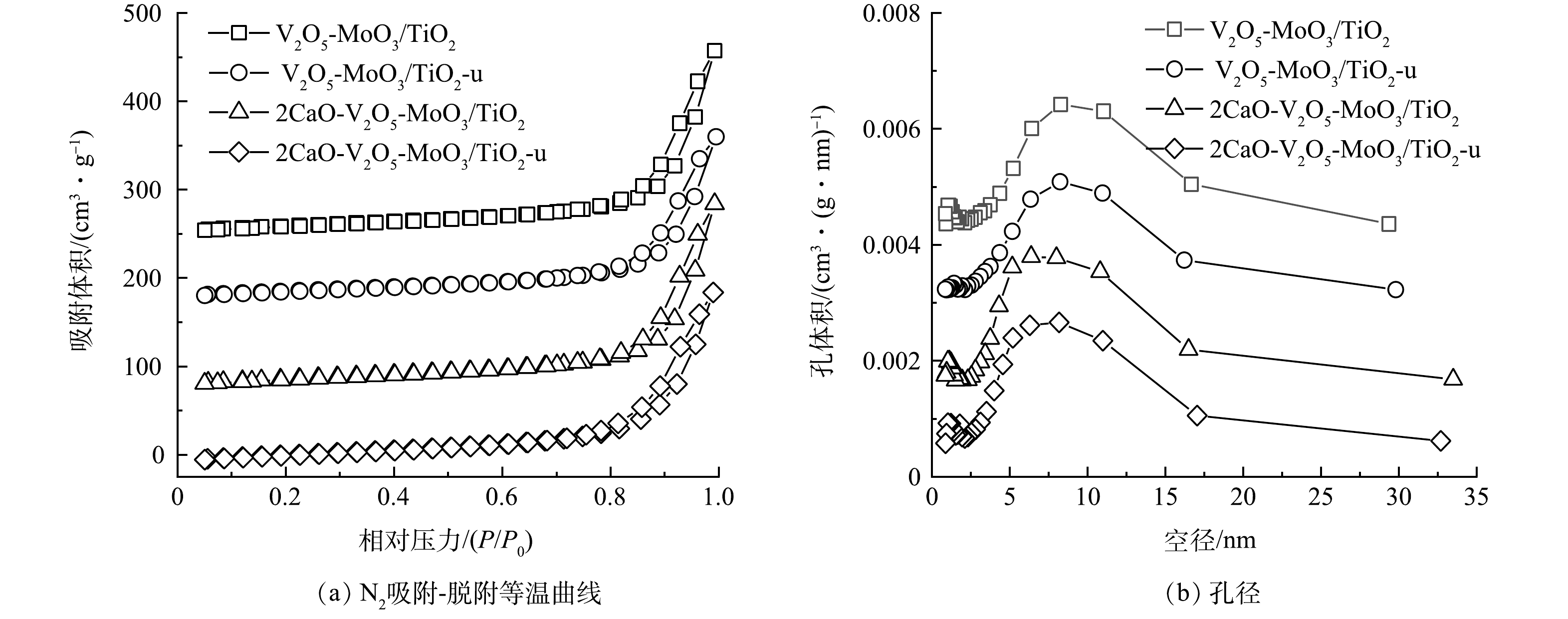
典型催化剂的比表面积、孔容和平均孔径的测定结果见表1。由表1可知,新鲜粉末2CaO-V2O5-MoO3/TiO2催化剂的比表面积略高于V2O5-MoO3/TiO2催化剂,说明少量CaO的掺杂有助于提高催化剂的比表面积。对比抗水抗硫稳定性反应前后的催化剂可以看出,反应后催化剂的比表面积、孔容略有下降,平均孔径略有上升,而这种下降和上升趋势,V2O5-MoO3/TiO2催化剂更为明显,这可能是由于硫酸铵盐沉积于催化剂孔道造成的,而这种沉积在V2O5-MoO3/TiO2-u催化剂上相对更严重,进一步说明V2O5-MoO3/TiO2-u催化剂中毒更为严重,因此脱硝效率显著下降。
图3 (a)为新鲜和失活后的催化剂的氮吸附-解吸等温线,根据Brunauer-Deming-Deming -Teller(BDDT)分类[19],他们均属于具有H3型滞后环的 IV 型(介孔毛细凝聚型),即催化剂的孔隙类型属于狭缝型,这种介孔在高压下达到吸附极限后,会发生毛细凝集现象。该现象表明催化剂具有相互交错的三维孔结构。
图3(b)为抗硫稳定性实验前后催化剂的孔径分布曲线。可见,新鲜和失活后的催化剂孔径均集中分布在1~15 nm,但在失活的V2O5-MoO3/TiO2-u催化剂中,孔径为1~3 nm 的孔明显减少。这是由于硫酸铵盐沉积于催化剂孔道造成,而2CaO-V2O5-MoO3/TiO2在反应前后的孔径分布未发生明显变化,进一步说明CaO的掺杂抑制了硫酸盐的沉积。
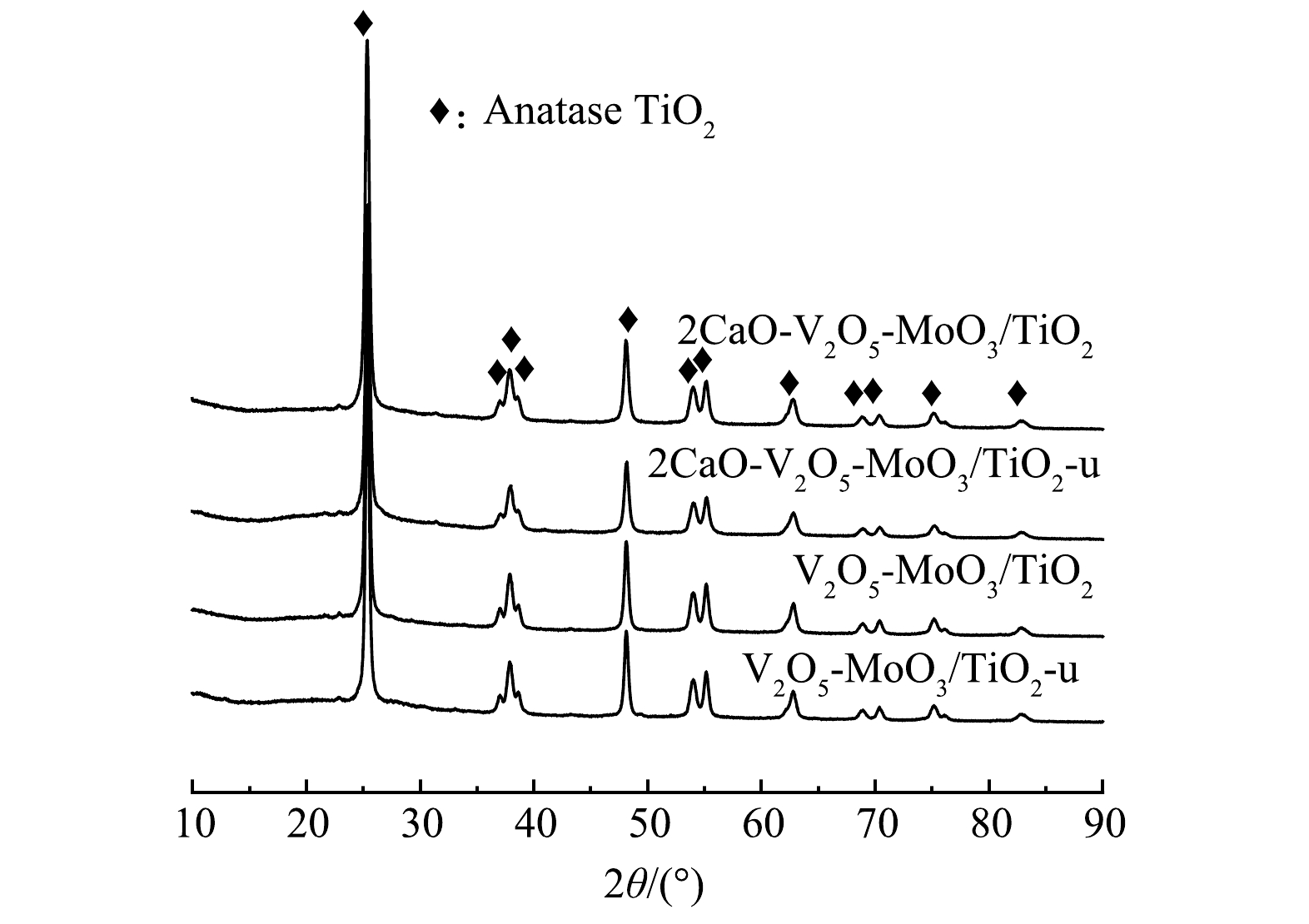
图4为抗硫稳定性实验前后催化剂的XRD谱图。由图4可知,4个样品的衍射峰以准锐钛矿二氧化钛峰(PDF#73-
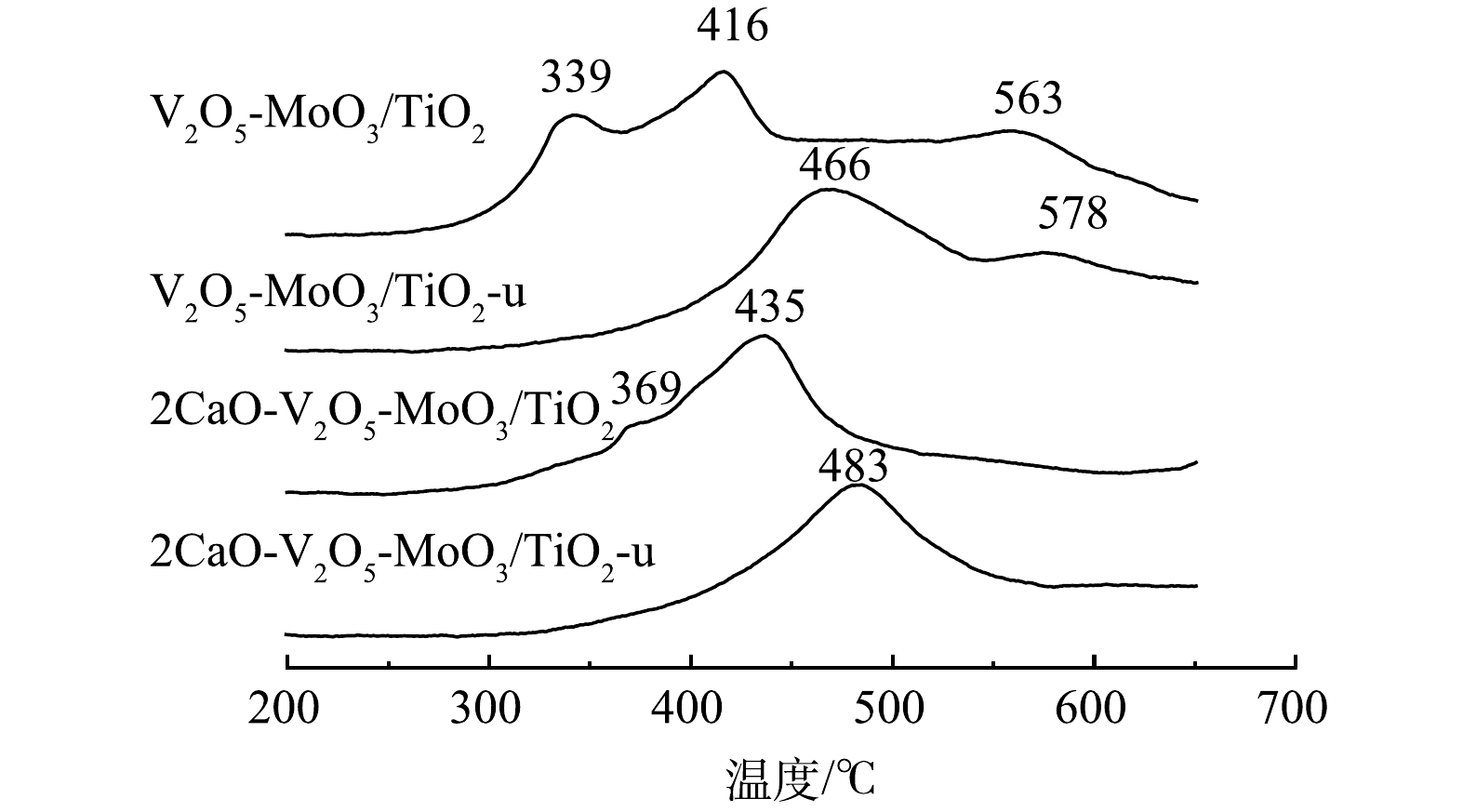
1764 )为主,并没有发现 V2O5、MoO3和CaO的衍射峰。这可能 V2O5、MoO3和CaO形成了非晶态或微晶太小,低于 XRD检测限,也有可能是V2O5、MoO3和CaO高度分散在载体表面[20]。通过H2-TPR测试来确定催化剂的氧化还原性能,结果如图5所示。对于V2O5-MoO3/TiO2催化剂具有2个重叠的峰,分别位于339 oC和416 oC,第1个峰归因于V5+→V3+的还原,第2个峰归因于表面Mo6+→Mo5/4+的还原[21]。而对于催化剂2CaO-V2O5-MoO3/TiO2,这2个峰分别迁移至369 oC和435 oC,说明CaO的掺杂降低了催化剂的氧化还原性能。而在经过抗硫稳定性实验后,这2个峰彻底重叠在一起,且向高温偏移,相对于2CaO-V2O5-MoO3/TiO2-u催化剂,V2O5-MoO3/TiO2-u向高温偏移的更严重,说明氧化还原性能降低更为明显。以上结果进一步说明了CaO的掺杂有利于保护活性物种的氧化还原性。
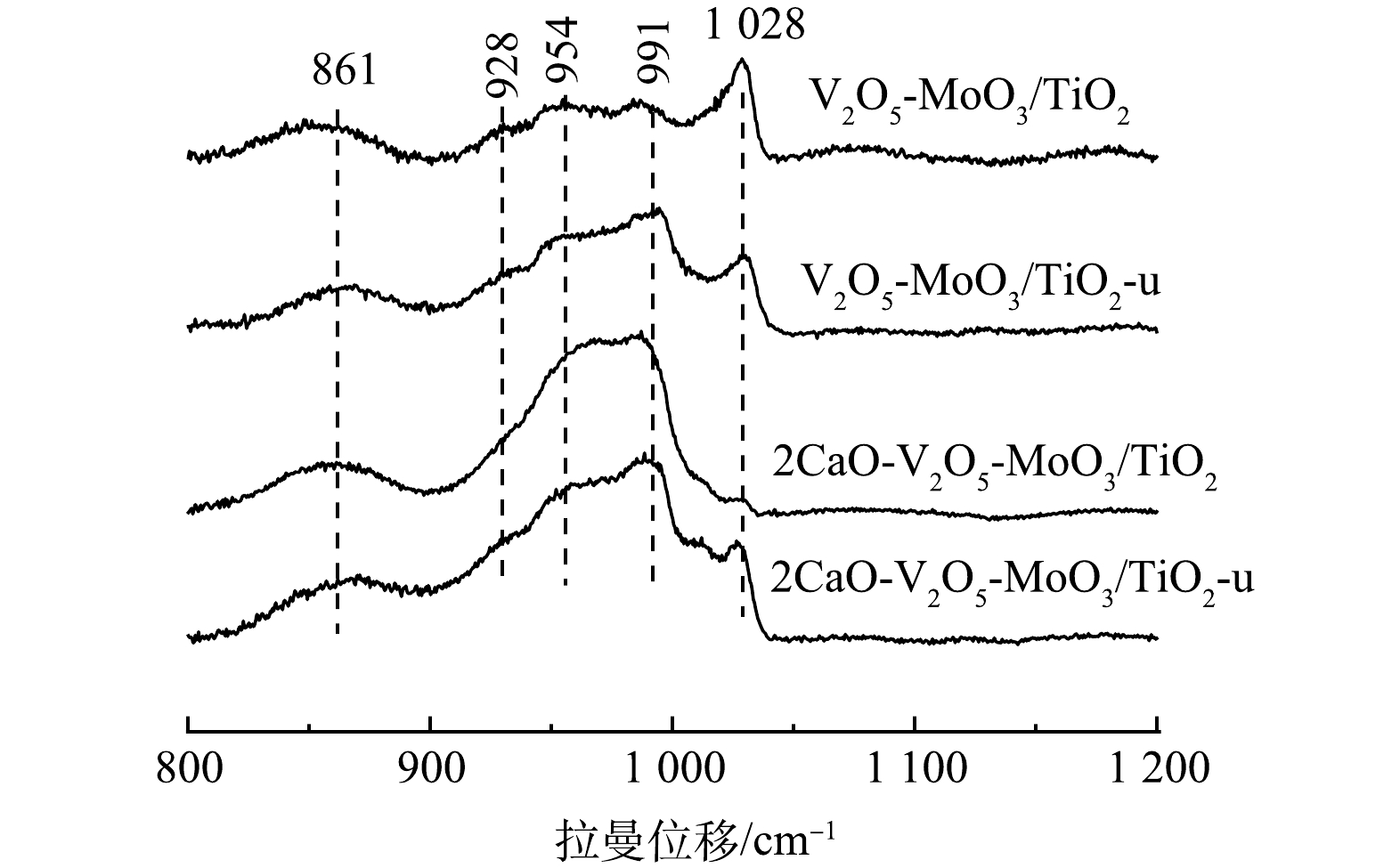
用拉曼光谱法测定了抗硫稳定性实验前后催化剂表面氧化钒物种和氧化钼物种的分散结构,结果如图6所示。已有研究表明,1 028、991和928 cm−1分别为单聚态氧化钒、晶体V2O5和聚合态氧化钒基的特征峰[22-24],954 cm−1归属于单体MoO42- 离子非对称伸缩振动峰[25-26]。反应前V2O5-MoO3/TiO2催化剂表面主要是单聚态钒氧物种,而经抗硫性能测试后形成了晶体V2O5,说明抗硫稳定性实验后,单聚钛的钒氧物种被破坏,发生了团聚,因此,催化活性有所降低。而对于2CaO-V2O5-MoO3/TiO2催化剂来说,新鲜的催化剂表面钒主要以单聚态氧化钒、晶体V2O5 形式以及聚合氧化态钒存在,而在进行抗硫反应后,可促进了氧化钒的分散,使得部分晶体V2O5 转变成单聚态氧化钒,由于单聚态氧化钒和聚合态氧化钒具有较好的活性,因此,2CaO-V2O5-MoO3/TiO2-u催化剂虽然氧化还原性能也降低,但具有较好的抗硫稳定性。这说明2CaO-V2O5-MoO3/TiO2-u催化剂抗硫稳定性实验后,酸度的提高增强了钒与载体的相互作用,因此,促进了氧化钒物种的分散性。
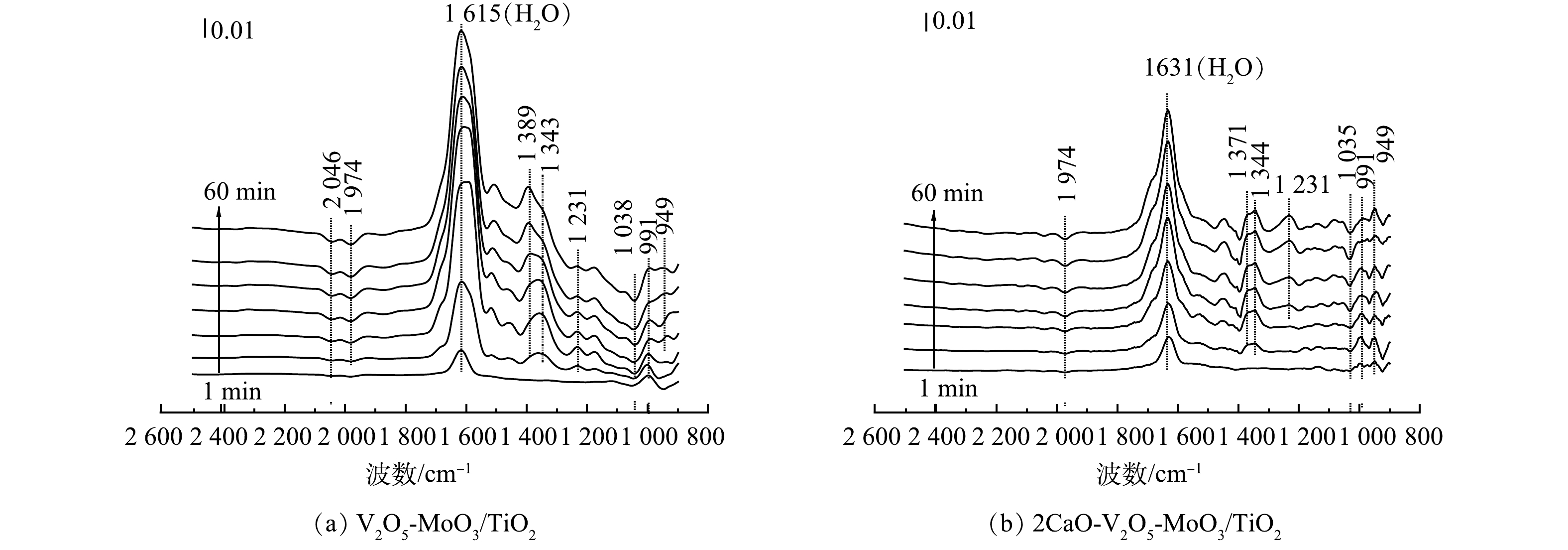
为了进一步揭示中毒机制,使用原位漫反射傅立叶变换红外光谱(in situ DRIFTS)检测硫物种沉积过程和稳定态的硫物种,测试过程在 180 oC下通入0.035% SO2+10% H2O+16% O2,结果如图7所示。由图7(a)可见,在引入H2O+SO2+O2后,V2O5-MoO3/TiO2催化剂,在1 630、1 371、1 344、1 231、991、941 cm−1处观察到正峰。其中1 631 cm−1归属于 H2O 的弯曲振动特征峰,1 371、1 178、991 cm−1分别为聚合硫酸盐(S2O72-)、双齿硫酸盐、表面硫酸盐的特征峰[27-34],1 231 cm−1为HSO4−的特征峰[31],950~800 cm−1为亚硫酸盐相关的红外峰[32]。此外,在2 046 cm−1和 1 033 cm−1处的峰来源于 V=O 的伸缩振动。V2O5-MoO3/TiO2催化剂在此处观察到明显的倒峰,表明吸附的SO2与表面的V=O反应,消耗V=O产生倒峰。同时在1 974 cm−1也处观察到的倒峰,此峰归属于Mo=O伸缩振动,产生倒峰,说明SO2与表面的部分Mo=O反应,催化剂表面的活性组分被明显的硫酸化。2CaO-V2O5-MoO3/TiO2表面也产生了表面硫酸氢盐(1 231 cm−1)、表面硫酸盐(1 371、1 178、991 cm−1)、亚硫酸盐(949 cm−1)的沉积,但在2 046 cm−1处未产生明显倒峰,在1 974 cm−1和1 033 cm−1处出现微弱的倒峰,相对于V2O5-MoO3/TiO2催化剂,硫酸盐物种的峰强度明显减弱,说明SO2与表面的V=O和Mo=O反应减弱,CaO的掺杂抑制了SO2与表面V=O和Mo=O的反应[33],因此,2CaO-V2O5-MoO3/TiO2催化剂具有较好的抗硫性能。
为揭示抗二氧化硫中毒的机理,以及二氧化硫物种对氨吸附和活化的影响,对反应前后V2O5-MoO3/TiO2和2CaO-V2O5-MoO3/TiO2催化剂进行了先NH3吸附后NO+O2瞬态原位红外实验。反应前新鲜V2O5-MoO3/TiO2和2CaO-V2O5-MoO3/TiO2催化剂上先NH3吸附后NO+O2瞬态原位红外实验光谱图如图8(a)和图8(c)所示。
通入NH3 60 min后,在3 386、3 267、3 173、1 653、1 602、1 563、1 423、1 423、1 237 cm−1处出现了一系列的NH3物种的吸收峰。其中,在3 367、3 262、3 172 cm−1处出现的峰归属于结合NH3中N—H伸缩振动峰,1 602 cm−1和1 229 cm−1处的峰的分别对应于吸附在Lewis酸位上的NH3的对称伸缩振动吸收峰和反对称伸缩振动吸收峰[35],1 423 cm−1和1 671 cm−1分别为Brønsted酸性位上NH4+的对称和反对称伸缩振动吸收峰[36]。在1 563 cm−1处出现NH2的剪切振动峰[37]。CaO的掺杂明显抑制了NH3在L酸性位上的吸附,降低了催化剂的酸性。当通入的气体转换成NO+O2时,所有吸附在Lewis酸性位和B酸性位上的NH3物种的吸收峰的强度均有所减弱,并在通入NO+O2 60 min后消失。在通入NO+O2 20 min后,在1 660 cm−1、1 477 cm−1处各出现了一个吸收峰,分别归属为N2O4的吸收峰、单齿硝酸盐物种的吸收峰[38-39]。说明在V2O5-MoO3/TiO2和2CaO-V2O5-MoO3/TiO2催化剂表面吸附的NH3物种在NH3-SCR反应中具有较高的催化反应活性。
反应后V2O5-MoO3/TiO2 和2CaO-V2O5-MoO3/TiO2催化剂上先NH3吸附后NO+O2瞬态原位红外实验光谱图如图8(b)和图8(d)所示,通过反应前后NH3吸附60 min的红外对比发现,抗水抗硫反应后V2O5-MoO3/TiO2-u催化剂 NH3吸附能力明显减弱,结合SO2+O2吸附原位红外的结构,可得抗水抗硫反应后,吸附的SO2与表面活性位点反应,形成硫酸盐,催化剂表面酸性位点减少,进一步解释了当SO2通入时间为60 h时,催化活性下降的原因。而2CaO-V2O5-MoO3/TiO2催化剂上,抗水抗硫反应后,1 229 cm−1处,在Lewis酸位上的NH3的振动吸收峰有轻微减弱,其他位置的峰未发生明显变化,说明酸性位点没有明显变化,进一步说明了掺CaO催化剂具有良好的抗硫性。
-
1)抗水抗硫反应后V2O5-MoO3/TiO2-u催化剂孔径为1~3 nm的孔明显减少,硫酸铵盐沉积于催化剂孔道,堵塞了孔结构,导致V2O5-MoO3/TiO2催化剂失活,而CaO的掺杂抑制了硫酸盐在催化上孔结构上的沉积,因此,具有较好的抗水抗硫性能。
2)经抗水抗硫反应后,与2CaO-V2O5-MoO3/TiO2-u催化剂相比,V2O5-MoO3/TiO2-u的氧化还原性能降低更为明显,进一步说明CaO的掺杂有利于保护活性物种的氧化还原性,因此,2CaO-V2O5-MoO3/TiO2催化剂具有较好的抗水抗硫性能。
3)抗水抗硫反应后,V2O5-MoO3/TiO2-u催化剂上的单聚态的氧化钒物种被破坏,发生了团聚,形成晶体V2O5,因此活性明显降低。而CaO的掺杂,促进了2CaO-V2O5-MoO3/TiO2-u催化剂上氧化钒的分散,使得部分晶体V2O5 转变成单聚态氧化钒,由于单聚态氧化钒和聚合态氧化钒具有较好的活性,因此,2CaO -V2O5 -MoO3/TiO2-u催化剂虽然氧化还原性能也降低,但仍具有较好的性能。
4)CaO的掺杂抑制了SO2与表面V=O物种和表面Mo=O反应,而且抗水抗硫反应后,V2O5-MoO3/TiO2-u催化剂,NH3吸附能力明显减弱,推断抗水抗硫反应后,吸附的SO2与表面活性位点反应,形成硫酸盐,催化剂表面酸性位点减少。而CaO的掺杂抑制了SO2与表面活性物种的反应,2CaO -V2O5 -MoO3/TiO2抗水抗硫反应后,酸性位点未发生明显变化,因此具有较好的抗水抗硫性能。
掺杂CaO对V2O5-MoO3/TiO2催化剂低温抗硫中毒性能的影响
Performance of anti-sulfur poisoning at low temperature by CaO-doped V2O5-MoO3/TiO2 catalysts
-
摘要: 针对中低温工业窑炉烟气脱硝技术需求,采用等体积浸渍法,以V2O5为活性组分、MoO3为助剂,制备了钙掺杂的高钒高钼含量的xCaO-V2O5-MoO3/TiO2 (x为样品中为CaO质量百分数/%)脱硝催化剂。在微型固定床反应器中,对制备的xCaO-V2O5-MoO3/TiO2催化剂进行以NH3为还原剂的选择性催化还原NO的反应活性及低温抗硫中毒性评价。结果表明,在反应气氛中通入H2O和SO2时,2CaO-V2O5-MoO3/TiO2催化剂具有较好的脱硝性能,且在180 ºC,通入H2O和SO2,NH3-SCR反应65 h以后,NOx转化率在85%以上,表明CaO掺杂可以有效提高催化剂的低温抗 SO2 和 H2O 中毒性能。采用BET、XRD、H2-TPR、Raman、in situ DRIFTS等表征手段对制备的催化剂进行了进一步的表征分析,结果表明,CaO的掺杂可抑制SO2与催化剂表面活性钒物种的反应,从而保护了催化剂表面的活性物种,进而抑制了表面钒物种的团聚。Abstract: Considering the demand of flue gas denitrification technology in middle and low temperature industrial kilns, a series of xCaO-V2O5-MoO3/TiO2 catalysts were prepared using incipient wetness impregnation method (x represents the mass percentage of CaO in the sample) when V2O5 and MoO3 were taken as active components and additive, respectively. Its activity and anti-sulfur poisoning performance at low temperature were evaluated in a micro fixed bed reactor using NH3 as the reductant for the selective catalytic reduction of NO. The results showed that when H2O and SO2 were introduced into the reaction atmosphere, the 2CaO-V2O5-MoO3/TiO2 catalyst had a better denitrification performance, and after 65 hours of NH3-SCR reaction at 180 oC, the NOx conversion rate was over 85%. The catalyst is identified to have an excellent resistance to the deactivation by SO2 and H2O at middle-low temperatures. The prepared fresh and used catalysts were characterized by BET, XRD, H2-TPR, Raman, in situ DRIFTS. The results showed that the doped CaO could inhibit the reaction between SO2 and the active vanadium species on the catalyst surface, then protecting them, thereby suppressing the aggregation of the surface vanadium species.
-

-
表 1 反应前后催化剂的结构参数
Table 1. Structural parameters of fresh and used catalysts
样品名称 比表面积/(m2·g−1) 孔容/(cm3·g−1) 孔径/nm V2O5-MoO3/TiO2 59.4 0.333 8.63 V2O5-MoO3/TiO2-u 57.3 0.257 10.4 2CaO- V2O5-MoO3/TiO2 65.2 0.329 9.17 2CaO- V2O5-MoO3/TiO2-u 64.9 0.313 9.55 -
[1] 郝吉明, 马广大, 大气污染控制工程[M], 北京: 高等教育出版, 2002. [2] 杨玲, 李茂, 李建军. SCR催化剂的研究进展[J]. 四川化工, 2012, 15: 26-29. doi: 10.3969/j.issn.1672-4887.2012.02.011 [3] 王玉云, 沈岳松, 纵宇浩, 等. Co、Ni掺入对Pd-Rh型催化剂三效净化C3H8、CO、NO的影响[J]. 环境工程, 2015, 13(5): 62-68. [4] MENG D M, ZHAN W C, GUO Y, et al. A highly effective catalyst of Sm-Mn mixed oxide for the selective catalytic reduction of NOx with ammonia: Effect of the calcination temperature[J]. Journal of Molecular Catalysis A: Chemical, 2016, 420: 272-281. doi: 10.1016/j.molcata.2016.04.028 [5] KIJLSTRA W S, BRANDS D S, POESLS E K, et al. Mechanism of the selective catalytic reduction of NO by NH3 over MnOx/Al2O3[J]. Journal of Catalysis, 2007, 171(1): 208-218. [6] 陈建军, 李俊华, 柯锐, 等. 钒和钨负载量对 V2O5-WO3/TiO2 表面形态及催化性能的影响[J]. 环境科学, 2007, 28(9): 1949-1953. doi: 10.3321/j.issn:0250-3301.2007.09.009 [7] 贾勇, 张松, 戴波, 等. 负载型磷酸氧钒低温脱硝催化剂的制备及其抗硫抗水性能[J]. 环境工程学报, 2019, 13(1): 125-133. doi: 10.12030/j.cjee.201805172 [8] 尹荣强. 钒基催化剂抗中毒及一体化除尘脱硝催化滤管开发研究[D]. 北京: 清华大学, 2023. [9] 朱廷钰, 刘青, 李玉然, 等. 钢铁烧结烟气多污染物的排放特征及控制技术[J]. 科技导报, 2014, 32(33): 51-56. [10] 谢珊珊, 袁章福, 罗坚, 等. 冶金烟气净化过滤脱硫脱硝一体化集成技术[J]. 有色金属(冶炼部分), 2018, 10: 81-86. [11] DVORAK R, CHLAPEK P, JECHA D, et al. New approach to common removal of dioxins and NOx as a contribution to environmental protection[J]. Journal of Cleaner Production, 2010, 18(9): 881-888. doi: 10.1016/j.jclepro.2010.01.024 [12] 喜静波, 陈涛, 窦磊. Ce-TiO2催化剂在含SO2气氛下的NH3-SCR中毒机理及其Co3O4改性性能[J]. 环境工程学报, 2023, 17(4): 1283-1293. doi: 10.12030/j.cjee.202210097 [13] CHEN L, LI J. GE. M. The poisoning effect of alkali metals doping over nano V2O5−WO3/TiO2 catalysts on selective catalytic reduction of NOx by NH3[J]. Chemical Engineering Journal, 2011, 170: 531-537. doi: 10.1016/j.cej.2010.11.020 [14] LI X, CHEN J, LI J, et al. An efficient novel regeneration method for Ca-poisoning V2O5-WO3/TiO2 catalyst[J]. Chemical Communications, 2016, 87: 45-48. [15] YU Y, WANG J, CHEN J, et al. Promotive effect of SO2 on the activity of a deactivated commercial selective catalytic reduction catalyst: An in situ DRIFT study[J]. Industrial Engineering Chemistry Research, 2014, 53: 16229-16234. doi: 10.1021/ie502065b [16] PUTLURU S S R, KRISTENSEN, S B, DUE-HANSEN, J, et al. Alternative alkali resistant deNOx catalysts[J]. Catalysis Today, 2012, 184: 192-196. doi: 10.1016/j.cattod.2011.10.012 [17] XIONG S C, CHEN J J, LIU H, et al. Like cures like: Detoxification effect between alkali metals and sulfur over the V2O5/TiO2 deNOx catalyst[J]. Environmental Science & Technology, 2022, 56: 3739-3747. [18] YANG Z, YANG G, LEI L, Poisoning process of the V2O5−CeO2/TiO2 catalyst by the cumulative effect of CaO[J]. Energy Fuels, 2021, 35, 14876−14884. [19] 何余生, 李忠, 奚红霞, 等. 气固吸附等温线的研究进展[J]. 离子交换与吸附, 2004, 20(4): 376-384. doi: 10.3321/j.issn:1001-5493.2004.04.012 [20] 周惠, 黄华存, 董文华. SiO2 掺杂对 V2O5-WO3/TiO2 脱硝催化性能的影响[J]. 环境工程学报, 2017, 11(8): 4677-4684. doi: 10.12030/j.cjee.201607199 [21] XU Y F, WU X D, LIN Q W. SO2 promoted V2O5-MoO3/TiO2 catalyst for NH3-SCR of NOx at low temperatures[J]. Applied Catalysis A, General, 2019, 570: 42-50. doi: 10.1016/j.apcata.2018.10.040 [22] BESSELMANN S, LOFFLER E, MUHLER M. On the role of monomeric vanadyl species in toluene adsorption and oxidation on V2O5/TiO2 catalysts: a Raman and in situ DRIFTS study[J]. Journal of Molecular Catalysis A: Chemical, 2000, 162: 401-411. doi: 10.1016/S1381-1169(00)00307-1 [23] KOBAYASHI M, HAGI M. V2O5-WO3/TiO2-SiO2-SO42+ catalysts: Influence of active componentsand supports on activities in the selective catalytic reduction of NO by NH3 and in the oxidation of SO2[J]. Applied Catalysis B: Environmental, 2006, 63: 104-113. doi: 10.1016/j.apcatb.2005.09.015 [24] YAN T, LIU Q, WANG S H, et al. Promoter rather than inhibitor: Phosphorus incorporation accelerates the activity of V2O5-WO3/TiO2 catalyst for selective catalytic reduction of NOx by NH3[J]. ACS Catalysis, 2020, 10(4): 2747-2753. doi: 10.1021/acscatal.9b05549 [25] KWON D W, PARK K H, HONG S C. Enhancement of SCR activity and SO2 resistance on VOx/TiO2 catalyst by addition of molybdenum[J]. Chemical Engineering Journal, 2016, 284: 315-324. doi: 10.1016/j.cej.2015.08.152 [26] PANAAGIOTOU G D, PETSI T, BOURIKAS K. Interfacial Impregnation Chemistry in the Synthesis of Molybdenum Catalysts Supported on Titania[J]. Journal of Physical Chemistry C, 2010, 114: 11868-11879. doi: 10.1021/jp101333t [27] CHEN J P, YANG R T. Selective catalytic reduction of NO with NH3 on SO42-/TiO2 superacid catalyst[J]. Journal of Catalysis, 1993, 139(1): 277-288. doi: 10.1006/jcat.1993.1023 [28] XIONG J, LI Y R, LIN Y T, et al. Formation of sulfur trioxide during the SCR of NO with NH3 over a V2O5/TiO2 catalyst[J]. RSC Advances, 2019, 9(67): 38952-38961. doi: 10.1039/C9RA08191G [29] LI C, SHEN M, YU T, et al. The mechanism of ammonium bisulfate formation and decomposition over V/WTi catalysts for NH3-selective catalytic reduction at various temperatures[J]. Physical Chemistry Chemical Physics, 2017, 19(23): 15194-15206. doi: 10.1039/C7CP02324C [30] SHA G M S E, PHILIP C A. Solid acids from persulphated and perchlorated physical mixtures of zirconium and titanium hydroxides[J]. Adsorption Science & Technology, 2002, 20(10): 977-993. [31] GUO Y Y, LUO L, MU B L. et[J]. al, Ash- and Alkali-Poisoning Mechanisms for Commercial Vanadium−Titanic-Based Catalysts[J], Industrial Engineering Chemistry Research, 2019, 58: 22418-22426. [32] WANG X M, DU X S, LIU S J, et al. Understanding the deposition and reaction mechanism of ammonium bisulfate on a vanadia SCR catalyst: A combined DFT and experimental study[J]. Applied catalysis. B, Environmental, 2020, 260: 118168. doi: 10.1016/j.apcatb.2019.118168 [33] LIN Y T, LI Y R, XU Z C, et al. Carbon consumption and adsorption-regeneration of H2S on activated carbon for coke oven flue gas purification[J]. Environmental Science and Pollution Research International, 2021, 28(43): 60557-60568. doi: 10.1007/s11356-021-14914-2 [34] GUO X, BARTHOLOMEW C, HECKER W, et al. Effects of sulfate species on V2O5/TiO2 SCR catalysts in coal and biomass-fired systems[J]. Applied catalysis B, Environmental, 2009, 92(1-2): 30-40. doi: 10.1016/j.apcatb.2009.07.025 [35] CASAPU M, KRCHER O, MEHRING M, et al. Characterization of Nb-containing MnOx-CeO2 catalyst for low-temperature selective catalytic reduction of NO with NH3[J]. Journal of Physical Chemistry, 2010, 114(21): 9791. [36] QU R Y, GAO X, CEN K F, et al. Relationship between structure and performance of a novel cerium-niobium binary oxide catalyst for selective catalytic reduction of NO with NH3[J]. Applied Catalysis B: Environmental, 2013, 142-143(5): 290. [37] LIU Z M, YI Y, LI J H, et al. A superior catalyst with dual redox cycles for the selective reduction of NOx by ammonia[J]. Chemical Communications, 2013, 49(70): 7726-7728. doi: 10.1039/c3cc43041c [38] TROVARELLI A. Catalytic properties of ceria and CeO2-containing materials[J]. Catalysis Reviews, 1996, 38(4): 439-520. doi: 10.1080/01614949608006464 [39] UNDEREOOD G M, MILLER T M, GRESSIAN V H. Transmission FT-IR and Knudsen cell study of the heterogeneous reactivity of gaseous nitrogen dioxide on mineral oxide particles[J]. The Journal of Physical Chemistry A, 1999, 103(31): 6184-6190. doi: 10.1021/jp991586i -




 下载:
下载: