-
邻苯二甲酸酯(phthalate esters, PAEs)又称酞酸酯,是一类重要的合成有机物,被广泛应用于塑料制造[1],常用作涂料、润滑剂、粘合剂、杀虫剂、包装和化妆品的添加剂[2]。有文献报道了国内23个城市的90个自来水厂141个水源水样中均检出了邻苯二甲酸单酯(MPAEs)[3],邻苯二甲酸二丁酯(DBP)是PAEs中的一种,在增塑剂中应用最为广泛,极易从塑料中释放到环境中[4-5],是一种环境激素类物质,具有致癌、致畸与致突变作用[6-8],因此,开展PAEs此类污染物在不同环境中的降解研究对于生态环境安全保障尤为重要。
目前,对DBP污染的生物降解研究主要集中在高效降解菌的筛选、驯化及降解机理等方面[9-10],游离态菌株在实际应用中存在降解周期长、菌体易流失、环境耐受性差等问题,因此,国内外学者利用固定化微生物技术解决生物降解的缺陷,已应用在处理生活废水[11]、池塘模拟废水[12]、难降解有机废水[13-14]等水污染治理方面。为了得到具有高固定化强度和高微生物活性的固定化系统,可选择两种及以上的固定化材料结合起来的复合固定化法,例如:采用聚乙烯醇和海藻酸钠为包埋材料、活性炭为吸附材料、CaCl2的饱和硼酸溶液为交联剂,同时,负载较强生物活性的高效降解混合菌势必会提高生物解吸的效率,最终获得对底物优异的降解性能[15],具有较强的实际应用性。
本研究以DBP为目标污染物,开展了DBP降解混合菌(以下简称DP3)的包埋-吸附-交联固定化条件优化及降解特性研究,以聚乙烯醇(PVA)和海藻酸钠(SA)为包埋材料、活性炭为吸附材料,CaCl2的饱和硼酸溶液为交联剂,采用正交试验确定最佳固定化制备条件,并以游离态混合菌为对照,研究了pH值、盐度、DBP浓度对固定化混合菌降解性能的影响,研究结果可为DBP降解菌在环境修复中的应用提供理论依据和技术支持。
全文HTML
-
本研究供试混合菌DP3由本实验室保存的DBP高效降解菌鲍曼不动杆菌、唐氏不动杆菌、弗氏柠檬酸杆菌菌悬液复配而成。各菌株的菌悬液制备方法为:将菌液接种到LB培养基,于30 ℃,150 r·min−1摇床活化培养,将活化好的培养液5000 r·min−1离心5 min,收集的菌体用pH=7.2磷酸盐缓冲液清洗2遍,生理食盐水清洗3遍,重新离心,弃去上清液。取适量湿菌体用无菌水配制成菌悬液,调节OD600至1.0。混合菌DP3由各菌悬液按3∶3∶2比例配制生成。
-
气相色谱-质谱联用仪(7890B-7000C,美国Agilent公司);超声清洗器(KQ5200DB,昆山市超声仪器有限公司); 旋转蒸发器(RE5299,海亚荣生化仪器厂);紫外分光光度计(UV-5100B,上海分析仪器有限公司)。
本研究所用药品除特别注释均为分析纯,其中邻苯二甲酸二丁酯标样购自美国Accustandard公司,色谱纯正己烷购自上海赛默飞世尔科技有限公司。
牛肉膏蛋白胨培养基(LB):牛肉膏5 g,蛋白胨10 g,NaCl 5 g,蒸馏水1 L,pH值为7.2—7.4。
无机盐培养基(MSM):K2HPO45.1 g,KH2PO4 2.5 g,(NH4)2SO4 2.0 g,MgCl2 0.16 g,微量元素溶液1.0 mL;微量元素溶液:CaCl2 20 mg,Na2MoO4·2H2O 2.4 mg,FeSO4·7H2O 1.8 mg,MnCl2·4H2O 1.5 mg。
模拟人工污水:葡萄糖0.1700 g;可溶性淀粉0.1600 g;CH3COONa 0.2330 g;NH4Cl 0.45 g;KNO3 0.1 g;(NH4)2SO4 0.0284 g;KH2PO4 0.0700 g;Na2CO3 0.0600 g;pH=7.2,去离子水1.0 L。121 ℃灭菌30 min后使用。
-
取待测的DBP无机培养基溶液50 mL于150 mL锥形瓶中,加入等体积正己烷,常温下超声提取30 min静置。利用分液漏斗取出上层有机相,加入4 g无水硫酸钠干燥并浓缩至0.5 mL,最后用正己烷定容至1 mL,转入棕色2 mL样品瓶,待测。
GC-MS色谱条件:Agilent HP-5MS UI色谱柱(30 m×0.25 mm×0.25 μm);进样口温度为280 ℃;程序升温:初始柱温80 ℃,保持1 min,以20 ℃·min−1上升至280 ℃,保持4 min,载气:氦气,流速1 mL·min−1; 进样方式:不分流进样;进样量:1 μL。
GC-MS质谱条件:电子轰击离子源模式(EI),离子源温度300 ℃,四极杆温度150 ℃,MSD传输线温度300 ℃,电子能量70 eV;扫描范围为50—550 m/z[16]。
-
取外形规则的固定化凝胶球用0.1 mol·L−1的PBS 缓冲溶液清洗3次,每次10—15 min,在4 ℃下,2.5%戊二醛固定12 h,0.1 mol·L−1的PBS缓冲溶液清洗3次,每次10—15 min,依次在50%、70%、80%、90%和100%质量浓度的乙醇溶液中脱水1次,每次30 min,然后用1∶1的乙醇和乙酸异戊酯置换乙醇1次,乙酸异戊酯置换乙醇2次,每次30 min,于CO2临界点干燥,切片,将样品固定在样品托上,喷金,待测。
-
选择PVA和SA包埋材料,活性炭粉末(过1 mm筛)作为吸附剂,氯化钙和硼酸作为交联剂。首先,称取一定量的活性炭,将制备好的5 mL菌悬液与活性炭混合,摇床振荡吸附0.5 h。然后,将PVA和SA按一定比例混合后加入30 mL蒸馏水浸泡12 h,灭菌后冷却至30 ℃后,加入吸附有菌体的活性炭,接着,用无菌水定容至50 mL,搅拌均匀后用注射器从20 cm高处将其缓慢匀速滴加至一定质量分数的氯化钙-饱和硼酸溶液中(用Na2CO3调pH 6.7左右),磁力搅拌,凝胶颗粒交联24 h。最后,用无菌水和生理盐水分别冲洗2次,保存于4 ℃冰箱中,备用。
为确定混合菌最佳固定化制备条件,选定海藻酸钠(SA)、聚乙烯醇(PVA)、活性炭(AC)和CaCl2质量分数为试验因素,各因素分别设置3个水平,按L9(34)正交表设计正交试验(表 1)。
-
取灭菌的无机盐培养基50 mL,保持DBP的最终浓度分别为10、20、50、100、200、500、1000 mg·L−1。根据最佳固定化制备条件结果(A2B2C3D1),将制备好的固定化凝胶球和不接菌空白凝胶球按照相同的接种量接种到锥形瓶中,于150 r·min−1、30 ℃恒温培养。每个处理设3个重复,测试24 h的降解率。
-
在灭菌的三角瓶中加入1000 mg·L−1的DBP的正己烷溶液0.5 mL,挥发尽正己烷,然后加入灭菌的无机盐培养基50 mL,保持DBP的最终浓度为10 mg·L−1,分别加入制备好的固定化微生物凝胶球和菌悬液,使接菌量保持一致。研究不同环境因素(pH、NaCl浓度和DBP浓度)对固定化微生物的降解性能:pH(4、5、6、7、8、9、10);NaCl浓度(5、10、20、50、100 g·L−1);DBP浓度(10、20、50、100、200 mg·L−1)。每个处理设3个重复。30 ℃、转速150 r·min−1下培养,测定3 d固定化和游离态混合菌的降解率。
-
取灭菌的无机盐培养基50 mL,加入制备好的固定化微生物凝胶球,保持DBP的最终浓度为10 mg·L−1,于150 r·min−1、30 ℃ 恒温培养 3 d。每个处理设3个重复,重复20次,研究固定化DBP混合菌的长期降解稳定性。
取灭菌的模拟人工污水50 mL,实验方法同长期稳定性试验,测定6 d固定化微生物凝胶球和游离态混合菌在模拟人工污水中的降解率。
-
采用一阶动力学模型对降解数据进行拟合,模型方程如下:
式中,Ct是t(d)时体系中DBP的总浓度(mg·L−1);C0是初始时DBP总浓度(mg·L−1);K是微生物降解一阶动力学参数(d−1);t1/2是半衰期(d)。
1.1. 供试菌剂及菌悬液制备
1.2. 仪器、药品和培养基
1.3. 测试分析方法
1.3.1. DBP提取及检测方法
1.3.2. 扫描电镜样品的制备
1.4. DBP混合菌固定化及正交试验
1.5. 固定化混合菌DP3和固定化空白凝胶球对DBP降解率的测定
1.6. 不同环境因素对固定化和游离态微生物降解性能的比较
1.7. 固定化DBP混合菌的长期稳定性及模拟人工污水DBP降解试验
1.8. 降解动力学模型
-
为考察聚乙烯醇(PVA)、海藻酸钠(SA)、活性炭(AC)、CaCl2浓度等4种因素对包埋小球降解DBP能力的综合影响,确定固定化载体最佳制备条件,以DBP去除率为目标值设计正交试验,结果如表2所示。对比各因素所对应的R值可知,各因素对固定化混合菌降解DBP能力的影响由大到小依次为C:AC含量>A:PVA含量>B:SA含量>D:CaCl2含量,根据各因素所对应的Ⅰj、Ⅱj、Ⅲj可知各因素之间最优组合为A2B2C3D1。
-
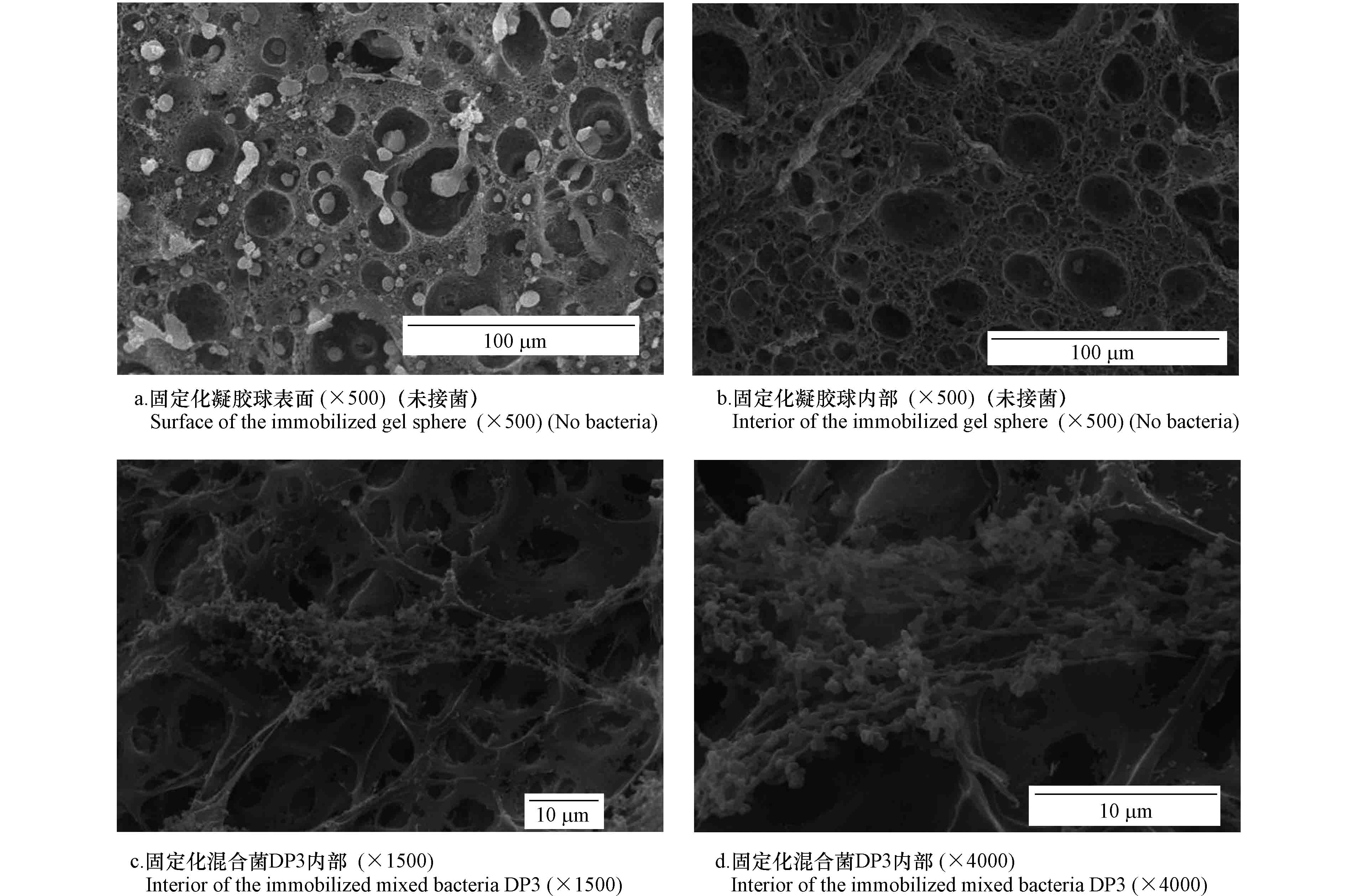
固定化空白和微生物凝胶球进行扫描电镜前处理制备,喷金后观察其表面和内部结构,结果如图1所示。由图1(a)可以发现,固定化空白凝胶球的表面不光滑,存在密集的孔穴;从图1(b)可知,在固定化空白凝胶球内部,PVA-SA-AC复合材料构筑由孔道相互连通的大量空腔,呈孔网结构。图1(c)、(d)发现,混合菌DP3以网状菌落交织被复合材料包埋吸附在凝胶球的内部,由于菌体明显小于内部孔径,有利于微生物在内部的自由运动、增殖和快速摄取营养物质和溶解氧[17]。邻苯二甲酸二丁酯分子自由进入凝胶球内部与微生物产生作用被降解,外密内疏结构对维持固定化微生物良好的内部环境起到了重要的作用,是保证固定化混合菌较高DBP降解率的重要因素。
-
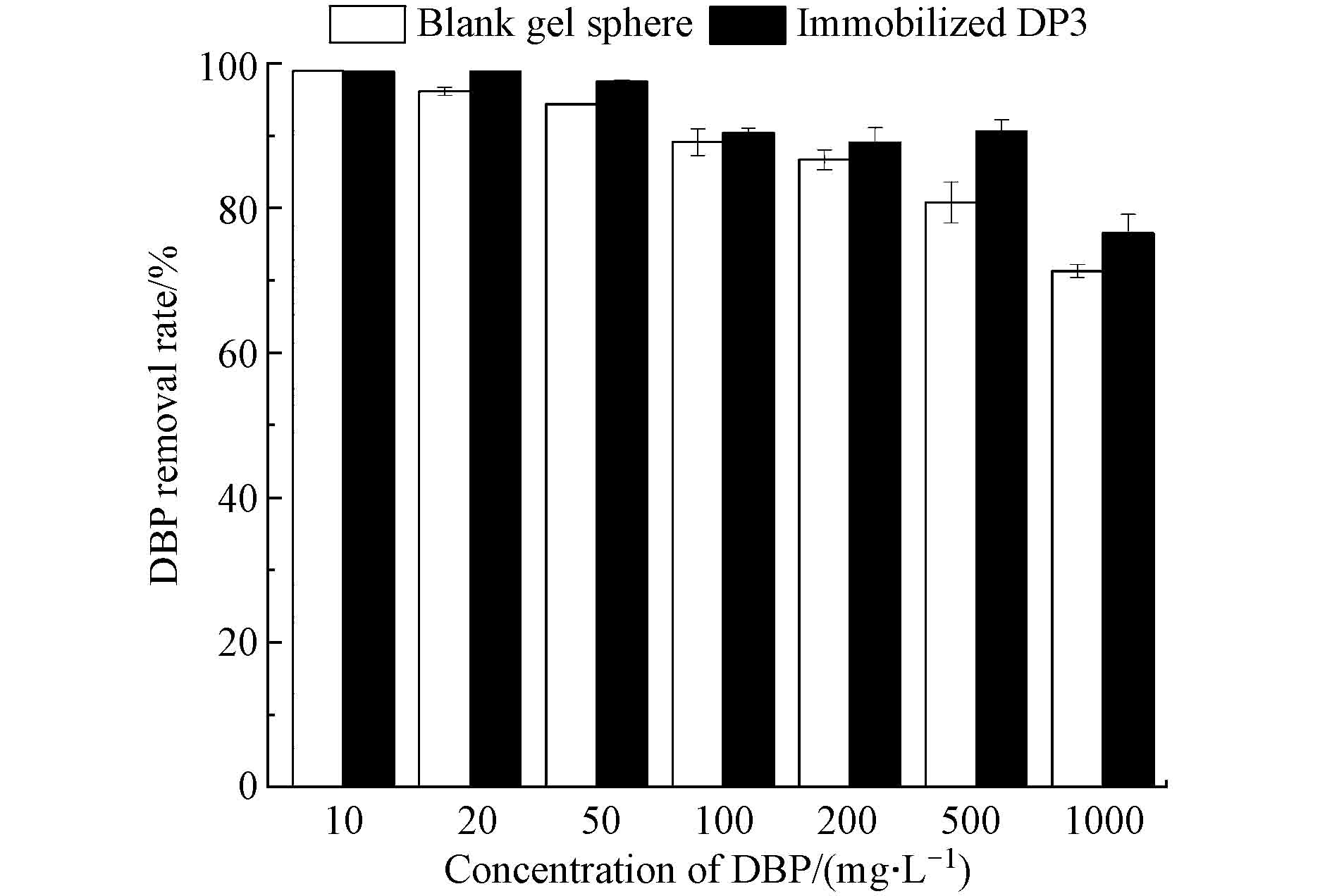
为了解固定化混合菌DP3去除DBP的机理,对比了固定化DP3和空白凝胶球对DBP的去除效果,结果如图2所示,DBP的浓度为10 mg·L−1时,固定化DP3和空白凝胶球对DBP的去除率均能达到99%以上;DBP的浓度在20—200 mg·L−1时,空白凝胶球对DBP的去除率呈现缓慢下降趋势,DBP的浓度为500 mg·L−1时,吸附平衡达到相对饱和,同时,DBP浓度的升高,为负载在小球中混合菌DP3提供可利用碳源,进而提高了微生物的活性[18],所以,DBP浓度在500—1000 mg·L−1时,固定化DP3对DBP去除效率显著优于空白凝胶球,随着DBP浓度的降低,平衡向吸附作用方向移动,残余的DBP被吸附至小球内被微生物降解,由此可见,经过包埋-吸附联合固定化后的混合菌DP3能够保持较高生物活性。
-
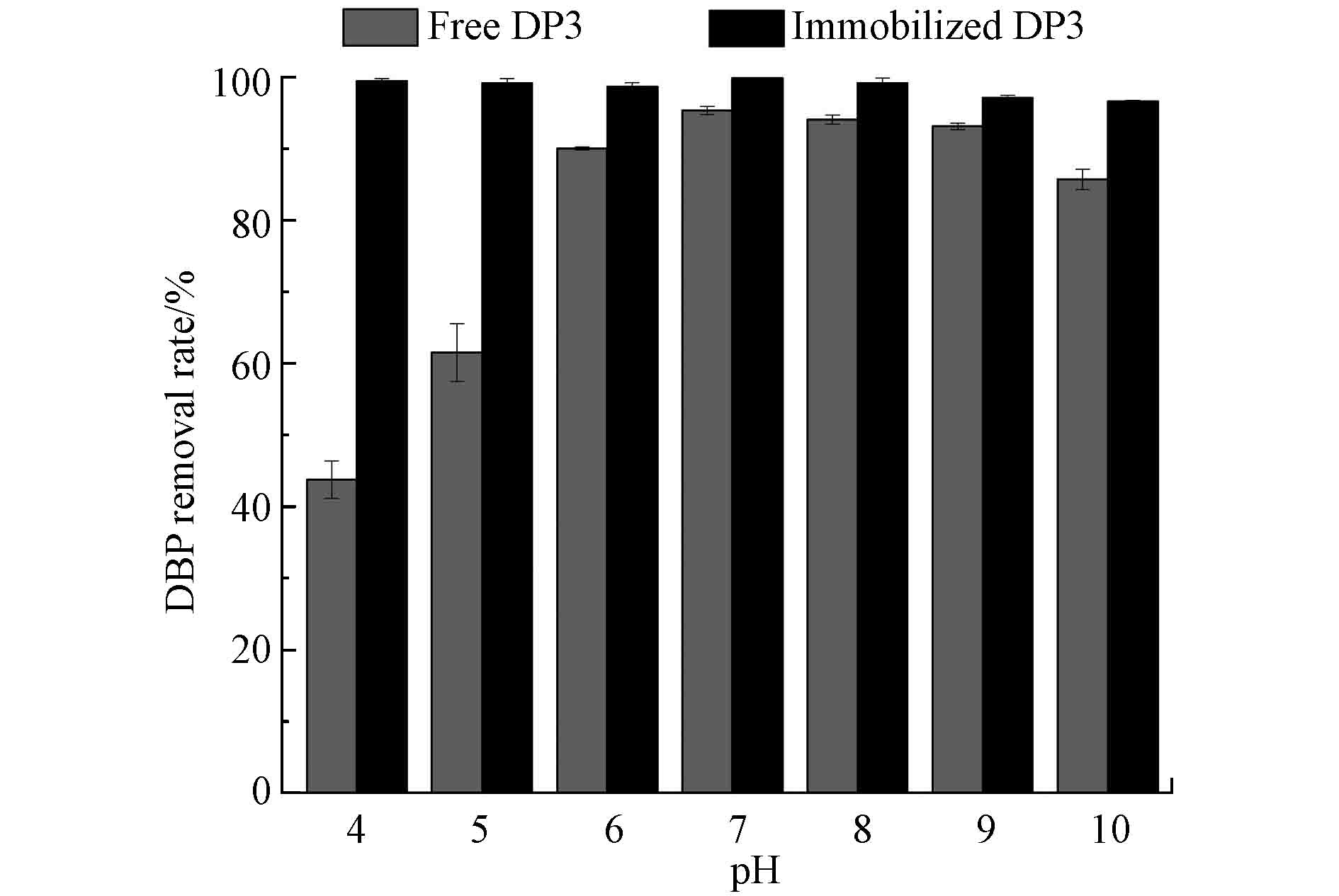
以游离态混合菌DP3为对照,开展了pH值对固定化DP3降解DBP的影响研究,如图3所示,pH值在6—9时,固定化和游离态混合菌DP3对DBP的降解能力相对较为稳定,pH值为7时,3 d内对DBP降解率均可达到最大值,而处于较强的酸碱条件时,游离态混合菌DP3的降解能力显著下降,在pH4—6之间时最为明显。而固定化混合菌DP3的pH值变化对DBP降解能力的影响极小,在pH9—10之间有极微小的变化,明显高于游离态混合菌DP3的降解能力。这是由于固定化凝胶球具有外层紧密,向内逐渐松散的结构特征,能够对包埋的混合菌起到一定的保护作用,而且固定化载体上负载的—NH2、—COOH等基团能够对酸碱环境进行缓冲[19]。对于游离态混合菌DP3来说,较强的酸碱条件改变了细胞膜的通透性,并且导致DBP降解酶失活[20-21],从而影响游离态混合菌对DBP的降解能力。所以,固定化混合菌DP3对pH的耐受范围明显高于游离态混合菌DP3,可以保持稳定的生物活性,显示出固定化技术的优势。
-
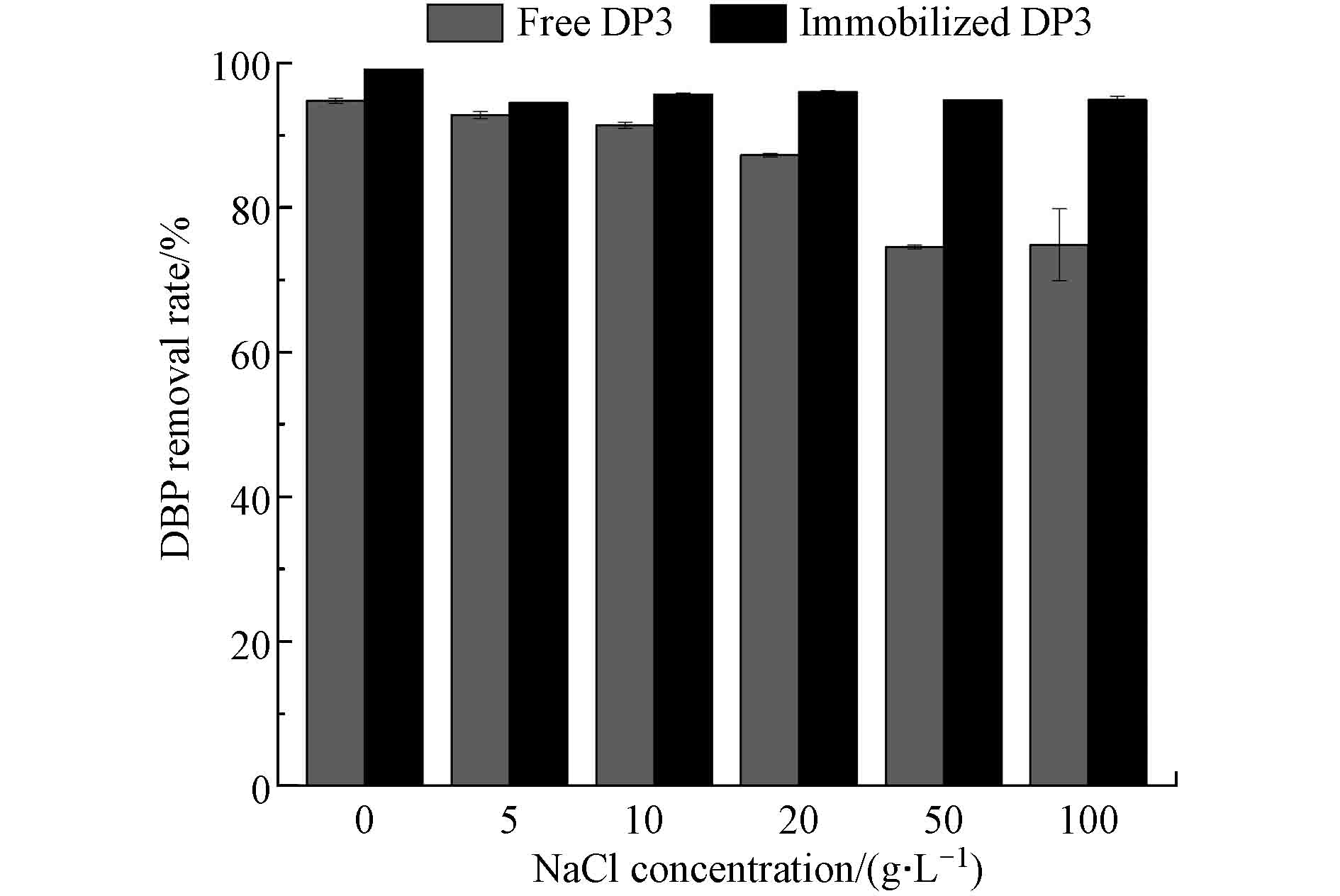
NaCl浓度对固定化和游离态混合菌DP3降解DBP的影响如图4所示,NaCl浓度为0 g·L−1时,固定化和游离态混合菌DP3对DBP在3 d时的降解率均可达到最大值,分别为99.13%和94.77%。NaCl浓度在5—10 g·L−1之间时,游离态混合菌对DBP降解效果较为稳定,NaCl浓度在20—100 g·L−1之间时,随着NaCl浓度增大,游离态混合菌对DBP的降解效果逐渐下降,而固定化后的混合菌对DBP的降解效果较为稳定,且显著高于游离态混合菌的降解效果。这是由于随着盐度提高,细胞内与外界的渗透压逐渐失去平衡,使得细胞内的水分慢慢向外界流失,致细胞脱水,菌株生长受到抑制,进而影响菌株对DBP的降解,而固定化后,固定化材料对混合菌起到良好的保护作用并为其提供一个适宜的生长环境,随着NaCl浓度增大,固定化复合菌对DBP的降解效果也有所降低,这可能是由于小球外表面附着的混合菌受到NaCl浓度影响,而失去活性,从而影响其对DBP的降解效果。
-
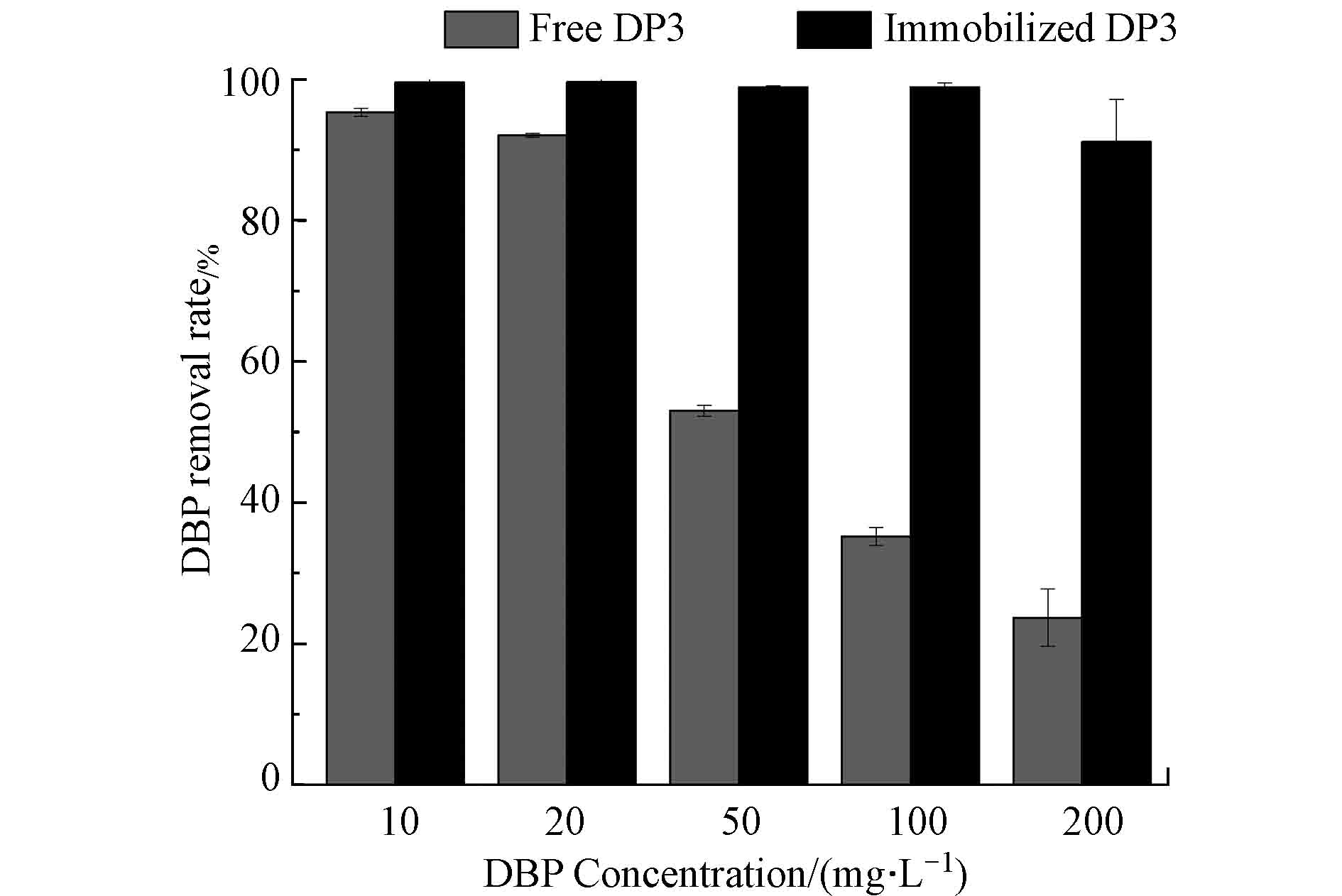
DBP浓度对固定化和游离态混合菌DP3降解DBP的影响如图5所示,当DBP浓度处于10—20 mg·L−1时,固定化和游离态混合菌DP3对DBP有着显著的降解作用,而且DBP浓度为10 mg·L−1,时,1 d内固定化混合菌DP3对DBP降解效果可达到98.84%,与游离态混合菌相比,其降解率显著提高35.11%,当DBP浓度大于20 mg·L−1时,随着DBP浓度的增加,游离态混合菌DP3对DBP的降解能力明显下降;而固定化混合菌DP3对DBP的降解能力随着DBP浓度的增加较为稳定,且显著高于游离态混合菌DP3。在DBP浓度为200 mg·L−1时,固定化混合菌DP3对DBP在3 d时的降解效果仍可达到91.15%。这是由于DBP具有细胞毒性[22],高浓度的DBP会抑制菌株的生长,进而影响游离态混合菌对DBP的降解效率,而固定化材料具有外紧内松的结构特征,DBP向内部扩散时浓度递减,对混合菌起到良好的缓冲作用[23]。可知,固定化的混合菌微生物密度较高,包埋、吸附材料对于DBP的吸附作用也可使微生物与污染物更好的接触,从而使得固定化混合菌对高浓度DBP降解能力明显高于游离态混合菌。
-
固定化和游离态混合菌DP3降解不同浓度的DBP(10、20、50、100、200 mg·L−1),从拟合方程(表3)可知,固定化和游离态混合菌DP3对底物降解符合一阶动力学方程,随着底物浓度的逐渐增大,固定化DP3对其降解性能降低,说明固定化DP3对底物DBP的浓度具有一定的耐受范围。相对游离态,降解同等浓度的底物,固定化DP3的半衰期缩短,降解速度明显增加,对底物DBP的耐受性增强,据推测是因为包埋载体的底物传质阻力降低了高浓度有毒底物的冲击,同时负载的微生物密度较高,少量菌体失活不会对整个体系微生物的降解活性产生影响[24]。
-
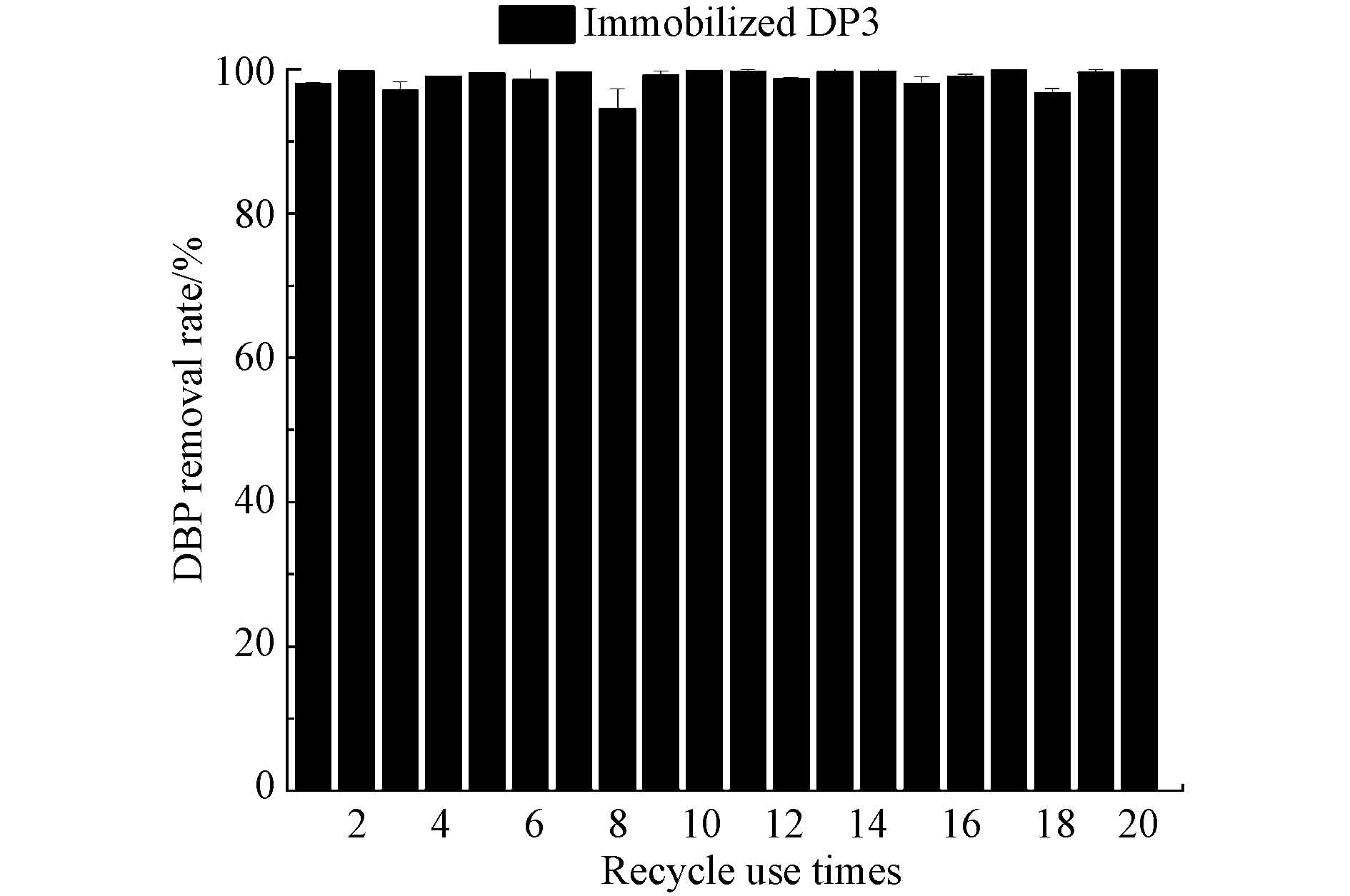
为考察固定化混合菌DP3重复使用的稳定性,在固定化DP3最佳制备和环境条件下,对10 mg·L−1 DBP进行降解实验,固定化混合菌DP3凝胶球重复循环使用20次,结果如图6所示,凝胶球始终保持良好的降解活性,且稳定,1 d内,重复20次固定化混合菌DP3对DBP的降解效果仍能达到99.95%,说明固定化混合菌在前期使用中受到DBP的驯化,催化其生物活性,重复过程中优化了降解性能,反映出固定化混合菌DP3降解DBP具有优异的长期稳定性,这就为实际应用中奠定了理论基础,达到节约成本的目的[25]。
-
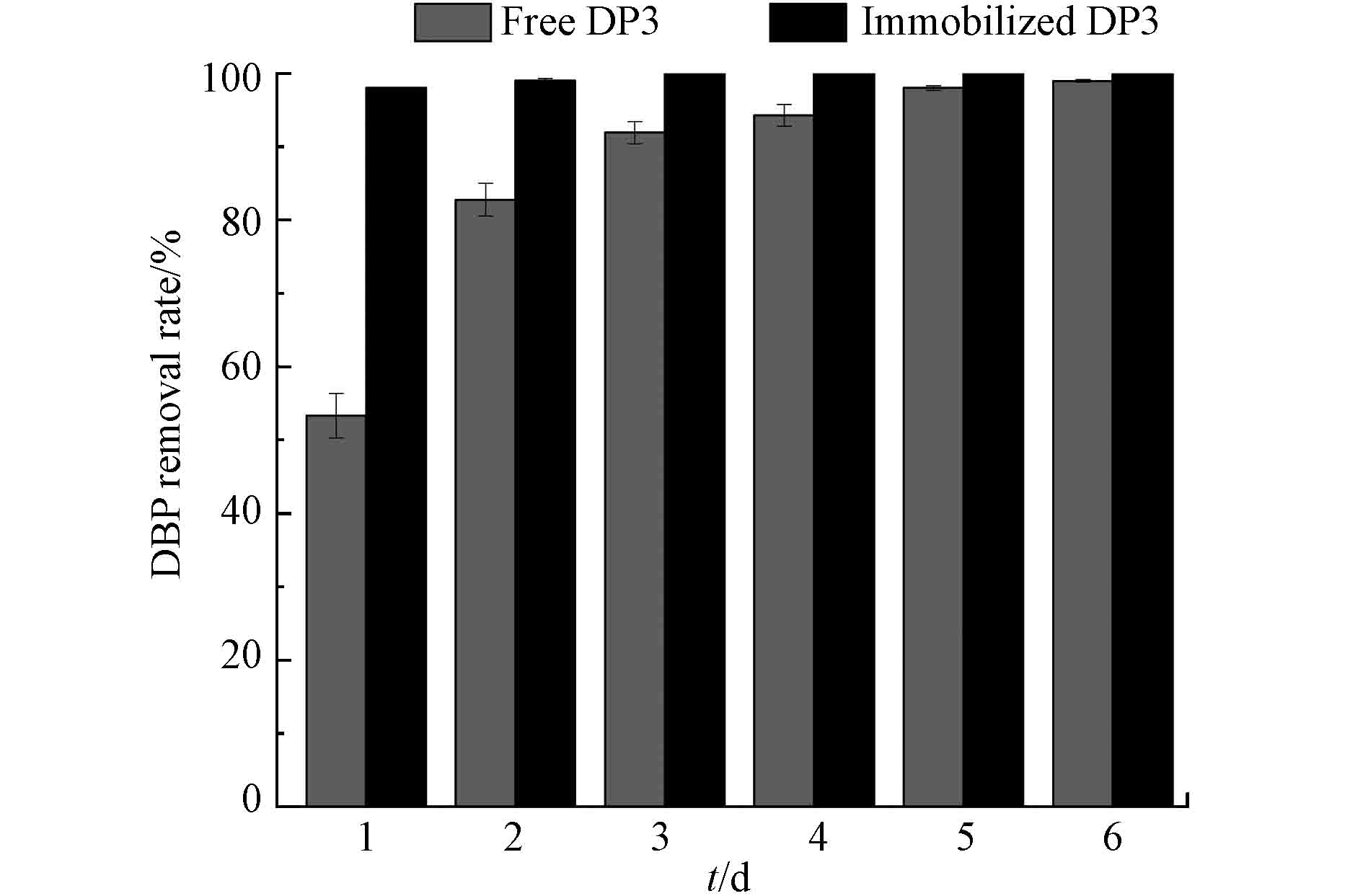
为验证固定化混合菌在实际生产中的降解能力,将固定化混合菌DP3加入10 mg·L−1 DBP的模拟人工污水中,以游离态混合菌DP3作为对照,由图7结果显示,在1 d时,游离态DP3对DBP的降解率为53.33%,固定化DP3为98.03%,降解效率显著提升,2 d后,固定化DP3达到99.98%,模拟人工污水中的DBP几乎可以完全降解,结果表明,固定化混合菌DP3表现出良好的降解能力,具有显著的应用价值。
2.1. DBP降解混合菌固定化条件优化
2.2. DBP降解混合菌固定化凝胶球微观结构分析
2.3. 固定化混合菌DP3和空白凝胶球对DBP的降解性能
2.4. 不同环境因素对固定化混合菌DP3降解能力的影响
2.4.1. pH
2.4.2. NaCl浓度
2.4.3. DBP浓度
2.4.4. 固定化混合菌DP3和游离态混合菌DP3的降解动力学
2.5. 固定化混合菌DP3的长期稳定性
2.6. 固定化混合菌降解模拟人工污水的DBP
-
(1)采用正交试验确定固定化混合菌DP3的最佳制备条件为:聚乙烯醇(PVA)质量分数10%,海藻酸钠(SA)质量分数2%,活性炭(AC)质量分数3%,CaCl2质量分数1%。与游离态混合菌的降解效果相比,该条件下所制备的固定化混合菌DP3,1 d时对DBP的降解效果可达到98.84%,降解率提升35.11%。
(2)考察了不同环境条件(pH值、NaCl浓度、底物浓度)对固定化与游离态混合菌DP3降解DBP的影响,在pH4—10、NaCl浓度在5—100 g·L−1、底物浓度在10-200 mg·L−1时,对DBP的降解率均在90%以上,固定化混合菌DP3的降解率显著优于游离态混合菌。此外,固定化混合菌DP3在模拟人工污水中1 d时对DBP的降解率可达98.03%,
(3)固定化混合菌DP3对底物降解符合一阶动力学方程,相比游离态而言,降解同等浓度的底物,固定化DP3的半衰期缩短,降解速度明显增加,对底物DBP的耐受性增强。同时,固定化混合菌DP3重复对DBP进行降解20次,降解效果仍可达到99.95%,且无破碎现象。SEM扫描结果表明固定化混合菌DP3以网状菌落交织被复合材料包埋吸附在凝胶球的内部。进一步证实并解释了固定化混合菌具有较高DBP降解效率的原因。



 下载:
下载: