-
溴代阻燃剂(brominated flame retardants,BFRs)具有成本低、阻燃性能强及材料相容性好等优势,是产量最高的有机阻燃剂之一[1]. 其中,四溴双酚A(tetrabromobisphenol A,TBBPA)应用范围最广[2-3]. 目前TBBPA已在各种环境介质中被检出[4-7],且具有内分泌干扰性和生物毒性[8-9],因此TBBPA的处理研究已成为学者们关注的热点.
TBBPA的去除方法大致可分为物理法(萃取法和吸附法)、化学法(光降解法、超声波降解法、氧化法和还原法等)和生物法[10-14]. 其中,电催化还原技术具有降解效率高、反应条件温和、不生成有毒副产物等优点,被视为很有发展前景的有机物脱卤处理技术[15-17]. 催化剂是污染物成功降解的重要因素之一,而Pd具有较强的活化氢气的能力,且析氢电位较低,因此常被视为理想催化活性组分[18-19]. 现有研究通常将催化剂固定在电极表面并以此作为阴极电极,但存在活性组分利用率低的问题[20].
本文采用浸渍法将Pd负载到不同载体上,将制备的催化剂均匀分散于阴极反应池中对TBBPA进行电催化还原脱溴,研究了载体、负载量和电流大小对反应初活性的影响,并对催化剂的可重复利用性进行评估.
-
本文所用载体有TiO2(Degussa公司)、Al2O3(上海五四化学试剂有限公司)、CeO2(沉淀法合成)和SiO2(上海奉贤奉城试剂厂). 为去除杂质,载体需纯化处理. 取定量TiO2、Al2O3、CeO2和SiO2放入坩埚,分别以300、500、600 ℃和300 ℃焙烧4 h.
CeO2的合成:配制250 mL 0.5 mol·L−1 Ce(NO3)3溶液,逐滴加入0.5 mol·L−1氨水,调节pH为10.0,室温持续搅拌1 h后抽滤、洗涤、105 ℃烘干,即可得到CeO2固体.
催化剂的制备(以质量分数为2%的Pd/TiO2为例):在烧杯中加入1 g载体(TiO2)、10 mL去离子水和8.332 mL PdCl2(4 g·L−1)溶液,室温下持续搅拌2 h后90 ℃水浴蒸干. 得到的固体在105 ℃烘箱充分烘干,接着在300 ℃马弗炉中焙烧4 h,冷却压片后在H2(300 ℃,40 mL·min−1)氛围中还原2 h,最后研磨过筛(100目),得到Pd(x)/TiO2,其中x为实际Pd负载量.
-
使用电感耦合等离子体-发射光谱仪(ICP-OES,美国Jarrel-Ash公司,J-A1100)对催化剂的Pd实际负载量进行测定分析;使用透射电子显微镜(TEM,日本电子株式会社,JEM-200CX)观察催化剂的微观形貌特征;使用X射线衍射仪(XRD,日本理学株式会社,D/max-RA)对催化剂进行物相分析;使用X射线光电子能谱仪(美国赛默飞世尔科技公司,ESCALAB250)分析催化剂表面Pd的化学形态;使用Zeta电位仪(Zeta PALS Brookhaven公司)测试不同载体Pd基催化剂表面电荷量.
-
泡沫镍的预处理:为除去泡沫镍表面的有机污层及镍氧化层,用丙酮溶液浸没裁剪好的泡沫镍片,超声处理20 min后,用去离子水冲洗掉残余丙酮,再用80 g·L−1硫酸浸没,超声处理5 min后,用去离子水冲洗至中性.
Pd/TiO2修饰的泡沫镍电极的制作:称取30 mg的Pd(1.99)/TiO2催化剂,放入离心管中,再加入1 mL Nafion(5%)和2 mL无水乙醇,混合均匀. 用移液枪(200 μL枪头)共吸取混合液1.5 mL,小心均匀涂抹于预处理后的泡沫镍片上,自然晾干后,即可得到Pd/TiO2修饰的泡沫镍电极.
-
本文选用双室反应池进行TBBPA的电催化还原反应,两侧反应池被质子交换膜分隔,体积相等(略大于100 mL). 采用传统的三电极系统,其中泡沫镍片(2 cm×5 cm)、铂片电极(1 cm×1 cm)和Ag/AgCl电极分别作为阴极电极、阳极电极和参比电极(阴极). 实验步骤如下:在阳极反应池内加入100 mL 5 mmol·L−1 Na2SO4溶液,阴极反应池加入一定量的TBBPA储备液,之后用5 mmol·L−1 Na2SO4溶液稀释至100 mL,并用1 mol·L−1 NaOH溶液调节pH=10.5. 在恒速(1000 r·min−1)搅拌条件下加入定量的催化剂,接着向阴极反应液中通氩气(40 mL·min−1),以排除反应液中氧气的影响. 30 min后连接电路,并在预设时间点收集样品,样品过0.22 μm滤膜后,通过高效液相色谱(HPLC,Aglient公司,1200)测定其中的TBBPA浓度. 其中,进样量为5 μL,流动相为
$ {V}_{{{\rm{CH}}}_{3}{\rm{OH}}} $ :$ {V}_{{{\rm{H}}}_{2}{\rm{O}}} $ =76:24的混合溶液,检测所用的紫外光波长为230 nm. TBBPA脱溴的中间产物通过液相色谱-质谱联用(HPLC-MS,Aglient公司,6500)进行定性检测,反应2 h后样品中的溴离子通过离子色谱(HPIC,Dionex公司,ICS-1100)进行检测.本文选用反应初活性(r0,mmol·L−1·g−1·h−1)评价不同催化剂的活性,表示当去除率低于25%的反应阶段,单位时间内单位质量催化剂降解的TBBPA浓度.
-
为了解催化剂的表面形态和表面元素信息,进行了Pd含量分析、TEM表征、XRD表征、XPS表征和Zeta电位测定. 其中,催化剂的基本性质见表1. 合成不同载体(TiO2、Al2O3、CeO2 和 SiO2)负载的 Pd 基催化剂和不同负载量(质量分数为 0.50%、1.00%、2.00% 和 3.00%)的 Pd/TiO2 催化剂,电感耦合等离子体-发射光谱仪(ICP-OES)测定实际 Pd 负载量(表 1 ),实际负载量与理论负载量基本一致.
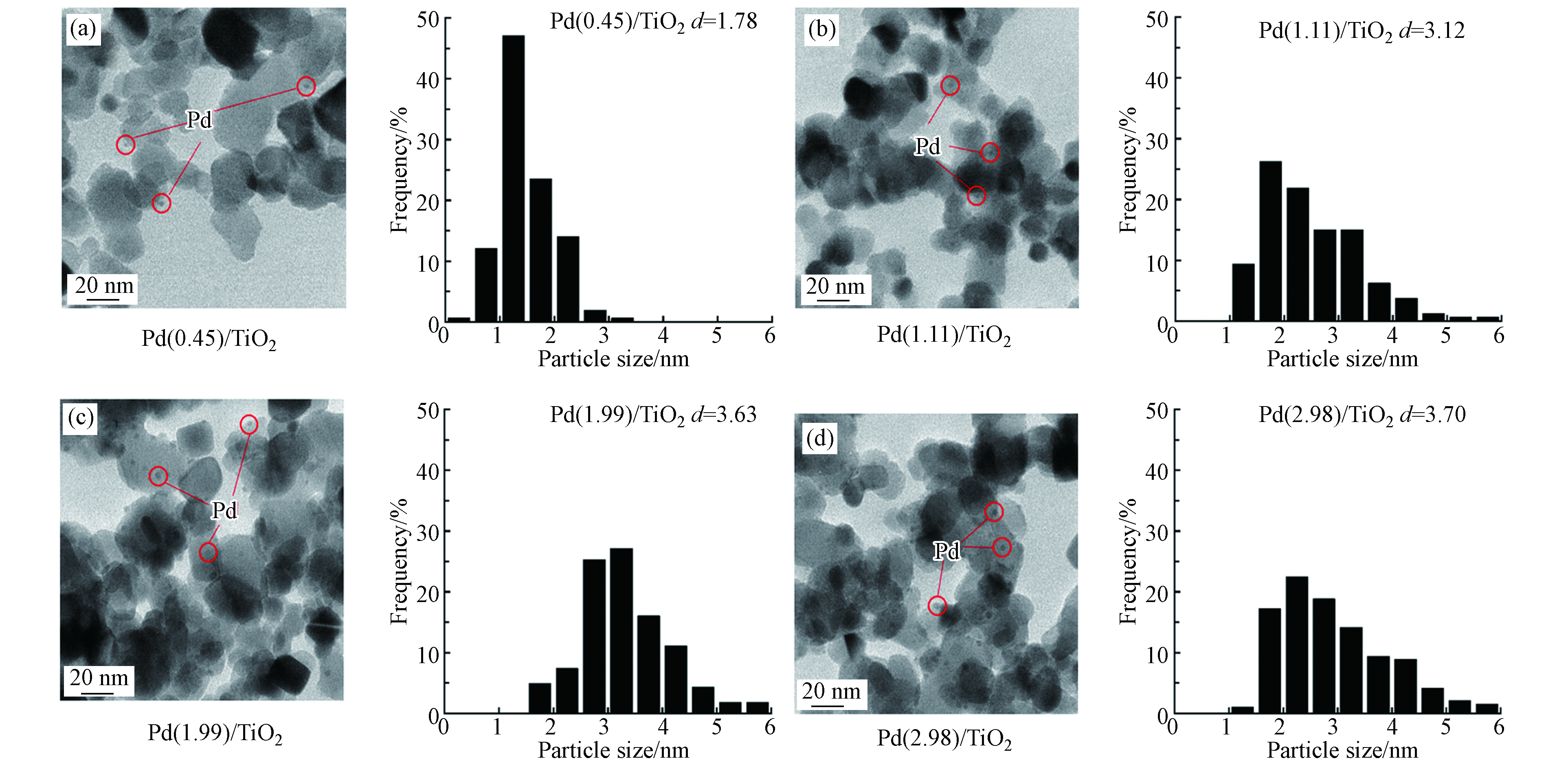
通过TEM图可以直观地观察Pd纳米颗粒的存在状态,再由公式(1)可计算Pd颗粒的平均粒径:
其中,ni(>150)表示直径为di(nm)的Pd纳米颗粒的数量,
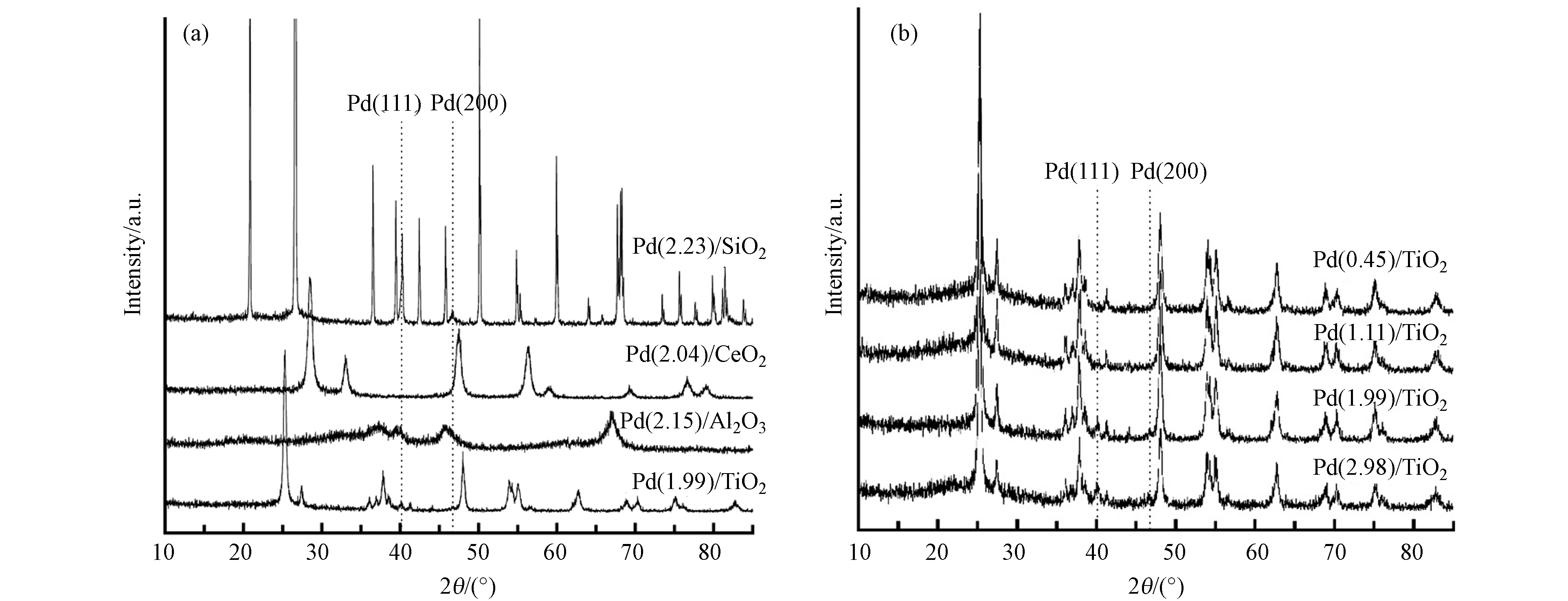
$ \stackrel{-}{{d}_{s}} $ (nm)表示平均粒径. 从表1及TEM图(图1)可以看出,Pd颗粒均匀地负载在TiO2上,且随着负载量增大,Pd颗粒的平均粒径逐渐增大. 可能是随着负载量增大,Pd 在载体表面分散度降低、团聚在一起.对催化剂进行了XRD测试,结果如图2所示。从图2(a)可以看出,对于Pd(1.99)/TiO2、Pd(2.15)/Al2O3和Pd(2.23)/SiO2催化剂,在2θ为40.1°和46.7°处能够明显观察到衍射峰,分别对应Pd(111)和Pd(200) 晶面,表明金属Pd成功负载到了金属氧化物载体上[21]. 而Pd(2.04)/CeO2催化剂未观察到Pd特征峰,可能是因为催化剂表面Pd纳米颗粒粒径较小. 从图2(b)中可以看出,随着负载量的增大,Pd的(111)和(200)晶面的特征衍射峰逐渐增强,说明Pd纳米颗粒的粒径随Pd含量增大而逐渐增大,这也与TEM的结果一致.
对不同负载量的Pd/TiO2催化剂进行了XPS测试,以分析Pd的化学形态. 图3为Pd 3d的XPS谱图,可观察到Pd 3d5/2区域的谱峰可被分为两个,结合能位置分别为334.6 eV和336.8 eV,对应Pd0和Pdn+. 表1记录了各负载量Pd/TiO2催化剂的Pdn+/Pd0值,随着负载量增大,比值逐渐减小. Pdn+是金属与载体间存在较强作用力导致的Pd电子转移形成的,当负载量变大,Pd颗粒粒径变大,其与TiO2间的作用力变小,因此Pdn+减少、Pdn+/Pd0值降低[22].
-
在电催化还原脱溴过程中,TBBPA会逐渐部分脱溴直至完全脱溴. 为鉴定TBBPA中间产物和最终产物,本文通过高效液相色谱和液质联用两种技术对不同时间阴极电解液进行分析. 实验条件:TBBPA初始浓度约为0.1 mmol·L−1、pH=10.5,Pd(1.99)/TiO2催化剂用量为15 mg,恒定电流为15 mA.
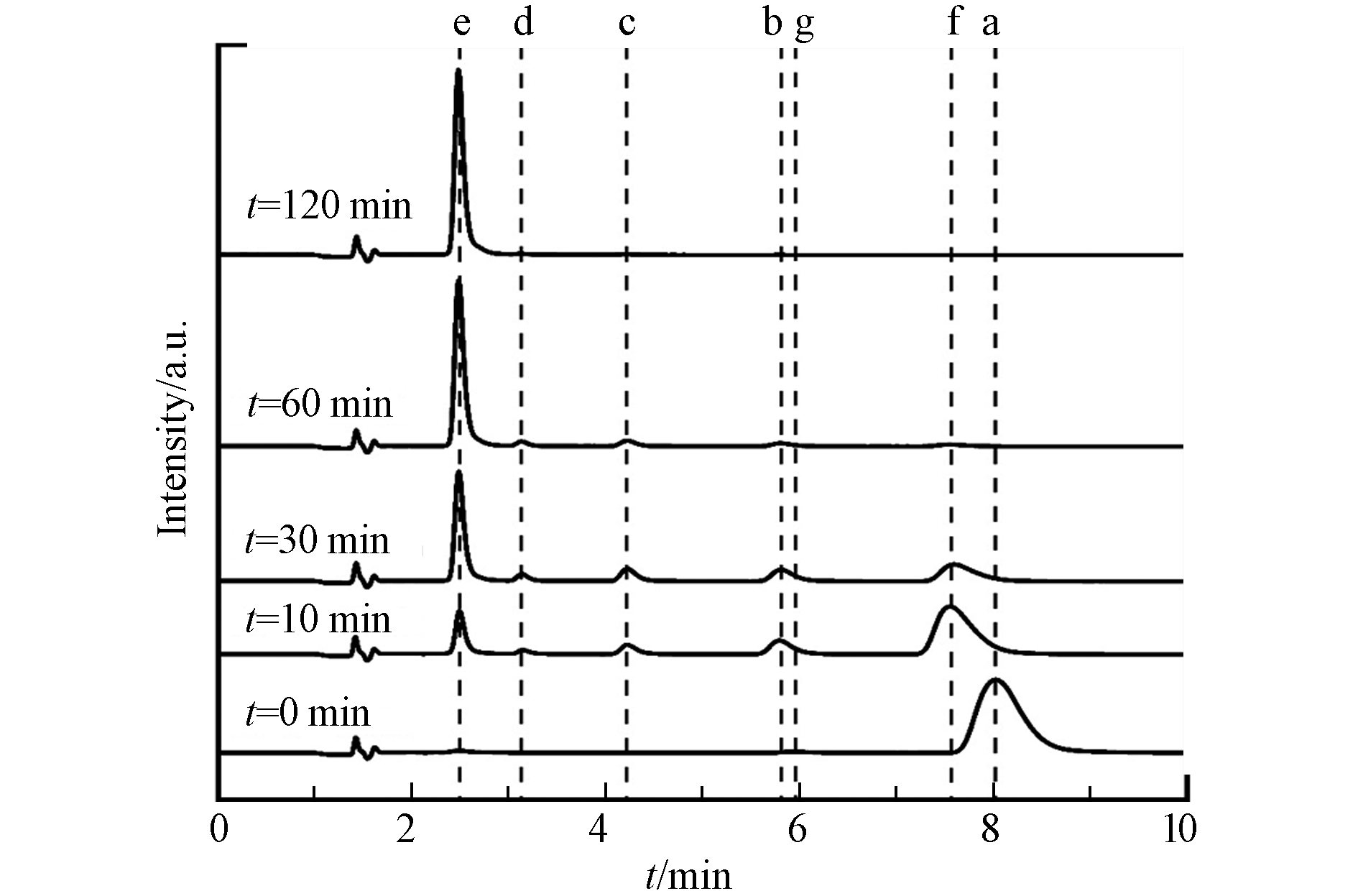
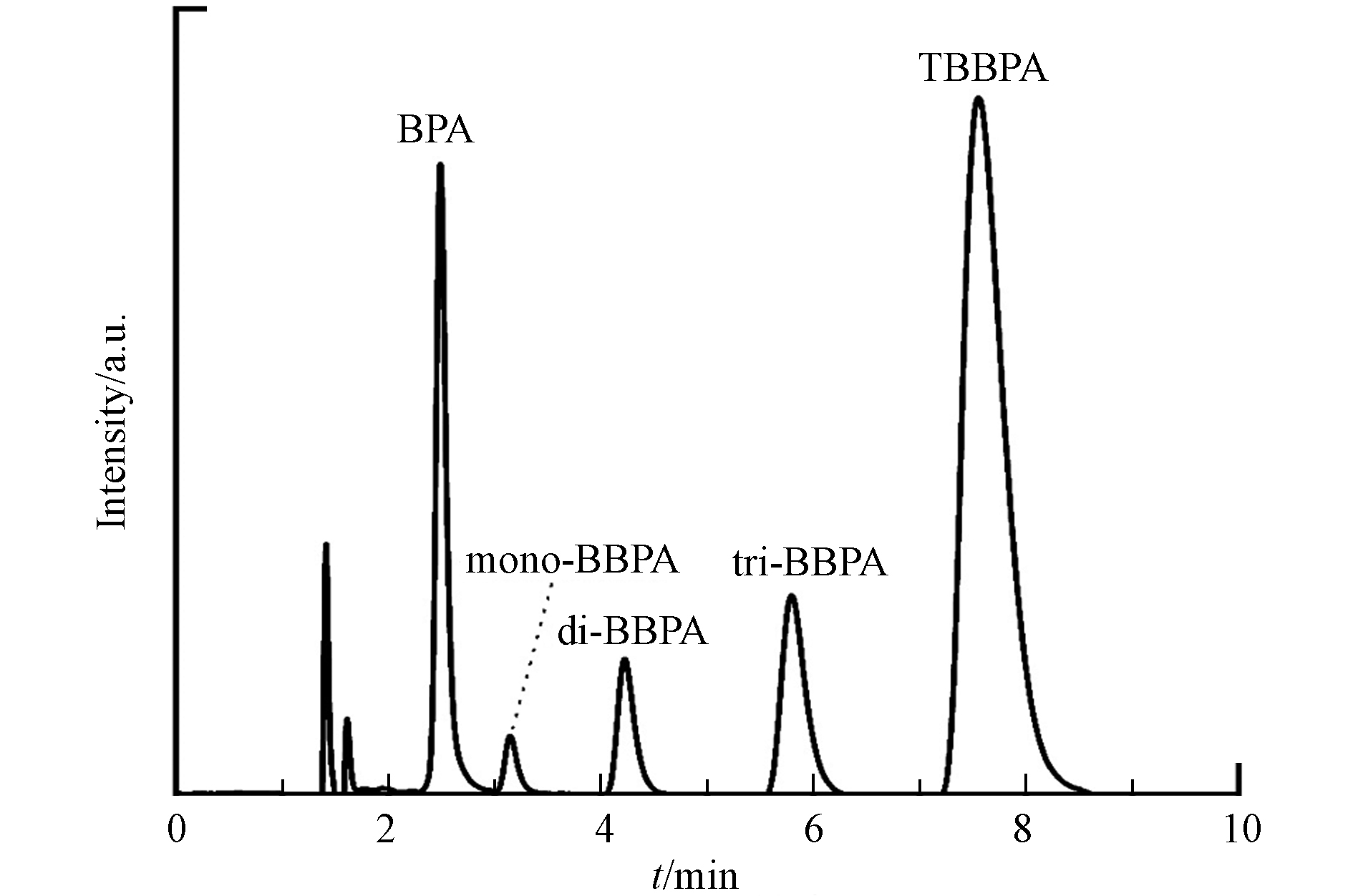
结合标准物分析液相色谱图(图4),反应0 min时出峰时间8.00 min的峰为TBBPA,反应120 min时出峰时间2.48 min的峰为完全脱溴产物双酚A(BPA). 反应10、30、60 min时,出峰时间3.13、4.22 、5.80 min的峰为不同中间产物峰. 图中峰随反应时间的偏移是由阴极电解液pH发生变化引起. 图5是通过液质联用技术测试分析反应10 min的电解液得到,出峰时间为2.48、3.13、4.22、5.80 、7.60 min的5个峰,质核比分别为227.11、307.02、384.93、464.84和542.75,对应双酚A(BPA)、一溴双酚A(mono-BBPA)、二溴双酚A(di-BBPA)、三溴双酚A(tri-BBPA)和四溴双酚A(TBBPA). 同时反应结束后检测了阴极电解液的溴离子浓度,为0.396 mmol·L−1,与理论浓度0.4 mmol·L−1基本一致.
-
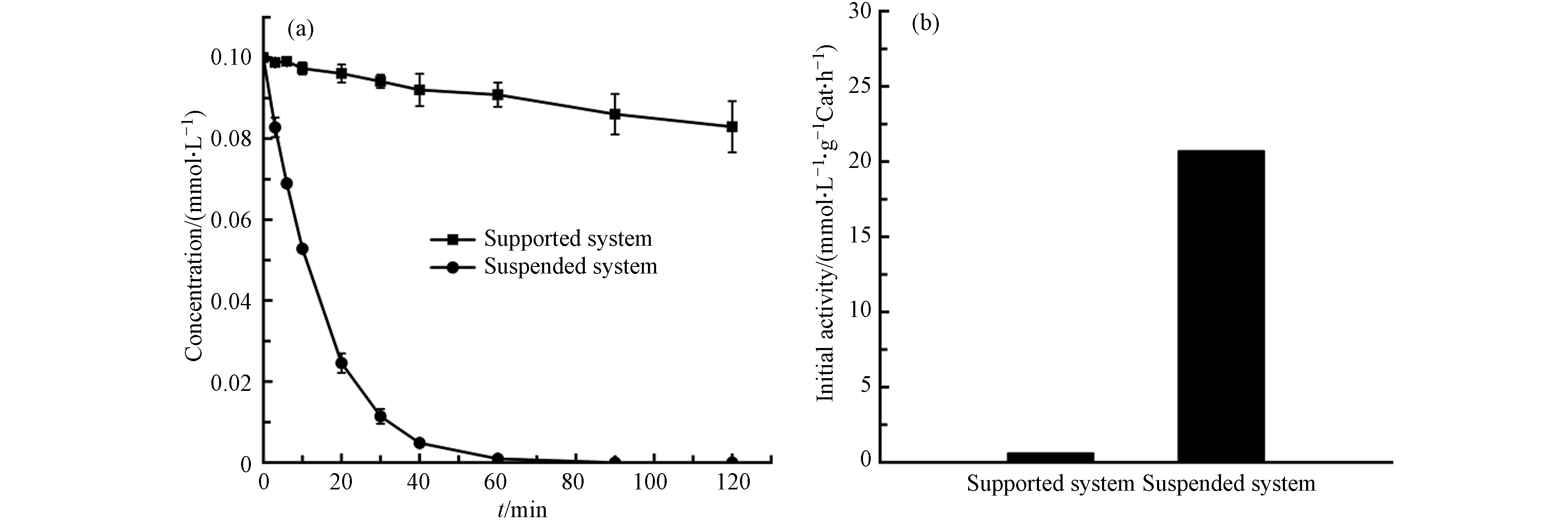
为探究Pd基催化剂的存在形式对TBBPA降解效果的影响,采用将催化剂均匀分散于阴极反应池(悬浮型)和固定到泡沫镍电极表面(固定型)两种方式进行TBBPA的电催化还原反应. 其中,TBBPA初始浓度约为0.1 mmol·L−1、pH=10.5,Pd(1.99)/TiO2催化剂用量为15 mg,恒定电流为15 mA.
从实验结果看出(图6),不论是反应速率还是反应初活性,悬浮体系均明显高于固定体系. 这主要是由于在悬浮体系中,Pd基催化剂具有更高的比表面积和反应活性面积,拥有更高的活性点位利用率,可吸附更多的TBBPA促进其浓缩转移. 由此可见,在本文实验条件下,以悬浮体系代替固定体系,能够有效提高Pd基催化剂对TBBPA的电催化还原活性和去除速率.
-
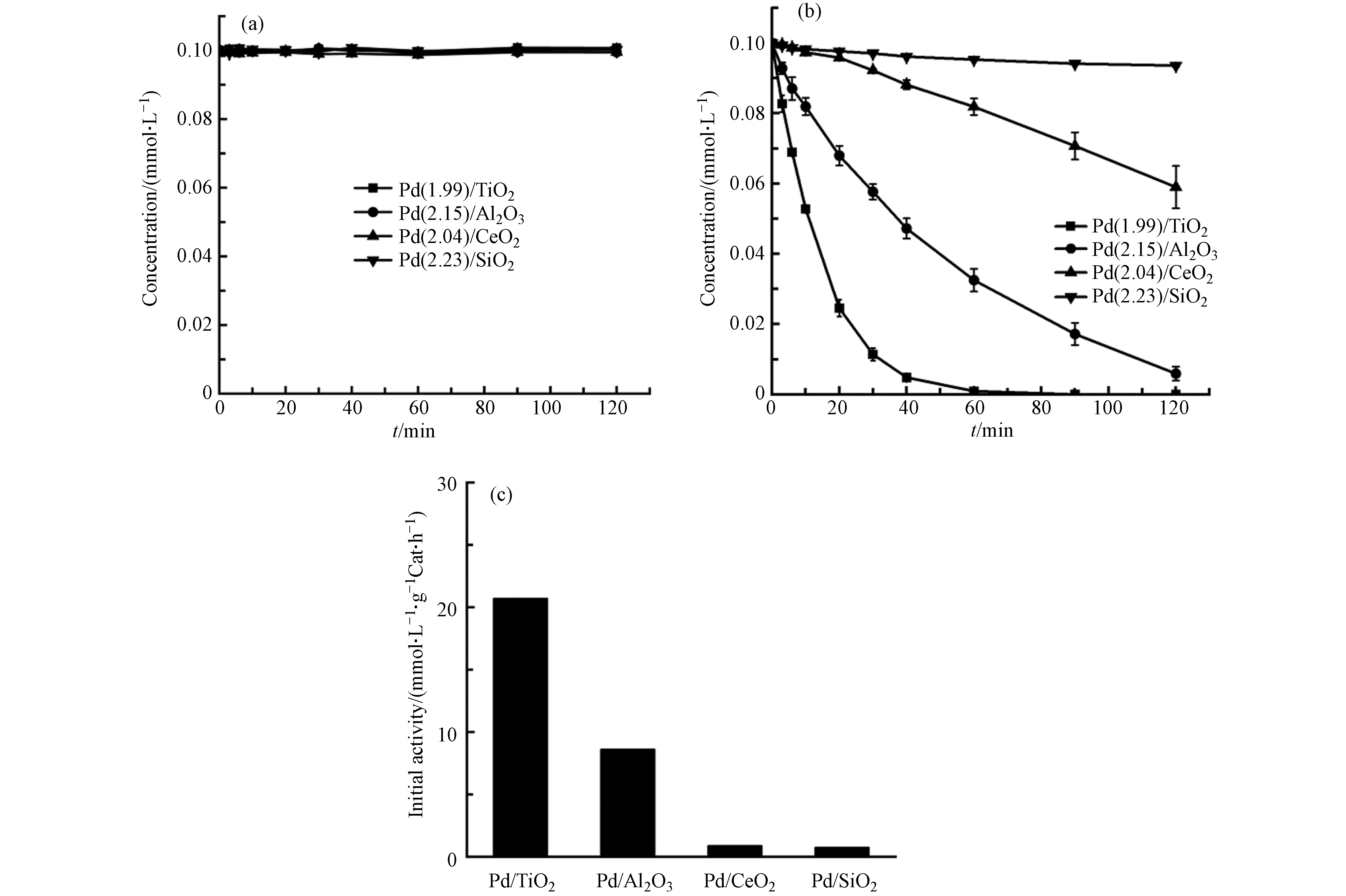
为探究悬浮反应体系中Pd基催化剂的载体对TBBPA电催化还原反应活性的影响,调节TBBPA初始浓度约为0.1 mmol·L−1、pH=10.5,分别投加15 mg的Pd(1.99)/TiO2、Pd(2.15)/Al2O3、Pd(2.04)/CeO2和Pd(2.23)/SiO2催化剂,在15 mA恒定电流条件下进行电催化还原反应,并在同等条件下(不通电)进行吸附对照试验.通过观察图7(a)可知,不同载体Pd基催化剂对TBBPA的吸附可忽略不计,即TBBPA是被电催化降解而非吸附去除.
反应进行2 h后,Pd(1.99)/TiO2、Pd(2.15)/Al2O3、Pd(2.04)/CeO2和Pd(2.23)/SiO2对TBBPA的去除率分别为100.0%、94.1%、41.0%和6.4%. 考虑到Pd/SiO2的催化效果很差,只对其他3种载体催化剂补充BET实验,结果显示Pd(1.99)/TiO2、Pd(2.15)/Al2O3和Pd(2.04)/CeO2的比表面积数据分别为54.5706、130.56和54.8046,对反应初活性进行比表面积归一化(r0,mmol·L−1·g−1Cat·h−1·m−2)后分别为0.3793、0.0067和0.1569,反应初活性最高的依旧为Pd(1.99)/TiO2. 对催化剂进行了Zeta电位测试,当pH=10.5时,Pd(1.99)/TiO2、Pd(2.15)/Al2O3、Pd(2.04)/CeO2和Pd(2.23)/SiO2表面电荷分别为−31.3 mV、−33.0 mV、−35.5 mV和−36.4 mV,而TBBPA在该pH条件下呈阴离子态,由于Pd(1.99)/TiO2与TBBPA之间的排斥力最弱,使得Pd(1.99)/TiO2的反应初活性最高[23]. 因此,选用TiO2为载体的Pd基催化剂进一步探究不同因素对TBBPA电催化还原反应的影响.
-
为了探究悬浮体系中传质阻力对反应的影响,调节TBBPA初始浓度约为0.1 mmol·L−1、pH=10.5,分别投加5、10、15、20、25 mg的Pd(1.99)/TiO2催化剂,在15 mA恒定电流条件下进行电催化还原反应. 图8可以看到,随着Pd(1.99)/TiO2催化剂投加量的增大,反应速度逐渐提高,但对催化剂投加量归一化后得到的初活性基本不变,表明在本文实验条件下,传质阻力可忽略[24].
-
Langmuir-Hinshelwood 机理是表示反应物吸附于催化剂表面活性点位附近并进行表面反应的一种机理[25] . 反应物在催化剂表面发生吸附是非均相催化反应的前提,因此反应物初始浓度会对反应产生显著影响. 调节TBBPA为不同初始浓度(0.05、0.10、0.15、0.20 mmol·L−1)、pH=10.5,投加15 mg的Pd(1.99)/TiO2催化剂,在15 mA恒定电流下进行电催化还原反应. 从实验结果看(图9),随着TBBPA初浓度不断增大,反应初活性增长变缓. 这是因为催化剂表面活性点位数量固定,当TBBPA浓度较低时,催化剂表面活性点位过剩,吸附量和反应速率均随着TBBPA浓度增大而增大;但当浓度增大到一定程度时,催化剂吸附TBBPA逐渐达到饱和,反应速率增长逐渐变缓.
接着使用Langmuir-Hinshelwood模型进行拟合:
其中,r0表示电催化还原反应初活性,C0表示TBBPA初始浓度,θs表示TBBPA在催化剂表面的覆盖率,k表示反应速率常数,b表示吸附平衡常数.
实验结果显示1/C0和1/r0呈线性关系(R2 = 0.97),基本符合Langmuir-Hinshelwood模型,证实了TBBPA电催化还原反应是吸附控制过程.
-
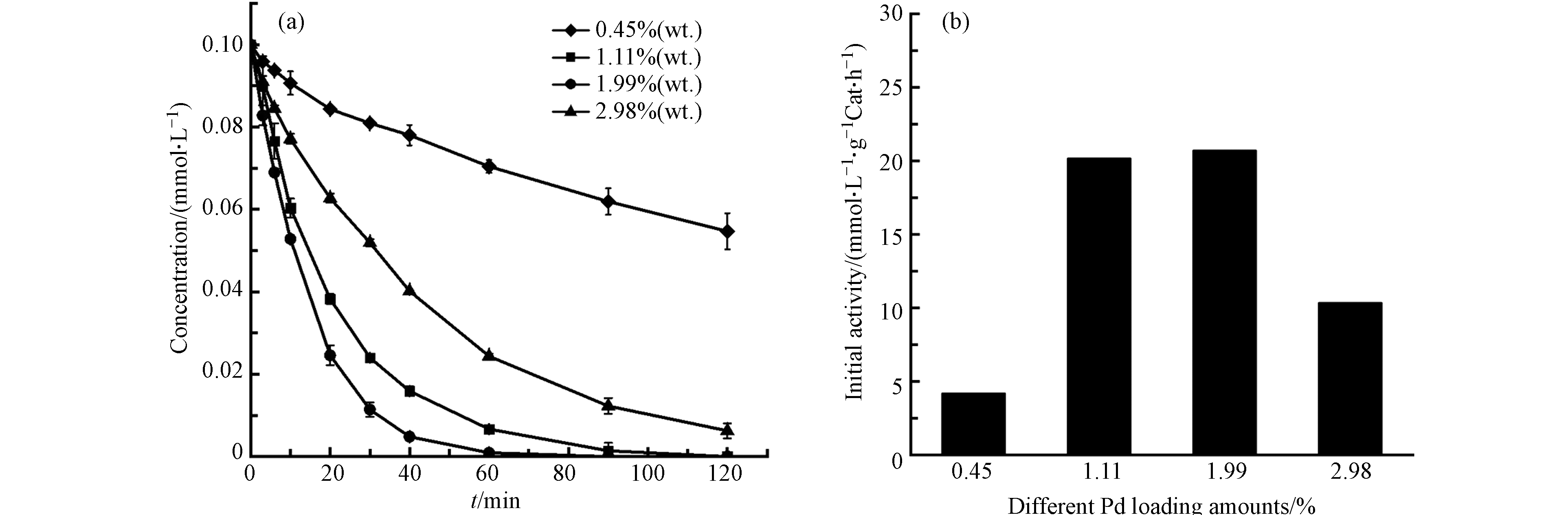
催化剂活性组分的含量会影响催化剂表面活性点位的数量和形态,进而影响催化活性. 调节TBBPA初始浓度约为0.1 mmol·L−1、pH=10.5,分别投加15 mg的Pd(0.45)/TiO2、Pd(1.11)/TiO2、Pd(1.99)/TiO2和Pd(2.98)/TiO2催化剂,在15 mA恒定电流条件下进行电催化还原反应.
实验结果如图10所示,当Pd负载量从0.45%上升到1.99%时,反应初活性不断增大,可能是随着负载量的提高,催化剂提供了更多的Pd活性位点;但当Pd负载量继续上升到2.98%时,反应初活性呈降低趋势,推测一方面是因为Pd颗粒的团聚减小了反应活性面积,另一方面因为Pdn+能活化碳卤键、Pd0能活化氢气,Pdn+占总钯比例减小,会减弱Pd/TiO2催化剂对C-Br键的活化能力[26-27],增强对H—H键的活化能力. 这说明在本反应体系中 C-Br 键的活化要比 H-H 键的活化起着更重要的作用.
-
TBBPA的电催化还原脱溴反应过程可简化为反应式(4)至(10),其中(4)为碱性条件下Volmer过程,会产生H*;(5)表示H*在钯表面形成吸附态;(6)表示TBBPA在钯表面形成吸附态;(7)表示H*作用下TBBPA的加氢还原脱溴;(8)表示加氢脱溴产物的解吸附;(9)表示Heyrovsky过程,即析氢反应;(10)表示氢气(析氢反应提供)被钯基催化剂活化为H*.
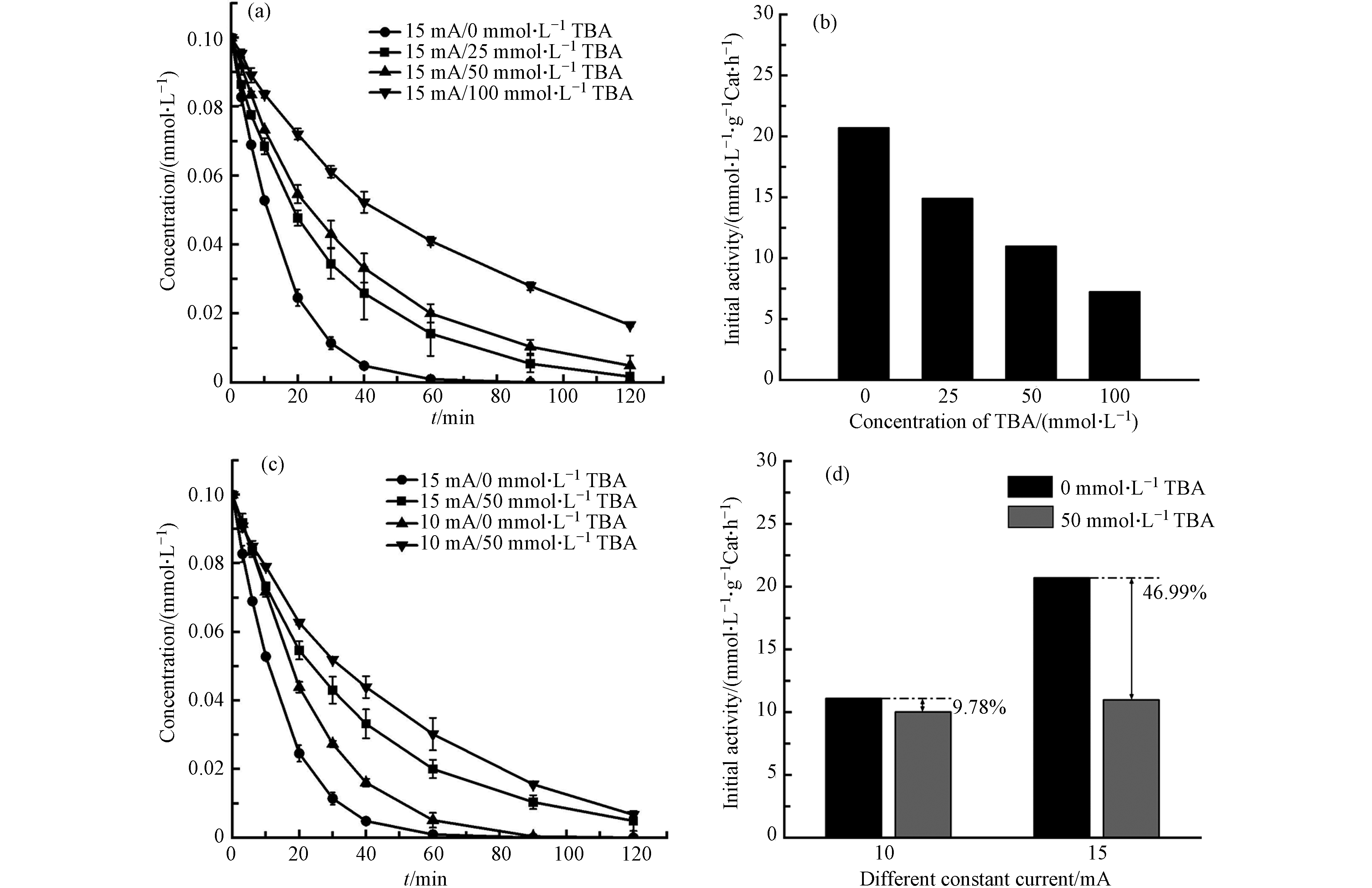
叔丁醇作为一种淬灭剂,常被用于鉴定电催化还原体系中H*的电催化脱卤作用[28]. 调节TBBPA初始浓度约为0.1 mmol·L−1、pH=10.5,投加15 mg的Pd(1.99)/TiO2催化剂、不同剂量的叔丁醇,在不同恒定电流条件下进行电催化还原反应. 从图11(a)和(b)可观察到,随着叔丁醇浓度从0增至100 mmol·L−1,TBBPA的去除率从100.0%降至83.4%,反应初活性降低了65.1%,即叔丁醇对TBBPA电催化还原反应的抑制作用随其浓度升高而不断加强,这说明了H*对TBBPA电催化还原脱溴的重要作用.
从图11(c)和(d)可知,叔丁醇(50 mmol·L−1)浓度一致时,10 mA条件下TBBPA去除率从100.0%降至93.4%、反应初活性降低9.8%;15 mA条件下TBBPA去除率从100.0%降至95.2%、反应初活性降低47.0%. 因此可知,15 mA条件下H*对TBBPA电催化还原脱溴的贡献相对更高.
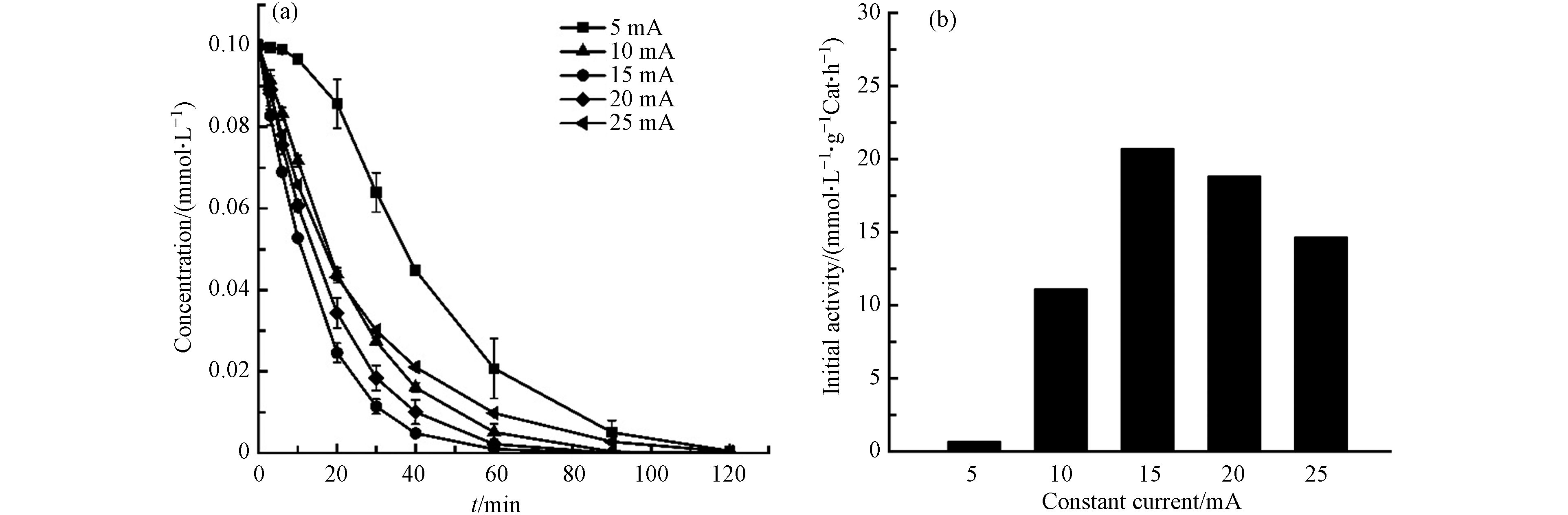
为寻找最佳工作电流,探究了电流大小对反应初活性的影响. 调节TBBPA初始浓度约为0.1 mmol·L−1、pH=10.5,投加15 mg的Pd(1.99)/TiO2催化剂,分别在5、10、15、20 、25 mA恒定电流条件下进行电催化还原反应,实验结果如图12所示. 当工作电流较低时,H*数量较少无法满足反应. 因此在5 mA至15 mA范围内,随着电流增大,H*生成速度加快,反应速率和反应初活性随之提高. 当继续增大电流,H*倾向于结合为氢气,一部分会被催化剂再次活化参与TBBPA的液相催化加氢反应,另一部分则直接逸出未被利用. 过量的氢气会阻碍TBBPA与催化剂的接触,使得反应初活性呈降低趋势. 因此,当电流大于15 mA时,随着电流不断增大,反应速率和反应初活性不升反降. 这说明在本文的实验条件下,TBBPA电催化还原反应的最佳工作电流为15 mA,此时可保持较高的降解效率.
-
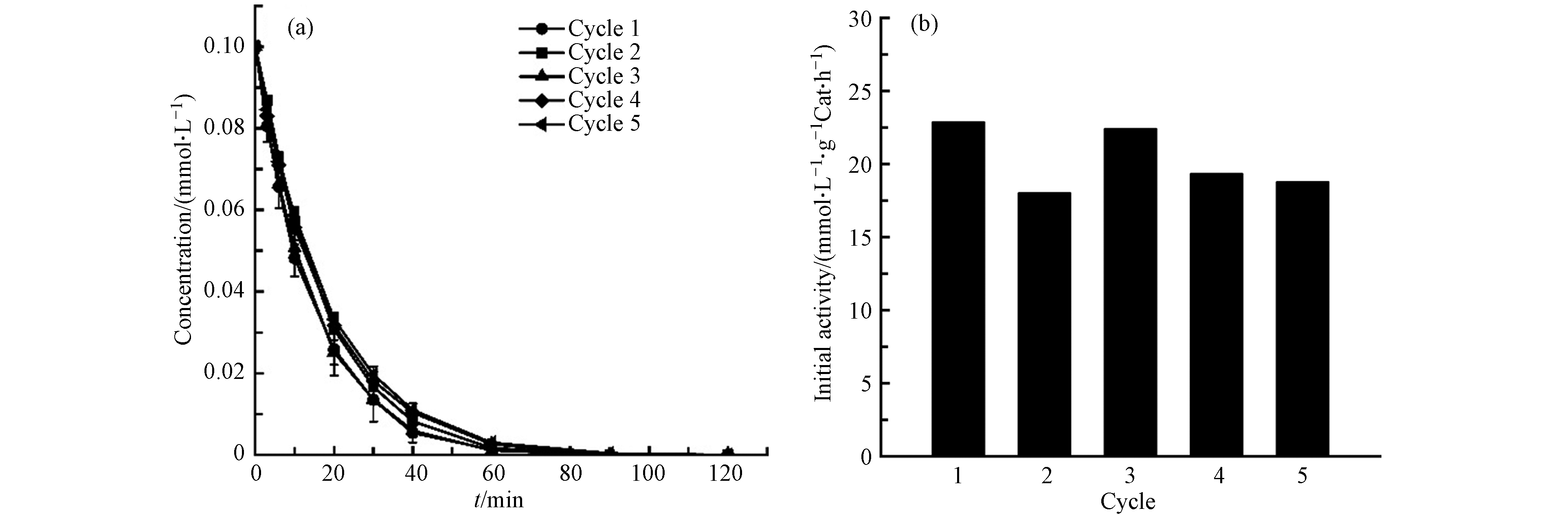
为了解悬浮体系中Pd基催化剂的可重复利用性,调节TBBPA初始浓度约为0.1 mmol·L−1、pH=10.5,投加15 mg的Pd(1.99)/TiO2催化剂,在15 mA恒定电流条件下进行5组连续的电催化还原实验. 实验结果显示(图13),经5次循环实验后,反应初活性降低了17.9%,这可能与活性组分Pd的脱落有关[29]. 但5次实验中TBBPA均可在90 min内全部降解,这说明分散型Pd基催化剂在TBBPA电催化还原实验中可保持良好的活性、稳定性,将其应用于降解水体中TBBPA污染物具有一定可行性.
-
(1)相比于固定体系,悬浮体系中Pd基催化剂对TBBPA的电催化活性更优;通过浸渍法合成了不同载体负载的Pd基催化剂,其中 Pd(1.99)/TiO2的TBBPA电催化还原活性最强.
(2)Pd/TiO2催化剂对TBBPA的电催化还原反应符合Langmuir-Hinshelwood模型,受控于TBBPA在催化剂表面的吸附过程.
(3)在一定范围内,增大恒定电流大小、Pd负载量,可提高TBBPA电催化还原反应初活性,但并不是无限制提高. 单因子影响实验表明:pH=10.5时,投加15 mg的Pd(1.99)/TiO2催化剂,在15 mA恒定电流下,可在90 min内将TBBPA(100 mL、0.1 mmol·L−1)完全降解.
(4)经5次循环使用后,分散型Pd/TiO2催化剂仍有较高的电催化还原活性,表现出较高稳定性.
Pd/TiO2催化水体中四溴双酚A的电催化还原脱溴
Study on electrocatalytic reduction of tetrabromobisphenol A on Pd/TiO2 in water
-
摘要: 以TiO2、Al2O3、CeO2和SiO2为载体,采用浸渍法制备Pd基催化剂,并通过透射电镜(TEM)、X射线衍射(XRD)、X射线光电子能谱(XPS)和电感耦合等离子体发射光谱(ICP-OES)等手段对催化剂的结构进行了详细表征. 以Pd/TiO2为催化剂,研究四溴双酚A(TBBPA)在阴极池的电催化还原. 结果表明,悬浮体系中Pd基催化剂的催化活性远高于固定体系;与其他载体相比,Pd/TiO2的电催化还原活性最高;反应过程符合Langmuir-Hinshelwood模型,受控于TBBPA在催化剂表面的吸附过程;随着恒定电流和Pd负载量的增大,TBBPA电催化还原反应的初活性呈现火山型变化规律;经过5次循环使用,Pd/TiO2催化剂仍能够完全去除TBBPA,具有良好的稳定性.Abstract: We prepared Pd based catalysts by the impregnation method with TiO2, Al2O3, CeO2 and SiO2 as the supports, and the structural properties of the catalysts were characterized by TEM, XRD, XPS and ICP-OES. The electrocatalytic debromination of tetrabromobisphenol A (TBBPA) was studied on Pd/TiO2. The results showed that the activity of Pd/TiO2 catalyst in suspension system was much higher than that in fixed system. The Pd/TiO2 catalyst had the highest electrocatalytic debromination activity among the test catalysts. The reaction process complied with the Langmuir-Hinshelwood model, and was controlled by the adsorption of TBBPA on the catalyst surface. With the increase of constant current and loading amounts of Pd, the initial activity of the catalyst for electrocatalytic reduction of TBBPA displayed a volcano-type dependency. Furthermore, complete debromination of TBBPA could be achieved on suspended Pd/TiO2 catalyst after five catalyst cycles, suggesting very high catalyst stability.
-
Key words:
- electrocatalytic reduction /
- tetrabromobisphenol A /
- suspension system /
- Pd/TiO2.
-

-
图 11 不同浓度叔丁醇对(a)TBBPA的电催化还原反应及(b)反应初活性的影响;不同电流条件下叔丁醇对(c)TBBPA的电催化还原反应及(d)反应初活性的影响
Figure 11. Effect of tert butyl alcohol with different initial concentration on (a) Electrocatalytic reduction of TBBPA and (b) Initial activity; Effect of tert butyl alcohol under different working current on (c) Electrocatalytic reduction of TBBPA and (d) Initial activity
表 1 催化剂的基本性质
Table 1. Basic properties of the catalysts
催化剂
CatalystPd实际负载量/ % a
Loading amount of PdPd平均粒径/ nm b
Average particle size of Pd表面电荷/ mV c
Surface chargePdn+/Pd0 Pd(0.45)/TiO2 0.45 1.78 N.D. 1.62 Pd(1.11)/TiO2 1.11 3.12 N.D. 1.38 Pd(1.99)/TiO2 1.99 3.63 -31.3 0.90 Pd(2.98)/TiO2 2.98 3.70 N.D. 0.61 Pd(2.15)/Al2O3 2.15 N.D. -33.0 N.D. Pd(2.04)/CeO2 2.04 N.D. -35.5 N.D. Pd(2.23)/SiO2 2.23 N.D. -36.4 N.D. 注:a电感耦合等离子发射光谱仪;b透射电子显微镜;c Zeta电位仪(pH=10.5);N.D.未测定 Notes:a ICP-OES; b TEM; c Zeta potentiometer(pH=10.5); N.D. means not determined. -
[1] 张月. 国内外阻燃剂市场分析 [J]. 精细与专用化学品, 2014, 22(8): 20-24. doi: 10.3969/j.issn.1008-1100.2014.08.004 ZHANG Y. Global market analysis of flame retardant [J]. Fine and Specialty Chemicals, 2014, 22(8): 20-24(in Chinese). doi: 10.3969/j.issn.1008-1100.2014.08.004
[2] LIU J, WANG Y F, JIANG B Q, et al. Degradation, metabolism, and bound-residue formation and release of Tetrabromobisphenol A in soil during sequential anoxic-oxic incubation [J]. Environmental Science & Technology, 2013, 47(15): 8348-8354. [3] WANG S F, SUN F F, WANG Y F, et al. Formation, characterization, and mineralization of bound residues of tetrabromobisphenol A (TBBPA) in silty clay soil under oxic conditions [J]. Science of the Total Environment, 2017, 599/600: 332-339. doi: 10.1016/j.scitotenv.2017.04.243 [4] INOUE K, YOSHIDA S, NAKAYAMA S, et al. Development of stable isotope dilution quantification liquid chromatography-mass spectrometry method for estimation of exposure levels of bisphenol A, 4-tert-octylphenol, 4-nonylphenol, tetrabromobisphenol A, and pentachlorophenol in indoor air [J]. Archives of Environmental Contamination and Toxicology, 2006, 51(4): 503-508. doi: 10.1007/s00244-005-0236-z [5] MATSUKAMI H, TUE N M, SUZUKI G, et al. Flame retardant emission from e-waste recycling operation in northern Vietnam: Environmental occurrence of emerging organophosphorus esters used as alternatives for PBDEs [J]. Science of the Total Environment, 2015, 514: 492-499. doi: 10.1016/j.scitotenv.2015.02.008 [6] YIN J F, MENG Z H, ZHU Y S, et al. Dummy molecularly imprinted polymer for selective screening of trace bisphenols in river [J]. Analytical Methods:Advancing Methods and Applications, 2011, 3(1): 173-180. [7] MORRIS S, ALLCHIN C R, ZEGERS B N, et al. Distribution and fate of HBCD and TBBPA brominated flame retardants in North Sea estuaries and aquatic food webs [J]. Environmental Science & Technology, 2004, 38(21): 5497-5504. [8] 陈玛丽, 刘青坡, 施华宏. 四溴双酚-A的甲状腺激素干扰活性研究进展 [J]. 环境与健康杂志, 2008, 25(10): 937-939. doi: 10.3969/j.issn.1001-5914.2008.10.039 CHEN M L, LIU Q P, SHI H H. Thyroid hormone disrupting activities of tetrabromobisphenol-A: A review [J]. Journal of Environment and Health, 2008, 25(10): 937-939(in Chinese). doi: 10.3969/j.issn.1001-5914.2008.10.039
[9] 杜青平, 彭润, 刘伍香, 等. 四溴双酚A对斑马鱼胚胎体内外发育的毒性效应 [J]. 环境科学学报, 2012, 32(3): 739-744. doi: 10.13671/j.hjkxxb.2012.03.005 DU Q P, PENG R, LIU W X, et al. Toxic effects of TBBPA on in vivo and in vitro developments in the zebrafish(Danio rerio) embryos [J]. Acta Scientiae Circumstantiae, 2012, 32(3): 739-744(in Chinese). doi: 10.13671/j.hjkxxb.2012.03.005
[10] EVANGELOPOULOS P, ARATO S, PERSSON H, et al. Reduction of brominated flame retardants (BFRs) in plastics from waste electrical and electronic equipment (WEEE) by solvent extraction and the influence on their thermal decomposition [J]. Waste Management, 2019, 94: 165-171. doi: 10.1016/j.wasman.2018.06.018 [11] ZHOU L C, JI L Q, MA P C, et al. Development of carbon nanotubes/CoFe2O4 magnetic hybrid material for removal of tetrabromobisphenol A and Pb(II) [J]. Journal of Hazardous Materials, 2014, 265: 104-114. doi: 10.1016/j.jhazmat.2013.11.058 [12] SANTOS M S F, ALVES A, MADEIRA L M. Chemical and photochemical degradation of polybrominated diphenyl ethers in liquid systems - A review [J]. Water Research, 2016, 88: 39-59. doi: 10.1016/j.watres.2015.09.044 [13] LIU Y M, CHEN S, QUAN X, et al. Nitrogen-doped nanodiamond rod array electrode with superior performance for electroreductive debromination of polybrominated diphenyl ethers [J]. Applied Catalysis B:Environmental, 2014, 154/155: 206-212. doi: 10.1016/j.apcatb.2014.02.028 [14] LIANG Z S, LI G Y, AN T C. Purifying, cloning and characterizing a novel dehalogenase from Bacillus sp. GZT to enhance the biodegradation of 2, 4, 6-tribromophenol in water [J]. Environmental Pollution, 2017, 225: 104-111. doi: 10.1016/j.envpol.2017.03.043 [15] MAO R, LI N, LAN H C, et al. Dechlorination of trichloroacetic acid using a noble metal-free graphene-Cu foam electrode via direct cathodic reduction and atomic H [J]. Environmental Science & Technology, 2016, 50(7): 3829-3837. [16] KORSHIN G V, JENSEN M D. Electrochemical reduction of haloacetic acids and exploration of their removal by electrochemical treatment [J]. Electrochimica Acta, 2001, 47(5): 747-751. doi: 10.1016/S0013-4686(01)00755-1 [17] LI Y P, CAO H B, ZHANG Y. Reductive dehalogenation of haloacetic acids by hemoglobin-loaded carbon nanotube electrode [J]. Water Research, 2007, 41(1): 197-205. doi: 10.1016/j.watres.2006.08.020 [18] YANG L M, CHEN Z L, CUI D, et al. Ultrafine palladium nanoparticles supported on 3D self-supported Ni foam for cathodic dechlorination of florfenicol [J]. Chemical Engineering Journal, 2019, 359: 894-901. doi: 10.1016/j.cej.2018.11.099 [19] CHAPLIN B P, REINHARD M, SCHNEIDER W F, et al. Critical review of Pd-based catalytic treatment of priority contaminants in water [J]. Environmental Science & Technology, 2012, 46(7): 3655-3670. [20] LOU Z M, XU J, ZHOU J S, et al. Insight into atomic H* generation, H2 evolution, and cathode potential of MnO2 induced Pd/Ni foam cathode for electrocatalytic hydrodechlorination [J]. Chemical Engineering Journal, 2019, 374: 211-220. doi: 10.1016/j.cej.2019.05.171 [21] SHARD A G, DHANAK V R, SANTONI A. Structures of chlorine on palladium (111) [J]. Surface Science, 2000, 445(2/3): 309-314. [22] NING X M, LI Y H, DONG B Q, et al. Electron transfer dependent catalysis of Pt on N-doped carbon nanotubes: Effects of synthesis method on metal-support interaction [J]. Journal of Catalysis, 2017, 348: 100-109. doi: 10.1016/j.jcat.2017.02.011 [23] BOURIKAS K, VAKROS J, KORDULIS C, et al. Potentiometric mass titrations: experimental and theoretical establishment of a new technique for determining the point of zero charge (PZC) of metal (hydr)oxides [J]. The Journal of Physical Chemistry B, 2003, 107(35): 9441-9451. doi: 10.1021/jp035123v [24] de PEDRO Z M, CASAS J A, GOMEZ-SAINERO L M, et al. Hydrodechlorination of dichloromethane with a Pd/AC catalyst: Reaction pathway and kinetics [J]. Applied Catalysis B:Environmental, 2010, 98(1/2): 79-85. [25] 陈诵英, 陈平, 李永旺, 等. 催化反应动力学[M]. 北京: 化学工业出版社, 2007. CHEN S Y, CHEN P, LI Y W, et al. Kinetics of catalytical reaction [M]. Beijing: Chemical Industry Press, 2007(in Chinese).
[26] BAEZA J A, CALVO L, GILARRANZ M A, et al. Catalytic behavior of size-controlled palladium nanoparticles in the hydrodechlorination of 4-chlorophenol in aqueous phase [J]. Journal of Catalysis, 2012, 293: 85-93. doi: 10.1016/j.jcat.2012.06.009 [27] GÓMEZ-SAINERO L M, SEOANE X L, FIERRO J L G, et al. Liquid-phase hydrodechlorination of CCl4 to CHCl3 on Pd/carbon catalysts: Nature and role of Pd active species [J]. Journal of Catalysis, 2002, 209(2): 279-288. doi: 10.1006/jcat.2002.3655 [28] MEZYK S P, COOPER W J, MADDEN K P, et al. Free radical destruction of N-nitrosodimethylamine in water [J]. Environmental Science & Technology, 2004, 38(11): 3161-3167. [29] LI M H, SUN Y H, TANG Y Q, et al. Efficient removal and recovery of copper by liquid phase catalytic hydrogenation using highly active and stable carbon-coated Pt catalyst supported on carbon nanotube [J]. Journal of Hazardous Materials, 2020, 388: 121745. doi: 10.1016/j.jhazmat.2019.121745 -



 下载:
下载: