-
全氟化合物(perfluorinated compounds,PFCs)是指烷烃分子链上的氢原子全部被氟原子取代而形成的一类化合物,诞生于上世纪30年代,是人工合成的一类有机化学物质,典型的如全氟辛酸(PFOA)、全氟辛烷磺酸 (PFOS)、全氟己酸(PFHxA)、全氟丁酸(PFBA)等. 全氟化合物具有独特的性质,其表面活性高,具有耐热性、耐酸性、疏水性和疏脂性[1],因此应用广泛,在工业上,可以作为聚合物、表面活性剂、润滑剂和农药[2-3];在商业上,可以用作纺织涂料、不粘涂料、去污剂、皮革制品、食品包装和消防泡沫[4-5]等. 但PFCs以其环境持久性、毒性大、生物蓄积性强等特性[6]可能会影响人类健康[7-8],特别是PFOA和PFOS在环境中具有持久性,在营养链中具有生物累积性,全氟化合物造成的环境污染和生态风险等问题引起了科学界和政府的关注. 2009年,《关于持久性有机污染物的斯德哥尔摩公约》将PFOS及其盐类列入持久性有机污染物(POPs)优控名单. 在国内PFOS被列入了《优先控制化学品名录》(第一批),PFOA被列入了《优先控制化学品名录》(第二批),均属于被鼓励替代的化学品,两者均纳入《国家鼓励的有毒有害原料(产品)替代品目录》. PFCs在日常生活中使用广泛,环境污染正逐步向有机污染的方向演化,环境有机污染日益得到人们的重视.
在国内外的研究中,水体中PFCs检出率最高的是8个碳原子的PFOS和PFOA[9] ,其应用广泛,而且是多种前体的最早转化产物,是最典型的两种全氟化合物. PFOA 在水环境中的整体污染水平要高于PFOS,我国自然水体PFCs研究主要集中于长江流域、河流及湖泊、辽河流域、海河和珠江流域[10-15],研究对象以PFOS和PFOA为主并同时监测其他种类PFCs,以获得水体PFCs污染的全面信息.
PFCs分析技术主要有色谱质谱联用技术、光谱技术和结合酶联免疫吸附测定的分析方法三大类[16]. 色谱质谱分析是应用最多和较为成熟的方法,基于色谱质谱的分析方法中以液相色谱串联质谱法(LC-MS/MS)较为成熟可靠,是分析PFCs的主流技术;环境水样PFCs含量一般都比较低,用LC-MS/MS方法测样前通常都需要对样品进行富集浓缩和净化,使用得比较普遍的方法是离线固相萃取-液相色谱串联质谱(SPE-HPLC-MS/MS)的方法[17-23],该方法成熟可靠,但前处理通常需要0.5—1.0 L大量的水样及前处理步骤多而繁杂,而且长距离采样时运输大量样品极为不便. 通过将固相萃取直接联接到高效液相色谱串联质谱进行分析,可以免去浓缩和重新溶解等几个步骤. 因而将离线方法开发成在线固相萃取方法可以提高工作效率及减少工作量并减少化学试剂的使用量. 用在线固相萃取-液相色谱串联质谱(On-Line SPE-HPLC-MS/MS)技术分析各种药物、激素等有机物的报道较多[24-31],但用On-Line SPE-HPLC-MS/MS技术分析PFCs的研究很少,仅在国外有少量应用[32-34],目前国内应用On-Line SPE-HPLC-MS/MS技术测定PFCs的方法还较少[35-36],本研究基于离线的分析方法开发成On-Line SPE-HPLC-MS/MS方法,应用于大样本的PFCs的筛查工作,有利于减少工作量及分析时间,同时为分析全自动化提供技术基础.
-
仪器:1260单元泵(美国Agilent公司)、G1170A六通阀(美国Agilent公司)、G1328C进样器(美国Agilent公司)、 1290二元泵(美国Agilent公司)、6460三重四极杆串联质谱仪(美国Agilent公司)、Masshunter色谱工作站(美国Agilent公司)、EP-C18(2.1 mm×12.5 mm,3.5 μm) 富集柱(美国Agilent公司)、EP- C18 (2.1 mm×100 mm,1.8 μm) 分析柱(美国Agilent公司)、Avanti J-26 XP高速冷冻离心机(美国贝克曼库尔特有限公司)、KH-500B 超声清洗机(昆山禾创超声仪器有限公司)、50 mL离心管(美国康宁公司)、25 mm ×0.22 μm一次性针头过滤器(中国安谱) .
试剂:甲醇、乙腈和异丙醇( 色谱纯,美国Fisher Scientific 公司),醋酸铵(纯度≥99.0%,美国Sigma-Aldrich公司),实验用水为 Milli-Q净化系统(法国 Millipore公司) 制备的超纯水( 18.2 MΩ·cm).
标准品:2 mg·L −1 PFCs自然标准混标(拿大Wellington公司)含12种PFCs、2 mg·L −1 PFCs同位素混标(加拿大Wellington公司)含9种同位素PFCs. 本研究标准物信息详见表1.
-
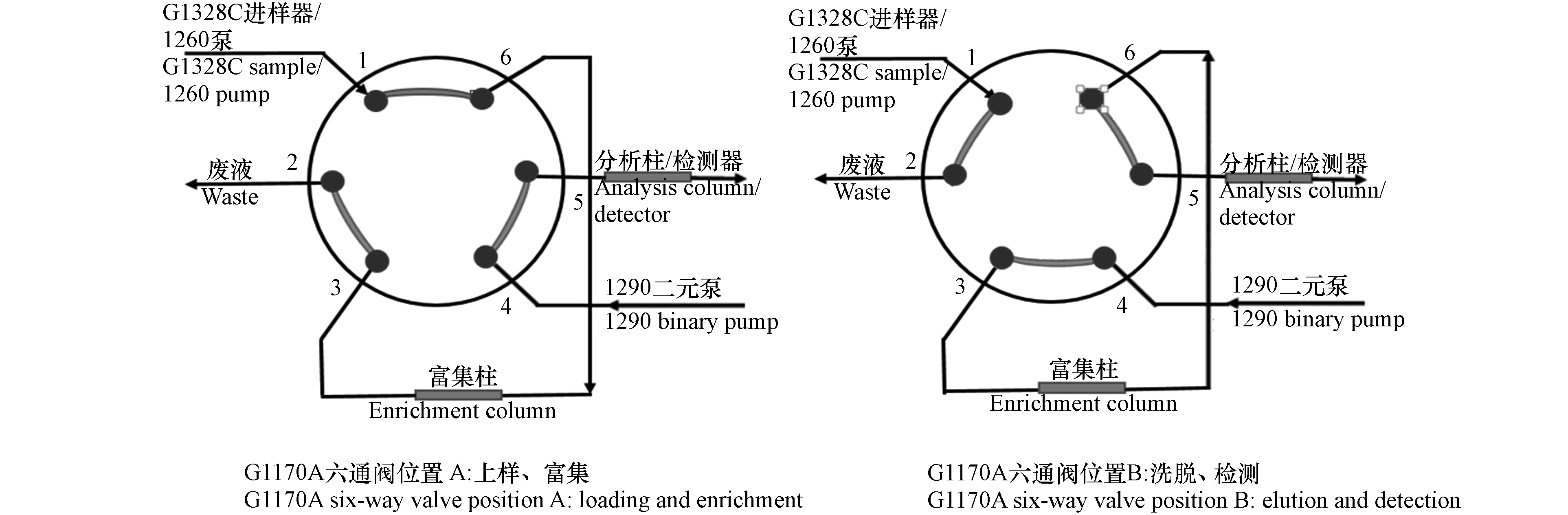
On-line SPE流路:仪器的分析程序由两个步骤完成,第一步是上样和目标物富集,期间G1328C进样器、1260单元泵和富集柱处于同一条流路,G1328C进样器配置了2 mL的定量环,样品由1260泵输入到上样流路中. 同时1290泵、分析柱和质谱检测器处于另一条流路,见图1中G1170A六通阀位置A,这一步骤完成目标物的富集;G1170A六通阀进行流路切换后,见图1中G1170A六通阀位置B,第二步是洗脱和检测,期间G1328C进样器和1260单元泵流路直接作为废液流出,这时1290泵、富集柱、分析柱和质谱检测器处于同一条流路,目标物被洗脱然后进入分析柱分离再由质谱检测.
液相色谱条件:EP- C18(2.1 mm×12.5 mm,3.5 μm) 为富集柱;EP- C18(2.1 mm×100 mm,1.8 μm)为分析柱;分析柱温度30 ℃;1260泵无机相A为1%甲醇水含2 mmol·L−1醋酸铵,流速0.4 mL·min−1;1290泵无机相A为2 mmol·L−1醋酸铵水溶液,有机相B为100%乙腈,流速0.3 mL·min−1;其他条件见表2.
质谱条件:采用ESI源在多反应监测(MRM)负模式下采集数据,干燥气温度350 ℃,干燥气流速9 L·min−1,雾化器压力40 psi,毛细管电压3500 V,其他参数见表3.
-
样品由中国科学院生态环境研究中心区域生态风险与环境管理研究组提供. 采样时用1 L聚丙烯(PP)瓶在水下10 cm处采集表层水,瓶盖水下开合,避免水面漂浮物,采样前瓶子用采集处的水润洗3次.
为防止冷冻后瓶子开裂,样品不能充满瓶子. 样品采集后用超纯水冲洗瓶外壁,吸水纸擦干后用自封袋密封,置于冰盒中运输,返回实验室后−20 ℃冷冻保存. 大凌河样品采集于2012年9月,小清河样品采集于2015年7月.
-
冰冻的样品放置到常温后摇匀,取50 mL样品于离心管中,加入内标物,使内标物在样品中浓度为25 ng·L−1,将样品置于超声清洗机中超声20 min, 4000 r·min−1离心15 min后用滤膜过滤得到待测液,用内标法定量.
-
2 mg·L−1自然标准混标母液和2 mg·L−1同位素混标母液逐级稀释,配置成50 mL的系列标准溶液,使标准系列溶液目标物浓度为0.25、0.50、2.5、5.0、25.0、50.0、100、250、500 ng·L−1,每个标准溶液中含同位素内标物浓度25 ng·L−1.
将配置好的系列标准溶液置于超声清洗机中超声20 min,然后用滤膜过滤等待上机.
-
在上机测定过程中,进样程序中设置了进样针清洗和泵头清洗操作,洗针液为1:1:1体积比的甲醇、乙腈和水的混合溶液,泵头清洗液为10%异丙醇水溶液. 以甲醇作为空白试剂,在运行标准曲线前后和每20个样品后运行空白试剂,测试仪器系统的背景值,防止系统干扰. 在运行空白试剂后,用标准曲线中间点250 ng·L−1的浓度回测,当标准点回测值波动在±10%以内时,继续测样,否则重新制作标准曲线,保证仪器误差在可控范围内. 以同位素内标法对目标分析物进行定量,标准曲线的线性(R2)至少为0.99时才可使用,上机测定时目标物超出标准曲线范围的情况下,将样品用超纯水稀释至适当范围再进行前处理,直到上机测定的目标物在线性范围之内.
-
本研究参考WANG等[13]用SPE-HPLC-MS/MS技术测定PFCs的方法,质谱参数使用了该方法参数,见表3. 基于该方法,本研究对进样系统及液相色谱条件部分进行了开发,使离线固相萃取转变成在线固相萃取富集目标物,再连接液相色谱串联四极杆质谱,达到在线分析的目的.
由G1328C进样器和1260单元泵构成在线固相萃取及富集系统,而1290二元泵和质谱构成洗脱和检测系统. 由G1170A六通阀进行流路切换,整个系统由G1328C进样器触发联动,实现在线固相萃取液质联用检测目标化合物.
在方法开发时,主要优化了富集效果和六通阀的切换时间,以达到目标分析物的最大提取效率和适当的分析时间的目的. 富集效果的影响因素是流动相溶液配比和流速以及富集柱的选择,在线固相萃取及富集系统上样流动相和富集柱的性质影响到目标分析物在富集柱上的保留强弱. 本研究在方法优化时分别设置了3.0%甲醇水(含2 mmol·L−1醋酸铵)、1.5%甲醇水(含2 mmol·L−1醋酸铵)、1.0%甲醇水(含2 mmol·L−1醋酸铵)和2 mmol·L−1醋酸铵水溶液作为1260泵的上样流动相分别进行分析,以选择富集效果强的流动相;以0.5 mL·min−1和0.4 mL·min−1的流速作为上样流速、以EP-C18 (2.1 mm×12.5 mm)和PLRP- S (2.1 mm×12.5 mm)作为富集柱分别进行分析,以选择最佳流速和富集柱. 测试结果以1.0%甲醇水(含2 mmol·L−1醋酸铵)作为流动相、上样流速为0.4 mL·min−1、EP- C18 (2.1 mm×12.5 mm)色谱柱作为富集柱得到的富集结果最佳,该系统的EP-C18 (2.1 mm×12.5 mm)色谱柱能够在12种PFCs中富集到11种PFCs. 而质谱中PFBA检出信号弱,说明该体系对PFBA富集效果差. 在线固相萃取法中,由于短碳链PFCs(PFBA、PFPeA、和PFBS)对预浓缩柱固定相的亲和力有限导致了目标物保留较少,其响应远低于直接注射法. 阀切换时间的设置主要考虑因素是,阀切换时间过短,将使目标分析物通过富集柱而随废液流失,而切换时间过长,将使整个分析时间延长,因而应该在目标物被全部富集之后,将阀切换成洗脱和检测模式达到定量分析的目的. 阀切换最短时间确定时,流动相为4:1体积比的2 mmol·L−1醋酸铵水溶液与乙腈的混合溶液,在上样流路的富集柱后直接联接质谱,用500 ng·L−1的标准溶液进样,由质谱的出峰时间来确定阀切换的最短时间为2.2 min,经过优化后阀切换时间调整为3.2 min. 在线固相萃取分析10 ng·L−1PFCs标准溶液色谱图见图2.
-
标准曲线设置了由0.25—500 ng·L−1之间共9个浓度点进行测试,标准曲线的线性(R2)至少为0.99时确定为线性范围,最终线性范围见表4 ,对线性方程未达到要求的PFCs不进行定量. PFBA虽然以相同结构同位素13C4-PFBA作为内标,但是由于富集效果差,线性及回收率都达不到要求. PFPeA、PFHpA和PFBS分别使用了13C4-PFOA、13C4-PFBA和18O2-PFHxS作为内标物,内标法线性R2达不到0.99的要求;经过分析发现,获得良好线性的PFCs所选择的内标物均为相同结构的同位素内标,而线性不满意的PFPeA、PFHpA和PFBS都选择了结构不同的同位素内标. 虽然长链PFHpA的响应值是比较高的,但内标物13C4-PFBA富集效果差也可能是导致相应的目标物PFHpA内标法定量产生不满意结果的原因. 在Castiglioni 等[34]的研究中也出现了相似的情况,在该研究中PFBA、PFPeA、和PFBS是以外标法定量的. 使用相同结构的同位素内标可以纠正基质对电离效率的影响,目标分析物和同位素内标的相互抑制作用是相等的,这确保了峰面积比与分析物浓度有良好线性关系. 因而以同位素内标法对目标分析物进行定量并选择结构尽可能接近目标分析物的内标物,可以最大限度减小测定的系统误差.
使用大凌河样品DL-6W进行加标测试,加标水平为25 ng·L−1的PFCs混标,加标回收率、线性范围和相关系数见表4. 使用样品加标的方法可以使基体更接近样品基体,减小基体效应带来的误差,8种PFCs的回收率在82.1%—103%之间,线性范围在0.66—500 ng·L−1之间,相关系数(R2)在0.991—0.998之间.
以大凌河DL-6W样品加标25 ng·L−1重复测定6次计算精密度,仪器的检出限和定量限分别以3倍信噪比和10倍信噪比确定,再根据进样量确定方法检出限和方法定量限. 由表5可见,方法精密度(RSD)在3.95%—6.29%之间,检出限(LOD)在0.20—2.43 ng·L−1之间,定量限(LOQ)在0.66—8.09 ng·L−1之间. 由表5可见,在线固相萃取液质联用法检出限高于离线方法[13],这是因为在线方法取样量少而离线方法取样量大,在取样量上离线方法是在线方法的上百倍甚至几百倍. 离线萃取甚至需要0.3—1.5 L水样[10,37-39],在线固相萃取的方法通常只需要2—5 mL[32-36],而本研究使用2 mL样品. 在线固相萃取由于减少了离线固相萃取的纯化和浓缩环节,很大程度地减少了有机溶剂的使用量,可以减少分析费用及工作量.
-
将建立的方法检测了9个大凌河流域水样和14个小清河水样,检测结果低于LOD时以ND表示,检测结果在LOD和LOQ之间时以<LOQ值表示. 对浓度超出标线范围的样品采取样品稀释的方法进行测定. 例如XQ14样品,为了保证样品的均匀性,先将原样超声15 min进行样品匀质,然后移取1 mL样品定容到100 mL,稀释了100倍,再次将样品溶液同样稀释100倍,最后XQ14样品稀释了10000倍. XQ14样品测定PFOA时使用稀释10000倍的样品进行前处理,测定PFHxA时使用稀释了100倍的样品前处理,然后分别测定目标化合物含量,确保目标物检测浓度在标准曲线范围内. 其他超标样品以此类推. 分析结果见表6.
所采集的大凌河流域水样当时主要分布了一家具有产能的氟化工企业,DL-15W、DL-16W、DL-17W和DL-18W样品点为所研究的大凌河河段的上游,该河段无氟化工企业,样品检测出的PFCs的含量较低,检测结果无排放特征,符合实际情况;DL-1W和DL-6W 分别为阜新市细河上下游的2个采样点,DL-1W样点为2012年大凌河流域一个主要的氟化工企业排放点的下游,这2个采样点PFCs明显较高,明显反映了PFCs有排放特征. 细河在大凌河样品点DL-18W之后汇入大凌河,DL-9W、DL-11W和DL-14W样品为细河汇入大凌河之后从上游至下游采集的样品,这一段河流并无氟化工企业,但这段河流检测出了PFCs,含量自上而下逐渐降低,并且具有DL-1W样品点的PFCs种类特征,分析认为是因为PFCs含量因受稀释和迁移等原因逐渐降低. 大凌河主要检出除了PFHxS的7种PFCs,其中,PFHxA、PFOA、PFDA、PFUdA和PFDoA检出率较高,PFHxA和PFOA检出水平最高分别达到88.2 ng·L−1和2051 ng·L−1,检出水平PFOA>PFHxA>PFDoDA>PFDA>PFUnDA.
小清河引入的是黄河水,样品XQ1~ XQ12采样点在小清河干流上,样品点位是从上游至下游的顺序,XQ1采自小清河源头闸口,XQ7采样点之后有一座氟化工企业的排污河道汇入小清河,而XQ8、XQ9、XQ10和XQ11检测到高浓度的PFCs,是因为上游受到氟化工企业排废的影响. 在XQ12样点小清河汇入莱州湾,XQ12位于入海口,受上游的影响较小因而PFCs检出浓度不高. XQ13和XQ14样品点为小清河的支流,XQ13为排污点的上游,未检测到高浓度PFCs,河水还未受到排污废水的污染,XQ14样点有另一家氟化工企业排污,因而检测到高浓度的PFCs. PFOA、PFHxA和PFNA水平分别达到4810、19.7、1.09 μg·L−1,小清河中除了PFHxS未检出,其余7种PFCs均有检出,检出水平PFOA>PFHxA>PFNA>PFDA>PFDoDA>PFUnDA>PFOS.
用On-Line SPE-HPLC-MS/MS技术检测水中的PFCs得到的结果与相关研究[40-41]相近. 因而可利用该方法用于污染物筛查的工作中.
-
本研究使用的On-Line SPE-HPLC-MS/MS方法可定量检测地表水中8种PFCs,包括PFHxA、PFHxS、PFOA、PFOS、PFNA、PFDA、PFUnDA和PFDoDA,虽然我国已经将PFOA和PFOS列入国家鼓励的有毒有害原料替代品目录,但目前国内PFCs最主要的污染物仍然是PFOA和PFOS[15,40-41],主要原因是工业排放,氟化工企业、制革、造纸、纺织印染、电镀等行业都有较强的排放,PFOA和PFOS被替代仍然需要时间,PFOA和PFOS仍然是PFCs中最重要的检测成分;而在MAZZONI M等的研究中PFHxA、PFOA和PFOS在地下水中的检出频率最高[32],因而本方法用于分析PFCs具有现实意义的. 本方法虽然仅分析了地表水,但应用范围可以扩展到地表水、地下水、饮用水和废水等[32-34].
-
本研究开发了一种On-Line SPE-HPLC-MS/MS方法,用于分析不同水体中的8种PFCs,与离线方法相比,样品用量、有机试剂用量及前处理步骤大大减少,提高了工作效率及减轻工作量,具有良好的实用性. 该方法以同位素作为内标物,使用内标法进行定量,有效地消除了ESI源电离抑制效应引起的误差[32],分析结果表明该方法准确度高、线性范围宽,虽然方法灵敏度稍低于离线方法,但仍然处于较低的检出限水平,是一种快速、可靠的PFCs检测方法. 在本研究中检测到的所有PFCs中,PFOA水平最高,其趋势与该领域其他研究的结果一致,具有较强的应用价值.
由于C8的PFOA和PFOS生产和使用受到限制,开发短链PFCs化学品取代C8或更高PFCs同系物成为趋势,环境中出现短链PFCs将成为趋势. 本方法对短链PFBA、PFPeA和PFBS富集效果不佳,后续的工作将对本方法做进一步探讨和改进.
致谢:感谢中国科学院生态环境研究中心所级技术中心对本研究的支持,感谢中国科学院生态环境研究中心区域生态风险与环境管理研究组为本研究提供了帮助.
在线固相萃取-高效液相色谱-串联质谱法测定地表水中8种全氟化合物
Determination of 8 perfluorinated compounds in surface water by on-line solid phase extraction-high performance liquid chromatography-tandem mass spectrometry
-
摘要: 建立了在线固相萃取-高效液相色谱-串联质谱法(On-Line SPE-HPLC-MS/MS)检测地表水中8种全氟化合物(perfluorinated compounds,PFCs)的分析方法. 该方法用电喷雾离子源(ESI)在选定的多反应监测(MRM)负模式下确定目标化合物并使用同位素内标法定量,测定了地表水中的PFCs. 8种PFCs的样品加标回收率在82.1%—103%之间,线性范围在0.66—500 ng·L−1之间,相关系数(R2)在0.991—0.998之间,精密度(RSD)在3.95%—6.29%之间,检出限(LOD)在0.20—2.43 ng·L−1之间,定量限(LOQ)在0.66—8.09 ng·L−1之间. 方法应用于大凌河及小清河地表水的分析,分析结果与该领域其他研究的结果一致,表明该方法具有实际应用意义.
-
关键词:
- 在线固相萃取 /
- 高效液相色谱串联质谱 /
- 地表水 /
- 全氟化合物.
Abstract: An on-line solid phase extraction high performance liquid chromatography tandem mass spectrometry (On-Line SPE-HPLC-MS/MS) method for determining eight perfluorinated compounds (PFCs) in surface water was established. In this method, the target compounds were qualitatively confirmed by electrospray ionization source (ESI) under the selected negative mode of multi reaction monitoring (MRM), and quantitatively determined by the isotope internal standard method. The spiked recoveries of 8 PFCs in surface water ranged from 82.1% to 103%, with a linear range of 0.66—500 ng·L−1 and a correlation coefficient (R2) of 0.991—0.998. The precision (RSD) ranged from 3.95% to 6.29% , the limit of detection (LOD) from 0.20 ng·L−1 to 2.43 ng·L−1, and the limit of quantification (LOQ) from 0.66 ng·L−1 to 8.09 ng·L−1. The method has been applied to analyze the surface water in Daling River and Xiaoqing River. And the analysis results are consistent with those of other studies in this field, indicating that the method is practical. -
全氟化合物(perfluorinated compounds,PFCs)是指烷烃分子链上的氢原子全部被氟原子取代而形成的一类化合物,诞生于上世纪30年代,是人工合成的一类有机化学物质,典型的如全氟辛酸(PFOA)、全氟辛烷磺酸 (PFOS)、全氟己酸(PFHxA)、全氟丁酸(PFBA)等. 全氟化合物具有独特的性质,其表面活性高,具有耐热性、耐酸性、疏水性和疏脂性[1],因此应用广泛,在工业上,可以作为聚合物、表面活性剂、润滑剂和农药[2-3];在商业上,可以用作纺织涂料、不粘涂料、去污剂、皮革制品、食品包装和消防泡沫[4-5]等. 但PFCs以其环境持久性、毒性大、生物蓄积性强等特性[6]可能会影响人类健康[7-8],特别是PFOA和PFOS在环境中具有持久性,在营养链中具有生物累积性,全氟化合物造成的环境污染和生态风险等问题引起了科学界和政府的关注. 2009年,《关于持久性有机污染物的斯德哥尔摩公约》将PFOS及其盐类列入持久性有机污染物(POPs)优控名单. 在国内PFOS被列入了《优先控制化学品名录》(第一批),PFOA被列入了《优先控制化学品名录》(第二批),均属于被鼓励替代的化学品,两者均纳入《国家鼓励的有毒有害原料(产品)替代品目录》. PFCs在日常生活中使用广泛,环境污染正逐步向有机污染的方向演化,环境有机污染日益得到人们的重视.
在国内外的研究中,水体中PFCs检出率最高的是8个碳原子的PFOS和PFOA[9] ,其应用广泛,而且是多种前体的最早转化产物,是最典型的两种全氟化合物. PFOA 在水环境中的整体污染水平要高于PFOS,我国自然水体PFCs研究主要集中于长江流域、河流及湖泊、辽河流域、海河和珠江流域[10-15],研究对象以PFOS和PFOA为主并同时监测其他种类PFCs,以获得水体PFCs污染的全面信息.
PFCs分析技术主要有色谱质谱联用技术、光谱技术和结合酶联免疫吸附测定的分析方法三大类[16]. 色谱质谱分析是应用最多和较为成熟的方法,基于色谱质谱的分析方法中以液相色谱串联质谱法(LC-MS/MS)较为成熟可靠,是分析PFCs的主流技术;环境水样PFCs含量一般都比较低,用LC-MS/MS方法测样前通常都需要对样品进行富集浓缩和净化,使用得比较普遍的方法是离线固相萃取-液相色谱串联质谱(SPE-HPLC-MS/MS)的方法[17-23],该方法成熟可靠,但前处理通常需要0.5—1.0 L大量的水样及前处理步骤多而繁杂,而且长距离采样时运输大量样品极为不便. 通过将固相萃取直接联接到高效液相色谱串联质谱进行分析,可以免去浓缩和重新溶解等几个步骤. 因而将离线方法开发成在线固相萃取方法可以提高工作效率及减少工作量并减少化学试剂的使用量. 用在线固相萃取-液相色谱串联质谱(On-Line SPE-HPLC-MS/MS)技术分析各种药物、激素等有机物的报道较多[24-31],但用On-Line SPE-HPLC-MS/MS技术分析PFCs的研究很少,仅在国外有少量应用[32-34],目前国内应用On-Line SPE-HPLC-MS/MS技术测定PFCs的方法还较少[35-36],本研究基于离线的分析方法开发成On-Line SPE-HPLC-MS/MS方法,应用于大样本的PFCs的筛查工作,有利于减少工作量及分析时间,同时为分析全自动化提供技术基础.
1. 材料与方法(Materials and methods)
1.1 仪器与试剂
仪器:1260单元泵(美国Agilent公司)、G1170A六通阀(美国Agilent公司)、G1328C进样器(美国Agilent公司)、 1290二元泵(美国Agilent公司)、6460三重四极杆串联质谱仪(美国Agilent公司)、Masshunter色谱工作站(美国Agilent公司)、EP-C18(2.1 mm×12.5 mm,3.5 μm) 富集柱(美国Agilent公司)、EP- C18 (2.1 mm×100 mm,1.8 μm) 分析柱(美国Agilent公司)、Avanti J-26 XP高速冷冻离心机(美国贝克曼库尔特有限公司)、KH-500B 超声清洗机(昆山禾创超声仪器有限公司)、50 mL离心管(美国康宁公司)、25 mm ×0.22 μm一次性针头过滤器(中国安谱) .
试剂:甲醇、乙腈和异丙醇( 色谱纯,美国Fisher Scientific 公司),醋酸铵(纯度≥99.0%,美国Sigma-Aldrich公司),实验用水为 Milli-Q净化系统(法国 Millipore公司) 制备的超纯水( 18.2 MΩ·cm).
标准品:2 mg·L −1 PFCs自然标准混标(拿大Wellington公司)含12种PFCs、2 mg·L −1 PFCs同位素混标(加拿大Wellington公司)含9种同位素PFCs. 本研究标准物信息详见表1.
表 1 本研究中全氟化合物的种类Table 1. The types of perfluorinated compounds in this study化合物 Compound 英文名称 English name 缩写 Abbreviations 分子式 Molecular formula 全氟丁酸 Perfluorobutyric acid PFBA C3F7COOH 全氟戊酸 Perfluoropentanoic acid PFPeA C4F9COOH 全氟己酸 Perfluorohexanoic acid PFHxA C5F11COOH 全氟庚酸 Perfluoroheptanoic acid PFHpA C6F13COOH 全氟辛酸 Perfluorooctanoic acid PFOA C7F15COOH 全氟壬酸 Perfluorononanoic acid PFNA C8F17COOH 全氟葵酸 Perfluorodecanoic acid PFDA C9F19COOH 全氟十一酸 Perfluoroundecanoic acid PFUnDA C10F21COOH 全氟十二酸 Perfluorodecanoic acid PFDoDA C11F23COOH 全氟丁烷磺酸 Perfluorobutane sulfonic acids PFBS C4F9SO3H 全氟已烷磺酸 Perfluorohexane sulfonic acid PFHxS C6F13SO3H 全氟辛烷磺酸 Perfluorooctane sulfonic acid PFOS C8F17SO3H 内标化合物 Internal standards 13C4全氟丁酸 Perfluoro-n-[13C4] butanoic acid 13C4-PFBA 13C2全氟己酸 Perfluoro-n-[13C2] hexanoic acid 13C2-PFHxA 13C4全氟辛酸 Perfluoro-n-[13C4] octanoic acid 13C4-PFOA 13C5全氟壬酸 Perfluoro-n-[13C5] nonanoic acid 13C5-PFNA 13C2全氟癸酸 Perfluoro-n-[13C2] decanoic acid 13C2-PFDA 13C2全氟十一烷酸 Perfluoro-n-[13C2] undecanoic acid 13C2-PFUnDA 13C2全氟十二烷酸 Perfluoro-n-[13C2] dodecanoic acid 13C2-PFDoDA 18O2全氟己烷磺酸 Perfluoro-n-hexane [18O2]sulphonate 18O2-PFHxS 13C4全氟辛酸 Perfluoro-n-octane [13C4]sulphonate 13C4-PFOS 1.2 仪器条件
On-line SPE流路:仪器的分析程序由两个步骤完成,第一步是上样和目标物富集,期间G1328C进样器、1260单元泵和富集柱处于同一条流路,G1328C进样器配置了2 mL的定量环,样品由1260泵输入到上样流路中. 同时1290泵、分析柱和质谱检测器处于另一条流路,见图1中G1170A六通阀位置A,这一步骤完成目标物的富集;G1170A六通阀进行流路切换后,见图1中G1170A六通阀位置B,第二步是洗脱和检测,期间G1328C进样器和1260单元泵流路直接作为废液流出,这时1290泵、富集柱、分析柱和质谱检测器处于同一条流路,目标物被洗脱然后进入分析柱分离再由质谱检测.
液相色谱条件:EP- C18(2.1 mm×12.5 mm,3.5 μm) 为富集柱;EP- C18(2.1 mm×100 mm,1.8 μm)为分析柱;分析柱温度30 ℃;1260泵无机相A为1%甲醇水含2 mmol·L−1醋酸铵,流速0.4 mL·min−1;1290泵无机相A为2 mmol·L−1醋酸铵水溶液,有机相B为100%乙腈,流速0.3 mL·min−1;其他条件见表2.
表 2 在线固相萃取和液相色谱条件Table 2. On-Line SPE and liquid chromatography conditions时间/ min Time 1260泵流动相 1260 pump flow phase 1290泵流动相 1290 pump flow phase G1170A阀位 G1170A valve position A/% A/% B/% 0 100 0 100 A 1.00 100 0 100 A 3.20 100 80 20 B 12.00 100 80 20 B 15.00 100 10 90 B 16.00 100 0 100 B 18.00 100 0 100 B 质谱条件:采用ESI源在多反应监测(MRM)负模式下采集数据,干燥气温度350 ℃,干燥气流速9 L·min−1,雾化器压力40 psi,毛细管电压3500 V,其他参数见表3.
表 3 目标化合物的MRM质谱参数Table 3. Mass spectrometer parameters used for MRM of target compounds化合物Compound name 内标物Internal standards 母离子Precursor ion(m/z) 子离子Product ion(m/z) 裂解电压/VFragmentor 碰撞能量/eVCollision energy 加速电压/VCell accelerator voltage PFDA No 513 468.9 86 3 7 13C2-PFDA Yes 515 470 86 3 7 PFDoDA No 613 569 90 5 7 13C2-PFDoDA Yes 615 570 90 5 7 PFHxA No 363 318.9 68 4 7 13C2-PFHxA Yes 315 270 68 3 7 PFHxS No 399 80 150 40 7 18O2-PFHxS Yes 403 103 150 40 7 PFOA No 413 368.9 82 4 7 13C4-PFOA Yes 417 372 82 4 7 PFOS No 498.9 80 154 47 7 13C4-PFOS Yes 503 80 154 47 7 PFUnDA No 563 519 90 5 7 13C2-PFUnDA Yes 565 520 90 5 7 PFNA No 463 419 82 3 7 13C5-PFNA Yes 468 423 82 3 7 1.3 样品采集
样品由中国科学院生态环境研究中心区域生态风险与环境管理研究组提供. 采样时用1 L聚丙烯(PP)瓶在水下10 cm处采集表层水,瓶盖水下开合,避免水面漂浮物,采样前瓶子用采集处的水润洗3次.
为防止冷冻后瓶子开裂,样品不能充满瓶子. 样品采集后用超纯水冲洗瓶外壁,吸水纸擦干后用自封袋密封,置于冰盒中运输,返回实验室后−20 ℃冷冻保存. 大凌河样品采集于2012年9月,小清河样品采集于2015年7月.
1.4 样品前处理方法
冰冻的样品放置到常温后摇匀,取50 mL样品于离心管中,加入内标物,使内标物在样品中浓度为25 ng·L−1,将样品置于超声清洗机中超声20 min, 4000 r·min−1离心15 min后用滤膜过滤得到待测液,用内标法定量.
1.5 标准曲线
2 mg·L−1自然标准混标母液和2 mg·L−1同位素混标母液逐级稀释,配置成50 mL的系列标准溶液,使标准系列溶液目标物浓度为0.25、0.50、2.5、5.0、25.0、50.0、100、250、500 ng·L−1,每个标准溶液中含同位素内标物浓度25 ng·L−1.
将配置好的系列标准溶液置于超声清洗机中超声20 min,然后用滤膜过滤等待上机.
1.6 上机测试
在上机测定过程中,进样程序中设置了进样针清洗和泵头清洗操作,洗针液为1:1:1体积比的甲醇、乙腈和水的混合溶液,泵头清洗液为10%异丙醇水溶液. 以甲醇作为空白试剂,在运行标准曲线前后和每20个样品后运行空白试剂,测试仪器系统的背景值,防止系统干扰. 在运行空白试剂后,用标准曲线中间点250 ng·L−1的浓度回测,当标准点回测值波动在±10%以内时,继续测样,否则重新制作标准曲线,保证仪器误差在可控范围内. 以同位素内标法对目标分析物进行定量,标准曲线的线性(R2)至少为0.99时才可使用,上机测定时目标物超出标准曲线范围的情况下,将样品用超纯水稀释至适当范围再进行前处理,直到上机测定的目标物在线性范围之内.
2. 结果与讨论 (Results and discussion)
2.1 方法优化
本研究参考WANG等[13]用SPE-HPLC-MS/MS技术测定PFCs的方法,质谱参数使用了该方法参数,见表3. 基于该方法,本研究对进样系统及液相色谱条件部分进行了开发,使离线固相萃取转变成在线固相萃取富集目标物,再连接液相色谱串联四极杆质谱,达到在线分析的目的.
由G1328C进样器和1260单元泵构成在线固相萃取及富集系统,而1290二元泵和质谱构成洗脱和检测系统. 由G1170A六通阀进行流路切换,整个系统由G1328C进样器触发联动,实现在线固相萃取液质联用检测目标化合物.
在方法开发时,主要优化了富集效果和六通阀的切换时间,以达到目标分析物的最大提取效率和适当的分析时间的目的. 富集效果的影响因素是流动相溶液配比和流速以及富集柱的选择,在线固相萃取及富集系统上样流动相和富集柱的性质影响到目标分析物在富集柱上的保留强弱. 本研究在方法优化时分别设置了3.0%甲醇水(含2 mmol·L−1醋酸铵)、1.5%甲醇水(含2 mmol·L−1醋酸铵)、1.0%甲醇水(含2 mmol·L−1醋酸铵)和2 mmol·L−1醋酸铵水溶液作为1260泵的上样流动相分别进行分析,以选择富集效果强的流动相;以0.5 mL·min−1和0.4 mL·min−1的流速作为上样流速、以EP-C18 (2.1 mm×12.5 mm)和PLRP- S (2.1 mm×12.5 mm)作为富集柱分别进行分析,以选择最佳流速和富集柱. 测试结果以1.0%甲醇水(含2 mmol·L−1醋酸铵)作为流动相、上样流速为0.4 mL·min−1、EP- C18 (2.1 mm×12.5 mm)色谱柱作为富集柱得到的富集结果最佳,该系统的EP-C18 (2.1 mm×12.5 mm)色谱柱能够在12种PFCs中富集到11种PFCs. 而质谱中PFBA检出信号弱,说明该体系对PFBA富集效果差. 在线固相萃取法中,由于短碳链PFCs(PFBA、PFPeA、和PFBS)对预浓缩柱固定相的亲和力有限导致了目标物保留较少,其响应远低于直接注射法. 阀切换时间的设置主要考虑因素是,阀切换时间过短,将使目标分析物通过富集柱而随废液流失,而切换时间过长,将使整个分析时间延长,因而应该在目标物被全部富集之后,将阀切换成洗脱和检测模式达到定量分析的目的. 阀切换最短时间确定时,流动相为4:1体积比的2 mmol·L−1醋酸铵水溶液与乙腈的混合溶液,在上样流路的富集柱后直接联接质谱,用500 ng·L−1的标准溶液进样,由质谱的出峰时间来确定阀切换的最短时间为2.2 min,经过优化后阀切换时间调整为3.2 min. 在线固相萃取分析10 ng·L−1PFCs标准溶液色谱图见图2.
2.2 线性、方法回收率、精密度、检测限、定量限
标准曲线设置了由0.25—500 ng·L−1之间共9个浓度点进行测试,标准曲线的线性(R2)至少为0.99时确定为线性范围,最终线性范围见表4 ,对线性方程未达到要求的PFCs不进行定量. PFBA虽然以相同结构同位素13C4-PFBA作为内标,但是由于富集效果差,线性及回收率都达不到要求. PFPeA、PFHpA和PFBS分别使用了13C4-PFOA、13C4-PFBA和18O2-PFHxS作为内标物,内标法线性R2达不到0.99的要求;经过分析发现,获得良好线性的PFCs所选择的内标物均为相同结构的同位素内标,而线性不满意的PFPeA、PFHpA和PFBS都选择了结构不同的同位素内标. 虽然长链PFHpA的响应值是比较高的,但内标物13C4-PFBA富集效果差也可能是导致相应的目标物PFHpA内标法定量产生不满意结果的原因. 在Castiglioni 等[34]的研究中也出现了相似的情况,在该研究中PFBA、PFPeA、和PFBS是以外标法定量的. 使用相同结构的同位素内标可以纠正基质对电离效率的影响,目标分析物和同位素内标的相互抑制作用是相等的,这确保了峰面积比与分析物浓度有良好线性关系. 因而以同位素内标法对目标分析物进行定量并选择结构尽可能接近目标分析物的内标物,可以最大限度减小测定的系统误差.
表 4 全氟化合物的碳链、方法的线性范围、线性方程、相关系数和加标回收率Table 4. Carbon chain of PFCs, linear range, linear equation, correlation coefficient and spiked recovery of the method化合物Compounds 碳链Carbon chain 线性范围/(ng·L−1)Linear range 线性方程Linear equation 相关系数(R2) 加标回收率/%Spiked recovery PFHxA C6 LOQ—500 y = 1.2551x -0.1093 0.997 95.6 PFHxS C6 LOQ—500 y =3.8093x -1.3226 0.991 103 PFOA C8 LOQ—500 y = 1.4761x – 0.2853 0.998 82.1 PFOS C8 LOQ—500 y = 1.4947x – 0.3389 0.997 94.7 PFNA C9 LOQ—500 y = 1.4192x – 0.2586 0.998 94.3 PFDA C10 LOQ—500 y = 1.2761x – 0.2216 0.996 97.5 PFUnDA C11 LOQ—500 y = 1.3074x – 0.1549 0.993 99.8 PFDoDA C12 LOQ—500 y = 1.1165x – 0.1013 0.993 90.2 注:加标回收率由25 ng·L−1的混标测试. Note: The spiked recoverys is tested by a mixed standard of 25 ng·L−1 使用大凌河样品DL-6W进行加标测试,加标水平为25 ng·L−1的PFCs混标,加标回收率、线性范围和相关系数见表4. 使用样品加标的方法可以使基体更接近样品基体,减小基体效应带来的误差,8种PFCs的回收率在82.1%—103%之间,线性范围在0.66—500 ng·L−1之间,相关系数(R2)在0.991—0.998之间.
以大凌河DL-6W样品加标25 ng·L−1重复测定6次计算精密度,仪器的检出限和定量限分别以3倍信噪比和10倍信噪比确定,再根据进样量确定方法检出限和方法定量限. 由表5可见,方法精密度(RSD)在3.95%—6.29%之间,检出限(LOD)在0.20—2.43 ng·L−1之间,定量限(LOQ)在0.66—8.09 ng·L−1之间. 由表5可见,在线固相萃取液质联用法检出限高于离线方法[13],这是因为在线方法取样量少而离线方法取样量大,在取样量上离线方法是在线方法的上百倍甚至几百倍. 离线萃取甚至需要0.3—1.5 L水样[10,37-39],在线固相萃取的方法通常只需要2—5 mL[32-36],而本研究使用2 mL样品. 在线固相萃取由于减少了离线固相萃取的纯化和浓缩环节,很大程度地减少了有机溶剂的使用量,可以减少分析费用及工作量.
表 5 方法精密度、检测限和定量限Table 5. Precision, detection limit and quantitative limit of the method化合物Compound 精密度RSD%Precision(n=6) 检出限/(ng·L−1)LOD 定量限/(ng·L−1)LOQ 在线固相萃取On-Line SPE 离线固相萃取Off-Line SPE[13] 在线固相萃取On-Line SPE 离线固相萃取Off-Line SPE[13] PFHxA 5.72 0.40 0.04 1.32 0.15 PFHxS 4.91 0.20 0.01 0.66 0.06 PFOA 4.22 0.30 0.05 1.01 0.19 PFOS 4.85 0.63 0.03 2.10 0.10 PFNA 4.42 0.30 0.06 0.99 0.13 PFDA 3.95 0.25 0.05 0.84 0.15 PFUnDA 4.73 0.40 0.03 1.34 0.08 PFDoDA 6.29 2.43 0.05 8.09 0.13 2.3 样品分析
将建立的方法检测了9个大凌河流域水样和14个小清河水样,检测结果低于LOD时以ND表示,检测结果在LOD和LOQ之间时以<LOQ值表示. 对浓度超出标线范围的样品采取样品稀释的方法进行测定. 例如XQ14样品,为了保证样品的均匀性,先将原样超声15 min进行样品匀质,然后移取1 mL样品定容到100 mL,稀释了100倍,再次将样品溶液同样稀释100倍,最后XQ14样品稀释了10000倍. XQ14样品测定PFOA时使用稀释10000倍的样品进行前处理,测定PFHxA时使用稀释了100倍的样品前处理,然后分别测定目标化合物含量,确保目标物检测浓度在标准曲线范围内. 其他超标样品以此类推. 分析结果见表6.
表 6 样品分析结果Table 6. Results of sample analysis河流及样品编号River and sample No. PFHxA/(ng·L−1) PFHxS/(ng·L−1) PFOA/(ng·L−1) PFOS/(ng·L−1) PFNA/(ng·L−1) PFDA/(ng·L−1) PFUnDA/(ng·L−1) PFDoDA/(ng·L−1) 大凌河Daling River DL-15W 6.39 ND 16.8 ND ND <0.84 <1.34 16.4 DL-16W ND ND 11.3 ND ND <0.84 <1.34 9.25 DL-17W ND ND 6.8 ND ND <0.84 <1.34 9.26 DL-18W 6.39 ND 7.82 ND 2.38 <0.84 <1.34 12.4 DL-1W 33.6 ND 2051 ND 4.53 6.50 4.90 121 DL-6W 88.2 0.77 320 15.1 7.29 8.12 <1.34 10.4 DL-9W 56.0 ND 145 6.26 9.76 6.95 <1.34 10.8 DL-11W 59.3 ND 128 12.1 9.53 7.74 <1.34 9.47 DL-14W 16.3 ND 34.6 4.57 ND 13.0 72.6 ND 小清河Xiaoqing River XQ1 6.29 ND 19.4 12.5 4.77 14.7 32.6 57.6 XQ2 9.65 ND 32.0 8.61 2.57 6.21 4.68 16.7 XQ3 11.0 ND 25.1 8.49 2.39 5.86 4.81 19.2 XQ4 15.8 ND 19.8 9.22 ND 6.01 4.49 19.2 XQ5 14.2 ND 19.5 7.85 2.26 6.01 3.74 10.8 XQ6 9.65 ND 26.0 7.90 ND 5.56 4.04 9.76 XQ7 20.2 ND 46.9 7.82 ND 5.46 3.34 9.84 XQ8 1165 ND 39500 8.96 16.7 6.76 3.31 11.5 XQ9 2243 ND 67500 7.76 27.5 7.81 3.31 9.31 XQ10 3603 ND 98000 6.31 39.8 9.40 4.61 12.4 XQ11 2632 ND 63700 8.92 26.6 8.25 <1.34 9.49 XQ12 9.84 ND 97.5 13.0 2.41 7.95 11.4 14.4 XQ13 29.5 ND 42.7 7.76 7.70 5.13 3.58 14.4 XQ14 19700 ND 4810000 8.25 1090 122 25.9 26.0 注:ND:未检出. ND: not detected. 所采集的大凌河流域水样当时主要分布了一家具有产能的氟化工企业,DL-15W、DL-16W、DL-17W和DL-18W样品点为所研究的大凌河河段的上游,该河段无氟化工企业,样品检测出的PFCs的含量较低,检测结果无排放特征,符合实际情况;DL-1W和DL-6W 分别为阜新市细河上下游的2个采样点,DL-1W样点为2012年大凌河流域一个主要的氟化工企业排放点的下游,这2个采样点PFCs明显较高,明显反映了PFCs有排放特征. 细河在大凌河样品点DL-18W之后汇入大凌河,DL-9W、DL-11W和DL-14W样品为细河汇入大凌河之后从上游至下游采集的样品,这一段河流并无氟化工企业,但这段河流检测出了PFCs,含量自上而下逐渐降低,并且具有DL-1W样品点的PFCs种类特征,分析认为是因为PFCs含量因受稀释和迁移等原因逐渐降低. 大凌河主要检出除了PFHxS的7种PFCs,其中,PFHxA、PFOA、PFDA、PFUdA和PFDoA检出率较高,PFHxA和PFOA检出水平最高分别达到88.2 ng·L−1和2051 ng·L−1,检出水平PFOA>PFHxA>PFDoDA>PFDA>PFUnDA.
小清河引入的是黄河水,样品XQ1~ XQ12采样点在小清河干流上,样品点位是从上游至下游的顺序,XQ1采自小清河源头闸口,XQ7采样点之后有一座氟化工企业的排污河道汇入小清河,而XQ8、XQ9、XQ10和XQ11检测到高浓度的PFCs,是因为上游受到氟化工企业排废的影响. 在XQ12样点小清河汇入莱州湾,XQ12位于入海口,受上游的影响较小因而PFCs检出浓度不高. XQ13和XQ14样品点为小清河的支流,XQ13为排污点的上游,未检测到高浓度PFCs,河水还未受到排污废水的污染,XQ14样点有另一家氟化工企业排污,因而检测到高浓度的PFCs. PFOA、PFHxA和PFNA水平分别达到4810、19.7、1.09 μg·L−1,小清河中除了PFHxS未检出,其余7种PFCs均有检出,检出水平PFOA>PFHxA>PFNA>PFDA>PFDoDA>PFUnDA>PFOS.
用On-Line SPE-HPLC-MS/MS技术检测水中的PFCs得到的结果与相关研究[40-41]相近. 因而可利用该方法用于污染物筛查的工作中.
2.4 方法适用性
本研究使用的On-Line SPE-HPLC-MS/MS方法可定量检测地表水中8种PFCs,包括PFHxA、PFHxS、PFOA、PFOS、PFNA、PFDA、PFUnDA和PFDoDA,虽然我国已经将PFOA和PFOS列入国家鼓励的有毒有害原料替代品目录,但目前国内PFCs最主要的污染物仍然是PFOA和PFOS[15,40-41],主要原因是工业排放,氟化工企业、制革、造纸、纺织印染、电镀等行业都有较强的排放,PFOA和PFOS被替代仍然需要时间,PFOA和PFOS仍然是PFCs中最重要的检测成分;而在MAZZONI M等的研究中PFHxA、PFOA和PFOS在地下水中的检出频率最高[32],因而本方法用于分析PFCs具有现实意义的. 本方法虽然仅分析了地表水,但应用范围可以扩展到地表水、地下水、饮用水和废水等[32-34].
3. 结论(Conclusion)
本研究开发了一种On-Line SPE-HPLC-MS/MS方法,用于分析不同水体中的8种PFCs,与离线方法相比,样品用量、有机试剂用量及前处理步骤大大减少,提高了工作效率及减轻工作量,具有良好的实用性. 该方法以同位素作为内标物,使用内标法进行定量,有效地消除了ESI源电离抑制效应引起的误差[32],分析结果表明该方法准确度高、线性范围宽,虽然方法灵敏度稍低于离线方法,但仍然处于较低的检出限水平,是一种快速、可靠的PFCs检测方法. 在本研究中检测到的所有PFCs中,PFOA水平最高,其趋势与该领域其他研究的结果一致,具有较强的应用价值.
由于C8的PFOA和PFOS生产和使用受到限制,开发短链PFCs化学品取代C8或更高PFCs同系物成为趋势,环境中出现短链PFCs将成为趋势. 本方法对短链PFBA、PFPeA和PFBS富集效果不佳,后续的工作将对本方法做进一步探讨和改进.
致谢:感谢中国科学院生态环境研究中心所级技术中心对本研究的支持,感谢中国科学院生态环境研究中心区域生态风险与环境管理研究组为本研究提供了帮助.
-
表 1 本研究中全氟化合物的种类
Table 1. The types of perfluorinated compounds in this study
化合物 Compound 英文名称 English name 缩写 Abbreviations 分子式 Molecular formula 全氟丁酸 Perfluorobutyric acid PFBA C3F7COOH 全氟戊酸 Perfluoropentanoic acid PFPeA C4F9COOH 全氟己酸 Perfluorohexanoic acid PFHxA C5F11COOH 全氟庚酸 Perfluoroheptanoic acid PFHpA C6F13COOH 全氟辛酸 Perfluorooctanoic acid PFOA C7F15COOH 全氟壬酸 Perfluorononanoic acid PFNA C8F17COOH 全氟葵酸 Perfluorodecanoic acid PFDA C9F19COOH 全氟十一酸 Perfluoroundecanoic acid PFUnDA C10F21COOH 全氟十二酸 Perfluorodecanoic acid PFDoDA C11F23COOH 全氟丁烷磺酸 Perfluorobutane sulfonic acids PFBS C4F9SO3H 全氟已烷磺酸 Perfluorohexane sulfonic acid PFHxS C6F13SO3H 全氟辛烷磺酸 Perfluorooctane sulfonic acid PFOS C8F17SO3H 内标化合物 Internal standards 13C4全氟丁酸 Perfluoro-n-[13C4] butanoic acid 13C4-PFBA 13C2全氟己酸 Perfluoro-n-[13C2] hexanoic acid 13C2-PFHxA 13C4全氟辛酸 Perfluoro-n-[13C4] octanoic acid 13C4-PFOA 13C5全氟壬酸 Perfluoro-n-[13C5] nonanoic acid 13C5-PFNA 13C2全氟癸酸 Perfluoro-n-[13C2] decanoic acid 13C2-PFDA 13C2全氟十一烷酸 Perfluoro-n-[13C2] undecanoic acid 13C2-PFUnDA 13C2全氟十二烷酸 Perfluoro-n-[13C2] dodecanoic acid 13C2-PFDoDA 18O2全氟己烷磺酸 Perfluoro-n-hexane [18O2]sulphonate 18O2-PFHxS 13C4全氟辛酸 Perfluoro-n-octane [13C4]sulphonate 13C4-PFOS 表 2 在线固相萃取和液相色谱条件
Table 2. On-Line SPE and liquid chromatography conditions
时间/ min Time 1260泵流动相 1260 pump flow phase 1290泵流动相 1290 pump flow phase G1170A阀位 G1170A valve position A/% A/% B/% 0 100 0 100 A 1.00 100 0 100 A 3.20 100 80 20 B 12.00 100 80 20 B 15.00 100 10 90 B 16.00 100 0 100 B 18.00 100 0 100 B 表 3 目标化合物的MRM质谱参数
Table 3. Mass spectrometer parameters used for MRM of target compounds
化合物Compound name 内标物Internal standards 母离子Precursor ion(m/z) 子离子Product ion(m/z) 裂解电压/VFragmentor 碰撞能量/eVCollision energy 加速电压/VCell accelerator voltage PFDA No 513 468.9 86 3 7 13C2-PFDA Yes 515 470 86 3 7 PFDoDA No 613 569 90 5 7 13C2-PFDoDA Yes 615 570 90 5 7 PFHxA No 363 318.9 68 4 7 13C2-PFHxA Yes 315 270 68 3 7 PFHxS No 399 80 150 40 7 18O2-PFHxS Yes 403 103 150 40 7 PFOA No 413 368.9 82 4 7 13C4-PFOA Yes 417 372 82 4 7 PFOS No 498.9 80 154 47 7 13C4-PFOS Yes 503 80 154 47 7 PFUnDA No 563 519 90 5 7 13C2-PFUnDA Yes 565 520 90 5 7 PFNA No 463 419 82 3 7 13C5-PFNA Yes 468 423 82 3 7 表 4 全氟化合物的碳链、方法的线性范围、线性方程、相关系数和加标回收率
Table 4. Carbon chain of PFCs, linear range, linear equation, correlation coefficient and spiked recovery of the method
化合物Compounds 碳链Carbon chain 线性范围/(ng·L−1)Linear range 线性方程Linear equation 相关系数(R2) 加标回收率/%Spiked recovery PFHxA C6 LOQ—500 y = 1.2551x -0.1093 0.997 95.6 PFHxS C6 LOQ—500 y =3.8093x -1.3226 0.991 103 PFOA C8 LOQ—500 y = 1.4761x – 0.2853 0.998 82.1 PFOS C8 LOQ—500 y = 1.4947x – 0.3389 0.997 94.7 PFNA C9 LOQ—500 y = 1.4192x – 0.2586 0.998 94.3 PFDA C10 LOQ—500 y = 1.2761x – 0.2216 0.996 97.5 PFUnDA C11 LOQ—500 y = 1.3074x – 0.1549 0.993 99.8 PFDoDA C12 LOQ—500 y = 1.1165x – 0.1013 0.993 90.2 注:加标回收率由25 ng·L−1的混标测试. Note: The spiked recoverys is tested by a mixed standard of 25 ng·L−1 表 5 方法精密度、检测限和定量限
Table 5. Precision, detection limit and quantitative limit of the method
化合物Compound 精密度RSD%Precision(n=6) 检出限/(ng·L−1)LOD 定量限/(ng·L−1)LOQ 在线固相萃取On-Line SPE 离线固相萃取Off-Line SPE[13] 在线固相萃取On-Line SPE 离线固相萃取Off-Line SPE[13] PFHxA 5.72 0.40 0.04 1.32 0.15 PFHxS 4.91 0.20 0.01 0.66 0.06 PFOA 4.22 0.30 0.05 1.01 0.19 PFOS 4.85 0.63 0.03 2.10 0.10 PFNA 4.42 0.30 0.06 0.99 0.13 PFDA 3.95 0.25 0.05 0.84 0.15 PFUnDA 4.73 0.40 0.03 1.34 0.08 PFDoDA 6.29 2.43 0.05 8.09 0.13 表 6 样品分析结果
Table 6. Results of sample analysis
河流及样品编号River and sample No. PFHxA/(ng·L−1) PFHxS/(ng·L−1) PFOA/(ng·L−1) PFOS/(ng·L−1) PFNA/(ng·L−1) PFDA/(ng·L−1) PFUnDA/(ng·L−1) PFDoDA/(ng·L−1) 大凌河Daling River DL-15W 6.39 ND 16.8 ND ND <0.84 <1.34 16.4 DL-16W ND ND 11.3 ND ND <0.84 <1.34 9.25 DL-17W ND ND 6.8 ND ND <0.84 <1.34 9.26 DL-18W 6.39 ND 7.82 ND 2.38 <0.84 <1.34 12.4 DL-1W 33.6 ND 2051 ND 4.53 6.50 4.90 121 DL-6W 88.2 0.77 320 15.1 7.29 8.12 <1.34 10.4 DL-9W 56.0 ND 145 6.26 9.76 6.95 <1.34 10.8 DL-11W 59.3 ND 128 12.1 9.53 7.74 <1.34 9.47 DL-14W 16.3 ND 34.6 4.57 ND 13.0 72.6 ND 小清河Xiaoqing River XQ1 6.29 ND 19.4 12.5 4.77 14.7 32.6 57.6 XQ2 9.65 ND 32.0 8.61 2.57 6.21 4.68 16.7 XQ3 11.0 ND 25.1 8.49 2.39 5.86 4.81 19.2 XQ4 15.8 ND 19.8 9.22 ND 6.01 4.49 19.2 XQ5 14.2 ND 19.5 7.85 2.26 6.01 3.74 10.8 XQ6 9.65 ND 26.0 7.90 ND 5.56 4.04 9.76 XQ7 20.2 ND 46.9 7.82 ND 5.46 3.34 9.84 XQ8 1165 ND 39500 8.96 16.7 6.76 3.31 11.5 XQ9 2243 ND 67500 7.76 27.5 7.81 3.31 9.31 XQ10 3603 ND 98000 6.31 39.8 9.40 4.61 12.4 XQ11 2632 ND 63700 8.92 26.6 8.25 <1.34 9.49 XQ12 9.84 ND 97.5 13.0 2.41 7.95 11.4 14.4 XQ13 29.5 ND 42.7 7.76 7.70 5.13 3.58 14.4 XQ14 19700 ND 4810000 8.25 1090 122 25.9 26.0 注:ND:未检出. ND: not detected. -
[1] 吴越超, 蒋强, 陶晓红, 等. 水环境中全氟化合物的污染现状及检测方法研究 [J]. 皮革与化工, 2017, 34(6): 29-31. doi: 10.3969/j.issn.1674-0939.2017.06.007 WU Y C, JIANG Q, TAO X H, et al. Research on pollution and detection of perfluorochemicals in water [J]. Leather and Chemicals, 2017, 34(6): 29-31(in Chinese). doi: 10.3969/j.issn.1674-0939.2017.06.007
[2] 王飞, 李晓明, 李建勇. 食品中全氟化合物检测前处理技术研究进展 [J]. 食品研究与开发, 2016, 37(14): 192-196. doi: 10.3969/j.issn.1005-6521.2016.14.047 WANG F, LI X M, LI J Y. Progress on pretreatment technology of perfluorinated compounds in food [J]. Food Research and Development, 2016, 37(14): 192-196(in Chinese). doi: 10.3969/j.issn.1005-6521.2016.14.047
[3] 张春晖, 刘育, 唐佳伟, 等. 典型工业废水中全氟化合物处理技术研究进展 [J]. 中国环境科学, 2021, 41(3): 1109-1118. doi: 10.3969/j.issn.1000-6923.2021.03.013 ZHANG C H, LIU Y, TANG J W, et al. Progress of research on treatment technology of perfluorinated compounds in typical industrial wastewater [J]. China Environmental Science, 2021, 41(3): 1109-1118(in Chinese). doi: 10.3969/j.issn.1000-6923.2021.03.013
[4] 刘葳, 张增强. 纺织品中全氟化合物检测技术研究现状 [J]. 化纤与纺织技术, 2016, 45(1): 27-32. doi: 10.3969/j.issn.1672-500x.2016.01.007 LIU W, ZHANG Z Q. Study process of perfluorinated compounds detection technology in textiles [J]. Chemical Fiber & Textile Technology, 2016, 45(1): 27-32(in Chinese). doi: 10.3969/j.issn.1672-500x.2016.01.007
[5] 周庆, 张满成, 卢宇飞, 等. 全氟类化合物的检测与治理研究进展 [J]. 环境科学与技术, 2008, 31(7): 44-52. doi: 10.3969/j.issn.1003-6504.2008.07.013 ZHOU Q, ZHANG M C, LU Y F, et al. Research trends on determination and treatment of perfluoronic compounds [J]. Environmental Science & Technology, 2008, 31(7): 44-52(in Chinese). doi: 10.3969/j.issn.1003-6504.2008.07.013
[6] 夏晓慧, 牛增元, 姚鹏, 等. 皮革中全氟化合物检测技术研究进展 [J]. 皮革科学与工程, 2019, 29(2): 33-39. XIA X H, NIU Z Y, YAO P, et al. Progress in the detection technology of perfluorinated compounds in leather [J]. Leather Science and Engineering, 2019, 29(2): 33-39(in Chinese).
[7] KNOX S S, JACKSON T, JAVINS B, et al. Implications of early menopause in women exposed to perfluorocarbons [J]. The Journal of Clinical Endocrinology & Metabolism, 2011, 96(6): 1747-1753. [8] 许罗, 林秋风, 李聪, 等. 典型全氟化合物污染现状及其处理技术研究进展 [J]. 中国给水排水, 2022, 38(10): 56-62. XU L, LIN Q F, LI C, et al. Current situation of typical perfluorinated compounds pollution and its treatment technology progress [J]. China Water & Wastewater, 2022, 38(10): 56-62(in Chinese).
[9] 宋彦敏, 周连宁, 郝文龙, 等. 全氟化合物的污染现状及国内外研究进展 [J]. 环境工程, 2017, 35(10): 82-86. doi: 10.13205/j.hjgc.201710017 SONG Y M, ZHOU L N, HAO W L, et al. Pollution status and related research progress of perfluorinated compounds [J]. Environmental Engineering, 2017, 35(10): 82-86(in Chinese). doi: 10.13205/j.hjgc.201710017
[10] SO M K, MIYAKE Y, YEUNG W Y, et al. Perfluorinated compounds in the Pearl River and Yangtze River of China [J]. Chemosphere, 2007, 68(11): 2085-2095. doi: 10.1016/j.chemosphere.2007.02.008 [11] JIN Y H, LIU W, SATO I, et al. PFOS and PFOA in environmental and tap water in China [J]. Chemosphere, 2009, 77(5): 605-611. doi: 10.1016/j.chemosphere.2009.08.058 [12] WANG T Y, LU Y L, CHEN C L, et al. Perfluorinated compounds in estuarine and coastal areas of north Bohai Sea, China [J]. Marine Pollution Bulletin, 2011, 62(8): 1905-1914. doi: 10.1016/j.marpolbul.2011.05.029 [13] WANG P, LU Y L, WANG T Y, et al. Occurrence and transport of 17 perfluoroalkyl acids in 12 coastal rivers in south Bohai coastal region of China with concentrated fluoropolymer facilities [J]. Environmental Pollution, 2014, 190: 115-122. doi: 10.1016/j.envpol.2014.03.030 [14] ZHOU Z, LIANG Y, SHI Y L, et al. Occurrence and transport of perfluoroalkyl acids (PFAAs), including short-chain PFAAs in Tangxun Lake, China [J]. Environmental Science & Technology, 2013, 47(16): 9249-9257. [15] 秦文友, 周云桥, 张梦, 等. 中国东南主要河流表层水中全氟烷基酸的赋存特征及风险评价 [J]. 环境化学, 2021, 40(6): 1749-1762. QIN W Y, ZHOU Y Q, ZHANG M, et al. Occurrence and risk assessment of perfluoroalkyl acids in surface water of the major rivers in southeast China [J]. Environmental Chemistry, 2021, 40(6): 1749-1762(in Chinese).
[16] 吴建刚, 龙强, 肖文, 等. 环境水样中全氟磺酸类和全氟羧酸类化合物分析方法研究进展 [J]. 环境化学, 2018, 37(8): 1851-1855,1857. doi: 10.7524/j.issn.0254-6108.2017122901 WU J G, LONG Q, XIAO W, et al. Analytical methods of perfluorosulfonic acids(PFSAs)and perfluorocarboxylic acids(PFCAs) in environmental water samples [J]. Environmental Chemistry, 2018, 37(8): 1851-1855,1857(in Chinese). doi: 10.7524/j.issn.0254-6108.2017122901
[17] 张萍, 史亚利, 蔡亚岐, 等. 高效液相色谱-串联质谱联用技术测定环境水样中的全氟化合物 [J]. 分析化学, 2007, 35(7): 969-972. doi: 10.3321/j.issn:0253-3820.2007.07.008 ZHANG P, SHI Y L, CAI Y Q, et al. Determination of perfluorinated compounds in water samples by high performance liquid chromatography-electrospray tandem mass spectrometry [J]. Chinese Journal of Analytical Chemistry, 2007, 35(7): 969-972(in Chinese). doi: 10.3321/j.issn:0253-3820.2007.07.008
[18] 刘莉治, 曾涛, 彭荣飞, 等. 大体积固相萃取浓缩-超高效液相色谱串联质谱法测定水中11种全氟化合物 [J]. 中国卫生检验杂志, 2013, 23(8): 1831-1834. LIU L Z, ZENG T, PENG R F, et al. Determination of 11 kinds of perfluorinated compounds in water by UPLC-MS/MS with large-volume SPE [J]. Chinese Journal of Health Laboratory Technology, 2013, 23(8): 1831-1834(in Chinese).
[19] 刘晓雷, 刘婕, 郭睿, 等. 超高效液相色谱-串联质谱法测定表层水中全氟及多氟化合物 [J]. 分析化学, 2018, 46(9): 1400-1407. doi: 10.11895/j.issn.0253-3820.171373 LIU X L, LIU J, GUO R, et al. Ultra performance liquid chromatography-tandem mass spectrometry for determination of per-and polyfluorinated compounds in surface water [J]. Chinese Journal of Analytical Chemistry, 2018, 46(9): 1400-1407(in Chinese). doi: 10.11895/j.issn.0253-3820.171373
[20] 张明, 唐访良, 俞雅雲, 等. 固相萃取-超高效液相色谱-电喷雾串联质谱法同时测定地表水中16种全氟有机化合物 [J]. 色谱, 2014, 32(5): 472-476. doi: 10.3724/SP.J.1123.2014.01042 ZHANG M, TANG F L, YU Y Y, et al. Simultaneous determination of sixteen perfluorinated organic compounds in surface water by solid phase extraction and ultra performance liquid chromatography with electrospray ionization tandem mass spectrometry [J]. Chinese Journal of Chromatography, 2014, 32(5): 472-476(in Chinese). doi: 10.3724/SP.J.1123.2014.01042
[21] 彭洁, 王娅南, 黄合田, 等. 超高效液相色谱-串联质谱法同时测定喀斯特地区地表水中10种全氟及多氟化合物 [J]. 现代预防医学, 2018, 45(16): 2997-3001. PENG J, WANG Y N, HUANG H T, et al. Simultaneous determination of 10 perfluoroalkyl substances in surface water of Karst terrain by ultra performance chromatography-tandem mass spectrometry [J]. Modern Preventive Medicine, 2018, 45(16): 2997-3001(in Chinese).
[22] 原盛广, 郎爽, 王颖, 等. 固相萃取-超高效液相色谱-串联质谱法测定污水中16种全氟和多氟烷基化合物[J]. 生态毒理学报, 2021.16(3)239-251. YUAN S G, , LANG S, WANG Y, et al. Determination of 16 Perfluoroalkyl and Polyfluoroalkyl Substances in Wastewater by Solid Phase Extraction-Ultraperformance Liquid Chromatography-Tandem Mass Spectrometry[J]. Asian Journal of Ecotoxicology. 2021, 16(3): 239-251(in Chinese).
[23] 张宪忠, 孙红文, 汪磊, 等. 固相萃取-高效液相色谱串联质谱技术测定污水中的全氟化合物 [J]. 环境化学, 2009, 28(6): 944-945. doi: 10.3321/j.issn:0254-6108.2009.06.033 ZHANG X Z, SUN H W, WANG L, et al. Solid phase extraction- high performance liquid chromatography tandem mass spectrometry determination of perfluorinated compounds in wastewater [J]. Environmental Chemistry, 2009, 28(6): 944-945(in Chinese). doi: 10.3321/j.issn:0254-6108.2009.06.033
[24] FAYAD P B, PRÉVOST M, SAUVÉ S. On-line solid-phase extraction coupled to liquid chromatography tandem mass spectrometry optimized for the analysis of steroid hormones in urban wastewaters [J]. Talanta, 2013, 115: 349-360. doi: 10.1016/j.talanta.2013.05.038 [25] GARCÍA-GALÁN M J, DÍAZ-CRUZ M S, BARCELÓ D. Determination of 19 sulfonamides in environmental water samples by automated on-line solid-phase extraction-liquid chromatography-tandem mass spectrometry (SPE-LC-MS/MS) [J]. Talanta, 2010, 81(1/2): 355-366. [26] LIU R Z, RUAN T, WANG T, et al. Determination of nine benzotriazole UV stabilizers in environmental water samples by automated on-line solid phase extraction coupled with high-performance liquid chromatography-tandem mass spectrometry [J]. Talanta, 2014, 120: 158-166. doi: 10.1016/j.talanta.2013.10.041 [27] FONTANALS N, MARCÉ R M, BORRULL F. On-line solid-phase extraction coupled to hydrophilic interaction chromatography-mass spectrometry for the determination of polar drugs [J]. Journal of Chromatography A, 2011, 1218(35): 5975-5980. doi: 10.1016/j.chroma.2010.12.028 [28] de CASTRO A, FERNANDEZ M D M R, LALOUP M, et al. High-throughput on-line solid-phase extraction-liquid chromatography-tandem mass spectrometry method for the simultaneous analysis of 14 antidepressants and their metabolites in plasma [J]. Journal of Chromatography A, 2007, 1160(1/2): 3-12. [29] VEGA-MORALES T, SOSA-FERRERA Z, SANTANA-RODRÍGUEZ J J. Development and optimisation of an on-line solid phase extraction coupled to ultra-high-performance liquid chromatography-tandem mass spectrometry methodology for the simultaneous determination of endocrine disrupting compounds in wastewater samples [J]. Journal of Chromatography A, 2012, 1230: 66-76. doi: 10.1016/j.chroma.2012.01.077 [30] 傅建捷, 高珂, 张爱茜. 一种全自动在线检测血清中全氟及多氟化合物的系统[P]. 中国专利: CN105510483B, 2018-02-16. FU J J, GAO K, ZHANG A Q. A fully automatic on-line detection in serum total fluoride and fluorine compound system[P]. Chinese Patent: CN105510483B, 2018-02-16.
[31] 高珂, 李义莉, 傅建捷, 等. 全自动在线湍流-固相萃取-高效液相-串联质谱方法检测血清中21种全氟及多氟类化合物[C]. 中国化学会第30届学术年会摘要集-第二十六分会: 环境化学. 2016: 139. GAO K, LI Y L, FU J J, et al. An automated On-line Turboflow-SPE-HPLC-MS/MS Method for detection of 21 Per- and polyfluoroalkyl substances in human serum[C]. Abstract of the 30th Annual Academic Conference of the Chinese Chemical Society - the 26th Branch: Environmental Chemistry, 2016: 139(in Chinese).
[32] MAZZONI M, RUSCONI M, VALSECCHI S, et al. An on-line solid phase extraction-liquid chromatography-tandem mass spectrometry method for the determination of perfluoroalkyl acids in drinking and surface waters [J]. Journal of Analytical Methods in Chemistry, 2015, 2015: 942016. [33] LLORCA M, FARRÉ M, PICÓ Y, et al. Analysis of perfluoroalkyl substances in waters from Germany and Spain [J]. Science of the Total Environment, 2012, 431: 139-150. doi: 10.1016/j.scitotenv.2012.05.011 [34] CASTIGLIONI S, VALSECCHI S, POLESELLO S, et al. Sources and fate of perfluorinated compounds in the aqueous environment and in drinking water of a highly urbanized and industrialized area in Italy [J]. Journal of Hazardous Materials, 2015, 282: 51-60. doi: 10.1016/j.jhazmat.2014.06.007 [35] 史亚利, 潘媛媛, 梁立娜, 等. 在线固相萃取-液质联用法分析环境水样中常见全氟化合物[C]. 首届极地及高山地区持久性有毒污染物学术研讨会论文集. 2013: 33-34. SHI Y L, PAN Y Y, LIANG L N, et al. On-line solid phase extraction-liquid mass ia analysis of common perfluorinated compounds in environmental water samples[C]. Proceedings of the first symposium on persistent toxic pollutants in polar and alpine regions. 2013: 33-34.
[36] 潘媛媛, 金燕. 在线固相萃取-液质联用法分析水样中的常见全氟化合物[C]. 第七届全国环境化学学术大会论文集. 2013: 151-152. PAN Y Y, JIN Y. Analysis of common fluorocarbon in water samples by on-line solid phase extraction-liquid mass spectrometry[C]. Proceedings of the 7th national conference on environmental chemistry academic. 2013: 151-152.
[37] PAN C G, YING G G, LIU Y S, et al. Contamination profiles of perfluoroalkyl substances in five typical rivers of the Pearl River Delta region, South China [J]. Chemosphere, 2014, 114: 16-25. doi: 10.1016/j.chemosphere.2014.04.005 [38] YAO Y M, ZHU H K, LI B, et al. Distribution and primary source analysis of per- and poly-fluoroalkyl substances with different chain lengths in surface and groundwater in two cities, North China [J]. Ecotoxicology and Environmental Safety, 2014, 108: 318-328. doi: 10.1016/j.ecoenv.2014.07.021 [39] ZHANG Y, MENG W, GUO C S, et al. Determination and partitioning behavior of perfluoroalkyl carboxylic acids and perfluorooctanesulfonate in water and sediment from Dianchi Lake, China [J]. Chemosphere, 2012, 88(11): 1292-1299. doi: 10.1016/j.chemosphere.2012.03.103 [40] LI Q F, ZHANG Y Q, LU Y L, et al. Risk ranking of environmental contaminants in Xiaoqing River, a heavily polluted river along urbanizing Bohai Rim [J]. Chemosphere, 2018, 204: 28-35. doi: 10.1016/j.chemosphere.2018.04.030 [41] 王佩. 环渤海地区全氟烷基酸排放与迁移的生态学过程研究[D] . 北京: 中国科学院大学, 2015: 40-48, 69-74. WANG P. Ecological processes of perfluoroalkyl acids emitted from fluorochemiacal industry in Bohai coastal Region[D]. Beijing: University of Chinese Academy of Sciences, 2015: 40-48, 69-74(in Chinese).
期刊类型引用(7)
1. 吴萍,王炜,刘惠敏,段秀锋,曲腊腊,尤本胜. 超高效液相色谱-串联质谱法测定复杂水质中25种全氟/多氟化合物. 化学分析计量. 2025(01): 12-20 .  百度学术
百度学术
2. 刘田,周宇齐,宋洲,吉义平,杨杰,方志成. 全自动固相萃取-UPLC-MS/MS法测定水中17种全氟化合物. 化学研究与应用. 2025(02): 410-418 .  百度学术
百度学术
3. 高珂,辛晓东,刘红,刘莉,宋艳,贾瑞宝. 超高效液相色谱-三重四极杆质谱联用仪测定环境水相和沉积物中19种全/多氟烷基化合物. 净水技术. 2024(08): 61-69+166 .  百度学术
百度学术
4. 陈斐. 上海市浦东新区地表水中17种全氟烷基酸污染水平及其生态风险熵. 生态毒理学报. 2024(05): 75-84 .  百度学术
百度学术
5. 李健,张海东,王修保,郭庆伟. 环境中全氟和多氟烷基化合物分析方法研究进展. 化学试剂. 2024(11): 17-26 .  百度学术
百度学术
6. 周画天,黄帝,刘晓雨,王献礼,饶钦雄,刘成斌,宋卫国. 超高效液相色谱-串联质谱法同时测定水中两类含氟新污染物. 分析试验室. 2024(12): 1655-1661 .  百度学术
百度学术
7. 张慧,马红青,蒋莹. 高效液相色谱串联质谱法同时测定学生用品中3种全氟化合物. 化学分析计量. 2024(12): 41-45 .  百度学术
百度学术
其他类型引用(3)
-






 DownLoad:
DownLoad: