-
N-亚硝胺(以下简称亚硝胺)是一类含亚硝基的有机污染物,化学通式为R1(R2)N—N=O,目前已报导的同系物有300多种. 在已知的亚硝胺当中,至少有90%对人类具有致癌作用,并且存在器官特异性,如N-亚硝基二甲胺(NDMA)以及N-亚硝基二乙胺(NDEA)会导致肝癌和鼻窦癌等疾病[1 − 2]. 此外,NDMA还可能诱导基因和染色体的突变以及引起DNA损伤[2]. 美国环境保护署综合风险信息系统(US EPA IRIS)[3]及国际癌症研究机构(IARC)[1]将9种亚硝胺(包括NDMA、NDEA、N-亚硝基甲基乙胺(NMEA)、N-亚硝基吡咯烷(NPYR)、N-亚硝基吗啉(NMOR)、N-亚硝基哌啶(NPIP)、N-亚硝基正丙胺(NDPA)、N-亚硝基二苯胺(NDPhA),和N-亚硝基正丁胺(NDBA))评定为(很)可能的人体致癌物[4 − 5].
近年来,人们在饮用水、污水、以及自然水体如河流、地下水中均发现了亚硝胺的存在[6 − 8],引起了人们对亚硝胺在水体中的分布、来源及其对人类健康产生的负面影响等一系列问题的关注[9 − 11]. 环境水体中的亚硝胺主要来源于工业废水、生活污水、农业和养殖废水的排放以及各类水体消毒过程[12]. 此外,受污染水体中广泛存在溶解性有机质(DOM)和多种胺类化合物等亚硝胺前体物,这些前体物可在不同条件下发生亚硝化等反应生成亚硝胺,从而增加环境水体中亚硝胺的浓度.
亚硝胺类化合物在水环境中的存在会对水生态安全和人体健康产生威胁. 水体中亚硝胺可通过多种不同的暴露途径影响人体健康,包括食物摄入、抽烟、呼吸、皮肤接触及使用药品和护理品[13]. 由于亚硝胺可能诱导基因和染色体的突变及引起DNA损伤,降低性激素活性,具有一定的遗传毒性,自然水体中的亚硝胺也可能对水生态环境造成潜在威胁[14].
随着人类活动的增多,排入环境中的亚硝胺类化合物将大量增加,环境水体(含饮用水源)中的亚硝胺污染日益严重,饮用水和自然水体中亚硝胺的污染特征及其所产生的生态风险和人体健康风险值得持续关注. 本文综述了亚硝胺及前体物在国内外饮用水及自然水体中的污染状况、来源、人体健康风险和生态风险,并确定了亚硝胺及其前体物的主要一次排放来源和二次生成的主要路径,以期为控制和治理亚硝胺污染提供参考.
-
表1展示了水中常见的9种亚硝胺的分子结构、理化性质和致癌等级. 从表1可以看出,亚硝胺大多为极易溶于水,不易溶于脂类且难于从水中挥发. 亚硝胺的来源及性质决定了此类化合物易于向自然水体分布扩散,并且还会通过一定的迁移转化过程进入到饮用水源,威胁饮用水安全[15 − 16].
-
饮用水中的亚硝胺较早报导于美国和加拿大的饮用水处理厂. BARRETT等[17]在21个水处理设施和分配系统的出水和自来水中检出了高达25 ng·L−1的NDMA,而在原水中几乎无检出. CHARROIS等[18]调查了安大略省179家水处理厂的亚硝胺含量,涉及进水、出水和自来水样品共计
3000 余份. 在接受调查的179个饮用水系统中,30%检出NDMA(ND—66 ng·L−1),部分水样中还检出NMOR(ND—2 ng·L−1)和NPYR(4 ng·L−1). 随后,其他国家相继对饮用水中亚硝胺的污染状态进行了调查研究. 如表2所示,巴西自来水中检测出7种亚硝胺,总浓度为110 ng·L−1[19],意大利检出4种亚硝胺,总浓度为113.1 ng·L−1[20]. 相比之下,英国、西班牙、日本和韩国饮用水中总亚硝胺(TNAs)浓度较低,分别为32.9 ng·L−1[21]、28.7 ng·L−1[22]、10 ng·L−1[23]和2.1 ng·L−1[24].我国饮用水亚硝胺污染状况调查研究显示,117个水样中,亚硝胺的检出率为76%,9种亚硝胺均有检出,总平均浓度为67.2 ng·L−1[16],与世界上其他国家相比处于中上水平. 上海(171.6 ng·L−1[25])和江苏(131.1 ng·L−1[26])的饮用水中亚硝胺浓度偏高. 南方某城市的饮用水中检测出8种亚硝胺,总浓度为16.8 ng·L−1[27]. 台湾地区饮用水中亚硝胺总浓度(39.7 ng·L−1[28]). LUO等[29]对华中地区采用二氧化氯和氯气组合的饮用水系统中的进水、出水和自来水进行监测,研究发现,在测定的9种亚硝胺中,NDMA检出率最高,平均浓度为2.5—67.4 ng·L−1,其次是NDEA(0.3—24.9 ng·L−1)和NPIP(0.3—10.3 ng·L−1). NDMA、NDEA和NPIP的平均浓度从进水、出水再到自来水呈下降趋势,体现了水处理对于降低饮用水中亚硝胺暴露风险的必要性.
一些专家认为饮水中亚硝胺高于7 ng·L−1时即对人体健康产生危害[30]. 但目前世界各国制定的饮水中亚硝胺的限值大多高于7 ng·L−1,且差异较大. 世界卫生组织(WHO)已将NDMA纳入其饮用水质量标准,建议的最大浓度为100 ng·L−1[31],澳大利亚也采用了此标准[32]. 德国提出NDMA和NMOR暂定的标准限值为10 ng·L−1[33]. 加拿大卫生部制定了饮用水中NDMA的最大标准值为40 ng·L−1[34]. 而加拿大安大略省环境部与美国加州公共卫生部对饮用水中NDMA、NDPA和NDEA制定了更严格的标准限值,分别为9 ng·L−1和10 ng·L−1[35 − 36]. 迄今为止,我国只有上海和深圳两个城市制定了当地的NDMA标准(100 ng·L−1),与WHO的规定相同[37].
总的来说,现有调查表明,饮用水中广泛检出亚硝胺,NDMA是饮用水中浓度和检出率最高的化合物. 与欠发达国家和区域相比,经济发达、人口密集和工农业高度发展的国家和区域饮用水中亚硝胺的污染更为广泛和严重. 饮用水中亚硝胺的出现归因于原水中亚硝胺类化合物的存在以及水处理过程中的氯化和氯胺化等消毒过程. 在饮用水分配系统中,余氯与残留的亚硝胺前体物反应生成亚硝胺也是自来水中亚硝胺存在的重要原因之一. 如何降低饮用水系统中亚硝胺的浓度和控制亚硝胺的生成仍是目前饮用水中亚硝胺研究的热点.
-
受工农业废水和生活污水[38]等的排放影响,亚硝胺在地表水体,含河流、湖泊、池塘等环境中均频繁检出[39 − 41],且呈现高度的空间变异性. 亚硝胺的低蒸气压、低亨利常数、低lgKow和强溶水性使其很难吸附于颗粒物或从水中挥发,易随着地表水进行迁移,并通过地表水和地下水的交互作用进入地下水[42],最终汇入海洋,污染河流下游地区、地下水环境及近海区域.
如表3所示,东京河水中的NDMA浓度为 < 0.5—3.4 ng·L−1,地下水中的浓度与地表水相似(< 0.5—5.2 ng·L−1)[43]. 韩国的汉江中,6种亚硝胺总浓度最高为44 ng·L−1,但在洛东江和釜山的地表水中,亚硝胺总浓度可分别高达735.7 ng·L−1[44]和
5180 ng·L−1[45]. 在美国洛杉矶地表水中NDMA浓度高达2534 ng·L−1[39]. 地下水中高含量的NDMA由美国加利福尼亚州卫生署在上世纪70年代发现,含量高达400000 ng·L−1,并指出这与火箭燃料不对称二甲肼(UDMH)基团的氧化有关[46].在我国,高浓度亚硝胺出现在贾鲁河流域(11.7—385.8 ng·L−1)[47]、松花江(1.6—62.4 ng·L−1)[42]和珠江流域(ND—
1090 ng·L−1)[48]. 相比之下,长江中下游(ND—32 ng·L−1)[38]、滦河(ND—12.4 ng·L−1)[49]和台湾高平河(ND—4.4 ng·L−1)[50]中亚硝胺浓度稍低(表2). 与地表水和地下水相比,河口和近海区域亚硝胺的报导十分缺乏. LEE等[45]对韩国釜山近岸海域海水中NDMA的研究是目前海水中亚硝胺的唯一报导,其结果显示,海水样品中8种亚硝胺的总浓度为44.2—166 ng·L−1,NDMA(40.0—166 ng·L−1)和NPYR(1.2—32.7 ng·L−1)是浓度最高且检出率高的两种化合物.河口-近海区域是人口、工业和农业的密集区,是污水排放的最终受纳体,陆域水体中的亚硝胺在排入河流中后,随水流进行迁移,最终汇入海洋. 对长江秭归至东海段河水中亚硝胺的研究显示,每年从长江带入东海的亚硝胺大约5.4 t[38]. 由于亚硝胺仍属于未被监管污染物,且海水不涉及饮水安全管理的范畴,目前国内外关于近岸海域海洋环境中亚硝胺的污染研究仍十分缺乏. 在我国重点海域生态环境问题大力整治的背景下,针对极具致癌风险的亚硝胺的污染特征揭示和来源研究十分必要.
-
污水中亚硝胺的含量水平显著高于其他类型水体. 我国和美国污水中亚硝胺的浓度分别高达82.0—607.9 ng·L−1[47]和130—
12700 ng·L−1[53]. 工业污水中亚硝胺的含量通常高于农业污水和生活污水. CHEN等[48]对珠三角中不同类型的工厂、生活污水处理厂和农业养殖污水的亚硝胺浓度进行了调查,结果显示,电镀废水(3920 ng·L−1)和印染废水(4320 ng·L−1)中亚硝胺的浓度最高,其次为养殖废水(1000 ng·L−1),最后为生活污水(60 ng·L−1)和医药污水(28 ng·L−1). 美国加利福尼亚州的电子印刷厂废水中检测到的NDMA浓度(65—170 ng·L−1)也明显高于当地居民区的生活污水(17—63 ng·L−1)[54]. 在日本釜山的工业园区(主要包括:机械电子厂、纺织和石油化工厂)检出亚硝胺含量高达1440 —29100 ng·L−1[45]. -
生活污水和工农业污水的排放是河流等环境水体中亚硝胺最重要的点源. 生活污水中,含有洗发水、洗手液、洗碗皂和洗涤剂的灰水和黑水均含有亚硝胺,洗衣水是亚硝胺最常见的来源,其次是淋浴水和尿液[55]. ZENG等[55]在洗衣水、尿液和淋浴水中均检测出高浓度的亚硝胺,TNAs平均浓度为680、210、54 ng·L−1. 工业污水中亚硝胺通常来自于所使用的工业原料(或受亚硝胺污染的工业原料)和工业过程的非故意生成. 比如,美国加利福尼亚奥兰治县服务区电镀废水中高浓度的NDMA(高达
105000 ng·L−1)经调查发现来自于被NDMA污染的二甲基二硫代氨基甲酸盐(dimethyldithiocarbamate,此化学品用于去除废水中的重金属)[56]. -
对亚硝胺而言,除一次排放外,二次生成也是环境中亚硝胺不可忽视的来源,体现为地表水、地下水等环境水体中高浓度的亚硝胺生成势(FP). WANG等[42]在松花江流域的河水和地表水分别检测出6种和5种亚硝胺FP,总浓度分别为1.7—72.1 ng·L−1和1.1—37.3 ng·L−1. 此外,在长江中下游中检测出6种亚硝胺FP,总浓度为ND—141 ng·L−1,其中NDMA-FP浓度最高,平均浓度为64 ng·L−1[38]. 长江三角洲的水库中检测出NDMA-FP为16—60 ng·L−1[16]. 其他在土耳其的布于科切克美杰流域中的湖泊和河流中检测出NDMA-FP高达
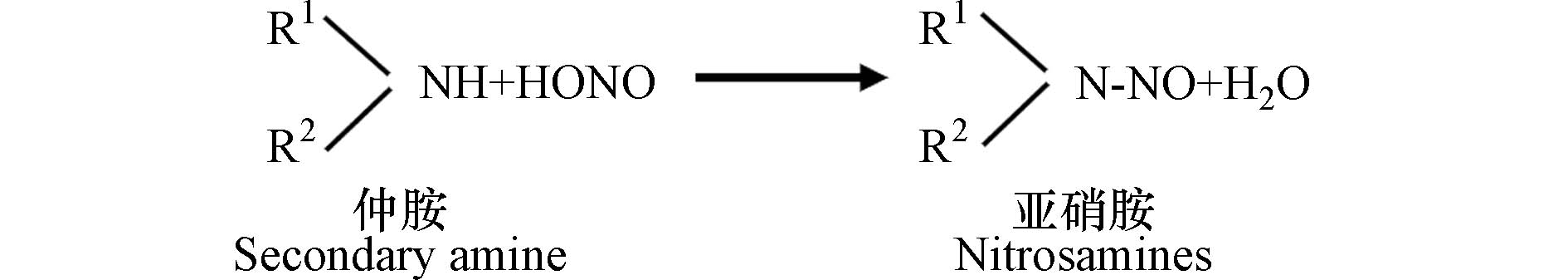
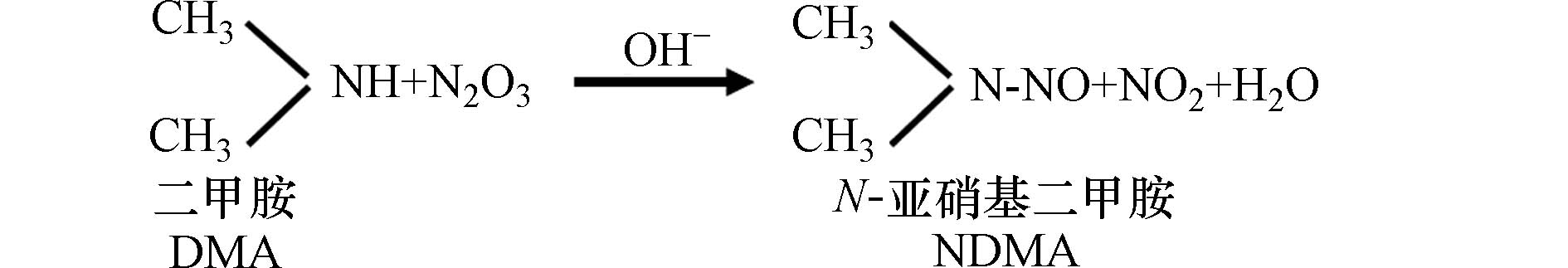
1648 ng·L−1[57],西班牙水库NDMA-FP为16—60 ng·L−1[58],东京河流和地下水中也检测出NDMA-FP,浓度分别为0.7—7.8 ng·L−1和ND—10.8 ng·L−1[43]. 同时,CHARROIS等[18]对艾伯塔省公共饮用水分配系统的研究发现,其一个公共设施水中的有机氮浓度异常高,这导致了高浓度NDMA(系统中部为66 ng·L−1,系统末端为100 ng·L−1)的形成,水中亚硝胺的存在可能与有机氮的存在正相关.水环境中亚硝胺的二次生成涉及化学、光和生物过程. 胺类物质在弱氧化、弱交互的环境下可发生亚硝化反应生成亚硝胺类化合物[59]. 在光解反应过程中,亚硝胺很容易在水体中由二甲胺(DMA)和N2O3合成[60],反应途径如图1所示. 微生物对亚硝胺二次生成的影响在于其可转化或分解产生亚硝胺前体物氨氮和亚硝酸盐[61],亚硝酸盐在酸性水体中产生亚硝酸,亚硝酸与仲胺相互作用,形成亚硝胺[62],反应途径如图2所示. 此外,富营养化刺激下水体中藻类生物的密集生长将促进胺的形成,胺在亚硝化催化剂的存在下可与其代谢物合成亚硝胺[63]. 微生物的参与也可催化中性或碱性条件下亚硝胺的形成(通常该条件下亚硝胺不易形成)[64].
目前在复杂环境水体中亚硝胺的生成潜力及机制研究尚不充分. 通过FP实验揭示环境水体中亚硝胺的二次生成潜力,对于未来推测亚硝胺的最佳赋存环境和污染控制,以及潜在风险评估,均具有重要意义.
-
针对亚硝胺生成机理的研究多涉及无机的和有机的含氮化合物[65]. 事实上,环境水体中几乎所有人为排放的或天然的含氮化合物均有可能在特定条件下参与反应生成亚硝胺或其前体物,直接或间接导致水体中亚硝胺浓度的增加. 不同国家(如美国、中国、西班牙和澳大利亚)已对地表水、地下水和废水[47 − 48,58,66 − 67]中亚硝胺的关键前体物进行了大量研究. 与亚硝胺生成相关的直接前体物可分为DOM、有机胺类、水处理过程中使用的含胺聚合物和人类生活和生产活动大量使用的药品、个人护理产品和杀虫剂等几大类.
(1)DOM
DOM是水生环境中天然有机物(NOM)的主要部分[68]. 在消毒过程中DOM可以转化为亚硝胺等消毒副产物(DBPs)[69]. 室内实验中也发现DOM会促进DBPs的形成[70],证明DOM是水中亚硝胺的重要前体物之一. 在某些研究中,DOM甚至被用作地表水体和水处理厂中DBPs前体物的替代品[71].
DOM作为亚硝胺的前体物与DOM的结构和成分有关. DOM的亲水部分比其疏水部分容易形成更高的NDMA[72 − 73]. WANG等[73]系统研究了不同馏分DOM对NDMA-FP的影响,发现亲水馏分对NDMA-FP的影响程度是疏水馏分的1.3—3.5倍[72]. 降低溶解有机碳(DOC)/溶解有机氮(DON)的比例可增加NDMA的浓度,说明DON可能是NDMA的有效前体[73]. 因NOM和DOM的结构具有高度可变性和地点特异性,上述研究强调了DOM在亚硝胺形成中的复杂作用. 就分子大小而言,与大分子相比,低分子量(< 1 kDa)的DOM更有利于NDMA、NPYR、NMOR和NPIP的形成. 一项使用高分辨率质谱(HRMS,Orbitrap)来分析DOM和NDMA-FP之间关系的研究发现,氢/碳原子比(H/C)> 1.5的DOM成分与NDMA-FP呈正相关[74]. 这些成分是含有较高杂原子DOM中可被生物分解的部分,可作为水体中潜在的废水输入或藻类繁殖的标志[75].
(2)有机胺类
有机胺类化合物的氧化被确定为水中亚硝胺形成的主要途径. 仲胺、叔胺和季胺都是亚硝胺的直接前体. 水体中有机胺的主要来源是由动植物(含人类)、农业和工业排放物排放的有机物质的分解. 据了解,人体排泄物中的脂肪族胺(如DMA)占废水中NDMA-FP的20%—30%[76]. 地表水中DMA的典型浓度在1—3 μg·L−1范围内,但在接收大量污水排放的地表水中,浓度可达到mg·L−1水平. 因此,DMA被广泛用作研究NDMA生成机理的模型前体[41].
一些研究还调查了消毒过程中含有DMA官能团的叔胺和季胺形成NDMA的情况,结果说明不含DMA官能团的叔胺和季胺不会产生大量的NDMA[77 − 78]. MITCH等[79]研究了甲胺(MA)、DMA、三甲胺(TMA)和四甲胺(QMA)的氯胺化作用,以探究氮原子周围的甲基数量对NDMA生成的影响,结果发现MA和QMA对NDMA生成无显著影响. 同样,FIDDLER等[80]的研究发现,亚硝化含TMA官能团的季胺比亚硝化TMA形成的NDMA含量低4个数量级,含DMA或TMA官能团的季胺在氮上缺乏自由孤对电子是NDMA生成减少的重要原因之一. 因此,DMA和带有DMA官能团的叔胺被认为是亚硝胺的有效前体. 叔胺可通过两个步骤生成NDMA:(1)与氯或氯胺反应将叔胺脱烷基为DMA;(2)将DMA亚硝化为NDMA[81].
(3)含胺聚合物
基于胺的水处理聚合物已经被证明是NDMA和其他亚硝胺的重要前体物. 聚合物在饮用水和废水处理厂中是用以去除悬浮颗粒和消毒的凝结剂和絮凝剂. 用这些聚合物处理饮用水和废水的可能导致NDMA和其它亚硝胺的形成. 这类聚合物包括:聚胺、聚二甲基二烯丙基氯化胺(PolyDADMAC)、氨甲基化聚丙烯酰胺(Mannich)、丙烯酰氧乙基三甲基氯化胺(ADAMQUAT),以及阳离子聚丙烯酰胺(CPAM)共聚物[78,82 − 84].
亚硝胺的形成取决于聚合物的性质,如结构、分子量、纯度和合成过程中涉及的中间体,以及消毒参数,如pH值、接触时间和使用氧化剂的剂量[85]. 为了抑制两种常用聚合物PolyDADMAC和环氧氯丙烷-二甲胺(Epi-DMA)中亚硝胺的形成,ZENG等[86]通过两种方式改变聚合物的结构:1)使用甲基碘(MeI)将聚合物结合的叔胺基团转化为氯胺活性较低的季胺基团(NDMA的形成降低了75%);2)合成具有二丙基氨基取代基的聚合物,使氯胺与季胺基团反应减少(没有NDMA形成,而是形成产率低20倍的NDPA). 因此,使用具有季胺基团的高分子量聚合物更能降低水处理厂中NDMA形成的风险. 阳离子胺基聚合物,如CPAM,其分子结构缺乏DMA基团[87],本身不具备生成高产量亚硝胺的能力[88],但由于在水处理过程中,为了保证处理效果常被过量投放,其在水中的高残留也会导致亚硝胺的生成. 因此,在水处理过程中,选择合适的聚合物并注意控制用量都是减少亚硝胺生成的有效手段.
(4)药品、个人护理品和杀虫剂
水环境中部分痕量或超痕量的药品和个人护理品(PPCPs)[89 − 90]及农药[91]也是亚硝胺的重要前体物. 例如,美国食品药品管理局(FDA)批准的新药贝曲沙班经氯胺消毒后,NDMA生成量超过1%[92]. 其他被证实为亚硝胺前体物的PPCPs和农药还包括美沙酮[93]、氯苯那敏[94]和二硫代氨基甲酸盐[95].
这些前体物的亚硝胺生成潜力取决于母体化合物、其转化产物和代谢物[96]. LE ROUX等[97]研究发现,与DMA相比,一些含有DMA的药物和农药具有更高的NDMA生成潜力. SHEN等[98]也发现在所有研究的20种带有DMA基团的药品中,有8种药品显示NDMA-FP超过1%. 这些研究证明了叔胺的结构特征使药物和农药具有更高的NDMA摩尔转化率. 一些药物(如雷尼替丁)可在不经过仲胺中间体的情况下产生较高含量的NDMA[87]. 考虑到某些PPCPs和杀虫剂对NDMA的生成量高于DMA,从水源水中去除这些痕量污染物对降低消毒过程中NDMA的生成至关重要.
-
(1)天然来源
天然源是环境中有机胺的来源之一. 生物胺可通过氨基酸脱羧(通常通过微生物过程)或酮和醛的胺化形成[99]. 对海洋系统的研究表明,脂肪族胺(伯胺、仲胺和叔胺)通常源自生物,许多水生生物能够产生并向水中释放胺(包括伯胺和更复杂的化合物),这些化合物在偏远海洋环境的碳和氮循环中发挥着重要作用[100 − 101]. 水生生物在活着和死后被微生物分解的过程中会释放出许多亚硝胺的前体物[102]. 例如,伯胺是在哺乳动物和细菌细胞膜中发现的磷脂重要降解产物,同时胺可以通过氨基酸的脱羧形成[103]. 而腐烂的鱼发出的气味是由于富含蛋白质的组织中的氨基酸分解而释放出TMA[104]. 这些过程可能是水生生态系统中胺的重要原位来源.
除原位来源外,水环境中胺类化合物还可能来自于陆地集水区域. 胺和胺前体是土壤有机氮的重要组成部分[105],可以从集水区经地表径流冲刷输送到水生系统. 淡水中胺的其他潜在天然来源包括海鸟和其他迁徙的野生动物. 这些生物可通过粪便和尿液将胺和胺相关化合物直接释放或通过集水区间接释放到水中. 在沿海水域,大量从陆地来源的腐殖质可经光化学过程形成伯胺[106].
(2)污废水的一次排放
与亚硝胺相似,环境水体中亚硝胺前体物同样被认为大多与生活废水和工业污水的一次排放有关[107]. 生活废水中洗发水、洗手液、洗碗皂和洗涤剂的灰水和黑水含有亚硝胺前体物[55],废水中的蛋白质和含氮化合物也会形成仲胺和叔胺[47]. 大量无机和有机的含氮化合物也随各行业的废水进入环境水体中,包括养殖场、酿酒厂、啤酒厂、海鲜加工厂、乳制品厂、肉类加工厂、药品制造工厂和个人卫生用品生产行业[108]. 在贾鲁河流域附近的工业园区污水、居民区生活污水和入河下水道均检测到亚硝胺前体物,浓度分别为53.18、12.64、8.69 μg·L−1[47]. 从天然气中去除二氧化碳的工业流程也会向大气释放胺[109],胺进一步沉降到环境水体,增加环境水体中亚硝胺FP. 此外,燃烧后的二氧化碳捕集可能成为环境中胺的一个重要工业来源,在二氧化碳捕获过程中,胺会发生亚硝化作用,产生亚硝胺[110].
前体物作为工业原料常用于工业产品的合成、染色等,成为了工业废水中前体物的主要来源. 比如,仲胺(一种重要的亚硝胺直接前体物)大量用作化学、杀虫剂和药物合成的中间体[47]. 1,6-六亚甲基-双(N,N-二甲基氨基脲)(HDMS)和双(N,N-二甲基酰肼氨基-4-苯基)甲烷(TDMS)在工业上常用于防止聚氨酯纤维变黄. 这两种化合物都含有DMA基团,其经过臭氧氧化后会产生大量NDMA(50 mmol·L−1 染料溶液能够产生超过
1000 ng·L−1[111]). 这些染料在工业废水中的出现将显著增加废水臭氧化后NDMA的浓度,从而增加了接收河水中NDMA的浓度[112]. -
亚硝胺属于典型的DBPs,原水经氯消毒、氯胺消毒、臭氧消毒、紫外线消毒等处理均能生成亚硝胺类化合物[113]. 对污水厂二级处理的出水进行氯消毒通常会导致20—100 ng·L−1 NDMA的生成[114]. 与氯消毒相比,氯胺化反应有更高的亚硝胺生成潜力[65,79,82]和检出率[115]. ZHAO等[116]对美国11个污水处理厂不同消毒方式下NDMA的生成情况进行了更为全面的对比. 结果显示,原水中NDMA的浓度为ND—53 ng·L−1,化学消毒导致NDMA浓度增加到ND—118 ng·L−1;氯化、氯胺化和二氧化氯消毒均可使出水中NDMA浓度增加[116 − 118],但使用臭氧和二氧化氯可减少NDMA生成的效率,减少程度取决于源水中亚硝胺前体的性质. 部分水体经过高级氧化处理(AOP、H2O2/UV)后NDMA含量高于源水[116]. 高锰酸盐也被证明在氧化DMA时(特别是在亚硝酸盐存在的情况下)可产生少量的NDMA,此过程中MnO2充当了催化剂[119].
亚硝胺在消毒过程中的生成主要源于残留消毒剂和水中有机物之间的相互作用[113]. 使用氯胺消毒时,在典型的氯胺化条件下,二氯胺总是与一氯胺共存(2NH2Cl + H+
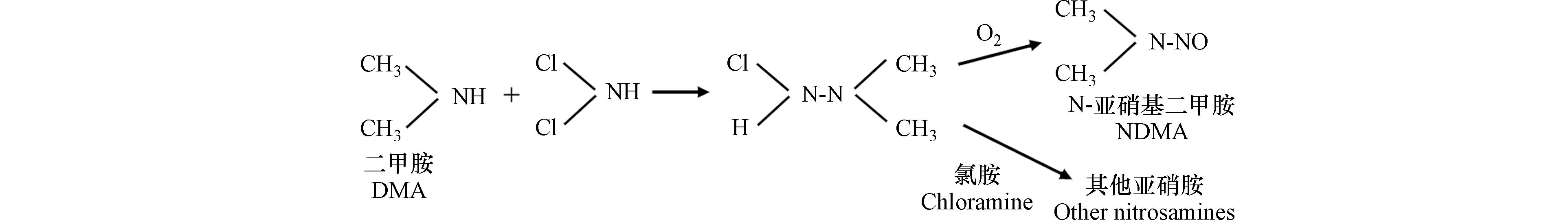
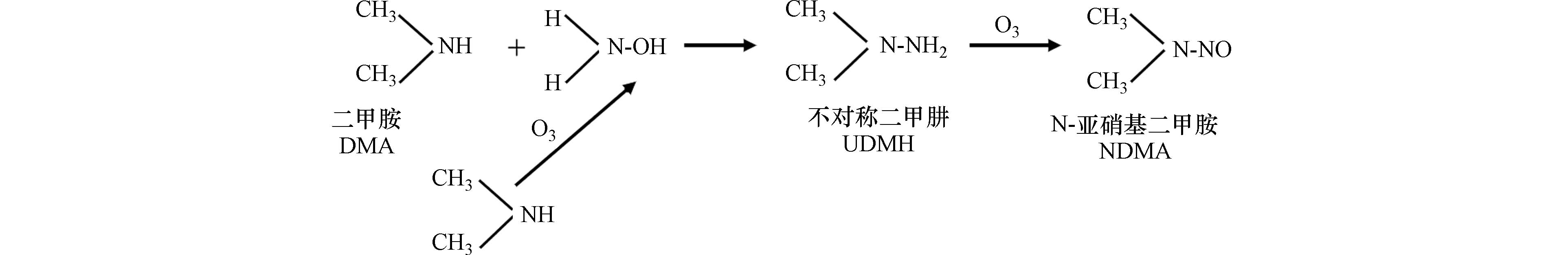
$ \leftrightarrow $ NHCl2+NH4+),因此几乎所有亚硝胺的形成都可以通过涉及低浓度二氯胺(5%)的反应来解释[120]. 比如,未质子化的DMA会对二氯胺进行亲核攻击,形成氯化的偏二烷基肼中间体(如Cl-UDMH),然后被溶解氧氧化成相应的亚硝胺[120],该途径可能是水处理中亚硝胺生成最重要的途径(图3).在臭氧氧化下,氧化剂与DMA接触,部分DMA被氧化成亚硝酸盐和硝酸盐(通常也会检测到甲醛和甲酸),亚硝酸盐转化为更强的亚硝化剂N2O4. 增强的亚硝化作用有助于DMA臭氧化生成NDMA,但产率受水中pH的显著影响:在pH值为10.5时,DMA的臭氧氧化生成NDMA的产率为0.4%;在pH < 8时,几乎不可能出现NDMA[59],此外,在臭氧氧化条件下,水体中DMA在初始阶段氧化形成羟胺(NH2OH),羟胺与DMA亲核取代形成UDMH中间体,经过臭氧氧化生成NDMA. 随着pH值的增加,更多的氢氧根离子(OH−)加速了臭氧分解,产生羟基自由基,随后将DMA氧化为更多的羟胺,从而产生更多的NDMA,反应路径如图4所示[117]. 因此,在常规水处理中(原水pH多为中性),臭氧氧化DMA不是NDMA生成的主要路径,但对于污水消毒和水回用仍具有一定的适用性.
除消毒方式外,影响亚硝胺生成的其他因素还包括氧化剂的接触时间和用量. 一般来说,在消毒过程中,亚硝胺的生成会随着氧化剂的接触时间和剂量的增加而增加. 例如,绿麦隆与2 mmol·L−1氯胺反应240 h后,由绿麦隆生成的NDMA从4 mg·L−1逐渐增加到23.3 mg·L−1[122]. 在一氯胺存在的情况下,用辐射剂量为350—850 mJ·cm−2范围的UV(254 nm)照射氯化仲胺会增加亚硝胺的浓度[123].
-
由于亚硝胺的高致癌性,摄入、吸入或皮肤接触环境水体(水源水、地表水和地下水)中亚硝胺,可能会对人类健康造成巨大威胁. 为更好地了解水中亚硝胺对人体健康的潜在风险及危害程度,可根据《超级基金风险评估指南》A、E、F部分,进行人类健康风险评估,以评价环境水体中亚硝胺对人体的致癌风险[124 − 126]. 考虑到暴露途径和吸收特征的差异,化学品的健康风险往往反映了暴露于所有外源化合物的综合效应[127]. 综合暴露风险一直是毒理学效应评估中的一个难题. 从风险评估的角度来看,风险评估方法应能够预测潜在的最大风险,因此通常采用效应相加的方法评估混合暴露风险. 美国环保局(US EPA)指出,对于小于0.1的总致癌风险,精确结果和简单添加模型结果之间的差异非常小[126]. 因此,暴露于多种亚硝胺的影响可使用简单的添加模型来进行计算.
国内外学者对亚硝胺的人体致癌风险评价已开展大量研究. 一项全国性的调查结果显示,我国20个省份饮用水中NDMA和NDEA致癌风险值分别为1.25×10−5和1.3×10−6,高于癌症风险可接受水平(10−6)[37]. 上海TNAs(8.29×10−5)、NDMA(5.58×10−5)、NDEA(3.32×10−5)[25];绍兴TNAS(3.49×10−5)、NDMA(1.00×10−5)、NDEA(2.26×10−5)[128];淮安TNAs(3.11×10−5)、NDMA(0)、NDEA(2.51×10−5)[26];南京TNAs(1.03×10−5)、NDMA(5.56×10−6)、NDEA(2.92×10−6)[26]和台湾TNAs(1.35×10−5)、NDMA (6.39×10−6)、NDEA(4.41×10−6)[28]部分饮用水中亚硝胺的致癌风险均高于US EPA可接受风险. 一项针对我国南方某城市3个饮用水处理系统亚硝胺的动态监测显示了同样存在潜在风险的NDMA(7.67×10−6)和NDEA(3.48×10−6)[27]. 对使用河流地表水以及地下水作为直接饮用水的地区而言,长江中下游(2.5×10−5)[38]、松花江(1.6×10−5)[42]和贾鲁河流域地下水(1.36×10−5)[47]中亚硝胺也将造成显著致癌风险.
与其他国家的饮水致癌风险相比,中国大陆地区平均水平NDMA(1.25×10−5)高于加拿大[6]NDMA(8.45×10−6)和日本[23]NDMA(2.19×10−6). US EPA[129]针对美国饮水的调查数据显示NDMA(1.31×10−5)与中国大陆平均水平相似.
不同暴露途径以及不同人群之间的对比研究显示,对于暴露于水环境中亚硝胺而言,口服摄入的风险通常远高于皮肤吸收的风险,而儿童和青少年的患癌风险明显高于成人[25 − 26,28 − 29,38].
目前,饮水中亚硝胺的广泛存在及其所造成的高致癌风险已引起了全世界人民对饮水安全的担忧,政府和供水机构应引起高度重视.
-
亚硝胺及其前体物在不同物种中会诱导恶性肿瘤的发生. DMA、NDMA和NDEA主要在各种哺乳动物(恒温动物)中诱发肝肿瘤、胆管肿瘤和肝细胞癌[130 − 131]. 尽管变温动物(鱼和两栖动物)和恒温哺乳动物之间存在显著的物种差异,但亚硝胺诱导的肿瘤在定位和形态结构上往往是相似的. 在环境水体中,高浓度亚硝胺及其前体物的存在直接或间接地影响着水环境生态系统健康和发展. 因此对亚硝胺进行生态风险评价以评估其对水生态环境危害,可为环境决策或与其相关的标准或基准的制定提供参考依据[132].
据现有的生态风险评价技术指南,可使用风险熵值法(RQ)评估水环境中亚硝胺在急性毒性水平下对鱼类、水蚤和藻类3个种群造成的生态风险[133 − 134]. 根据RQ值的不同,生态风险分为低风险(RQ ≤ 0.1)、中风险(0.1 < RQ ≤1.0)和高风险(RQ > 1.0)3个级别[135]. CHEN等[38]对长江中下游的亚硝胺进行生态风险评价,结果显示亚硝胺对鱼类、水蚤和绿藻的生态风险较低(RQ < 0.01);不同物种之间对比,亚硝胺对绿藻的生态风险最高,其次是水蚤和鱼类. LI等[136]对华东地区研究也有相似的结果,9种亚硝胺对鱼类、水蚤和绿藻的生态风险都较低(RQ < 0.01). 亚硝胺对水体生态环境的风险评估研究仍不广泛,因此目前的研究结果并不能完全排除亚硝胺对生态系统造成的风险. 环境水体中普遍存在亚硝胺污染,考虑到亚硝胺对生物的高致癌和致畸性,需对亚硝胺所造成的生态风险作进一步研究.
-
亚硝胺是世界公认的三大致癌物之一. 本研究根据近20年国内外发表的研究报告,总结了水体中亚硝胺的污染状况、来源及风险. 目前针对饮用水和环境水体中亚硝胺的调查研究大多在大国和发达地区进行,在小国和欠发达地区的研究较少. 基于风险评估,水体中亚硝胺的广泛存在已对人体健康造成潜在致癌风险. 为降低饮用水和环境水体中亚硝胺的赋存水平,保障饮水安全和生态系统健康,未来的研究重点应着重以下几个方面:
(1)优化自来水厂和污水处理厂的消毒方案,处理过程中使用非胺替代聚合物和开发针对亚硝胺的新处理工艺以提高水中亚硝胺及其前体物的去除.
(2)含高浓度亚硝胺的工农业污水的排放是环境水体中亚硝胺的重要点源. 规范各类工农业和污水处理厂的废水排放,制定和建立亚硝胺的污水排放标准,并加强环境监测将是减少环境水体中亚硝胺污染的有效手段.
(3)据目前少量研究,地下水存在多种亚硝胺,平均总浓度低于世卫组织规定的限值(100 ng·L−1),但对于某些直接饮用地下水的地区(欠发达地区和农村偏远地区)而言,此限值过高,亚硝胺所造成的致癌风险被忽视,应进一步加强地下水中亚硝胺的污染研究和风险评估.
(4)河口-近海区域是污水排放的最终受纳体,在近海水体亚硝胺总浓度可高达166 ng·L−1,开展对极具致癌风险的亚硝胺的污染特征揭示和来源研究十分必要.
(5)目前生态风险评估方法较简单,未考虑多种亚硝胺及其前体物的综合效应以及遗传毒性,有必要基于多种亚硝胺在环境浓度水平下对基因和后代的长期影响,建立准确可靠的风险评估模型,以更准确地评估亚硝胺的生态风险,为亚硝胺环境标准的制定提供科学依据.
水中N-亚硝胺的污染状况、来源及风险
Occurrence, sources, and risk of N-nitrosamines and precursors in water: A review
-
摘要: N-亚硝胺类化合物是一类被国际癌症研究机构列为高毒性和强致癌性的有机污染物,是世界公认的除黄曲霉素、二噁英之外的第三大致癌物. N-亚硝胺水溶性强,广泛存在于环境水体(地表水、地下水)和饮用水当中. 局部地区(特别是城市地区)环境水体及饮用水中的高浓度亚硝胺已对人体和生态健康构成较大威胁. 除工业、农业和生活的一次排放外,前体物存在情况下的二次生成也是水体中亚硝胺持续存在的关键原因,某些情况下可能比一次来源更为重要. 本文综述了环境水体及饮用水中N-亚硝胺的污染水平、组成和空间分布,给出水体中亚硝胺污染的重点化合物和重点区域;总结了导致亚硝胺二次生成的重要前体物,并归纳了N-亚硝胺在环境水体及饮用水系统中的一次来源及二次生成的机理过程,探索降低水体中亚硝胺污染的可行措施,为保障饮水安全和生态健康提供关键支撑.Abstract: : N-nitrosamines with high toxicity and carcinogenicity are one of the three carcinogens in addition to aflatoxin and dioxins. With high water solubility and low volatility, they widely occur in environmental water (including surface water and groundwater) and drinking water systems. The high concentrations of N-nitrosamines in environmental waters and drinking water (especially in urban areas) have posed a significant threat to the health of human beings and ecological systems. N-nitrosamines mainly originate from the primary emission of industrial, agricultural, and domestic wastewater. Secondary generation in the presence of precursors is also the key reason for the occurrence of N-nitrosamines in water bodies, which may be more important than primary sources in some cases. This paper reviews the pollution level and composition of N-nitrosamines in environmental water and drinking water, highlighting the dominant and prevalent N-nitrosamine compounds in the water. Furthermore, this paper introduces the critical precursors that lead to the secondary generation of N-nitrosamines and summarizes the primary sources and secondary generation process of N-nitrosamines in the water. Results should shed light on the exploration of feasible measures to reduce N-nitrosamine’ pollution in the water and provide critical support for ensuring drinking water safety and ecological health.
-
Key words:
- environmental water /
- drinking water /
- N-nitrosamines /
- precursors /
- primary discharge /
- secondary generation.
-

-
表 1 水体中常见的9种亚硝胺的物理化学性质及致癌等级分类
Table 1. Physical and chemical properties and carcinogenic grade classification of 9 nitrosamines commonly found in water
化合物
Compound化学结构
Chemical structure相对分子质量/
(g·mol−1)
Relative molecular mass辛醇/水分配系数
lgKow溶水性/
( mg·L−1)25 ℃
Solubility亨利常数/
(atm m3·mol−1)25 ℃
Henry’s constant致癌等级a
Carcinogenic gradeUS EPA IRIS IARC N-亚硝基二甲胺 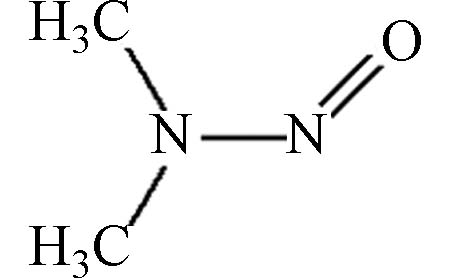
74.08 –0.57 1,000,000 1.20×10–6 B2 2A N-亚硝基甲基乙基胺 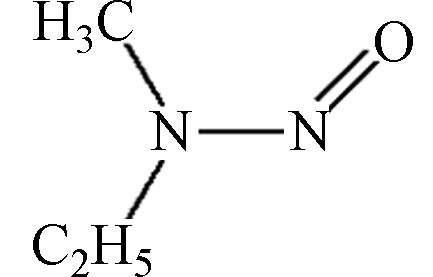
88.11 0.04 300,000 1.44×10–6 B2 2B N-亚硝基二乙基胺 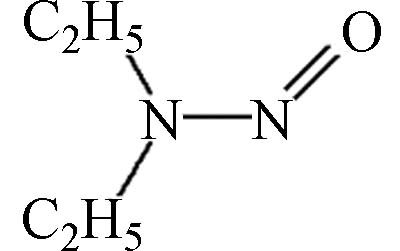
102.14 0.48 106,000 1.73×10–6 B2 2A N-亚硝基二丙基胺 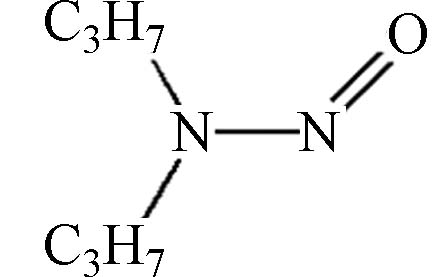
130.19 1.36 13,000 3.46×10–6 B2 2B N-亚硝基吡咯烷 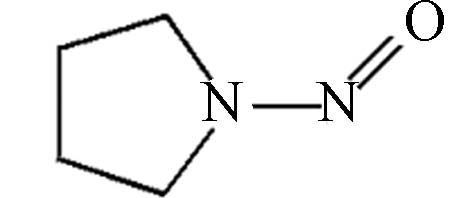
100.1 -0.19 1,000,000 1.99×10–7 B2 2B N-亚硝基吗啉 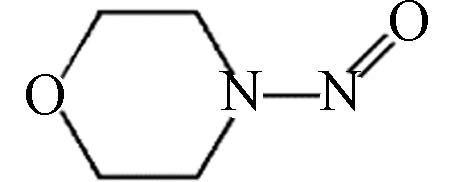
116.12 -0.44 861,528 2.13×10–10
—2B N-亚硝基哌啶 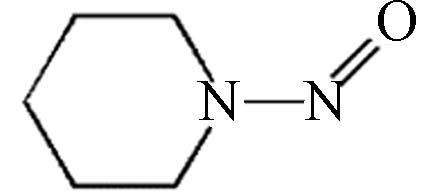
114.15 0.36 76,480 2.81×10–7
—2B N-亚硝基二丁基胺 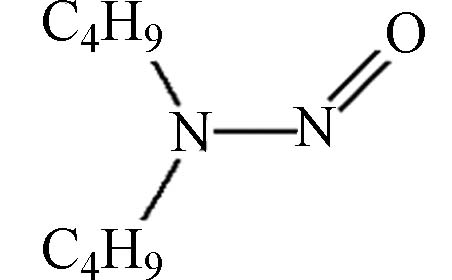
158.24 2.63 1,270 9.96×10–6 B2 2B N-亚硝基二苯胺 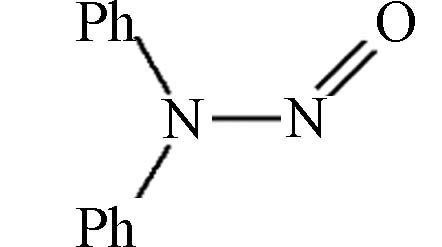
198.22 3.13 35 1.38×10–5 B2 — 注:B2,2B:表示可能的人体致癌物质,具有充分的动物实验资料,但对人体的致癌证据有限;2A:表示很可能的人体致癌物质,具有充分的动物实验资料,并且对人体有理论上的致癌性,但是实验性数据有限. ;“—”:表示缺少相关数据.
Note: B2, 2B: probable human carcinogen with sufficient animal data, but limited evidence of carcinogenicity in humans; 2A: very probable human carcinogen with sufficient animal data and theoretical carcinogenicity in humans, but limited experimental data; “—” : data not available.表 2 世界各国饮用水中亚硝胺的浓度水平(ng·L−1).
Table 2. Concentrations of N-nitrosamines in the drinking water of different countries
中国
China加拿大
Canada巴西
Brazil韩国
South Korea西班牙
Spain美国
United States英国
Britain日本
Japan意大利
ItalyNDMA 33 66 33 0.9 4.5 9 7.2 10 NA NDEA 3.3 NA 9 0.3 0.8 15 NA NA 10.3 NPIP 2.9 NA 22 NA 12 NA NA NA NA NMEA 3.1 NA 11 0.2 NA 4 NA NA NA NPYR 2.4 4 14 NA NA 5 NA NA NA NMOR 7.8 2 NA 0.4 2.9 NA 6.9 NA 83.7 NDPA 9.5 NA 10 NA NA NA NA NA 8.1 NDBA 2.7 NA 11 0.3 6.7 8 18.8 NA 11 NDPhA 2.5 NA 0 NA 1.8 NA NA NA NA 总含量 67.2 72 110 2.1 28.7 41 32.9 10 113.1 参考文献 [16] [18] [19] [24] [22] [16] [21] [23] [20] 注:NA:表示缺少相关数据. Note: NA: data not available. 表 3 世界各国环境水体中亚硝胺的浓度水平
Table 3. Concentrations of N-nitrosamines in surface water, groundwater, and seawater of different countries
研究区
Research area国家
Country亚硝胺种类
Number of
N-nitrosamines地表水/
(ng·L−1)
Surface water地下水/
(ng·L−1)
Groundwater海水/
(ng·L−1)
Sea water参考文献
Reference贾鲁河流域 中国 7 11.7—385.8 ND—101.1 NA [47] 松花江 中国 7 1.6—62.4 ND—60.8 NA [42] 珠江流域 中国 5 ND— 1090 NA NA [48] 珠江三角洲地区 中国 6 ND—517.1 ND—79.6 NA [30] 长江中下游 中国 6 ND—32 NA NA [38] 滦河 中国 3 ND—12.4 NA NA [49] 台湾高平河 中国 6 ND—4.4 NA NA [50] 洛东江 韩国 6 ND—735.7 NA NA [44] 汉江 韩国 6 4—44 NA NA [51] 釜山 韩国 8 26— 5180 NA 1.2—166 [45] 东京 日本 1(NDMA) ND—5.2 ND—3.4 NA [43] 洛杉矶 美国 1(NDMA) ND— 2534 ND—13 NA [39] 加利福尼亚州 美国 1(NDMA) NA 最高400,000 NA [52] 注:ND:表示未检出;NA:表示缺少相关数据. Note: ND: not detectable; NA: data not available. -
[1] WHO. International Agency for Research on Cancer, IARC monographs on the evaluation of the carcinogenic risk of chemicals to humans: Some N-nitroso compounds[R]. Lyon, France: WHO IARC, 1978: Volume 17. [2] LIVIAC D, CREUS A, MARCOS R. Genotoxic evaluation of the non-halogenated disinfection by-products nitrosodimethylamine and nitrosodiethylamine[J]. Journal of Hazardous Materials, 2011, 185(2/3): 613-618. [3] U. S. EPA IRIS. Chemical Assessment Summary[R]. U. S. EPA IRIS, 2012. [4] U. S. EPA IRIS. A-Z List of Substances[R]. U. S. EPA IRIS, 2015. [5] WHO. International agency for research on cancer, iarc monographs on the evaluation of carcinogenic risks to human: Agents classified by the IARC monographs[R]. WHO IARC, 2014: Volumes 1-111. [6] QIAN Y C, WU M H, WANG W, et al. Determination of 14 nitrosamines at nanogram per liter levels in drinking water[J]. Analytical Chemistry, 2015, 87(2): 1330-1336. doi: 10.1021/ac504104k [7] 李婷, 鲜啟鸣, 孙成, 等. 水中N-亚硝胺类消毒副产物的污染现状及分析技术[J]. 环境化学, 2012, 31(11): 1767-1774. LI T, XIAN Q M, SUN C, et al. The level and analysis of N-nitrosamines in waters[J]. Environmental Chemistry, 2012, 31(11): 1767-1774 (in Chinese).
[8] MCCURRY D L, KRASNER S W, VON GUNTEN U, et al. Determinants of disinfectant pretreatment efficacy for nitrosamine control in chloraminated drinking water[J]. Water Research, 2015, 84: 161-170. doi: 10.1016/j.watres.2015.07.024 [9] WANG W F, REN S Y, ZHANG H F, et al. Occurrence of nine nitrosamines and secondary amines in source water and drinking water: Potential of secondary amines as nitrosamine precursors[J]. Water Research, 2011, 45(16): 4930-4938. doi: 10.1016/j.watres.2011.06.041 [10] WANG W F, GUO Y L, YANG Q X, et al. Characterization of the microbial community structure and nitrosamine-reducing isolates in drinking water biofilters[J]. Science of the Total Environment, 2015, 521/522: 219-225. doi: 10.1016/j.scitotenv.2015.03.133 [11] WANG W F, HU J Y, YU J W, et al. Determination of N-nitrosodimethylamine in drinking water by UPLC-MS/MS[J]. Journal of Environmental Sciences, 2010, 22(10): 1508-1512. doi: 10.1016/S1001-0742(09)60281-3 [12] KRAUSS M, LONGRÉE P, DORUSCH F, et al. Occurrence and removal of N-nitrosamines in wastewater treatment plants[J]. Water Research, 2009, 43(17): 4381-4391. doi: 10.1016/j.watres.2009.06.048 [13] HECHT S S. Approaches to cancer prevention based on an understanding of N-nitrosamine carcinogenesis[J]. Proceedings of the Society for Experimental Biology and Medicine, 1997, 216(2): 181-191. doi: 10.3181/00379727-216-44168 [14] WATSON K, SHAW G, LEUSCH F D L, et al. Chlorine disinfection by-products in wastewater effluent: Bioassay-based assessment of toxicological impact[J]. Water Research, 2012, 46(18): 6069-6083. doi: 10.1016/j.watres.2012.08.026 [15] RICHARDSON S D, PLEWA M J, WAGNER E D, et al. Occurrence, genotoxicity, and carcinogenicity of regulated and emerging disinfection by-products in drinking water: A review and roadmap for research[J]. Mutation Research/Reviews in Mutation Research, 2007, 636(1/2/3): 178-242. [16] BEI E, SHU Y Y, LI S X, et al. Occurrence of nitrosamines and their precursors in drinking water systems around mainland China[J]. Water Research, 2016, 98: 168-175. doi: 10.1016/j.watres.2016.04.013 [17] BARRETT S, HWANG C, CARRIE GUO Y, et al. Occurrence of NDMA in drinking water: a North American survey, 2001-2002[C]. 2003 AWWA Annual Conference. Denver: 2003. [18] CHARROIS J W A, BOYD J M, FROESE K L, et al. Occurrence of N-nitrosamines in Alberta public drinking-water distribution systems[J]. Journal of Environmental Engineering and Science, 2007, 6(1): 103-114. doi: 10.1139/s06-031 [19] DE CAROLI VIZIOLI B, HANTAO L W, MONTAGNER C C. Drinking water nitrosamines in a large metropolitan region in Brazil[J]. Environmental Science and Pollution Research, 2021, 28(25): 32823-32830. doi: 10.1007/s11356-021-12998-4 [20] POZZI R, BOCCHINI P, PINELLI F, et al. Determination of nitrosamines in water by gas chromatography/chemical ionization/selective ion trapping mass spectrometry[J]. Journal of Chromatography A, 2011, 1218(14): 1808-1814. doi: 10.1016/j.chroma.2011.02.009 [21] TEMPLETON M R, CHEN Z. NDMA and seven other nitrosamines in selected UK drinking water supply systems[J]. Journal of Water Supply:Research and Technology-Aqua, 2010, 59(4): 277-283. doi: 10.2166/aqua.2010.077 [22] JURADO SÁNCHEZ B, BALLESTEROS E, GALLEGO M. Occurrence of aromatic amines and N-nitrosamines in the different steps of a drinking water treatment plant[J]. Water Research, 2012, 46(14): 4543-4555. doi: 10.1016/j.watres.2012.05.039 [23] ASAMI M, OYA M, KOSAKA K. A nationwide survey of NDMA in raw and drinking water in Japan[J]. Science of the Total Environment, 2009, 407(11): 3540-3545. doi: 10.1016/j.scitotenv.2009.02.014 [24] HASHEMI S, PARK J H, YANG M, et al. Long-term monitoring and risk assessment of N-nitrosamines in the finished water of drinking water treatment plants in South Korea[J]. Environmental Science and Pollution Research, 2022, 29(3): 3930-3943. doi: 10.1007/s11356-021-15814-1 [25] CHEN Z Y, YANG L, HUANG Y, et al. Carcinogenic risk of N-nitrosamines in Shanghai drinking water: Indications for the use of ozone pretreatment[J]. Environmental Science & Technology, 2019, 53(12): 7007-7018. [26] ZHAO C, LU Q, GU Y, et al. Distribution of N-nitrosamines in drinking water and human urinary excretions in high incidence area of esophageal cancer in Huai'an, China[J]. Chemosphere, 2019, 235: 288-296. doi: 10.1016/j.chemosphere.2019.06.124 [27] MAQBOOL T, ZHANG J X, LI Q Y, et al. Occurrence and fate of N-nitrosamines in three full-scale drinking water treatment systems with different treatment trains[J]. Science of the Total Environment, 2021, 783: 146982. doi: 10.1016/j.scitotenv.2021.146982 [28] FAN C C, LIN T F. N-nitrosamines in drinking water and beer: Detection and risk assessment[J]. Chemosphere, 2018, 200: 48-56. doi: 10.1016/j.chemosphere.2018.02.025 [29] LUO Q, BEI E, LIU C, et al. Spatial, temporal variability and carcinogenic health risk assessment of nitrosamines in a drinking water system in China[J]. Science of the Total Environment, 2020, 736: 139695. doi: 10.1016/j.scitotenv.2020.139695 [30] 赵仑山, 岑况, 刘秀丽, 等. 珠江三角洲含N-亚硝胺地下水与地区性癌症[J]. 地学前缘, 2019, 26(2): 335-349. doi: 10.13745/j.esf.sf.2019.1.19 ZHAO L S, CEN K, LIU X L, et al. N-nitrosamine containing underground waters and regional cancer incidence in the Pearl River Delta region[J]. Earth Science Frontiers, 2019, 26(2): 335-349 (in Chinese). doi: 10.13745/j.esf.sf.2019.1.19
[31] WHO. N-nitrosodimethylamine in drinking-water: background document for development of WHO guidelines for drinking-water quality[R]. Geneva: WHO, 2008. [32] KADMI Y, FAVIER L, WOLBERT D. N-nitrosamines, emerging disinfection by-products of health concern: An overview of occurrence, mechanisms of formation, control and analysis in water[J]. Water Supply, 2015, 15(1): 11-25. doi: 10.2166/ws.2014.095 [33] JURADO-SÁNCHEZ B, BALLESTEROS E, GALLEGO M. Screening of N-nitrosamines in tap and swimming pool waters using fast gas chromatography[J]. Journal of Separation Science, 2010, 33(4/5): 610-616. [34] HEALTH CANADA. N-nitrosodimethylamine NDMA in drinking water[R]. Ottawa, Ontario, Canada: Federal Provincial Territorial Committee on Drinking Water, Health Canada, 2010. [35] ONTARIO MINISTRY OF THE ENVIRONMENT. Technical Support Document for Ontario Drinking Water Standards, Objectives And Guidelines[R]. Ontario, Canada: Ontario Ministry of the Environment, 2003. [36] CALIFORNIA DEPARTMENT OF PUBLIC HEALTH. Public Health Goal for N-nitrosodimethylamine in Drinking Water[R]. California, U S: California Department of Public Health, 2006. [37] LI X, BEI E, QIU Y, et al. Intake of volatile nitrosamines by Chinese residents in different provinces via food and drinking water[J]. Science of the Total Environment, 2021, 754: 142121. doi: 10.1016/j.scitotenv.2020.142121 [38] CHEN Y J, CHEN W W, HUANG H F, et al. Occurrence of N-nitrosamines and their precursors in the middle and lower reaches of Yangtze River water[J]. Environmental Research, 2021, 195: 110673. doi: 10.1016/j.envres.2020.110673 [39] ZHOU Q L, McCRAVEN S, GARCIA J, et al. Field evidence of biodegradation of N-nitrosodimethylamine (NDMA) in groundwater with incidental and active recycled water recharge[J]. Water Research, 2009, 43(3): 793-805. doi: 10.1016/j.watres.2008.11.011 [40] PRESCOTT M, KRASNER S W, GUO Y C. Estimation of NDMA precursor loading in source water via artificial sweetener monitoring[J]. Journal - American Water Works Association, 2017, 109: E243-E251. [41] SCHREIBER I M, MITCH W A. Occurrence and fate of nitrosamines and nitrosamine precursors in wastewater-impacted surface waters using boron as a conservative tracer[J]. Environmental Science & Technology, 2006, 40(10): 3203-3210. [42] WANG X Z, LIU Z M, WANG C, et al. Occurrence and formation potential of nitrosamines in river water and ground water along the Songhua River, China[J]. Journal of Environmental Sciences, 2016, 50: 65-71. doi: 10.1016/j.jes.2016.05.021 [43] VAN HUY N, MURAKAMI M, SAKAI H, et al. Occurrence and formation potential of N-nitrosodimethylamine in ground water and river water in Tokyo[J]. Water Research, 2011, 45(11): 3369-3377. doi: 10.1016/j.watres.2011.03.053 [44] KIM G A, SON H J, KIM C W, et al. Nitrosamine occurrence at Korean surface water using an analytical method based on GC/LRMS[J]. Environmental Monitoring and Assessment, 2013, 185(2): 1657-1669. doi: 10.1007/s10661-012-2658-1 [45] LEE J H, OH J E. A comprehensive survey on the occurrence and fate of nitrosamines in sewage treatment plants and water environment[J]. Science of the Total Environment, 2016, 556: 330-337. doi: 10.1016/j.scitotenv.2016.02.090 [46] DHS. California Department of Health Services; NDMA in California Drinking Water[R]. California U S: DHS, 2002. [47] MA F J, WAN Y, YUAN G X, et al. Occurrence and source of nitrosamines and secondary amines in groundwater and its adjacent Jialu River Basin, China[J]. Environmental Science & Technology, 2012, 46(6): 3236-3243. [48] CHEN W W, CHEN Y J, HUANG H F, et al. Occurrence of N-nitrosamines in the Pearl River Delta of China: Characterization and evaluation of different sources[J]. Water Research, 2019, 164: 114896. doi: 10.1016/j.watres.2019.114896 [49] WANG C K, LIU S M, WANG J, et al. Monthly survey of N-nitrosamine yield in a conventional water treatment plant in North China[J]. Journal of Environmental Sciences, 2015, 38: 142-149. doi: 10.1016/j.jes.2015.05.025 [50] CHEN W H, WANG C Y, HUANG T H. Formation and fates of nitrosamines and their formation potentials from a surface water source to drinking water treatment plants in Southern Taiwan[J]. Chemosphere, 2016, 161: 546-554. doi: 10.1016/j.chemosphere.2016.07.027 [51] YOON W H, LEE J H, LEE H J, et al. Investigation of N-nitrosamines using GC-MS/MS in Han-river water supply systems[J]. Journal of Korean Society on Water Environment, 2016, 32(5): 410-418. doi: 10.15681/KSWE.2016.32.5.410 [52] MITCH W A, SHARP J O, TRUSSELL R R, et al. N-nitrosodimethylamine (NDMA) as a drinking water contaminant: A review[J]. Environmental Engineering Science, 2003, 20(5): 389-404. doi: 10.1089/109287503768335896 [53] KRASNER S W, WESTERHOFF P, CHEN B Y, et al. Occurrence of disinfection byproducts in United States wastewater treatment plant effluents[J]. Environmental Science & Technology, 2009, 43(21): 8320-8325. [54] SEDLAK D L, DEEB R A, HAWLEY E L, et al. Sources and fate of nitrosodimethylamine and its precursors in municipal wastewater treatment plants[J]. Water Environment Research:a Research Publication of the Water Environment Federation, 2005, 77(1): 32-39. doi: 10.2175/106143005X41591 [55] ZENG T, MITCH W A. Contribution of N-nitrosamines and their precursors to domestic sewage by greywaters and blackwaters[J]. Environmental Science & Technology, 2015, 49(22): 13158-13167. [56] DISTRICT O C S. Sources of nitrosodimethylamine in the Orange County Sanitation District Service Area[J]. Report. Source Control Division, Orange County Sanitation District, California, 2002. [57] AYDIN E, YAMAN F B, ATES GENCELI E, et al. Occurrence of THM and NDMA precursors in a watershed: Effect of seasons and anthropogenic pollution[J]. Journal of Hazardous Materials, 2012, 221/222: 86-91. doi: 10.1016/j.jhazmat.2012.04.012 [58] FARRÉ M J, JAÉN-GIL A, HAWKES J, et al. Orbitrap molecular fingerprint of dissolved organic matter in natural waters and its relationship with NDMA formation potential[J]. The Science of the Total Environment, 2019, 670: 1019-1027. doi: 10.1016/j.scitotenv.2019.03.280 [59] ANDRZEJEWSKI P, KASPRZYK-HORDERN B, NAWROCKI J. N-nitrosodimethylamine (NDMA) formation during ozonation of dimethylamine-containing waters[J]. Water Research, 2008, 42(4/5): 863-870. [60] LEE C H, YOON J. UV-a induced photochemical formation of N-nitrosodimethylamine (NDMA) in the presence of nitrite and dimethylamine[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2007, 189(1): 128-134. doi: 10.1016/j.jphotochem.2007.01.022 [61] MIKHAYLENKO V M, SHEVCHENKO T F, GLAVIN A A. Influence of N-nitrosamines on the development of phytoplankton[J]. Hydrobiological Journal, 2002, 38(3): 9. [62] CHOI J, VALENTINE R L. N-nitrosodimethylamine formation by free-chlorine-enhanced nitrosation of dimethylamine[J]. Environmental Science & Technology, 2003, 37(21): 4871-4876. [63] MOISEENKO T I. Evolution of biogeochemical cycles under anthropogenic loads: Limits impacts[J]. Geochemistry International, 2017, 55(10): 841-860. doi: 10.1134/S0016702917100081 [64] CHOI J, VALENTINE R L. Formation of N-nitrosodimethylamine (NDMA) from reaction of monochloramine: A new disinfection by-product[J]. Water Research, 2002, 36(4): 817-824. doi: 10.1016/S0043-1354(01)00303-7 [65] MITCH W A, GERECKE A C, SEDLAK D L. A N-nitrosodimethylamine (NDMA) precursor analysis for chlorination of water and wastewater[J]. Water Research, 2003, 37(15): 3733-3741. doi: 10.1016/S0043-1354(03)00289-6 [66] DAI N, MITCH W A. Relative importance of N-nitrosodimethylamine compared to total N-nitrosamines in drinking waters[J]. Environmental Science & Technology, 2013, 47(8): 3648-3656. [67] KRISTIANA I, LIEW D, HENDERSON R K, et al. Formation and control of nitrogenous DBPs from Western Australian source waters: Investigating the impacts of high nitrogen and bromide concentrations[J]. Journal of Environmental Sciences, 2017, 58: 102-115. doi: 10.1016/j.jes.2017.06.028 [68] KITIS M, KILDUFF J E, KARANFIL T. Isolation of dissolved organic matter (DOM) from surface waters using reverse osmosis and its impact on the reactivity of DOM to formation and speciation of disinfection by-products[J]. Water Research, 2001, 35(9): 2225-2234. doi: 10.1016/S0043-1354(00)00509-1 [69] IKE I A, KARANFIL T, CHO J, et al. Oxidation byproducts from the degradation of dissolved organic matter by advanced oxidation processes–A critical review[J]. Water Research, 2019, 164: 114929. doi: 10.1016/j.watres.2019.114929 [70] GAN W H, HUANG S R, GE Y X, et al. Chlorite formation during ClO2 oxidation of model compounds having various functional groups and humic substances[J]. Water Research, 2019, 159: 348-357. doi: 10.1016/j.watres.2019.05.020 [71] YANG L Y, HAN D H, LEE B M, et al. Characterizing treated wastewaters of different industries using clustered fluorescence EEM–PARAFAC and FT-IR spectroscopy: Implications for downstream impact and source identification[J]. Chemosphere, 2015, 127: 222-228. doi: 10.1016/j.chemosphere.2015.02.028 [72] WANG C K, ZHANG X J, WANG J, et al. Effects of organic fractions on the formation and control of N-nitrosamine precursors during conventional drinking water treatment processes[J]. Science of the Total Environment, 2013, 449: 295-301. doi: 10.1016/j.scitotenv.2013.01.080 [73] WANG C K, ZHANG X J, CHEN C, et al. Factors controlling N-nitrosodimethylamine (NDMA) formation from dissolved organic matter[J]. Frontiers of Environmental Science & Engineering, 2013, 7(2): 151-157. [74] FARRÉ M J, INSA S, LAMB A, et al. Occurrence of N-nitrosamines and their precursors in Spanish drinking water treatment plants and distribution systems[J]. Environmental Science:Water Research & Technology, 2020, 6(1): 210-220. [75] D'ANDRILLI J, COOPER W T, FOREMAN C M, et al. An ultrahigh-resolution mass spectrometry index to estimate natural organic matter lability[J]. Rapid Communications in Mass Spectrometry:RCM, 2015, 29(24): 2385-2401. doi: 10.1002/rcm.7400 [76] RADJENOVIC J, FARRÉ M J, GERNJAK W. Effect of UV and UV/H2O2 in the presence of chloramines on NDMA formation potential of tramadol[J]. Environmental Science & Technology, 2012, 46(15): 8356-8364. [77] KEMPER J M, WALSE S S, MITCH W A. Quaternary amines as nitrosamine precursors: A role for consumer products?[J]. Environmental Science & Technology, 2010, 44(4): 1224-1231. [78] PADHYE L, LUZINOVA Y, CHO M, et al. PolyDADMAC and dimethylamine as precursors of N-nitrosodimethylamine during ozonation: Reaction kinetics and mechanisms[J]. Environmental Science & Technology, 2011, 45(10): 4353-4359. [79] MITCH W A, SEDLAK D L. Formation of N-nitrosodimethylamine (NDMA) from dimethylamine during chlorination[J]. Environmental Science & Technology, 2002, 36(4): 588-595. [80] FIDDLER W, PENSABENE J W, DOERR R C, et al. Formation of N-nitrosodimethylamine from naturally occurring quaternary ammonium compounds and tertiary amines[J]. Nature, 1972, 236(5345): 307. [81] MITCH W A, SCHREIBER I M. Degradation of tertiary alkylamines during chlorination/chloramination: Implications for formation of aldehydes, nitriles, halonitroalkanes, and nitrosamines[J]. Environmental Science & Technology, 2008, 42(13): 4811-4817. [82] MITCH W A, SEDLAK D L. Characterization and fate of N-nitrosodimethylamine precursors in municipal wastewater treatment plants[J]. Environmental Science & Technology, 2004, 38(5): 1445-1454. [83] PARK S H, PIYACHATURAWAT P, TAYLOR A E, et al. Potential N-nitrosodimethylamine (NDMA) formation from amine-based water treatment polymers in the reactions with chlorine-based oxidants and nitrosifying agents[J]. Water Supply, 2009, 9(3): 279-288. doi: 10.2166/ws.2009.452 [84] PIYACHATURAWAT P. Potential N-nitrosodimethylamine (NDMA) formation from water treatment polymers[D]. Georgia Institute of Technology, 2005. [85] PARK S H, WEI S T, MIZAIKOFF B, et al. Degradation of amine-based water treatment polymers during chloramination as N-nitrosodimethylamine (NDMA) precursors[J]. Environmental Science & Technology, 2009, 43(5): 1360-1366. [86] ZENG T, LI R J, MITCH W A. Structural modifications to quaternary ammonium polymer coagulants to inhibit N-nitrosamine formation[J]. Environmental Science & Technology, 2016, 50(9): 4778-4787. [87] KRASNER S W, MITCH W A, MCCURRY D L, et al. Formation, precursors, control, and occurrence of nitrosamines in drinking water: A review[J]. Water Research, 2013, 47(13): 4433-4450. doi: 10.1016/j.watres.2013.04.050 [88] DING S K, DENG Y, BOND T, et al. Disinfection byproduct formation during drinking water treatment and distribution: A review of unintended effects of engineering agents and materials[J]. Water Research, 2019, 160: 313-329. doi: 10.1016/j.watres.2019.05.024 [89] KUMAR R, SARMAH A K, PADHYE L P. Fate of pharmaceuticals and personal care products in a wastewater treatment plant with parallel secondary wastewater treatment train[J]. Journal of Environmental Management, 2019, 233: 649-659. [90] WILKINSON J, HOODA P S, BARKER J, et al. Occurrence, fate and transformation of emerging contaminants in water: An overarching review of the field[J]. Environmental Pollution, 2017, 231: 954-970. doi: 10.1016/j.envpol.2017.08.032 [91] CHEN W H, YOUNG T M. Influence of nitrogen source on NDMA formation during chlorination of diuron[J]. Water Research, 2009, 43(12): 3047-3056. doi: 10.1016/j.watres.2009.04.020 [92] JASEMIZAD T, BROMBERG L, HATTON T A, et al. Oxidation of betrixaban to yield N-nitrosodimethylamine by water disinfectants[J]. Water Research, 2020, 186: 116309. doi: 10.1016/j.watres.2020.116309 [93] HANIGAN D, THURMAN E M, FERRER I, et al. Methadone contributes to N-nitrosodimethylamine formation in surface waters and wastewaters during chloramination[J]. Environmental Science & Technology Letters, 2015, 2(6): 151-157. [94] ZHANG A, LI Y M, SONG Y, et al. Characterization of pharmaceuticals and personal care products as N-nitrosodimethylamine precursors during disinfection processes using free chlorine and chlorine dioxide[J]. Journal of Hazardous Materials, 2014, 276: 499-509. doi: 10.1016/j.jhazmat.2014.05.069 [95] PADHYE L P, KIM J H, HUANG C H. Oxidation of dithiocarbamates to yield N-nitrosamines by water disinfection oxidants[J]. Water Research, 2013, 47(2): 725-736. doi: 10.1016/j.watres.2012.10.043 [96] ALABA P A, SANI Y M, OLUPINLA S F, et al. Toward N-nitrosamines free water: Formation, prevention, and removal[J]. Critical Reviews in Environmental Science and Technology, 2017, 47(24): 2448-2489. doi: 10.1080/10643389.2018.1430438 [97] LE ROUX J, GALLARD H, CROUÉ J P. Chloramination of nitrogenous contaminants (pharmaceuticals and pesticides): NDMA and halogenated DBPs formation[J]. Water Research, 2011, 45(10): 3164-3174. doi: 10.1016/j.watres.2011.03.035 [98] SHEN R Q, ANDREWS S A. Demonstration of 20 pharmaceuticals and personal care products (PPCPs) as nitrosamine precursors during chloramine disinfection[J]. Water Research, 2011, 45(2): 944-952. doi: 10.1016/j.watres.2010.09.036 [99] SILLA SANTOS M H. Biogenic amines: Their importance in foods[J]. International Journal of Food Microbiology, 1996, 29(2/3): 213-231. [100] FACCHINI M C, DECESARI S, RINALDI M, et al. Important source of marine secondary organic aerosol from biogenic amines[J]. Environmental Science & Technology, 2008, 42(24): 9116-9121. [101] MÜLLER C, IINUMA Y, KARSTENSEN J, et al. Seasonal variation of aliphatic amines in marine sub-micrometer particles at the Cape Verde Islands[J]. Atmospheric Chemistry and Physics, 2009, 9(24): 9587-9597. doi: 10.5194/acp-9-9587-2009 [102] WANG X C, LEE C. Sources and distribution of aliphatic amines in salt marsh sediment[J]. Organic Geochemistry, 1994, 22(6): 1005-1021. doi: 10.1016/0146-6380(94)90034-5 [103] GARSIN D A. Ethanolamine utilization in bacterial pathogens: Roles and regulation[J]. Nature Reviews Microbiology, 2010, 8(4): 290-295. doi: 10.1038/nrmicro2334 [104] SHIMIZU M, KOZONO M, MURAYAMA N, et al. Bonitos with low content of malodorous trimethylamine as palliative care for self-reported Japanese trimethylaminuria subjects[J]. Drug Metabolism and Pharmacokinetics, 2009, 24(6): 549-552. doi: 10.2133/dmpk.24.549 [105] YU Z, ZHANG Q, KRAUS T E C, et al. Contribution of amino compounds to dissolved organic nitrogen in forest soils[J]. Biogeochemistry, 2002, 61(2): 173-198. doi: 10.1023/A:1020221528515 [106] BUSHAW-NEWTON K L, MA M R. Photochemical formation of biologically available nitrogen from dissolved humic substances in coastal marine systems[J]. Aquatic Microbial Ecology, 1999, 18: 285-292. doi: 10.3354/ame018285 [107] ZENG T, GLOVER C M, MARTI E J, et al. Relative importance of different water categories as sources of N-nitrosamine precursors[J]. Environmental Science & Technology, 2016, 50(24): 13239-13248. [108] VAL DEL RÍO Á, CAMPOS GÓMEZ J L, MOSQUERA CORRAL A. Technologies for the Treatment and Recovery of Nutrients from Industrial Wastewater[M]. IGI Global, 2017. [109] KARADAS F, ATILHAN M, APARICIO S. Review on the use of ionic liquids (ILs) as alternative fluids for CO2Capture and natural gas sweetening[J]. Energy & Fuels, 2010, 24(11): 5817-5828. [110] ALI MAZARI S, ALABA P, SAEED I M. Formation and elimination of nitrosamines and nitramines in freshwaters involved in post-combustion carbon capture process[J]. Journal of Environmental Chemical Engineering, 2019, 7(3): 103111. doi: 10.1016/j.jece.2019.103111 [111] OYA M, KOSAKA K, ASAMI M, et al. Formation of N-nitrosodimethylamine (NDMA) by ozonation of dyes and related compounds[J]. Chemosphere, 2008, 73(11): 1724-1730. doi: 10.1016/j.chemosphere.2008.09.026 [112] KOSAKA K, ASAMI M, KONNO Y, et al. Identification of antiyellowing agents as precursors of N-nitrosodimethylamine production on ozonation from sewage treatment plant influent[J]. Environmental Science & Technology, 2009, 43(14): 5236-5241. [113] CHEN W H, HUANG T H, WANG C Y. Impact of pre-oxidation on nitrosamine formation from a source to drinking water: A perspective on cancer risk assessment[J]. Process Safety and Environmental Protection, 2018, 113: 424-434. doi: 10.1016/j.psep.2017.11.016 [114] MITCH W A, SEDLAK D L. Factors controlling nitrosamine formation during wastewater chlorination[J]. Water Supply, 2002, 2(3): 191-198. doi: 10.2166/ws.2002.0102 [115] KRISTIANA I, TAN J, JOLL C A, et al. Formation of N-nitrosamines from chlorination and chloramination of molecular weight fractions of natural organic matter[J]. Water Research, 2013, 47(2): 535-546. doi: 10.1016/j.watres.2012.10.014 [116] ZHAO Y Y, BOYD J M, WOODBECK M, et al. Formation of N-nitrosamines from eleven disinfection treatments of seven different surface waters[J]. Environmental Science & Technology, 2008, 42(13): 4857-4862. [117] YANG L, CHEN Z L, SHEN J M, et al. Reinvestigation of the nitrosamine-formation mechanism during ozonation[J]. Environmental Science & Technology, 2009, 43(14): 5481-5487. [118] ANDRZEJEWSKI P, KASPRZYK-HORDERN B, NAWROCKI J. The hazard of N-nitrosodimethylamine (NDMA) formation during water disinfection with strong oxidants[J]. Desalination, 2005, 176(1/2/3): 37-45. [119] ANDRZEJEWSKI P, NAWROCKI J. N-nitrosodimethylamine (NDMA) as a product of potassium permanganate reaction with aqueous solutions of dimethylamine (DMA)[J]. Water Research, 2009, 43(5): 1219-1228. doi: 10.1016/j.watres.2008.12.005 [120] SCHREIBER I M, MITCH W A. Nitrosamine formation pathway revisited: The importance of chloramine speciation and dissolved oxygen[J]. Environmental Science & Technology, 2006, 40(19): 6007-6014. [121] SHAH A D, MITCH W A. Halonitroalkanes, halonitriles, haloamides, and N-nitrosamines: A critical review of nitrogenous disinfection byproduct formation pathways[J]. Environmental Science & Technology, 2012, 46(1): 119-131. [122] XU B, QIN C, HU C Y, et al. Degradation kinetics and N-nitrosodimethylamine formation during monochloramination of chlortoluron[J]. Science of the Total Environment, 2012, 417/418: 241-247. doi: 10.1016/j.scitotenv.2011.12.056 [123] SOLTERMANN F, LEE M J, CANONICA S, et al. Enhanced N-nitrosamine formation in pool water by UV irradiation of chlorinated secondary amines in the presence of monochloramine[J]. Water Research, 2013, 47(1): 79-90. doi: 10.1016/j.watres.2012.09.034 [124] U. S. EPA. Risk assessment guidance for Superfund. Volume 1. Human Health Evaluation Manual. Part A. Interim report (Final)[R]. Washington, DC: Office of Emergency and Remedial Response, 1989 [125] U. S. EPA. Risk Assessment Guidance for Superfund: Human Health Evaluation Manual (Part E, Supplemental Guidance for Dermal Risk Assessment)[R]. Washington, DC: Office of Superfund Remediation and Technology Innovation, 2004: Volume 1. [126] U. S. EPA. Risk Assessment Guidance for Superfund: Human Health Evaluation Manual (Part F, Supplemental Guidance for Inhalation Risk Assessment)[R]. Washington, DC: Office of Superfund Remediation and Technology Innovation, 2009: Volume 1. [127] U. S. EPA. Supplementary Guidance for Conducting Health Risk Assessment of Chemical Mixtures. [R]. Washington, DC: Risk Assessment Forum, 2000. [128] YIN Y Y, LI T, KUANG D Y, et al. Probabilistic health risk assessment of nitrosamines in drinking water of Shaoxing, Zhejiang, China[J]. Environmental Science and Pollution Research, 2019, 26(6): 5485-5499. doi: 10.1007/s11356-018-4026-3 [129] U. S. EPA. Monitoring the Occurrence of Unregulated Drinking Water Contaminants[R]. U. S. EPA, 2013. [130] BIENIARZ K, EPLER P, KIME D, et al. Effects of N, N-dimethylnitrosamine (DMNA) on in vitro oocyte maturation and embryonic development of fertilized eggs of carp (Cyprinus carpio L. ) kept in eutrophied ponds[J]. Journal of Applied Toxicology, 1996, 16(2): 153-156. doi: 10.1002/(SICI)1099-1263(199603)16:2<153::AID-JAT323>3.0.CO;2-Z [131] GOODALL C M, KENNEDY T H. Carcinogenicity of dimethylnitramine in NZR rats and NZO mice[J]. Cancer Letters, 1975, 1: 295-298. doi: 10.1016/S0304-3835(75)97975-6 [132] 雷炳莉, 黄圣彪, 王子健. 生态风险评价理论和方法[J]. 化学进展, 2009, 21(增刊1): 350-358. LEI B L, HUANG S B, WANG Z J. Theories and methods of ecological risk assessment[J]. Progress in Chemistry, 2009, 21(Sup 1): 350-358 (in Chinese).
[133] GODOY A A, DOMINGUES I, ARSÉNIA NOGUEIRA A J, et al. Ecotoxicological effects, water quality standards and risk assessment for the anti-diabetic metformin[J]. Environmental Pollution, 2018, 243: 534-542. doi: 10.1016/j.envpol.2018.09.031 [134] AYDIN S, AYDIN M E, ULVI A, et al. Antibiotics in hospital effluents: Occurrence, contribution to urban wastewater, removal in a wastewater treatment plant, and environmental risk assessment[J]. Environmental Science and Pollution Research, 2019, 26(1): 544-558. doi: 10.1007/s11356-018-3563-0 [135] HELA D G, LAMBROPOULOU D A, KONSTANTINOU I K, et al. Environmental monitoring and ecological risk assessment for pesticide contamination and effects in Lake Pamvotis, northwestern Greece[J]. Environmental Toxicology and Chemistry, 2005, 24(6): 1548-1556. doi: 10.1897/04-455R.1 [136] LI Z G, LIU X Y, HUANG Z J, et al. Occurrence and ecological risk assessment of disinfection byproducts from chlorination of wastewater effluents in East China[J]. Water Research, 2019, 157: 247-257. doi: 10.1016/j.watres.2019.03.072 -



 下载:
下载: