-
页岩气是一种比传统化石燃料更清洁的非常规天然气,其开发利用可缓解天然气的供需矛盾,提高国家能源安全,促进能源战略转型[1]. 中国拥有丰富的页岩气资源,储量大约32万亿 m3[2],随着自主开发技术的发展,中国已成为世界上第三个页岩气开发商业化的国家[3],然而快速发展的页岩气开采行业引起了人们对其潜在环境影响的忧虑[4]. 国内外对页岩气开采环境风险的研究主要集中在压裂返排液的潜在影响,发现压裂返排液可能对周边水环境产生不利影响,也可能污染周边农田,影响农作物生长[5 − 14]. 中国超过65%的页岩气资源埋藏深度大于
3500 m,地层环境复杂,为降低开采事故发生率,降低开采成本,在压裂液外,也广泛使用高稳定性、耐高温性、润滑性的油基钻井液[15 − 17]. 油基钻井液含高浓度的烷烃、多环芳烃(polycyclic aromatic hydrocarbons, PAHs)、重金属等[18 − 20],可能泄露进入周边土壤环境,王兵等[21]指出页岩气开采场地中石油烃污染最严重的土壤往往在钻井液堆放区附近,但是相关土壤毒性数据目前相当匮乏. 弹尾目生物跳虫是一种小型节肢动物,分布广泛,是陆地生态系统中最丰富的无脊椎动物,在土壤生态功能中发挥着至关重要的作用. 跳虫以土壤微生物为食物,是最早接触土壤污染物的生物之一,因此常用作土壤污染的预警[22]. 剖析油基钻井液污染土壤对跳虫的不良效应,有助于评估页岩气开采对周边土壤生态系统的潜在威胁.土壤中污染物的生物有效性是其风险的决定因素之一[23]. 污染物在土壤中主要以结合态、可解吸态和游离态的形式存在,而只有可解吸态及游离态才可被生物所吸收利用并产生效应,研究发现仅少部分PAHs(0.7%—41.2%)能真正能被生物所用,ISO-
17402 -2008[24]明确指出生物效应与土壤中污染物的总浓度无关,而应考虑生物有效性,即污染物到达生物体或靶标器官的净通量[25]. 影响生物有效性的因素众多,老化是一个重要原因,即污染物和土壤成分间的相互作用随时间推移而变化,通常污染物与土壤接触时间越长,污染物生物有效性会降低. 虽然生物测试能清楚直观获取土壤生物效应信息,但实验耗时耗力,成本高且重现性较差,难以广泛运用,而且单纯生物测试无法提供关键致毒物信息[26]. 因此,有必要结合生物测试和化学分析,评估土壤中主要污染物的生物有效性,明晰老化作用对毒性的影响,提高环境风险评估的准确性[27].为预测油基钻井液意外泄露对周边土壤的长期潜在风险,本研究分析了270 d期间油基钻井液污染土壤对跳虫的毒性变化规律,并结合耗竭式和Tenax萃取探明了主要污染物的生物有效性的变化趋势,揭示了其与毒性的关联.
-
标准品与试剂:目标物包括了16种PAHs以及碳数从10到33的23种正构烷烃;回收率指示物包括了萘-d8、苊-d10、菲-d10、䓛-d12和苝-d12;内标包括2-氟-1,1'-联苯、对三联苯-d14和二苯并[a,h]蒽-d14,以上药品纯度均为99%,购自AccuStandard(康涅狄格州,美国). 乙腈、二氯甲烷、正己烷均为HPLC级,购自上海安谱公司,而分析纯的丙酮购自广州化学试剂厂,重蒸后使用. Tenax树脂(60—80目)购自Scientific Instrument Services(美国纽泽西州),实验前,将Tenax用丙酮/正己烷溶液(1:1, V/V)超声清洗3次,常温下风干备用. 石英砂(分析纯、60—80目)和高岭土(填料级)购自上海阿拉丁公司,泥炭土(粒径<10 mm)购自丹麦PINDSTRIP,使用前风干并过2 mm筛网,碳酸钙(分析纯)自广东台山粤侨试剂塑料有限公司.
主要仪器:气相色谱-质谱联用仪(QP2010-GC-MS,Shimadzu公司,日本),色谱柱为SH-Rxi-5Sil MS (30 m × 0.25 mm, 0.25 μm 膜厚)、气相色谱-质谱/质谱联用仪(TQ8040-GC-MS/MS,Shimadzu公司,日本)、快速溶剂萃取仪(ASE-350,Thermo Fisher公司,美国),快速组织细胞破碎仪(TissuePre TP-24,Bio-xplorer 公司,中国)、Sorvall Legend Micro 17R离心机(Thermo Fisher公司,美国)、Alpha 1-2 LD-plus冷冻干燥机(Christ公司,德国).
-
实验所用油基钻井液采自四川武隆某页岩气开采场地. 实验所用土壤为人工配置的干净土壤,将质量分数分别为70%、19.3%、10%的石英砂、高岭土、泥炭土充分混匀后加入0.7%碳酸钙将pH调节至6.0 ± 0.5,密封室温保存,具体配制方法参考ISO-
11267 [28].为明晰油基钻井液泄露对周边土壤的影响,参考前期文献[21]报道页岩气场地土壤中污染物浓度范围,称取人工土壤
2520 g以及480 g页岩气场地油基钻井液,将其加入到1 L的大玻璃瓶中,封盖后不断滚动搅拌48 h,使土壤充分混合均匀,最终配制成含16%质量分数的油基钻井液的污染土壤. 为考察老化作用对土壤毒性的影响,将污染土壤室温下避光保存,并分别在0、15、30、90、150、270 d 混匀后取样进行生物测试和化学分析. -
在预定时间点,采集污染土壤样品,用干净土壤稀释为不同浓度(0.125%、0.25%、0.5%、1%、2%、4%、8%、16%),充分混合后,按照ISO-
11267 -2014方法开展跳虫急性毒性测试,每个浓度处理组设置 4 个平行样,每次测试均含1组空白对照[28].测试生物为白符跳虫(Folsomia candida),为降低跳虫个体大小、成长状态差异引起的实验误差,跳虫需经同龄化处理. 实验前将50—60只成虫移入新的培养基质中,当有新幼虫出现后,移走成虫,第3天将幼虫移入新的培养基继续培养9 d,以获得处于9—12 日龄的生物用于测试[28]. 测试在装有30 g土壤的100 mL烧杯中进行,在土壤中添加适量纯水,充分混匀,以达到最大持水量的55%. 每个烧杯中加入10 只适龄跳虫,用封口膜封口,放入生物培养箱,保持温度为(20 ± 1)℃,光照与黑暗循环为16:8 h. 在96 h的生物测试期间内,不喂食,不另外补充水分. 测试结束后,采用水浮法计量成虫存活数量,并收集存活跳虫于1.5 mL离心管中,冷冻干燥后置于- 80 ℃保存.
-
加速溶剂萃取仪用于提取土壤中污染物总量,属于耗竭式萃取,其具有萃取效率高,方法简便,是目前固体环境样品分析的主流前处理方法之一[29]. 将冷冻干燥的土壤样品与硅藻土混合均匀后装入 ASE 萃取池中,加入25 ng的回收率指示物,上机萃取. 萃取溶剂为正己烷/二氯甲烷/丙酮(2:2:1,V/V) ,温度 100 ℃, 压力
1500 psi,静态提取 5 min,循环 2 次. 萃取液通过氮吹浓缩并溶剂置换至 2 mL 正己烷中,转移至硅胶氧化铝层析柱进行净化. 层析柱从下至上分别为6 cm氧化铝、12 cm硅胶和2 cm无水硫酸钠,洗脱液为70 mL正己烷和二氯甲烷的混合溶液(7:3,V/V). 洗脱液收集后,氮吹浓缩并置换溶剂为正己烷,加入25 ng的内标,定容至0.5 mL,以备仪器分析. -
土壤中烷烃和PAHs的生物有效性通过Tenax仿生萃取测定[30]. 称取0.2 g 不同老化时间下冻干的污染土样、0.05 g Tenax树脂、13 mL纯水加入玻璃离心管中,盖上螺旋盖后在试管旋转器上充分振荡. 24 h后离心分离,收集 Tenax 树脂,加入5 mL丙酮超声 5 min,移出萃取液,再加入5 mL正己烷和丙酮溶液(1:1,V/V) 超声 5 min ,提取3 次后将提取液合并浓缩,利用硅胶氧化铝层析柱净化.
-
跳虫生物样品中的有机污染物使用乙腈进行超声萃取,冷冻离心净化除脂,具体流程如下. 首先,在装有跳虫的离心管中加入5 颗不锈钢珠、0.5 mL乙腈、回收率指示物后,使用快速组织细胞破碎仪将生物破碎均浆,功率设置为中速,运行时间2 min,30 s间歇. 结束后,将样品超声10 min,功率100 W. 然后,4 ℃下冷冻离心5 min,转速
9000 r·min−1 ,上清液转移至新的离心管. 重复破碎、超声和离心3次后,萃取液合并,-20℃冷冻12 h,再在4 ℃和9000 r·min−1下离心5 min,将上清液置换溶剂为正己烷,过无水硫酸钠,加入25 ng内标定容至100 μL. -
萃取液中PAHs通过GC-MS分析,色谱柱为SH-Rxi-5Sil MS (30 m × 0.25 mm, 0.25 μm 膜厚),载气为He,柱流速为 1.0 mL·min−1. 1 μL样品通过不分流模式进样,进样口温度为260 ℃. 初始柱温为80 ℃,以20 ℃·min−1的速率升到250 ℃,保持2 min,再以 10 ℃·min−1速率升至300 ℃,保持9.5 min. 传输线、离子源和四极杆温度分别为250、230、150 ℃. 质谱检测采用电子轰击电离源与选择性离子检测模式,内标法定量,标准曲线范围为1—200 ng·mL−1.
萃取液中的正构烷烃在GC-MS/MS上分析,色谱柱同上,载气为He,流速为 1.2 mL·min−1. 采用不分流模式进样,进样口温度为250 ℃,进样体积为1 μL. 柱温程序如下:初始温度为80 ℃,以20 ℃·min−1的速率升到180 ℃,再以 5 ℃·min−1速率升至300 ℃,保持5 min. 传输线、离子源和四极杆温度分别为250、230、150 ℃. 离子源及监测模式为EI与Q3 SIM模式,标准曲线定量范围为10—500 ng·mL−1.
土壤和跳虫中污染物浓度分别用干重和湿重表示. 为保证化学分析的可靠性,分析实际样品同时也包含了一系列质控样品. 在仪器分析过程中,每进10个样品,间插1个标准样以检查仪器稳定性,这些检查样间的相对标准偏差均小于20%. 每10个样品同时分析1个溶剂空白、1个基质空白(干净土壤或未暴露的跳虫)、2个加标样品(加入25 ng的目标物). 此外,所有样品在萃取前均加入25 ng回收率指示物,以确保样品前处理过程合格. 对于土壤样品,萘的回收率相对较低(33%—45%),其他PAHs回收率为76%—130%,相对标准偏差在8%—17%之间;跳虫样品中所有PAHs的回收率为56%—110% ,相对标准偏差小于 19% . 所有土壤样品的回收率指示物(萘-d8、苊-d10、菲-d10、䓛-d12和苝-d12)的回收率分别为46%±3%、130%±30%、65%±8%、108%±16%以及76%±9%,而在跳虫样品中回收率指示物(萘-d8、苊-d10、菲-d10、䓛-d12和苝-d12)的回收率分别为36%±8%、107%±12%、136%±23%、60%±10%以及118%±18%.
为定量表征老化对生物有效性变化的影响,生物有效性(bioavailability, %)以Tenax和ASE萃取的PAHs的比值表示(公式1)[31].
式中,Total PAHs为土壤耗竭性萃取的PAHs总浓度,mg·kg−1;Tenax PAHs为土壤仿生萃取的PAHs总浓度,mg·kg−1;
土壤污染物的生物有效性随老化时间的变化趋势则通过一级动力学模型进行拟合(公式2).
式中,k为速率常数,d−1;t为土壤老化时间,d;A+b是初始状态下土壤污染物的生物有效性;b是达到稳态后土壤污染物的估计生物有效性.
-
油气开采行业,开采、加工、运输等环节,往往会伴随石油污染物泄漏、排放发生,多环芳烃、烷烃是石油污染物的重要组成,常会导致周边PAHs污染[32],如在页岩气水力压裂返排液[33]、钻屑残渣等[18]均检出大量PAHs,潜在威胁周边土壤环境. 中国某油气田开发所产生的含油污泥中PAHs高达107—314 mg·kg-1[34],而受人工制气厂污染的土壤中PAHs总量严重者甚至可达近十万mg·kg-1[35]. 本研究中,质量分数为16%油基钻井液的污染土壤中16种PAHs测定浓度为38.3 mg·kg−1,主要以二、三环形式存在,这与其他油气田含油污泥相似[34].
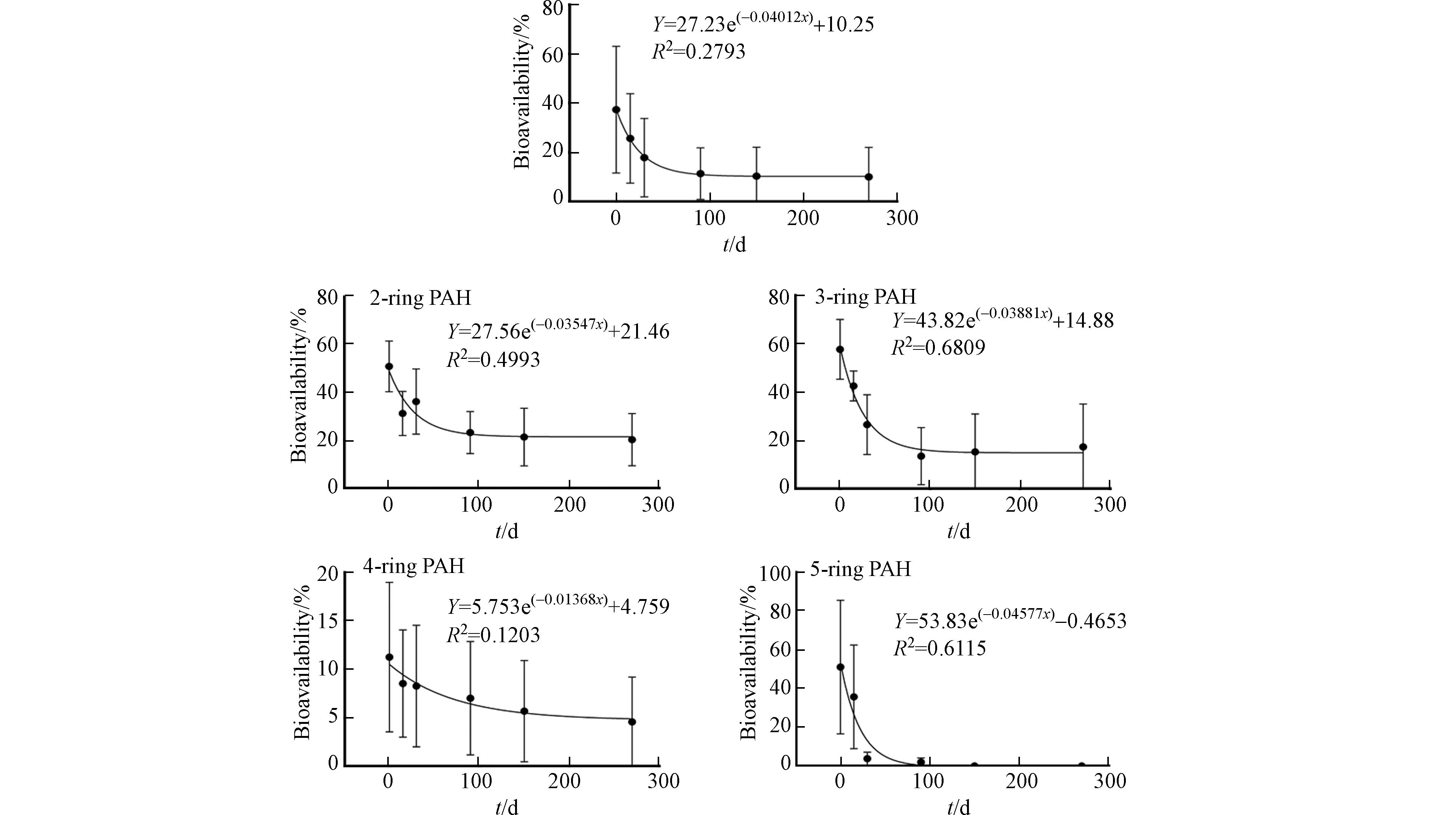
为明晰老化对页岩气钻井液污染的土壤中PAHs总浓度及生物有效性的影响,同时采用ASE耗竭式萃取和Tenax仿生萃取两种模式分析了土壤中PAHs在老化0、15、30、90、150、270 d 后的变化情况,结果如图1所示. 耗竭式萃取测定的土壤中PAHs总浓度虽然在第15 天与实验开始时接近,但随老化时间进一步延长,30 d后其总浓度逐步下降,但是不同时间点土壤中不同环数PAHs的浓度比一直基本维持在一个稳定范围. 对于Tenax萃取而言,在0 d时,土壤中PAHs的生物有效浓度尚未达到耗竭式萃取测定的总浓度的三分之一,随老化时间的增加,PAHs的生物有效浓度迅速下降,但是与耗竭式萃取结果不同的是,高环(四环以上)化合物在生物有效PAHs中的相对占比,随老化时间延长逐步减小.
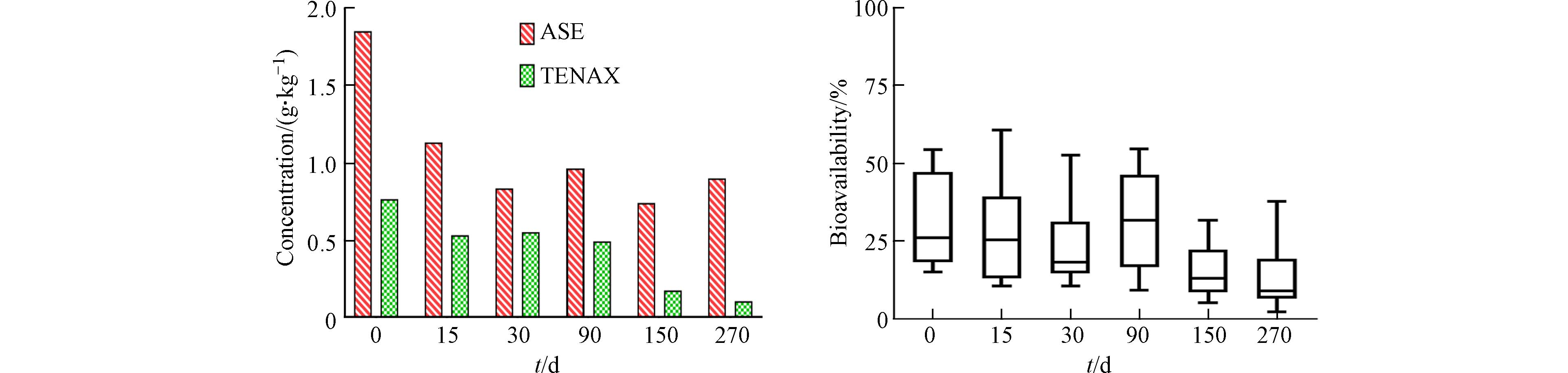
如图2所示,在270 d的老化过程中,不仅油基钻井液污染土壤中PAHs浓度随时间降低,而且其生物有效性(浓度比)呈现前30 天先迅速下降,然后逐步趋于平缓的趋势,这与Chen等的报道相符[36],即随着污染物和土壤接触时间的推移,污染物的生物有效性降低.
本研究用一级动力学模型模拟了生物有效性变化趋势,发现除了四环PAHs曲线拟合的r 2较低(0.12),二、三和五环PAHs的拟合程度均较好,r 2分别为0.50、0.68和0.61,而总PAHs的拟合r 2为0.28. 此外,不同环数PAHs的生物有效性变化速率也存在显著差异,二环、三环、四环和五环的PAHs的生物有效性从初始的40%、45%、11%和56%逐步下降,第270 天为16%、30%、4%和趋于0. Chen等[36]指出,在有机碳含量较高的土壤中,随时间增加,高疏水性有机物与土壤的有机成分结合更为紧密,且大分子量化合物更易被束缚在土壤孔隙或腐殖质中,从而导致其生物有效性显著下降. 我们的结果也显示污染土壤中疏水性更强的高环PAHs生物有效性比低环化合物更低,且随老化时间延长更快下降,甚至后期难以被生物所利用.
-
王兵等[21]发现页岩气开采场地内,受污染土壤中石油烃类污染物主要以正构烷烃的形式存在,正构烷烃一般可占到总石油烃含量的60%—70%,在某些受严重污染的土壤中正构烷烃的浓度高达0.99—3.08 g·kg−1,同时,他们还发现整个开采场地中石油烃污染最严重的土壤主要位于钻井液堆放区附近. 故此,本研究特别考虑了页岩气钻井液的泄露对土壤污染的影响,所配制的质量分数为16%油基钻井液污染的土壤中正构烷烃的含量测定为1.85 g·kg−1,该浓度水平和实际污染土壤接近,可较好代表真实环境情况.
图3显示了在不同老化时间下,通过ASE和Tenax萃取测定的土壤中正构烷烃的浓度及生物有效性. 油基钻井液混入土壤后,其中正构烷烃相对快速被降解,在 15 d后只余下实验初始的60%左右,而该浓度直到270 d均维持在相对稳定的水平. Chen等[20]测定了页岩气钻井液在土壤环境中第63 天的降解情况,发现其中石油烃的降解率在47.22%—57.64%,并指出降解主要与假单胞菌有关. 本研究中,页岩气油基钻井液烷烃的降解率在15 d到270 d平均为57.6%,其结果与Chen等研究结果相近[20],显示微生物降解是导致污染土壤中石油烃类物质总浓度下降的主要原因. 此外,和PAHs情况类似,正构烷烃的生物有效性基本低于50%,且随时间延长而逐步降低. 虽然在15—270 d老化时间范围内,土壤中烷烃总浓度基本不变,但其生物有效性在150 d后显著降低.
-
为评估页岩气开采场地污染土壤的潜在风险,测定了油基钻井液污染土壤对白符跳虫的毒性. 研究结果显示,油基钻井液污染土壤(质量分数16%,PAHs和正构烷烃的含量分别为38.3 mg·kg−1和1850 mg·kg−1)对白符跳虫具有极高的急性致死毒性,即使经过270 d老化后,该土壤仍表现出近100%的96 h致死效应. 相类似的, Gospodarek等[37]发现,野外土壤被柴油泄露污染540 d后,依然对跳虫表现很强不良效应. 如前所述,本研究所涉及石油烃浓度接近部分高污染页岩气开采场地土壤的检出浓度[21],这表明页岩气钻井液泄露对周边土壤生物的环境风险不容忽视.
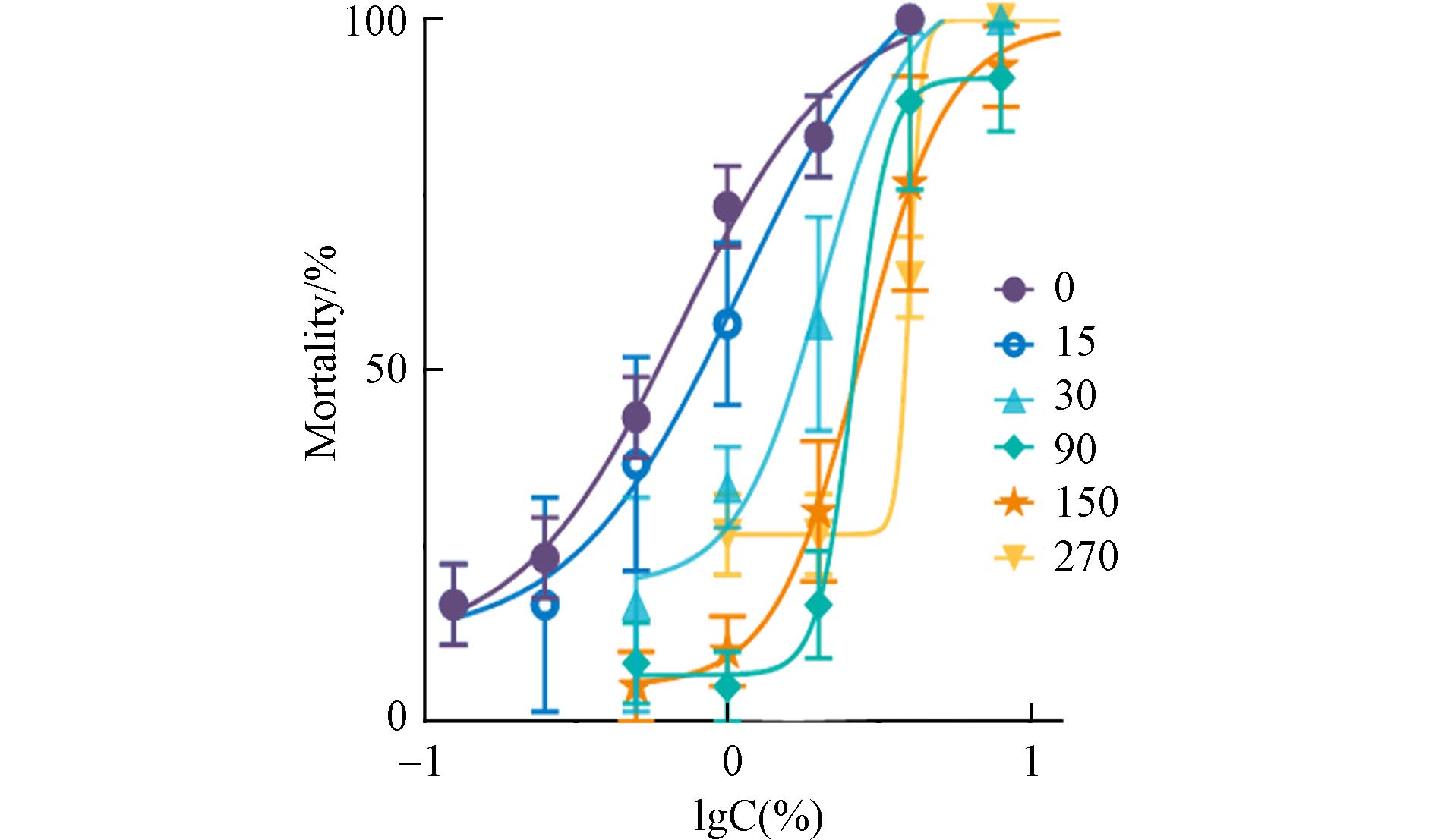
通过干净土壤逐级稀释后进行跳虫96 h毒性测试,获得了不同老化时间下,污染土壤对跳虫的剂量-效应曲线,并估算了半数致死浓度(LC50). 由图4 可见,随老化时间延长,剂量-效应曲线右移,说明老化作用使土壤对跳虫的毒性不断下降,0、15、30、90、150、270 d的LC50分别为0.583%、1.07%、2.00%、2.61%、2.77%、4.00%. 土壤对跳虫毒性的变化趋势和其中污染物的生物有效性具有很好的相关性,如图5所示,跳虫的LC50与Tenax萃取测定的PAHs 生物有效浓度正相关(P <0.05, r2 = 0.89),这表明源自油基钻井液的多环芳烃等物质是污染土壤导致跳虫高致死率的因素之一.
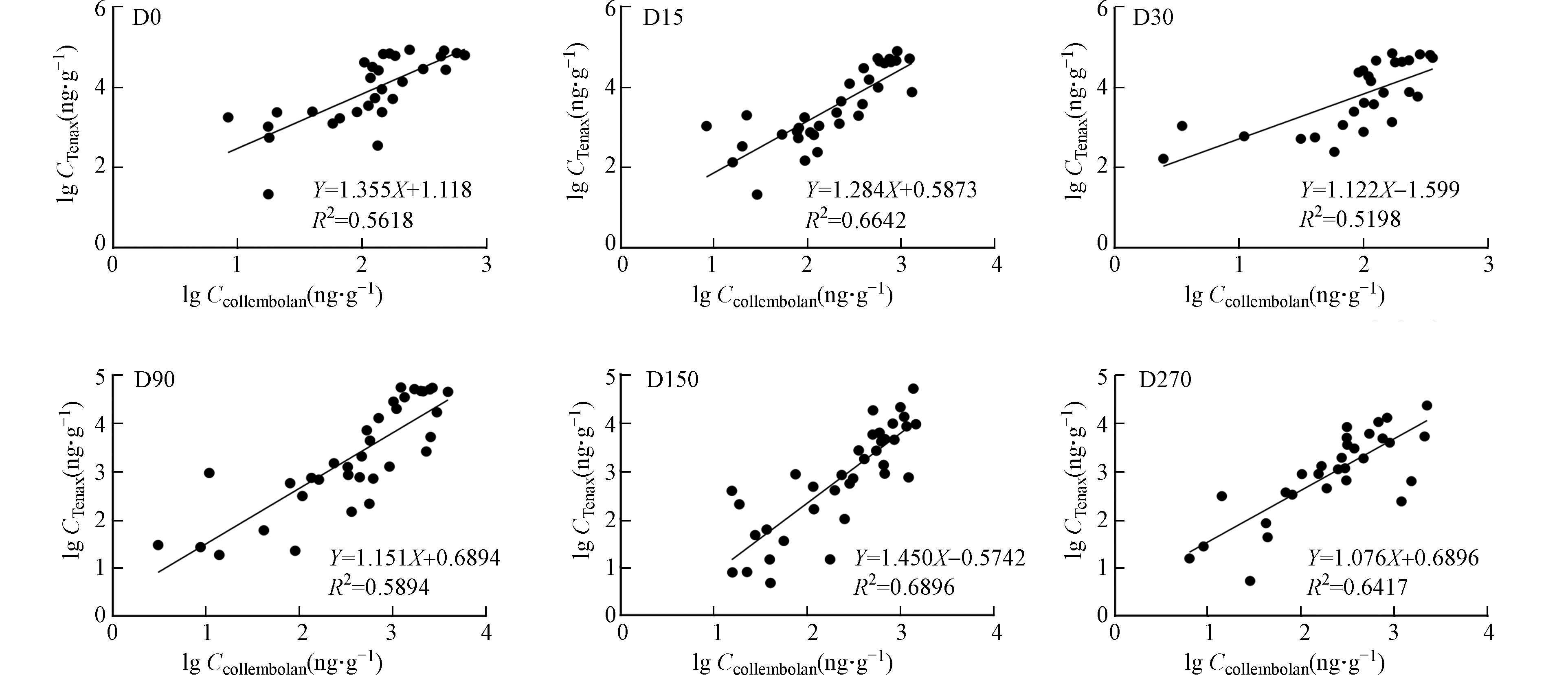
为进一步验证污染土壤中生物有效PAHs对跳虫毒性的贡献,收集暴露在1%油基钻井液污染的土壤中存活的跳虫,分析其体内蓄积PAHs和正构烷烃的浓度. 如图6所示,在不同老化时间点,跳虫体内蓄积污染物浓度与Tenax 萃取所测定生物有效浓度存在显著相关性(P值均小于
0.0001 ,r2范围为0.52—0.69). 早期有文献表明Tenax萃取成功地模拟了土壤动物蚯蚓对PAHs和有机氯农药(DDT、林丹)等污染物的生物有效性,以及植物上海青对土壤中邻苯二甲酸酯的生物有效性[38 − 41]. 本研究也说明Tenax萃取测定的污染物生物有效浓度可较好地预测污染物在跳虫体内的富集能力,并进一步估算其毒性效应. -
油基钻井液具有突出的强抑制性和强井壁稳定性,对于维持页岩气开采水平钻井的高温、高压的复杂地层环境下的稳定性,不可或缺,然而其广泛使用造成了周边土壤环境潜在风险. 本研究选用真实环境中油基钻井液污染土壤的可能浓度,即38.3 mg·kg−1,测定了被污染土壤对模式生物跳虫的毒性,发现污染土壤对跳虫有强致死性(96-h LC50为0.583%),但该毒性随着土壤老化时间的延长而减弱,270 d后96-h LC50降为4.00%. 另外,钻井液污染土壤的主要污染物——正构烷烃和PAHs,随老化时间延长,总体趋势均为在实验开始时浓度较快下降,此后随时间延长而降低,直至实验中后期总量趋于稳定. 同时,还发现对比ASE耗竭式萃取,基于生物有效性的Tenax萃取与跳虫体内富集污染物的浓度相关性更好,其P值小于
0.0001 ,而且生物有效PAHs浓度与土壤对跳虫的毒性作用趋势相吻合,这表明页岩气钻井液污染土壤的毒性随老化作用降低,且与土壤中主要污染物的生物有效性有关,而PAHs是可能主要致毒因素之一. 鉴于油基钻井液是一个复杂的混合物,未来需要进一步开展关键致毒物的筛查和确认的工作.
页岩气钻井液污染土壤中石油烃类污染物的生物有效性及毒性的时间变化趋势
Temporal variation in bioavailability and toxicity of petroleum hydrocarbons in soil contaminated by shale gas drilling fluids
-
摘要: 页岩气开发有助于促进能源结构转型,了解页岩气开采过程的潜在风险对行业的可持续发展至关重要. 油基钻井液含高浓度的石油烃类物质,可造成周边土壤污染,但目前对污染土壤的毒性效应知之甚少. 为考察老化对页岩气开采污染土壤中典型污染物的生物有效性和毒性的影响,本研究将油基钻井液污染土壤老化至270 d,利用耗竭性萃取和Tenax萃取分析了不同时间点土壤中多环芳烃(PAHs)和烷烃总浓度和生物有效浓度,同时测试了土壤对白符跳虫的96-h致死性以及存活跳虫中富集的污染物. 结果表明,油基钻井液污染土壤中PAHs主要以低环形式存在,污染物生物有效性随老化时间延长显著下降,且高环PAHs生物有效性降低更快. 场地环境可检出浓度下,即使老化270 d,钻井液污染土壤仍对跳虫表现高毒性(96-h LC50为4.00%),但毒性随老化时间延长,逐步下降,且与土壤中多环芳烃生物有效浓度以及生物体内富集有机物浓度密切相关. 本研究揭示了老化时间对钻井液污染土壤中主要污染物生物有效性和毒性的影响,有利于全面认识页岩气开采过程对周边土壤的潜在风险.Abstract: The development of shale gas is conducive to energy structure transformation. Understanding potential risks related to shale gas exploitation is crucial to the sustainable development of this industry. Oil-based drilling fluids contain high concentrations of petroleum hydrocarbons, which may pollute surrounding soils, but the toxicity of contaminated soil is largely unknown currently. To investigate the impact of aging on the bioavailability and toxicity of typical pollutants in soil contaminated by shale gas extraction, oil-based drilling fluid contaminated soil was aged until 270 d, and the total and bioavailable concentrations of polycyclic aromatic hydrocarbons (PAHs) and alkanes were analyzed in soils with different aging time using exhaustive and Tenax extraction. In addition, 96-h lethality of the contaminated soil to springtails was examined and the pollutants accumulated in surviving springtails were also assessed. Results showed that PAHs in oil-based drilling fluid-contaminated soil mainly occurred in low-ring forms. The bioavailability of pollutants decreased with increasing aging time, and the bioavailability of high-ring PAHs decreased faster than the low-rings. At the concentrations similar to those in the shale gas extraction sites, even if aged for 270 d, soil contaminated by drilling fluid was still highly toxic to the springtails (96-h LC50 of 4.00%), but the toxicity gradually reduced with aging time. The toxicity was related to the bioavailable concentration of PAHs in the soil and body residues in organisms. The present study revealed the impact of aging time on the bioavailability and toxicity of main pollutants in drilling fluid-contaminated soil, which is beneficial to a comprehensive understanding of potential risks of the shale gas extraction process to surrounding soil.
-
Key words:
- Polycyclic aromatic hydrocarbons /
- bioavailability /
- soil toxicity /
- aging /
- Collembola
-

-
-
[1] WANG Q, LI S Q. Shale gas industry sustainability assessment based on WSR methodology and fuzzy matter-element extension model: The case study of China[J]. Journal of Cleaner Production, 2019, 226: 336-348. doi: 10.1016/j.jclepro.2019.03.346 [2] U. S. Energy Information Administration - EIA - Independent Statistics and Analysis[EB/OL]. [2023-10-26]. [3] 蔡勋育, 刘金连, 张宇, 等. 中国石化“十三五” 油气勘探进展与“十四五” 前景展望[J]. 中国石油勘探, 2021, 26(1): 31-42. CAI X Y, LIU J L, ZHANG Y, et al. Oil and gas exploration progress of Sinopec during the 13th Five-Year Plan period and prospect forecast for the 14th Five-Year Plan[J]. China Petroleum Exploration, 2021, 26(1): 31-42 (in Chinese).
[4] LI L, WU F, CAO Y Y, et al. Sustainable development index of shale gas exploitation in China, the UK, and the US[J]. Environmental Science and Ecotechnology, 2022, 12: 100202. doi: 10.1016/j.ese.2022.100202 [5] MA L T, HURTADO A, EGUILIOR S, et al. Acute and chronic risk assessment of BTEX in the return water of hydraulic fracturing operations in Marcellus Shale[J]. Science of the Total Environment, 2024, 906: 167638. doi: 10.1016/j.scitotenv.2023.167638 [6] ZHONG C, ZOLFAGHARI A, HOU D Y, et al. Comparison of the hydraulic fracturing water cycle in China and North America: A critical review[J]. Environmental Science & Technology, 2021, 55(11): 7167-7185. [7] TAO Z, LIU C H, HE Q, et al. Detection and treatment of organic matters in hydraulic fracturing wastewater from shale gas extraction: A critical review[J]. Science of the Total Environment, 2022, 824: 153887. doi: 10.1016/j.scitotenv.2022.153887 [8] MA L T, HURTADO A, EGUILIOR S, et al. Exposure risk assessment to organic compounds based on their concentrations in return water from shale gas developments[J]. Science of the Total Environment, 2022, 822: 153586. doi: 10.1016/j.scitotenv.2022.153586 [9] HUANG C, JIN B, HAN M, et al. Identifying persistent, mobile and toxic (PMT) organic compounds detected in shale gas wastewater[J]. Science of the Total Environment, 2023, 858: 159821. doi: 10.1016/j.scitotenv.2022.159821 [10] WILLEMS D J, KUMAR A, NUGEGODA D. Mixture toxicity of three unconventional gas fracking chemicals, Barium, O-cresol, and sodium chloride, to the freshwater shrimp Paratya australiensis[J]. Environmental Toxicology and Chemistry, 2023, 42(2): 481-494. doi: 10.1002/etc.5538 [11] ZHANG G Y, ZHAO F, CHENG X W, et al. Resource utilization from solid waste originated from oil-based shale drilling cutting during shale gas development[J]. Chemosphere, 2022, 298: 134318. doi: 10.1016/j.chemosphere.2022.134318 [12] ZHOU S B, LI Z Q, PENG S C, et al. River water influenced by shale gas wastewater discharge for paddy irrigation has limited effects on soil properties and microbial communities[J]. Ecotoxicology and Environmental Safety, 2023, 251: 114552. doi: 10.1016/j.ecoenv.2023.114552 [13] KOOKANA R S, WILLIAMS M, GREGG A, et al. Sorption, degradation and microbial toxicity of chemicals associated with hydraulic fracturing fluid and produced water in soils[J]. Environmental Pollution, 2022, 309: 119754. doi: 10.1016/j.envpol.2022.119754 [14] GOLDING L A, KUMAR A, ADAMS M S, et al. The influence of salinity on the chronic toxicity of shale gas flowback wastewater to freshwater organisms[J]. Journal of Hazardous Materials, 2022, 428: 128219. doi: 10.1016/j.jhazmat.2022.128219 [15] 王中华. 国内油基钻井液研究与应用综述[J]. 中外能源, 2022, 27(8): 29-36. WANG Z H. A review of oil-based drilling fluid research and application in China[J]. Sino-Global Energy, 2022, 27(8): 29-36 (in Chinese).
[16] 孙金声, 蒋官澄, 贺垠博, 等. 油基钻井液面临的技术难题与挑战[J]. 中国石油大学学报(自然科学版), 2023, 47(5): 76-89. SUN J S, JIANG G C, HE Y B, et al. Technical difficulties and challenges faced by oil-based drilling fluid[J]. Journal of China University of Petroleum (Edition of Natural Science), 2023, 47(5): 76-89 (in Chinese).
[17] XIONG D M, HAN X. Particular pollutants, human health risk and ecological risk of oil-based drilling fluid: A case study of Fuling shale gas field[J]. Environmental Geochemistry and Health, 2023, 45(3): 981-995. doi: 10.1007/s10653-022-01259-z [18] XIE B X, QIN J H, SUN H, et al. Release characteristics of polycyclic aromatic hydrocarbons (PAHs) leaching from oil-based drilling cuttings[J]. Chemosphere, 2022, 291: 132711. doi: 10.1016/j.chemosphere.2021.132711 [19] LI Y T, ZHENG B P, YANG Y H, et al. Soil microbial ecological effect of shale gas oil-based drilling cuttings pyrolysis residue used as soil covering material[J]. Journal of Hazardous Materials, 2022, 436: 129231. doi: 10.1016/j.jhazmat.2022.129231 [20] CHEN K J, HE R, WANG L A, et al. The dominant microbial metabolic pathway of the petroleum hydrocarbons in the soil of shale gas field: Carbon fixation instead of CO2 emissions[J]. Science of the Total Environment, 2022, 807: 151074. doi: 10.1016/j.scitotenv.2021.151074 [21] 王兵, 李珍珍, 李琋, 等. 页岩气井场土壤石油类污染特性及对理化性质的影响[J]. 安全与环境学报, 2018, 18(4): 1598-1604. WANG B, LI Z Z, LI X, et al. On the contamination features and their relationship with the physicochemical properties of petroleum hydrocarbon polluted soils in the shale gas fields[J]. Journal of Safety and Environment, 2018, 18(4): 1598-1604 (in Chinese).
[22] XU Q, WU W, XIAO Z F, et al. Responses of soil and collembolan (Folsomia candida) gut microbiomes to 6PPD-Q pollution[J]. Science of the Total Environment, 2023, 900: 165810. doi: 10.1016/j.scitotenv.2023.165810 [23] CIPULLO S, PRPICH G, CAMPO P, et al. Assessing bioavailability of complex chemical mixtures in contaminated soils: Progress made and research needs[J]. Science of the Total Environment, 2018, 615: 708-723. doi: 10.1016/j.scitotenv.2017.09.321 [24] OLIVER M, ADROVER M, FRONTERA A, et al. In-vitro prediction of the membranotropic action of emerging organic contaminants using a liposome-based multidisciplinary approach[J]. Science of the Total Environment, 2020, 738: 140096. doi: 10.1016/j.scitotenv.2020.140096 [25] CHEN H Y, TIAN Y X, CAI Y X, et al. A 50-year systemic review of bioavailability application in Soil environmental criteria and risk assessment[J]. Environmental Pollution, 2023, 335: 122272. doi: 10.1016/j.envpol.2023.122272 [26] CHEN Y J, FENG X J, LIU X G, et al. Bioavailability assessment of difenoconazole to earthworms (Eisenia fetida) in soil by oleic acid-embedded cellulose acetate membrane[J]. Science of the Total Environment, 2023, 905: 167276. doi: 10.1016/j.scitotenv.2023.167276 [27] YI X Y, LI H Z, MA P, et al. Identifying the causes of sediment-associated toxicity in urban waterways in South China: Incorporating bioavailabillity-based measurements into whole-sediment toxicity identification evaluation[J]. Environmental Toxicology and Chemistry, 2015, 34(8): 1744-1750. doi: 10.1002/etc.2970 [28] REINECKE A J, van WYK M, REINECKE S A. The influence of soil characteristics on the toxicity of oil refinery waste for the springtail Folsomia candida (collembola)[J]. Bulletin of Environmental Contamination and Toxicology, 2016, 96(6): 804-809. doi: 10.1007/s00128-016-1792-9 [29] 由宗政, 孔德洋, 许静, 等. 加速溶剂萃取-气相色谱法测定土壤、植物样品中13种多溴联苯醚[J]. 环境化学, 2013, 32(7): 1410-1416. doi: 10.7524/j.issn.0254-6108.2013.07.040 YOU Z Z, KONG D Y, XU J, et al. Determination of 13 polybrominated biphenyl ethers in soil and plant using accelerated solvent extraction and gas chromatography[J]. Environmental Chemistry, 2013, 32(7): 1410-1416 (in Chinese). doi: 10.7524/j.issn.0254-6108.2013.07.040
[30] YOU J, PEHKONEN S, LANDRUM P F, et al. Desorption of hydrophobic compounds from laboratory-spiked sediments measured by Tenax absorbent and matrix solid-phase microextraction[J]. Environmental Science & Technology, 2007, 41(16): 5672-5678. [31] LI C, XU S, GUAN D X, et al. Comparison of in vitro strategies for predicting Dichlorodiphenyltrichloroethane (DDT) and its metabolites bioavailability from soils[J]. Ecotoxicology and Environmental Safety, 2023, 256: 114885. doi: 10.1016/j.ecoenv.2023.114885 [32] 宫兆波, 郭瑛瑛, 张燕萍, 等. 基因工程菌在石油污染修复中的研究进展与前景[J]. 环境化学, 2024, 43(1): 14-26. GONG Z B, GUO Y Y, ZHANG Y P, et al. The application of genetically engineered bacteria in petroleum hydrocarbon pollution remediation: progress and challenges[J]. Environmental Chemistry,2024, 43(1): 14-26 (in Chinese).
[33] 韩民, 黄晨, 刘世洋, 等. 页岩气开采水力压裂返排水中化学污染物的组成特征[J]. 环境化学, 2022, 41(1): 305-314. doi: 10.7524/j.issn.0254-6108.2021050302 HAN M, HUANG C, LIU S Y, et al. Compositional characteristics of chemical pollutants in flowback water during shale gas hydraulic fracking[J]. Environmental Chemistry, 2022, 41(1): 305-314 (in Chinese). doi: 10.7524/j.issn.0254-6108.2021050302
[34] 蒙恬, 单翀, 罗欢, 等. 油田典型含油污泥污染特性对比分析[J]. 石油化工应用, 2023, 42(5): 52-56. MENG T, SHAN C, LUO H, et al. Comparative analysis of pollution characteristics of typical oily sludge in oilfields[J]. Petrochemical Industry Application, 2023, 42(5): 52-56 (in Chinese).
[35] STOUT S A, BREY A P. Appraisal of coal- and coke-derived wastes in soils near a former manufactured gas plant, Jacksonville, Florida[J]. International Journal of Coal Geology, 2019, 213: 103265. doi: 10.1016/j.coal.2019.103265 [36] CHEN X X, LI C, CAO X Y, et al. Bioaccessibility and bioavailability of NPAHs in soils using in vitro-in vivo assays: Comparison of laboratory and outdoor environmental aging effect[J]. Science of the Total Environment, 2023, 868: 161619. doi: 10.1016/j.scitotenv.2023.161619 [37] GOSPODAREK J, RUSIN M. Effect of soil polluted with petroleum-DerivedSubstances during bioremediationon the occurrence of collembolaand Acarina[J]. Polish Journal of Environmental Studies, 2020, 29(5): 3115-3125. doi: 10.15244/pjoes/114259 [38] MIAO J J, CHEN X L, XU T, et al. Bioaccumulation, distribution and elimination of lindane in Eisenia foetida: The aging effect[J]. Chemosphere, 2018, 190: 350-357. doi: 10.1016/j.chemosphere.2017.09.138 [39] MORRISON D E, ROBERTSON B K, ALEXANDER M. Bioavailability to earthworms of aged DDT, DDE, DDD, and dieldrin in soil[J]. Environmental Science & Technology, 2000, 34(4): 709-713. [40] WANG J, TAYLOR A, XU C Y, et al. Evaluation of different methods for assessing bioavailability of DDT residues during soil remediation[J]. Environmental Pollution, 2018, 238: 462-470. doi: 10.1016/j.envpol.2018.02.082 [41] GUO M X, GONG Z Q, LI X J, et al. Polycyclic aromatic hydrocarbons bioavailability in industrial and agricultural soils: Linking SPME and Tenax extraction with bioassays[J]. Ecotoxicology and Environmental Safety, 2017, 140: 191-197. doi: 10.1016/j.ecoenv.2017.02.044 -




 下载:
下载: