-
近几十年来,抗生素的使用量逐年增加,在人类生产生活中发挥着越来越重要的作用[1]. 环丙沙星(CIP),作为第三代喹诺酮类药物,因其广谱、抗菌性强、吸收效果好等特点,广泛应用于人类和动物抗感染类疾病的治疗和预防[2 − 3]. 但其在实际应用中只有少量被生物体吸收,大部分以原药或者代谢产物的形式流入水环境中[4]. 在地下水、地表水、沉积物、土壤、污水处理厂污水及污泥等介质中均已检测到CIP,虽然浓度为ng·L−1至mg·L−1,但CIP具有难生物降解、半衰期长等特征,对生态环境和人类健康构成潜在威胁[5 − 6]. 因此,研究对水体中CIP的高效去除技术具有重要意义. 目前常用的抗生素去除方法主要包括高级氧化法、混凝法、膜分离法、生物法和吸附法等[7 − 10]. 其中吸附法因制备简单、价格低廉、去除效率高等优势,受到人们广泛关注[11].
气凝胶是一种具有高孔隙率、高比表面积和低密度及表面化学结构性质易调控的三维多孔材料,在污染物的吸附分离方面具有良好应用潜力[12]. 前期工作中发现,羧甲基纤维素(CMC)和κ-卡拉胶(κ-CG)互穿网络气凝胶(CMC/κ-CG)具有疏松多孔的三维结构、力学性能良好、对CIP具有较好的吸附效果,但因吸附机制以静电吸引作用为主,在碱性和高浓度共存无机盐存在条件下,吸附性能明显下降,不利于CMC/κ-CG气凝胶的实际应用[13]. MIL-53是由Fe3+和对苯二甲酸在水热条件下组装合成的一种常见金属有机框架材料,具有良好的耐酸碱性和热稳定性,同时也具有良好的吸附性能,但粉末状MIL-53存在粒径小、在实际水体中易流失、难以回收等问题,使得其实际应用受到较大限制[14].
基于此,本课题分别以CMC和CMC/κ-CG气凝胶为基底,原位负载MIL-53,合成有机-无机复合气凝胶CMC/MIL-53和CMC/κ-CG/MIL-53,利用傅里叶变换红外光谱(FTIR)、X射线衍射(XRD)、比表面积分析仪、热重分析(TGA)和场发射扫描电子显微镜(FESEM)等手段分析CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶的化学结构和物化特性,详细研究pH、离子强度、吸附时间、初始溶液浓度等因素对复合气凝胶吸附CIP的影响, 同时还考察了复合气凝胶的重复利用性和在实际水体中对CIP的吸附选择性,结合吸附动力学、吸附等温线研究结果以及吸附前后的FTIR和X射线光电子能谱(XPS)谱图变化,分析复合气凝胶对CIP的多重吸附机理,为有机-无机复合气凝胶应用于抗生素的高效去除提供实验实践和理论支撑.
-
CMC(1500-3100 mPa·s)、κ-CG、环氧氯丙烷(ECH, A.R.)、对苯二甲酸(>99%)、N, N-二甲基甲酰胺(DMF, A.R.)、甲醇(A.R.)、CIP(>98%)、氯化铁六水合物(FeCl3·6H2O, A.R.)均购自阿拉丁公司(美国),乙腈(A.R.)、乙酸(A.R.)、氯化钠(A.R.)、氢氧化钠(A.R.)和盐酸(A.R.)等试剂购自国药集团化学试剂有限公司(中国).
-
首先制备CMC/κ-CG及CMC气凝胶,具体步骤如下:分别称取3.0 g CMC和2.0 g κ-CG溶于100 mL去离子水中,在60 ℃条件下加热1 h后,向溶液中逐滴加入5 mL ECH,在60 ℃条件下继续交联10 h后,倒入模具中冷冻,然后经冷冻干燥48 h后得到CMC/κ-CG气凝胶. 不加κ-CG,仅加入5.0 g CMC,通过同样方法制备CMC气凝胶.
将0.5406 g(2.0 mmol) FeCl3·6H2O和0.1661 g(1.0 mmol) 对苯二甲酸分别充分溶于30 mL和20 mL DMF溶液中分别记为A和B溶液;将1.0 g制得的CMC/κ-CG气凝胶加入到上述A溶液中,搅拌0.5 h后,再将上述混合物倒入B溶液,在110 ℃条件下水热反应20 h后,常温下先分别利用DMF和甲醇各清洗3次,每次10 min,再用去离子水洗至中性,冷冻干燥后得到复合气凝胶CMC/κ-CG/MIL-53, 以CMC气凝胶代替CMC/κ-CG气凝胶,通过同样方法制备CMC/MIL-53气凝胶. 此外,不加气凝胶,利用同样方法制备MIL-53颗粒,在60 ℃条件下烘干48 h得到橙黄色粉末.
-
利用Tensor 27傅里叶红外光谱仪(Bruker,德国)和PHI 5000 VersaProbe III X射线光电子能谱仪(UlVAC-PHI, 日本)分析材料结构,利用D8 Advance型X射线衍射仪(Bruker, 德国)对材料晶体结构进行表征(Cu靶,衍射角2θ扫描范围为3—70°),利用FESEM(Thermo scientific, 美国)观察材料表面微观形貌,利用Instron 5944万能试验机(Instron,美国)测定气凝胶的抗压强度. 利用ASAP2020比表面积分析仪(Micromeritics, 美国)测定材料的比表面积和孔径分布,利用TG-DSC_STA 449 F3型热重分析仪(NETZSCH, 德国)测定材料的热稳定性.
-
将5.0 mg吸附剂投加到30 mL 0.20 mmol·L−1 CIP溶液中,在298 K条件下,以180 r·min−1转速连续振荡24 h达到吸附平衡,利用高效液相色谱仪(安捷伦HPLC 1200,美国)测定吸附前后溶液中CIP浓度. 并根据式(1)计算吸附剂对CIP的吸附量(mmol·g−1):
式中,C0和Ce分别为污染物初始浓度和吸附平衡浓度(mmol·L−1),V为溶液体积(L),m为吸附剂质量(g).
分别研究不同pH(3.0—9.0)、初始浓度(0.05—0.25 mmol·L−1)、反应时间(0—12 h)和离子强度(NaCl(1—100 mmol·L−1))对复合气凝胶吸附CIP的影响. 利用0.001 mol·L−1盐酸和甲醇的混合溶液(3:1, V:V)对达到吸附饱和的CMC/κ-CG/MIL-53气凝胶脱附再生,共进行5次吸附-解吸附循环实验. 研究CMC/MIL-53和CMC/κ-CG/MIL-53在不同pH条件下吸附CIP后的Fe3+浸出情况,并利用电感耦合等离子体质谱仪(ICP-MS, 德国)测定Fe3+浸出浓度. 分别以去离子水、自来水和地表水(南京市九乡河水)为水源,经0.45 μm滤膜过滤后,分别以3种水源为基质,配制0.002 mmol·L−1的CIP溶液,考察CMC/κ-CG/MIL-53和CMC/κ-CG气凝胶对不同水体中CIP的吸附效果.
-
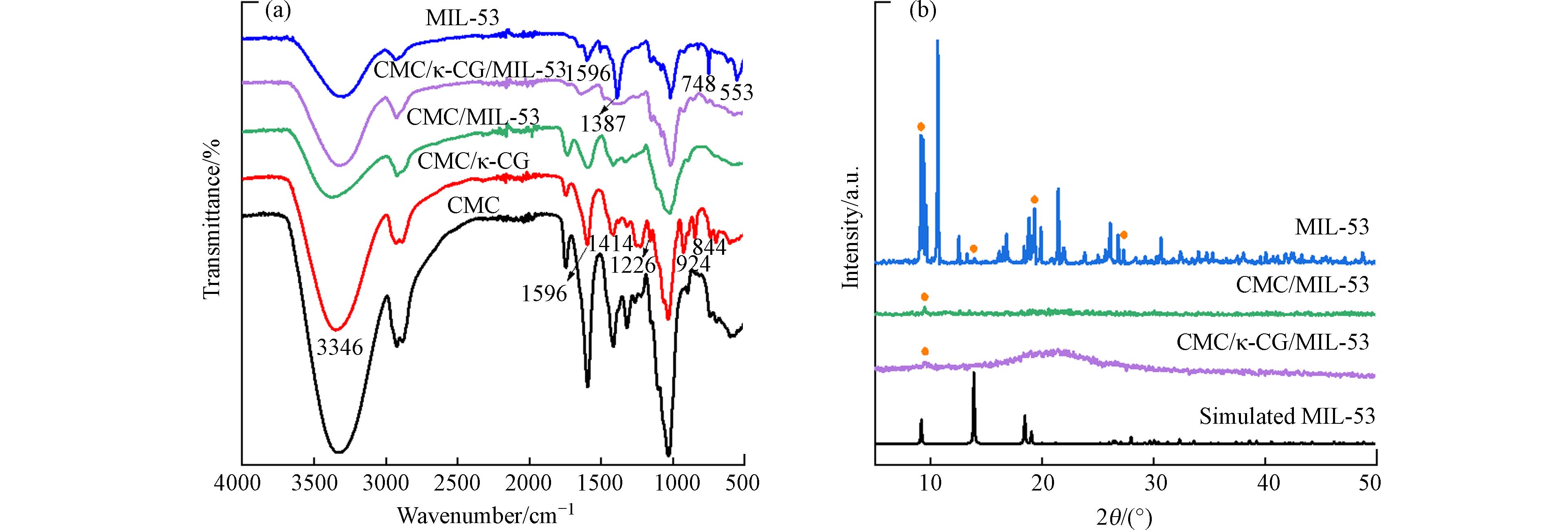
负载MIL-53的两种复合气凝胶通过原位法制得,详细制备步骤参见实验部分. 各种气凝胶红外光谱如图1(a)所示,3346、1596、1414 cm−1处特征峰分别对应CMC上—OH和—COOH伸缩振动峰[15],924 cm−1和844 cm−1分别对应κ-CG上3, 6-脱水-D-半乳糖和糖苷键的伸缩振动峰,在1226 cm−1处特征峰为κ-CG中—OSO3−的伸缩振动峰[15];对于负载MIL-53的两种复合气凝胶,在553 cm−1和748 cm−1出现的特征峰分别对应于MIL-53上Fe—O和苯环上C—H伸缩振动峰[16],而1387 cm−1和1596 cm−1处特征峰是与Fe配位的羧基—COO−的不对称伸缩和对称伸缩振动峰[16];另外,CMC/MIL-53和CMC/κ-CG/MIL-53上—OH、—COOH及—OSO3−特征峰,分别与CMC和CMC/κ-CG相比,峰强度减弱,且峰位置发生移动,说明MIL-53可能主要以—OH、—COOH和—OSO3−基团为原位生长的成核位点并通过氢键或络合作用进一步与CMC和CMC/κ-CG气凝胶结合[17 − 19],以上结果证明两种复合气凝胶均已成功制备.
MIL-53、CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶的XRD谱图如图1(b)所示,MIL-53在2θ为9.3°、13.3°、19.3°处的衍射峰分别对应(200)、(110)和(111)晶面,和模拟计算的MIL-53标准卡结果吻合[20],说明MIL-53已成功制得. 而CMC/MIL-53和CMC/κ-CG/MIL-53复合气凝胶中原对应MIL-53的(110)和(111)晶面衍射峰消失,在2θ为9.4°处存在相对较弱的(200)晶面衍射峰,证明复合气凝胶成功制得,而衍射峰强度减弱可能是由于MIL-53负载量相对较低造成的. 此外,CMC/κ-CG/MIL-53在2θ为15°—30°范围内,出现了一个较宽衍射峰,说明结构较为无规,生长的晶体尺寸也小,但相对于CMC/MIL-53,CMC/κ-CG/MIL-53仍具有较高的有序度,这说明气凝胶的存在不同程度地干扰了MIL-53晶体的有序生长[21 − 22].
-
采用FESEM直接观察各种气凝胶及MIL-53的表面形态结构,如图2(a-g)所示,CMC(图2(a))和CMC/κ-CG气凝胶(图2(b))主要呈光滑的层状多孔的三维结构,CMC/κ-CG由于引入成胶性较强的κ-CG,片层结构较为紧密,显示出较强刚性[23]. 而MIL-53呈中间宽两头尖的规则纺锤形结构(图2(c)),与文献报道一致[14,24]. 根据图2(d)和(f),CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶仍保持层状的三维多孔结构特征,且含有一些不完全规则的颗粒晶体,其表面还具有一定褶皱(图2(e)和(g)),相比于CMC和CMC/κ-CG,其粗糙表面可提供更多与污染物接触的反应位点[22]. 复合气凝胶上MIL-53颗粒晶体分布较为分散,与纯MIL-53颗粒相比,尺寸较小,且其结构具有较大缺陷趋于无规形态,说明MIL-53晶体在气凝胶上原位生长过程中受到一定干扰,晶体结构被破坏,这与图1(b)中XRD结果一致;同时气凝胶和MIL-53功能基团的氢键和螯合作用不均匀,可能导致了晶体不均匀地随机生成[25]. 此外,图2(d-g)显示,相较于CMC/MIL-53,CMC/κ-CG/MIL-53气凝胶中MIL-53的颗粒形状更为规则,尺寸也更小,这与XRD中结果一致. 图2(h)为4种气凝胶的数码照片,CMC/MIL-53和CMC/κ-CG/MIL-53呈棕褐色,CMC/MIL-53相对于CMC气凝胶体积并未发生太大变化,内部层状多孔结构更为显著;而与CMC/κ-CG气凝胶相比,CMC/κ-CG/MIL-53气凝胶体积相对较小,可能是由于CMC/κ-CG与CMC/κ-CG/MIL-53制备条件不同引起的,CMC/κ-CG的合成是在去离子水中进行,而CMC/κ-CG/MIL-53是在DMF中制备,并经DMF和甲醇溶剂清洗,κ-CG在DMF和甲醇溶剂中更容易发生塌缩,导致CMC/κ-CG/MIL-53气凝胶体积进一步收缩[23].
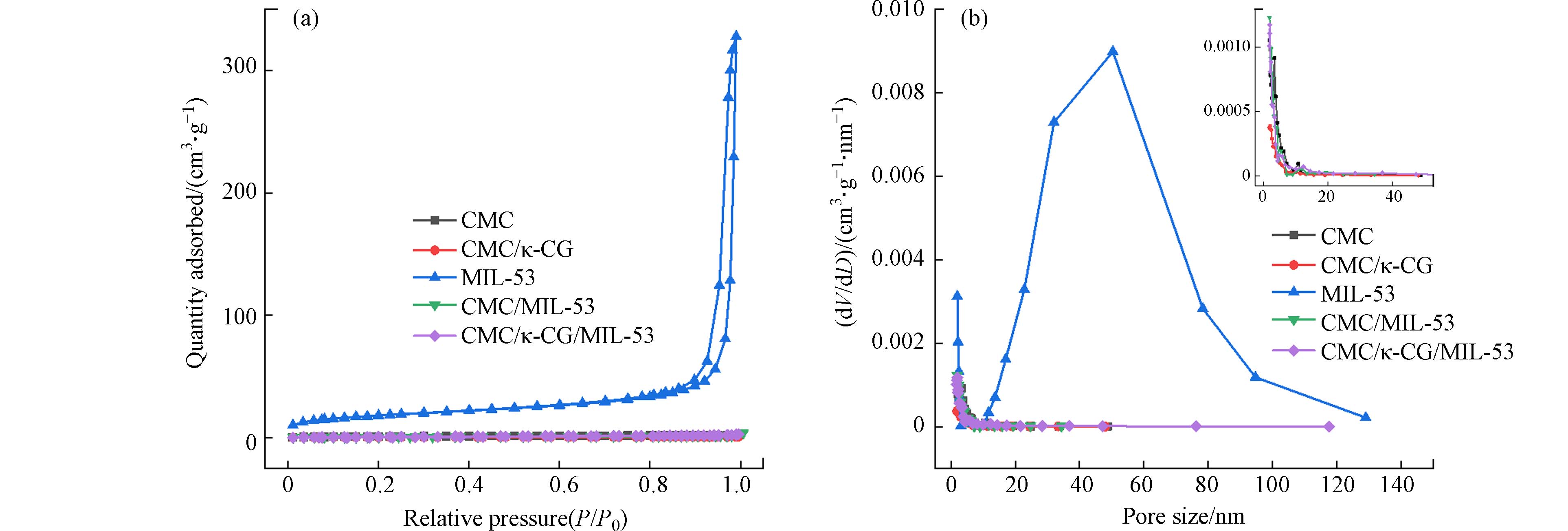
不同材料的比表面积和孔隙率通过N2吸附-脱附等温线测定,从图3(a)可以看出,与4种气凝胶不同,MIL-53颗粒表现出IV型等温线特征,当相对压力达到80%以上,N2吸收率急剧增加,有明显的磁滞回线出现,表明MIL-53中存在丰富的介孔结构[26]. 此外,MIL-53比表面积(65.701 m2·g−1)远高于4种气凝胶,一方面可能是由于气凝胶的孔隙较大,导致相对较小的比表面积[27 − 28],另一方面可能由于CMC和CMC/κ-CG气凝胶表面原位生长的MIL-53与粉末状MIL-53结构存在显著差异,因此并未提升复合气凝胶的比表面积,这与XRD(图1(b))及FESEM(图2)观察结果一致,CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶的比表面积分别为3.096 m2·g−1和3.505 m2·g−1. 图3(b)是不同吸附剂的孔径分布曲线,根据图3(b),MIL-53颗粒是一种多孔纳米材料,平均孔径91.323 nm;从图3(b)内插图可以看出,CMC负载MIL-53后孔径变化不大,CMC/κ-CG/MIL-53介孔数量略大于CMC/κ-CG,说明气凝胶成功负载MIL-53.
-
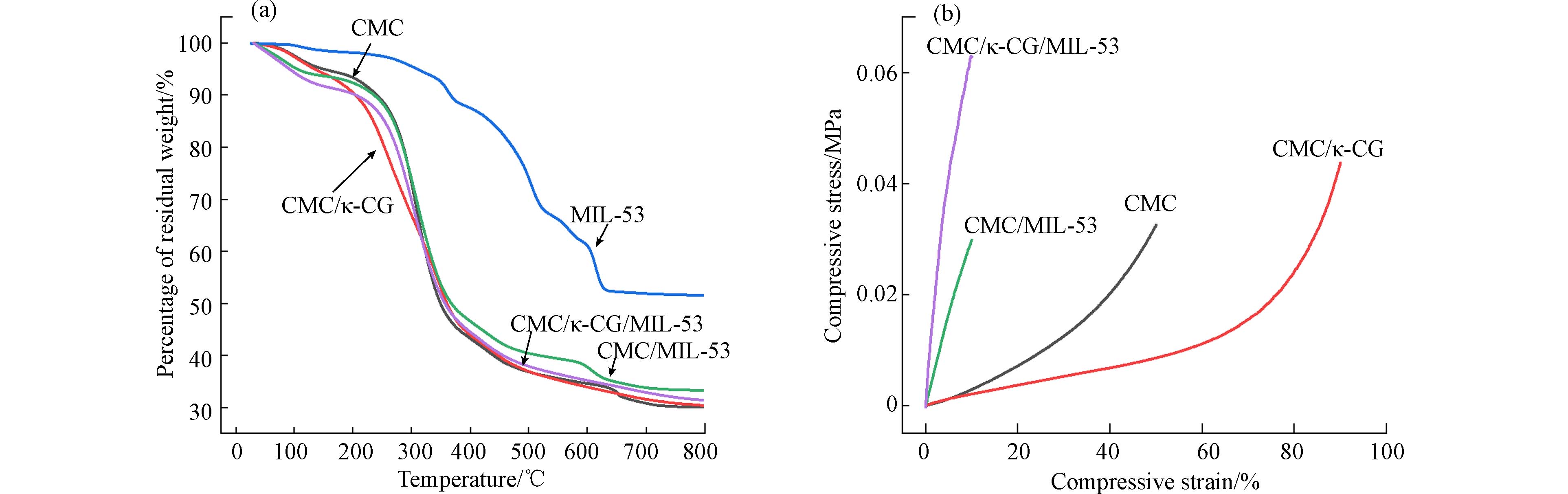
热重分析有助于了解复合气凝胶中各组分热稳定性质与含量,各材料在N2条件下的热重分析结果如图4(a)所示,复合气凝胶的热重曲线大致可分为0—200 ℃、200—400 ℃和400 ℃以上三个失重阶段. 在0—200 ℃范围内10%的重量损失主要是由于孔隙中残留水分蒸发所致,在200—400 ℃范围内的重量损失主要是CMC和κ-CG的热分解,其含氧基团被热分解为二氧化碳和水蒸气[13],温度大于400 ℃的重量损失主要是MIL-53中有机配体的分解所造成的[29]. 当温度达到800 ℃时,CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶的残余重量高于CMC和κ-CG,说明由于MIL-53的引入,气凝胶的热稳定性增强,根据各材料在800 ℃时的剩余质量,可计算得出CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶中MIL-53的负载量分别为17.4%和11.8%.
不同气凝胶的抗压强度如图4(b)所示,CMC和CMC/κ-CG气凝胶最高压缩应变分别可达到50%和90%,对应的压缩应力分别为32.64 kPa和43.76 kPa. 相比于CMC和CMC/κ-CG,CMC/MIL-53和CMC/κ-CG/MIL-53复合气凝胶弹性明显减弱,最高压缩应变均降至10%. 这可能一方面由于其制备方法和制备基质不同所导致,CMC和CMC/κ-CG的合成是在去离子水中进行,而CMC/MIL-53和CMC/κ-CG/MIL-53是在DMF基质中制备,并又经DMF和甲醇溶剂清洗. CMC和CMC/κ-CG由于自身材料特性,在DMF和甲醇中浸泡会变硬变脆[24]. 另一方面,MIL-53的复合也导致了气凝胶弹性减弱,从图2(e)和2(g)看,MIL-53在气凝胶骨架上分散并不均匀,可能导致其力学性能进一步下降. 因此,两方面因素共同造成了CMC/MIL-53和CMC/κ-CG/MIL-53复合气凝胶弹性明显减弱,脆性增强.
-
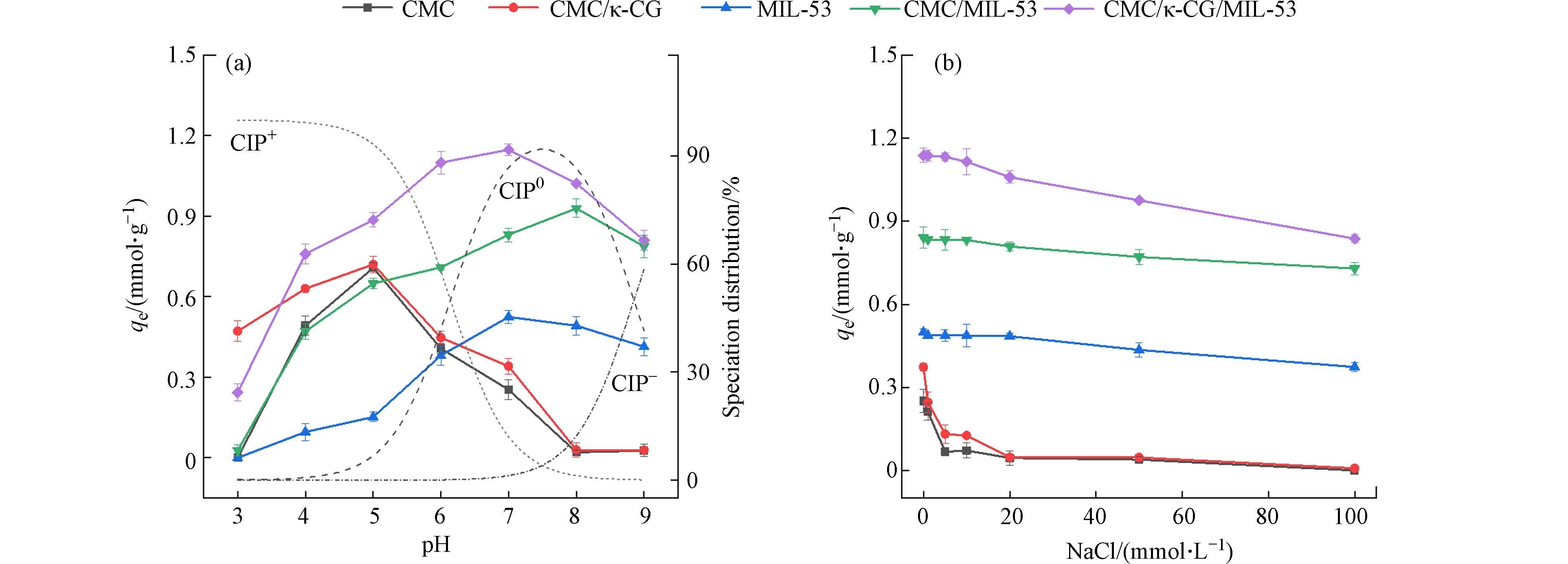
溶液pH可以改变吸附剂和吸附质的表面电荷状态,并对吸附过程产生影响[30]. 不同pH条件下,不同材料对CIP的吸附效果如图5(a)所示. 四种气凝胶及MIL-53在不同pH条件下对CIP的吸附量变化趋势基本一致:随着pH的升高,均呈先升高后降低的趋势. 但不同的是,在中性及碱性条件下,CMC/MIL-53、CMC/κ-CG/MIL-53和MIL-53对CIP的吸附量随pH升高的降低趋势明显平缓,并显著高于CMC和CMC/κ-CG,表现出良好的耐碱性;且两种复合气凝胶吸附量也均远大于MIL-53,表明有机-无机复合气凝胶中不同组分间具有高效的协同吸附作用. 此外,CMC/κ-CG/MIL-53和CMC/κ-CG在酸性条件下也表现出对CIP较为良好的吸附效果,说明κ-CG的引入也较好地改善了CMC气凝胶的吸附性能,甚至在pH为3.0时,CMC/κ-CG吸附量还高于CMC/κ-CG/MIL-53,这是因为MIL-53在强酸条件下对CIP几乎没有吸附作用.
根据CIP的pKa值,其在不同pH水平下的结构形式分布也画在图5(a)中,pH<6.14、6.14<pH<8.85和pH>8.85时,CIP在水溶液中的优势结构形式分别为:+HN—CIP、HN—CIP—COOH和CIP—COO−[31]. 而经测定得到的CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶的pHzpc分别为5.638和5.505,当pH>pHzpc,复合气凝胶带有负电荷,因此在pHzpc<pH<7.0,复合气凝胶表面的—O−、—COO−、—OSO3−和Fe—O−等阴离子基团与+HN—CIP由于静电吸引作用(式(2)和(3))[13],使其具有良好的吸附效果;随着pH的降低,由于质子浓度的增加,其竞争吸附作用导致各吸附剂吸附量下降. 而两种含κ-CG气凝胶材料仍能在强酸条件下具有一定的吸附效果,是由于其引入的强酸型硫酸基团此时对CIP仍具有一定静电吸附作用. 但事实上,根据图5(a),pH为7.0时,CMC/κ-CG/MIL-53对CIP的吸附量才达到最大,约为1.147 mmol·g−1,远高于CMC/κ-CG气凝胶,此时CIP主要以中性HN—CIP—COOH形式存在,静电吸附作用已有所减弱,说明CMC/κ-CG/MIL-53与CIP间除了静电吸附,还可能有其他相互作用的贡献,如氢键作用(式(4)-(7));此外,由于MIL-53的引入,还可能导致π—π电子供体—受体(EDA)相互作用(式(8))和络合作用(式(9))的存在. 当pH>7.0,带负电性的气凝胶和CIP—COO−之间的静电斥力致使其原静电吸附作用降至0,实际吸附量下降(图5(a))[13],而此时复合气凝胶对CIP的吸附可能主要来自络合作用、π—π EDA作用和氢键作用[32 − 34]. CMC/κ-CG和CMC由于没有引入MIL-53,在高pH条件下,静电排斥作用导致其吸附量大幅下降,且静电排斥作用使得吸附剂与吸附质间难以接近,造成相对较弱的氢键作用被严重削弱,导致其吸附量进一步降低(图5(a)).
-
实际水体成份比较复杂,往往包含各种无机盐等,影响吸附剂的吸附性能[35]. 以NaCl(浓度1—100 mmol·L−1)为例,在中性条件下,研究共存离子强度对复合气凝胶吸附CIP的影响(如图5(b)所示). CMC/MIL-53、CMC/κ-CG/MIL-53气凝胶和MIL-53的变化趋势相似,低浓度(≤20 mmol·L−1)NaCl对CIP的吸附影响不大,高浓度(>20 mmol·L−1)NaCl对CIP的吸附产生一定抑制作用,当NaCl浓度升至100 mmol·L−1,吸附量基本达到平衡. 据此,可估算CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶对CIP的吸附过程中静电吸附作用的贡献,分别为13.25%和26.39%. 而CMC和CMC/κ-CG气凝胶受NaCl影响较大,随着NaCl浓度的升高,对CIP的吸附量急剧下降,当NaCl浓度升高至100 mmol·L−1,CMC和CMC/κ-CG气凝胶对CIP的吸附量几乎降为0[13]. 说明CMC和CMC/κ-CG气凝胶复合MIL-53后,抗盐性显著增强,其吸附机制由以静电吸附作用为主导转变为静电吸附、π—π EDA作用、络合作用和氢键作用等多重作用的协同贡献.
-
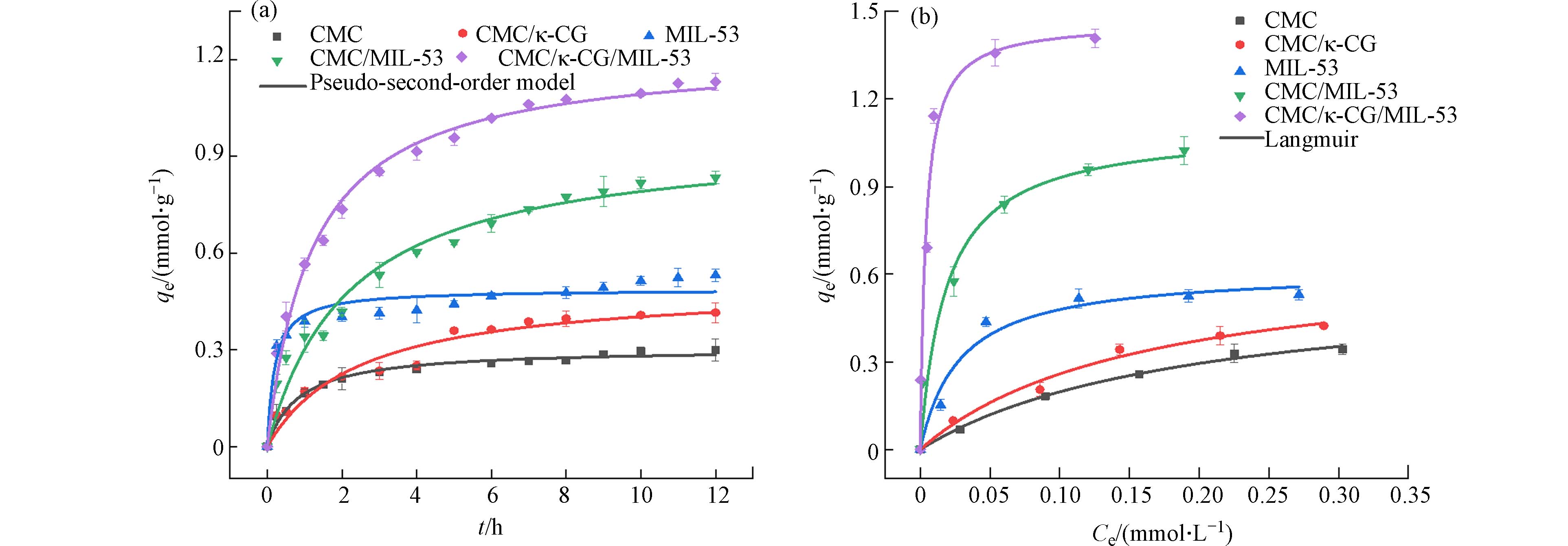
在pH=7.0条件下,吸附时间对不同材料吸附CIP的影响如图6(a)所示. 在初始2 h内,粉末状MIL-53对CIP的吸附速率较快,MIL-53比表面积大,表面有着大量的活性吸附位点,2 h时,MIL-53对CIP吸附量可达到平衡吸附量的75.55%,2 h后随着大量吸附位点被占用,进入缓慢吸附阶段,直至12 h基本达到吸附平衡. 四种气凝胶吸附速率低于MIL-53,在初始4 h吸附速率较快,CMC/MIL-53和CMC/κ-CG/MIL-53对CIP吸附量达到平衡吸附量的72.23%和80.87%,至12 h基本达到吸附平衡. 利用准一级和准二级动力学模型对CIP的吸附动力学数据进行拟合[36 − 37](图6(a)),拟合结果列于表1中. 根据表1,准二级动力学模型拟合度R2值高于准一级动力学模型,说明CIP在气凝胶上的吸附以化学吸附过程为主[37].
不同材料对CIP的等温吸附结果如图6(b)所示,随着初始浓度的增加,吸附剂对CIP的吸附量逐渐增加,直至达到平衡,进一步说明吸附过程主要是以吸附位点为驱动的化学吸附过程[37],结合不同等温模型[38 − 39]的拟合结果(表1),不同气凝胶及MIL-53对CIP的吸附均主要遵循Langmuir模型,说明其对CIP的吸附主要为单分子层化学吸附过程,根据Langmuir模型拟合结果,CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶对CIP的理论最大吸附量分别为1.105 mmol·g−1和1.464 mmol·g−1. CMC/κ-CG/MIL-53对CIP的最大吸附量大于MIL-53和CMC/κ-CG的总和,说明MIL-53和CMC/κ-CG复合后对CIP具有协同增强吸附效应,较强的静电吸引与络合作用有利于吸引CIP富集在气凝胶表面,进而促进π—π EDA作用和氢键作用的产生,上述多重作用协同提高了复合气凝胶对CIP的吸附.
-
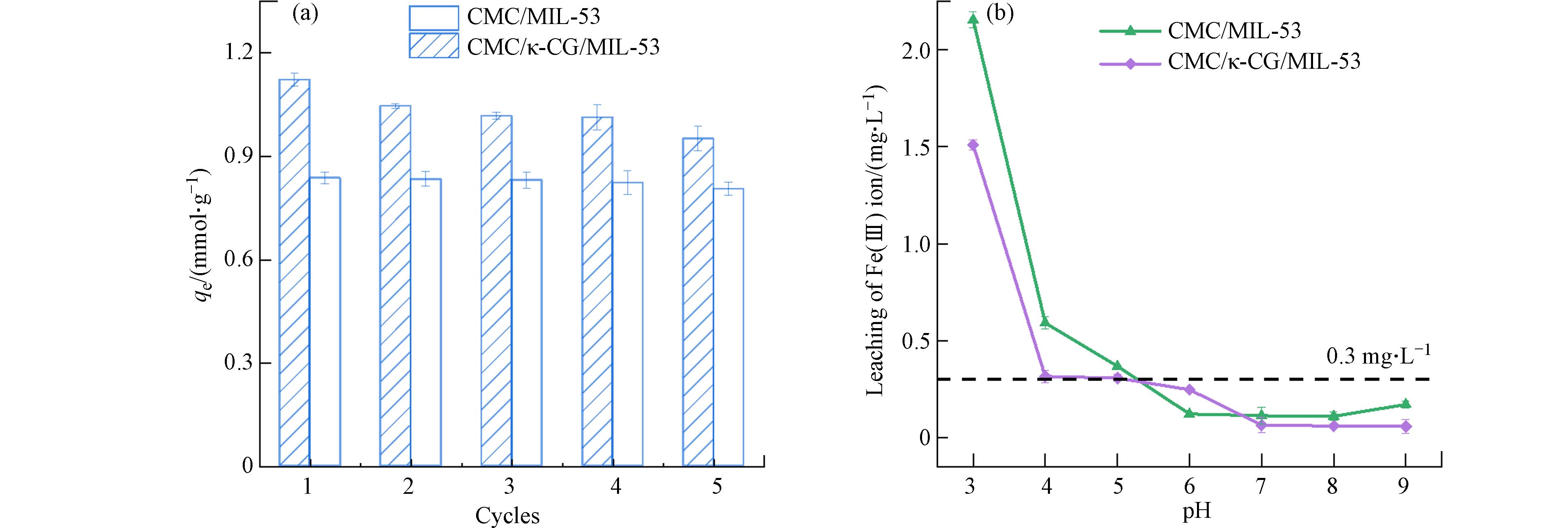
吸附剂的回收再利用性能是其在实际应用中的关键指标,大块CMC/κ-CG和CMC/κ-CG/MIL-53气凝胶可实现方便快速地从污染物溶液中分离出来,解吸再生后可直接进入下一个吸附循环. CMC/κ-CG和CMC/κ-CG/MIL-53气凝胶在中性条件下经5次连续吸附-解吸附实验结果如图7(a)所示,经过5次循环后,两种气凝胶仍然保持原有的块状结构. CMC/κ-CG对CIP的吸附量降幅小于3.8%,重复利用性优良;CMC/κ-CG/MIL-53对CIP的吸附量降幅高于CMC/κ-CG,但仍能达到第一次吸附量的85%左右,吸附量的下降可能是由于CMC/κ-CG/MIL-53和CIP结合紧密,导致解吸过程较难实现完全去除CMC/κ-CG/MIL-53气凝胶表面吸附的CIP分子,占据了少量活性位点,另一方面可能由于多次解吸导致少量MIL-53脱落[40]. 但CMC/κ-CG/MIL-53仍保持较高的吸附量,表明两种气凝胶均具有较好的重复利用性,体现出对CIP吸附去除的实际应用潜力.
-
为了评估CMC和CMC/κ-CG/MIL-53材料在使用过程中与MIL-53结合的稳定性,进一步考察了CMC/MIL-53和CMC/κ-CG/MIL-53在不同pH条件下吸附CIP后Fe3+离子浸出情况,从图7(b)可以看出,CMC/κ-CG/MIL-53的Fe3+离子浸出量总体低于CMC/MIL-53,可能是由于CMC/MIL-53气凝胶中MIL-53的负载量高于CMC/κ-CG/MIL-53;另外,CMC/κ-CG的交联互穿网络结构和富含多种功能基团的特性使其与MIL-53结合更为紧密,使结构更加稳定[41]. 在强酸性(pH=3.0)条件下Fe3+离子浸出量最高,在中性和碱性条件下,CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶的Fe3+离子浸出量均远低于酸性条件,Fe3+离子浓度(当pH≥6时)低于世界卫生组织(WHO)规定的浓度阈值(0.3 mg·L−1),说明CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶在中性或碱性条件下更为稳定,对CIP吸附量也较高(图5(a)),结合重复利用性研究结果,在中性条件下CMC/κ-CG/MIL-53吸附CIP的Fe3+离子浸出量对气凝胶的重复利用性影响较小,是一种较安全和稳定的吸附剂.
-
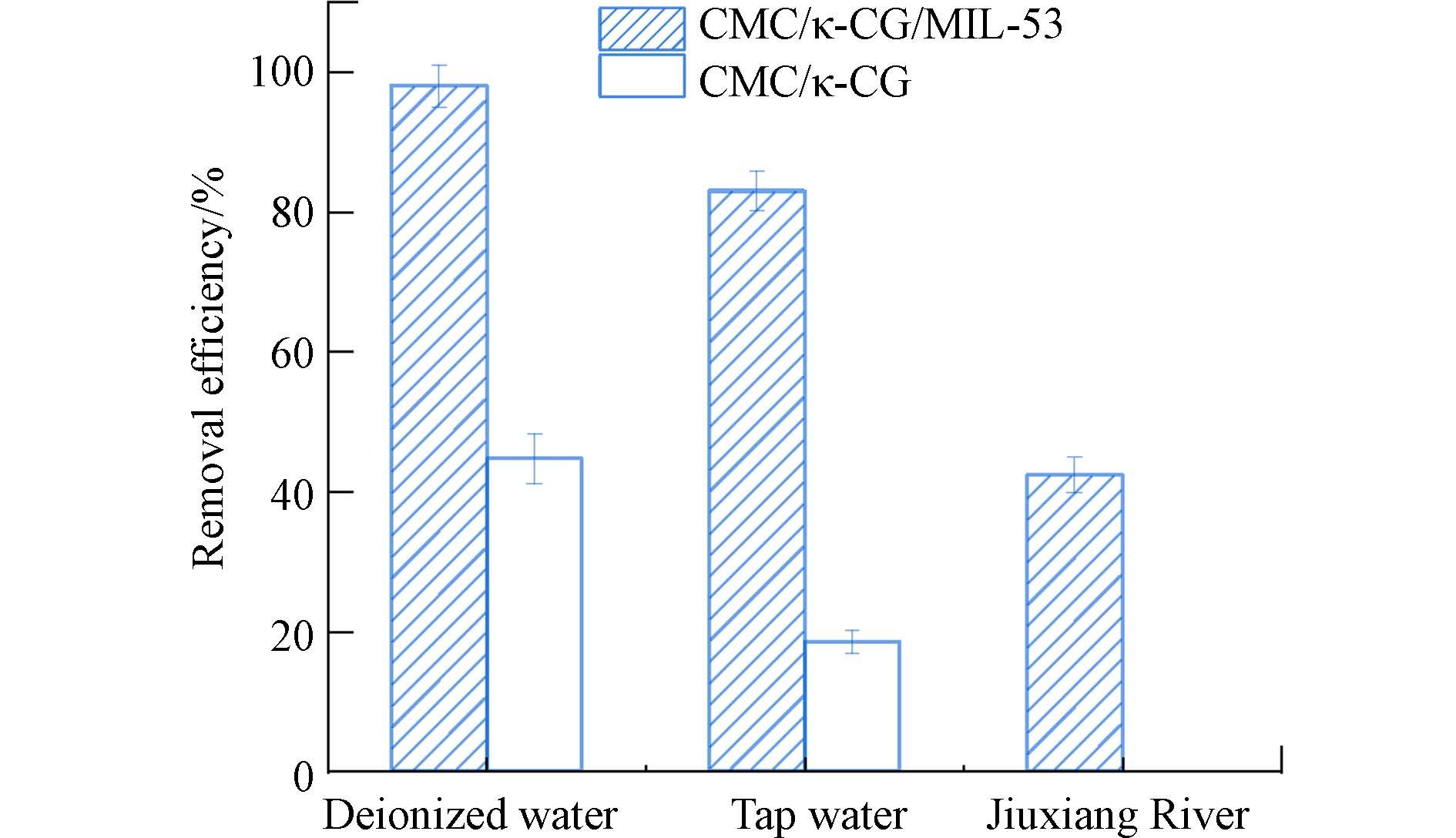
从吸附性能和Fe3+离子浸出结果来看,CMC/κ-CG/MIL-53复合气凝胶在实际水体中CIP的吸附去除上具有更好的应用潜力,进一步考查并比较了CMC/κ-CG/MIL-53和CMC/κ-CG气凝胶在去离子水、自来水和南京市九乡河水中对低浓度CIP(0.002 mmol·L−1)的去除效率,从图8可以看出,CMC/κ-CG/MIL-53气凝胶在去离子水和自来水中对CIP均有较好的去除效果,去除效率分别为97.87%和82.85%,在九乡河水中CIP的去除效率下降至56.87%,这可能是,一方面真实河水中共存无机盐除了静电屏蔽作用外,其阳离子与CMC/κ-CG/MIL-53间静电吸引作用,影响了CMC/κ-CG/MIL-53对CIP的吸附性能[42],另一方面水体中腐殖酸等天然有机物由于富含大量含氧功能基团对CMC/κ-CG/MIL-53也具有一定的竞争吸附作用[13,43]. 然而,未负载MIL-53的CMC/κ-CG对自来水和九乡河水中CIP的去除效率下降明显,对九乡河水中CIP的去除效率几乎为0,说明CMC/κ-CG负载MIL-53后,明显提高了对复杂基质中CIP的选择性吸附能力.
-
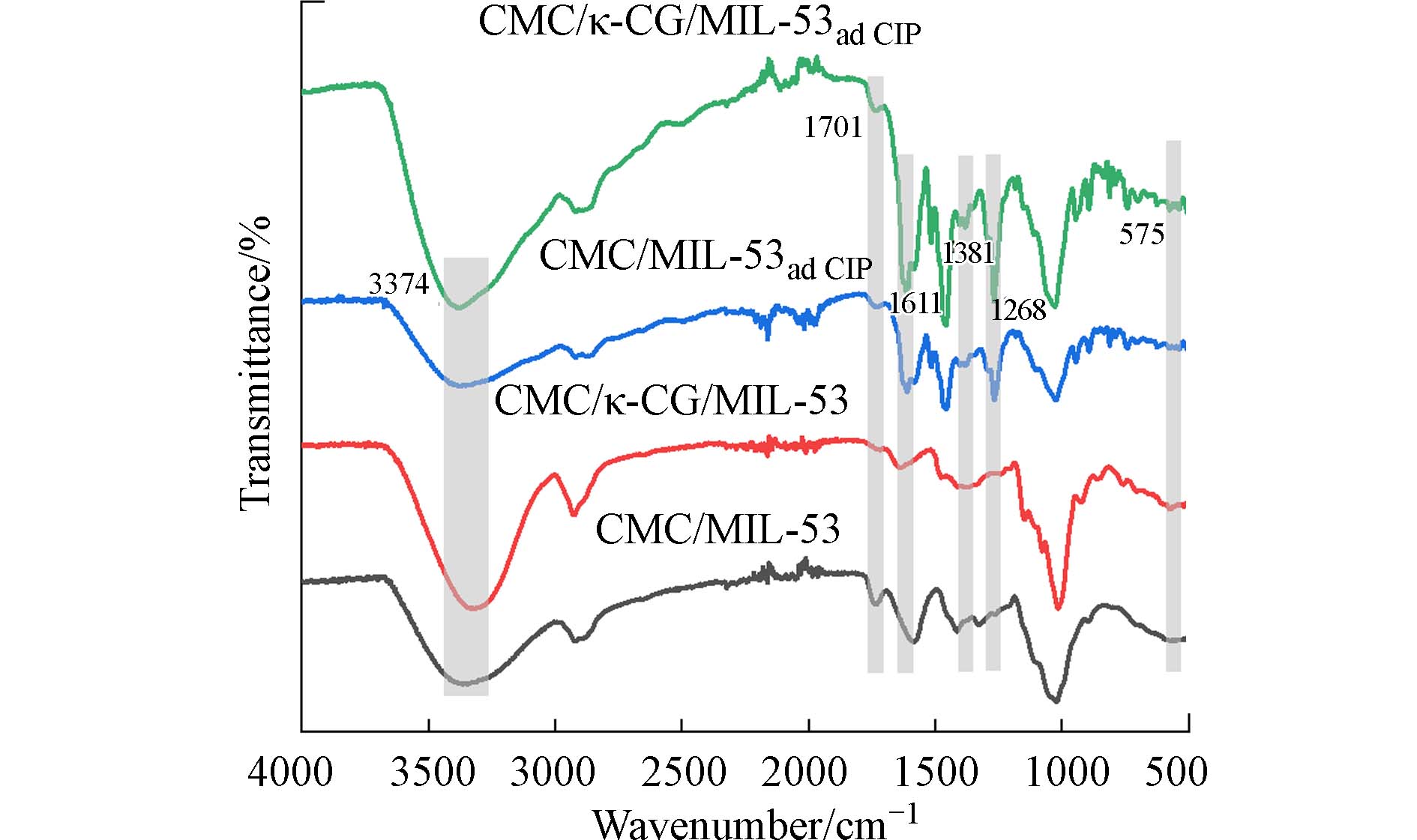
为了从分子水平上深入考察CIP在CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶上的吸附机理,进一步对比分析CIP吸附前后的复合气凝胶FTIR和XPS光谱图,如图9所示,CIP在1718、1617、1286 cm−1处的特征峰分别归属于羧基C=O的拉伸振动、酮C=O的拉伸振动以及羧基中C—O拉伸和O—H变形振动的耦合[13],在1376 cm−1处的特征峰属于哌嗪结构中质子化氨基的特征吸收峰;吸附CIP后,CMC/MIL-53和CMC/κ-CG/MIL-53气凝胶均出现以上特征峰,并且氨基特征峰发生蓝移,说明CIP的质子化氨基可能和复合气凝胶表面的阴离子基团发生静电吸附作用[31]. CMC/κ-CG/MIL-53气凝胶位于1478 cm−1的芳香环的伸缩振动峰,在吸附后红移至1456 cm−1,可能是CMC/κ-CG/MIL-53气凝胶与CIP间的π—π EDA相互作用导致的[44];此外,吸附后CMC/κ-CG/MIL-53在3316 cm−1处O—H伸缩振动峰发生蓝移,说明复合气凝胶的羟基可能与CIP的羧基及氨基形成氢键[42]. 在571 cm−1处属于MIL-53的Fe—O特征峰发生蓝移,进一步说明CMC/κ-CG/MIL-53气凝胶的Fe—O基团可能与CIP发生氢键作用或络合作用[45].
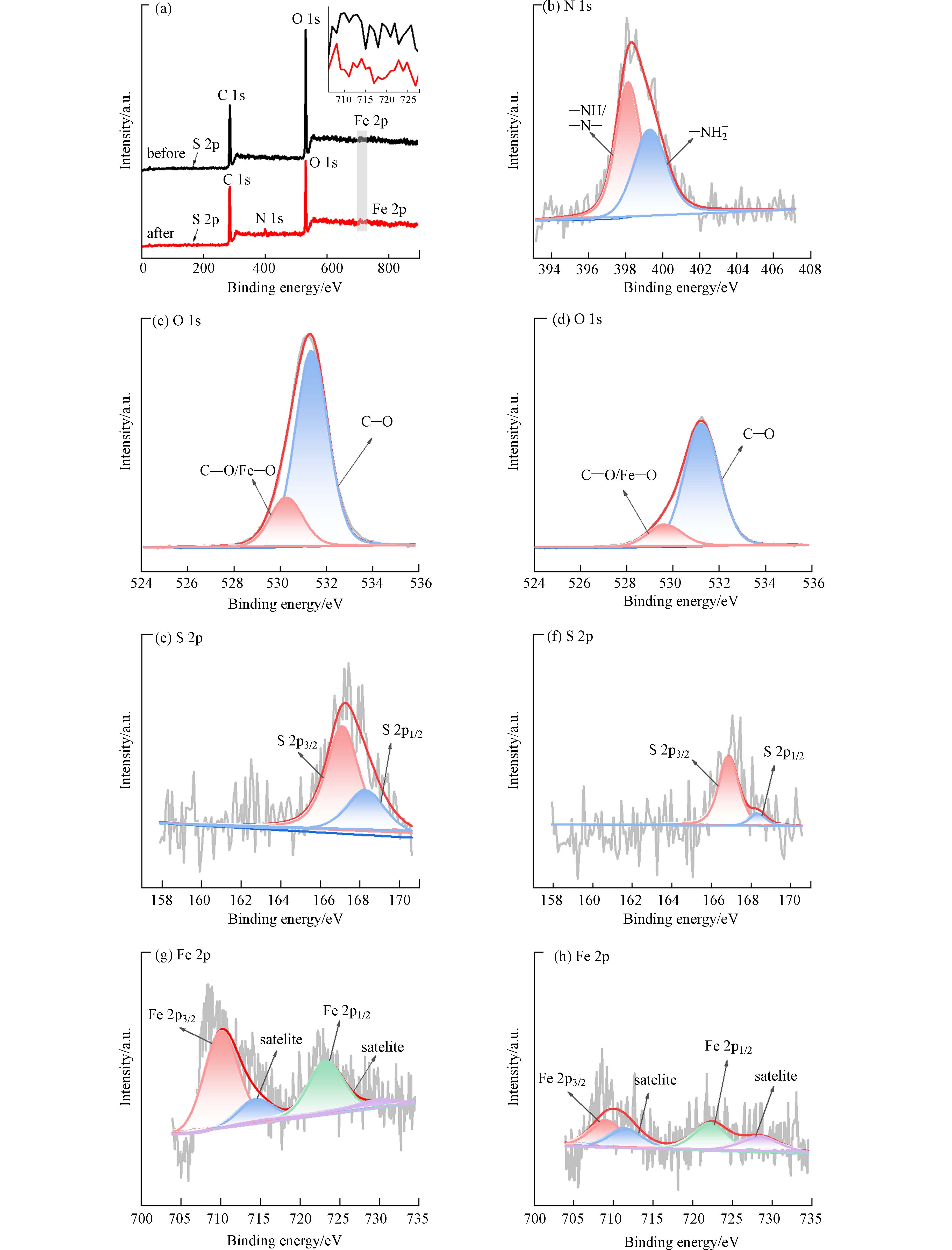
从图10(a)中CMC/κ-CG/MIL-53气凝胶吸附CIP前后的XPS谱图可以看出,CMC/κ-CG/MIL-53谱图中包含了C、O、S、Fe元素的特征峰[20];吸附CIP后出现了N 1s的特征峰,N 1s在398.14eV和399.31 eV处的特征峰可分属于—NH/—N—和—NH2+基团(图10(b))[43,46],说明CIP被有效吸附至CMC/κ-CG/MIL-53气凝胶上[47 − 48].
图10(c-d)中O 1s特征峰是两个结合能分别为530.27 eV和531.36 eV特征峰的叠合,分别归属于C=O/Fe—O和C—O基团[49],对比CMC/κ-CG/MIL-53气凝胶吸附CIP前后的O 1s特征峰发现,C=O/Fe—O特征峰强度减弱,且向低结合能处发生位移,说明C=O/Fe—O可能参与了络合作用[45]. S 2p对应结合能在167.12 eV和168.30 eV处的特征峰在吸附CIP后明显减弱,且结合能分别降至166.96 eV 和168.22 eV(图10(e-f)),可能是由于CMC/κ-CG/MIL-53气凝胶上硫酸基团与CIP氨基发生静电吸附或氢键作用[50]. Fe 2p特征峰可拟合为四个结合能分别为710.04、714.42、723.27、729.95 eV的特征峰,结合能为710.04 eV和723.27 eV的特征峰分别归属于Fe 2p3/2和Fe 2p1/2,另外两个特征峰属于Fe 2p的卫星峰[24,51]. 吸附CIP后,Fe 2p特征峰强度减弱,并向更低结合能方向移动(Fe 2p3/2和Fe 2p1/2特征峰的结合能分别降至709.14 eV和722.30 eV(图 10(g-h)),说明Fe—O基团和CIP上—COOH可能发生络合作用[51]. 根据吸附前后的FTIR和XPS光谱表征结果进一步证实了CMC/κ-CG/MIL-53对CIP的吸附是静电吸附(式(2-3))、氢键作用(式(4-7))、π—π EDA作用(式(8))及络合作用(式(9))等多重作用的结果.
-
本研究以CMC和CMC/κ-CG气凝胶为基底,利用原位合成负载MIL-53颗粒,合成了CMC/MIL-53和CMC/κ-CG/MIL-53复合气凝胶,并应用于吸附去除水体中CIP. 研究发现:
1)CMC/MIL-53与CMC/κ-CG/MIL-53在较低MIL-53负载率(17.4%和11.8%)情况下,吸附性能明显优于CMC、CMC/κ-CG和MIL-53,当pH为7.0—8.0时吸附量达到最大. 此外,由于κ-CG的引入,CMC/κ-CG/MIL-53相比于CMC/MIL-53具有更佳的吸附性能,CMC/κ-CG/MIL-53在中性条件下的理论最大吸附量可达1.464 mmol·g−1.
2)CMC/MIL-53和CMC/κ-CG/MIL-53克服了CMC和CMC/κ-CG在碱性和高离子强度条件下吸附性能明显下降的不足,这是由于通过MIL-53的引入,其吸附机制由静电吸附作用为主导转变为静电吸附、π—π EDA作用、络合作用和氢键作用等多重作用的协同贡献. 其中CMC/MIL-53和CMC/κ-CG/MIL-53的静电吸附贡献率分别为13.25%和26.39%. 其多重吸附机制也得到了吸附前后FTIR和XPS光谱表征结果的证实.
3)CMC/κ-CG/MIL-53气凝胶具有较好的重复利用性,在中性和碱性条件下,Fe3+离子浸出浓度低于WHO规定的浓度阈值. 与CMC/κ-CG相比,CMC/κ-CG/MIL-53明显提高了对实际水体中低浓度CIP的选择性吸附性能,进一步证实了CMC/κ-CG/MIL-53在实际水处理中对CIP等抗生素吸附去除具有优良的应用前景.
羧甲基纤维素/κ-卡拉胶/MIL-53复合气凝胶对水体中环丙沙星的吸附去除
Adsorptive removal of ciprofloxacin from water by carboxymethyl cellulose/κ-carrageenan/MIL-53 composite aerogel
-
摘要: 环丙沙星(CIP)是一种常见氟喹诺酮类抗生素,已广泛应用于人类和动物抗感染类疾病的治疗和预防,但其大部分以原药或代谢产物的形式流入水体环境中,研究CIP的高效去除技术对保障生态环境和人类健康具有重要意义. 本研究分别利用羧甲基纤维素(CMC)和CMC/κ-卡拉胶(κ-CG)气凝胶为载体,原位负载一种常见金属有机框架材料MIL-53,制备CMC/MIL-53和CMC/κ-CG/MIL-53复合气凝胶,并研究复合气凝胶对CIP的吸附效果和吸附机理. 相比于CMC和CMC/κ-CG气凝胶,CMC/MIL-53和CMC/κ-CG/MIL-53复合气凝胶不仅吸附量得以提高,其耐碱性及抗盐性均得到有效改善,在pH 4.0—9.0范围内和高盐浓度下对CIP均保持较好的吸附效果. CMC/MIL-53和CMC/κ-CG/MIL-53复合气凝胶对CIP的吸附均为单分子层的化学吸附过程,在中性条件下的理论最大吸附量分别为1.105 mmol·g−1和1.464 mmol·g−1. 结合表观吸附性能结果和吸附前后的FTIR和XPS光谱特征分析得出,CMC/MIL-53和CMC/κ-CG/MIL-53复合气凝胶对CIP的高效吸附是氢键、静电吸附、π—π电子供体—受体相互作用和络合作用等多重作用的结果. 在中性和碱性条件下,Fe3+离子浸出量低于世界卫生组织规定的浓度阈值,较好地解决了原粉末状MIL-53在实际水体中易流失难回收的问题. 相比于CMC/MIL-53,CMC/κ-CG/MIL-53复合气凝胶对水体中CIP具有更佳的吸附去除性能,有着更为优良的应用潜力.Abstract: Ciprofloxacin (CIP), a kind of popular fluoroquinolone antibiotics, has been widely used in the treatment and prevention of anti-infective diseases in humans and animals, but most of CIP is excreted to aqueous environment in the form of original drugs or metabolites. It is of great significance to investigate the efficient removal of CIP in water for the protection of ecological environment and human health. In the work, carboxymethyl cellulose (CMC)/MIL-53 and CMC/κ-carrageenan (κ-CG)/MIL-53 composite aerogels were prepared by using CMC and CMC/κ-CG aerogels as carriers and in situ loading of MIL-53, a popular metal-organic framework material. The performance and mechanisms of these composite aerogels on adsorptive removal of CIP were studied. CMC/MIL-53 and CMC/κ-CG/MIL-53 composite aerogels represented high adsorption capacity for CIP at pH ranging from 4.0 to 9.0 and high salt concentration, showing good both salt and alkali resistance. The adsorption of CIP on CMC/MIL-53 and CMC/κ-CG/MIL-53 composite aerogels are monolayer chemisorption process with theoretical maximum adsorption capacities of 1.105 mmol·g−1 and 1.464 mmol·g−1, respectively, at neutral condition. Combined with the results of apparent adsorption performance and the analysis of FTIR and XPS spectra before and after CIP adsorption, it can be concluded that the multi-adsorption mechanisms were involved in adsorption of CIP by these composite aerogels, including hydrogen bonding, electrostatic adsorption, π—π electron donor-acceptor interaction and complexation. Under neutral and alkaline conditions, the leaching amount of Fe3+ ions is lower than the concentration threshold specified by the World Health Organization. It effectively solves the problems of easy loss and difficult recovery of the original powdered MIL-53 in water. In comparison to CMC/MIL-53, CMC/κ-CG/MIL-53 composite aerogel has higher performance in CIP removal and better application potential in actual water.
-
Key words:
- aerogel /
- carboxymethyl cellulose /
- κ-carrageenan /
- MIL-53 /
- ciprofloxacin /
- adsorption performance /
- adsorption mechanism
-

-
图 2 (a) CMC气凝胶,(b) CMC/κ-CG气凝胶,(c) MIL-53,(d)和(e) CMC/MIL-53气凝胶,(f)和(g) CMC/κ-CG/MIL-53气凝胶FESEM图,和 (h) 四种气凝胶照片
Figure 2. (a-g) FESEM micrographs of various adsorbents (a) CMC aerogel, (b) CMC/κ-CG aerogel, (c) MIL-53, (d) and (e) CMC/MIL-53 aerogel, (f) and (g) CMC/κ-CG/MIL-53 aerogel respectively; (h) Snapshots of four aerogels
图 5 (a)不同pH条件下各种材料吸附CIP的影响和CIP结构形态分布,(b) 在pH为7.0,CIP初始浓度为0.20 mmol·L−1条件下, NaCl共存对各种材料吸附CIP的影响
Figure 5. (a) Effects of pH on the CIP uptakes of various materials and the distributions of the various CIP species under different pH levels. (b) Effects of coexisting NaCl on various materials for adsorption of CIP, at pH 7.0, with the initial CIP concentration of 0.20 mmol·L−1.
图 7 (a) CMC/κ-CG和CMC/κ-CG/MIL-53气凝胶吸附CIP的重复利用性,(b) 在不同pH条件下CMC/MIL-53和CMC/κ-CG/MIL-53吸附CIP后的Fe3+离子浸出量变化
Figure 7. (a) Recyclability of CMC/κ-CG and CMC/κ-CG/MIL-53 aerogel for adsorption of CIP; (b) The variation of leaching of Fe3+ ions after CIP adsorption by CMC/MIL-53 and CMC/κ-CG/MIL-53 under different pH conditions.
表 1 不同吸附剂吸附CIP的吸附动力学和吸附等温模型拟合参数
Table 1. Fitting parameters of the adsorption kinetics and isotherms models for various adsorbents in adsorption of CIP
吸附剂
Adsorbentsqmax,exp/
(mmol·g−1)准一级动力学模型
Pseudo-first-order model准二级动力学模型
Pseudo-second-order modelqe/(mmol·g−1) k1/min−1 R2 qe/(mmol·g−1) K2/[g·(mmol·min)−1] R2 CMC 0.300 0.272 0.871 0.945 0.304 3.865 0.983 CMC/κ-CG 0.415 0.414 0.353 0.936 0.502 0.807 0.952 MIL-53 0.532 0.463 3.381 0.876 0.488 10.369 0.934 CMC/MIL-53 0.834 0.797 0.402 0.945 0.965 0.473 0.967 CMC/κ-CG/MIL-53 1.132 1.068 0.646 0.963 1.224 0.681 0.991 吸附剂
Adsorbentsqmax,exp/
(mmol·g−1)朗缪尔模型
Langmuir model弗兰德里希模型
Freundlich modelqm,cal/(mmol·g−1) b/(L·mmol−1) R2 Kf n R2 CMC 0.342 0.582 5.128 0.994 0.741 1.687 0.958 CMC/κ-CG 0.424 0.670 6.280 0.985 0.883 1.812 0.948 MIL-53 0.530 0.614 35.434 0.964 0.843 3.525 0.694 CMC/MIL-53 1.024 1.105 53.433 0.973 1.756 3.378 0.967 CMC/κ-CG/MIL-53 1.408 1.464 255.323 0.974 2.400 4.639 0.819 -
[1] YANG Q, GAO Y, KE J, et al. Antibiotics: An overview on the environmental occurrence, toxicity, degradation, and removal methods[J]. Bioengineered, 2021, 12(1): 7376-7416. doi: 10.1080/21655979.2021.1974657 [2] THAI V A, DANG V D, THUY N T, et al. Fluoroquinolones: Fate, effects on the environment and selected removal methods[J]. Journal of Cleaner Production, 2023, 418: 137762. doi: 10.1016/j.jclepro.2023.137762 [3] CUPRYS A, PULICHARLA R, BRAR S K, et al. , Fluoroquinolones metal complexation and its environmental impacts[J]. Coordination Chemistry Reviews, 2018, 376: 46-61. doi: 10.1016/j.ccr.2018.05.019 [4] REDGRAVE L S, SUTTON S B, WEBBER M A, et al. Fluoroquinolone resistance: mechanisms, impact on bacteria, and role in evolutionary success[J]. Trends Microbiol, 2014, 22(8): 438-445. doi: 10.1016/j.tim.2014.04.007 [5] BEN W, ZHU B, YUAN X, et al. Occurrence, removal and risk of organic micropollutants in wastewater treatment plants across China: Comparison of wastewater treatment processes[J]. Water Research, 2018, 130: 38-46. doi: 10.1016/j.watres.2017.11.057 [6] YAO L, WANG Y, TONG L, et al. Occurrence and risk assessment of antibiotics in surface water and groundwater from different depths of aquifers: A case study at Jianghan Plain, central China[J]. Ecotoxicology and Environmental Safety, 2017, 135: 236-242. doi: 10.1016/j.ecoenv.2016.10.006 [7] CONKLE J L, LATTAO C, WHITE J R, et al. Competitive sorption and desorption behavior for three fluoroquinolone antibiotics in a wastewater treatment wetland soil[J]. Chemosphere, 2010, 80(11): 1353-1359. doi: 10.1016/j.chemosphere.2010.06.012 [8] ALEXANDER J T, HAI F I, AL-ABOUD T M. Chemical coagulation-based processes for trace organic contaminant removal: Current state and future potential[J]. Journal of Environmental Management, 2012, 111: 195-207. [9] NASROLLAHI N, Vatanpour V, KHATAEE A. Removal of antibiotics from wastewaters by membrane technology: Limitations, successes, and future improvements [J]. Science of the Total Environment, 2022, 838(Pt 1): 156010. [10] JIANG Y, RAN J, MAO K, et al. Recent progress in Fenton/Fenton-like reactions for the removal of antibiotics in aqueous environments[J]. Ecotoxicolgy and Environmental Safety, 2022, 236: 113464. doi: 10.1016/j.ecoenv.2022.113464 [11] AHMED M B, ZHOU J L, NGO H H, et al. Adsorptive removal of antibiotics from water and wastewater: Progress and challenges[J]. Science of the Total Environment, 2015, 532: 112-126. doi: 10.1016/j.scitotenv.2015.05.130 [12] GANESAMOORTHY R, VADIVEL V K, KUMAR R, et al. Aerogels for water treatment: A review[J]. Journal of Cleaner Production, 2021, 329: 129713. doi: 10.1016/j.jclepro.2021.129713 [13] LI N, GAO B, YANG R, et al. Simple fabrication of carboxymethyl cellulose and κ-carrageenan composite aerogel with efficient performance in removal of fluoroquinolone antibiotics from water[J]. Frontiers of Environmental Science and Engineering, 2022, 16(10): 133. doi: 10.1007/s11783-022-1568-x [14] JIA J, XU F, LONG Z, et al. Metal-organic framework MIL-53(Fe) for highly selective and ultrasensitive direct sensing of MeHg+[J]. Chemical Communications, 2013, 49(41): 4670-4672. doi: 10.1039/c3cc40821c [15] SALGUEIRO A M, DANIEL-DA-SILVA A L, GIRAO A V, et al. Unusual dye adsorption behavior of κ-carrageenan coated superparamagnetic nanoparticles[J]. Chemical Engineering Journal, 2013, 229: 276-284. doi: 10.1016/j.cej.2013.06.015 [16] LI X, GUO W L, LIU Z H, et al. Fe-based MOFs for efficient adsorption and degradation of acid orange 7 in aqueous solution via persulfate activation[J]. Applied Surface Science, 2016, 369: 130-136. doi: 10.1016/j.apsusc.2016.02.037 [17] MA X, XIONG Y, LIU Y S, et al. When MOFs meet wood: From opportunities toward applications[J]. Chemistry, 2022, 8(9): 2342-2361. doi: 10.1016/j.chempr.2022.06.016 [18] SHAO B, HAN Z, PANG R, et al. The crystalline structure transition and hydrogen bonds shift determining enhanced enzymatic digestibility of cellulose treated by ultrasonication[J]. Science of the Total Environment, 2023, 876: 162631. doi: 10.1016/j.scitotenv.2023.162631 [19] LIU J, HAO D D, SUN H W, et al. Integration of MIL-101-NH2 into cellulosic foams for efficient Cr(VI) reduction under visible light[J]. Industrial and Engineering Chemistry Research, 2021, 60(33): 12220-12227. doi: 10.1021/acs.iecr.1c01777 [20] ABDPOUR S, KOWSARI E, MOGHADDAM M R A. Synthesis of MIL-100(Fe)@MIL-53(Fe) as a novel hybrid photocatalyst and evaluation photocatalytic and photoelectrochemical performance under visible light irradiation[J]. Journal of Solid State Chemistry, 2018, 262: 172-180. doi: 10.1016/j.jssc.2018.03.018 [21] AMALY N, PANDEY P, EL-MOGHAZY A Y, et al. Cationic microcrystalline cellulose-Montmorillonite composite aerogel for preconcentration of inorganic anions from dairy wastewater[J]. Talanta, 2022, 242: 123281. doi: 10.1016/j.talanta.2022.123281 [22] REN W, GAO J K, LEI C, et al. Recyclable metal-organic framework/cellulose aerogels for activating peroxymonosulfate to degrade organic pollutants[J]. Chemical Engineering Journal, 2018, 349: 766-774. doi: 10.1016/j.cej.2018.05.143 [23] SUN G, LIANG T Q, TAN W Y, et al. Rheological behaviors and physical properties of plasticized hydrogel films developed from κ-carrageenan incorporating hydroxypropyl methylcellulose[J]. Food Hydrocolloids, 2018, 85: 61-68. doi: 10.1016/j.foodhyd.2018.07.002 [24] YUAN Z, CHEN Y L, QIU C P, et al. Simple ultrasonic integration of shapeable, rebuildable, and multifunctional MIL-53(Fe)@cellulose composite for remediation of aqueous contaminants[J]. International Journal of Biological Macromolecules, 2023, 249: 126118. doi: 10.1016/j.ijbiomac.2023.126118 [25] KONG Y, ZHUANG Y, HAN K, et al. Enhanced tetracycline adsorption using alginate-graphene-ZIF67 aerogel[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2020, 588: 124360. doi: 10.1016/j.colsurfa.2019.124360 [26] CHONG S, THIELE G, KIM J. Excavating hidden adsorption sites in metal-organic frameworks using rational defect engineering[J]. Nature Communications, 2017, 8(1): 1539. doi: 10.1038/s41467-017-01478-4 [27] DONG D, GUO H, LI G, et al. Assembling hollow carbon sphere-graphene polylithic aerogels for thermoelectric cells[J]. Nano Energy, 2017, 39: 470-477. doi: 10.1016/j.nanoen.2017.07.029 [28] MEADOR M A, MALOW E J, SILVA R, et al. Mechanically strong, flexible polyimide aerogels cross-linked with aromatic triamine[J]. ACS Applied Materials and Interfaces, 2012, 4(2): 536-544. doi: 10.1021/am2014635 [29] ZHANG Z, CHEN X Y, TAN Y, et al. Preparation of millimeter-scale MIL-53(Fe)@ polyethersulfone balls to optimize photo-Fenton process[J]. Chemical Engineering Journal, 2022, 441: 135881. doi: 10.1016/j.cej.2022.135881 [30] AWAD A M, SHAIKH S M R, JALAB R, et al. Adsorption of organic pollutants by natural and modified clays: A comprehensive review[J]. Separation and Purification Technology, 2019, 228: 115719. doi: 10.1016/j.seppur.2019.115719 [31] WU Q, LI Z, HONG H, et al. Adsorption and intercalation of ciprofloxacin on montmorillonite[J]. Applied Clay Science, 2010, 50: 204-211. doi: 10.1016/j.clay.2010.08.001 [32] 常慊慊, 高博强, 刘波, 等. 单宁酸-钛复合吸附剂的制备及其对氟喹诺酮类抗生素的吸附去除研究[J]. 环境化学, 2022, 41(7): 2180-2192. doi: 10.7524/j.issn.0254-6108.2022012005 CHANG Q Q, GAO B Q, LIU B, et al. Preparation of tannic acid-titanium composite adsorbent and its adsorption performance and mechanisms in removal of fluoroquinolone antibiotics[J]. Environmental Chemistry, 2022, 41(7): 2180-2192(in Chinese). doi: 10.7524/j.issn.0254-6108.2022012005
[33] BEIRANVAND M, FARHADI S, MOHAMMADI-GHOLAMI A. Adsorptive removal of tetracycline and ciprofloxacin drugs from water by using a magnetic rod-like hydroxyapatite and MIL-101(Fe) metal-organic framework nanocomposite[J]. RSC Advances, 2022, 12: 34438-34453. doi: 10.1039/D2RA06213E [34] GHANI A A, DEVARAYAPALLI K C, KIM B, et al. Sodium-alginate-laden MXene and MOF systems and their composite hydrogel beads for batch and fixed-bed adsorption of naproxen with electrochemical regeneration[J]. Carbohydrate Polymers, 2023, 318: 121098. doi: 10.1016/j.carbpol.2023.121098 [35] WANG Y, XIONG Y, WANG J, et al. Ultrasonic-assisted fabrication of montmorillonite-lignin hybrid hydrogel: Highly efficient swelling behaviors and super-sorbent for dye removal from wastewater[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2017, 520: 903-913. doi: 10.1016/j.colsurfa.2017.02.050 [36] HO Y S, MCKAY G. Sorption of dye from aqueous solution by peat[J]. Chemical Engineering Journal, 1998, 70(2): 115-124. doi: 10.1016/S0923-0467(98)00076-1 [37] LAGERGREN S. About the theory of so-called sorption of soluble substances[J]. Kungliga Svenska Vetenskapsakademiens Handlingar, 1989, 24: 1-39. [38] LANGMUIR I. The adsorption of gases on plane surfaces of glass, mica and platinum[J]. Journal of the American Chemical Society, 1918, 40(9): 1361-1403. doi: 10.1021/ja02242a004 [39] FREUNDLICH H M F. Over the adsorption in solution[J]. Journal of Physical Chemistry, 1906, 57: 385-470. [40] CHATTERJEE A, JANA A K, BASU J K. Silica supported binary metal organic framework for removing organic dye involving combined effect of adsorption followed by photocatalytic degradation[J]. Materials Research Bulletin, 2021, 138: 111227. doi: 10.1016/j.materresbull.2021.111227 [41] WANG S, XU Y, FU R, et al. Rational construction of hierarchically porous Fe-Co/N-doped carbon/rGO composites for broadband microwave absorption[J]. Nano-micro Letters, 2019, 11(1): 76. doi: 10.1007/s40820-019-0307-8 [42] LI N, TAO K, XIA W, et al. A novel cellulose/lignin/montmorillonite ternary hybrid aerogel for efficiently adsorptive removal of antibiotics from water[J]. Chemical Engineering Journal, 2023, 466: 143265. doi: 10.1016/j.cej.2023.143265 [43] GAO B, CHANG Q, CAI J, et al. Removal of fluoroquinolone antibiotics using actinia-shaped lignin-based adsorbents: Role of the length and distribution of branched-chains[J]. Journal of Hazardous Materials, 2021, 403: 123603. doi: 10.1016/j.jhazmat.2020.123603 [44] TAO K, GAO B, LI N, et al. Efficient adsorption of chloroquine phosphate by a novel sodium alginate/tannic acid double-network hydrogel in a wide pH range[J]. Science of the Total Environment, 2024, 912: 168740. doi: 10.1016/j.scitotenv.2023.168740 [45] GUO X, KANG C F, HUANG H L, et al. Exploration of functional MOFs for efficient removal of fluoroquinolone antibiotics from water[J]. Microporous and Mesoporous Materials, 2019, 286: 84-91. doi: 10.1016/j.micromeso.2019.05.025 [46] ZHANG H, DANG Q, LIU C, et al. Fabrication of methyl acrylate and tetraethylenepentamine grafted magnetic chitosan microparticles for capture of Cd(II) from aqueous solutions[J]. Joural of Hazardous Materials, 2019, 366: 346-357. doi: 10.1016/j.jhazmat.2018.12.006 [47] ZHENG Y, THAVORN-AMORNSRI T, PEREIRA M F R, et al. Kapok fiber oriented-polyaniline nanofibers for efficient Cr(VI) removal[J]. Chemical Engineering Journal, 2012, 191: 154-161. doi: 10.1016/j.cej.2012.02.088 [48] MA J, JIANG Z, CAO J, et al. Coadsorption behavior and mechanism of ciprofloxacin and Cu(II) on graphene hydrogel wetted surface[J]. Chemical Engineering Journal, 2020, 380: 122387. doi: 10.1016/j.cej.2019.122387 [49] YANG Z, XU X, LEI C, et al. MIL-53(Fe)-graphene nanocomposites: Efficient visible-light photocatalysts for the selective oxidation of alcohols[J]. Applied Catalysis B: Environmental, 2016, 198: 112-123. doi: 10.1016/j.apcatb.2016.05.041 [50] GAO Y, LI Y, ZHANG L, et al. Adsorption and removal of tetracycline antibiotics from aqueous solution by graphene oxide[J]. Journal of Colloid and Interface Science, 2012, 368: 540-546. doi: 10.1016/j.jcis.2011.11.015 [51] YANG T, YU D, WANG D, et al. Accelerating Fe(Ⅲ)/Fe(Ⅱ) cycle via Fe(Ⅱ) substitution for enhancing Fenton-like performance of Fe-MOFs[J]. Applied Catalysis B: Environmental, 2021, 286: 119859. doi: 10.1016/j.apcatb.2020.119859 -



 下载:
下载: