-
阻燃剂(flame retardant,FR)是降低聚合物可燃性的重要助剂,按使用方法分为添加型和反应型;前者通过机械混合方式加入,与聚合物无化学键约束,容易释放进入环境;后者则作为单体与聚合物发生化学反应,使聚合物本身含有阻燃成分. FRs按化学组成可分为卤系、磷系、氮系、金属和矿物质类等[1],其中卤系FRs具有阻燃效果好、添加量少、对材料性能影响小等优势,一直处于市场领先地位, 尤其是溴系阻燃剂(brominated flame retardants, BFRs). 但近年来大量研究表明,多溴联苯醚(polybrominated diphenyl ethers, PBDEs)、六溴环十二烷(hexabromocyclododecanes, HBCDs)等典型BFRs在环境中普遍存在,并表现出持久性、长距离迁移性、生物富集性和毒性,还可生成毒性更强的羟基/甲氧基代谢物以及溴代二噁英/呋喃,被先后列入斯德哥尔摩公约新增持久性有机污染物(persistent organic pollutants, POPs)清单,在世界范围内逐步禁用. 与此同时,其替代品的用量呈现显著增长,相应安全性和风险已成为环境领域新一轮的研究热点.
有机磷酸酯(organophosphate esters, OPEs)主要通过凝聚相阻燃,烟和有毒/腐蚀气体生成量少,被认为是BFRs的理想代替品. 近年来随着BFRs被逐步禁用,OPEs的全球用量持续攀升:2011年达50余万吨,2015年预估为68万吨[1]. 我国的OPEs产量也预计以15%/年的速度持续增长,2007年为7万余吨[2],2011年达10万吨[3]. 但多数OPEs为添加型助剂,极易通过挥发、浸出、产品使用磨损等过程释放进入环境[4]. 目前OPEs已在全球包括两极在内的空气、水体、土壤和生物体中广泛检出[5-10],并表现出环境持久性、长距离迁移性和生物可利用性,其环境行为归趋和风险迅速引起国内外的广泛关注[11]. OPEs种类繁多且来源复杂,化合物之间性质差异大(lg KOW=−0.65—9.49),目前尚未有全面分析环境中可能存在的OPEs及代谢产物的标准方法. 多数研究仅针对少数典型OPEs的污染水平和分布特征,对其环境行为的研究尚不够深入. 本文检索了近15年的相关文献,综述了OPEs的污染现状及其环境行为、分析方法、毒性等的研究进展,并针对目前存在的问题提出今后的主要研究方向.
-
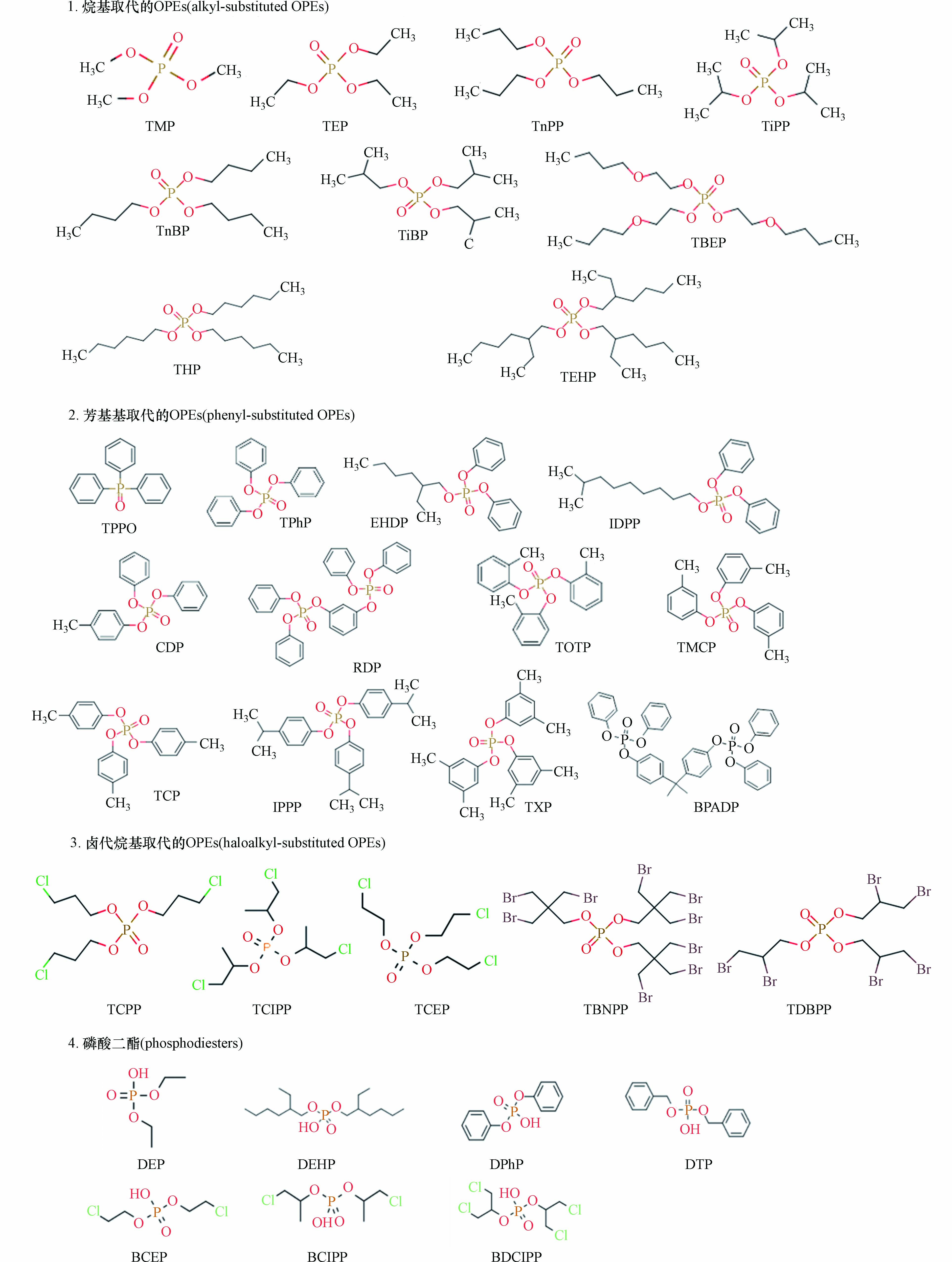
目前报道的 OPEs 及代表性二酯的结构如图1所示. OPEs由烷基、苯基或卤代烷基取代磷酸上的氢形成,取代基不同,其物化性质也存在很大差异.
表1列出了已报道OPEs的常用物化性质参数. 其中磷酸三甲酯(trimethyl phosphate, TMP)分子量最小(140.075),沸点最低(197 ℃),极性和挥发性均最强(lg KOW =−0.65, 25 ℃蒸气压为55.5 Pa );而磷酸三(2-乙基己基)酯(tris(2-ethylhexyl)phosphate, TEHP)则极难溶于水(1.46×10−5 mg·L−1; lg KOW =9.49),且沸点较高(449.7 ℃),不易挥发(25 ℃蒸气压为6.07×10−7 mm Hg).
根据取代基是否含有卤原子可将OPEs分为卤代OPEs和非卤代OPEs. 其中,卤代烷基取代的OPEs主要用作阻燃剂,如磷酸三(2-氯乙基)酯(tris(2-chloroethyl)phosphate, TCEP)、磷酸三(2-氯丙基)酯(tris(3-chloropropyl)phosphate, TCPP)、磷酸三(1,3-二氯-2-丙基)酯(tris(1,3-dichloro-2-propyl)phosphate, TDCIPP)等. 这些OPEs中的氯原子可使可燃气体失去H+和OH·自由基,从而减缓燃烧速率,阻止火势扩散,常被用于聚氨酯泡沫等材料的阻燃. 除卤代OPEs外,一些烷基或苯基取代的非卤代OPEs也具有阻燃性能,其被加热后可形成强脱水剂聚偏磷酸,使得聚合物表面迅速脱水形成炭化层,隔绝氧气和材料表面接触,从而达到阻燃目的[12].
除阻燃性能外,烷/苯基取代的OPEs还表现出优良的增塑和润滑效果,是常用的增塑剂、去泡剂、液压剂等,被广泛用于建筑材料、电子电器、塑料、家装饰品、纺织品、地板蜡、油漆、涂料等行业. 如磷酸三苯酯(triphenyl phosphate, TPhP)是不饱和聚酯树脂和聚氯乙烯常用的增塑剂[13];磷酸三丁氧乙酯(tris(butoxyethyl)phosphate, TBEP)、TPhP 和磷酸三正丁酯(tri-n−butyl phosphate, TnBP)可充当液压液、润滑液、转化液、机油等的极压剂和抗磨剂;TnBP 可用作去泡剂和核燃料萃取剂等.
-
水体是目前开展OPEs研究最多的环境介质. 已有研究表明,环境水体中的OPEs主要来源于工业/城市污水、垃圾渗滤液、干湿沉降、地表径流传输、城市保洁和雨水冲刷等[14−16]. 多数OPEs水溶性较强(表1),地表水浓度在几ng·L−1到几μg·L−1之间,在污水中浓度可达数十μg·L−1,在水体沉积物中的浓度一般为几到数百ng·g−1,污水处理厂活性污泥中的OPEs可高达数百ng·g−1到数百μg·g−1.
-
污水中OPEs的浓度和组成与其用途用量、理化性质、样品类型和来源密切相关:生活污水和工业污水中的优势OPEs略有不同,不同地区/国家的样品数据及其中相同OPEs的污水-污泥分配比例均存在显著差异[17].
现有研究表明,生活污水中丰度较高的OPEs有TBEP、TCPP、TCEP、TnBP等,浓度在几百ng·L−1到数十μg·L−1. Pang等[18]对河南24家污水处理厂(1家纯工业污水,其余为纯生活污水或混合污水)的样品进行了分析,其中OPEs的总浓度在38.6—508 ng·L−1范围内,以TBEP、TCEP、TCPP和TnBP为主. Gao等[19]分析了2008—2014年北京8家污水处理厂(包括生活和工业污水)污泥中的OPEs,发现TEHP、磷酸三对甲苯酯(tri-p−cresyl phosphate, TCP)和TBEP是优势污染物,检出率100%,平均浓度分别为232、137、90 ng·g−1,此外,强极性的TMP在污泥中的平均浓度也达到了1.2 ng·g−1. Zeng等[20]研究了珠三角一生活污水处理厂脱水污泥中的OPEs,发现TnBP、TBEP和TPhP的含量最高,浓度分别为7.1—804.9 ng·g−1、25.1—783.7 ng·g−1和未检出(n.d.)—656.7 ng·g−1.
对于工业污水,孙佳薇等[21]发现TDCIPP在电子厂和汽车部件厂污水进水中占绝对主导地位(>90%),浓度在73.76—222.65 μg·L−1之间,而TnBP和TBEP则是相应污泥中的主要成分,浓度在n.d.—300 μg·g−1. 赵赛等[22]分析了合肥市电子电器、汽车部件、医药等污水处理厂进出水中的OPEs,其中TCEP和TCPP两种氯代OPEs在进水中占比达79%,浓度分别为546.69 ng·L−1和324.42 ng·L−1,而TBEP、TEHP和TnBP等烷基OPEs在进水中的比例只占19%. 同样是对电子电器厂污水的研究,Xu等[23]的分析结果显示进水中OPEs的总浓度为65.8—2842 ng·L−1,氯代OPEs的丰度均较高,这与其它研究相似,但TDCIPP浓度仅为7.6 ng·L−1. 由此可见,氯代OPEs是电子电器工业污水中的特征污染物,这与其主要用作阻燃剂有关. Xu等[23]还发现油漆涂料污水中TPhP的浓度最高,纺织污水中TnBP的丰度最高,而纸板纸箱污水中磷酸三(2-氯异丙基)酯(tris(1-chloro-2-propanyl)phosphate, TCIPP)和TPhP的浓度是所有污水样品中最高的,分别为638 ng·L−1和290 ng·L−1.
一般认为,烷基和苯基取代的OPEs在常规污水处理过程中可被有效去除,而氯代OPEs的去除率较低. 但实际研究结果并非如此:并非所有烷基/苯基取代OPEs都能被有效去除,也并非所有氯代OPEs的去除率都偏低,OPEs的去除率受污水处理工艺、pH等因素影响. 孙佳薇等[21]对比了8个污水处理厂(7个为厌氧-缺氧-好氧(anaerobic-anoxic-oxic, A2/O)工艺,1个为氧化沟)进出水中OPEs的浓度,发现多数污水厂对TCEP、TCPP和TDCIPP的去除率<50%,但其中3个采用A2/O工艺的污水厂对TDCIPP的去除率>87%,甚至可达99%;此外8个污水厂对优势TnBP的去除率均不理想,其中4个去除率<65%;大部分污水厂对TBEP的去除率均>89%,但有2个污水厂的TBEP去除率很低,仅为8%和44%,这两个污水厂对其它OPEs的去除率也偏低(8%—87%). 赵赛等[22]也发现,经过厌氧池、氧化沟等处理工艺后,大部分烷基和苯基取代OPEs的去除率可>70%,但TnBP的去除率只有62%;氯代OPEs中TCEP的去除率为29%,而TCPP和TDCIPP的出水浓度比进水浓度还高,作者推测可能是输水管道中存在氯代OPEs释放所致. Xu等[23]的出水数据也表明,部分污水厂对TnBP的去除率不佳,但TCIPP的去除率却可达到99%,而其它含氯OPEs的出水浓度高于进水浓度. 由此可见,虽然同样是A2/O工艺,但不同污水厂对同种OPEs的去除率却存在很大差别,说明还有其它影响OPEs去除率的关键因有待于进一步深入研究.
国外污水厂的研究结果也呈现类似规律. Woudneh等[24]研究了加拿大生活污水处理厂进出水中的13种OPEs,发现进水中的OPEs以TBEP、TnBP和TCEP为主,浓度分别为3293、747、598 ng·L−1,经过生化处理后浓度分别下降为547、581、133 ng·L−1;对于氯代OPEs,TCPP的出水浓度大于进水浓度,TDCIPP的进出水含量相同,这与赵赛等[22]的研究结果相似;此外污泥中TBEP的浓度最高(达1069 ng·g−1,占总OPEs的50%以上),其次是TCPP(196 ng·g−1)和TnBP(174 ng·g−1). Kim等[25]发现美国纽约州一个生活污水厂样品中的TBEP浓度最高(69500 ng·L−1),其次为TCIPP(14500 ng·L−1);3种氯代OPEs(TCIPP、TCEP和TDCIPP)和2种烷基OPEs(TiBP和TnBP)在初级和次级出水中的去除率均为负值(即出水浓度高于进水浓度),作者认为这可能与污染物物化性质和微生物利用率低有关,但没有进一步解释. Schreder[15]也发现氯代OPEs去除率出现负值的现象.
-
工业和生活污水排放已被证实是地表水体中OPEs的最主要来源[16],由于不同地区的工业/污水处理程度、排放结构等存在差异,其地表水体中OPEs的污染浓度、种类、组成和空间分布也不尽相同,其中地表水中检出率较高的OPEs主要是难降解的氯代OPEs、TBEP、TEP、TnBP等,而沉积物中丰度较高的OPEs为亲脂性强的TEHP和TPhP.
在我国,Wang等[26]研究了环渤海地区40条河流水体中11种OPEs和三苯基氧膦(triphenylphosphine oxide, TPPO)的时空分布,发现TCPP、TCEP、TDCPP等氯代OPEs占OPEs总量的69%—99%,说明华北地区生产/使用的OPEs以氯代OPEs为主,OPEs合成中间体TPPO在样品中浓度也较高,为0.7—5852 ng·L−1,应引起关注. 陈玫宏等[27]发现,太湖水中的OPEs以TEP和TCPP为主,浓度分别为120—1421 ng·L−1和12—287 ng·L−1,25个水样中仅有1个样品检出了TBEP;相应沉积物样品中的OPEs则以TPhP(n.d.—54.7 ng·g−1)和TEHP(4.4—377 ng·g−1)为主,TEP和TCPP的浓度较低(n.d.—2.6 ng·g−1). 另有关于太湖的研究也得到类似结果[28]:TEP和TCPP是水样中的优势OPEs,浓度分别为53—1400 ng·L−1和12—290 ng·L−1,TBEP浓度仅为n.d.—2.7 ng·L−1,沉积物中的OPEs以TPhP和TEHP为主,浓度分别为n.d.—55 ng·g−1和4.4—380 ng·g−1. 吴迪等[29]发现,成都锦江地表水中的优势OPEs为TBEP,浓度为27.68—10186.61 ng·L−1,相应沉积物中TBEP浓度(64.46—225.03 ng·g−1)远高于TPhP(8.36—14.10 ng·g−1)和TEHP(4.78—7.66 ng·g−1),说明当地的TBEP污染十分严重.
珠三角是我国改革开放先行地区,工业和经济发展迅速,汽车、电子电器、塑料等工业众多,其环境中的阻燃剂和增塑剂污染近年来受到大量关注[30−33]. 2016年刘静等[30]发现TBEP(n.d.—200 ng·g−1)、TnBP(3.21—178 ng·g−1)、TCEP(3.54—75.4 ng·g−1)、TCPP(2.47—62.6 ng·g−1)和TPhP(2.74—58 ng·g−1)是珠江广州段沉积物中的优势OPEs. 同年Tan等[31]也报道了这一结果,但部分化合物浓度与刘静[30]等的数据存在差异,这可能与采样点位置和采样季节不同有关. 2018年Zeng等[32]再次证实珠江广州段沉积物中的OPE以TPhP、TBEP和TnBP为主,浓度与两年前没有明显变化,同时作者发现珠江佛山段沉积物中的TPhP浓度达到56.6—70.5 ng·g−1,远超珠三角其它河段,但其TBEP和TnBP的浓度相对较低,说明该城市生产/使用的OPEs主要是TPhP. 与沉积物不同的是,珠三角地表水中的OPEs以TnBP(29.6—125 ng·L−1)、TCEP(21.2—102 ng·L−1)和TCPP(32.3—215 ng·L−1)为主[33],这与不同OPEs的物化性质和沉积物-水分配系数有关. 上述研究表明,珠三角地区主要生产/使用的OPEs是TBEP、TnBP、TCEP、TCPP、TPhP等.
国际上对于地表水中的OPEs也有大量报道. Kim等[34]调查了美国多个河流和湖泊中14种OPEs的污染水平和组成特征,发现TBEP、TCEP、TCIPP和TDCIPP为其主要污染物,其中TBEP的浓度最高达689 ng·L−1,平均浓度在43.8—66.2 ng·L−1之间,3种氯代OPEs的浓度范围分别为TCEP: 14.6—17.9 ng·L−1, TCIPP: 59.4—74.6 ng·L−1,TDCIPP: 20.9—21.1 ng·L−1,但样品中TPhP和TnBP的含量均较低. Wolschke等[35]发现德国易北河水中的优势OPEs为TEP、TDCIPP、TCIPP和TCEP,平均浓度依次为168、155、126和81 ng·L−1,而TnBP的含量较低,TBEP未检出. 与我国的数据相比,欧美等区域地表水中的OPEs以氯代OPEs为主,但TPhP和TnBP的相对比例较低. 这种组成差异应该与不同国家/地区的消费和产业结构有关,但截止目前尚未有各国生产使用OPEs种类用量的详细数据.
-
除污水和地表水外,OPEs在世界各国多个城市的自来水中也被广泛检出.
Li等[36]报道了我国8个城市自来水中OPEs的总浓度在85.1—325 ng·L−1之间,以TBEP、TPhP和TCPP为主,浓度范围依次为19.5—81.7 ng·L−1、2.57—14.8 ng·L−1和1.33—16.2 ng·L−1,而TDCIPP、2-乙基己基二苯基磷酸酯(2-ethylhexyl diphenyl phosphate, EHDP)和TEHP仅在两个城市的自来水中检出. 朱孔睿等[37]调查了我国11个城市自来水厂水源水中OPEs的污染情况,发现TnBP、TEHP、TEP和TCPP的浓度最高,平均值分别为93.91、189.02、42.53、56.38 ng·L−1;同时作者发现,在不同自来水处理工艺中,以硫酸铝为混凝剂时对TDCIPP、TCP、TBEP等OPEs的去除率可达100%,投加臭氧对苯系OPEs的去除率比较明显,Calgon F300活性炭对OPEs的吸附去除率可达81.33%.
对美国纽约州58个自来水样品的调查结果表明[34],TBEP和TCIPP为优势OPEs,检出率>90%,平均浓度分别为10.16 ng·L−1 和11.6 ng·L−1;TnBP的检出率仅40%,但最高浓度达133 ng·L−1,是所有检出OPEs中的最高浓度;TPhP的检出率为0. Cristale等[38]发现西班牙一自来水厂进水中的OPEs以TCEP、TCPP和TDCIPP为主,浓度分别为320、220、30 ng·L−1,经过臭氧化/颗粒活性炭过滤后TCEP降为210 ng·L−1,TCPP降为30 ng·L−1,而经过超滤/反渗透处理工艺后TCEP降为70 ng·L−1,TCPP降为20 ng·L−1,认为后者对OPEs的去除率更优;此外采用臭氧化/颗粒活性碳工艺处理时,臭氧化后水中TCEP的浓度为110 ng·L−1,但经过活性炭后浓度又升为210 ng·L−1. 这一发现与一些污水处理厂的研究结果类似,说明自来水厂也可能存在类似管道引入OPEs的现象.
-
OPEs在国内外各地的环境大气中普遍存在,浓度在几十到几千pg· m−3之间,电子垃圾拆解、工业活动等是大气中OPEs的主要污染来源[39−40],TCIPP、TCP、TPhP、TnBP等是各地大气中常见的优势OPEs,但不同区域大气中OPEs的组成各异,城市地区主要受当地城市活动和工业结构的组成及迁移变化影响,偏远地区则受OPEs污染来源变化及大气迁移转化过程影响[39]. 此外,季节、温度和气候变化等均会影响大气中OPEs的浓度和组成[41−44].
Zeng等[39]研究了华南地区电子垃圾拆解厂(清远)、对照点(肇庆鼎湖山)、城市工业区和非工业区(广州等)大气PM2.5中的OPEs,发现电子垃圾拆解厂附近的OPEs浓度平均值达12625 pg· m−3,以TCIPP、TCP和TPhP为主,远超对照点和城市样品数据,证实电子垃圾拆解可释放大量的OPEs;电子垃圾拆解和城市工业活动均对对照点大气PM2.5中的OPEs有明显贡献,但对照点OPEs的污染组成与电子垃圾拆解区和工业区并不完全相同,这可能是大气运输或大气反应损失所致. Wang等[40]也报道了清远电子垃圾拆解厂和广州、佛山等城市大气PM2.5中的OPEs,与Zeng等[39]的结果不同,清远电子垃圾拆解厂大气PM2.5中OPEs的浓度平均值(4350 pg· m−3)低于广州等城市(平均5815 pg· m−3),且前者以TPhP、TCIPP和TCP为主,后者以TCP、TCIPP和TnBP为主. 目前对于国外大气中的OPEs也有不少报道. 2013年Salamova等[45]报道了美国五大湖区芝加哥、克利夫兰等5个采样点大气中的OPEs,其中,芝加哥大气中的TCIPP浓度最高,其次为TBEP、TnBP和TCEP;克利夫兰空气中OPEs的污染水平和组成与芝加哥相近,这两个经济发达城市的苯基OPEs浓度显著高于其它地区. 这种OPEs组成模式与我国存在较大差别,与国内外工业结构及生产/使用的优势OPEs不同有关. 2020年该团队[46]再次采集和分析了相同采样点大气中的OPEs,发现各OPEs的相对比例与2013年的结果类似,但总体浓度均有下降,5个采样点中仍以芝加哥和克利夫兰的污染最为严重,但此前污染较低的两个采样点的TCIPP浓度呈现明显增加,其中Point Petre大气中的TCIPP浓度甚至超过了芝加哥,作者推测这可能与当地一些工业迁移趋势有关.
季节对大气中OPEs的浓度和组成有明显影响. Liang等[41]发现天津市冬夏两季大气中总OPEs含量没有明显差异,但夏季大气中TnBP和TCIPP的含量明显高于冬季大气,而冬季大气中另外一些OPEs(TnBP,TiBP,TCEP,TEHP)的含量则明显高于夏季大气. Li等[42]的研究也得出了相似结论,作者发现我国渤海黄海一带大气中的9种OPEs以TCPP、TCEP、TiBP和TnBP为主,春夏秋冬季大气中OPEs总浓度的平均值分别为220、190、210、200 pg· m−3,没有明显季节变化,但其气相和颗粒相浓度表现出一定的季节变化:夏季气相中总OPEs及个别OPEs的浓度显著高于冬季样品,而冬季颗粒相中的TPhP和TEHP浓度显著高于夏季样品; 作者认为颗粒相浓度并不能很好的反映当地大气中OPEs的季节变化,因为冬季气团大部分源于蒙古利亚和俄罗斯,而夏季气团则主要源于黄海;经初步估算,该区域OPEs的大气年沉降量为每年12吨.
OPEs可随大气发生迁移. 房晓静等[47]提出OPEs的归宿主要包括大气迁移和沉降,气团来源是影响OPEs浓度分布的主要因素. Javier等[48]报道了地中海和黑海附近大气中14种OPEs的总浓度在400—6000 pg· m−3范围内,优势OPEs为TCEP、TCPP、TiBP和TnBP,这一组成与Li等[42]的结果相似,但作者预计每年会有13—260吨OPEs通过大气沉降到该区域,高于Li等[42]的预测结果,作者解释这可能是因为样品采集点靠近污染源头. Castro-Jiménez 等[49]发现浓度本应较高的TCPP在北非突尼斯沿海大气中的浓度远低于其他海洋大气,认为除区域排放模式差异外,较强的太阳辐射可能会加快大气中此类OPEs的降解. 对日本海、北太平洋、我国东海等[50−51]海域大气中的优势OPEs为TCEP、TCPP等氯代OPEs,但TDCIPP浓度并不高,仅个别样品例外. Na等[43]研究了大气中OPEs从西北太平洋到北冰洋的迁移规律,提出温度可能是OPEs长距离迁移的驱动因素. 侯超等[44]报道了OPEs在极地大气的迁移行为,同样提出温度可能是影响大气OPEs空间分布的驱动因素之一, TCEP和TCPP的海气交换净通量由大气指向海水,说明氯代OPEs在极地发生了大气沉降现象,也侧面表明氯代OPEs正在逐步进入极地,需要引起关注;另外,作者认为科考站附近的人类活动是极地氯代OPEs的潜在来源之一. Wang等[52]报道了南极中国长城站2014—2018年大气中OPEs的总浓度为33.9—404 pg· m−3,其中TnBP在颗粒相中占主导地位,TCIPP和TCEP则是气相中的优势OPEs, 且其浓度在一年内增长了1倍,说明氯代OPEs正在持续进入南极地区;作者认为大气长距离迁移是南极大气中OPEs的主要来源,但TnBP的持久性和温度依赖性均较低,其通过大气迁移进入极地的过程仍需探究,作者猜想可能与TnBP能和颗粒相高效结合有关.
-
如前所述,OPEs被广泛用于电子产品、家具装饰品、纺织品等室内/车内易燃物品的阻燃和增塑,目前在中国[53−57]、美国[57−58]、挪威[59]、荷兰[60]、埃及[61]等多个国家的居民室内、工厂车间及汽车内灰尘中检出高浓度的OPEs,最高可达几μg·g−1甚至几百μg·g−1,电子垃圾拆解区室内灰尘中的OPEs浓度甚至超过了传统最优势的BFRs[53].
He等[53]于2015年采集并分析了清远电子垃圾拆解厂车间、拆解厂附近及广州市居民室内灰尘中的OPEs,发现电子垃圾拆解车间灰尘中的OPEs浓度显著高于其它地区,其中磷酸三对甲苯酯(tri-p−cresyl phosphate,TCP)浓度最高(范围0.52—46.6 μg·g−1,平均值15.3 μg·g−1),其次为TCIPP(平均浓度7.18 μg·g−1)和TPhP(6.7 μg·g−1),其余OPEs浓度和的平均值为300 μg·g−1;广州室内灰尘中的OPEs则以TCEP为主(平均浓度5.18 μg·g−1),其次是TDCIPP、TCPP、TnBP、TCP、EHDP等,平均浓度在0.71—1.26 μg·g−1之间. Christia等[54]2017年采集了10个广州家庭的室内灰尘样品并进行OPEs分析,同样发现TCIPP、TCEP和EHDP是其中的优势OPEs,平均浓度分别为797、493、204 ng·g−1,TCIPP和TCEP的最高浓度分别达到6137 ng·g−1和3809 ng·g−1. 这两篇报道均表明氯代OPEs是广州市室内灰尘中的优势OPEs,浓度在几百—几千ng·g−1之间. Du等[56]于2020年也报道了清远电子垃圾车间灰尘中的优势OPEs为TCIPP、TPhP和TCP的同分异构体磷酸三邻甲苯酯(Tri-o−totyl phosphate, TOTP),浓度范围(平均值)分别为0.48—24.6 (4.84) μg·g−1、0.69—8.42 (2.17)μg·g−1和0.13—13.4 (1.77) μg·g−1,但与He等[53]2015年的数据相比,这些优势OPEs的浓度有所下降,这可能与当地对粗放式电子垃圾拆解行业的管理和规范有关. Tan等[57]分析并比较了广州和美国卡本代尔室内灰尘中的OPEs和磷酸二酯,发现后者的OPEs浓度明显高于广州,其中TBEP和TCIPP的浓度差异最为明显(卡本代尔:19500 ng·g−1和5600 ng·g−1;广州:408 ng·g−1和695 ng·g−1),说明两地室内产品中所使用的OPEs存在较大差异;两地样品中多数磷酸二酯的浓度没有明显差别,但磷酸二苯酯(diphenyl phosphate,DPhP)的浓度差异显著,最高达20倍,具体原因尚不清楚.
Du等[56]和Tan等[57]分别计算了广州和清远地区不同人群通过室内灰尘接触对OPEs和磷酸二酯的日摄入剂量,其中广州成年人为16.1和4.1,儿童为502和129[56];清远非电子垃圾拆解工人为11.2和2.7,而电子垃圾拆解厂工人为48.5和60.6. 可见电子垃圾拆解工人对灰尘中OPEs的暴露水平显著高于普通城市居民,同等条件下儿童的暴露风险远高于成人.
OPEs在车用塑料和织物中的大量使用使得车内微环境中的OPEs污染也受到不少研究人员的关注. 荷兰一项研究[60]发现汽车座位附近8个灰尘样品中的TBEP平均浓度为42 μg·g−1,TDCIPP的平均浓度高达110 μg·g−1,研究人员推测电子仪表、皮革纺织品等汽车用品可能是车内灰尘中OPEs的污染来源. Fang等[58]发现美国车内灰尘中的2,2-双(氯甲基)-1,3-丙二基双(2-氯乙基)磷酸酯(2,2-bis(chloromethyl)-1,3-propanediyl bis(bis(2-chloroethyl)phosphate, V6)和TCEP浓度分别为103 ng·g−1和1080 ng·g−1,远高于其在居民室内灰尘中的浓度,且V6和TCEP的浓度显著相关.
-
土壤中的OPEs近年来也受到了广泛关注[62−71],其污染浓度在几ng·g−1到上千ng·g−1之间,其中人类活动密集场所污染相对严重. TBEP、TEHP、TPhP、TCP和氯代OPEs是土壤中常报道的优势OPEs,但国内外不同地区的差别较大,与各地的产业结构有关.
在国内,温佳欣[62]于2010年报道了广州市土壤中OPEs的总浓度在31.7—503.0 ng·g−1之间;相比于烷基和苯基取代的OPEs,氯代OPEs如TCPP和TDCIPP的浓度较高,分别为n.d.—13.7 ng·g−1和n.d—214 ng·g−1,为主要污染物;工业区、垃圾转运站和交通主干道土壤中的OPEs污染较为严重. 2017年Cui等[63]对广州市土壤的报道与温佳欣[62]的结果相近,TBEP(42.8%±15.4%)、TCP(17.2%±11.9%)、TnBP(10.9%±6.85%)和TCEP(9.70%±9.56%)为主要污染物,城市道路绿化带和人类活动密集场所土壤中OPEs污染相对严重. 印红玲等[64]于2014年报道了成都市土壤中的OPEs,其中TBEP为优势污染物,占OPEs总浓度的52%—92%,其次是TCEP和TnBP,但TEHP、TPhP和其他氯代OPEs的含量极低. 2018年He等[65]研究了中国89个城市住宅土壤中的OPEs,发现住宅土壤中的OPEs浓度与点源土壤相比偏低,说明前者受OPEs污染的程度较小;在这些土壤样品中,TCIPP为主要污染物,其次为TBEP、TCEP和TPhP;空间分布结果表明环渤海、长三角和山西省土壤中的OPEs污染程度较高. 2019年Wang等[66]调查了全国范围土壤中的OPEs,发现北京(126 ng·g−1)、上海(388 ng·g−1)和广州(430 ng·g−1)城市土壤中的OPEs污染最为严重,氯代OPEs是主要污染物,占总OPEs浓度的74%以上. Wan等[70]研究了河北省塑料回收厂及附近农场土壤样品中的OPEs,前者浓度为38—1250 ng·g−1,后者的OPEs含量和组成前者显著相关,均以TBEP和TCEP为主,两者在过半数样品中的浓度比例>50%,说明塑料废物回收过程中的OPEs污染释放是其周边土壤中OPEs的主要污染来源. Pang等[71]研究了4种不同类型土壤对OPEs的吸附情况,发现土壤中的有机碳含量会影响OPEs在土壤上的吸附动态平衡过程,随着土壤中溶解有机碳浓度的增加,OPEs的平衡浓度持续下降,当前者浓度为50 mg·L−1时可使土壤中OPEs的毒性降低53%—60%.
在国外,2010年Elke[67]报道了德国8种土壤样品的OPEs,其中TCEP的浓度为n.d.—18.2 ng·g−1,TCPP为0.59—8.33 ng·g−1,TBEP为定量限(LOQ)—13 ng·g−1;作者认为研究选取的采样点不受河水灌溉或污水污泥扩散影响,由此推断相应土壤中的OPEs污染与大气沉降过程有关. Kurt-Katakus等[68]于2017年采集并分析了土耳其布尔萨8个采样点的土壤样品,OPEs总浓度在38—468 ng·g−1之间,其中6个样品中的OPEs以烷基OPEs为主,剩余2个样品则以氯代OPEs为主,从郊区到城市和工业区,烷基OPEs对样品中总OPEs的贡献比例降低,而氯代OPEs的贡献率则上升;作者通过比较土壤和空气中OPEs的含量,推测空气中的OPEs可能有部分来自于土壤. 尼泊尔加德满都[69]土壤样品中的OPEs以TCP(17—25300 ng·g−1)、TCIPP(11.2—991 ng·g−1)和TEHP(8.52—858 ng·g−1)为主,其余OPEs的浓度平均值在18.7—37.9 ng·g−1之间;其较高的OPEs污染浓度可能与消费材料的终端使用、交通排放及采样点靠近工业区等有关;此外,作者还发现OPEs总浓度与土壤中的总有机碳和黑炭含量存在中度正相关,表明土壤有机碳与OPEs的污染分布有一定关联.
-
虽然研究相对有限,但OPEs在生物体内的频繁检出已经证实其具有一定的生物可利用性,但不同OPEs在不同物种中的生物富集特征存在很大差异.
Santin等[72]在西班牙3种鱼体内检测到部分OPEs,其中TEHP和TBEP含量较高,分别达326 ng·g−1和296 ng·g−1,但同类鱼之间OPEs的浓度没有明显的关联. 索莉莉等[73]在我国南昌市淡水鱼、带鱼、虾、青蛙、泥鳅、黄鳝等生物样本中发现了较高水平的TiBP、TnBP和TCPP,其浓度范围分别为1.04—1.77 ng·g−1、0.92—1.68 ng·g−1和23.7—30.9 ng·g−1. Bekele等[74]系统研究了OPEs在我国莱州湾海洋食物网中的生物积累与迁移,各生物体中OPEs的总浓度在21.1—3510 ng·g−1之间,生物累积因子随化合物亲脂性增强而上升,不同OPEs的营养放大因子在1.06—2.52之间,均大于1,说明其在海洋生物中有生物富集放大潜力. Greaves等[75]发现美国大洋区雌海鸥的蛋(蛋黄和蛋清)及脂肪、肌肉、肝、脑红细胞、血清等不同部位中的OPEs浓度和组成均存在很大差异,其中肝脏血清和脑红细胞中未检出OPEs,但脂肪中的OPEs最高达到32.3 ng·g−1;TBEP在蛋清中的丰度达到66%,但在蛋黄中仅为13%. 但2011—2013年加拿大的一项研究[76]发现OPEs在海鸥蛋中的检出率<16%. Fernie等[77]给圈养的美国红隼喂食剂量为22 ng·g−1的OPEs(包含TBEP、TCEP、TCIPP和TDCIPP),但21 d后在其肾和肝脏中并未检测到OPEs,说明红隼对OPEs的代谢很快,但作者发现红隼的多个内分泌指标受到了影响.
除可被动物吸收富集外,OPEs还可被植体吸收转移. Liu等[78]研究了OPEs在几种植物中的积累和转移规律,发现植物根系的蛋白质含量越高,对OPEs的吸收越快,脂肪含量越高则对OPEs的积累量越高,而lg KOW值会影响OPEs在植物体内的迁移效率,lg KOW值越低亲水性越强的OPEs越容易从根部迁移到芽部,从而导致人体摄入OPEs风险的上升.
-
人类也可通过呼吸、日常生活中对灰尘的手口接触、饮食等[57, 79]途径摄入OPEs. 近年来OPEs在人体尿液、指甲、头发、母乳等样品中频频检出,且被证实可代谢成磷酸二酯等产物,其中一些OPEs(如TPhP、TnBP、EHDP等)和磷酸二酯可作为OPEs人体暴露的标志物[80].
目前在人体尿液中检出的磷酸二酯包括磷酸二乙酯(diethyl phosphate,DEP)、磷酸双(2-氯乙基)酯(bis(2-chloroethyl)phosphate,BCEP)、磷酸双(2-氯丙基)酯(bis(2-chloropropyl) phosphate,BCPP)、DPhP、磷酸二丁酯(dibutyl phosphate,DBP)、磷酸二苄酯(dibenzyl phosphate,DTP)、磷酸二(1,3-二氯-2-丙基)酯(bis(1,3-dichloro-2-propyl) phosphate,BDCPP)等(基本信息见表1和图1). Li等[81]发现人体尿液中的BCEP浓度最高达到3.88 μg·L−1,DBP最高浓度为2.53 μg·L−1,去掉异常高值后BCEP和DBP的浓度分别为n.d.—0.84 μg·L−1和n.d.—0.93 μg·L−1. Cequier等[82]报道了42对母子组合尿样中DPhP的平均浓度分别为1.1 μg·L−1和0.57 μg·L−1,BDCIPP的平均浓度分别为0.13 μg·L−1和0.20 μg·L−1,BCEP和DBP均未检出. Craig等[83]对比了美国美甲从业者上班前后尿液中的磷酸二酯浓度,发现后者与前者相比显著增加,表明美甲行业的工作环境会增加人体对OPEs的暴露风险. Hoffman等[84]总结并发现了2002—2015年间美国居民尿液样品中的磷酸二酯浓度呈现显著上升趋势,最高浓度是2002年数据的16倍之多,侧面反映出人体对OPEs的暴露风险越来越高. Liu等[85]在人体手/脚指甲和头发样品中也检测到了OPEs,其中头发中TPhP、TDCIPP和TCIPP的检出率分别为98%、90%和88%,以TCIPP和TDCIPP为主,平均浓度分别为530 ng·g−1和390 ng·g−1,TPhP的平均浓度为280 ng·g−1;而手脚指甲中的OPEs以TPhP为主,浓度平均值分别为700 ng·g−1和1980 ng·g−1,检出率74%,远高于氯代OPEs(平均浓度140—320 ng·g−1,平均检出率<50%);但作者在人体血清中未检测到OPEs.
母乳是母体中污染物向子代传递的重要途径. Kim等[86]采集并分析了越南、日本、菲律宾等国不同年龄、身高、体重母亲的母乳样品,发现日本和菲律宾样品中的OPEs组成相似,以TPhP、TBEP和TCEP为主,但三者在菲律宾母乳中的浓度(n.d.—140 ng·g−1、n.d.—206 ng·g−1、n.d.—512 ng·g−1)显著高于日本(n.d.—15 ng·g−1、n.d.—127 ng·g−1、n.d.—20 ng·g−1);越南母乳样品中的OPEs组成与日本和菲律宾的样品存在较大差异,以TPhP(平均值4.9 ng·g−1)和TnBP(平均值2.0 ng·g−1)为主,TBEP和TCEP的平均浓度均低于检出限,作者认为这种差异反映了各个国家OPEs的使用情况.
-
OPEs进入环境后可通过大气迁移、干湿沉降、土壤渗透等途径在介质间迁移,并在迁移过程中发生水解/光解、微生物降解[87]、生物体/人体代谢等转化行为.
-
Fang等[88]研究了TDCIPP、TCEP、TCPP、TBEP、TEP等的水解过程,发现大多数OPEs在中性条件下不易水解,但在碱性条件下(pH=9—12)水解速度显著加快;pH=12时TEP的水解速率最快,其次是TBEP、TCPP、TCEP和TDCIPP,其中TCPP和TBEP差距不大,金属氧化物的存在可加速OPEs水解. Su等[89]比较了不同pH下16种OPEs的水解情况,发现pH=13时,除TnBP和TEHP外的OPEs均有水解,速率为烷基OPEs>氯代OPEs>芳基OPEs,当pH值调低为11、9和7时大部分OPEs不水解. 一般的水处理工艺如活性炭、厌氧好氧等可基本去除非氯代OPEs,但氯代OPEs在现有污水处理工艺中的去除效率低[21−22, 90],通过调节pH以加快OPEs水解可能是提升氯代OPEs去除率的方法之一.
Cristale等[91]研究了9种OPEs在河水和腐殖质中的光降解,发现除TCEP外的其他OPEs均有显著降解,其中苯基OPEs的光解速率大于烷基和氯代OPEs,腐殖质会降低其光解效率;OPEs降解的主要机制不是阳光直射,而是光照使OPEs显示光敏特性,然后通过活性氧促进其降解. Sun等[92]对比了水环境中TCP在直接光照和加入NO2−、Fe3+、腐殖酸等条件下的光降解特征,发现NO2−和Fe3+可促进其光解,而腐殖酸则抑制其光解.
-
Kulkarni等[93]在污染土壤中分离出Klebsiella pneumoniae S3用于降解TnBP,该菌可在48 h内将1 g·L−1的TnBP降解为DBP,并且对TnBP的耐受性高达17 g·L−1. Liu等[94]筛选出Sphingomonas sp.来降解TnBP,通过产物鉴定表明降解产物包括DBP和磷酸一丁酯,TnBP降解为DBP时发生了P—O键断裂. 卫昆等[95]利用短芽孢杆菌(Brevibacillus brevis)降解TPhP,发现其降解效率与投菌量、温度和pH有关;当投菌量为2 g·L−1,温度为30 ℃,pH=7时TPhP的降解率可达92.1%,且降解产物毒性低于母体,作者由此认为生物强化是一种原位修复TPhP污染水体的潜在方法. Jurgens等[96]研究了20 mg·L−1的TPhP、双酚A磷酸二苯酯(PBDPP)和间苯二酚双(二苯基)磷酸酯(BPA-BDPP)在活性污泥中的矿化反应和初级生物降解,发现TPhP和PBDPP的半衰期分别为2.8 d和<1 d,但BPA-BDPP在56 d后仍基本无降解. Liu等[97]利用Brevibacillus brevis
来降解磷酸三间甲苯酯(tri-m-cresyl phosphate,TMCP)、TCP和TOTP,投菌量2 g·L−1时三者5 d内的降解率分别为82.91%、93.91%和53.92%,在降解过程中该菌 吸收K+、PO43-、MG2+和SO42-,并释放Na+和Cl−. 与非氯代OPEs相比,氯代OPEs不易被微生物降解,但Takahashi等[98]以TCEP和TDCIPP为唯一磷源,在好氧条件下分离出可降解这两种氯代OPEs的两种菌株(TCM1和TDK1),但TCM1降解TCEP和TDCIPP时会产生有毒副产物. 该团队在后续研究中又筛选出了Xanthobacter autortrophicus Strain GJ10,与TCM1协同降解TCEP生成无毒产物,再用TCM1降解TDCIPP产生的有毒副产物作为唯一磷源,筛选出Arthrobacter sp. Strain PY1,与TCM1协同降解TDCIPP使过程无毒化[99-100].
-
根据已有报道,OPEs在生物体/人体中的代谢产物包括羟基化磷酸三酯、磷酸二酯、羟基化磷酸二酯及羟基化后与葡萄糖醛酸的结合物等[101].
Reemtsma等[102]认为OPEs的C—O键容易在酶的攻击下生成二酯,二酯的C—O键也可在酶的进一步攻击下转化为单酯. 汪国威等[103]发现斑马鱼的肝脏和肠道是OPEs的重要代谢器官,脑、卵和肌肉不能代谢OPEs;烷基OPEs的每条支链尤其是支链尾端的碳是另一个进攻活性位点,氧化这些位置易产生羟基化代谢产物. 杜仲坤等[104]分别将斑马鱼肝脏暴露于一定浓度的OPEs中,发现9种OPEs可导致其葡萄糖含量升高,琥珀酸、胆碱、乙酰肉碱、谷氨酸和谷氨酰胺浓度降低,说明OPEs可抑制斑马鱼肝脏中糖、脂、氨基酸的代谢供能过程,其中氯代OPEs对肝脏糖代谢的影响更加显著,而苯基OPEs对氨基酸和脂肪酸代谢的影响更为显著. Van等[105]在斑马鱼肝脏中发现了OPEs的羟基化代谢产物,认为OPEs在斑马鱼体中经历了氧化代谢,且细胞色素P450是主导该代谢的主要酶系. 此外,人体肝脏微粒[106]和禽类肝脏细胞[107]均可在体外将TBEP、TDCIPP、TPhP等OPEs转化成各自的磷酸二酯和羟基化产物,说明OPEs在生物体/人体中可能存在相似的代谢过程.
-
如前所述,氯代OPEs已在偏远/两极地区的环境中广泛检出,如各大洋空气[6]、北极空气[7− 8, 50]、北极土壤[108]、北极海洋沉积物[9]和海水等[10],TnBP也在南极大气颗粒物中大量检出[52],说明这些OPEs有一定的环境稳定性和持久性,可通过大气长距离迁移至偏远地区,温度可能是此迁移的重要驱动因素[43−44]. 此外,大气中的OPEs可通过沉降进入土壤,是一些地区土壤中OPEs的重要来源,同样土壤中的OPEs挥发也是部分地区空气中OPEs的来源[67−68].
-
目前对于OPEs的毒性已有不少研究[109]. 但主要集中在氯代OPEs上[110−120],TCEP、TCPP和TDCIPP已被证明具有致癌性、内分泌毒性、神经毒性、生殖发育毒性等,但其它非氯代OPEs的毒性数据相对较少,对苯基取代的OPEs[121−123](如TPhP、EHDP等)的毒性有一定报道,对烷基取代OPEs的毒性研究则集中在TnBP上[124−125].
-
目前的数据证实,氯代OPEs对鱼、鸡、蚯蚓等均可产生生殖发育毒性. Farhat等[114]通过鸡蛋对TDCIPP和TCPP的暴露实验发现,TCPP能明显影响孵化成功率,浓度为51600 ng·g−1时会减小小鸡脚踝长度,TDCIPP可使小鸡头喙长度减小、胚胎质量下降、胆囊变小等. 斑马鱼暴露实验显示[115],TDCIPP可致雌鱼体长变短重量下降,高浓度(6300 ng·L−1, 21 d)暴露可使雌鱼产卵量显著下降. 斑马鱼早期胚胎的暴露研究证实[116],TDCIPP可使其胚胎内组织和器官发育异常,从而改变胚胎的正常发育轨迹. Zhu等[117]研究了TDCIPP暴露对土壤中蚯蚓的影响,发现经过28 d 5000 ng·g−1的TDCIPP暴露后,蚯蚓体重明显减轻,并观察到表皮和精囊受损,出生数量减少25%,说明TDCIPP对蚯蚓产生了明显的生殖毒性.
-
多种OPEs被证实具有神经毒性[126]. Ta等[127]将PC12细胞暴露在不同浓度的TDCIPP和TCEP中,3 d后观察到细胞神经突触变短且数量减少. Dishaw等[118]发现等摩尔浓度下TDCIPP的神经毒性≥毒死蜱,且可抑制DNA合成,此外TDCIPP、TCEP、TCPP、磷酸三(2,3-二溴丙基)酯(tris(2,3-dibromopropyl) phosphate, TDBPP)等OPEs均可减少细胞数量并影响神经分化. 除氯代OPEs外,苯基取代OPEs也可引起神经毒性. Hong等[121]在鱼类暴露研究中发现,TPhP暴露28 d可显著提高鱼类血脑屏障渗透性,激活其神经炎症反应,并降低鱼脑中相关mRNA水平.
-
OPEs的内分泌干扰效应也已得到证实. Li等[122]在鱼暴露实验中发现,EHDP可抑制鱼体中雄激素受体活性,浓度为37.5 μmol·L−1时抑制率已达50%;经过100 d暴露后,雌雄同体鱼的数量显著上升. 另外有研究发现,室内灰尘中的TDCIPP水平与男性甲状腺激素和催乳素水平的降低有关[119].
-
Yan等[124]通过3种不同浓度OPEs对淡水蛤蜊的30 d暴露实验发现,TnBP和TDCIPP可引起蛤蜊细胞凋亡,并表现出基因毒性,且毒性与浓度呈显著正相关;相同浓度下TDCIPP的基因毒性大于TnBP. 还有文献指出[123],苯基取代的TPhP和TCP、氯代的TCPP和TCEP等OPEs也具有细胞毒性,可引起细胞凋亡,毒性强度为TPhP>TCP>TCPP>TCEP,即苯基OPEs的细胞毒性>氯代OPEs,作者认为这可能是因为暴露实验只进行了24—48 h,还需要开展慢性暴露实验去确定各OPEs的长期暴露毒性. 此外,TPhP可通过干扰斑马鱼的转录调节因子表达引起心脏毒性[128]. Su等[129]研究了TPhP及其一级代谢产物DPhP对鸡肝细胞的细胞和基因毒性,发现经36 h暴露后,TPhP剂量大于10 μmol·L−1即可产生细胞毒性,但DPhP剂量达到1000 μmol·L−1也未表现出细胞毒性;但同样是10 μmol·L−1的暴露浓度,DPhP改变了27个基因中的9个,而TPhP仅改变了4个,这表明虽然DPhP的细胞毒性不明显,但存在潜在的基因毒性.
-
随着环境中的OPEs越来越受到关注,目前已经发展出针对各类环境样品中OPEs的前处理和仪器分析方法[130].
-
一般来说,水样等液体样品中的OPEs可通过液液萃取(liquid-liquid extraction, LLE)[131]、固相萃取(solid-phase extraction, SPE)[132-133]、固相微萃取(solid-phase microextraction, SPME)[134]、膜辅助萃取(membrane-assisted solvent extraction, MASE)[135]、分散液液微萃取(dispersive liquid-liquid microextraction, DLLME)[136]等进行提取/富集.
其中,LLE受水样基质影响较小,样品可不经过过滤直接萃取,普适性强,但有机溶剂用量大,对极性较高OPEs的萃取效率不理想,且自动化程度低,操作繁琐费时. SPME处理水样时无需过滤,有机溶液用量少甚至可不用,萃取后可直接在气相色谱-质谱联用仪(gas chromatograph-mass spectrometer, GC-MS)中解吸进样,方便快捷,但SPME对于弱极性和难挥发OPEs的回收率并不理想. SPE是通过不同固相填料,选择性吸附通过水样中的待测组分,在提取的同时实现待测组分的分离和富集,操作简便快速,有机溶剂用量少,是目前痕量污染物分析使用最多的水样前处理方法. 常用的SPE小柱有SAX(强阴离子交换柱)、WAX(弱阴离子交换柱)、C18、HLB(亲水亲油平衡柱)等. SAX和WAX柱较少用于OPEs,C18柱对弱/非极性的待测组分选择性较强,HLB柱适用范围最广,极性非极性都可用,适合极性(亲脂性)跨度比较大的OPEs(lg KOW=−0.65—9.49),是目前液态样品中OPEs前处理选择最多的SPE柱[23, 25, 28, 33−34, 132−133]. 常用HLB柱的容量有150、200、500 mg,使用时可根据样品提取量、受污染程度、基质复杂程度等选择.
采用HLB小柱净化前需要对样品辅以过滤、离心等步骤,或采用其它分离方法,将其中的不溶物/颗粒与溶解相分离. Cequier等[82]将尿液样品从-20 ℃放置至常温后取1.5 mL,在18210 r·min−1离心力下离心4 min,取上清液加入内标后直接仪器分析其中的磷酸二酯,没有净化过程. 同样是检测尿液中的磷酸二酯,Li等[81]先将样品解冻后离心,然后采用WAX柱进行净化. Kim等[86]取10 mL母乳样品冷冻干燥,然后加入无水硫酸钠混合均匀,采用正己烷和丙酮混合溶剂加速萃取,将提取液用正己烷定容至10 mL获得待测液.
-
固体样品包括污泥、土壤、沉积物、大气颗粒相、生物样品(体液除外)等,提取前一般需要进行冷冻干燥. 此外多数固态样品有机质含量高,可能存在比较强的基质效应,其提取液多数需要经过净化才能进行仪器分析.
固体样品的提取方法主要有加速溶剂萃取(accelerated solvent extraction, ASE)[21, 75]、超声辅助萃取(ultrasound-assisted extraction, UAE)[72−73, 137]、微波辅助萃取(microwave-assisted extraction, MAE)[90]、振荡萃取[132]和索氏提取. 索氏提取是固体样品中有机物提取的传统方法,简单易行,但耗时耗力且有机溶剂用量大,现已少有应用. ASE法通过高温高压增强溶剂对固体样品中待测组分的溶解和萃取能力,具有萃取时间短、效率高、有机溶剂用量少、自动化程度高等优点,但该方法不适于热敏性化合物,同时会增加提取液中的干扰基质,对净化步骤要求较高. UAE法通过超声波的震动、粉碎、搅拌、加热等作用提高溶剂渗透力,从而使待测组分快速进入溶剂,还可破坏生物样品的细胞壁,提高其提取效率,但该方法一般需要多次提取操作以保证萃取效率. MAE法通过微波加热均匀、内外同步升温来提高溶剂对待测组分的萃取效率,可大大缩短萃取时间,但其仅适于极性萃取溶剂. 振荡萃取是通过机械运动使溶剂和样品充分混合从而提取待测组分的方法,可通过外部加热提高萃取速度和效率,但方法耗时较长,且需多次提取.
固体样品提取液常用净化方法是层析柱法,通过柱填料的选择性吸附和洗脱对样品中的待测组分进行富集、分离和净化. 常用的吸附填料有:(1)无机材料,如硅胶、氧化铝、硅酸镁(Florisil)、活性炭等;(2)以硅胶为基质的键合材料,如C18、C8、SAX柱等;(3)高分子聚合物,如各类聚苯乙烯-二乙烯苯吸附剂,包括凝胶渗透柱、HLB柱、WAX柱等的填料. 层析柱可自行装填(主要是无机材料),也可采用商用SPE小柱,后者是OPEs分离净化的常用方法,其操作过程与水样的前处理方法类似,可用小柱类型包括HLB柱、C18柱、硅胶柱、氧化铝柱等,可根据实际样品处理需求,灵活选用其中的一种或多种进行串联. Moller等[138]将旋转蒸发后的样品提取物通过2.5 g 10%水失活的硅胶柱进行净化,先用20 mL正己烷洗脱去除非极性烷烃类杂质,再用丙酮/二氯甲烷混合溶剂洗脱OPEs. 印红玲等也采用类似方法[64],选用氧化铝/硅胶复合柱对样品进行净化,上样后先用正己烷洗脱去杂,再用乙酸乙酯/丙酮洗脱出OPEs. Kurt-Karakus等[68]、Cao等[139]和Yadav等[69]均采用Florisil小柱对样品中的OPEs进行分离净化. HLB柱也常被用于固体样品提取液的净化[25, 28, 31−32]. 除SPE外,也有一些研究采用SPME净化富集样品中的OPEs. Elke等[67]将吹干后的样品提取物重新用1 mL甲醇和13 mL水溶解,过0.2 μm滤膜后采用SPME净化富集其中的OPEs.
空气样品一般通过主动或被动采样器将空气的颗粒相和/或气相收集到事先准备好的滤膜和吸附材料中[42, 48],其前处理按照固体样品的前处理方法进行.
-
在已有研究报道中,OPEs可用气相色谱-氮磷检测器(gas chromatograph-nitrogen and phosphorus detector, GC-NPD)[136, 140]、GC-MS [32, 53, 133, 141−142]、液相色谱-双质谱联用仪(liquid chromatograph-tandem mass spectrometer, LC-MS/MS)[27, 37, 73, 143]等仪器进行检测. 与GC-MS相比,GC-NPD对含磷化合物选择性更好,灵敏度更高,但NPD检测器无法定性,且使用过程中铷珠易损耗,导致检测结果稳定性下降,需定期更换,在OPEs分析中的应用十分有限. GC-MS和LC-MS/MS是目前OPEs仪器分析的主流方法.
-
目前多数研究采用电子轰击离子源(electron impact, EI)-GC-MS对OPEs进行分析,其中GC毛细管柱具有分离同分异构体的优势,MS定性能力强大且EI源有丰富的标准谱库,使得该方法具有基质干扰效应小、灵敏度高、选择性和鉴定能力强、分离度好等优点,在典型OPEs的分析上应用较多. Brandsma等[60]比较了GC-MS和LC-MS/MS对室内和汽车内灰尘中10种OPEs的检测结果,发现GC-MS对其中7种OPEs的回收率在82%—112%之间,但对TEHP和TCP的回收率分别为140%和155%,TBEP的回收率则只有65%;LC-MS/MS对其中6种OPEs的回收率达到79%—101%,但其余4种OPEs(TDCIPP、TBEP、EHDP和TCP)的离子抑制信号超过50%,所以作者最终选择GC-MS作为OPEs的仪器检测方法.
GC-MS适用于非/弱极性、易挥发并具有一定热稳定性的有机物,对于一些极性较强OPEs的分析效果并不理想,如强极性的低取代OPEs、磷酸二酯等. 一些新型OPEs,如间苯二酚双(二苯基)磷酸酯(resorcinol bis(diphenyl)phosphate, RDP)、V6、双酚A双磷酸二苯酯(bisphenol A diphenyl phosphate, BPADP)等具有分子量大(574.45—692.63)、沸点高(587.1—679.6 ℃)、难挥发等特点,在GC-MS上的响应也较差,检出限高. 此外,有研究表明,磷酸甲酚二苯酯(cresyl diphenyl phosphate, CDP)、异丙基化磷酸三苯酯(tris(p−isopropylphenyl)phosphate, IPPP)等苯基OPEs在GC柱上会因高温而分解成为TPhP,从而导致测样结果不准确[72]. 上述种种情况均限制了GC-MS在OPEs分析上的应用.
-
采用LC-MS/MS法分析OPEs时,多数研究选用电喷雾离子源(electron spray ionization,ESI)和多反应离子监测(muti-reaction monitoring, MRM)模式. ESI源适用范围宽,对分子量大、不易挥发的OPEs(如RDP、V6、BPADP等)也有较好的电离效果;MRM模式选择性和抗干扰能力强,灵敏性高,当水样中OPEs浓度较高时可直接将样品过滤后上机测试,无需再用有机溶剂提取转移. 此外,LC-MS/MS还可通过灵活调节离子化模式来测定不同极性的OPEs及相关化合物,如ESI+模式主要测定OPEs原型化合物,ESI−模式可测定磷酸二酯. 但LC-MS/MS也有一定的局限性:LC色谱柱在分离OPEs同分异构体上效果不太理想;复杂样品分析时存在严重的基质干扰效应,导致结果出现偏差. 例如与地表水样相比,污水样品在用LC-MS/MS分析OPEs时灵敏度会大幅降低,检出限提高至前者的2—10倍,甚至上百倍[25].
综上所述,环境样品中OPEs的分析方法目前主要存在两个问题[144−145]:
(1)基质和背景干扰,除基质效应外,OPEs及其相关塑料制品的广泛使用使得OPEs在实验室环境中无处不在,甚至仪器组件中也含有OPEs,从而使得实验过程极易引入背景干扰;
(2)缺乏统一分析方法,不同实验室间的数据可比对性差,准确度有待提高.
-
已有的研究已证实,OPEs种类繁多,用途广泛,在各类环境介质中普遍存在,并表现出持久性、长距离迁移性、生物可利用性和毒性,但目前国内外对其环境行为归趋和风险的研究尚未全面展开,仍存在以下问题:
(1)缺乏对环境中OPEs及代谢产物统一全面的分析方法. OPEs同系物和异构体众多,且物化性质差异很大,主流的OPEs仪器分析手段GC-MS和LC-MS/MS各有优点和缺陷. 如何同步分析和表征复杂样品中可能存在的全部OPEs及其转化产物对环境分析化学家来说是很大的挑战.
(2)目前对环境中OPEs的研究主要集中在水体、沉积物、污水污泥、灰尘等介质,对于土壤、生物体/人体中的OPEs研究相对较少,尤其对其在生物体和人体中代谢产物和机理的研究十分有限,无法准确把握OPEs在环境中的迁移转化行为、归趋、影响因素、毒性和健康/生态风险.
(3)目前的研究主要集中于OPEs的污染水平,对于其污染来源、不同污染源OPEs的组成特征及来源追溯的研究极为有限.
(4)已有研究中的OPEs种类相对有限,主要集中在3种氯代OPEs和几种常见的烷基/苯基取代OPEs上,对其它OPEs及代谢产物,以及近年来新兴的RDP、BPADP、V6等的研究有待进一步展开.
(5)目前对OPEs的毒性研究主要集中在氯代OPEs上,对非氯代OPEs以及OPEs代谢产物的毒性研究相对有限.
作为一类新兴污染物,OPEs不仅在环境中普遍存在,而且被证实具有内分泌干扰效应、生殖发育毒性、神经毒性甚至致癌性,其污染和风险已引起国内外环境领域研究学者的广泛关注,可以预见,随着研究方法和技术手段的不断发展进步,关于OPEs及其转化产物的污染和生态/健康风险研究将会全面展开. 结合OPEs目前的研究现状和存在的问题,今后相关的研究应集中在:
(1)建立环境样品中OPEs及其转化产物全分析的标准方法和质控体系,为研究环境中可能存在的所有OPEs及其代谢物提供方法和技术支撑,同时提高不同实验室研究数据间的可比对性.
(2)探讨OPEs不同污染源的排放成分谱和污染排放特征,判识和追溯不同环境介质中OPEs的污染来源和环境行为,深入研究OPEs在各类环境介质以及生物体/人体间的迁移转化行为和规律.
(3)系统开展OPEs及其代谢产物的毒性研究,为准确评估其潜在生态和健康风险提供科学依据.
有机磷酸酯(OPEs)的环境污染特征、毒性和分析方法研究进展
The pollution characteristics, toxicity and analytical methods of organophosphate esters (OPEs) in environments: A review
-
摘要: 随着溴系阻燃剂在世界范围内被禁止,其主要替代物有机磷酸酯(OPEs)在近年来的生产和使用量均呈现快速增长. 但作为塑料添加剂,OPEs与材料间无化学键束缚,极易在产品生命周期中释放进入环境. 目前,OPEs作为一类新兴污染物,已在全球各地的污水、自来水及其它各类环境介质和人体中广泛检出,包括极地地区,表现出长距离迁移能力,因此,其环境污染和毒性迅速受到国内外的广泛关注,但目前对其环境行为和潜在风险尚不完全清楚. 本文对近15年来发表的相关文献进行了检索,综述了OPEs在各类环境介质和人体中的污染特征和现状、迁移转化行为、毒性和分析方法的研究进展. 结果表明:OPEs在全球环境中普遍存在,可通过室内灰尘接触、呼吸、食物链传递等途径被生物体和人体吸收,并表现出内分泌干扰、神经毒性、生殖发育毒性等多种毒性效应;OPEs在生物体/人体中可被转化为低取代的二酯、单酯等代谢产物,但目前对其代谢转化途径尚不明确. 鉴于OPEs生产使用历史悠久,用途广泛且用量巨大,污水处理去除效率有限,其环境行为过程和机理以及由此导致的潜在生态和健康风险值得引起持续关注. 此外,OPEs种类繁多,化合物之间性质差异较大(lg KOW=−0.65—9.49),目前报道中所采用的前处理及仪器分析方法均有所侧重,缺乏统一全面的标准分析方法,无法同步分析环境中可能存在的所有OPEs及其代谢转化产物,不同实验室间的数据可比对性也比较差,如何建立OPEs及其代谢产物的全分析方法也是目前研究亟待解决的问题.Abstract: As the major substitutes of brominated flame retardants which are being banned worldwide, organophosphate esters (OPEs) exhibit rapid rise both in production and use in recent years. However, as plastic additives, OPEs are not chemically bonded with the materials, and therefore are apt to release into the environment over the products’ life cycle. Up to now, as a kind of emerging pollutants, OPEs have been widely detected in waste water, tap water, other environmental media and human worldwide, including the polar regions, and demonstrated long-range transportability. Therefore, the environmental pollution and toxicity of OPEs rapidly attracted the global attention. However, their environmental behaviors and potential risks still remain unclear so far. In this paper, OPEs relevant literatures published in recent fifteen years were retrieved, and their pollution characteristics and status, migrations and transformation behaviors in various environments and human, as well as the toxicity and analysis methods were reviewed. The existing data show that OPEs are ubiquitous in global environments; They can be ingested by organism and human via dust contact, inhalation and food chain, and then demonstrate multiple biotoxicities, e.g. endocrine disrupting effects, neurotoxicity, reproductive and developmental effects, etc.; OPEs can be metabolized by organisms and human to phosphodiesters and phosphomonoesters, whereas their metabolic pathways are still unclear. Considering that OPEs have long using history, versatility and great consumption, and demonstrate limited removal efficiency during sewage disposal, continuous attention should be paid to their environmental behaviors, processes and mechanisms, as well as their potential ecological and health risks. In addition, OPEs conprise quite a few congeners with distinctly different physic-chemical properties (lg KOW=−0.65—9.49), while the existing sample pretreatment procedures and instrumental analysis methods are only applicable for a few or dozen OPE congeners. So far, the standard and comprehensive analysis method for all possible OPEs and their metabolites in environments is still unavailable. Moreover, data from different labs showed low comparability. How to establish a comprehensive co-analysis method for OPEs and their metabolites has become an important issue that must be solved.
-

-
表 1 OPEs及部分磷酸二酯的化学信息和物化性质参数1
Table 1. Chemical information and physic-chemical parameters of OPEs and some phosphodiesters1
中文名
Chinese name英文名
English name缩写
Abbreviation化学式
Chemical formula分子量
Chemical weightCAS
lg KOW
沸点2/℃
Boiling point蒸气压3/mm Hg
Vapor pressure水溶解度3/(mg·L−1)
Solubility磷酸三甲酯 Trimethyl phosphate TMP C3H9O4P 140.075 512-56-1 −0.65 197 0.415 3.00×105 磷酸三乙酯 Triethyl phosphate TEP C6H15O4P 182.155 78-40-0 0.8 215 0.165 1.12×104 三(2-氯乙基)磷酸酯 Tris(2-chloroethyl)phosphate TCEP C6H12Cl3O4P 285.490 115-96-8 1.44 347.4 3.91×10−4 8.78×102 磷酸三丙酯 Tri-n−propylphosphate TnPP C9H21O4P 224.234 513-08-6 1.87 281.64 0.0231 8.27×102 2,2-双(氯甲基)-1,3-丙二基双(2-氯乙基)磷酸酯 2,2-Bis(chloromethyl)1,3-propanediyl bis(bis(2-chloroethyl)phosphate V6 C13H24Cl6O8P2 582.990 38051-10-4 1.92 620.3 0.0±1.7 — 磷酸三异丙酯 Triisopropyl phosphate TiPP C9H21O4P 224.234 513-02-0 2.12 222.2 0.138 5.01×102 磷酸三(2-氯异丙基)酯 Tris(1-chloro-2-propanyl)phosphate TCIPP C9H18Cl3O4P 327.570 13674-84-5 2.59 358.5 5.64×10−5 51.9 三苯基氧膦 Triphenylphosphine oxide TPPO C18H15OP 278.285 791-28-6 2.83 462.9 2.82×10−7 62.8 磷酸三(氯丙基)酯 Tris(3-chloropropyl)phosphate TCPP C9H18Cl3O4P 327.570 26248-87-3 3.11 406.9 4.79×10−6 18.8 磷酸三异丁酯 Triisobutyl phosphate TiBP C12H27O4P 266.314 126-71-6 3.60 205 1.28×10−2 16.2 磷酸三(1,3-二氯异丙基)酯 Tris(1,3-dichloro-2-propyl)phosphate TDCIPP C9H15Cl6O4P 430.905 13674-87-8 3.65 457.4 2.86×10−7 1.50 磷酸三(2,3-二溴丙基)酯 Tris(2,3-dibromopropyl)phosphate TDBPP C9H15Br6O4P 697.611 126-72-7 3.71 544.2 0.0±1.4 — 磷酸三(丁氧基乙基)酯 Tris(butoxyethyl)phosphate TBEP C18H39O7P 398.472 78-51-3 3.75 413.9 1.23×10−6 1.96 磷酸三(正)丁酯 Tri-n−butyl phosphate TnBP C12H27O4P 266.314 126-73-8 4.00 326.73 3.49×10−3 7.36 磷酸三苯酯 Triphenyl phosphate TPhP C18H15O4P 326.283 115-86-6 4.59 412.4 4.72×10−7 1.03 磷酸甲酚二苯酯 Cresyl diphenyl phosphate CDP C19H17O4P 340.310 26444-49-5 5.25 405.9 1.04×10−7 0.234 磷酸三邻甲苯酯 Tri-o−totyl phosphate TOTP C21H21O4P 368.363 78-30-8 5.48 476.49 0.0±0.9 — 2-乙基己基二苯基磷酸酯 2-ethylhexyl diphenyl phosphate EHDP C20H27O4P 362.400 1241-94-7 5.73 421.2 3.34×10−5 6.66×10−2 间苯二酚双(二苯基)磷酸酯 Resorcinol bis(diphenyl)phosphate RDP C30H24O8P2 574.454 57583-54-7 5.97 587.1 0.0±1.6 — 磷酸三间甲苯酯 Tri-m−cresyl phosphate TMCP C21H21O4P 368.363 563-04-2 6.34 441.7 1.09×10−7 1.84×10−2 磷酸三对甲苯酯 Tri-p−cresyl phosphate TCP C21H21O4P 368.363 1330-78-5 6.34 476.49 3.49×10−8 1.84×10−2 磷酸三己基酯 Trihexyl phosphate THP C18H39O4P 350.474 2528-39-4 6.76 354.1 2.47×10−6 1.03×10−2 磷酸异葵基二苯酯 Isodecyl diphenyl phosphate IDPP C22H31O4P 390.453 29761-21-5 7.28 448.4 4.72×10−8 2.13×10−3 磷酸三(二甲苯)酯 Tris(3,5-xylenyl)phosphate TXP C24H27O4P 410.443 25155-23-1 7.98 490.8 2.06×10−8 4.00×10−4 磷酸三(三溴新戊基)酯 Tris(tribromo neopentyl)phosphate TBNPP C15H24Br9O4P 1018.458 19186-97-1 8.51 595.9 0.0±1.6 — 双酚A双磷酸二苯酯 Bisphenol A diphenyl phosphate BPADP C39H34O8P2 692.630 5945-33-5 8.66 679.6 0.0±2.0 — 异丙基化磷酸三苯酯 Tris(p−isopropylphenyl)phosphate IPPP C27H33O4P 452.522 68937-41-7 9.07 489.7 2.06×10−8 2.59×10−5 磷酸三(2-乙基己基)酯 Tris(2-ethylhexyl)phosphate TEHP C24H51O4P 434.633 78-42-2 9.49 449.67 6.07×10−7 1.46×10−5 磷酸二乙酯 Diethyl phosphate DEP C4H11O4P 154.102 598-02-7 0.32 200.3 1.84×10−3 3.84×104 磷酸双(2-氯乙基)酯 Bis(2-chloroethyl)phosphate BCEP C4H9Cl2O4P 222.992 3040-56-0 0.83 301.8 4.42×10−6 6.46×103 磷酸双(2-氯丙基)酯 Bis(2-chloropropyl)phosphate BCIPP C6H13Cl2O4P 251.045 789440-10-4 0.91 316.2 0.0±1.4 — 磷酸二(1,3-二氯-2-丙基)酯 Bis(1,3-dichloro-2-propyl)phosphate BDCIPP C6H11Cl4O4P 319.935 72236-72-7 2.18 396.9 2.58×10−8 1.30×102 磷酸二丁酯 Dibutyl phosphate DBP C8H19O4P 210.208 107-66-4 2.29 275.3 1.82×10−5 4.30×102 磷酸二苄酯 Dibenzyl phosphate DTP C14H15O4P 278.240 1623-08-1 2.76 427.6 1.26×10−8 72.4 磷酸二苯酯 Diphenyl phosphat DPhP C12H11O4P 250.187 838-85-7 2.88 377.7 9.12×10−8 82.4 磷酸二(2-乙基己基)酯 Bis(2-ethylhexyl)phosphate DEHP C16H35O4P 322.421 298-07-7 6.07 400.41 1.80×10−7 5.93×10−2 1 数据来源自EPI计算和ACD/Labs计算;2 760mm Hg条件下数据;3 25 ℃条件下数据. 1 Data were calculated via EPISuite 4.0 and ACD/Labs;2 Data at 760mm Hg;3 Data at 25 ℃. -
[1] VAN DER VEEN I, DE BOER J. Phosphorus flame retardants: Properties, production, environmental occurrence, toxicity and analysis [J]. Chemosphere, 2012, 88(10): 1119-1153. doi: 10.1016/j.chemosphere.2012.03.067 [2] 王晓伟, 刘景富, 阴永光. 有机磷酸酯阻燃剂污染现状与研究进展 [J]. 化学进展, 2010, 22(10): 1983-1992. WANG X W, LIU J F, YIN Y G. The pollution status and research progress on organophosphate ester flame retardants [J]. Progress in Chemistry, 2010, 22(10): 1983-1992(in Chinese).
[3] 欧育湘. 我国有机磷阻燃剂产业的分析与展望 [J]. 化工进展, 2011, 30(1): 210-215. OU Y X. Developments of organic phosphorus flame retardant industry in China. [J]. Chemical Industry and Engineering Progress, 2011, 30(1): 210-215(in Chinese).
[4] ANNELI MARKLUND S, ULRIKA O, PETER H. Organophosphorus flame retardants and plasticizers in marine and fresh water biota and in human milk [J]. Journal of Environmental Monitoring, 2010, 12(4): 943-951. doi: 10.1039/b921910b [5] 高小中, 许宜平, 王子健. 有机磷酸酯阻燃剂的环境暴露与迁移转化研究进展 [J]. 生态毒理学报, 2015, 10(2): 56-68. GAO X Z, XU Y P, WANG Z J. Progress in environment exposure, transport and transform of organophosphorus flame retardants. [J]. Asian Journal of Ecotoxicology, 2015, 10(2): 56-68(in Chinese).
[6] CASTRO-JIMENEZ J, GONZALEZ-GAYA B, PIZARRO M, et al. Organophosphate ester flame retardants and plasticizers in the global oceanic atmosphere [J]. Environmental Science & Technology, 2016, 50(23): 12831-12839. [7] SALAMOVA A, HERMANSON M H, HITES R A. Organophosphate and halogenated flame retardants in atmospheric particles from a European Arctic site [J]. Environmental Science & Technology, 2014, 48(11): 6133-6140. [8] SUHRING R, DIAMOND M L, SCHERINGER M, et al. Organophosphate esters in Canadian arctic air: Occurrence, levels and trends [J]. Environmental Science & Technology, 2016, 50(14): 7409-7415. [9] MA Y, XIE Z, LOHMANN R, et al. Organophosphate ester flame retardants and plasticizers in ocean sediments from the North Pacific to the Arctic Ocean [J]. Environmental Science & Technology, 2017, 51(7): 3809-3815. [10] LI J, XIE Z, MI W, et al. Organophosphate esters in air, snow, and seawater in the North Atlantic and the Arctic [J]. Environmental Science & Technology, 2017, 51(12): 6887-6896. [11] 王艺璇, 段玉双, 耿存珍. 有机磷酸酯在水环境中的残留及生态风险评价 [J]. 环境与健康杂志, 2015, 32(10): 935-939. WANG Y X, DUAN Y S, GENG C Z. Occurrence of organophosphate ester in aquatic environment and ecological risk assessment. [J]. Journal of Environment and Health, 2015, 32(10): 935-939(in Chinese).
[12] 刘佳. 有机磷酸酯阻燃剂污染现状及降解过程研究进展 [J]. 应用化工, 2018, 47(12): 2705-2710, 2714. doi: 10.3969/j.issn.1671-3206.2018.12.036 LIU J. Review of contamination status and degradation processes of organophosphate ester (OPE) flame retardants [J]. Applied Chemical Industry, 2018, 47(12): 2705-2710, 2714(in Chinese). doi: 10.3969/j.issn.1671-3206.2018.12.036
[13] 王雪松, 李志娟, 李青山, 等. 磷系阻燃剂的应用与展望 [J]. 化工时刊, 2001(6): 1-5. doi: 10.3969/j.issn.1002-154X.2001.06.001 WANG X S, LI Z J, LI Q S, et al. Application and prospect of phosphorus flame retardant [J]. Chemical Industry Times, 2001(6): 1-5(in Chinese). doi: 10.3969/j.issn.1002-154X.2001.06.001
[14] ANDRESEN J A, GRUNDMANN A, BESTER K. Organophosphorus flame retardants and plasticisers in surface waters [J]. Science of the Total Environment, 2004, 332(1-3): 155-166. doi: 10.1016/j.scitotenv.2004.04.021 [15] SCHREDER E D, LA GUARDIA M J. Flame retardant transfers from U. S. households (dust and laundry wastewater) to the aquatic environment [J]. Environmental Science & Technology, 2014, 48(19): 11575-11583. [16] CRISTALE J, GARCIA VAZQUEZ A, BARATA C, et al. Priority and emerging flame retardants in rivers: occurrence in water and sediment, daphnia magna toxicity and risk assessment [J]. Environment International, 2013, 59: 232-243. doi: 10.1016/j.envint.2013.06.011 [17] 李成辉, 张冬蕊, 李胜红, 等. 污水处理厂中有机磷酸酯的研究进展 [J]. 生态毒理学报, 2019, 14(6): 32-46. LI C H, ZHANG D R, LI S H, et al. A review on the occurrence of organophosphate esters in wastewater treatment plants [J]. Asian Journal of Ecotoxicology, 2019, 14(6): 32-46(in Chinese).
[18] PANG L, YUAN Y, HE H, et al. Occurrence, distribution, and potential affecting factors of organophosphate flame retardants in sewage sludge of wastewater treatment plants in Henan Province, Central China [J]. Chemosphere, 2016, 152: 245-251. doi: 10.1016/j.chemosphere.2016.02.104 [19] GAO L, SHI Y, LI W, et al. Occurrence and distribution of organophosphate triesters and diesters in sludge from sewage treatment plants of Beijing, China [J]. Science of the Total Environment, 2016, 544: 143-149. doi: 10.1016/j.scitotenv.2015.11.094 [20] ZENG X, HE L, CAO S, et al. Occurrence and distribution of organophosphate flame retardants/plasticizers in wastewater treatment plant sludges from the Pearl River Delta, China [J]. Environmental Toxicology and Chemistry, 2014, 33(8): 1720-1725. doi: 10.1002/etc.2604 [21] 孙佳薇, 丁炜楠, 张占恩, 等. 污水处理厂中有机磷阻燃剂的污染特征 [J]. 环境科学, 2018, 39(5): 2230-2238. SUN J W, DING W N, ZHANG Z E, et al. Pollution characteristics of organophosphorus flame retardants in a wastewater treatment plant [J]. Environmental Science, 2018, 39(5): 2230-2238(in Chinese).
[22] 赵赛, 刘世龙, 张华, 等. 污水处理工艺对有机磷酸酯的去除效果 [J]. 中国给水排水, 2018, 34(5): 88-91. ZHAO S, LIU S L, ZHANG H, et al. Removal efficiency of organophosphate esters in wastewater treatment processes [J]. China Water & Wastewater, 2018, 34(5): 88-91(in Chinese).
[23] XU L, HU Q, LIU J, et al. Occurrence of organophosphate esters and their diesters degradation products in industrial wastewater treatment plants in China: Implication for the usage and potential degradation during production processing [J]. Environment Pollution, 2019, 250: 559-566. doi: 10.1016/j.envpol.2019.04.058 [24] WOUDNEH M B,BENSKIN J P,WANG J H,et al. Quantitative determination of 13 organophosphorous flame retardants and plasticizers in a wastewater treatment system by high performance liquid chromatography tandem mass spectrometry [J]. Journal of Chromatography A, 2015, 1400(26): 149-155. [25] KIM U J, OH J K, KANNAN K. Occurrence, removal, and environmental emission of organophosphate flame retardants/plasticizers in a wastewater treatment plant in New York State [J]. Environmental Science & Technology, 2017, 51(14): 7872-7880. [26] WANG R, TANG J, XIE Z, et al. Occurrence and spatial distribution of organophosphate ester flame retardants and plasticizers in 40 rivers draining into the Bohai Sea, north China [J]. Environment Pollution, 2015, 198: 172-178. doi: 10.1016/j.envpol.2014.12.037 [27] 陈玫宏, 徐怀洲, 宋宁慧, 等. 高效液相色谱-串联质谱法同时测定水体和沉积物中12种有机磷酸酯类化合物 [J]. 分析化学, 2017, 45(7): 987-995. doi: 10.11895/j.issn.0253-3820.170180 CHEN M H, XU H Z, SONG N H, et al. Simultaneous determination of 12 kinds of organophosphates in water and sediment by high performance liquid chromatography-tandem mass spectrometry [J]. Chinese Journal of Analytical Chemistry, 2017, 45(7): 987-995(in Chinese). doi: 10.11895/j.issn.0253-3820.170180
[28] LIU Y, SONG N, GUO R, et al. Occurrence and partitioning behavior of organophosphate esters in surface water and sediment of a shallow Chinese freshwater lake (Taihu Lake): Implication for eco-toxicity risk [J]. Chemosphere, 2018, 202: 255-263. doi: 10.1016/j.chemosphere.2018.03.108 [29] 吴迪, 印红玲, 李世平, 等. 成都市锦江表层水和沉积物中有机磷酸酯的污染特征 [J]. 环境科学, 2019, 40(3): 1245-1251. WU D, YIN H L, LI S P, et al. Pollution characteristics of OPEs in the surface water and sediment of the Jinjiang River in Chengdu City [J]. Environmental Science, 2019, 40(3): 1245-1251(in Chinese).
[30] 刘静, 何丽雄, 曾祥英, 等. 珠江主干和东江河流表层沉积物中有机磷酸酯阻燃剂/增塑剂分布 [J]. 生态毒理学报, 2016, 11(2): 436-443. LIU J, HE L X, ZENG X Y, et al. Occurrence and distribution of organophosphorus flame retardants/plasticizer in surface sediments from the Pearl River and Dongjiang River [J]. Asian Journal of Ecotoxicology, 2016, 11(2): 436-443(in Chinese).
[31] TAN X X, LUO X J, ZHENG X B, et al. Distribution of organophosphorus flame retardants in sediments from the Pearl River Delta in South China [J]. Science of the Total Environment, 2016, 544: 77-84. doi: 10.1016/j.scitotenv.2015.11.089 [32] ZENG X, XU L, LIU J, et al. Occurrence and distribution of organophosphorus flame retardants/plasticizers and synthetic musks in sediments from source water in the Pearl River Delta, China [J]. Environmental Toxicology and Chemistry, 2018, 37(4): 975-982. doi: 10.1002/etc.4040 [33] SHI Y, ZHANG Y, DU Y, et al. Occurrence, composition and biological risk of organophosphate esters (OPEs) in water of the Pearl River Estuary, South China [J]. Environmental Science and Pollution Research, 2020, 27(13): 14852-14862. doi: 10.1007/s11356-020-08001-1 [34] KIM U J, KANNAN K. Occurrence and distribution of organophosphate flame retardants/plasticizers in surface waters, tap water, and rainwater: Implications for human exposure [J]. Environmental Science & Technology, 2018, 52(10): 5625-5633. [35] WOLSCHKE H, SUHRING R, XIE Z, et al. Organophosphorus flame retardants and plasticizers in the aquatic environment: A case study of the Elbe River, Germany [J]. Environment Pollution, 2015, 206: 488-493. doi: 10.1016/j.envpol.2015.08.002 [36] LI J, YU N, ZHANG B, et al. Occurrence of organophosphate flame retardants in drinking water from China [J]. Water Research, 2014, 54: 53-61. doi: 10.1016/j.watres.2014.01.031 [37] 朱孔睿. 水中有机磷酸酯阻燃剂分析方法的建立及在不同饮用水处理工艺中的去除研究[D]. 重庆: 重庆大学, 2017. ZHU K R. Establishment of analytical method for organophosphate flame retardant in water and its removal in different drinking water treatment processes[D]. Chongqing: Chongqing University, 2017 (in Chinese).
[38] CRISTALE J, QUINTANA J, CHALER R, et al. Gas chromatography/mass spectrometry comprehensive analysis of organophosphorus, brominated flame retardants, by-products and formulation intermediates in water [J]. Journal of Chromatography A, 2012, 1241: 1-12. doi: 10.1016/j.chroma.2012.04.013 [39] ZENG Y, DING N, WANG T, et al. Organophosphate esters (OPEs) in fine particulate matter (PM2.5) in urban, e-waste, and background regions of south China [J]. Journal of Hazardous Materials, 2020, 385: 121583. doi: 10.1016/j.jhazmat.2019.121583 [40] WANG T, DING N, WANG T, et al. Organophosphorus esters (OPEs) in PM2.5 in urban and e-waste recycling regions in southern China: Concentrations, sources, and emissions [J]. Environmental Research, 2018, 167: 437-444. doi: 10.1016/j.envres.2018.08.015 [41] LIANG Y, WANG H, YANG Q, et al. Spatial distribution and seasonal variations of atmospheric organophosphate esters (OPEs) in Tianjin, China based on gridded field observations [J]. Environment Pollution, 2020, 263: 114460. doi: 10.1016/j.envpol.2020.114460 [42] LI J, TANG J, MI W, et al. Spatial distribution and seasonal variation of organophosphate esters in air above the Bohai and Yellow Seas, China [J]. Environmental Science & Technology, 2018, 52(1): 89-97. [43] NA G, HOU C, LI R, et al. Occurrence, distribution, air-seawater exchange and atmospheric deposition of organophosphate esters (OPEs) from the Northwestern Pacific to the Arctic Ocean [J]. Marine Pollution Bulletin, 2020, 157: 111243. doi: 10.1016/j.marpolbul.2020.111243 [44] 侯超. 极地大气有机磷酸酯介质分配机制研究[D]. 上海: 上海海洋大学, 2020. HOU C. Research on the medium partitioning mechanism of atmospheric organophosphate esters in polar regions[D]. Shanghai: Shanghai Ocean University, 2020(in Chinese).
[45] SALAMOVA A, MA Y, VENIER M, et al. High levels of organophosphate flame retardants in the Great Lakes atmosphere [J]. Environmental Science & Technology Letters, 2013, 1(1): 8-14. [46] WU Y, VENIER M, SALAMOVA A. Spatioseasonal variations and partitioning behavior of organophosphate esters in the Great Lakes atmosphere [J]. Environmental Science & Technology, 2020, 54(9): 5400-5408. [47] 房晓静, 杨圣文, 张洪海, 等. 海洋及其上空大气中有机磷酸酯的研究进展 [J]. 海洋科学, 2020, 44(9): 154-165. FANG X J, YANG S W, ZHANG H H, et al. Review of organophosphate esters in oceans and atmospheres [J]. Marine Sciences, 2020, 44(9): 154-165(in Chinese).
[48] CASTRO-JIMENEZ J, BERROJALBIZ N, PIZARRO M, et al. Organophosphate ester (OPE) flame retardants and plasticizers in the open Mediterranean and Black Seas atmosphere [J]. Environmental Science & Technology, 2014, 48(6): 3203-3209. [49] CASTRO-JIMÉNEZ J, SEMPéRé R. Atmospheric particle-bound organophosphate ester flame retardants and plasticizers in a North African Mediterranean coastal city (Bizerte, Tunisia) [J]. Science of the Total Environment, 2018, 642: 383-393. doi: 10.1016/j.scitotenv.2018.06.010 [50] MOLLER A, STURM R, XIE Z, et al. Organophosphorus flame retardants and plasticizers in airborne particles over the Northern Pacific and Indian Ocean toward the Polar Regions: Evidence for global occurrence [J]. Environmental Science & Technology, 2012, 46(6): 3127-3134. [51] CHENG W, XIE Z, BLAIS J M, et al. Organophosphorus esters in the oceans and possible relation with ocean gyres [J]. Environment Pollution, 2013, 180: 159-164. doi: 10.1016/j.envpol.2013.05.032 [52] WANG C, WANG P, ZHAO J, et al. Atmospheric organophosphate esters in the Western Antarctic Peninsula over 2014-2018: Occurrence, temporal trend and source implication [J]. Environment Pollution, 2020, 267: 115428. doi: 10.1016/j.envpol.2020.115428 [53] HE C T, ZHENG J, QIAO L, et al. Occurrence of organophosphorus flame retardants in indoor dust in multiple microenvironments of southern China and implications for human exposure [J]. Chemosphere, 2015, 133: 47-52. doi: 10.1016/j.chemosphere.2015.03.043 [54] CHRISTIA C, TANG B, YIN S S, et al. Simultaneous determination of legacy and emerging organophosphorus flame retardants and plasticizers in indoor dust using liquid and gas chromatography–tandem mass spectrometry: method development, validation, and application [J]. Analytical and Bioanalytical Chemistry, 2019, 411(26): 7015-7025. doi: 10.1007/s00216-019-02078-5 [55] WANG L, JIA Y, KANG Q, et al. Nontarget discovery of 11 aryl organophosphate triesters in house dust using high-resolution mass spectrometry [J]. Environmental Science & Technology, 2020, 54(18): 11376-11385. [56] DU B, SHEN M, CHEN H, et al. Beyond traditional organophosphate triesters: Prevalence of emerging organophosphate triesters and organophosphate diesters in indoor dust from a mega e-waste recycling industrial park in south China[J]. Environmental Science & Technology, 2020, 54(19): 12001. [57] TAN H, YANG L, YU Y, et al. Co-existence of organophosphate di- and tri-esters in house dust from south China and midwestern United States: Implications for human exposure [J]. Environmental Science & Technology, 2019, 53(9): 4784-4793. [58] FANG M, WEBSTER T F, GOODEN D, et al. Investigating a novel flame retardant known as V6: Measurements in baby products, house dust, and car dust [J]. Environmental Science & Technology, 2013, 47(9): 4449-4454. [59] CEQUIER E, IONAS A C, COVACI A, et al. Occurrence of a broad range of legacy and emerging flame retardants in indoor environments in Norway [J]. Environmental Science & Technology, 2014, 48(12): 6827-6835. [60] BRANDSMA S H, DE BOER J, VAN VELZEN M J, et al. Organophosphorus flame retardants (PFRs) and plasticizers in house and car dust and the influence of electronic equipment [J]. Chemosphere, 2014, 116: 3-9. doi: 10.1016/j.chemosphere.2014.02.036 [61] ABDALLAH M A, COVACI A. Organophosphate flame retardants in indoor dust from Egypt: implications for human exposure [J]. Environmental Science & Technology, 2014, 48(9): 4782-4789. [62] 温家欣. 有机磷酸酯阻燃剂的分离分析技术及其应用研究[D]. 广州: 中山大学, 2010. WEN J X. Separation and analysis of organophosphate flame retardant and its application[D]. Guangzhou: Sun Yat-sen University, 2010 .
[63] CUI K, WEN J, ZENG F, et al. Occurrence and distribution of organophosphate esters in urban soils of the subtropical city, Guangzhou, China [J]. Chemosphere, 2017, 175: 514-520. doi: 10.1016/j.chemosphere.2017.02.070 [64] 印红玲, 李世平, 叶芝祥, 等. 成都市土壤中有机磷阻燃剂的污染特征及来源分析 [J]. 环境科学学报, 2016, 36(2): 606-613. YIN H L, LI S P, YE Z X, et al. Pollution characteristics and sources of OPEs in the soil of Chengdu City [J]. Acta Scientiae Circumstantiae, 2016, 36(2): 606-613(in Chinese).
[65] HE J, LI J, MA L, et al. Large-scale distribution of organophosphate esters (flame retardants and plasticizers) in soil from residential area across China: Implications for current level [J]. Science of the Total Environment, 2019, 697: 133997. doi: 10.1016/j.scitotenv.2019.133997 [66] WANG Y, YAO Y, LI W, et al. A nationwide survey of 19 organophosphate esters in soils from China: Spatial distribution and hazard assessment [J]. Science of the Total Environment, 2019, 671: 528-535. doi: 10.1016/j.scitotenv.2019.03.335 [67] ELKE F, IVANA M. Pollution of soils with organophosphorus flame retardants and plasticizers [J]. Journal of Environmental Monitoring, 2011, 13(10): 2692-2694. doi: 10.1039/c1em10538h [68] KURT-KARAKUS P, ALEGRIA H, BIRGUL A, et al. Organophosphate ester (OPEs) flame retardants and plasticizers in air and soil from a highly industrialized city in Turkey [J]. Science of the Total Environment, 2018, 625: 555-565. doi: 10.1016/j.scitotenv.2017.12.307 [69] YADAV I C, DEVI N L, LI J, et al. Concentration and spatial distribution of organophosphate esters in the soil-sediment profile of Kathmandu Valley, Nepal: Implication for risk assessment [J]. Science of the Total Environment, 2018, 613-614: 502-512. doi: 10.1016/j.scitotenv.2017.09.039 [70] WAN W, ZHANG S, HUANG H, et al. Occurrence and distribution of organophosphorus esters in soils and wheat plants in a plastic waste treatment area in China [J]. Environment Pollution, 2016, 214: 349-353. doi: 10.1016/j.envpol.2016.04.038 [71] PANG L, LIU J, YIN Y, et al. Evaluating the sorption of organophosphate esters to different sourced humic acids and its effects on the toxicity to Daphnia magna [J]. Environmental Toxicology and Chemistry, 2013, 32(12): 2755-2761. doi: 10.1002/etc.2360 [72] SANTIN G, ELJARRAT E, BARCELO D. Simultaneous determination of 16 organophosphorus flame retardants and plasticizers in fish by liquid chromatography-tandem mass spectrometry [J]. Journal of Chromatography A, 2016, 1441: 34-43. doi: 10.1016/j.chroma.2016.02.058 [73] 索莉莉, 朱群英, 胡美华. 超声辅助萃取-液相色谱-串联质谱法同时检测水产品中11种有机磷酸酯类阻燃剂 [J]. 食品工业科技, 2018, 39(6): 210-216. SUO L L, ZHU Q Y, HU M H, et al. Simultaneous determination of 11 organophosphate esters in aquatic product by ultrasound-assisted extraction coupled with LC-MS/MS [J]. Science and Technology of Food Industry, 2018, 39(6): 210-216(in Chinese).
[74] BEKELE T G, ZHAO H, WANG Q, et al. Bioaccumulation and trophic transfer of emerging organophosphate flame retardants in the marine food webs of Laizhou Bay, north China [J]. Environmental Science & Technology, 2019, 53(22): 13417-13426. [75] GREAVES A K, LETCHER R J. Comparative body compartment composition and in ovo transfer of organophosphate flame retardants in North American Great Lakes herring gulls [J]. Environmental Science & Technology, 2014, 48(14): 7942-7950. [76] LU Z, MARTIN P A, BURGESS N M, et al. Volatile methylsiloxanes and organophosphate esters in the eggs of European starlings (Sturnus vulgaris) and congeneric gull species from locations across Canada [J]. Environmental Science & Technology, 2017, 51(17): 9836-9845. [77] FERNIE K J, PALACE V, PETERS L E, et al. Investigating endocrine and physiological parameters of captive American kestrels exposed by diet to selected organophosphate flame retardants [J]. Environmental Science & Technology, 2015, 49(12): 7448-7455. [78] LIU Q, WANG X, YANG R, et al. Uptake kinetics, accumulation, and long-distance transport of organophosphate esters in plants: Impacts of chemical and plant properties [J]. Environmental Science & Technology, 2019, 53(9): 4940-4947. [79] TAN H, CHEN D, PENG C, et al. Novel and Traditional organophosphate esters in house dust from South China: Association with hand wipes and exposure estimation[J]. Environmental Science & Technology. 2018, 52(19): 11017-11026. [80] 符元证, 史亚利, 逯晓波, 等. 有机磷酸酯阻燃剂暴露的毒性效应及生物标志物研究进展 [J]. 中华预防医学杂志, 2020, 54(10): 1152-1160. FU Y Z, SHI Y L, L X B, et al. Research progress on toxic effects and biomarkers of organophosphate ester flame retartant exposure [J]. Chinese Journal of Preventive Medicine, 2020, 54(10): 1152-1160(in Chinese).
[81] LI P, ZENG X Y, CUI J T, et al. Determination of seven urinary metabolites of organophosphate esters using liquid chromatography-tandem mass spectrometry [J]. Chinese Journal of Analytical Chemistry, 2017, 45(11): 1648-1654. doi: 10.1016/S1872-2040(17)61048-X [82] CEQUIER E, MARCE R M, BECHER G, et al. A high-throughput method for determination of metabolites of organophosphate flame retardants in urine by ultra performance liquid chromatography-high resolution mass spectrometry [J]. Analytica Chimica Acta, 2014, 845: 98-104. doi: 10.1016/j.aca.2014.06.026 [83] CRAIG J A, CEBALLOS D M, FRUH V, et al. Exposure of nail salon workers to phthalates, di(2-ethylhexyl) terephthalate, and organophosphate esters: A pilot study [J]. Environmental Science & Technology, 2019, 53(24): 14630-14637. [84] HOFFMAN K, BUTT C M, WEBSTER T F, et al. Temporal trends in exposure to organophosphate flame retardants in the United States [J]. Environmental Science & Technology Letters, 2017, 4(3): 112-118. [85] LIU L Y, HE K, HITES R A, et al. Hair and nails as noninvasive biomarkers of human exposure to brominated and organophosphate flame retardants [J]. Environmental Science & Technology, 2016, 50(6): 3065-3073. [86] KIM J W, ISOBE T, MUTO M, et al. Organophosphorus flame retardants (PFRs) in human breast milk from several Asian countries [J]. Chemosphere, 2014, 116: 91-97. doi: 10.1016/j.chemosphere.2014.02.033 [87] 孙敦宇, 杨绍贵, 向伟铭, 等. 有机磷酸酯阻燃剂降解方法的研究进展 [J]. 环境化学, 2021, 40(2): 474-486. doi: 10.7524/j.issn.0254-6108.2020051603 SUN D Y, YANG S G, XIANG W M, et al. Research progress on degradation methods of organophosphorus flame retardants [J]. Environmental Chemistry, 2021, 40(2): 474-486(in Chinese). doi: 10.7524/j.issn.0254-6108.2020051603
[88] FANG Y, KIM E, STRATHMANN T J. Mineral- and base-catalyzed hydrolysis of organophosphate flame retardants: Potential major fate-controlling sink in soil and aquatic environments [J]. Environmental Science & Technology, 2018, 52(4): 1997. [89] SU G, LETCHER R J, YU H. Organophosphate flame retardants and plasticizers in aqueous solution: pH-dependent hydrolysis, kinetics, and pathways [J]. Environmental Science & Technology, 2016, 50(15): 8103-8111. [90] 庞龙, 张肖静, 庞榕, 等. 城市污水处理工艺对有机磷酸酯类化合物的去除 [J]. 河南师范大学学报(自然科学版), 2016, 44(3): 98-103. PANG L, ZHANG X J, PANG R, et al. Removal of organophosphate esters in municipal wastewater treatment process [J]. Journal of Henan Normal University(Natural Science Edition), 2016, 44(3): 98-103(in Chinese).
[91] CRISTALE J, DANTAS R F, DE LUCA A, et al. Role of oxygen and DOM in sunlight induced photodegradation of organophosphorous flame retardants in river water [J]. Journal of Hazardous Materials, 2017, 323: 242-249. doi: 10.1016/j.jhazmat.2016.05.019 [92] SUN S, JIANG J, ZHAO H, et al. Photochemical reaction of tricresyl phosphate (TCP) in aqueous solution: Influencing factors and photolysis products [J]. Chemosphere, 2020, 241: 124971. doi: 10.1016/j.chemosphere.2019.124971 [93] KULKARNI S V, MARKAD V L, MELO J S, et al. Biodegradation of tributyl phosphate using Klebsiella pneumoniae sp. S3 [J]. Applied Microbiology and Biotechnology, 2013, 98(2): 919-929. [94] LIU J, LIN H, DONG Y, et al. Elucidating the biodegradation mechanism of tributyl phosphate (TBP) by Sphingomonas sp. isolated from TBP-contaminated mine tailings [J]. Environment Pollution, 2019, 250: 284-291. doi: 10.1016/j.envpol.2019.03.127 [95] 卫昆. 磷酸三苯酯的微生物降解机制及其降解产物毒性研究[D]. 广州: 华南理工大学, 2018. WEI K. Biodegradation mechanism of triphenyl phosphate and toxicity of its metabolites[D]. Guangzhou: South China University of Technology, 2018(in Chinese).
[96] JURGENS S S, HELMUS R, WAAIJERS S L, et al. Mineralisation and primary biodegradation of aromatic organophosphorus flame retardants in activated sludge [J]. Chemosphere, 2014, 111: 238-242. doi: 10.1016/j.chemosphere.2014.04.016 [97] LIU Y, YIN H, WEI K, et al. Biodegradation of tricresyl phosphate isomers by Brevibacillus brevis: Degradation pathway and metabolic mechanism [J]. Chemosphere, 2019, 232: 195-203. doi: 10.1016/j.chemosphere.2019.05.188 [98] SHOUJI T, IKUKO S, ISAO K, et al. Isolation and identification of persistent chlorinated organophosphorus flame retardant-degrading bacteria [J]. Applied and Environmental Microbiology, 2010, 76(15): 5292-5296. doi: 10.1128/AEM.00506-10 [99] TAKAHASHI S, MIURA K, ABE K, et al. Complete detoxification of tris(2-chloroethyl) phosphate by two bacterial strains: Sphingobium sp. strain TCM1 and Xanthobacter autotrophicus strain GJ10 [J]. Journal of Bioscience and Bioengineering, 2012, 114(3): 306-311. doi: 10.1016/j.jbiosc.2012.04.010 [100] TAKAHASHI S, OBANA Y, OKADA S, et al. Complete detoxification of tris(1, 3-dichloro-2-propyl) phosphate by mixed two bacteria, Sphingobium sp. strain TCM1 and Arthrobacter sp. strain PY1 [J]. Journal of Bioscience and Bioengineering, 2012, 113(1): 79-83. doi: 10.1016/j.jbiosc.2011.08.020 [101] HOU R, XU Y, WANG Z. Review of OPFRs in animals and humans: Absorption, bioaccumulation, metabolism, and internal exposure research [J]. Chemosphere, 2016, 153: 78-90. doi: 10.1016/j.chemosphere.2016.03.003 [102] REEMTSMA T, LINGOTT J, ROEGLER S. Determination of 14 monoalkyl phosphates, dialkyl phosphates and dialkyl thiophosphates by LC-MS/MS in human urinary samples [J]. Science of the Total Environment, 2011, 409(10): 1990-1993. doi: 10.1016/j.scitotenv.2011.01.032 [103] 汪国威. 有机磷酸酯阻燃剂在鱼体内的富集、分布和代谢及其机制[D]. 南京: 南京大学, 2017. WANG G W. Accumulation, distribution and transformation of organophosphate flame retardants in fish and their underlying mechanism[D]. Nanjing: Nanjing University, 2017(in Chinese).
[104] 杜仲坤. 常用有机磷酸酯阻燃剂对斑马鱼发育及肝脏代谢的影响[D]. 南京: 南京大学, 2016. DU Z K. Effects of organophosphate flame retardants on zebrafish embryo development and liver metabolism[D]. Nanjing: Nanjing University, 2016(in Chinese).
[105] VAN DEN EEDE N, ERRATICO C, EXARCHOU V, et al. In vitro biotransformation of tris(2-butoxyethyl) phosphate (TBOEP) in human liver and serum [J]. Toxicology and Applied Pharmacology, 2015, 284(2): 246-253. doi: 10.1016/j.taap.2015.01.021 [106] VAN DEN EEDE N, MAHO W, ERRATICO C, et al. First insights in the metabolism of phosphate flame retardants and plasticizers using human liver fractions [J]. Toxicology Letters, 2013, 223(1): 9-15. doi: 10.1016/j.toxlet.2013.08.012 [107] GREAVES A K, SU G, LETCHER R J. Environmentally relevant organophosphate triesters in herring gulls: In vitro biotransformation and kinetics and diester metabolite formation using a hepatic microsomal assay [J]. Toxicology and Applied Pharmacology, 2016, 308: 59-65. doi: 10.1016/j.taap.2016.08.007 [108] HAN X, HAO Y, LI Y, et al. Occurrence and distribution of organophosphate esters in the air and soils of Ny-Alesund and London Island, Svalbard, Arctic[J]. Environment Pollution, 2020, 263(Pt A): 114495. [109] 徐怀洲, 王智志, 张圣虎, 等. 有机磷酸酯类阻燃剂毒性效应研究进展 [J]. 生态毒理学报, 2018, 13(3): 19-30. doi: 10.7524/AJE.1673-5897.20170601001 XU H Z, WANG Z Z, ZHANG S H, et al. Research progress on toxicity effects of organophosphate flame retardants [J]. Asian Journal of Ecotoxicology, 2018, 13(3): 19-30(in Chinese). doi: 10.7524/AJE.1673-5897.20170601001
[110] HOFFMAN K, DANIELS J L, STAPLETON H M. Urinary metabolites of organophosphate flame retardants and their variability in pregnant women [J]. Environment International, 2014, 63: 169-172. doi: 10.1016/j.envint.2013.11.013 [111] LI J, ZHAO L, LETCHER R J, et al. A review on organophosphate Ester (OPE) flame retardants and plasticizers in foodstuffs: Levels, distribution, human dietary exposure, and future directions [J]. Environment International, 2019, 127: 35-51. doi: 10.1016/j.envint.2019.03.009 [112] YANG J, ZHAO Y, LI M, et al. A review of a class of emerging contaminants: the classification, distribution, intensity of consumption, synthesis routes, environmental effects and expectation of pollution abatement to organophosphate flame retardants (OPFRs) [J]. International Journal of Molecular Sciences, 2019, 20(12): 2874. doi: 10.3390/ijms20122874 [113] 单岳, 王诗雨, 谷雷严, 等. 有机磷酸酯暴露水平与毒性效应的研究进展 [J]. 环境科学与管理, 2019, 44(6): 15-18. doi: 10.3969/j.issn.1673-1212.2019.06.004 SHAN Y, WANG S Y, GU L Y, et al. Research progress on exposure levels and toxic effects of organophosphates [J]. Environmental Science and Management, 2019, 44(6): 15-18(in Chinese). doi: 10.3969/j.issn.1673-1212.2019.06.004
[114] FARHAT A, CRUMP D, CHIU S, et al. In Ovo effects of two organophosphate flame retardants-TCPP and TDCPP-on pipping success, development, mRNA expression, and thyroid hormone levels in chicken embryos [J]. Toxicological Sciences, 2013, 134(1): 92-102. doi: 10.1093/toxsci/kft100 [115] ZHU Y, MA X, SU G, et al. Environmentally relevant concentrations of the flame retardant tris(1, 3-dichloro-2-propyl) phosphate inhibit growth of female zebrafish and decrease fecundity [J]. Environmental Science & Technology, 2015, 49(24): 14579-14587. [116] DASGUPTA S, CHENG V, VLIET S M F, et al. Tris(1, 3-dichloro-2-propyl) phosphate exposure during the early-blastula stage alters the normal trajectory of zebrafish embryogenesis [J]. Environmental Science & Technology, 2018, 52(18): 10820-10828. [117] ZHU Y, ZHANG J, LIU Y, et al. Environmentally relevant concentrations of the flame retardant tris(1, 3-dichloro-2-propyl) phosphate inhibit the growth and reproduction of earthworms in soil [J]. Environmental Science & Technology Letters, 2019, 6(5): 277-282. [118] DISHAW L V, POWERS C M, RYDE I T, et al. Is the penta BDE replacement, tris (1, 3-dichloro-2-propyl) phosphate (TDCPP), a developmental neurotoxicant? Studies in PC12 cells [J]. Toxicology and Applied Pharmacology, 2011, 256(3): 281-289. doi: 10.1016/j.taap.2011.01.005 [119] MEEKER J D, STAPLETON H M. House dust concentrations of organophosphate flame retardants in relation to hormone levels and semen quality parameters [J]. Environmental Health Perspectives, 2010, 118(3): 318-323. doi: 10.1289/ehp.0901332 [120] 李素珍, 付卫强, 冯承莲. 有机磷酸酯阻燃剂的环境暴露、环境行为和毒性效应研究进展 [J]. 环境工程, 2018, 36(9): 180-184,35. LI S Z, FU W Q, FENG C L. Research progress in envionmental exposure, behaviour and toxic effect of organophosphorus flame retardants [J]. Environmental Engineering, 2018, 36(9): 180-184,35(in Chinese).
[121] HONG X, CHEN R, HOU R, et al. Triphenyl phosphate (TPHP)-induced neurotoxicity in adult male Chinese rare minnows (Gobiocypris rarus) [J]. Environmental Science & Technology, 2018, 52(20): 11895-11903. [122] LI Y, KANG Q, CHEN R, et al. 2-Ethylhexyl diphenyl phosphate and its hydroxylated metabolites are anti-androgenic and cause adverse reproductive outcomes in male Japanese Medaka (Oryzias latipes) [J]. Environmental Science & Technology, 2020, 54(14): 8919-8925. [123] YU X, YIN H, PENG H, et al. OPFRs and BFRs induced A549cell apoptosis by caspase-dependent mitochondrial pathway [J]. Chemosphere, 2019, 221: 693-702. doi: 10.1016/j.chemosphere.2019.01.074 [124] YAN S, WANG Q, YANG L, et al. Comparison of the toxicity effects of tris(1, 3-dichloro-2-propyl)phosphate (TDCIPP) with tributyl phosphate (TNBP) reveals the mechanism of the apoptosis pathway in Asian freshwater clams (Corbicula fluminea) [J]. Environmental Science & Technology, 2020, 54(11): 6850-6858. [125] 杨扬. 有机磷酸酯(OPEs)对赤子爱胜蚓的毒性效应及机制研究[D]. 南京: 南京大学, 2018. YANG Y. Ecotoxicity effect and mechanism of organophosphorus esters(OPEs)on earthworm Eisenia fetida[D]. Nanjing: Nanjing University, 2018.
[126] 顾杰, 顾爱华, 石利利, 等. 有机磷酸酯环境分布及神经毒性研究进展 [J]. 环境与健康杂志, 2018, 35(3): 277-281. GU J, GU A H, SHI L L, et al. Environmental distribution and neurotoxicity of organic phosphate: A review of recent studies [J]. Journal of Environment and Health, 2018, 35(3): 277-281(in Chinese).
[127] TA N, LI C, FANG Y, et al. Toxicity of TDCPP and TCEP on PC12 cell: Changes in CAMKII, GAP43, tubulin and NF-H gene and protein levels [J]. Toxicology Letters, 2014, 227(3): 164-171. doi: 10.1016/j.toxlet.2014.03.023 [128] DU Z, WANG G, GAO S, et al. Aryl organophosphate flame retardants induced cardiotoxicity during zebrafish embryogenesis: By disturbing expression of the transcriptional regulators [J]. Aquatic Toxicology, 2015, 161: 25-32. doi: 10.1016/j.aquatox.2015.01.027 [129] SU G, CRUMP D, LETCHER R J, et al. Rapid in vitro metabolism of the flame retardant triphenyl phosphate and effects on cytotoxicity and mRNA expression in chicken embryonic hepatocytes [J]. Environmental Science & Technology, 2014, 48(22): 13511-13519. [130] 闫振飞, 廖伟, 冯承莲, 等. 典型有机磷酸酯阻燃剂分析方法研究进展 [J]. 生态毒理学报, 2020, 15(1): 94-108. doi: 10.7524/AJE.1673-5897.20190509002 YAN Z F, LIAO W, FENG C L, et al. Research progress on analysis methods of typical organophosphate esters ( OPEs) flame retardants [J]. Asian Journal of Ecotoxicology, 2020, 15(1): 94-108(in Chinese). doi: 10.7524/AJE.1673-5897.20190509002
[131] MARTíNEZ-CARBALLO E, GONZáLEZ-BARREIRO C, SITKA A, et al. Determination of selected organophosphate esters in the aquatic environment of Austria [J]. Science of the Total Environment, 2007, 388(1): 290-299. [132] 高立红. 北京市城市环境有机磷酸酯污染水平和分布特征研究[D]. 北京: 北京科技大学, 2016. GAO L H. Study on pollution level and distribution characteristics of organophosphate esters in urban environment of Beijing[D]. Beijing: Beijing University of Science and Technology, 2016(in Chinese).
[133] 严小菊. 典型有机磷酸酯阻燃剂在太湖水体和底泥中存在水平和分布特征[D]. 南京: 南京大学, 2013. YAN X J. The level and distribution of typical organophosphate flame retardants in water and sediment of Taihu Lake[D]. Nanjing: Nanjing University, 2013(in Chinese) .
[134] RODRíGUEZ I, CALVO F, QUINTANA J B, et al. Suitability of solid-phase microextraction for the determination of organophosphate flame retardants and plasticizers in water samples [J]. Journal of Chromatography A, 2006, 1108(2): 158-165. doi: 10.1016/j.chroma.2006.01.008 [135] QUINTANA J B, REEMTSMA T. Potential of membrane-assisted solvent extraction for the determination of phosphoric acid triesters in wastewater samples by liquid chromatography–tandem mass spectrometry [J]. Journal of Chromatography A, 2006, 1124(1): 22-28. [136] GARCíA-LóPEZ M, RODRíGUEZ I, CELA R. Development of a dispersive liquid-liquid microextraction method for organophosphorus flame retardants and plastizicers determination in water samples [J]. Journal of Chromatography A, 2007, 1166(1-2): 9-15. doi: 10.1016/j.chroma.2007.08.006 [137] CRISTALE J, LACORTE S. Development and validation of a multiresidue method for the analysis of polybrominated diphenyl ethers, new brominated and organophosphorus flame retardants in sediment, sludge and dust [J]. Journal of Chromatography A, 2013, 1305(1): 267-275. [138] MOLLER A, XIE Z, CABA A, et al. Organophosphorus flame retardants and plasticizers in the atmosphere of the North Sea [J]. Environment Pollution, 2011, 159(12): 3660-3665. doi: 10.1016/j.envpol.2011.07.022 [139] CAO D, GUO J, WANG Y, et al. Organophosphate esters in sediment of the Great Lakes [J]. Environmental Science & Technology, 2017, 51(3): 1441-1449. [140] GARCíA-LóPEZ M, RODRíGUEZ I, CELA R. Evaluation of liquid–liquid microextraction using polypropylene microporous membranes for the determination of organophosphorus flame retardants and plasticizers in water samples[J]. Analytica Chimica Acta, 2008, 625(2): 145-153. [141] 何丽雄, 曹曙霞, 曾祥英, 等. 固相萃取/气相色谱-质谱联用技术快速测定水中有机磷酸酯阻燃剂与增塑剂 [J]. 分析测试学报, 2013, 32(4): 437-441. doi: 10.3969/j.issn.1004-4957.2013.04.008 HE L X, CAO S X, ZENG X Y, et al. Determination of organophosphate flame retardants and plasticizers in water using solid phase extraction coupled with GC-MS [J]. Journal of Instrumental Analysis, 2013, 32(4): 437-441(in Chinese). doi: 10.3969/j.issn.1004-4957.2013.04.008
[142] 秦宏兵, 范苓, 顾海东. 固相萃取-气相色谱/质谱法测定水中6种有机磷酸酯类阻燃剂和增塑剂 [J]. 分析科学学报, 2014, 30(2): 259-262. QIN H B, FAN L, GU H D. Determination of organophosphorus flame retardants and plasticizers in environmental water by solid phase extraction coupled with gas chromatography/mass spectrometry [J]. Journal of Analytical Science, 2014, 30(2): 259-262(in Chinese).
[143] MARKLUND A, ANDERSSON B, HAGLUND P. Organophosphorus flame retardants and plasticizers in Swedish sewage treatment plants [J]. Environmental Science & Technology, 2005, 39(19): 7423. [144] BRANDSMA S H, DE BOER J, LEONARDS P E G, et al. Organophosphorus flame-retardant and plasticizer analysis, including recommendations from the first worldwide interlaboratory study [J]. Trends in Analytical Chemistry, 2013, 43: 217-228. doi: 10.1016/j.trac.2012.12.004 [145] STUBBINGS W A, RIDDELL N, CHITTIM B, et al. Challenges in the analyses of organophosphate esters [J]. Environmental Science & Technology Letters, 2017, 4(7): 292-297. -



 下载:
下载:

