-
氯酚类化合物是分子结构中含有一个或多个氯原子取代基的酚类化合物,其作为杀虫剂、防腐剂和除草剂已经使用数10年[1]. 有研究发现,氯酚类化合物及其钠盐具有较强的生物蓄积毒性和“三致”效应[2],其中五氯酚被国际癌症研究机构列为2B类致癌物[3]. 美国环境保护署(ΜSEPA)早在20世纪70年代就已将包括2-氯酚、2,4-二氯酚、2,4,6-三氯酚和五氯酚在内的11种苯酚类化合物列为优先控制污染物,我国也于20世纪90年代将五氯酚、2,4,6-三氯酚和2,4-二氯酚定为水中优先控制污染物. 在生态环境部公布的重点管控新污染物清单(2023年版)中,五氯苯酚及其盐类和酯类被列为重点管控新污染物[4]. 由于该类物质难降解、脂溶性强且具有高生物富集性[5],可长期存在于自然环境中,导致持久性有机物污染. 长期饮用含氯酚的生活饮用水会出现头昏、贫血、皮疹和多种神经系统疾病,甚至导致中毒,严重危害生物体健康[6]. 我国《生活饮用水卫生标准》(GB5749—2022)已将五氯酚和2,4,6-三氯酚列为水质扩展指标,规定其在生活饮用水中的限值分别为0.009 mg·L−1和0.2 mg·L−1 [7].
在国家标准《生活饮用水标准检验方法》(GB/T
5750 —2023)中,仅有五氯酚和2,4,6-三氯酚的检测方法,包括衍生化气相色谱法、顶空固相微萃取-气相色谱法、固相萃取-气相色谱-质谱法和液相色谱-串联质谱法[8]. 在已有文献报道中,氯酚类化合物的测定方法主要包括气相色谱法[9 − 14]、液相色谱法[15 − 16]、气相色谱-质谱法[17 − 21]和液相色谱-串联质谱法[22]等. 在各类方法中,对于水样的前处理,衍生化处理操作较为繁琐[9 − 10];液液萃取法需消耗较多有机溶剂[15 − 16];固相萃取则耗时长[11,17 − 20]. 顶空固相微萃取[12 − 14,21,23 − 24]作为一种新型高效的样品前处理技术,集萃取、富集、解吸、进样于一体,在萃取过程中不需要与样品直接接触,有利于萃取头的多次使用,同时可减少非特异性吸附引起的基体干扰,且不需要消耗有机溶剂,对实验人员和环境均比较友好,特别适合水中半挥发性及挥发性污染物的分析. 目前,在水中氯酚的检测中,多采用顶空固相微萃取与气相色谱联用的方法,但是相比质谱检测器其定性能力不强,从而会影响结果的准确性.因此,本研究将全自动顶空固相微萃取和气相色谱-质谱法联用,在线化实现生活饮用水中2-氯酚、2,4-二氯酚、2,4,6-三氯酚和五氯酚的同时测定. 该法简便、快速、灵敏,减少了环境污染,能够满足现行国家卫生标准(GB
5749 —2022)的卫生限值要求,适合于生活饮用水中多种氯酚的测定,同时也可为我国生活饮用水标准检验方法的修订提供一定的基础数据支持. -
2-氯酚标准品,100 mg,纯度99.8%,坛墨质检;2,4-二氯酚标准品,100 mg,纯度99.9%,坛墨质检;2,4,6-三氯酚标准品,10 mg,纯度99.6%,坛墨质检;五氯酚标准溶液,浓度为100 μg·mL−1,坛墨质检;甲醇:质谱纯,美国Thermo Fisher公司;硫代硫酸钠:基准试剂,天津市科密欧化学试剂有限公司;抗坏血酸:优级纯,成都市科隆化学品有限公司;氯化钠:优级纯,天津市光复精细化工研究所;盐酸,优级纯,上海振兴化工一厂;实验用水:超纯水,自制.
-
7890A型气相色谱-5975C型质谱联用仪,美国Agilent公司;全自动多功能自动进样系统:PAL RTC型(带HS-SPME模块),广州智达实验室科技有限公司;BS224S型电子天平:德国Sartorius 公司;色谱柱:DB-5MS(30 m × 0.32 mm,0.25 μm),美国Agilent公司;Mili-Q超纯水系统,美国Millipore 公司.
-
标准储备液的配制:将2-氯酚(100 mg)、2,4-二氯酚(100 mg)与2,4,6-三氯酚的标准品(10 mg)用甲醇完全溶解,转移至10 mL容量瓶中,定容至刻度,分别配制成浓度为10.0 mg·mL−1、10.0 mg·mL−1与1.00 mg·mL−1的标准储备液;将五氯酚标准溶液(100 μg·mL−1)用甲醇稀释成10.0 mg·L−1的标准储备液,置于−20 ℃冰箱保存.
混合标准应用液的配制:分别准确吸取一定量各单组分标准储备液于装有适量甲醇的10 mL容量瓶中,定容至刻度,配制成浓度为
1000 μg·L−1的混合标准应用液. -
于 20 mL顶空瓶中,准确加入10 mL水样,而后加入3.6 g氯化钠和0.1 mL 1 mol·L−1的盐酸溶液,加盖密封,置于自动进样器样品架待测.
-
进样口温度:280 ℃;载气:氦气(99.999%);流速:1.2 mL·min−1;色谱柱:Agilent DB-5MS(30 m×0.32 mm,0.25 μm);柱温采用程序升温:初始温度设置为40 ℃,保持3 min;之后以10 ℃·min−1速率升到120 ℃,继续以15 ℃·min−1速率升至240 ℃,保持10 min;进样体积: 1 μL,不分流进样.
-
电子轰击电离源(EI),电子能量70 eV,四极杆温度150 ℃,离子源温度230 ℃,传输线温度230 ℃. 采用选择离子监测(SIM)模式进行检测,4种氯酚的保留时间、定性离子、定量离子等参数见表1.
-
采用DVB/PDMS萃取头,萃取时间60 min,萃取温度60 ℃,振摇速率450 r·min−1,进样深度50 mm,脱附时间300 s,老化温度280 ℃. 每次萃取样品前,萃取头均需先老化5 min.
-
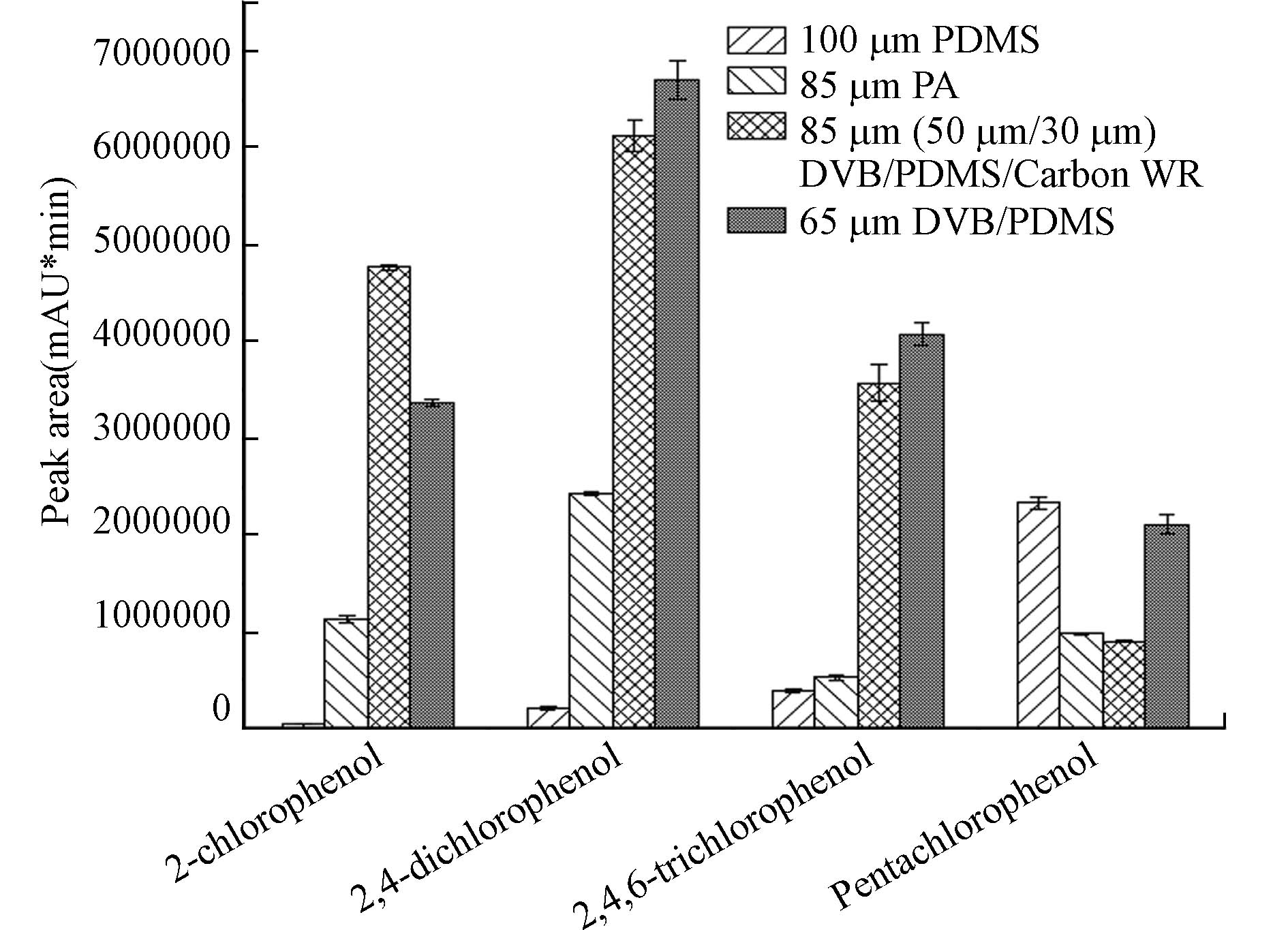
萃取头的类型对萃取效果的影响较大,目标化合物在萃取头的涂层材料和样品之间的分配系数影响萃取效果. 在现有文献报道中,聚丙烯酸酯(PA)使用较多[12 − 14,21],考虑到4种氯酚分子量和极性的差异,本研究除了选择单一涂层的85 μm聚丙烯酸酯(PA)和100 μm聚二甲基硅氧烷(PDMS)外,还选取了复合涂层的65 μm二乙烯基苯/聚二甲基硅氧烷(DVB/PDMS)以及85 μm(50 μm/30 μm)DVB/PDMS/Carbon WR共4种萃取头进行萃取效果比较实验. 分别配制10.0 μg·L−1的氯酚混合标准溶液,在其余分析条件相同的情况下采用上述4种萃取头进行实验,通过比较各目标物定量离子峰面积的大小,确定最佳萃取纤维的类型. 从图1可以看出,PDMS萃取头仅对五氯酚萃取效果较好;PA萃取头更适用于酚类等极性半挥发性化合物的分析,故2-氯酚和2,4-二氯酚的响应明显增加;采用DVB/PDMS/Carbon WR萃取头时,2-氯酚、2,4-二氯酚与2,4,6-三氯酚的响应均有明显提高,相较于PDMS,五氯酚响应则下降;而使用DVB/PDMS萃取头后,4种氯酚均获得较好的萃取效果,故综合考虑选择65 μm DVB/PDMS.
-
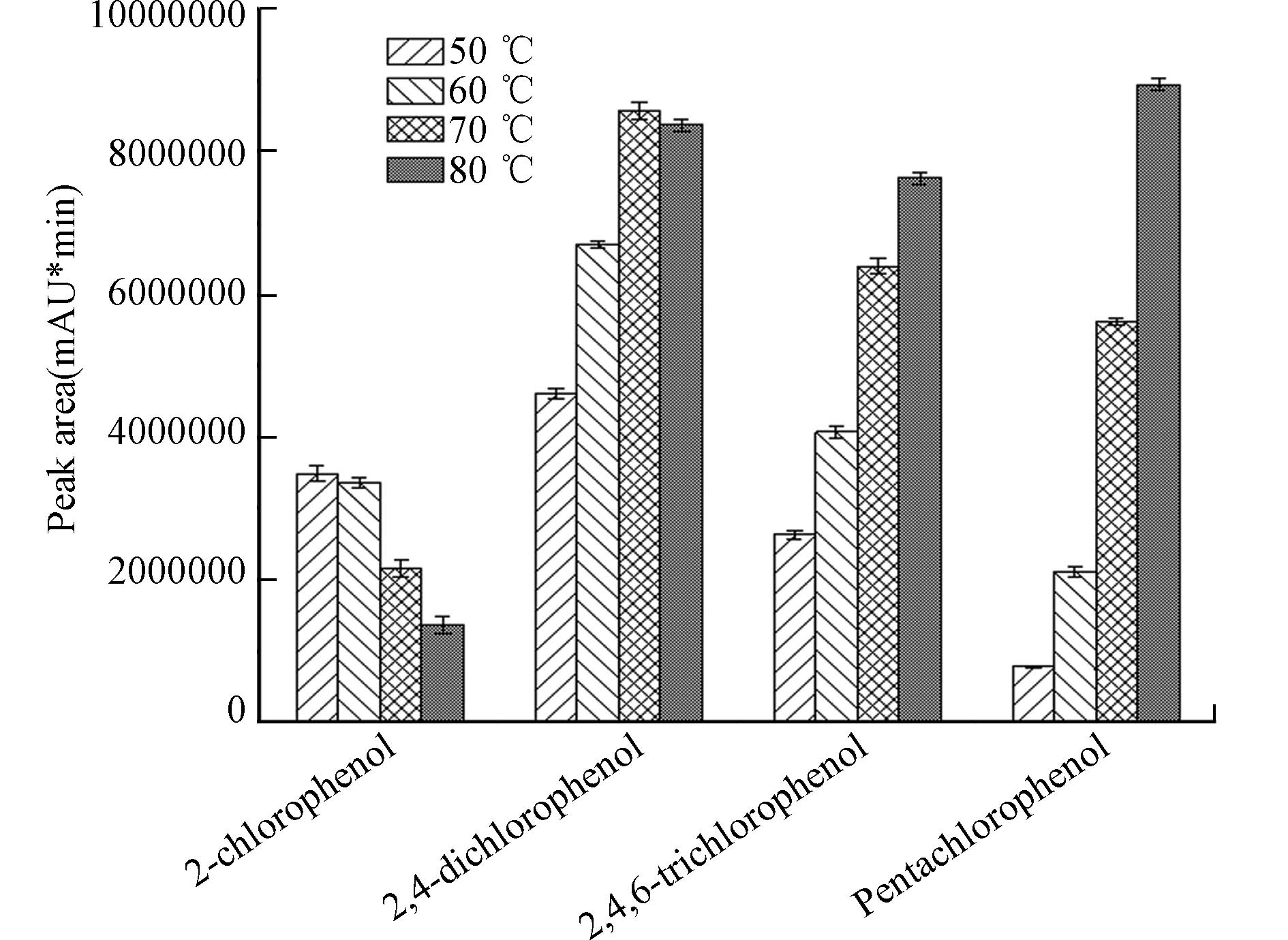
萃取温度也是影响萃取效果的一个重要因素,参考相关文献[25],本研究分别配制10 μg·L−1的氯酚混合标准溶液,在其余分析条件相同的情况下考察了萃取温度为50、60、70、80 ℃时各氯酚的萃取效果. 如图2所示,在50—80 ℃范围内,2,4,6-三氯酚和五氯酚的响应随着萃取温度升高而不断增加,而2,4-二氯酚的响应在80 ℃略有下降,2-氯酚的响应则在70 ℃出现明显下降. 出现这种现象的原因可能在于2-氯酚分子量和沸点均较低,有研究表明[24],纤维涂层对分析物的吸附是一个放热过程,对于某些挥发性较高的低分子量有机物,温度过高会导致萃取纤维的萃取效率降低,因此需要选择合适的萃取温度. 综合考虑,选择萃取温度为60 ℃.
-
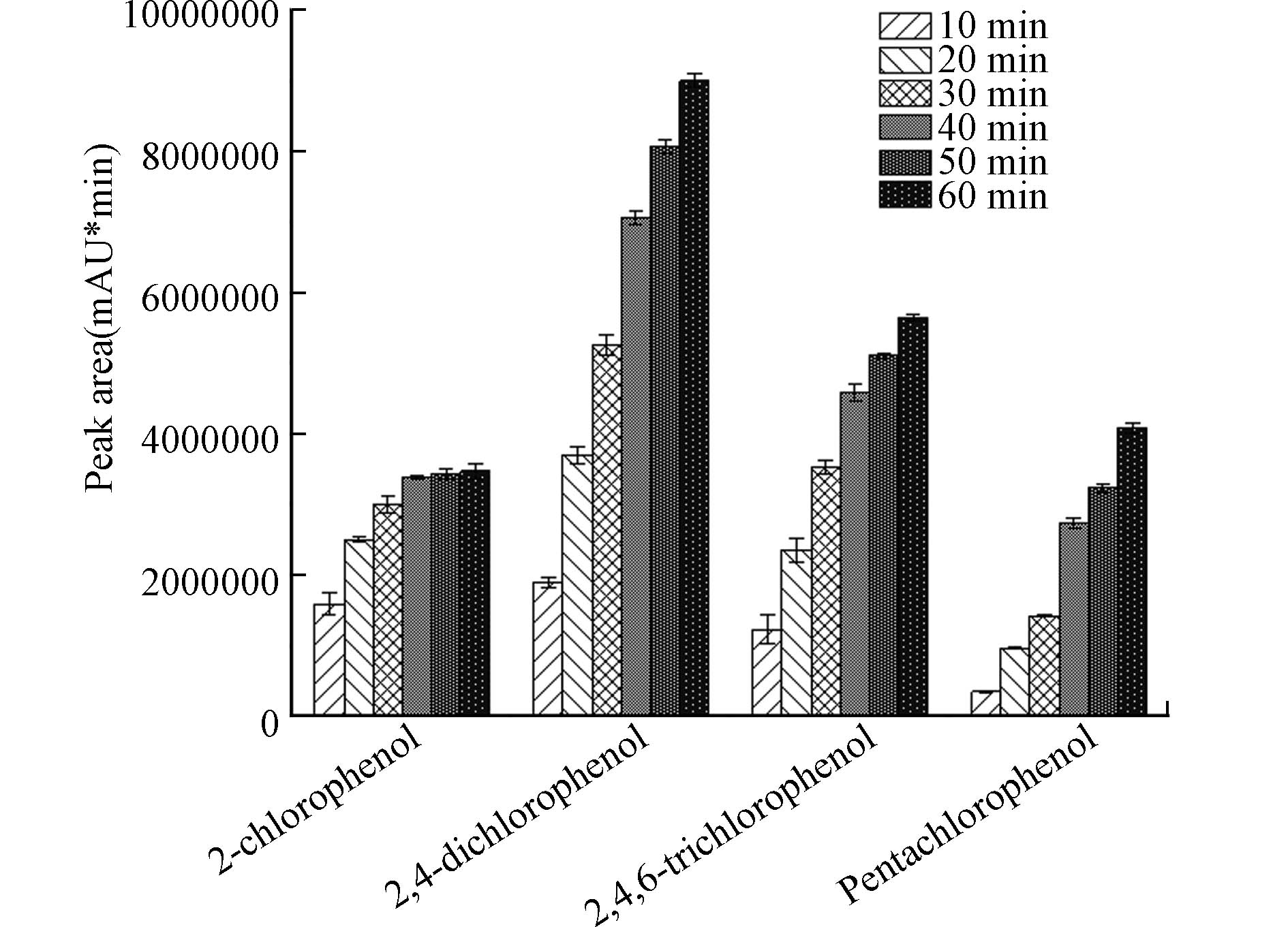
萃取时间对萃取效果也有着较大影响,本研究分别配制10 μg·L−1的氯酚混合标准溶液,在其余分析条件相同的情况下考察了萃取时间分别为10、20、30、40、50、60 min时4种氯酚的萃取效果. 如图3所示,2-氯酚在萃取40 min后响应不再显著增加,在40 min时基本达到平衡;而2,4-二氯酚、2,4,6-三氯酚以及五氯酚的响应在萃取时间10—40 min的范围内有明显增加,40 min以后增加趋势变缓. 综合考虑实验效率及长时间萃取造成的萃取纤维中水分增多的影响[26],本实验选择的萃取时间为60 min.
-
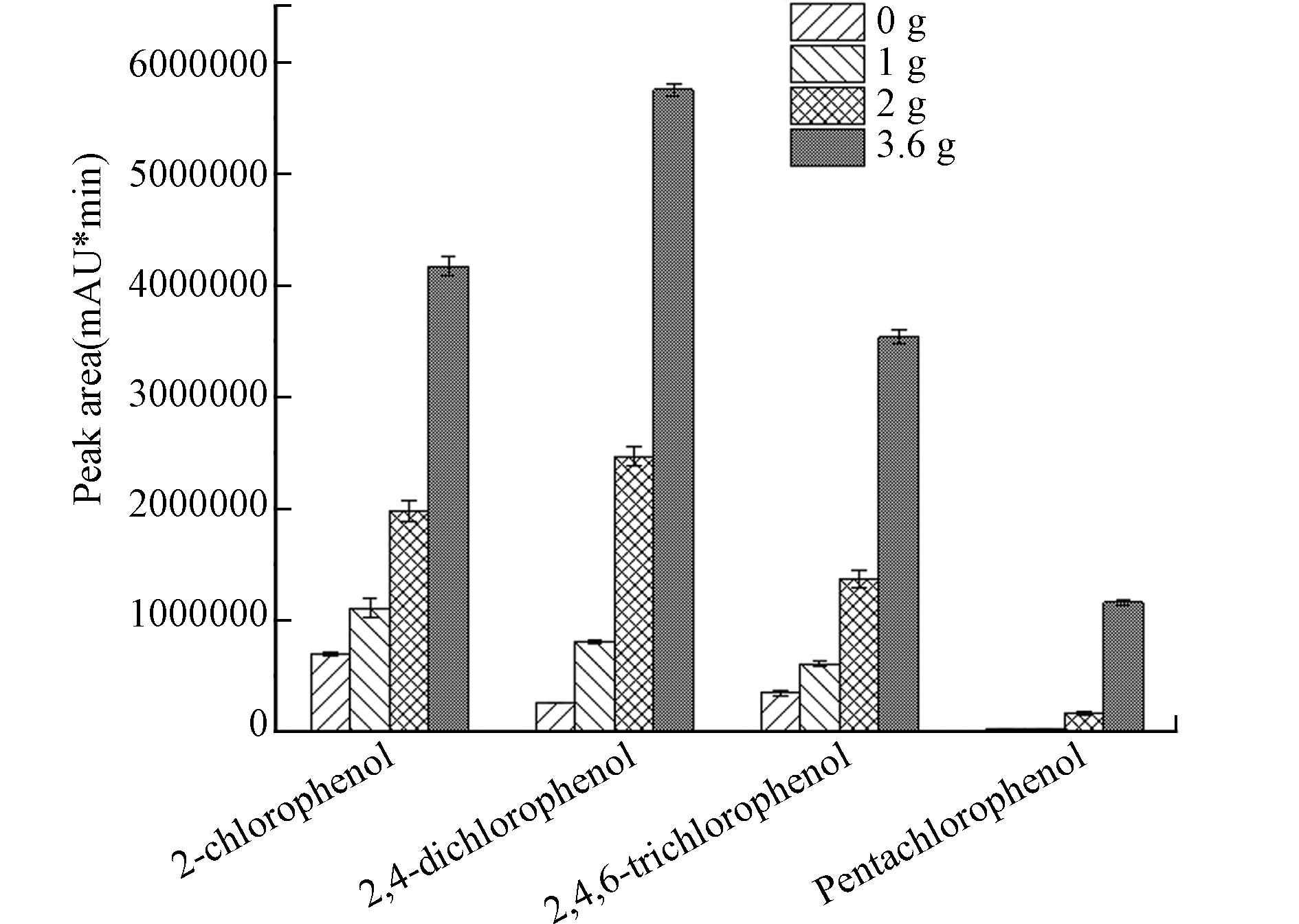
本研究分别配制10 μg·L−1的氯酚混合标准溶液,在其余分析条件相同的情况下,通过加入不同量的氯化钠(0、1、2、3.6 g)改变溶液的离子强度,探究离子强度对萃取效果的影响. 如图4所示,随着氯化钠加入量的增加,4种氯酚的响应均明显提高,因此选择向10 mL水样中添加3.6 g氯化钠至饱和状态.
-
本研究分别配制10 μg·L−1的氯酚混合标准溶液,在其余分析条件相同的情况下,加入不同体积(0、0.10、0.20、0.50 mL)1.0 mol·L−1盐酸溶液改变溶液的酸度,考察pH对萃取效果的影响. 如图5所示,加酸之后, 2,4,6-三氯酚和五氯酚的响应明显提高,当盐酸溶液体积超过0.10 mL之后,2-氯酚、2,4-二氯酚、2,4,6-三氯酚的响应均出现下降趋势. 由于酸性过强会损坏萃取纤维的固定相影响萃取效率,故选择在10 mL水样中加入0.10 mL 1.0 mol·L−1盐酸溶液.
-
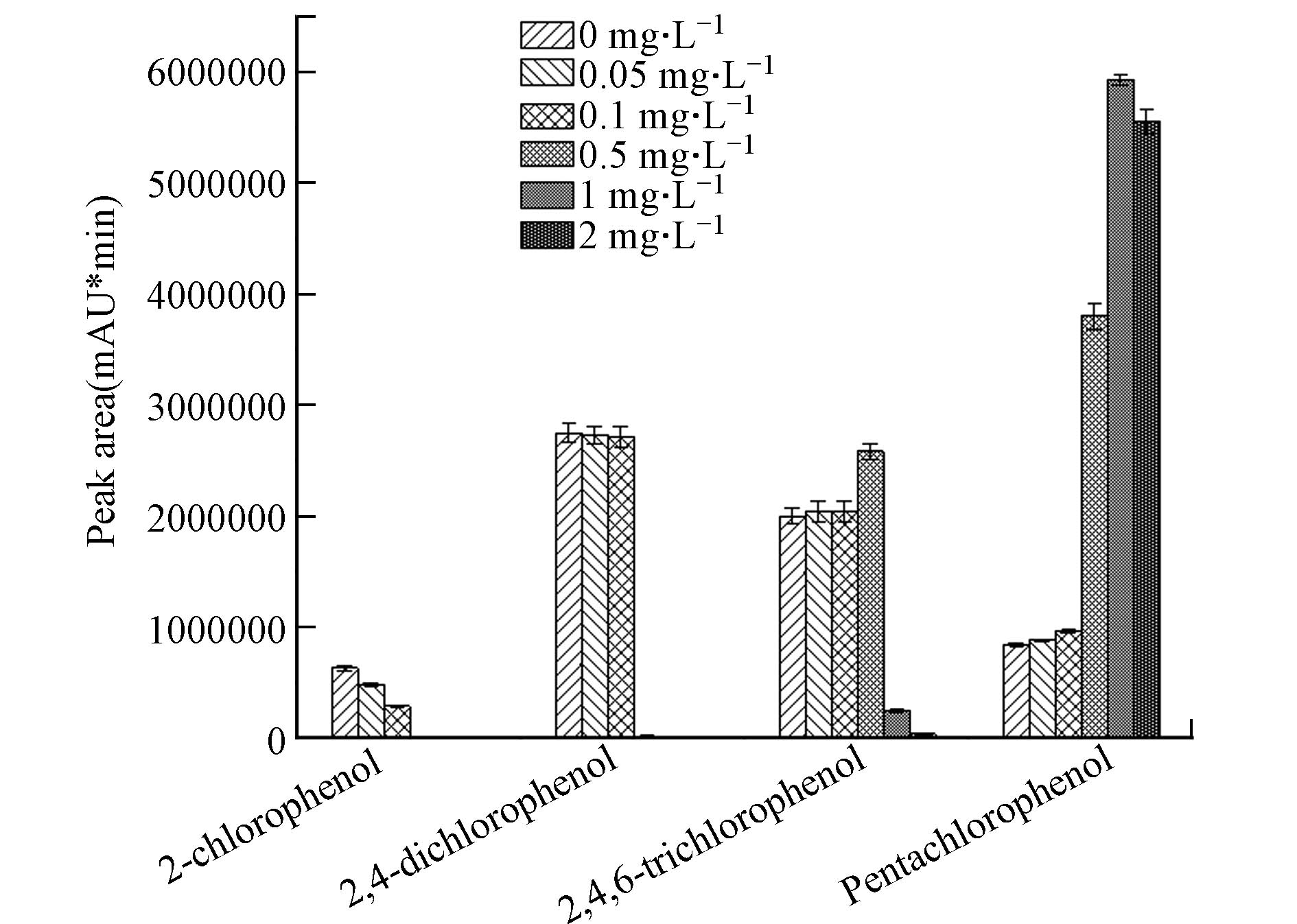
目前,生活饮用水大多使用氯化消毒,而水中酚类在氯化消毒过程中会和消毒剂反应生成氯代酚[27],五氯酚和2,4,6-三氯苯酚由于其毒性和致癌性而成为最常研究的氯酚[28],但是国内外研究并未深入探讨消毒后游离氯对氯酚检测结果的影响,本实验详细考察了其影响. 在游离氯浓度分别为0、0.05 mg·L−1、0.10 mg·L−1、0.50 mg·L−1、1.0 mg·L−1、2.0 mg·L−1的超纯水中,加入混合标准氯酚溶液并使其终浓度为10 μg·L−1,在其余分析条件相同的情况下考察不同游离氯浓度对萃取效果的影响. 结果如图6所示,游离氯浓度超过0.10 mg·L−1之后,2-氯酚和2,4-二氯酚的响应明显下降,2,4,6-三氯酚和五氯酚的响应有所增加;游离氯浓度超过0.50 mg·L−1之后,2,4,6-三氯酚的响应也明显下降,出现这种现象的原因可能在于游离氯与2-氯酚、2,4-二氯酚、2,4,6-三氯酚发生了氯代反应生成了五氯酚. 有研究也表明[29 − 30],在预氯化或氯消毒过程中,氯与苯酚的反应是一个连续的过程,首先是氯取代苯环上的氢原子依次生成2-氯酚、二氯酚和三氯酚,接着发生烯醇化、水解和脱碳反应,最终生成三卤甲烷(THMs)和卤乙酸(HAAs). 在我国《生活饮用水卫生标准》(GB5749—2022)中,规定管网末梢水中游离氯的含量在0.05—2 mg·L−1的范围. 因此,在采集水样时,有必要加入适量还原剂消除游离氯,从而获得准确的检测结果.
-
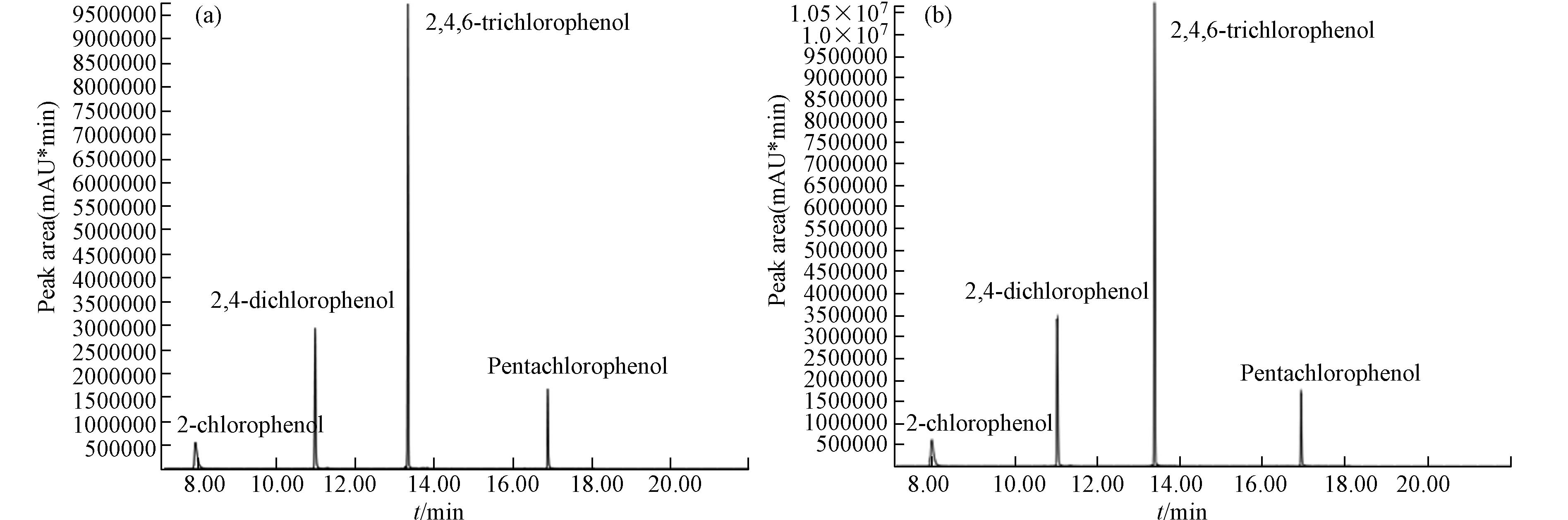
配制浓度分别为0.05、0.20、0.50、1.0、2.0、5.0、10、20 μg·L−1的混合标准系列溶液,按照1.3.2节同水样进行相同前处理后,再按照1.3.3节与1.3.4节的仪器条件进行分析,绘制标准曲线,求得回归方程和相关系数,并以3倍基线噪声和10倍基线噪声所对应的待测组分含量计算4种氯酚的方法检出限和定量限,结果见表2. 由表2可知,该方法检出限为0.015—0.060 μg·L−1,方法定量限为0.050—0.20 μg·L−1,标准色谱图见图7.
-
在标准曲线范围内,在生活饮用水中分别加入1.0、5.0、10 μg·L−1 的3个浓度氯酚混合标准溶液,每个添加水平平行测定6 次,进行方法准确度和精密度实验. 结果如表3所示,方法的平均回收率为90.4%—115%,相对标准偏差RSD为0.47%—6.91%. 加标样品色谱图见图7.
-
采用本方法检测成都市某辖区内4份生活饮用水,4种氯酚含量均低于方法定量限(0.05—0.20 μg·L−1). 在已有文献报道[10,13,31]中,氯酚检出率和检出浓度都不高,如张权等[13]采用顶空固相微萃取—气相色谱法对50份生活饮用水中的4种氯酚进行了检测,除1份水样有检出且未超出国家限值,其余样品均未检出.
-
本实验建立了全自动在线顶空固相微萃取-气相色谱-质谱法同时测定生活饮用水中4种氯酚,相比液液萃取、固相萃取、衍生化等操作,该方法样品前处理简便、自动化程度高,避免了有机溶
剂的使用. 同固相微萃取-气相色谱法相比,固相微萃取与气相色谱-质谱联用,在获得高灵敏度与精密度的同时,特异性更强,定性定量结果更加准确可靠. 4种氯酚浓度-响应线性关系良好,相关系数r均大于
0.9994 ,方法检出限为0.015—0.060 μg·L−1,方法定量限为0.050—0.20 μg·L−1,方法平均回收率为90.4%—115%,相对标准偏差为0.47%—6.91%. 此外,本研究对顶空固相微萃取条件进行了系统优化,除了萃取头类型、萃取时间、萃取温度、pH、离子强度等传统条件的选择,特别是对生活饮用水中消毒剂游离氯对检测结果的影响进行了详细讨论,水样消毒后游离氯的存在会不同程度的影响4种氯酚的浓度,所以在采集水样时,有必要加入适量还原剂消除游离氯,从而获得准确的检测结果.
基于全自动在线顶空固相微萃取-气相色谱-质谱联用技术测定生活饮用水中4种氯酚
Determination of four chlorophenols in drinking water based on automatic online headspace solid-phase microextraction coupled with gas chromatography-mass spectrometry
-
摘要: 建立了全自动在线顶空固相微萃取-气相色谱-质谱联用(HS-SPME-GC-MS)分析法同时测定生活饮用水中2-氯酚、2,4-二氯酚、2,4,6-三氯酚和五氯酚. 通过单因素实验设计考察了萃取纤维、萃取温度、萃取时间、加盐量、加酸量、消毒剂余量等对萃取效果的影响. 优化后的顶空固相微萃取条件为:取10 mL水样于20 mL顶空瓶中,加入3.6 g NaCl、0.1 mL 1 mol·L−1盐酸溶液,使用65 μm DVB/PDMS纤维头,萃取温度 60 ℃,萃取时间60 min,振摇速率450 r·min−1,解吸时间5 min,解吸温度 280 ℃. 4种氯酚浓度-响应线性关系良好,相关系数r均大于
0.9994 ,方法检出限为0.015—0.060 μg·L−1,方法定量限为0.050—0.20 μg·L−1,平均回收率为90.4%—115%,相对标准偏差为0.47%—6.91%. 该方法具有准确、便捷、灵敏度高等优点,适用于生活饮用水中多种氯酚的同时测定.Abstract: An automatic online headspace solid-phase microextraction (HS-SPME)-gas chromatography-mass spectrometry (GC-MS) method has been developed for simultaneous determination of 2-chlorophenol, 2,4-dichlorophenol, 2,4,6-trichlorophenol, and pentachlorophenol in drinking water. The effects of extraction fiber type, extraction temperature, extraction time, salt concentration, acid concentration and residual chlorine on the extraction efficiencies were investigated by one-way experimental design. The optimized HS-SPME parameters were as follows: A 10 mL water sample was taken in a 20-mL headspace bottle with addition of 3.6 g NaCl and 0.1 mL 1 mol·L−1 hydrochloric acid solution. The target chlorophenols were extracted for 60 min with a 65 μm DVB/PDMS fiber coating under an extraction temperature of 60 ℃ and with a shaking rate of 450 r·min−1, desorbed for 5 min under desorption temperature of 280 ℃. Good concentration-response linear relationship was obtained for four target chlorophenols with the correlation coefficients (r) greater than 0.9994. The limits of detection (LODs) were from 0.015 μg·L−1 to 0.060 μg·L−1, and the limits of quantification (LOQs) were from 0.050 μg·L−1 to 0.20 μg·L−1. The average recoveries of the four chlorophenols ranged from 90.4% to 115%, and the relative standard deviations were 0.47% to 6.91%. The established method has the advantages of accuracy, rapidity and high sensitivity, and is suitable for simultaneous determination of multiple chlorophenols in drinking water. -

-
表 1 4种氯酚的质谱参数
Table 1. MS parameters for the 4chlorophenols
化合物
Compound保留时间/min
Retention time定性离子m/z
Qualitative ion定量离子m/z
Qualitative ion2-氯酚 7.9 64,92 128 2,4-二氯酚 11.0 63,126 162 2,4,6-三氯酚 13.4 97,132 196 五氯酚 16.9 130,165 266 表 2 4种氯酚的线性范围、回归方程、相关系数、检出限和定量限
Table 2. Linear range, linear equation, correlation coefficient(r), LOD and LOQ of the 4 chlorophenols
化合物
Compound线性范围/(μg·L−1)
Linear range线性回归方程
Linear equation相关系数
r检出限/(μg·L−1)
LODs定量限/(μg·L−1)
LOQs2-氯酚 0.20—20 y= 358778 x−26857 0.9994 0.060 0.20 2,4-二氯酚 0.050—20 y= 1000000 x+10445 0.9999 0.015 0.050 2,4,6-三氯酚 0.050—20 y= 650278 x+3070.2 0.9998 0.015 0.050 五氯酚 0.20—20 y= 462060 x−28366 0.9998 0.060 0.20 表 3 方法的准确度和精密度(n=6)
Table 3. Method precision and accuracy test(n=6)
化合物
Compound本底值/(μg·L−1)
Background加标浓度/(μg·L−1)
Spiked加标后平均测定值/(μg·L−1)
Detected平均回收率/%
Mean recoveries相对标准偏差/%
RSD2-氯酚 ND 1.0 0.955 95.5 6.91 5.0 5.36 107 1.42 10 9.48 94.8 0.47 2,4-二氯酚 ND 1.0 0.968 96.8 5.64 5.0 4.88 97.6 1.86 10 9.14 91.4 1.44 2,4,6-三氯酚 ND 1.0 0.992 99.2 6.47 5.0 4.82 96.4 2.27 10 9.04 90.4 2.21 五氯酚 ND 1 1.15 115 5.02 5 5.28 106 3.40 10 10.2 102 3.25 注:ND为未检出. ND means not detected. -
[1] CAGNETTA G, ROBERTSON J, HUANG J, et al. Mechanochemical destruction of halogenated organic pollutants: A critical review[J]. Journal of Hazardous Materials, 2016, 313: 85-102. doi: 10.1016/j.jhazmat.2016.03.076 [2] GUO J Q, WU C H, LV S L, et al. Associations of prenatal exposure to five chlorophenols with adverse birth outcomes[J]. Environmental Pollution, 2016, 214: 478-484. doi: 10.1016/j.envpol.2016.04.074 [3] World Health Organization & International Programme on Chemical Safety: health and safety guide No. 19, pentachlorophenol[EB/OL]. [2024-08-21]. [4] 中华人民共和国生态环境部. 《重点管控新污染物清单(2023年版)》[EB/OL]. [2024-08-21]. [5] 甄一尘. 新型管式磁膜光催化反应体系对氯酚废水的降解效果与机制研究[D]. 保定: 河北大学, 2020. ZHEN Y C. A study of the degradation effect and mechanism for chlorophenol wastewater by a novel tubular magnetic film photocatalysis system[D]. Baoding: Hebei University, 2020 (in Chinese).
[6] YADAV S, KUMAR S, HARITASH A K. A comprehensive review of chlorophenols: Fate, toxicology and its treatment[J]. Journal of Environmental Management, 2023, 342: 118254. doi: 10.1016/j.jenvman.2023.118254 [7] 国家市场监督管理总局, 国家标准化管理委员会. 生活饮用水卫生标准: GB 5749—2022[S]. 北京: 中国标准出版社, 2022. State Administration for Market Regulation, Standardization Administration of the People’s Republic of China. Standards for drinking water quality: GB 5749—2022[S]. Beijing: Standards Press of China, 2022 (in Chinese).
[8] 国家市场监督管理总局, 国家标准化管理委员会. 生活饮用水标准检验方法: GB/T 5750—2023[S]. 北京: 中国标准出版社, 2023. State Administration for Market Regulation, Standardization Administration of the People’s Republic of China. Standard examination methods for drinking water quality: GB/T 5750—2023[S]. Beijing: Standards Press of China, 2023(in Chinese)
[9] 崔君, 顾华, 张强. 改进的五氟苄基溴衍生化反应测定水中酚类化合物[J]. 分析试验室, 2021, 40(1): 54-58. CUI J, GU H, ZHANG Q. Improved pentafluorobenzyl bromide derivatization reaction for determination of phenolic compounds in water[J]. Chinese Journal of Analysis Laboratory, 2021, 40(1): 54-58 (in Chinese).
[10] 张权, 李磊, 林野, 等. 正交实验优化BSTFA衍生-气相色谱法快速测定水中4种氯酚化合物[J]. 环境与职业医学, 2017, 34(9): 831-835. ZHANG Q, LI L, LIN Y, et al. Rapid determination of four chlorophenols in water by orthogonal experiment optimization-BSTFA derivatization-gas chromatography[J]. Journal of Environmental & Occupational Medicine, 2017, 34(9): 831-835 (in Chinese).
[11] 彭礼枚, 谭丽君, 蒋建军, 等. 固相萃取–气相色谱法测定水中20种酚类化合物[J]. 化学分析计量, 2022, 31(6): 6-9. PENG L M, TAN L J, JIANG J J, et al. Determination of 20 phenolic compounds in water by gas chromatography with solid phase extraction[J]. Chemical Analysis and Meterage, 2022, 31(6): 6-9 (in Chinese).
[12] 姚远, 宋维涛, 张洋, 等. 顶空固相微萃取-气相色谱法测定水中氯酚类化合物[J]. 环境监控与预警, 2015, 7(6): 22-25. doi: 10.3969/j.issn.1674-6732.2015.06.006 YAO Y, SONG W T, ZHANG Y, et al. Determination of chlorophenols in water samples using headspace solid-phase microextraction coupled with gas chromatography[J]. Environmental Monitoring and Forewarning, 2015, 7(6): 22-25 (in Chinese). doi: 10.3969/j.issn.1674-6732.2015.06.006
[13] 张权, 殷忠. 顶空固相微萃取—气相色谱法测定生活饮用水中的氯酚化合物[J]. 微量元素与健康研究, 2020, 37(2): 64-66. ZHANG Q, YIN Z. Determination 0f chlorophenols in drinking water by headspace solid phase microextraction and gas chromatography[J]. Studies of Trace Elements and Health, 2020, 37(2): 64-66 (in Chinese).
[14] 奚晔, 詹铭. 顶空固相微萃取-气相色谱法测定饮用水中5种氯酚[J]. 理化检验(化学分册), 2014, 50(6): 775-777. XI Y, ZHAN M. Determination of five chlorophenols in drinking water by headspace solid phase microextraction and gas chromatography[J]. PTCA (PART B: CHME. ANAL. ), 2014, 50(6): 775-777 (in Chinese).
[15] 魏冬梅, 李会兰, 李玉勇, 等. 高效液相色谱法测定水样中3种氯酚类化合物[J]. 云南化工, 2023, 50(8): 79-82. WEI D M, LI H L, LI Y Y, et al. Determination of three chlorophenolic compounds in water by high performance liquid chromatography[J]. Yunnan Chemical Technology, 2023, 50(8): 79-82 (in Chinese).
[16] 郑晓峰, 李鹏鹏, 张晓霞, 等. 液液萃取-液相色谱法测定饮用水中的2, 4, 6-三氯酚和五氯酚[J]. 城镇供水, 2019(2): 27-29, 69. doi: 10.3969/j.issn.1002-8420.2019.02.008 ZHENG X F, LI P P, ZHANG X X, et al. Determination of 2, 4, 6-trichlorophenol and pentachlorophenol in drinking water by liquid-liquid extraction and high performance liquid chromatography[J]. City and Town Water Supply, 2019(2): 27-29, 69 (in Chinese). doi: 10.3969/j.issn.1002-8420.2019.02.008
[17] POKRYSHKIN S A, KOSYAKOV D S, KOZHEVNIKOV A Y, et al. Highly sensitive determination of chlorophenols in sea water by gas Chromatography−Tandem mass spectrometry[J]. Journal of Analytical Chemistry, 2018, 73(10): 991-998. doi: 10.1134/S1061934818100088 [18] 周继恩, 杨振清, 赵永信, 等. 气相色谱质谱联用法同时测定水中2,4, 6-三氯酚、五氯酚、2,4-二氯苯氧乙酸和灭草松[J]. 预防医学, 2021, 33(12): 1282-1285. ZHOU J E, YANG Z Q, ZHAO Y X, et al. Simultaneous determination of 2,4,6-trichlorophenol, pentachlorophenol, 2,4-dichlorophenoxyacetic acid and bentazone in drinking water by gas chromatography-mass spectrometry[J]. Preventive Medicine, 2021, 33(12): 1282-1285 (in Chinese).
[19] 张艳萍. 饮用水中多种氯酚化合物的气相色谱-质谱测定法[J]. 职业与健康, 2013, 29(15): 1900-1902. ZHANG Y P. Determination of multi-chlorophenols in drinking water by gas chromatography[J]. Occupation and Health, 2013, 29(15): 1900-1902 (in Chinese).
[20] 王冰霜. 池州市贵池区水源水氯酚的风险评价和社区居民氯酚内暴露水平研究[D]. 合肥: 安徽医科大学, 2016. WANG B S. ecological risk assessment of chlorophenols from source water and internal dose of chlorophenols in the residents from Guichi District, Chizhou[D]. Hefei: Anhui Medical University, 2016 (in Chinese).
[21] 刘斌, 孙红梅, 陈山, 等. 顶空固相微萃取-气相色谱-串联质谱法测定水中2, 4, 6-三氯酚[J]. 环境监控与预警, 2019, 11(3): 36-39. LIU B, SUN H M, CHEN S, et al. Determination of 2, 4, 6-trichlorophenol in water by HS-SPME-GC-MS-MS[J]. Environmental Monitoring and Forewarning, 2019, 11(3): 36-39 (in Chinese).
[22] 付正伟, 朱峰, 张昊, 等. 高效液相色谱-串联质谱法测定水体中三氯酚的6种同分异构体[J]. 分析科学学报, 2022, 38(3): 389-392. FU Z W, ZHU F, ZHANG H, et al. Determination of six isomers of trichlorophenol in water by high performance liquid chromatography-tandem mass spectrometry[J]. Journal of Analytical Science, 2022, 38(3): 389-392 (in Chinese).
[23] 俞嘉斌, 邹波, 魏春明, 等. 全自动在线顶空固相微萃取-气相色谱-质谱联用检测水样中24种常见农药[J]. 农药学学报, 2022, 24(6): 1526-1534. YU J B, ZOU B, WEI C M, et al. Determination of 24 common pesticides in water samples by automatic online HS-SPME-GC/MS[J]. Chinese Journal of Pesticide Science, 2022, 24(6): 1526-1534 (in Chinese).
[24] 夏雪, 陈倩茹, 王川, 等. 顶空固相微萃取-气相色谱-质谱联用测定黑臭水体中的4种主要异味物质[J]. 环境化学, 2019, 38(12): 2789-2796. doi: 10.7524/j.issn.0254-6108.2019011601 XIA X, CHEN Q R, WANG C, et al. Determination of four major odor compounds in black and odorous water by headspace solid phase microextraction combined with gas chromatography-mass spectrometry[J]. Environmental Chemistry, 2019, 38(12): 2789-2796 (in Chinese). doi: 10.7524/j.issn.0254-6108.2019011601
[25] 杨杨, 张成敏, 刘娜, 等. 固相微萃取-气相色谱质谱法测定纺织品中五氯苯酚含量[J]. 中国纤检, 2016(2): 78-80. doi: 10.3969/j.issn.1671-4466.2016.02.024 YANG Y, ZHANG C M, LIU N, et al. Determination of PCP content for textiles using solid-phase microextraction with gas chromatography mass spectrometry[J]. China Fiber Inspection, 2016(2): 78-80 (in Chinese). doi: 10.3969/j.issn.1671-4466.2016.02.024
[26] 狄欣宜. 顶空固相微萃取-气质联用法测定水中4种痕量环状缩醛类异嗅物质[J]. 净水技术, 2024, 43(3): 194-203. DI X Y. Trace level quantification of four cyclic acetals odorous compounds in water by use of headspace SPME followed by GC-MS[J]. Water Purification Technology, 2024, 43(3): 194-203 (in Chinese).
[27] 易欣源, 曲鑫璐, 龙昕, 等. 饮用水中典型消毒副产物的化学特性、生成转化及毒性研究进展[J]. 生态毒理学报, 2023, 18(2): 97-110. YI X Y, QU X L, LONG X, et al. Research progress on chemical properties, transformation and toxicity of typical disinfection byproducts in drinking water[J]. Asian Journal of Ecotoxicology, 2023, 18(2): 97-110 (in Chinese).
[28] HEBERT A, FORESTIER D, LENES D, et al. Innovative method for prioritizing emerging disinfection by-products (DBPs) in drinking water on the basis of their potential impact on public health[J]. Water Research, 2010, 44(10): 3147-3165. doi: 10.1016/j.watres.2010.02.004 [29] HEASLEY V L, ANDERSON M E, COMBES D S, et al. Investigations of the structure and reactions of the intermediate in the chlorination of resorcinol[J]. Environmental Toxicology and Chemistry, 1993, 12(9): 1653-1659. doi: 10.1002/etc.5620120914 [30] PATNAIK P, YANG M, POWERS E. Phenol-chlorine reaction in environmental waters: Formation of toxic chlorophenol derivatives[J]. Am Lab New, 2000, 32(19): 16. [31] 朱惠芳, 胡美华, 胡贵祥. 自动顶空固相微萃取与气相色谱-质谱联用同时测定饮用水中的4种氯酚[J]. 现代预防医学, 2015, 42(11): 2037-2039,2041. ZHU H F, HU M H, HU G X. Determination of four chlorophenols in drinking waters using gas chromatography-mass spectrometry coupled with auto headspace solid-phase micro extraction[J]. Modern Preventive Medicine, 2015, 42(11): 2037-2039,2041(in Chinese).
-



 下载:
下载: