-
磷作为一种生命必需的元素,在我们的日常生活中起着不可替代的作用,但过量的磷排放会造成水体生态系统破坏,引起水体富营养化,对用水安全构成严重威胁[1]。我国对水体中磷污染物的排放标准日趋严格。《城镇污水处理厂污染物排放标准GB 18918-2002》规定,出水总磷(TP,以P计)质量浓度应满足一级A(TP≤0.5 mg·L−1)标准。北京市要求新(改、扩)建城镇污水处理厂排入地表II、III类水体出水TP质量浓度执行A≤0.2 mg·L−1要求[2]。尽管如此,水体中TP质量浓度超过0.02 mg·L−1就可能造成水体富营养化[3],这一浓度阈值反映了磷对水生生态系统平衡的敏感性,以及去除水体中低质量浓度磷的重要性。磷酸盐(PO43−-P)是水中TP的主要成分,其高度可溶性增加了从水体中完全去除的难度[4]。因此,以合理的成本有效且高效地将水体中低质量浓度磷酸盐(PO43−-P≤0.5 mg·L−1)进一步降低到极低(PO43−-P≤0.2 mg·L−1)水平是具有挑战性的[5],这对提高水体水质,解决水体富营养化具有重要意义[6]。
目前,污水厂主要通过强化混凝技术对磷进行深度处理,运行过程需要混凝絮体回流、持续补充微砂等,且需要多台机泵、水力旋流器等配套设施,成本较高且占地面积相对较大。近年来,吸附法因其操作简便、低成本、高效率、低污染以及运行效果稳定而受到研究者的重视。吸附法不仅能有效去除水体中可溶性磷,将其浓度降至极低水平,还具备回收磷资源的潜力,可采用适当的解吸方法回收磷资源,以缓解全球磷资源的短缺[7]。高吸附容量吸附剂的制备是吸附法研究重点。镧(La)基吸附剂,因La与PO43−-P之间的溶度积常数极低(Ksp=3.7×10−23),即使在痕量水平也对PO43−-P表现出很强的亲和力,成为了当前研究热点[8]。但目前主流La基吸附剂常为粉末状,不宜回收,为此需要新型颗粒状载体制备载La吸附剂[9]。壳聚糖(CS)因其来源丰富、无毒且价格低廉,含有丰富的羟基和氨基等官能团,对PO43−-P具有很高的吸附潜力,常被用作载体使用,然而CS容易在低pH时溶解[10],常掺入其他材料,如聚乙烯醇(PVA)等,形成水凝胶(CS/PVA)作为载体使用。此外,为解决吸附剂回收问题,引入磁性结构,通过磁力回收是一种高效可行的方案。磁性纳米颗粒四氧化三铁(M-Fe3O4)是一种优良的可回收磁性材料[11],可以尝试与吸附剂结合,提高吸附剂的分离效率,并实现吸附剂的循环利用和资源的节约。
本研究以CS/PVA为载体,负载金属La,并掺入M-Fe3O4,制备了一种可磁性分离回收的除磷吸附剂(M-La-CS/PVA),用于从水体中去除低质量浓度PO43−-P。通过分析M-La-CS/PVA的组成、形貌、结构特征及金属La负载情况等,结合考察pH、共存阴离子等工艺参数对水体中PO43−-P的吸附性能的影响,研究其循环使用性能,并结合实验结果和表征结果分析吸附机理,以期为M-La-CS/PVA吸附剂在实际应用中提供支撑。
-
实验中所需要实验试剂纯度均为分析纯。CS(脱乙酰度为90%)、醋酸(CH3COOH)、盐酸(HCl)、氢氧化钠(NaOH)和磷酸二氢钾(KH2PO4)购自天津市大茂化学试剂厂。PVA(聚合度为124)、硝酸镧六水合物(La(NO3)3·6H2O)和M-Fe3O4购自上海麦克林生化科技股份有限公司。实验溶液均采用去离子水(DI)配置。
用KH2PO4配制质量浓度为50 mg·L−1磷酸盐储备液,不同PO43−-P质量浓度的废水由磷酸盐储备液稀释,调节pH=7后使用。低质量浓度(0.5 mg·L−1)磷酸盐废水,用0.1 mol·L−1 HCl和NaOH调节,高质量浓度(10~100 mg·L−1)磷酸盐废水用5 mol·L−1 HCl和NaOH调节。
-
M-La-CS/PVA制备流程如图1所示。首先将3 g CS溶解于50 mL 2%CH3COOH中,磁力搅拌至完全溶解;将6 g PVA加入100 ml DI中加热至95 °C并不断搅拌,使PVA充分溶解。将上述两种溶液混合均匀,然后向混合溶液中加入6.5 g La(NO3)3·6H2O固体,搅拌均匀,确保La均匀分散在溶液中后,再加入1 g M-Fe3O4粉末,搅拌均匀,并超声5 min消除气泡。最后,将得到的溶液逐滴滴入1 mol·L−1 NaOH溶液中,形成直径约5 mm的球状水凝胶,静置3 h后用DI洗至中性,置于−20 °C下冰箱中冷冻12 h后放入冷冻干燥机中冷冻干燥24 h,得到M-La-CS/PVA吸附剂。制备过程中,若不加La(NO3)3·6H2O固体,则得到M-CS/PVA吸附剂;若不加M-Fe3O4粉末,则得到La-CS/PVA吸附剂;若不加La(NO3)3·6H2O固体也不加M-Fe3O4粉末,则得到CS/PVA载体。
-
1)吸附性能研究。在恒温振荡箱内进行实验,PO43−-P质量浓度为0.5 mg·L−1,温度为25 ℃,转速为150 r·min−1。考察溶液pH,吸附剂投加量,共存阴离子等因子对M-La-CS/PVA吸附除磷效果的影响。pH考察范围为1~12,取整数值。参考天然水体pH(pH=6.8~7.2),在中性条件下,即pH=7时,考察M-La-CS/PVA投加量对吸附除磷效果的影响,M-La-CS/PVA投加量分别为0.5、1.0、1.5、2.0、4.0和6.0 g·L−1。在pH=7时,M-La-CS/PVA最佳投加量,即2 g·L−1时,考察不同浓度(1 mmol·L−1和10 mmol·L−1)共存阴离子NO3−、Cl−、CO32−和SO42−对M-La-CS/PVA吸附除磷性能的影响。在考察吸附时间因子,进行了预实验,结果表明, 在M-La-CS/PVA投加量2 g·L−1 ,pH=7条件下,反应60 min后,PO43−-P质量浓度低于0.1 mg·L−1,因此,最大吸附时间选择60 min。
为了进一步考察M-Fe3O4掺杂对M-La-CS/PVA吸附除磷效果的影响,在pH=7时, M-La-CS/PVA和La-CS/PVA投加量均为2 g·L−1时,对比相同吸附时间后水中PO43−-P质量浓度。
2)吸附动力学分析。在恒温振荡箱内进行,在初始PO43−-P质量浓度为0.5 mg·L−1,温度为25 ℃,转速为150 r·min−1,pH=7,M-La-CS/PVA投加量2 g·L−1条件下,在不同吸附时间,即5、15、30、45、60、75、90、120、150、180和240 min时取样,测定PO43−-P质量浓度。分别采用准一级动力学方程(式(1))、准二级动力学方程(式(2))和颗粒内扩散方程(式(3))对吸附动力学实验数据进行拟合。
式中:qe为平衡时的吸附量,mg·g−1;qt为t时刻时的吸附量,mg·g−1;t 为吸附时间,min;k1为准一级动力学常数,L·min−1;k2为准二级动力学常数,g·(min·mg)−1; kdi为颗粒内扩散的速率常数,mg·min−0.5·g−1;C为常数,颗粒内扩散方程的截距。
3)吸附等温线。在恒温振荡箱内进行,分别考察25、35和45 ℃时,不同初始PO43−-P质量浓度(10~100 mg·L−1)下M-La-CS/PVA的吸附性能。反应条件:转速150 r·min−1,M-La-CS/PVA投加量1 g·L−1,pH=7,反应时间24 h。采用 Langmuir模型(式(4))和 Freundlich模型(式(5))对数据进行拟合。
式中:Ce为平衡时吸附质的浓度,mg·L−1; qe为平衡时吸附质的吸附量,mg·g−1;qm为吸附剂的最大吸附量,mg·g−1;KL为 Langmuir常数,L·mg−1;KF为 Freundlich常数,mg·g−1·(L·mg−1)1/n;n为与吸附强度有关的常数。
4)吸附热力学分析。通过式((6)、式(7)和式(8))计算吉布斯自由能变、焓变和熵变3个热力学参数。
式中:KC为吸附平衡常数,mg·L−1;ΔG°为吉布斯自由能变,kJ·mol−1;R为通用气体常数,8.314 J·(mol·K)−1;T为吸附反应的温度,K;ΔS°为熵变,kJ·(mol·K)−1;ΔH°为焓变,kJ·mol−1。
-
为研究M-La-CS/PVA吸附PO43−-P的循环使用性能,在确定解吸液的基础上,进行5次吸附-脱附循环实验。解吸液共6种,分别为2种浓度(0.1 mol·L−1和1 mol·L−1)的HCl溶液、3种浓度(0.1、1和3 mol·L−1)的NaOH溶液及3 mol·L−1NaOH与1.5 mol·L−1NaCl混合溶液。反应条件:PO43−-P质量浓度为100 mg·L−1,温度25 ℃,转速150 r·min−1,吸附饱和的M-La-CS/PVA投加量1 g·L−1,反应时间24 h。
-
通过全自动比表面积及孔隙分析仪(BET,Micromeritics ASAP
2460 ,USA)测定M-La-CS/PVA孔隙结构特征;采用流变仪(Anton Paar MCR 302,AT)测定M-La-CS/PVA的储能模量;采用扫描电子显微镜(SEM,Tescan Mira Lms,CZ)分析M-La-CS/PVA和M-CS/PVA的表面和内部形貌;采用X射线衍射仪(XRD,Rigaku Ultima IV,JPN)测定M-La-CS/PVA的晶体结构;采用傅里叶红外光谱(FTIR,Thermo Scientific Nicolet iS20,USA)测定M-La-CS/PVA的官能团;采用热重分析仪(TG,Netzsch STA 449 F5,DE)测定M-La-CS/PVA的热稳定性;采用振动样品磁强计(VSM,LakeShore7404 ,USA)测定M-La-CS/PVA的饱和磁化强度;采用Zeta电位分析仪(DLS,Malvern Zetasizer Nano ZS ZEN3600,UK)测定M-La-CS/PVA的Zeta电位;采用X射线光电子能谱仪(XPS,Thermo Scientific K-Alpha,USA)对M-La-CS/PVA进行化学成分分析;采用钼酸铵分光光度法(GB11893 -89)测定水中PO43−-P质量浓度。 -
1)比表面积及平均孔径。通过BET表征,考察CS/PVA、M-CS/PVA和M-La-CS/PVA比表面积及平均孔径大小。结果发现,载体CS/PVA比表面积为0.925 6 m2·g−1,总孔容为0.006 5 cm3·g−1,平均孔径为28.049 5 nm;添加M-Fe3O4后,M-CS/PVA比表面积增加到1.909 0 m2·g−1,总孔容增至0.011 3 cm3·g−1,但平均孔径减至23.587 7 nm。M-La-CS/PVA的比表面积、总孔容、平均孔径比M-CS/PVA分别增加了52.90%、64.58%和25.00%,平均孔径比载体CS/PVA增加了10.82%。更高的比表面积以及更大的孔容和平均孔径利于磷酸盐在其内部扩散和吸附[12]。
2)弹性分析。图2为M-La-CS/PVA的储能模量和损耗模量随频率的变化曲线。M-La-CS/PVA的储能模量大于其损耗模量表现出较强的固态凝胶特性,主要发生弹性形变[13]。M-La-CS/PVA的储能模量在固定应变下随频率的增大逐渐缓慢提高,在23~45 kPa内,具有良好的机械强度,在承受外力时具有较好的抵抗变形能力[14]。主要归因于CS和PVA之间的分子纠缠和相互作用[15],PVA在水凝胶中起到胶水的作用,不仅能够与CS紧密结合,形成稳定的网络结构,还能够将M-La-CS/PVA中的无机成分La有效地连接起来,进一步增强M-La-CS/PVA的稳定性和机械性能[16]。
3)表面和内部形貌。图3为M-La-CS/PVA和M-CS/PVA 的SEM图像。M-La-CS/PVA外形呈近似球形(图3(a)),而M-CS/PVA形状不规则(图3(b))。这是因为M-La-CS/PVA混合液比M-CS/PVA混合液具有更低的黏度和更高的表面张力,液体分子之间的内聚力更高[17],导致M-La-CS/PVA溶液滴在NaOH溶液中形成了更加规则的球体。M-La-CS/PVA的横截面显示出多孔的内部结构(图3(c))。磷酸盐可在内部孔道充分扩散,并与更多吸附位点接触,促进吸附过程。
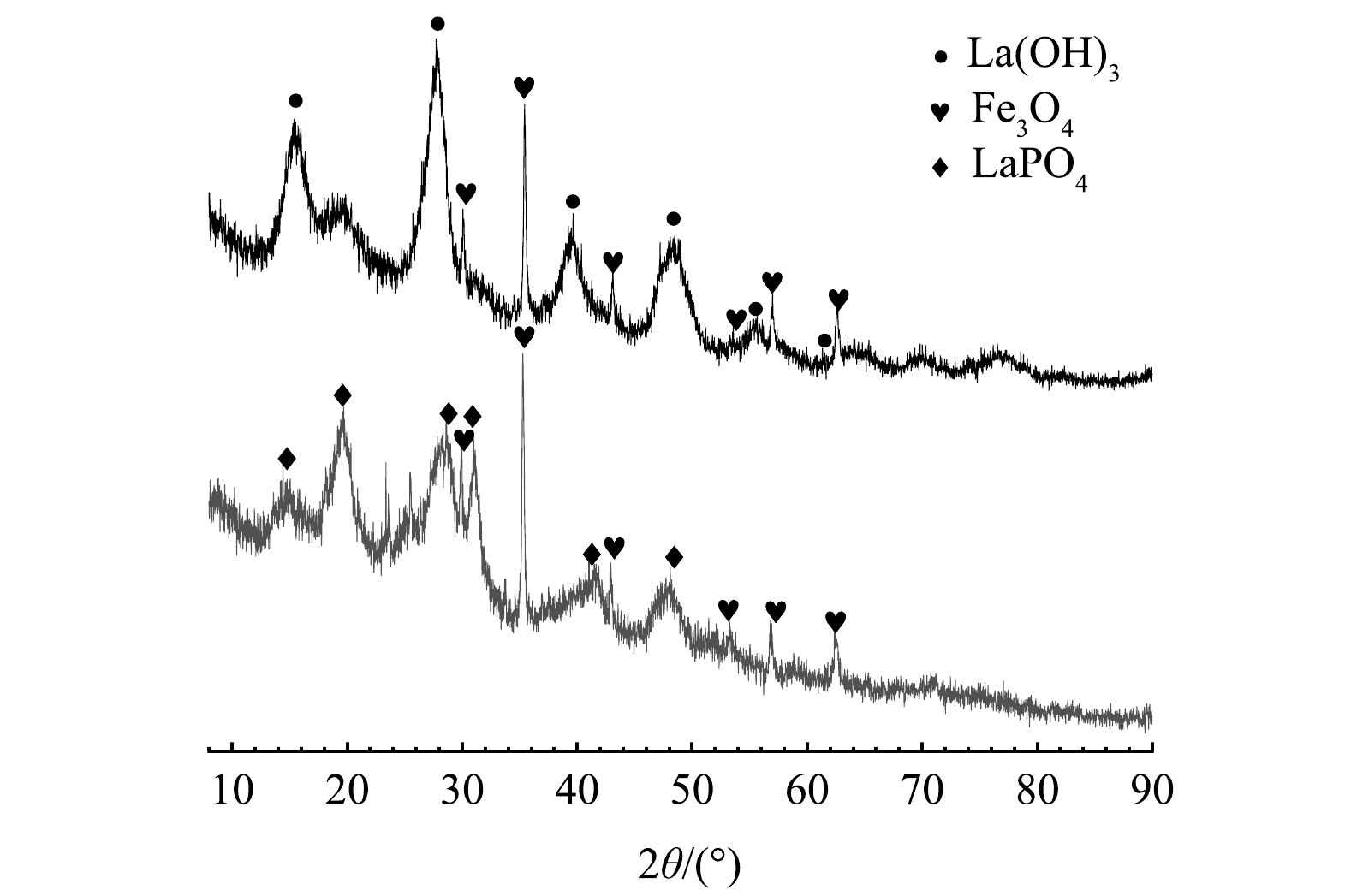
4)晶体结构分析。图4为M-La-CS/PVA吸附磷酸盐前后的XRD图。吸附前,在2θ=15.78°、27.74°、39.66°、48.34°、56.39°和58.94°处的特征衍射峰是La(OH)3结晶 [JCPDS 65-0585],这是由于在M-La-CS/PVA的制备过程中使用了NaOH溶液, La以La(OH)3形式负载于M-La-CS/PVA上[18]。在2θ=30.23°、35.65°、43.27°、53.57°、57.26°和62.83°处的6个衍射峰分别对应指数分别为(220)、(311)、(400)、(422)、(440)和(511),与具有尖晶石结构的Fe3O4晶体匹配良好[JCPDS 00-019-0629],表明凝胶性质不影响Fe3O4的结构[19]。吸附磷酸盐后出现LaPO4的特征衍射峰[JCPDS 04-009-
6183 ],即14.78°(100)、19.46°(101)、29.87°(200)、31.22°(211)、43.22°(212)和48.55°(312),表明部分磷酸盐与 La(OH)3 中的羟基发生了交换 ,在吸附剂上形成了LaPO4[20]。5)官能团分析。图5为M-La-CS/PVA吸附磷酸盐前后FTIR光谱图。M-La-CS/PVA吸附磷酸盐前在3 303 cm−1处有明显吸收峰,归因于M-La-CS/PVA中氨基和羟基拉伸振动引起的[21]。吸附磷酸盐后羟基的吸收峰位移到了3 391 cm−1处,是由于磷酸盐和M-La-CS/PVA发生了配体交换作用[22],导致了羟基的位置发生了变化。1 423 cm−1处为La-OH吸收峰[23],649 cm−1处的特征峰与Fe-O的拉伸振动有关[24],说明La和Fe被成功负载于CS/PVA载体上。M-La-CS/PVA吸附磷酸盐后在535 cm−1处出现新峰,该峰归因于P-O键的拉伸振动[25],表明M-La-CS/PVA已成功吸附了磷酸盐。
6)热重分析。图6为M-La-CS/PVA的热重分析曲线图。在氮气气氛下通过TG分析M-La-CS/PVA的热稳定性,M-La-CS/PVA的质量在整个过程中呈逐渐下降的趋势。从室温到200 ℃,M-La-CS/PVA的质量损失了10.91%,这是由于游离的水分蒸发所致[26];在200~350 ℃时,失质量率约为33.18%,主要原因是温度升高CS的三维网络结构发生分解,CS主链中C-O-C糖苷键断裂[12],还有一些不稳定的官能团,如氨基和一部分羟基的分解[27];350~800 ℃的失质量率约为21.61%,主要热重损失归因于PVA分子中羟基的分解[28];800 ℃仍有34.30%残留。这些结果表明,M-La-CS/PVA具有良好的热稳定性,可归因于CS和PVA之间通过疏水侧链聚集以及分子间和分子内氢键的相互作用,形成了相对致密的聚合物网络结构[29],使得La和M-Fe3O4负载在其上,需要更多的能量进行分解[30]。
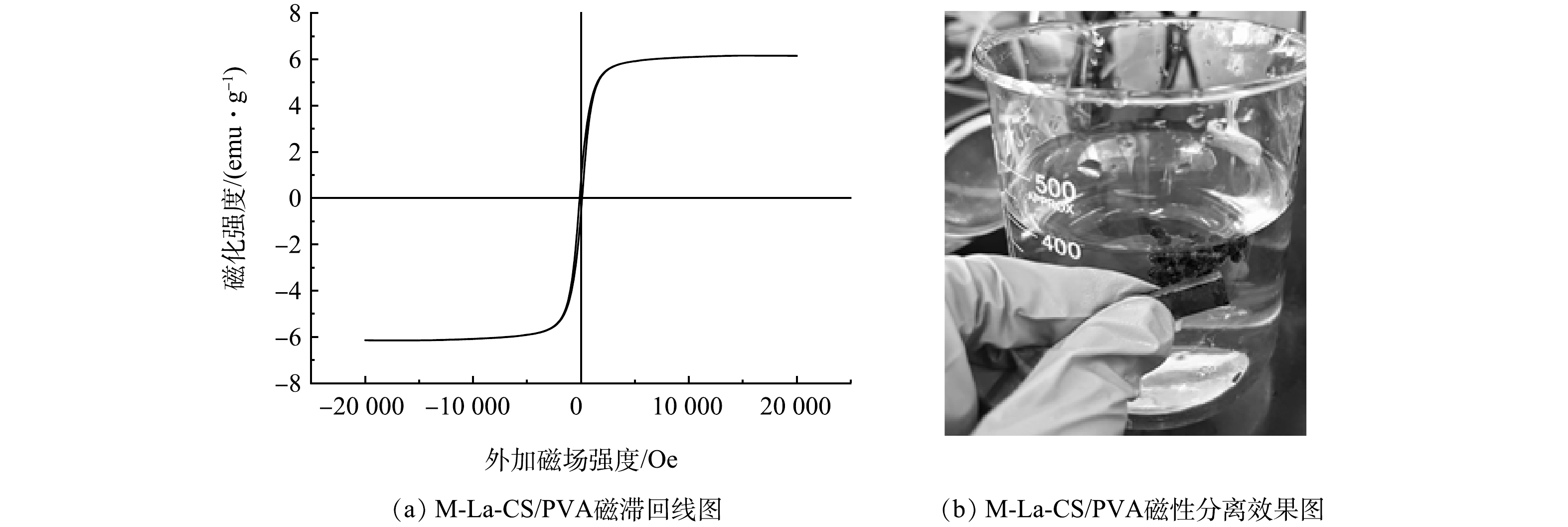
7)磁性分析。图7(a)为M-La-CS/PVA的磁滞回线图。M-La-CS/PVA的饱和磁化强度为6.14 emu·g−1。磁化强度随着外加磁场强度的增大而逐渐升高,表明M-La-CS/PVA对外加磁场的响应是积极的[31]。磁滞回线表现出与原点对称的 S 形,说明M-La-CS/PVA的磁化状态能够迅速且可逆地跟随磁场的变化,没有发生滞后现象。剩余磁性和矫顽力均为 0,表明M-La-CS/PVA在磁场去除后不会保留任何磁性,且不需要额外的反向磁场来消除其磁性[32]。可见,M-La-CS/PVA是一种超顺磁性材料。当添加外部磁场时(图7(b)),M-La-CS/PVA能够快速地被磁铁吸附,实现吸附剂在溶液中快速完全分离。
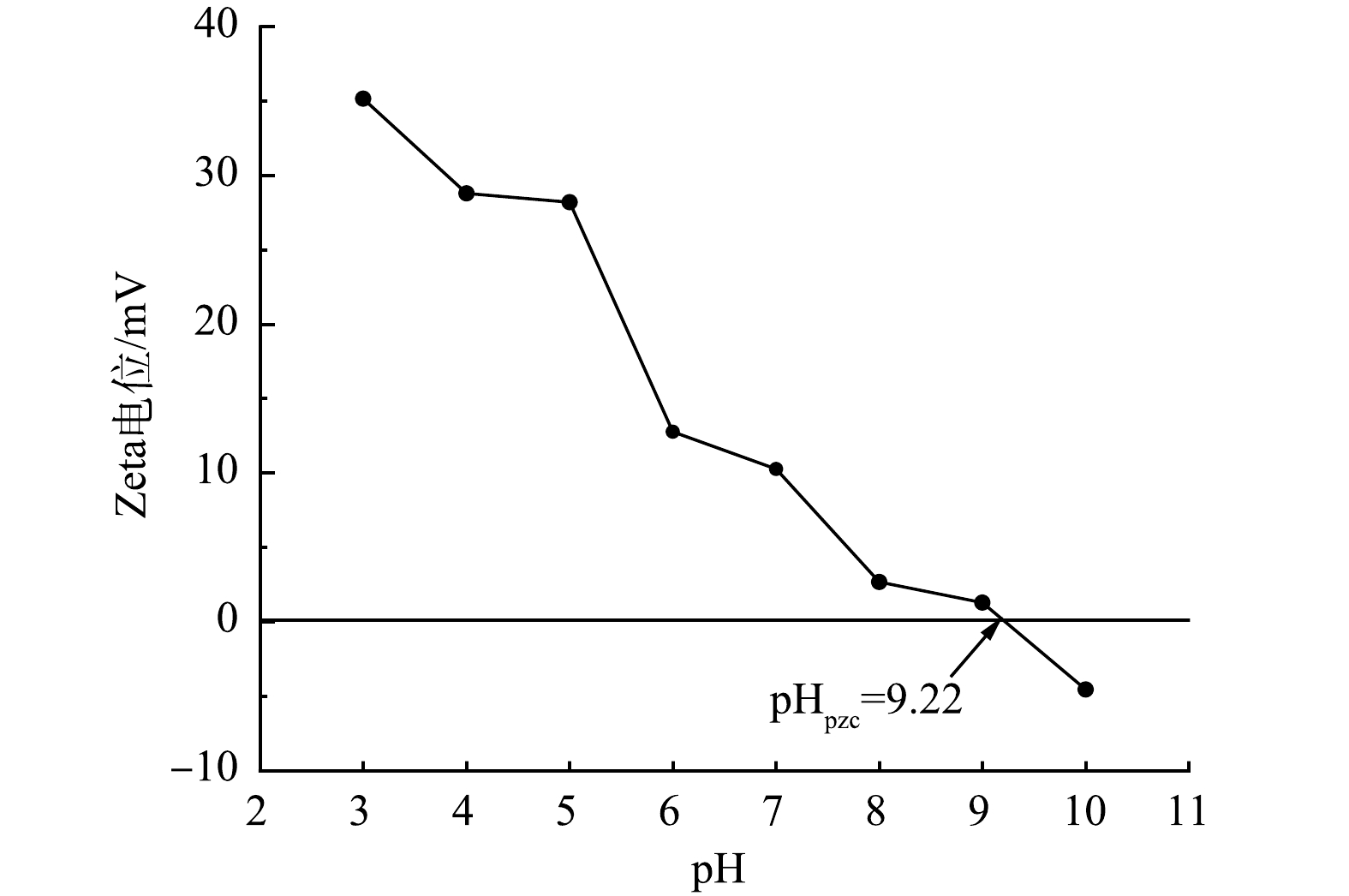
8)零电荷点分析。图8是M-La-CS/PVA在不同pH条件下的Zeta电位变化图。M-La-CS/PVA的表面电荷很大程度上取决于溶液的pH[33]。测得M-La-CS/PVA的零点电荷pHpzc=9.22,M-La-CS/PVA在很宽的pH范围内具有永久正电荷,这种永久正电荷特性可能是由于La的掺入增加了M-La-CS/PVA的正电性[34]。此外, CS和PVA之间的相互作用(如氢键)也促进了正电荷的保持。当溶液pH<pHpzc时,M-La-CS/PVA表面一些可质子化官能团会倾向于与溶液中的H+结合,从而发生质子化过程,导致表面带正电荷;当溶液pH>pHpzc时,M-La-CS/PVA表面已质子化的官能团与溶液中OH−发生反应,释放质子,从而发生去质子化过程,导致表面带有负电荷。
-
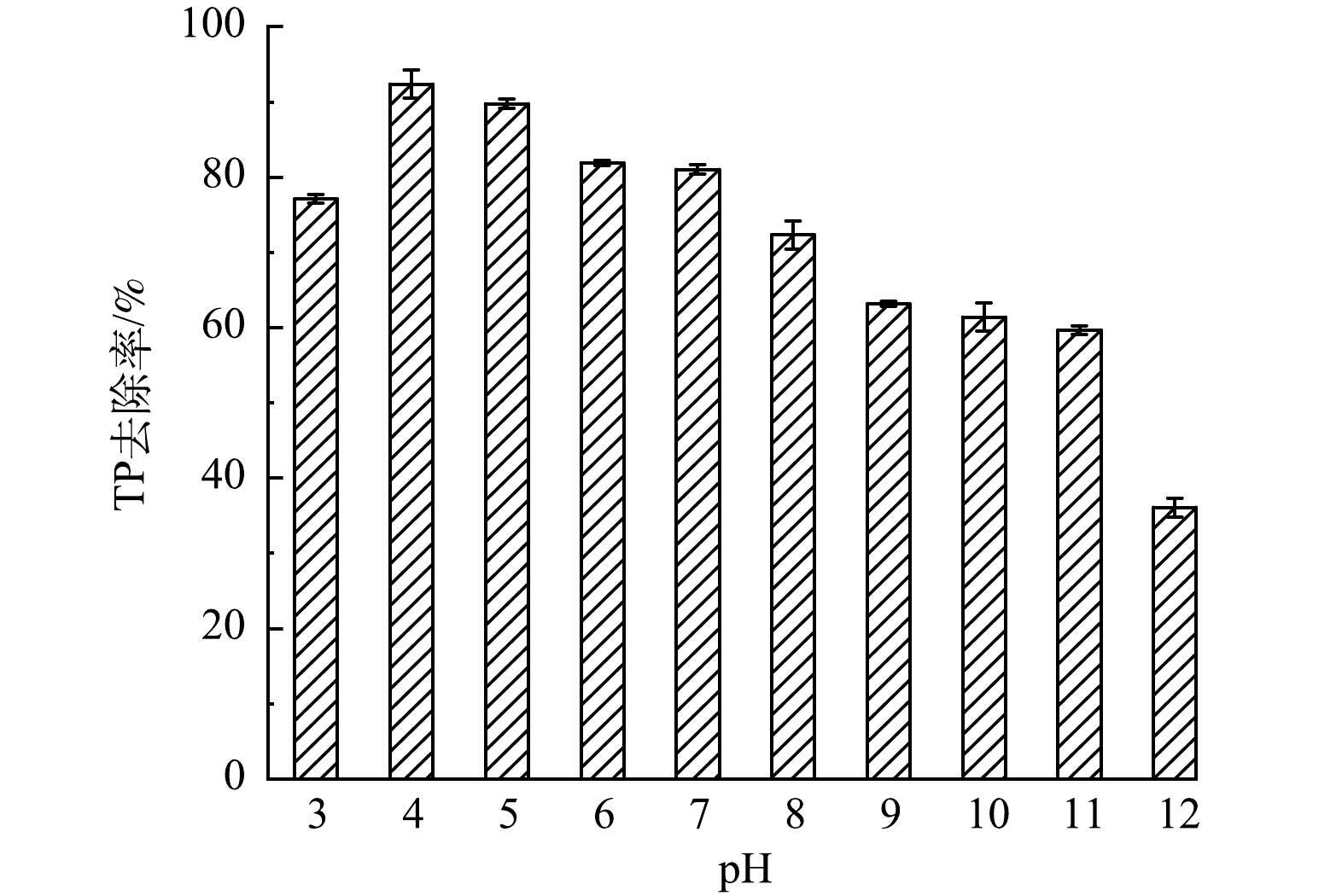
1)初始pH影响。图9是不同初始pH对M-La-CS/PVA吸附磷酸盐的影响。当pH为1和2时,无吸附效果。在酸性条件(pH=3~7)下,随着pH增加,PO43−-P去除率呈先增加后减小趋势,在pH=4时,M-La-CS/PVA吸附效果最好,PO43−-P去除率为92.37%。在碱性条件(pH=8~12)下,随着pH的增大,PO43−-P去除率逐渐降低,在pH=10时,PO43−-P去除率为61.40%,此时PO43−-P质量浓度为0.19 mg·L−1。pH=12时,PO43−-P去除率为36.11%。
PO43−-P去除率与不同pH下磷的存在形态及M-La-CS/PVA的pHpzc有关。在pH≤3时,水体中磷主要以H3PO4和H2PO4−的形态存在[35],而M-La-CS/PVA表面La以La-OH2+正电形态存在,这使得La-OH2+与H3PO4结合的难度增加[36],不利于磷的吸附。当pH=4时,水体中磷主要以H2PO4−形式存在[37],易于与荷正电的M-La-CS/PVA发生静电相互作用,提高磷酸盐吸附效率。当溶液pH继续增大,OH−浓度增加,与PO43−-P竞争吸附位点,且M-La-CS/PVA所带正电荷减少,静电作用减弱[38]。当溶液pH>7时,磷酸盐存在形态主要为HPO42−和PO43−,与一价的H2PO4−相比,HPO42−和PO43−的吸附自由能较高[39],不利于磷的吸附,且当溶液pH>9.22(pHpzc)时,M-La-CS/PVA表面去质子化带负电荷,与磷酸盐阴离子产生电荷排斥,导致M-La-CS/PVA吸附性能进一步降低。
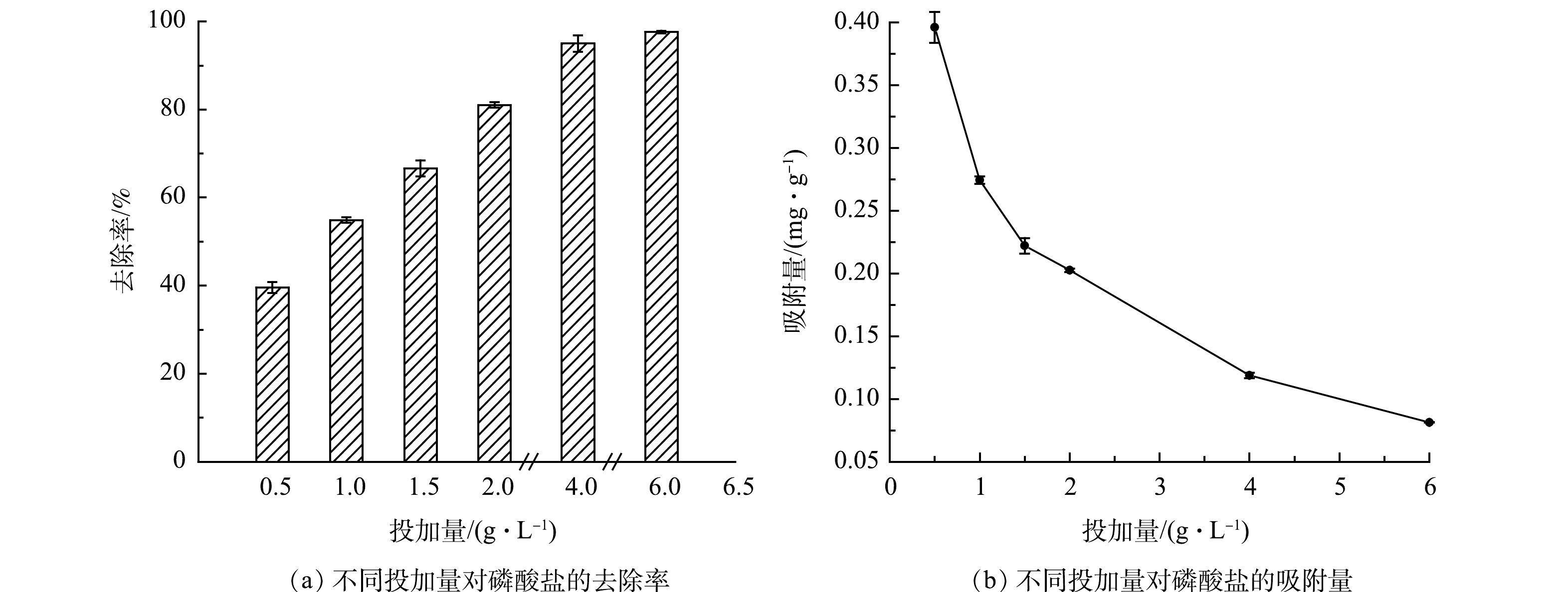
2)投加量影响。图10是M-La-CS/PVA不同投加量对磷酸盐吸附效果的影响。随着M-La-CS/PVA的投加量增大,PO43−-P去除率呈现出迅速提升后逐渐趋于平稳的趋势,当M-La-CS/PVA投加量从0.5 g·L−1增加到2.0 g·L−1时, PO43−-P去除率由39.60%升至81.03%,但M-La-CS/PVA对PO43−-P的吸附量由0.396 0 mg·g−1下降至0.202 6 mg·g−1(图10(b))。分析原因为,随着M-La-CS/PVA投加量的增加,可利用的吸附位点也逐渐增加,PO43−-P去除率随之增加。然而,水体中PO43−-P的量是有限的,当溶液中PO43−-P质量浓度低至一定程度时,M-La-CS/PVA吸附位点得不到有效利用,使得单位M-La-CS/PVA吸附剂对PO43−-P吸附量逐渐下降。当投加量从2.0 g·L−1增加到6.0 g·L−1时,PO43−-P去除率仅增加了16.57%,M-La-CS/PVA吸附量降至0.081 3 mg·g−1。因此,在实践中M-La-CS/PVA投加量推荐采用2.0 g·L−1。
3)共存阴离子影响。图11是不同浓度共存阴离子对M-La-CS/PVA吸附磷酸盐的影响。在实际废水中,常存在多种其他阴离子如NO3−、Cl−、CO32−及SO42−与磷酸盐共存[40]。这些共存阴离子的存在可能会对M-La-CS/PVA吸附PO43−-P的效果产生影响。由图11可以看出,共存阴离子NO3−、Cl−及SO42−对M-La-CS/PVA吸附磷酸盐几乎没有影响。
CO32−对会抑制M-La-CS/PVA对磷酸盐的吸附,当CO32−浓度为1 mmol·L−1和10 mmol·L−1时,PO43−-P去除率分别下降了4.36%和11.34%。分析认为,可能有2个方面原因。一方面是由于CO32−的添加导致溶液pH增加所致,添加1 mmol·L−1和10 mmol·L−1的CO32−后,溶液pH由7分别增大至8.17和8.39,此时溶液中98%以上碳酸化合物以HCO3−存在,pH增大抑制了M-La-CS/PVA与磷酸盐之间的静电作用[41]。若添加1 mmol·L−1和10 mmol·L−1的CO32−后调节溶液pH至中性后进行吸附,此时碳酸化合物80%以HCO3−存在,20%以CO32−存在, PO43−-P去除率下降幅度降低,分别下降了2.18%和6.98%。另一方面,HCO3−和CO32−均与La之间有强烈的亲和力,与M-La-CS/PVA表面含La活性位点进行配体交换生成La (HCO3)3和La2 (CO3)3 [42],La (HCO3)3与LaPO4溶度积常数相似,表明HCO3−和PO43−-P在与La结合时竞争力相当,La2(CO3)3的Ksp= 3.98×10−34远低于LaPO4(Ksp=3.7×10−23),表明CO32−与La的结合能力比PO43−-P与La的结合能力更强,会竞争更多的吸附位点,从而导致PO43−-P去除率降低[43]。
4) Fe元素影响。图12是M-La-CS/PVA和La-CS/PVA吸附剂对磷酸盐吸附性能的影响。在相同实验条件下,M-La-CS/PVA对磷酸盐的去除率均比La-CS/PVA略高,但均不超过6%。通过BET、XRD及FTIR等表征手段分析,可能是由于La和具有尖晶石结构M-Fe3O4的掺入,使M-La-CS/PVA具有较大的比表面积,以及提供了更多羟基基团作为活性位点,通过内球络合提高了磷吸附效果。M-La-CS/PVA的磁性特征使得M-La-CS/PVA表现出独特的优势。
-
M-La-CS/PVA准二级动力学模型(R2=0.989 3)比准一级动力学模型(R2=0.967 3)能更好的描述M-La-CS/PVA对磷酸盐的吸附过程(图13(a)),表明M-La-CS/PVA吸附磷酸盐的主要过程是化学吸附[44]。采用颗粒内扩散模型进一步考察M-La-CS/PVA吸附过程中速率步骤,发现M-La-CS/PVA吸附过程经历了3个阶段(图13(b))。首先,外扩散阶段(R2=0.994 6),此阶段溶液中的PO43−-P迅速扩散到M-La-CS/PVA表面,由于M-La-CS/PVA表面含有大量的吸附位点,可与PO43−-P充分结合。其次,孔隙扩散阶段(R2=0.923 1),此时PO43−-P从M-La-CS/PVA外表面扩散到内部。最后,扩散平衡阶段(R2=0.885 7),因为水体中剩余的PO43−-P浓度极低,并且较多吸附位点已被占用[45],导致PO43−-P去除率降低。由于3条拟合曲线未过原点,说明吸附速率由外扩散和孔隙扩散共同决定,因此,增加M-La-CS/PVA的孔隙度有利于提高其对磷酸盐的吸附,这与朱畅[46]的研究结果一致。
-
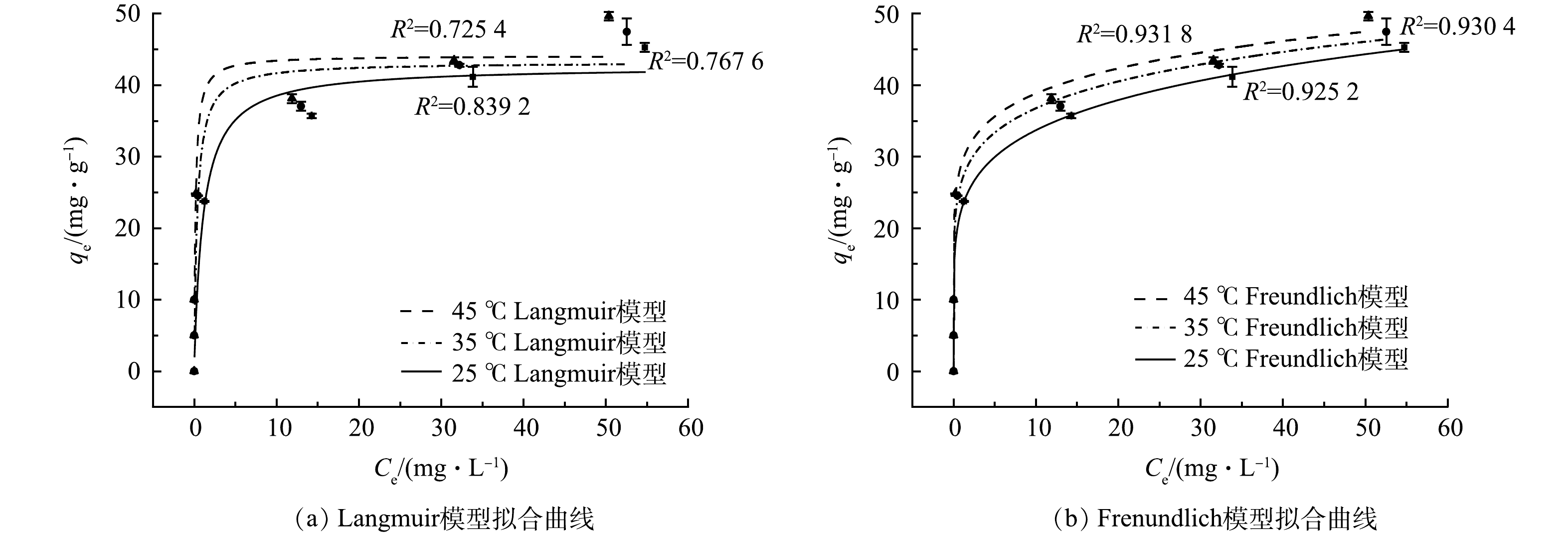
吸附等温线用于描述恒温下不同平衡浓度(Ce)与平衡吸附量(qe)之间的关系[47]。采用Langmuir和Freundlich模型对不同温度下M-La-CS/PVA吸附数据进行拟合。拟合结果见图14,拟合参数见表1。如图14所示,无论用Langmuir或Freundlich模型拟合,随着温度升高,M-La-CS/PVA对磷酸盐的吸附量均增加,说明该吸附过程为吸热反应,温度升高有利于吸附反应[48]。从表1可以看出,3种温度下,Freundlich模型均比Langmuir模型能更好地描述M-La-CS/PVA对磷酸盐的吸附过程,表明该吸附过程为非均相的多分子层吸附[49], n−1在0~1且接近0的范围内,表明M-La-CS/PVA对磷酸盐吸附良好[50]。M-La-CS/PVA在25 ℃时对PO43−-P的饱和吸附量(qm)为45.27 mg·g−1。
-
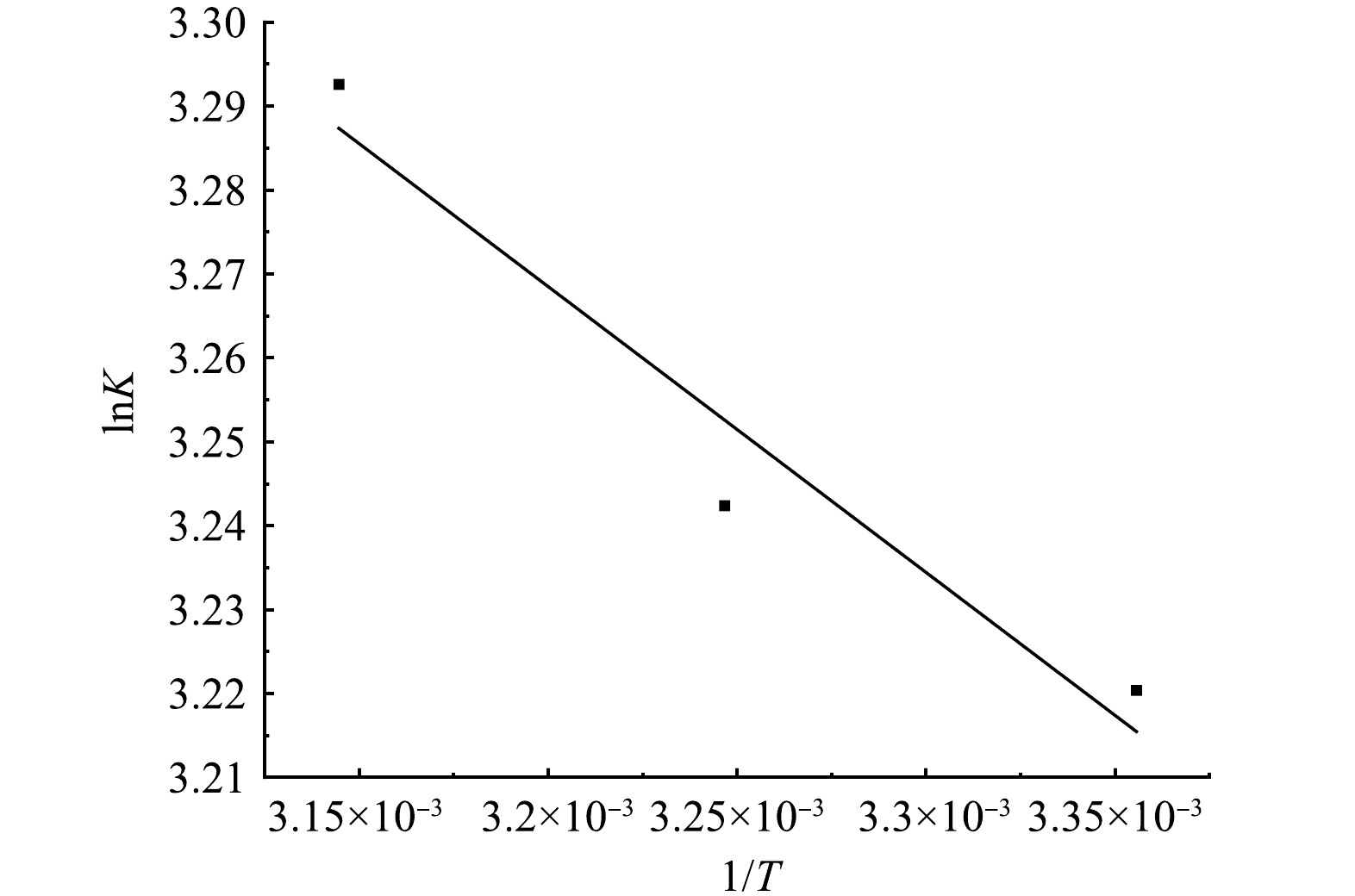
为了进一步研究M-La-CS/PVA对磷酸盐吸附的热力学行为,计算了在不同温度下热力学参数,包括吉布斯自由能变(ΔG°,kJ·mol−1)、焓变(ΔH°,kJ·mol−1)和熵变(ΔS°,kJ·mol−1·K−1)。结果如图15和表2所示,ΔG°在3个温度下均为负值,表明了M-La-CS/PVA对磷酸盐的吸附是可行的且是自发性的[19]。并且,随着温度的升高,ΔG°的绝对值逐渐增大,表明温度的升高有利于吸附的进行,同吸附等温线研究结果(图14)一致[51]。ΔH°为2.832 1 kJ·mol−1>0,表明M-La-CS/PVA吸附磷酸盐是一个吸热过程[52]。ΔS°为36.237 0 kJ·mol−1·K−1>0,表明在吸附过程中,M-La-CS/PVA与磷酸盐溶液界面处的随机性有所增加,磷酸盐与M-La-CS/PVA有较强的亲和力,使得磷酸盐能够更容易地吸附在M-La-CS/PVA的表面[38] 。
-
0.1和1 mol·L−1 HCl作为解吸液,M-La-CS/PVA在第1次循环后吸附能力分别为初始吸附能力的10.82%和13.00%,0.1 mol·L−1 NaOH作为解吸液第1次解吸后M-La-CS/PVA的吸附量仅有3.82 mg·g−1,故这3种解吸液不再进行后续吸附-解吸循环实验。其余不同解吸液完成5次吸附-解吸循环实验后M-La-CS/PVA吸附量及解吸量结果见表3。由表3可以看出,3 mol·L−1 NaOH和1.5 mol·L−1 NaCl混合液作为解吸液对M-La-CS/PVA的解吸效果最好,循环5次后,吸附容量仍保持初始吸附容量的73.03%,吸附容量为25.51 mg·g−1。分析认为NaOH可以降低吸附剂对磷酸盐的吸附能力,而NaCl则通过离子交换过程将磷酸盐从吸附剂中解吸出来[53]。此外,M-La-CS/PVA可以通过磁性回收,可见M-La-CS/PVA具有良好的分离回收及重复使用性能。
-
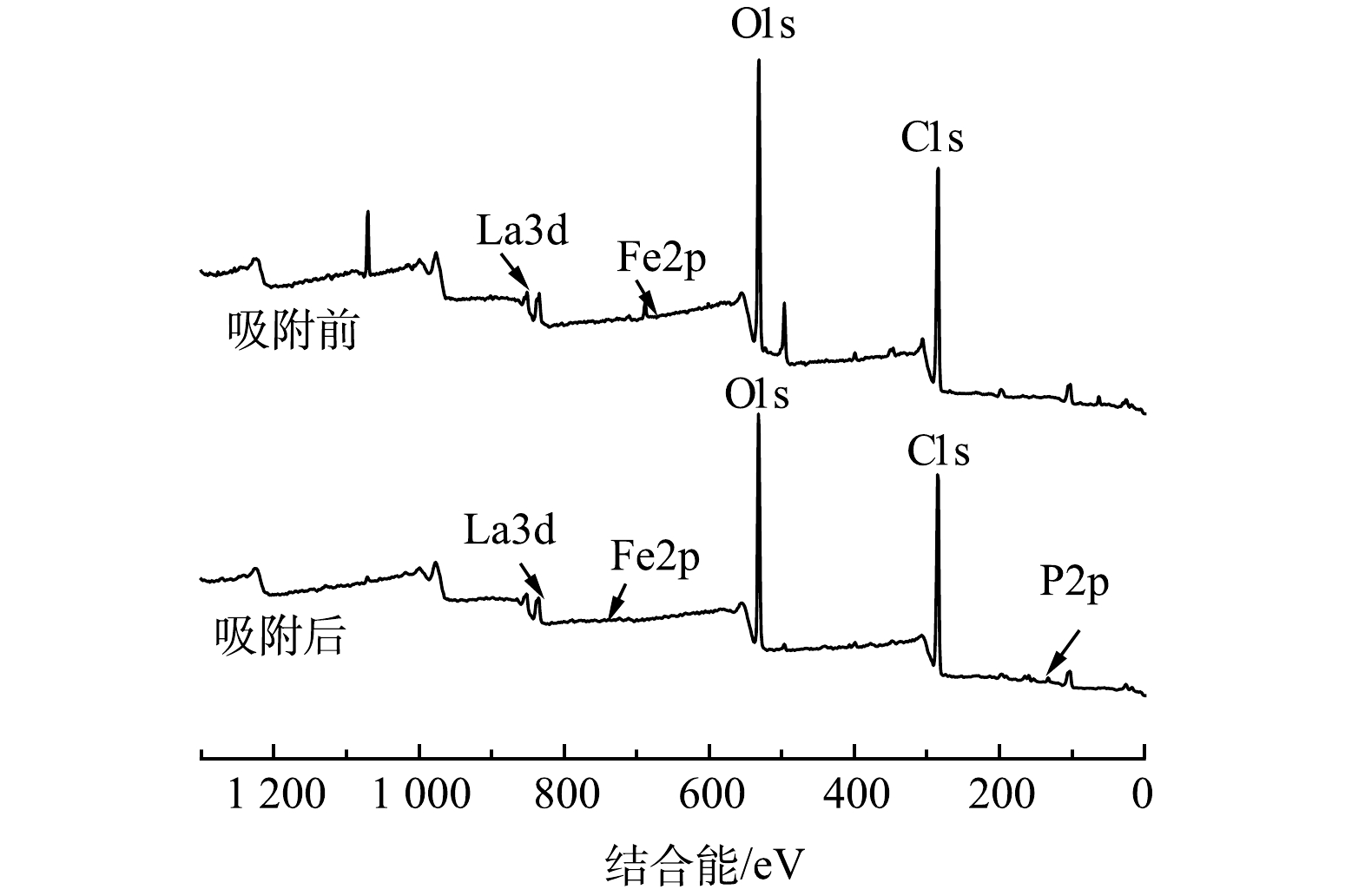
结合表征结果和吸附实验结果,探究M-La-CS/PVA的吸附机理。如图16所示,M-La-CS/PVA较大的比表面积和球状结构利于PO43−-P在其内部扩散和迁移,当PO43−-P与M-La-CS/PVA接触时,会发生化学反应。FTIR表征结果(图5)表明,M-La-CS/PVA上羟基与PO43−-P发生了配体交换反应[54],生成了P-O新官能团。XPS表征结果表明,M-La-CS/PVA吸附PO43−-P后,在132.08 eV处出现1个新峰,对应于P2p的特征峰,证明了PO43−-P已被成功吸附(图17)。吸附PO43−-P前La3d的峰分别位于834.08 eV和851.08 eV处,而吸附PO43−-P后这2个峰均正移了1.0 eV,即向更高能量的方向发生了偏移,这种偏移现象是由于La和PO43−-P发生了配体交换反应,形成了La-O-P内球络合物[55],并且出现的P2p的结合能(132.08 eV)低于KH2PO4中P2p的结合能(134.00 eV),说明吸附过程中有电子的重新分布,进一步证实了M-La-CS/PVA对磷酸盐的化学吸附作用[56]。此外,实验观察到M-La-CS/PVA吸附PO43−-P后溶液的pH略微增大,增加幅度在0.5~1.5,以初始pH=7时为例,吸附后溶液pH增至7.81,一方面,可能是由于M-La-CS/PVA在化学吸附过程中释放了额外的OH−到溶液中,另一方面,也可能形成的络合物碱性更强所致。
M-La-CS/PVA吸附PO43−-P过程也有静电吸附作用。Zeta电位表征结果(图8)表明当溶液pH<pHpzc时,M-La-CS/PVA可通过强烈的静电作用去除水体中PO43−-P。结合初始pH影响分析结果,证实了静电吸附在磷酸盐去除过程中的关键作用。综上所述, M-La-CS/PVA吸附磷酸盐主要是通过配体交换及静电吸附共同作用。
-
1) M-La-CS/PVA具有较大的比表面积、孔容和平均孔径,外部为球状,内部为多孔结构。具有良好的热稳定性及磁分离特性。FTIR、XPS等表征结果表明La和Fe被成功掺杂。
2) M-La-CS/PVA吸附磷酸盐过程受pH影响,在pH=3~11内保持较高的PO43−-P去除率,对于水中低质量浓度(0.5 mg·L−1)磷酸盐,出水PO43−-P质量浓度低于0.2 mg·L−1。在pH=4时PO43−-P去除率最高(92.37%);增加M-La-CS/PVA投加量能提高PO43−-P去除率,最佳投加量为2.0 g·L−1;共存阴离子NO3−、Cl−及SO42−对M-La-CS/PVA吸附磷酸盐几乎没有影响,CO32−离子(10 mmol·L−1)使得PO43−-P去除率降低了 11.34%。
3) M-La-CS/PVA吸附过程符合准二级动力学模型和Frenundlich等温模型,吸附过程为非均相的多分子层化学吸附,在25 ℃时饱和吸附量为45.27 mg·g−1。P-O与La-O-P之间的化学键和静电吸附作用在磷酸盐吸附中起主导作用。
4)以3 mol·L−1 NaOH和1.5 mol·L−1 NaCl混合液作为M-La-CS/PVA解吸液,经5次吸附-解吸循环,仍保持初始吸附容量的73.03%,M-La-CS/PVA可磁性分离,循环使用效果良好。
磁性载镧水凝胶对低浓度磷的吸附性能
Adsorption performance of magnetic lanthanum-loaded hydrogel towards low-concentration phosphorus
-
摘要: 以壳聚糖和聚乙烯醇为载体,采用共沉淀法制备了负载金属镧的磁性水凝胶吸附剂(M-La-CS/PVA),探究了其对水中磷酸盐的吸附特性及机理。M-La-CS/PVA饱和磁化强度为6.14 emu·g−1,在25 ℃时饱和吸附量为45.27 mg·g−1。在初始磷酸盐质量浓度为0.5 mg·L−1下,pH=3~10宽范围内磷酸盐去除率保持61.40%~92.37%,在pH=4时去除率最高。M-La-CS/PVA最佳投加量为2.0 g·L−1,共存阴离子NO3−、Cl−及SO42−对磷酸盐吸附几乎无影响,CO32−在10 mmol·L−1时会抑制磷酸盐吸附,磷酸盐去除率降低了11.34%。M-La-CS/PVA吸附磷酸盐的过程符合准二级动力学和Freundlich等温模型,为非均相多分子层化学吸附。P-O与La-O-P之间的化学键和静电吸附作用在磷酸盐吸附中起主导作用。以3 mol·L−1 NaOH和1.5 mol·L−1 NaCl为解吸液,经过5次吸附-解吸循环后,M-La-CS/PVA仍保持73.03%的吸附容量,是一种可磁性回收,性能稳定的高效磷酸盐吸附剂。Abstract: The magnetic hydrogel adsorbent loaded with lanthanum (M-La-CS/PVA) was prepared using the co-precipitation method with chitosan and polyvinyl alcohol as carriers. The adsorption characteristics and mechanisms of M-La-CS/PVA to phosphate in water were investigated. The saturation magnetization of M-La-CS/PVA was 6.14 emu·g−1, and the saturated adsorption capacity to phosphate was 45.27 mg·g−1 at 25 °C. When the initial phosphate mass concentration was 0.5 mg·L−1, the phosphate removal efficiency remained 61.40%~92.37% within the wide range of pH=3~10, and the highest removal efficiency occurred at pH=4. The optimum dosage of M-La-CS/PVA was 2.0 g·L−1. The coexisting anions, i.e. NO3−、Cl− and SO42− had slight effects on phosphate adsorption. CO32− anions at 10 mmol·L−1 could inhibit phosphate adsorption, and the phosphate removal rate decreased by 11.34%. The process of phosphate adsorption by M-La-CS/PVA conformed to the pseudo-second-order kinetics and Freundlich isotherm model, which was a type of heterogeneous and multi-molecular layer chemical adsorption. The chemical bonds between P-O and La-O-P and electrostatic adsorption played leading roles in phosphate adsorption. The desorption solution was selected as 3 mol·L−1 NaOH and 1.5 mol·L−1 NaCl, and after five adsorption-desorption cycles, 73.03% P adsorption capacity of M-La-CS/PVA still remained. M-La-CS/PVA was a type of highly efficient phosphate adsorbent with magnetic recovery and stable performance.
-
Key words:
- lanthanum /
- hydrogel /
- adsorption /
- phosphate /
- magnetic recycling
-

-
表 1 等温线拟合参数
Table 1. Isotherm fitting parameters
温度/
℃Langmuir Freundlich qm/(mg·g−1) KL R2 n−1 KF R2 25 42.627 1 0.931 2 0.839 2 0.170 4 25.037 4 0.925 2 35 43.195 6 2.696 8 0.767 6 0.140 3 25.594 6 0.930 4 45 44.114 8 6.064 6 0.725 4 0.124 9 26.912 6 0.931 8 表 2 热力学参数
Table 2. Thermodynamic parameters
温度/K ΔG°/(kJ·mol−1) ΔH°/(kJ·mol−1) ΔS°/(kJ·(mol·K)−1) 298 −7.978 7 2.832 1 36.237 0 308 −8.302 8 318 −8.705 1 表 3 不同解吸液下M-La-CS/PVA吸附量和解吸量
Table 3. Adsorption and desorption of M-La-CS/PVA with different desorption solutions
解吸液 第5次吸附量/
初始吸附量/%第5次
解吸量/(mg·g−1 )1 mol·L−1 NaOH 26.03 11.99 3 mol·L−1 NaOH 44.76 19.41 3 mol·L−1 NaOH和1.5 mol·L−1 NaCl 73.03 25.51 -
[1] LI X Y, NAN H Y, JIANG H R, et al. Research trends on phosphorus removal from wastewater: A review and bibliometric analysis from 2000 to 2022[J]. Journal of Water Process Engineering, 2023, 55: 104201. doi: 10.1016/j.jwpe.2023.104201 [2] 单苏洁. 镧基碳酸盐吸附剂对水中磷的去除效能及机制研究[D]. 哈尔滨: 哈尔滨工业大学, 2022. [3] 谢禹, 陈仁杰, 陶正凯, 等. 生活污水强化除磷技术研究进展[J]. 应用化工, 2021, 50(3): 821-824. doi: 10.3969/j.issn.1671-3206.2021.03.053 [4] SONG W, ZHANG L, GUO B, et al. Quaternized straw supported by La(OH)3 nanoparticles for highly-selective removal of phosphate in presence of coexisting anions: Synergistic effect and mechanism[J]. Separation and Purification Technology, 2023, 324: 124500. doi: 10.1016/j.seppur.2023.124500 [5] CAO Y, WU X, LI B, et al. Ca–La layered double hydroxide (LDH) for selective and efficient removal of phosphate from wastewater[J]. Chemosphere, 2023, 325: 138378. doi: 10.1016/j.chemosphere.2023.138378 [6] 崔婉莹, 艾恒雨, 张世豪, 等. 改性吸附剂去除废水中磷的应用研究进展[J]. 化工进展, 2020, 39(10): 4210-4226. [7] LIN Z, CHEN J. Magnetic Fe3O4@MgAl-LDH@ La(OH)3 composites with a hierarchical core-shell structure for phosphate removal from wastewater and inhibition of labile sedimentary phosphorus release[J]. Chemosphere, 2021, 264: 128551. doi: 10.1016/j.chemosphere.2020.128551 [8] WANG Z Y, KOH K Y, YANG Y, et al. Design and optimization of an innovative lanthanum/chitosan bead for efficient phosphate removal and study of process performance and mechanisms[J]. Chemosphere, 2022, 306: 135468. doi: 10.1016/j.chemosphere.2022.135468 [9] YIN X J, LI X, PETROPOULOS E, et al. Phosphate removal from actual wastewater via La(OH)3-C3N4 adsorption: Performance, mechanisms and applicability[J]. Science of the Total Environment, 2022, 814: 152791. doi: 10.1016/j.scitotenv.2021.152791 [10] ZHANG B A, CHEN N, FENG C P, et al. Adsorption for phosphate by crosslinked/non-crosslinked-chitosan-Fe (III)complex sorbents: characteristic and mechanism[J]. Chemical Engineering Journal, 2018, 353: 361-372. doi: 10.1016/j.cej.2018.07.092 [11] LIU S, ZHAO S, FAN F, et al. Magnetically separable and recyclable lanthanum/iron co-modified attapulgite: A sustainable option to efficiently control phosphate loading[J]. Journal of Cleaner Production, 2022, 348: 131294. doi: 10.1016/j.jclepro.2022.131294 [12] KONG H, WANG J, ZHANG G, et al. Synthesis of three-dimensional porous lanthanum modified attapulgite chitosan hydrogel bead for phosphate removal: Performance, mechanism, cost-benefit analysis[J]. Separation and Purification Technology, 2023, 320: 124098. doi: 10.1016/j.seppur.2023.124098 [13] 曾瑞琪, 苗钟化, 李苇舟, 等. 羧甲基纤维素钠对低酯果胶凝胶流变特性及凝胶形成的影响[J]. 食品与发酵工业, 2017, 43(8): 108-114. [14] 李维浩, 刘杰, 孙治斌, 等. GO/CNC/PVA复合水凝胶制备与性能[J]. 纺织高校基础科学学报, 2022, 35(4): 45-51. [15] PAN J, LI Y, CHEN K, et al. Enhanced physical and antimicrobial properties of alginate/chitosan composite aerogels based on electrostatic interactions and noncovalent crosslinking[J]. Carbohydrate Polymers, 2021, 266: 118102. doi: 10.1016/j.carbpol.2021.118102 [16] KANG A H, SHANG K, YE D D, et al. Rejuvenated fly ash in poly (vinyl alcohol)-based composite aerogels with high fire safety and smoke suppression[J]. Chemical Engineering Journal, 2017, 327: 992-999. doi: 10.1016/j.cej.2017.06.158 [17] FENG L H, ZHANG Q, JI F Y, et al. Phosphate removal performances of layered double hydroxides (LDH) embedded polyvinyl alcohol/lanthanum alginate hydrogels[J]. Chemical Engineering Journal, 2022, 430: 132754. doi: 10.1016/j.cej.2021.132754 [18] ZHAO Y, GUO L, SHEN W, et al. Function integrated chitosan-based beads with throughout sorption sites and inherent diffusion network for efficient phosphate removal[J]. Carbohydrate Polymers, 2020, 230: 115639. doi: 10.1016/j.carbpol.2019.115639 [19] WAN J, ZHU C, HU J, et al. Zirconium-loaded magnetic interpenetrating network chitosan/poly (vinyl alcohol) hydrogels for phosphorus recovery from the aquatic environment[J]. Applied Surface Science, 2017, 423: 484-491. doi: 10.1016/j.apsusc.2017.06.201 [20] 马培根. 壳聚糖为载体的除磷吸附剂的制备及其性能的研究[D]. 北京: 北京化工大学, 2020. [21] RAJESWARI A, AMALRAJ A, PIUS A. Removal of phosphate using chitosan-polymer composites[J]. Journal of Environmental Chemical Engineering, 2015, 3(4): 2331-2341. doi: 10.1016/j.jece.2015.08.022 [22] WANG B, HU X L, ZHOU D, et al. Highly selective and sustainable clean-up of phosphate from aqueous phase by eco-friendly lanthanum cross-linked polyvinyl alcohol/alginate/palygorskite composite hydrogel beads[J]. Journal of Cleaner Production, 2021, 298: 126878. doi: 10.1016/j.jclepro.2021.126878 [23] ZHOU Y Q, WANG Y L, DONG S X, et al. Phosphate removal by a La(OH)3 loaded magnetic MAPTAC-based cationic hydrogel: Enhanced surface charge density and Donnan membrane effect[J]. Journal of Environmental Sciences, 2022, 113: 26-39. doi: 10.1016/j.jes.2021.05.041 [24] CHEN L, LI Y Z, SUN Y B, et al. La(OH)3 loaded magnetic mesoporous nanospheres with highly efficient phosphate removal properties and superior pH stability[J]. Chemical Engineering Journal, 2019, 360: 342-348. doi: 10.1016/j.cej.2018.11.234 [25] LIU S, FAN F Q, NI Z K, et al. Sustainable lanthanum-attapulgite/alginate hydrogels with enhanced mechanical strength for selective phosphate scavenging[J]. Journal of Cleaner Production, 2023, 385: 135649. doi: 10.1016/j.jclepro.2022.135649 [26] XI H, LI Q, YANG Y, et al. Highly effective removal of phosphate from complex water environment with porous Zr-bentonite alginate hydrogel beads: Facile synthesis and adsorption behavior study[J]. Applied Clay Science, 2021, 201: 105919. doi: 10.1016/j.clay.2020.105919 [27] 曾学阳. 功能化氢氧化锆交联聚乙烯醇微球的制备及除磷特性研究[D]. 广州: 广州大学, 2019. [28] WU N, NIU F, LANG W, et al. Highly efficient flame-retardant and low-smoke-toxicity poly (vinyl alcohol)/alginate/ montmorillonite composite aerogels by two-step crosslinking strategy[J]. Carbohydrate Polymers, 2019, 221: 221-230. doi: 10.1016/j.carbpol.2019.06.007 [29] LI X, LI Y, YE Z. Preparation of macroporous bead adsorbents based on poly (vinyl alcohol)/chitosan and their adsorption properties for heavy metals from aqueous solution[J]. Chemical Engineering Journal, 2011, 178: 60-68. doi: 10.1016/j.cej.2011.10.012 [30] KONG H, LI Q, ZHENG X, et al. Lanthanum modified chitosan-attapulgite composite for phosphate removal from water: Performance, mechanisms and applicability[J]. International Journal of Biological Macromolecules, 2023, 224: 984-997. doi: 10.1016/j.ijbiomac.2022.10.183 [31] 万骏. 基于功能设计的水凝胶对水中磷酸盐去除研究[D]. 武汉: 华中科技大学, 2019. [32] WANG Y, LI J, YUAN Y, et al. La(OH)3 loaded magnetic nanocomposites derived from sugarcane bagasse cellulose for phosphate adsorption: characterization, performance and mechanism[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2021, 626: 127060. doi: 10.1016/j.colsurfa.2021.127060 [33] YU Y, CHEN J P. Key factors for optimum performance in phosphate removal from contaminated water by a Fe–Mg–La tri-metal composite sorbent[J]. Journal of Colloid and Interface Science, 2015, 445: 303-311. doi: 10.1016/j.jcis.2014.12.056 [34] WANG S, WANG Y, DONG S, et al. Synchronously construction of hierarchical porous channels and cationic surface charge on lanthanum-hydrogel for rapid phosphorus removal[J]. Environmental Research, 2023, 236: 116730. doi: 10.1016/j.envres.2023.116730 [35] QING Z L, WANG L J, QIN Q R, et al. A stable rare earth-based layered double hydroxide embedded chitosan hydrogel beads for enhanced phosphate removal from aqueous solution: Performance, mechanisms and applicability[J]. Journal of Water Process Engineering, 2024, 59: 104989. doi: 10.1016/j.jwpe.2024.104989 [36] HU H, TONG Y W, HE Y L. Current insight into enhanced strategies and interaction mechanisms of hydrogel materials for phosphate removal and recovery from wastewater[J]. Science of the Total Environment, 2023: 164514. [37] WU Z, HAN Y, ZAN F X, et al. Highly efficient removal of phosphate by La-diatomite and sodium alginate composite hydrogel beads[J]. Environmental Science: Water Research & Technology, 2023, 9(4): 1205-1215. [38] CHEN Z H, LUO H Y, RONG H W. Development of polyaminated chitosan-zirconium (IV) complex bead adsorbent for highly efficient removal and recovery of phosphorus in aqueous solutions[J]. International Journal of Biological Macromolecules, 2020, 164: 1183-1193. doi: 10.1016/j.ijbiomac.2020.07.218 [39] LAN Z C, LIN Y, YANG C P. Lanthanum-iron incorporated chitosan beads for adsorption of phosphate and cadmium from aqueous solutions[J]. Chemical Engineering Journal, 2022, 448: 137519. doi: 10.1016/j.cej.2022.137519 [40] DAI M, ZHANG Y, ZHANG L, et al. Multipurpose Polysaccharide-based composite hydrogel with magnetic and thermoresponsive properties for phosphorus and enhanced copper (II) removal[J]. Composites Part A: Applied Science and Manufacturing, 2022, 157: 106916. doi: 10.1016/j.compositesa.2022.106916 [41] MENDEZ J C, HIEMSTRA T. Carbonate adsorption to ferrihydrite: competitive interaction with phosphate for use in soil systems[J]. ACS Earth and Space Chemistry, 2018, 3(1): 129-141. [42] 李小林. La(OH)3负载的磁性阳离子水凝胶对水中低浓度磷的吸附特征及其放大制备研究[D]. 北京: 北京林业大学, 2021. [43] JIA Z, ZENG W, XU H, et al. Adsorption removal and reuse of phosphate from wastewater using a novel adsorbent of lanthanum-modified platanus biochar[J]. Process Safety and Environmental Protection, 2020, 140: 221-232. doi: 10.1016/j.psep.2020.05.017 [44] 徐冉. La(OH)3改性磁性CoFe2O4纳米复合材料的制备及其吸附磷酸盐的研究[D]. 长沙: 湖南大学, 2022. [45] WANG G Y, YUE X Z, ZHANG S R, et al. La(III) loaded Fe(III) cross-linked chitosan composites for efficient removal of phosphate from wastewater: Performance and mechanisms[J]. Journal of Cleaner Production, 2022, 379: 134833. doi: 10.1016/j.jclepro.2022.134833 [46] 朱畅. 含镧互穿网络水凝胶对水中磷的吸附研究[D]. 武汉: 华中科技大学, 2019. [47] LIU B, YU Y Y, HAN Q F, et al. Fast and efficient phosphate removal on lanthanum-chitosan composite synthesized by controlling the amount of cross-linking agent[J]. International Journal of Biological Macromolecules, 2020, 157: 247-258. doi: 10.1016/j.ijbiomac.2020.04.159 [48] ZHANG S P, DING J, TIAN D Y. Incorporation of MIL-101(Fe or Al) into chitosan hydrogel adsorbent for phosphate removal: Performance and mechanism[J]. Journal of Solid State Chemistry, 2022, 306: 122709. doi: 10.1016/j.jssc.2021.122709 [49] ZHANG W, WU Y P, CHEN H L, et al. Efficient phosphate removal from water by multi-engineered PVA/SA matrix double network hydrogels: Influencing factors and removal mechanism[J]. Separation and Purification Technology, 2024: 126261. [50] WANG B, ZHANG W, LI L, et al. Novel talc encapsulated lanthanum alginate hydrogel for efficient phosphate adsorption and fixation[J]. Chemosphere, 2020, 256: 127124. doi: 10.1016/j.chemosphere.2020.127124 [51] CHEN B, LI Y, DU Q, et al. Synthesis, characterization, adsorption properties and mechanism of gravity-assisted zirconium alginate hydrogel fiber for removal of methylene blue from water[J]. Materials Today Communications, 2022, 32: 104004. doi: 10.1016/j.mtcomm.2022.104004 [52] WU X, LEI Y, ZHANG Y, et al. Alkali-treated yttrium-containing chitosan-based hydrogels for phosphate recover with highly selective in wide pH aqueous solution[J]. Surfaces and Interfaces, 2024, 45: 103851. doi: 10.1016/j.surfin.2024.103851 [53] WU Y, LI X M, YANG Q, et al. Hydrated lanthanum oxide-modified diatomite as highly efficient adsorbent for low-concentration phosphate removal from secondary effluents[J]. Journal of Environmental Management, 2019, 231: 370-379. [54] ZHANG Y Z, QIN J F, WANG X J, et al. Advanced treatment of phosphorus-containing tail water by Fe-Mg-Zr layered double hydroxide beads: Performance and mechanism[J]. Journal of Environmental Management, 2021, 296: 113203. doi: 10.1016/j.jenvman.2021.113203 [55] LIU X, ZHANG L. Removal of phosphate anions using the modified chitosan beads: Adsorption kinetic, isotherm and mechanism studies[J]. Powder Technology, 2015, 277: 112-119. doi: 10.1016/j.powtec.2015.02.055 [56] LIU Y, ZHONG D, XU Y, et al. Adsorption of phosphate in water by La/Al bimetallic-organic frameworks-chitosan composite with wide adaptable pH range[J]. Journal of Environmental Chemical Engineering, 2023, 11(5): 110309. doi: 10.1016/j.jece.2023.110309 -




 下载:
下载: