-
高氯酸盐是一种无机化学物质,其来源与分布广泛,在特定的环境下,由氯化物与大气中的臭氧发生光化学反应自然生成[1-2]。人工合成的高氯酸盐主要用于航天火箭燃料、烟花生产制造、安全气囊中的爆炸填充物和食品包装领域[3-4]。高氯酸盐在生成过程中会产生大量含有高氯酸盐的废水,随着其暴露于大气、土壤、水体等公共环境中,相较于自然来源,会更容易导致环境高氯酸盐浓度超标。
高氯酸盐同时也是一种持久性的有毒污染物质,随着其进入人体内后,会与碘离子竞争性地进入人体甲状腺器官,对甲状腺的正常功能产生干扰,影响人体的新陈代谢和生长发育,也会对胎儿的发育产生不可逆的损伤[5-7]。我国对此也开始重视,并把高氯酸盐纳入了《生活饮用水卫生标准》(GB5749—2022)[8]的管控标准中,对其限值70 ug·L−1,其含量超标问题亟待解决。
高氯酸盐易溶于水、分子量小且化学性质稳定,导致其广泛存在于水体和土壤这类环境介质中,而且难以通过净水厂的常规水处理工艺来将其去除[9]。目前已有大量报道介绍通过吸附来去除高氯酸盐,研究主要集中在新型吸附材料的探索研发和吸附剂表面改性技术[10-13]。然而吸附效果受限于高氯酸盐初始浓度、接触时间、pH值大小和水中竞争离子,并且在改性过程中也容易出现二次污染问题[14]。而压力驱动膜过滤技术,被认为是去除高氯酸盐的有效工艺[15]。近年以来膜滤技术发展迅速,在水处理中得到了广泛应用,用于饮用水深度处理的纳滤技术,目前已经实际应用于部分自来水厂[16]。通过调整膜制造工艺,可以调控纳滤膜的孔径,改变膜表面物理化学性质,从而以体积排阻、弱相互作用等方式高效去除目标污染物[17-18]。但目前关于纳滤去除水中高氯酸盐的研究较少且都以单一高氯酸盐溶液作为研究对象,而在实际水体中存在大量有机物的情况下,势必会造成膜通量下降、膜表面物理化学性质的改变和膜污染等问题影响高氯酸盐的去除率。此外也有文章研究,发现天然有机物(NOM)也能与一些水中污染离子发生相互作用从而提高其在纳滤过程中的去除率,比如Sr、As(Ⅲ)[19-21],两者在水中的相互作用关系也暂未清楚。
因此本研究采用动态错流过滤装置,考察在有机物共存时,纳滤膜对高氯酸盐的去除行为的影响效应,以及污染物之间的作用方式。并探究该体系中纳滤膜去除高氯酸盐的影响因素,最后对膜污染的表面形貌进行深入研究,为后续纳滤膜投入处理地表水中高氯酸盐的应用提供依据,提高高氯酸盐的去除效率。
-
1)实验化学药品。无水氯化钙(CaCl2)、氯化钠(NaCl)、异丙醇(CH3CHOHCH3)、海藻酸钠(SA)、谷氨酸(Glu)、组氨酸(His)、氢氧化钠(NaOH)、盐酸(HCl)、高氯酸钠(NaClO4)均为分析纯,腐殖酸(HA,≥90%),牛血清蛋白(BSA,≥96%)。溶液均采用去离子水配置。
2)实验膜材料。本研究使用的纳滤膜为商用纳滤膜对应型号为NF245和DK,NF245相应的可互换产品参考为DL。纳滤膜在到货后先裁开,放在1.5% NaHSO3中浸泡,便于长期保存。在实验使用之前,对膜上仍残留的有机物进行预处理,先用去离子水浸泡,振荡5 min;然后用25%(V/V)异丙醇溶液浸泡,振荡5 min;最后再纯水浸泡、振荡清洗3次。膜的具体参数见表1。
-
1)储备液的配制与保存方法。实验选取腐殖酸(HA)、牛血清蛋白(BSA)、海藻酸钠、谷氨酸和组氨酸,以覆盖有机物特性的广泛范围。腐殖酸储备液的制备:在25 °C下将2.0 g NaOH和1.0 g HA的粉末溶解在1 L的超纯水中,并搅拌24 h,然后用0.45 μm玻璃纤维膜过滤去除悬浮颗粒及未溶解的有机物,置于4 °C的黑暗环境中。其余有机物母液现用现配。
配置含有有机物的进水,模拟地表水进行纳滤膜截留高氯酸盐实验,使实验背景水基质条件均为1 mmol·L−1 CaCl2、5 mmol·L−1 NaCl,并使用HCl或NaOH将水溶液的pH值调节至7±0.1(除pH值实验以外)。在有机物种类实验和pH实验中,控制有机物浓度(以TOC计)为10 mg·L−1,高氯酸盐浓度为0.5 mg·L−1;在有机物浓度实验中,控制高氯酸盐浓度为0.5 mg·L−1;在高氯酸盐浓度实验中,控制有机物浓度为10 mg·L−1。
2)错流过滤实验方法。取预处理完的纳滤膜片,裁下适当尺寸并安装于错流装置上,首先在0.6 MPa压力下用去离子水预压膜片0.5 h,再用实验运行压力0.4 MPa预压膜片0.5 h,用天平实时检测膜的水通量变化情况,直至纳滤膜水通量稳定,记录下通量J0,然后进行后续实验。其次在原料液一侧换上体积为1 L的待处理液,控制运行压力为0.4 MPa,运行过滤时间为1 h,取截留液并记录通量变化情况,产水不进行回流。上一步骤完成后,去除膜片,使用一定浓度的异丙醇溶液和自来水清洗管路,然后再用超纯水多次清洗管路,为下一次实验做准备。
-
1)离子色谱仪(ICS-
1500 ,Dionex)。配置Dionex IonPacTM AS20 4-mm色谱柱,将待测水样经过0.22 μm水系针孔式微滤膜过滤后直接上机检测,根据进水和出水的高氯酸根峰面积,计算得出膜对高氯酸盐的截留性能。离子色谱条件,淋洗液为碳酸氢钠和碳酸钠;淋洗液流速,1 mL·min−1;进样量,500 μL;检测池温度,35 °C;柱温,30 °C;抑制器电流,112 mA;数据采集时间,20 min。2)总有机碳仪分析仪(TOC)。采用TOC-VCSH总有机碳分析仪,测定进料液和渗透液的有机物质量浓度,以高纯空气作为载气。电炉温度,680 °C;进样量设定,9 mL;除湿器温度,1 °C;加酸量,1.5%;载气流量,150 mL·min−1。
3)傅里叶变换红外光谱(FTIR)。将纳滤膜进行充分干燥后,使用红外光谱仪(美国Thermo Fisher Scientific Nicolet iS20),在ATR模式下进行红外光谱表征,波数范围控制在4 000~400 cm−1,扫描次数为32,分辨率为4 cm−1。
4)扫描电子显微镜(SEM)。取完全干燥后的纳滤膜样品,裁剪成1 cm×1 cm的样品,直接沾到导电胶上,随后使用扫描电子显微镜(捷克TESCAN MIRA LMS)拍摄样品形貌。设置实验条件为:9.5 mm的工作距离,扫描电镜电子加速电压为15 keV,放大倍率为1 100倍。
5)固体表面Zeta电位仪。将样品加入样品池中后,以KCl测试液作为电解质溶液,采用盐酸和氢氧化钠调节pH范围并收集数据,利用Zeta电位测定仪(Anton Paar surpass3)测量不同pH条件下膜电荷情况。
6)原子力显微镜(AFM)。在5 μm×5 μm的扫描区域进行表征,将干燥处理的膜片固定于载玻片上,然后采用原子力显微镜(德国Bruker Dimension Icon),用轻敲模式对每个样品选取3个不同的位置进行测试。
7)纳米粒度分析仪(英国Malvern Zetasizer Nano ZS90),通过仪器系统中的动态光散射(DLS)技术,测量水样中不同有机物种类的粒径大小和粒径分布。
-
用去离子水进行膜稳压条件实验,运行时间总共为1 h,测试条件为温度(25±1) °C,有效膜面积为12.5 cm2。每组过滤实验,为保证准确性,3张膜同时过滤,过滤实验过程中,记录单位时间出水质量,并取截留液进行测样。
膜通量及膜截留性能分别按下列公式(1)和(2)进行计算。
式中:J为膜通量,L·m−2·h−1;V为出水量的体积,L;A为膜的有效面积,m2;t为过滤时间,h;R为截留率,%;Cp与Ct分别为溶质出水与溶质进水的质量浓度,mg·L−1。
-
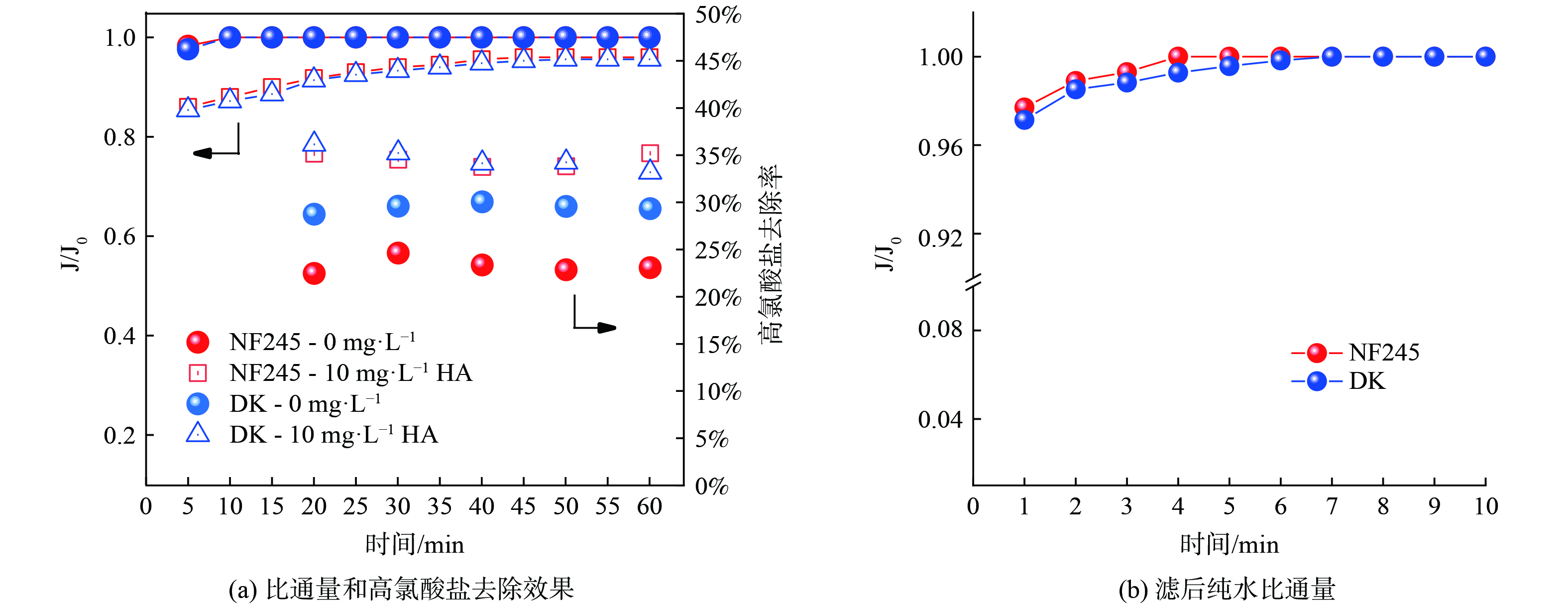
在恒定压力下(0.4 MPa),考察两种纳滤膜(即NF245和DK),待处理液中加入有机物前后,膜的比通量随过滤时间的变化情况,结果如图1(a)所示。在过滤待处理液前,记录稳态通量J0,NF245(220 L·m−2·h−1·MPa−1)稳态时的纯水通量高于DK(124 L·m−2·h−1·MPa−1),这一结果的原因是NF245的孔径更大,透水性能更好。当待处理液中只含高氯酸盐时,对于2种膜来说,膜的比通量值约等于1,即高氯酸盐几乎不影响膜通量。而又加入有机物后,在膜面上形成了有机污染,降低了膜的比通量。
图1(a)还考察2种膜,待处理液中加入有机物前后,膜对高氯酸盐的截留率随过滤时间的变化。从图1(a)所示,可以发现高氯酸盐的截留率几乎不随过滤时间而变化。在未添加有机物时,与DK(28.74%~30.05%)相比,NF245的高氯酸盐去除率较低(22.4%~24.6%),这是由于大孔径膜的trade-off效应所导致。水中天然存在的有机物可能与高氯酸盐相互作用,从而影响膜的表面电荷或改变污染物的尺寸,导致纳滤膜的去除性能的变化。在有机物腐殖酸存在的情况下,对比不添加有机物,如图1(a)显示2种纳滤膜的水通量都有所下降,而高氯酸盐去除率增加。加入腐殖酸后,NF245对高氯酸盐的去除率(33.75%~35.21%)提高到与DK(33.19%~36.15%)相似的程度,但NF245的水通量却是DK水通量的1.8倍,结果也表明在有机物共存体系下,NF245比DK在处理高氯酸盐方面具有更优越的性能。将进料液换成纯水继续过滤,考察受到有机物污染后的膜在后续纯水过滤中的情况,结果如图1(b)所示,通量在6 min后又恢复到过滤前的纯水通量,且对高氯酸盐的去除率几乎保持不变。从重复性和经济性角度,纳滤膜用于实际生产中的高氯酸盐去除具备可行性。
此外,原水中离子强度也是影响膜净水效率的关键指标[22],考虑到正常地表水Na+的大致范围(0.06~345 mg·L−1)[23],试验选取了NaCl浓度梯度1、10、100 mmol·L−1,发现对于通量和高氯酸盐去除率皆无影响,仅在NaCl浓度为100 mmol·L−1时TOC去除率略微上升(<2%),其原因为无机盐会引起盐析效应使更多的有机物被膜吸附在膜上[24]。因此,后续不进一步对原水中无机盐进行探究,维持基质水条件为1 mmol·L−1CaCl2、5 mmol·L−1 NaCl。
-
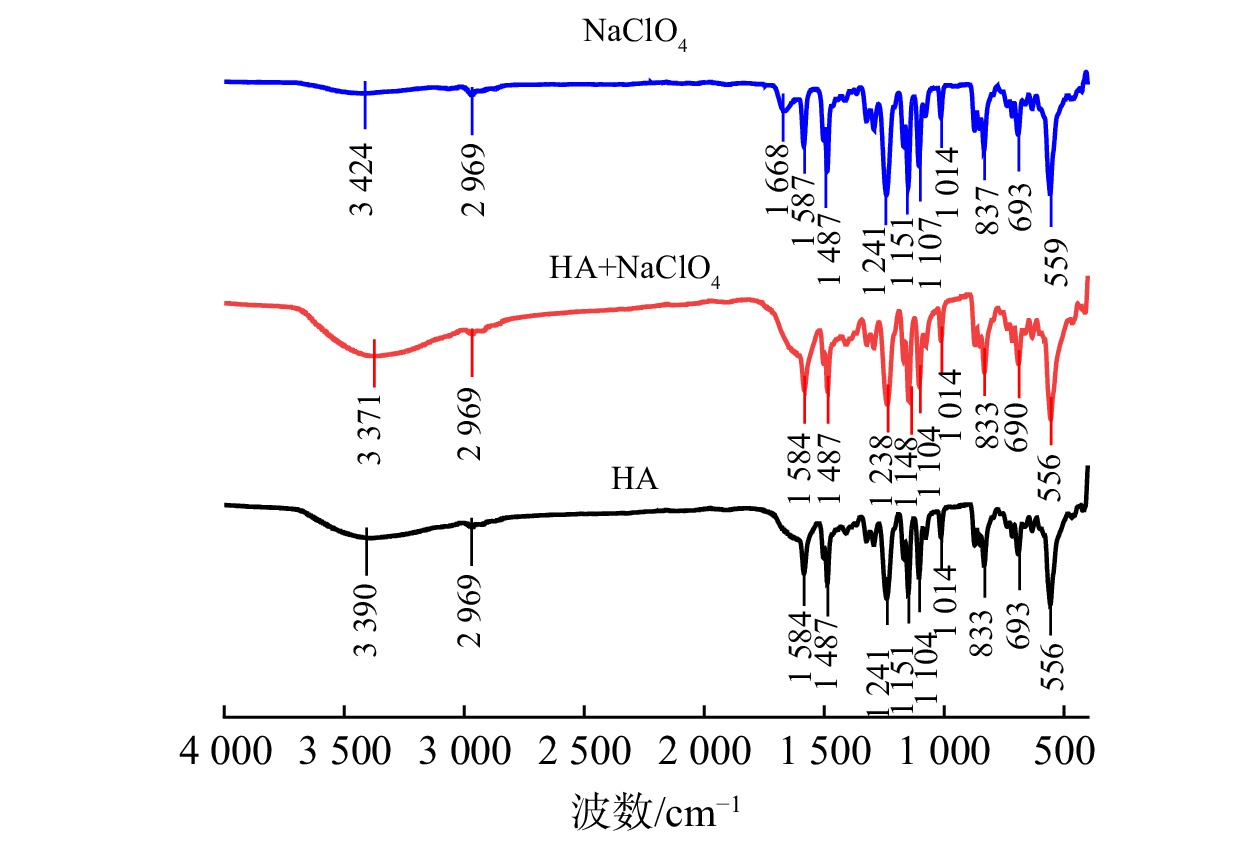
图2显示了对0.5 mg·L−1高氯酸钠溶液、40 mg·L−1腐殖酸溶液、40 mg·L−1腐殖酸和0.5 mg·L−1高氯酸钠混合溶液过滤后NF245膜表面的红外光谱图。腐殖酸(HA)的几个典型吸收峰分别为3 390 cm−1处是O-H键的伸缩振动峰,来源于腐殖酸中含有的酚类和羧酸基团;1 584 cm−1处是C=C双键的伸缩振动峰,腐殖酸中存在丰富的芳香族结构单元;1 487 cm−1处与脂肪族链中的亚甲基(-CH2-)的弯曲振动有关,腐殖酸中可能含有一定量的脂肪族碳链或环状结构;1 241、1 151、1 104和1 014 cm−1处是C-O键的伸缩振动峰,来自腐殖酸中含有的大量酚类和醇类结构单元。从图2腐殖酸和高氯酸盐(HA+NaClO4)的红外光谱图中可以看出,3 371 cm−1处是O-H键的伸缩振动峰,主要来源于腐殖酸中的羟基或酚羟基。该吸收峰相对于HA在此处的吸收峰发生了红移并且得到了增强,可能表明腐殖酸与高氯酸钠中的氧原子形成了氢键,使得O-H伸缩振动变得更为显著;1 584 cm−1处是C=C双键的伸缩振动峰,腐殖酸中含有丰富的芳香结构和羧基,因此该峰是其主要特征之一。在复合物中,该吸收峰的增强可能是由于高氯酸钠中的Cl-O伸缩与腐殖酸中的芳香环或羧基发生了相互作用,可能是通过静电相互作用或氢键,导致这些键的振动模式变化,从而增强了吸收峰的强度;并且发现在556 cm−1处吸收峰得到了增强,该处主要与ClO4−离子中的Cl-O弯曲振动模式有关,该吸收峰的增强可能表明ClO4−离子与腐殖酸的某些官能团(如羟基、羧基或酚羟基)之间存在显著的相互作用。这种相互作用可能是通过氢键或静电相互作用,使得ClO4−的弯曲振动模式变得更加显著,从而增强了该吸收峰的强度。
综上所述,腐殖酸与高氯酸钠复合物的形成过程中存在氢键和静电相互作用,这些相互作用显著影响了红外光谱中的特定吸收峰的强度,证实了腐殖酸与高氯酸根离子之间的相互作用。因此,通过使用具有高酸度(具有更多的酚羟基和羧基)的载体物质,结合更多高氯酸盐,使高氯酸盐随着载体一并被膜截留,提高高氯酸盐去除率。另一方面,从水样预处理入手,增加水中有机物与高氯酸盐的结合位点,改变溶液Zeta电位,使膜对高氯酸盐的去除率提高。
-
1)有机物种类对纳滤膜去除高氯酸盐的影响。为了确定高氯酸盐去除率的提高是否取决于有机物(OM)物质特性,下图显示过滤了5种不同有机物类型的膜性能(水通量、有机物去除率和高氯酸盐去除率)。这些有机物按其表观分子量的递增顺序排列。所选有机物的分子量从147 Da(Glu)到最高66 kDa(BSA),如图3所示。正如预期那样,如图3(b)所示,有机物的去除率随着分子量的增加而增加。DK对有机物的去除率高于NF245,这是由于膜孔径大小不同,引起的膜截留分子量差异导致的。
添加5种有机物后,图3(c)显示两种NF膜的高氯酸盐去除率变化范围为31.24%~35.77%(NF245)和32.58%~37.58%(DK)。然而高氯酸盐去除率的变化与有机物去除率的变化不成比例,这可能是由以下2个原因造成的:1)高氯酸盐与不同有机物相互作用力的大小不同,所以导致一些有机物能结合更多的高氯酸盐,进而引起有机物被截留在膜表面时高氯酸盐去除率升高;2)有机物(带有固定的净负电荷)可使膜表面带更多的负电荷,通过增强电荷的相互作用增加高氯酸盐的去除率。所以高氯酸盐潜在的去除机制包括尺寸筛分作用和静电作用。
为了验证这种ClO4−去除率的提高是否是由于膜表面电荷的改变(更负)而导致的。在pH相同时,对5种有机物过滤后,NF245的Zeta电位进行测量。在pH值为7.0±0.1时,NF245的膜表面电位(−55 mV)并没有明显的变化。
接着探究高氯酸盐的加入对有机物溶液中水力学粒径的影响,从图3(d)中可以看出,随着高氯酸盐的加入,溶液中的水力学粒径有所增加。这与前面所探究高氯酸盐与有机物形成复合物的结论相印证,高氯酸盐结合在OM表面,导致溶液中的有机物水力学粒径增大。不同的有机物受高氯酸盐影响粒径情况不同。比较而言,粒径增大幅度大小顺序为His>HA>BSA>SA>Glu。
这些结果表明,在有机物存在的情况下,ClO4− 与膜的电荷相互作用并没有得到增强,但ClO4− 的去除率得到了增强,说明在有机物种类为变量的情况下,高氯酸盐去除率的变化主要是由尺寸筛分作用主导,即与有机物发生相互作用而结合的高氯酸盐,由于空间位阻效应增强而被去除,膜表面电荷的变化不是去除ClO4− 的主要机制。
2)有机物浓度对纳滤膜去除高氯酸盐的影响。自然水体中的有机物浓度随天气和季节变化而变化,并容易因气候变化而增加。这可能会增强有机物与ClO4− 的相互作用,从而影响纳滤膜对ClO4− 的去除率。因此,将考察有机物浓度如何影响ClO4− 的去除效果。根据2.2中的讨论结果,OM与ClO4−的结合能力可以用OM其上的总酚羟基和羧酸根的数量,及OM的净电荷量来定性分析。所以除了常用的HA外,还选择了BSA作为典型有机物在NF245膜上进行过滤试验。鉴于2者特性不同,HA的芳香性比BSA高80倍,HA的净阴离子电荷量约为BSA的5倍[25],也都是常用的典型有机物,这可能会揭示不同的机制。
如图4(b)和4(d)所示,提高浓度可以使NF245对ClO4− 的去除率从28.3%~46.2%(HA)和29.4%~48.4%(BSA),减少了水通量,然后在高有机物浓度时维持稳定。为了深入分析有机物对纳滤膜去除高氯酸盐的影响,做了一组对比试验:在膜污染阶段,先单独过滤40 mg·L−1的腐殖酸30 min待膜通量稳定,然后换上只有0.5 mg·L−1高氯酸盐的原水过滤,记录后续通量变化和去除率变化情况。从图4(a)可以看出,污染层在膜表面的形成并没有使高氯酸盐的去除率得到改善,相比单独过滤ClO4-(23.3%),其在初始阶段的高氯酸盐去除率反而有些许下降(21.6%),可能的原因是大分子有机物聚集在纳滤膜表面的同时会屏蔽纳滤膜的负电荷斥力[26]。伴随着过滤时间延长,高氯酸盐的去除率上升,说明有机物对纳滤膜处高氯酸盐的影响主要是通过两者之间的相互作用,高氯酸盐被拦截去除。
分析图4(c)~(d)的结果,发现有机物去除率和高氯酸盐去除率随着有机物浓度升高的变化趋势几乎一致,都是先增加而后保持稳定,并且通过纳米粒度分析仪对10、40 mg·L−1的HA溶液进行测试,溶液的粒度分别为361、797 nm,证明了高氯酸盐的去除主要得益于膜对有机物的截留,因为溶液中的有机物与ClO4−作用导致OM-ClO4−复合物的形成,OM-ClO4−复合物比溶解的ClO4−尺寸更大,更容易被膜尺寸筛分而截留。但单看有机物去除率和高氯酸盐去除率在有机物初期增加时的变化幅度,高氯酸盐去除率的变化幅度明显更大,说明在有机物浓度为10 mg·L−1时,即OM/ ClO4−质量浓度比值为20时,OM与ClO4−数量关系中ClO4−占优,仍有过量的ClO4−未与OM反应,但随着OM/ClO4−质量浓度比值为80时,ClO4− 与OM相互作用达到饱和,两者去除率随着有机物浓度增加的变化幅度几乎一致。
另外,BSA导致较高的高氯酸盐去除率相比HA,可能是BSA与ClO4− 的相互作用更强。除了尺寸筛分机制外,ClO4−的去除还可能因OM- ClO4−复合物与膜的相互作用而增加。这意味着被截留的复合物会沉积在膜上,并改变这些膜的截留特性。
3)高氯酸盐浓度对纳滤膜去除高氯酸盐的影响。高氯酸盐在天然水体中的浓度和分布因地理位置、人为活动和水体而异。这些因素势必会影响有机物存在时纳滤对高氯酸盐的去除。为研究OM/ClO4−比率在决定ClO4− 迁移中的作用,ClO4− 浓度在0.1~20.0 mg·L−1 的范围内变化,而OM浓度为10 mg·L−1。水通量、有机物去除率和ClO4− 去除率随高氯酸盐的浓度变化关系如图5所示。
伴随着增加高氯酸盐浓度到20 mg·L−1,发现对于有机物共存时的水通量影响不大,但却导致了有机物去除率的小幅上升和更低的高氯酸盐去除率。有机物去除率的上升的原因,正如图3(d)所示,添加了高氯酸盐的溶液,其平均水力学粒径增大,导致膜对有机物的空间位阻效应更强。高氯酸盐去除率降低的原因,这归结于膜表面的ClO4−浓度与初始ClO4−浓度呈线性增长,更高的ClO4−初始浓度加剧了ClO4−在纳滤膜中的扩散。由于在高浓度高氯酸盐(20 mg·L−1)下,即OM/ ClO4−的比率为0.5,BSA对ClO4−的去除率要高于HA对ClO4−的去除率,结合上一节的分析得知,此时ClO4−处于过量状态,HA- ClO4−和BSA-ClO4−复合物的结合程度不是影响ClO4−去除率的决定因素。现从尺寸筛分和电荷排斥角度来进行分析。
现比较使用不同的有机物(BSA和HA)过滤后的纯水渗透性。由图5(a)所示,NF245的纯水渗透性在BSA-ClO4−过滤后比HA-ClO4−过滤后要下降得多一些,这表明BSA-ClO4−比HA-ClO4−复合物更容易造成膜堵塞。所以BSA引起的膜上尺寸筛分效果要强于HA所引起的,以至于导致更高的高氯酸盐去除率。
测量过滤OM- ClO4−复合物后膜的表面电位,以评估表面膜荷电量对高氯酸盐去除的影响。结果显示在pH为7时,沉积了HA-ClO4−的NF245的Zeta电位(−55.7 mV)要低于沉积了BSA-ClO4− 的Zeta电位(−51.6 mV)。HA-ClO4−复合物沉积使膜表面带更多负电荷,有利于膜对ClO4− 的去除。因此本应该是同HA过滤时对高氯酸盐的去除率高于同BSA过滤时,但实际情况却是相反,说明在不同种有机物(HA和BSA)污染后,尺寸筛分对高氯酸盐去除率的贡献因素要高于电荷排斥作用。接下来也将通过探究pH的变化,来进一步了解电荷排斥对于高氯酸盐去除率的影响。
4)pH对纳滤膜去除高氯酸盐的影响。给水pH值的变化会影响膜表面电荷、有机物结构、OM-ClO4−相互作用,这势必会影响纳滤膜对高氯酸盐的去除效果。纳滤膜的性能与pH的函数关系如图6所示。
pH过高的情况下导致了较高的高氯酸盐去除率,这可能是由于膜表面电负性增强,导致ClO4−与膜的电荷排斥作用变大。而pH为2.5时也有不错的高氯酸盐去除率,结合OM的去除率变化图,pH在2.5时OM的去除率最高,可能是由于HA在pH酸性条件下其尺寸会随着pH的降低而变大[27],导致膜对HA的尺寸筛分作用增大,从而使得更多与HA结合的高氯酸盐被去除。最低的ClO4−去除率在pH为4~6之间,可能是由于更弱的电荷排斥作用加之HA尺寸变小。
为总结研究成果,提出不同pH值的HA对ClO4− 的潜在去除机制。与其他因素相比(如有机物的种类),pH扮演一个更重要的角色对于高氯酸盐的去除。在酸性条件下,HA尺寸增大,HA-ClO4−更易被膜的尺寸筛分作用给去除。碱性pH时,膜上带更多负电荷,导致ClO4−被膜表面电荷排斥。在pH为4~6时,相对于高pH,膜电荷减少且HA几乎尺寸一致,导致ClO4−的去除率最低。不同的OM类型对ClO4−去除也有不同的影响,不同的OM类型主要导致以下3种主要机制来影响ClO4−的去除:1)能与OM形成OM-ClO4−复合物的数量;2)OM-ClO4−的沉积导致膜电荷的改变;3)OM-ClO4−复合物导致膜的孔径减小,改变了膜的尺寸筛分作用。因此,多种机制的协同作用促进了有机物在纳滤过程中对于高氯酸盐的去除。
-
1)SEM的结垢层分析。为了更直观地描述膜的表面污染状态,对单一高氯酸盐污染和添加5种不同有机物污染后的膜进行SEM成像表征。如图7所示。
图7展示了分别过滤0.5 mg·L−1 NaClO4、0.5 mg·L−1 NaClO4+10 mg·L−1 HA、0.5 mg·L−1 NaClO4+10 mg·L−1 BSA、0.5 mg·L−1 NaClO4+10 mg·L−1 SA、0.5 mg·L−1NaClO4+10 mg·L−1 His、0.5 mg·L−1 NaClO4+10 mg·L−1 Glu六种不同给水基质后纳滤膜的扫描电镜图。本研究所使用的纳滤膜在仅仅过滤高氯酸盐给水后可以发现膜表面有些许聚合物颗粒,如图7(a)可见,这可能是由于膜表面吸附高氯酸盐颗粒所致。对于典型有机物污染,观察图7(b)、(d),HA和SA分别污染的膜表面有明显结垢层,HA污染的膜表面有较大块的颗粒及聚合物,可能是原水基质中的钙离子与腐殖酸发生络合反应形成了HA-Ca2+-ClO4−更大的大分子聚合物。SA污染后的膜原本表面较平整的结构被相互交联的大分子结构所覆盖,表面也负载了更多的聚合物颗粒。至于BSA、His和Glu这3者分别污染的膜表面,如图7(c)~(f)所示,发现膜上的褶皱结构仍然存在,没有发现明显的污染层。对于BSA污染的膜表面,结合发现负载膜上的聚合物明显减少,说明BSA在膜上的吸附量很少,而BSA污染后的膜能取得不错的高氯酸盐截留率,可能是因为BSA与高氯酸盐结合在一起后,由于BSA和高氯酸盐的疏水作用力,使得BSA和高氯酸盐被膜排斥,从而提高了纳滤对高氯酸盐的去除效果。对于两种小分子氨基酸污染的膜表面,可以发现His污染过后的膜表面负载了大量的小颗粒,远超出单一高氯酸盐污染膜上负载的量,可能是由于His与高氯酸盐有更强的相互作用,也解释2.3.1中,His和Glu同为小分子有机物,His污染后的膜却能取得更高的高氯酸盐截留率。
2)AFM形貌分析。采用AFM测量了不同进料液过滤后的膜表面粗糙度。利用AFM分析软件计算得出了粗糙度参数。图8分别为0.5 mg·L−1 NaClO4、0.5 mg·L−1 NaClO4+10 mg·L−1 HA、0.5 mg·L−1 NaClO4+10 mg·L−1 BSA、0.5 mg·L−1 NaClO4+10 mg·L−1 SA、0.5 mg·L−1 NaClO4+10 mg·L−1 His、0.5 mg·L−1NaClO4+10 mg·L−1 Glu污染膜的AFM显微图。
膜表面污染层会导致膜表面形态与结构发生改变。只过滤了高氯酸盐的纳滤膜表面最光滑,平均粗糙度为186 nm。结果表明这5种有机物可以增加过滤过程中膜表面的粗糙度,而粗糙度的增加可以提高分离能力[28]。观察图8(a)、(c)可见,过滤了HA与BSA的膜表面小凸起和褶皱相应增多,粗糙度也增大,均方根粗糙度Rq增长到251、221 nm。图8(d)代表SA污染的膜表面,污染膜上的结垢层较均匀,发现几乎很少小峰,高峰分布分散且形态上由竹笋状转为柱状,由于高低峰差距大导致Rq值为263 nm。图8(e)~(f)代表His和Glu污染的膜表面,发现与图8(a)膜表面起伏一致,也说明污染层的形成不明显,与SEM表征结构相符,对于His污染的膜表面与单一高氯酸盐污染的膜表面相比,膜上呈现更密集竹笋状结构,且高峰的数量也更多更集中,符合SEM图中其上污染物分布密集的特点。而Glu污染的膜表面较于图8(a)只是小峰相应的增加,故图8(e)、(f)膜对应的Rq值为261、224 nm。
-
1)水基质中存在有机物能显著提高纳滤膜对高氯酸盐的截留能力,并且对膜通量影响不大。加入10 mg·L−1 HA后,NF245和DK对高氯酸盐的去除率增加幅度为48.1%和17.3%,对高氯酸盐的去除率几乎相当,分别为34.5%和34.6%,但NF245的水通量却是DK的1.8倍。并且对受到有机污染后的膜用纯水进行过滤,几分钟后通量又恢复到了未受到有机污染的水平。通过红外光谱分析膜表面污染物化学结构,证明了腐殖酸与高氯酸盐形成了复合结构,结合的关键为氢键的形成和静电作用力。
2)有机物种类的不同和有机物浓度变化可以改变纳滤膜对高氯酸盐的截留表现,主要是由于溶质之间相互作用力发生了变化,并且对于HA和BSA的OM/ ClO4−质量浓度比值在80时,高氯酸盐与有机物作用达到饱和,继续增大有机物浓度不会导致高氯酸盐去除率的增加。在与有机物共存的体系中,高氯酸盐浓度的升高会导致截留率的下降,其原因可能是增强了游离的高氯酸盐透过纳滤膜的扩散作用。在低pH值(pH2.5)时,HA-ClO4−复合物尺寸增加,高氯酸盐去除率提高;在高pH值(pH 11)时,道南效应提高了高氯酸盐的去除率。
3)共存体系下去除高氯酸盐的主要机理,即两者通过氢键和静电作用力形成复合物,有机物被膜截留的同时,伴随着与有机物相结合的高氯酸盐也被截留,从而提高了高氯酸盐的去除率。结合扫描电镜图发现,同为小分子的His和Glu,两者的有机物去除率几乎相同,但His能结合更多的高氯酸盐,从而取得更高的高氯酸盐去除率。此外,BSA通过相互作用与高氯酸盐结合后,溶质与膜由于疏水作用,BSA和高氯酸盐一同被膜排斥,膜上观察不到明显污染层。
有机物共存条件下纳滤对高氯酸盐去除效能
Removal efficiency of perchlorate by nanofiltration under the coexistence of organic matter
-
摘要: 近年来高氯酸盐被纳入最新的《生活饮用水卫生标准》,并因其持久性、化学稳定性强、生物毒性严重危害环境安全和人体健康。但由于其易溶于水、分子量小且化学性质稳定,导致净水厂常规的处理工艺无法对其有效去除。纳滤膜常用于低分子量物质的去除,对去除高氯酸盐具有显著的优势和潜力。考虑水体的复杂性,研究有机物(OM)与高氯酸盐共存体系下纳滤膜的性能表现,并进行形貌形态表征和污染物化学结构分析,系统分析有机物对纳滤膜去除高氯酸盐的影响因素和机理。结果表明,水基质中存在腐殖酸(HA)能显著提高纳滤膜对高氯酸盐的去除效果,对于NF245和DK纳滤膜,在操作压力0.4 MPa,进水高氯酸盐浓度为0.5 mg·L−1的条件下,体系中存在10 mg·L−1的HA可使高氯酸盐的截留率从23.3%和29.5%提升至34.5%和34.6%。对膜污染物进行红外光谱分析,表明了腐殖酸与高氯酸盐的结合方式主要为氢键和静电相互作用。研究发现了OM的种类和浓度、高氯酸盐的浓度和pH 2.5~11主要通过尺寸筛分作用、电荷排斥作用及溶质之间的相互作用来影响纳滤对高氯酸盐的去除效果。结果表明对于NF245而言,添加不同的有机物(5种)和有机物的浓度的增加(1~80 mg·L−1)将高氯酸盐的去除率提高了7.9%~12.5%和5.2%~23%。此外,对于HA和牛血清蛋白(BSA),当有机物与高氯酸盐的质量浓度比值为80时,两者相互作用达到饱和;高氯酸盐初始浓度(0.1~20 mg·L−1)的增加会降低高氯酸盐的去除率(39.3%~31.1%),其可能的原因是游离的高氯酸盐透过纳滤膜的扩散作用增强;当水基质中存在HA,pH 4~6时,高氯酸盐去除率最小,而过低和过高的pH值会导致高氯酸盐去除率升高,主要通过影响有机物的去除和改变膜表面的Zeta电位。最后结合膜表征,推测截留机理及解释规律,发现有机物与高氯酸盐一同被膜截留在其表面,而BSA依靠疏水作用被膜排斥,未能在膜表面形成明显的污染层;同为小分子的组氨酸和谷氨酸,由于组氨酸与高氯酸盐之间相互作用更强,导致了更高的高氯酸盐去除率。Abstract: In recent years, perchlorate has been included in the latest' Sanitary Standard for Drinking Water', and seriously endangers environmental safety and human health due to its persistence, strong chemical stability and biological toxicity. However, due to its easy solubility in water, small molecular weight and stable chemical properties, it cannot be effectively removed by conventional treatment processes in water purification plants. Nanofiltration membrane is commonly used for the removal of low molecular weight substances, which has significant advantages and potential for the removal of perchlorate. In this study, considering the complexity of water body, the performance of nanofiltration membrane under the coexistence system of organic matter (OM) and perchlorate was studied, and the morphological characterization and chemical structure analysis of pollutants were carried out. The influencing factors and mechanism of organic matter on perchlorate removal by nanofiltration membrane were systematically analyzed. The results showed that the presence of humic acid (HA) in the water matrix could significantly improve the removal efficiency of perchlorate by nanofiltration membrane. For NF245 and DK nanofiltration membranes, when the operating pressure of 0.4 MPa and the influent perchlorate concentration of 0.5 mg·L−1, the presence of 10 mg·L−1 HA in the system could increase the rejection rate of perchlorate from 23.3% and 29.5% to 34.5% and 34.6%. The infrared spectrum analysis of membrane pollutants showed that the binding mode of humic acid and perchlorate was mainly hydrogen bond and electrostatic interaction. It was found that the type and concentration of OM, the concentration of perchlorate and pH 2.5~11 mainly affected the removal efficiency of perchlorate by nanofiltration through size and/or charge exclusions as well as solute-solute interactions. The results showed that for NF245, the addition of different organic matter (5 types) and the increase of organic matter concentration (1~80 mg·L−1) increased the removal rate of perchlorate by 7.9%~12.5% and 5.2%~23%. In addition, for HA and bovine serum albumin (BSA), when the mass concentration ratio of organic matter to perchlorate was 80, the interaction between the two reached saturation. The increase of initial perchlorate concentration (0.1~20 mg·L−1) would reduce the removal rate of perchlorate (39.3%~31.1%). The possible reason was that the diffusion of free perchlorate through nanofiltration membrane was enhanced. When HA was present in the water matrix and the pH was 4~6, the perchlorate removal rate was the smallest, while too low and too high pH values would lead to an increase in perchlorate removal rate, mainly by affecting the removal of organic matter and changing the Zeta potential of the membrane surface. Finally, combined with the membrane characterization, the rejection mechanism and explanation rule were speculated. It was found that the organic matter was retained on the surface of the membrane together with perchlorate, while BSA was rejected by the membrane by hydrophobic interaction, and no obvious fouling layer was formed on the membrane surface. Histidine and glutamic acid, both small molecules, have higher perchlorate removal rate due to the stronger interaction between histidine and perchlorate.
-
Key words:
- perchlorate /
- nanofiltration /
- natural organic matter /
- solute-solute interaction
-

-
表 1 纳滤膜的基本性质
Table 1. The basic properties of nanofiltration membrane
名称 材料 截留分子量/Da 截留率 水通量a/LMH NF245 聚酰胺 200~300 ≥99.0% 55 DK 聚酰胺 150~250 ≥99.0% 38 注:a水通量和截留率是基于测试条件为2 000 mg·L−1 MgSO4、0.76 MPa。 -
[1] CHANG W H, CHEN P H, HERIANTO S, et al. Aggregating exposures and toxicity equivalence approach into an integrated probabilistic dietary risk assessment for perchlorate, nitrate, and thiocyanate: Results from the national food monitoring study and national food consumption database[J]. Environmental Research, 2022, 211: 13. [2] TRUMPOLT W C, CRAIN M, CULLISION D G, et al. Perchlorate: Sources, uses, and occurrences in the environment[J]. Remediation Journal, 2005, 16(1): 65-89. doi: 10.1002/rem.20071 [3] COUNCIL R N, STUDIES L A E O D, TOXICOLOGY A S E O B, et al. Health implications of perchlorate ingestion[M]. The National Academies Press, 2005: 276. [4] V M M, LEONARDO T, G T N. Perchlorate and diet: Human exposures, risks, and mitigation strategies[J]. Current Environmental Health Reports, 2016, 3(2): 107-17. doi: 10.1007/s40572-016-0090-3 [5] WANG H R, JIANG Y S, SONG J Y, et al. The risk of perchlorate and iodine on the incidence of thyroid tumors and nodular goiter: A case-control study in southeastern China[J]. Environmental Health, 2022, 21(1): 4. doi: 10.1186/s12940-021-00818-8 [6] 吴春笃, 李顺, 许小红, 等. 高氯酸盐的环境毒理学效应及其机制的研究进展[J]. 环境与健康杂志, 2013, 30(1): 85-89. [7] MARTINE B, BARBARA D, PHILIPPE G, et al. Response to the letter by middlebeek and veuger[J]. The Journal of Clinical Endocrinology And Metabolism, 2015, 100(6): L54-55. doi: 10.1210/jc.2015-2221 [8] 中国国家市场监督管理总局, 中国国家标准化管理委员会. 生活饮用水卫生标准: GB5749-2022[S]. 北京: 中国标准出版社, 2022. [9] 于佳, 唐玄乐, 宋建平, 等. 高氯酸盐的急性毒性和遗传毒性研究[J]. 毒理学杂志, 2007(4): 267-269. doi: 10.3969/j.issn.1002-3127.2007.04.008 [10] KRISHNAN G R, PRABHAHARAN K, GEORGE B K. Watermelon rind derived carbon monolith as potential regenerable adsorbent for perchlorate[J]. Bioresource Technology Reports, 2023, 21: 101361. doi: 10.1016/j.biteb.2023.101361 [11] BAIDAS S, DEYAIN A K, MENG X, et al. Competitive removal of perchlorate Ions by quaternary amine modified reed in the presence of nitrate and phosphate[J]. Adsorption Science & Technology, 2023, 2023: 3087629. [12] MENG Z L, FAN J X, CUI X Y, et al. Removal of perchlorate from aqueous solution using quaternary ammonium modified magnetic Mg/Al-layered double hydroxide[J]. Colloids And Surfaces A: Physicochemical And Engineering Aspects, 2022, 647: 129111. doi: 10.1016/j.colsurfa.2022.129111 [13] KRISHNAN G R, PRABHAHARAN K, GEORGE B K. N-doped activated carbon with hierarchical pores for the efficient removal of perchlorate from water[J]. Microporous And Mesoporous Materials, 2021, 315: 110892. doi: 10.1016/j.micromeso.2021.110892 [14] 滕俊, 张云英, 王艳, 等. 人群暴露高氯酸盐污染及其在饮用水中去除技术: 综述[J]. 环境化学, 2024(4): 1-13. [15] YOON J, AMY G, CHUNG J, et al. Removal of toxic ions (chromate, arsenate, and perchlorate) using reverse osmosis, nanofiltration, and ultrafiltration membranes[J]. Chemosphere, 2009, 77(2): 228-235. doi: 10.1016/j.chemosphere.2009.07.028 [16] 贺鑫, 王少华, 施立宪, 等. 纳滤饮用水厂的膜工艺处理效能与系统运行[J]. 同济大学学报(自然科学版), 2023, 51(10): 1509-1517. doi: 10.11908/j.issn.0253-374x.23260 [17] MOHAMMAD A W, TEOW Y H, ANG W L, et al. Nanofiltration membranes review: Recent advances and future prospects[J]. Desalination, 2015, 356: 226-254. doi: 10.1016/j.desal.2014.10.043 [18] OATLEY D L, LLENAS L, PÉREZ R, et al. Review of the dielectric properties of nanofiltration membranes and verification of the single oriented layer approximation[J]. Advances in Colloid And Interface Science, 2012, 173: 1-11. doi: 10.1016/j.cis.2012.02.001 [19] CAI H Y, AKHIL G, QILIN D, et al. Removal of strontium by nanofiltration: Role of complexation and speciation of strontium with organic matter[J]. Water Research, 2024, 253: 121241. doi: 10.1016/j.watres.2024.121241 [20] BOUSSOUGA Y A, MOHANKUMAR M B, GOPALAKRISHNAN A, et al. Removal of arsenic(III) via nanofiltration: contribution of organic matter interactions[J]. Water Research, 2021, 201: 117315. doi: 10.1016/j.watres.2021.117315 [21] 王子阳. 天然有机质对纳米银颗粒在混凝、吸附处理工艺中去除的影响[D]. 济南: 山东大学, 2019. [22] MIAO R, WANG L, ZHU M, et al. Effect of hydration forces on protein fouling of ultrafiltration membranes: The role of protein charge, hydrated ion species, and membrane hydrophilicity[J]. Environmental Science & Technology, 2017, 51(1): 167-174. [23] MEYBECK M, HELMER R. The quality of rivers: From pristine stage to global pollution[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 1989, 75(4): 283-309. doi: 10.1016/0031-0182(89)90191-0 [24] FREGER V, ARNOT T C, HOWELL J A. Separation of concentrated organic/inorganic salt mixtures by nano filtration[J]. Journal of Membrane Science, 2000, 178(1-2): 185-193. doi: 10.1016/S0376-7388(00)00516-0 [25] CAI Y H, GOPALAKRISHNAN A, DESHMUKH K P, et al. Renewable energy powered membrane technology: Implications of adhesive interaction between membrane and organic matter on spontaneous osmotic backwash cleaning[J]. Water Research, 2022, 221: 118752. doi: 10.1016/j.watres.2022.118752 [26] OH J I, LEE S H, YAMAMOTO K. Relationship between molar volume and rejection of arsenic species in groundwater by low-pressure nano fltration process[J]. Journal of Membrane Science, 2004, 234(1-2): 167-175. doi: 10.1016/j.memsci.2004.01.023 [27] BRIGANTE M, ZANINI G, AVENA M. Effect of pH, anions and cations on the dissolution kinetics of humic acid particles[J]. Colloids And Surfaces A: Physicochemical and Engineering Aspects, 2009, 347(1): 180-186. [28] NGUYEN T V, PENDERGAST M M, PHONG M T, et al. Relating fouling behavior and cake layer formation of alginic acid to the physiochemical properties of thin film composite and nanocomposite seawater RO membranes[J]. Desalination, 2014, 338: 1-9. doi: 10.1016/j.desal.2014.01.013 -



 下载:
下载: