-
大气颗粒物(particulate matter,PM)污染是全球关注的环境问题之一,尤其是细颗粒如PM2.5(空气动力学当量直径≤2.5 μm)污染由于其负健康效应而成为研究热点[1 − 3]. PM2.5不仅对大气环境产生影响,而且可通过呼吸道、消化道、皮肤等途径进入人体,通过血液循环到达各器官,穿越机体的生理屏障,导致机体多器官的损伤以及死亡[4]. 然而,PM相关健康影响的作用机制尚未完全清晰了解. 流行病学和毒理学研究表明:PM对于健康的影响与活性氧化物和氧化应激有关[5 − 6],这一观点目前被认为是PM暴露对健康造成许多不良影响的核心驱动机制[7]. 即ROS在人体内的过度积累会引起机体氧化应激,从而引发各种生物学效应,例如炎症、DNA损伤、RNA或蛋白质的改变、细胞损伤及死亡等[8]. 研究发现PM2.5的独特代谢物与急性炎症、核酸损伤和修复以及能量扰动密切相关,这些过程的干扰会导致炎症因子和ROS的产生,最终导致氧化应激和全身炎症增强[9].
氧化潜势(oxidative potential,OP)是描述颗粒物诱导生物体产生ROS的能力. 活性氧化物(reactive oxygen species,ROS)是指存在于机体内或PM上含氧且性质活泼的物质总称,是由超氧化物和不完全还原反应产生的一种短寿命亲电化学物质,由于具有化学反应活性,对细胞和组织具有一定的毒性作用[10]. ROS主要包括O2−·、O3、H2O2、·OH等[4]. 颗粒物中的氧化还原性物质经过反应后会产生一定的ROS,当ROS过量生成时可能会导致其在细胞内的降解失衡,从而使细胞内ROS浓度水平升高,一旦超过细胞耐受性,就会导致机体的氧化应激或者全身炎症. 另外,还有研究进一步证明了导致机体氧化应激的是PM的成分,而非质量浓度,这也表明OP是比质量浓度更适合描述大气PM造成的健康影响的指标[11 − 13].
目前,OP的研究主要集中在部分地区PM中OP值的分析测定, OP与PM化学组成及粒径的关系、季节分布特征、OP来源解析以及健康效应等. 评估大气PM中OP的方法有细胞法和非细胞法两类,其中非细胞法快速、简便、低廉、应用广泛[14]. 随着OP非细胞测定技术的发展,有效促进了大气OP的相关研究. 常见的非细胞测定法包括二硫苏糖醇(dithiothreitol, DTT)法、抗坏血酸(ascorbic acid, AA)法、谷胱甘肽(glutathione, GSH)法以及电子顺磁/自旋(electron paramagnetic/spin resonance, EPR/ESR)法、二氯二氢荧光素(dichlorodihydrofluorescein, DCFH)法等等. 其中DTT和AA法比较直观且重复性好,被国内外研究者们广泛采用. 但DTT对光敏感,必须在黑暗的条件下进行,AA法对粗粒径PM中的过渡金属较为敏感,但OPAA无法体现季节变化. OPGSH与健康效应的相关性最强,但不能很好地反映交通源贡献的OP;ESR法可以直接定量测定·OH从而获得OP值,但仅用·OH代表整个ROS是不全面的,没有包含·OH以外的其它ROS物质. 说明不同方法所表征的OP侧重点、角度和机理存在差异. 然而,分析测定PM的OP是准确评估大气PM所造成的氧化应激及健康风险的基础,这方面的系统归纳总结未见报道. 本文对各种OP非细胞分析方法机理及进展进行归纳总结,从而为开展大气PM中OP产生的健康效应进行准确评估提供基础参考.
-
OP的测定需要先通过滤膜捕集法采集大气PM(包括PM10、PM2.5等),将滤膜夹在大气颗粒物采样器上进行采样. PM样品的采样滤膜主要包括:聚四氟乙烯滤膜、过氯乙烯滤膜、石英纤维滤膜、玻璃纤维滤膜等,没有一种滤膜可以同时适宜所有的化学分析,根据具体测定组分和方法要求而选择适宜滤膜,目前应用最普遍的是石英纤维滤膜. 采样前将石英滤膜在马弗炉内450 ℃左右焙烧4—6 h,以除去有机杂质和干扰物,室温后放置干燥器中备用. 采样之后要低于−20 ℃黑暗密封保存样品,为了避免挥发性物质损失[15]. 近年来采样仪器也逐渐向着半自动、自动化发展. 如Berg等[16]评估了一种半自动分析方法,与手动方法具有相当的准确性和灵敏度且还可节省83%的时间. 而Quinn等[17]研究了一种便携式的自动微环境气溶胶采样器,用来评估家庭、学校等地方的暴露情况. 不断发展的自动化采样以及测定方法使实验操作更加便捷、结果更加精确.
滤膜捕集后,在仪器测定之前需要前处理样品. OP的前处理方法有振荡、磁力搅拌、超声、涡旋法等. 其中超声提取法应用较多,操作流程如下:陶瓷剪刀剪碎样品滤膜,放入离心管中加入一定溶剂,低于室温进行超声提取. 静置后将提取液通过0.22 µm的PTFE滤膜,制备出PM2.5提取液. 萃取中受到诸多因素影响,如溶剂[18]以及处理条件等均会造成OP值波动. 张曼曼等[19]研究发现超声时DTT衰减波动较大,而采用振荡的方式提取,可减少误差,对OP结果有一定的改善. Frezzini等[20]与之观点类似,认为超声会诱导自由基的形成从而产生较大误差,通过使用旋转搅拌器提取样品的方式较超声好,且具有一定的再现性和重复性.
-
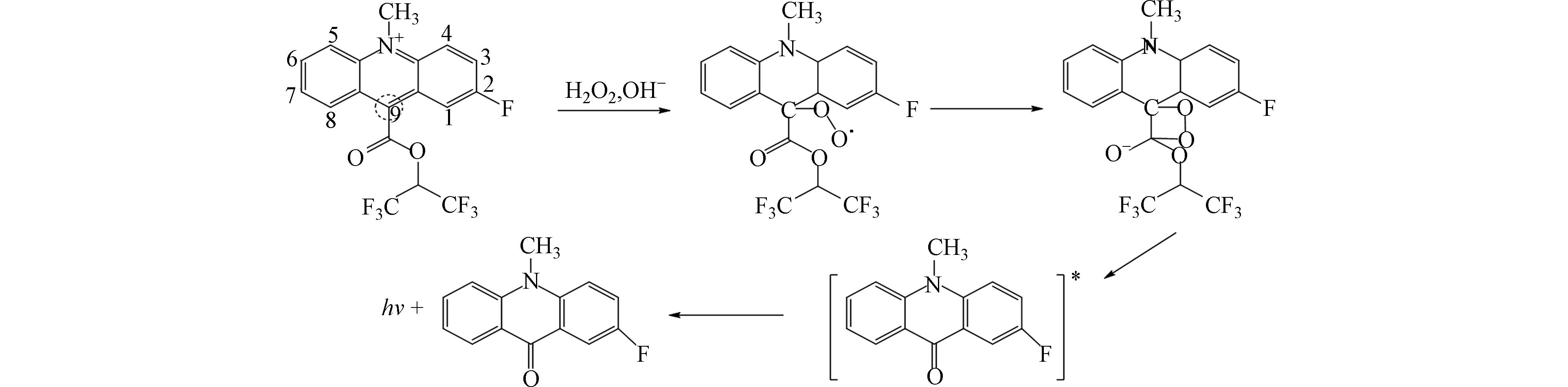
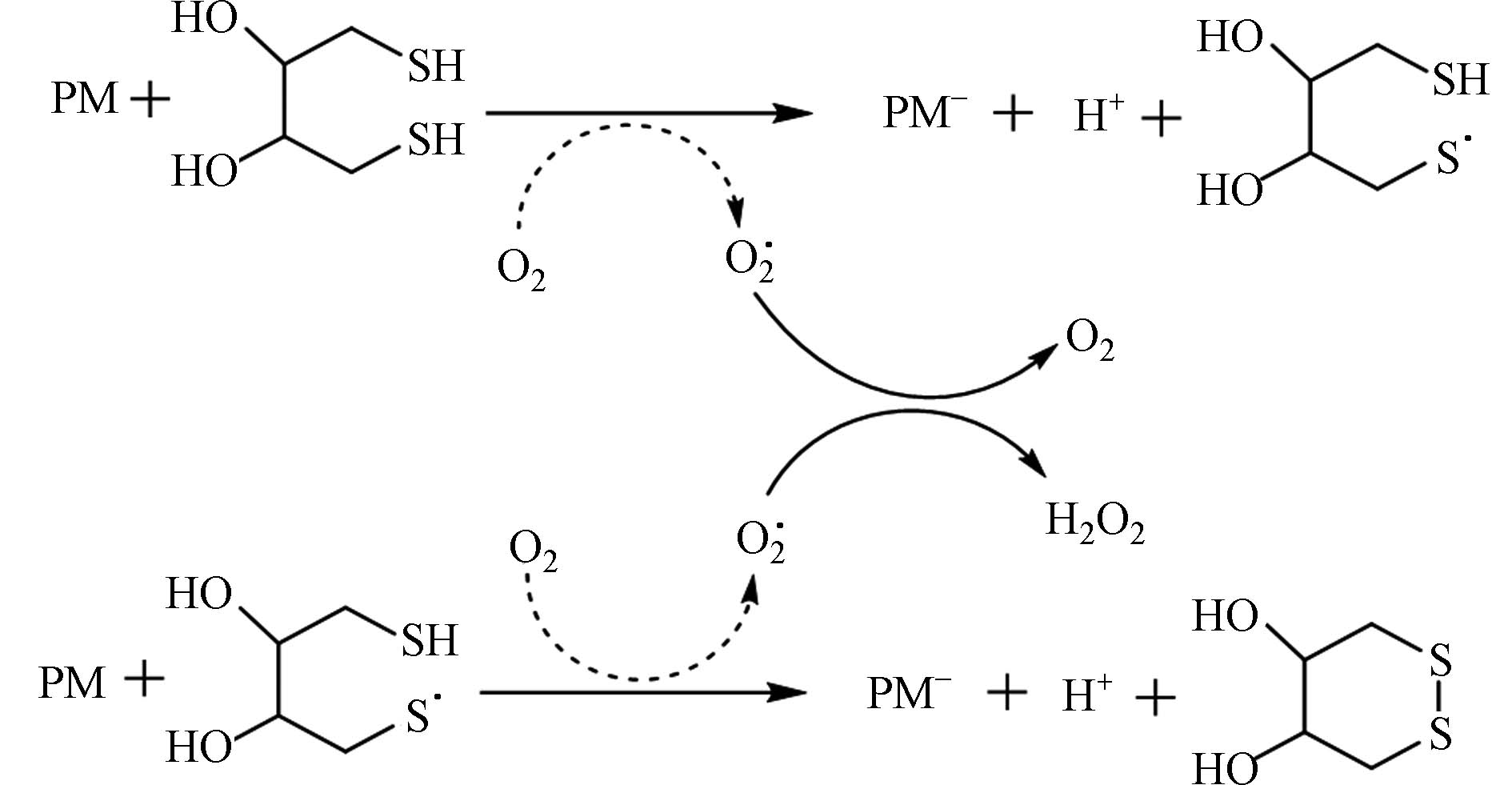
DTT法是一种有效的体外测定大气PM中OP的目前应用较多方法. DTT是一种强还原剂,因而可替代细胞内的硫醇抗氧化剂. 原理如图1[21]所示,PM中具有氧化性的化合物催化DTT使其向氧气转移电子生成O2·,O2·进一步与H2O生成H2O2和O2,DTT被氧化成硫化物. 此过程用来模拟PM2.5在人体内氧化还原产生ROS的过程,通过DTT的消耗速率来表征大气颗粒物中OP水平. OPDTT有两种形式:第一种为DTTm,表示为单位质量PM的DTT消耗速率,衡量PM本身的OP,计算见式①. 第二种为DTTv ,表示单位体积PM对DTT的消耗速率,该值与人体呼吸暴露有关,计算见式②[22].
其中,rs:样品DTT消耗速率;rb:空白膜DTT消耗速率;M:总采样PM质量;As:滤膜提取面积;At:滤膜总面积;Vr:参与反应样品体积;Ve:样品总提取体积.
诸多学者开展了DTT法测定大气OP的相关研究. Kumagai等[23]于2002年首次采用DTT法测定柴油机废气颗粒物诱导ROS的产生,发现柴油机废气颗粒包含醌类等物质,它可促进ROS的生成,从而产生氧化应激. 2005年,Cho等[24]研究了洛杉矶盆地基于DTT法的PM氧化还原活性,研究表明随着PM粒径的增大其OP值会减小. 2012年,Charrier等[25]测量了金属、醌类以及多环芳烃(PAHs)对DTT的损失率,以确定哪些物种会导致大气PM的DTT损失,结果表明:约80%的DTT损失是来自过渡金属(尤其是Cu和Mn),而醌类约占20%. 2015年,Fang等[26]设计研发了一套基于DTT法测定OP的半自动化系统,与手动结果相比具有良好的一致性(r2=0.92). 目前评估PM的OP时部分研究中仍采用此方法.
-
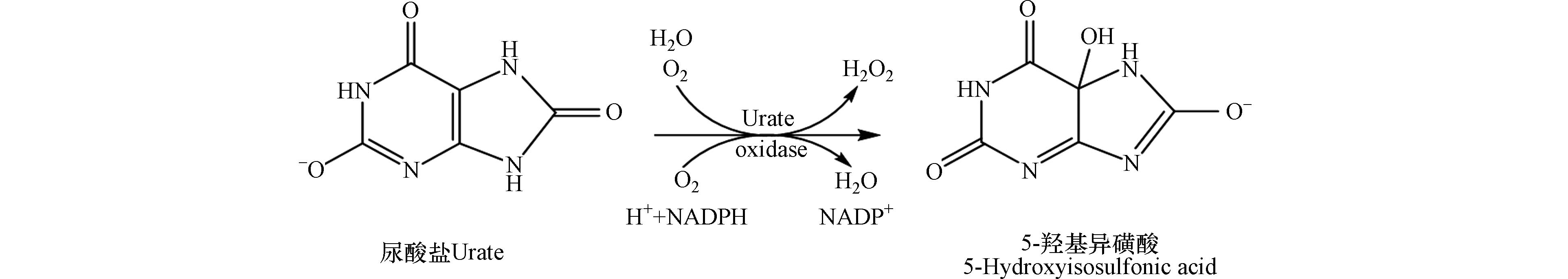
呼吸道衬液(respiratory tract lining fuid,RTLF)测定法是一种非细胞测定模型. RTLF作为PM进入人体后的第一道保护屏障和防线已被证明含有低分子量高浓度的抗氧化剂,如AA、GSH和尿酸等(uric qcid, UA)[27]. 它主要通过测定衬液中GSH、AA及UA消耗率反映PM氧化活性. 将采集的颗粒物样品在合成的RTLF溶液中于37 ℃孵育4 h,孵育后测量其中抗氧化剂的浓度. 在排除空白干扰后,UA、GSH和AA随时间消耗的速率即为颗粒物的OP,分别表示为OPUA、OPGSH和OPAA. UA盐的结构及其反应如图2[28]所示,PM中具有氧化性的物质与UA盐在还原性辅酶II(NADPH)的作用下,生成H2O2的同时将尿酸盐转化成5-羟基异磺酸(5-hydroxyisosulfonic acid,5-HIU).
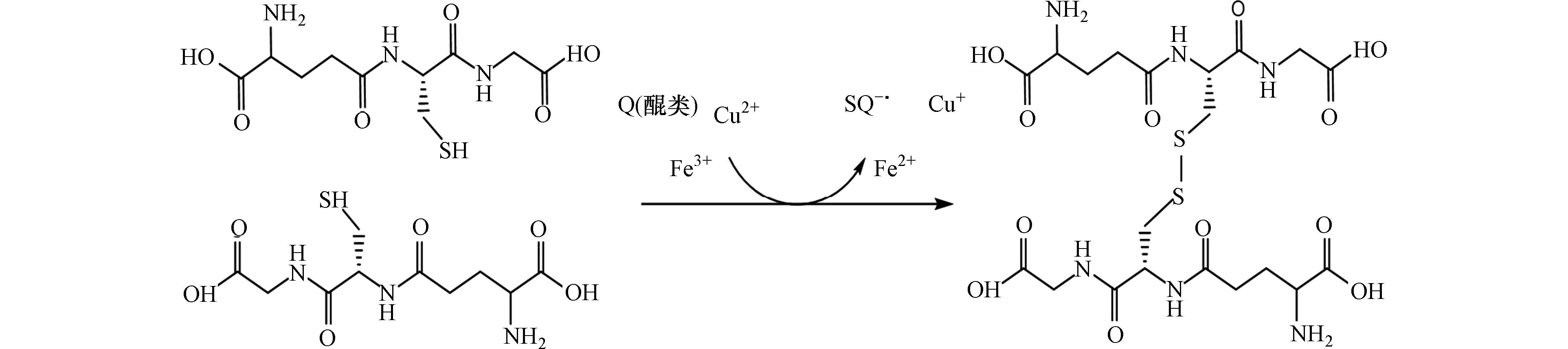
1)GSH法:GSH法是通过测量细胞的抗氧化剂的化学替代物GSH的消耗率来评估ROS的生成率,从而测定OP的方法[29]. GSH由谷氨酸、半胱氨酸和甘氨酸通过肽键组成,分子中有一特殊的γ-肽键,即由谷氨酸的γ-COOH与半胱氨酸的α-NH2缩合成的肽键,不同于其他蛋白质中的普通肽键. 发生反应时如方程式(1)所示,首先GSH与PM中活性物质反应产生硫基(GS·)自由基,GS·与GS-反应形成谷胱甘肽自由基二硫化物阴离子(GSSG·-),进而形成 O2·-和GSSH[30]. 其中反应过程如图3[31]所示,在醌类和金属的催化作用下,2分子的GSH以二硫键相连形成谷胱甘肽二硫化物. GSH抗氧化剂消耗速率计算如公式③所示[31]:
其中GSHT:孵化T时间后的GSH浓度;GSH0:开始的GSH浓度;T为孵化时间.
国内对于GSH法的研究较少,国外部分研究是将GSH法和其他非细胞法进行方法及对物种敏感程度对比. 在加拿大多伦多和蒙特利尔分别使用AA和GSH法分析PM2.5样品的OP,结果表明,PM2.5的ROS生成量、OPAA、OPGSH和磁铁矿纳米颗粒存在细微的空间尺度差异性[32]. 2016—2017年,同样在加拿大多伦多分别利用AA、GSH和DTT法测定了PM2.5的OP,结果表明PM2.5的OP在城市内部变化很大,并且在局部范围内OP存在明显季节差异[33].
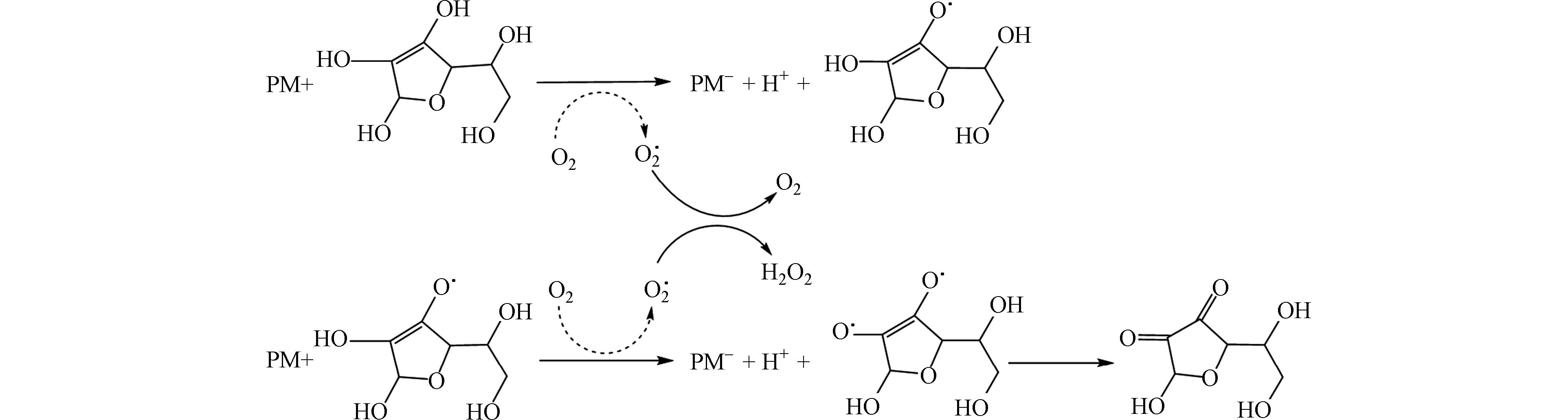
2)AA法:AA法是通过测定AA随时间的消耗速率来反映PM消耗RTLF中抗氧化剂的能力,从而测定OP的一种方法. AA是一种还原剂,分子结构中具有烯二醇结构和内酯环,且有2个手性碳原子. 如图4[19]所示PM中的氧化性物种会转移一个电子给氧分子,从而促进ROS的形成,同时AA被氧化为脱氢抗坏血酸,该物质在紫外/可见区265 nm波长处有吸收,AA消耗速率计算公式如④所示,OPAA计算公式如⑤所示[34]:
其中,σAbs:空白吸光度与时间的斜率;Abs0:初始吸光度;N0:反应的AA摩尔数;σAAs:样品AA消耗率;σAAb:空白AA消耗率;Ve:萃取体积;Va:样品体积;Vs是PM采样体积.
AA法最初用于测量微量金属催化氧化过程. 相对于DTT法,该方法应用于OP研究时间较晚. 2016年,Fang等[35]使用AA法分析了美国东南部气溶胶的OP值,该研究表明水溶性AAv活性具有明显的区域和季节分布特征. 2019年,Calas[36]同时采用DTT和AA法研究了法国7个城市一年内OP的季节性变化,研究表明冬季的OP值明显高于全年平均水平,且OC、EC、单糖和Cu与OP相关性较高,因此可通过减少这些物质含量从而降低PM对机体的危害性. 该测定法也可以使用单一抗氧化剂AA对颗粒物OP进行定量,并用作RTLF中AA分析的简化替代方法. 然而,国内外单独AA法测定OP的季节性变化和相关性研究仍然缺乏.
-
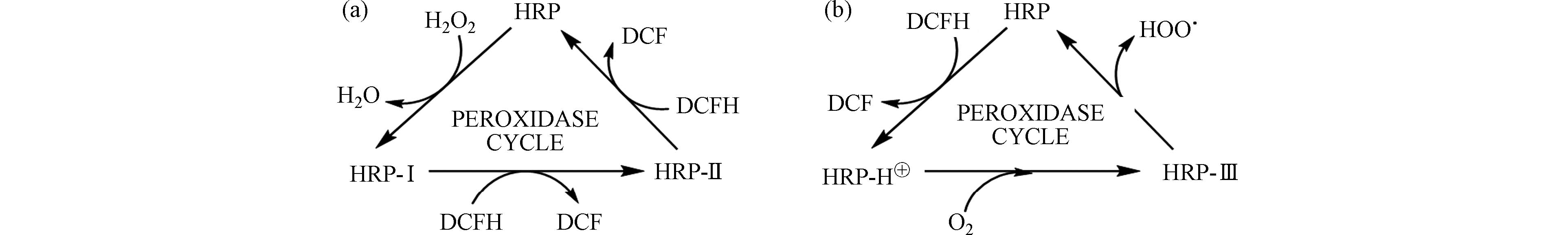
DCFH法是采用荧光光度法测定DCFH的一种方法. DCFH是一种非荧光试剂,将溶解在磷酸钠缓冲液中的DCFH试剂和辣根过氧化氢酶(horseradish peroxidase,HRP)添加到样品溶液中时,其中的H2O2(或大气PM中的ROS)会与HRP反应生成中间产物HRP-I,进而转化成HRP-II,随后DCFH脱氢被氧化成二氯荧光素(2',7'-dichlorofluorescein,DCF)[32]. 此外,如图5[37]所示大气中的氧也可以与HRP反应,在氧化酶循环中将DCFH氧化成DCF. DCFH法主要用H2O2标准溶液得到校正曲线,将荧光强度转换成H2O2当量,作为反应物种反应性的指示剂,从而得到OPDCFH值[38].
早期DCFH作为细胞法中最受欢迎的荧光探针之一,常用来测定细胞内的ROS[39]. 近年才被改用为一种非细胞法;虽然在一定程度上有所改善,但仍然具有一定的局限性. 比如DCFH法与AA及DTT法相比,未出现明显季节、时间和空间变化特征,并且灵敏度也较低[40]. DCFH法由于简单而被推广使用,但由于荧光物质容易分解,所以背景信号也相对较高[41]. 此外,研究者还尝试采用不同的荧光探针如二氢罗丹明、氢化乙锭等测定ROS的生成. 这类荧光探针法的原理是借助ROS使无荧光性的探针转化成荧光产物,或使原本强荧光性物质的荧光强度变弱或消失,通过测定荧光强度的变化间接实现对ROS的量化分析.
-
吖啶酯化学发光(chemiluminescent reductive acridinium triggering, CRAT)测定法是一种相对较新的方法,目前还尚未广泛用于空气污染研究. 机理如图6[42]所示:吖啶酯是一类可用作化学发光标记物的化学物质,在CRAT法中采用DTT、AA或GSH作为还原剂与PM反应生成H2O2. 在碱性条件下,H2O2与吖啶酯的C9发生加成,形成的过氧负离子,再与羰基上的碳发生亲核反应,进一步形成不稳定的四元环中间体,开环后形成激发态的吖啶酮,其返回到基态的过程中释放出光子,即可量化H2O2的生成速率[33]. CRAT是一种相对较新的技术,已广泛应用于化学、食品安全、生物医学等领域,而在大气环境检测中还未得到关注.
-
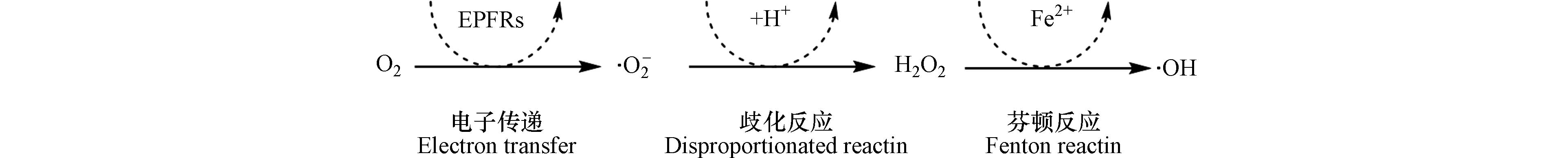
ESR法是通过电子的自旋共振作用而直接定量测定·OH的常用方法之一. 以5,5-二甲基吡咯-氧化物(5,5-dimethylpyrrole oxide, DMPO)作为自旋陷阱的电子自旋共振用来测量·OH的生成,常与H2O2结合使用[43]. 研究表明环境持久性自由基(environmental persistent free radicals, EPFRs)在机体的氧化还原循环系统中可产生ROS;图7[44]为采用EPR法测定EPFRs生成ROS的作用机理分为以下三部分:在EPFRs作用下电子转移给氧生成·O2-,随后通过歧化反应产生H2O2,最后在Fe2+作用下发生芬顿反应生成比H2O2氧化性更强的·OH. EPR法即通过测量特定ROS(包括·OH和H2O2)的产生速率从而得到相应地OP值.
-
由于水杨酸(salicylic acid,SA)法、对苯二甲酸(terephthalic acid, TA)法、苯甲酸盐(benzonate, BA)法等都是通过测量·OH而间接评估OP的方法. ·OH作为最具反应活性和强氧化能力的ROS种类,一直受到研究者们广泛的关注[36]. 故本文将这三种方法归纳为苯甲酸(Benzoic Acid, BAc)类测定法.
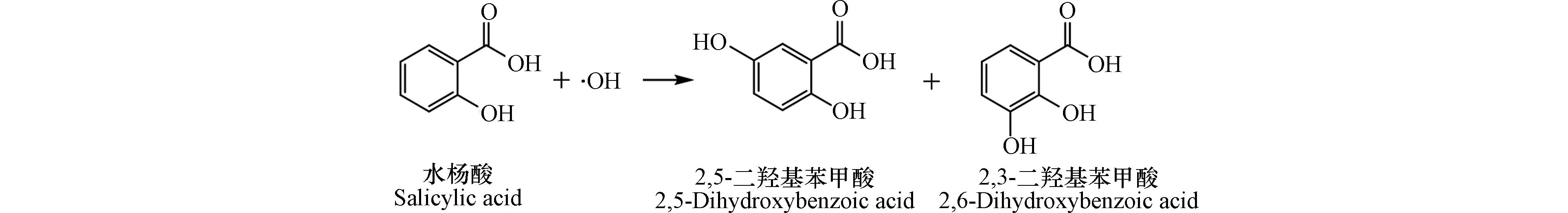
SA法:SA法是将SA作为自由基·OH捕捉剂,定量测定·OH的一种方法. 反应机理如图8[12]所示:SA与溶液中·OH反应生成两种同分异构体即2,3-二羟基苯甲酸(2,3-DHBA)和2,5-二羟基苯甲酸(2,5-DHBA),这两种物质在紫外区有较强吸光性. 该方法的缺点在于SA在紫外区也有较强吸光度,所以无法准确区别反应物和产物. 因此先用HPLC定性分析和分离后,再用紫外检测器或紫外分光光度计进行定量.
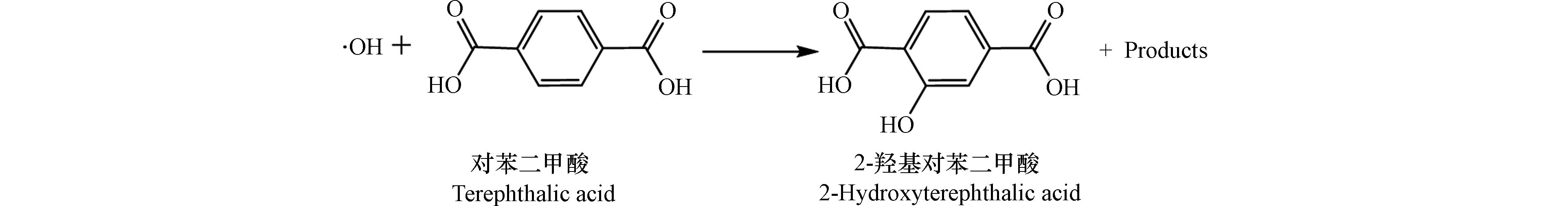
TA法:TA测定法是一种专门测定·OH的一种方法. TA可用于测定替代肺液(surrogate lung fluid, SLF)溶液中产生的·OH. SLF不同于真正的肺液,主要由磷酸盐溶液(PBS)与4种抗氧化剂包括L-抗坏血酸(L-ascorbic acid, Asc)、柠檬酸(citric acid, Cit)、GSH、UA组成. 该方法反应机理如图9[45]所示:PM与SLF反应生成的·OH与TA反应生成稳定且具有强荧光性的2-羟基对苯二甲酸(2-hydroxyterephthalic acid, TAOH),通过不同时间的荧光强度量化TAOH的量,从而确定·OH浓度并计算·OH 的产生速率, 计算公式见式⑥。
其中c(·OH)为·OH的浓度;c(TAOH)为所测量的TAOH的浓度;γTAOH为SLF中·OH与TA反应生成的TAOH的摩尔产率(在pH=7.2时为0.35).
BA法:BA测定法是将BA作为一种探针,其不参与ROS的产生,因此该方法能够定量化学物质(包括过渡金属和有机物)产生的·OH[46]. 反应过程中BA与·OH发生反应生成对羟基苯甲酸酯(p-hydroxybenzonate,p-HBA),通过HPLC测定p-HBA进而得到OP·OH. 计算公式⑦如下[47]:
其中,c(·OH)为·OH的浓度;[p-HBA]为HPLC测量的浓度;Yp-HBA为实验条件下p-HBA的摩尔产率(一般取值为0.215 ± 0.018); fBA为在SLF中与BA反应的·OH的分数(fBA计算为OH与BA的反应速率除以OH与所有溶液组分的反应速率之和,其值与溶液浓度以及与·OH二级反应速率常数相关).
-
其他测定方法比如对羟基苯乙酸(p-hydroxyphenylacetic acid, P-HOPAA)法、荧光硝基氧探针(profluorescent nitroxide probes, PFN)法等. PFN最初于1980s可定量检测自由基的生成,目前该方法主要应用于检测各种燃烧源和大气气溶胶生成的ROS.
-
测定OP有细胞法和非细胞法两大类;细胞法使用细胞培养法来评估PM造成的人体效应,一般采用巨噬细胞、人肺泡、细支气管和支气管上皮细胞等. 非细胞法是在体外模拟反应,由于其简单易操作等原因而被广泛使用. 非细胞法主要包括上面提到的DTT法、RTLF法(AA法、GSH法)、DCFH法、CRAT法、ESR法、BAc类法等. 如表1所示对各种非细胞法进行了分析比较.
根据表1可知,每一种方法在粒径敏感、OP物种以及应用上均有差异,显示出一定优点和局限性. 例如DCFH测定法与DTT和AA测定法相比,前者测定的OP值没有明显的空间和季节变化,且DCFH测定具有更低的灵敏度[40]. DTT对光敏感,因而DTT法需要在避免光照条件下进行;DTT对少数物种有反应性(物种特异性)且DTT实验还需要与DTNB反应,这可能会增加实验误差. 另外,不同方法对不同粒径PM的敏感度不同,如DTT和DCFH法对细颗粒较为敏感,而AA则对粗颗粒敏感,ESR法则无粒径选择性. 此外,不同方法对OP物种的敏感度也有差异,如AA法对过渡金属更敏感,对醌类则不敏感,而DTT法对PAHs、水溶性OC和醌类物质等有机化合物以及部分过渡金属敏感等. 这说明,每种非细胞法测定OP时均对ROS具有一定的特异性,使得没有一种方法可被用作评估环境PM毒性的标准方法和统一方法[48],这也是在大气颗粒物OP研究中存在的挑战.
-
目前国内研究主要集中在发达及沿海地区,基本采用DTT法测定了大气PM的OP,并对PM2.5的OP值及其季节和日变化、疫情或严重污染时期OP的变化、化学组分的影响、来源解析及空间分布均有涉及.
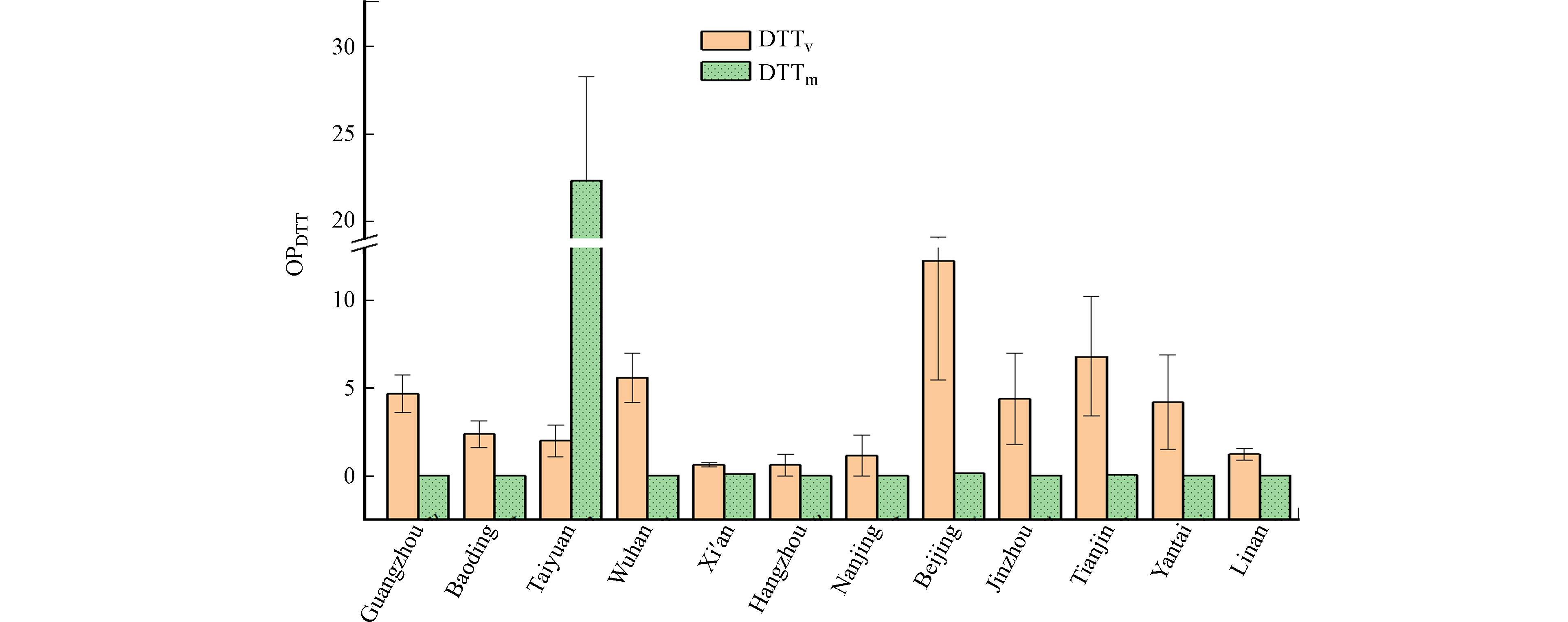
我国大气PM的OP研究主要集中在京津冀和长江三角洲等经济发达和沿海地区. 研究者发现PM2.5中OP具有一定的季节特征,如西安市2017年冬季的DTTv水平最高,其次是春季、夏季和秋季[49]. 临安2019年DTTv冬季大于2018年夏季,但DTTm却低于夏季[50]. 南京市DTTv和DTTm季节变化分别为冬季>春季>秋季>夏季和秋季>冬季>夏季>春季[51]. 可知,颗粒物OP值一般都呈现出冷季高于暖季,原因是由于温度较低时风速也较缓,大气污染物及颗粒物扩散受阻,另外DTTv值与PM2.5的质量浓度呈正相关,浓度较高会导致DTT降解速率更快,从而呈现较高DTT值,然而暖季DTT降解则较为缓慢,DTT值较低.
当前我国的OP研究基本采用DTT法,极少涉及AA法或EPR以及其他法. 如图10所示的地区均采用DTT法测定OP,其中与人体呼吸暴露有关的DTTv值较高的城市主要是那些人口众多,大气污染和雾霾较为突出的城市,其分别是:北京、天津、重污染时期的武汉和广州等. 研究者分析北京DTTv污染源认为,不同季节污染源来源和贡献存在明显差异,如春季频繁的沙尘天气是DTTv值的主要贡献者;车辆尾气排放贡献了夏季和秋季DTTv污染源的50%以上;车辆尾气排放和煤炭燃烧是冬季DTTv的主要贡献者,二次气溶胶的形成会大大增加全年DTTv 值[52]. 另外,太原市DTTm最高,这表明PM本身的OP较高. 其研究结果进一步证明:随着空气质量的恶化,DTTv逐步上升,尤其到重污染时其值迅速增加到中度污染的1.8倍[53].
目前OP的国外研究主要集中在OP和化学组分、颗粒物粒径的相关关系、时空分布特征、影响OP的排放源、OP分析法等方面. 2019年,Puthussery等[59]在德里采用DTT法测量了环境PM2.5的OP,并利用多种在线仪器对PM2.5的化学成分进行了测量,想要确定驱动OP的化学成分,研究结果表明:二次有机气溶胶(secondary organic aerosols,SOA)是PM2.5固有OP变化的主要驱动因素. Cesari等[60]使用DTT法测定分析PM2.5样品以确定离子、金属、含碳成分和OP活性,结果表明:DTTv与含碳成分和NO3-和Ca2+等离子相关性较高,说明燃烧、二次PM和地壳来源的PM可能对OP活性有贡献. 另外,有研究进一步证实了PM中不同金属元素与有机物对于OP的影响,这影响可能是协同或拮抗作用[61]. Wong等[62]评估了通过三种方法测定OP,分别是OPAA、OPDCFH和OPDTT法. 然而,三种检测方法对不同PM源的敏感性表现出明显差异. OPAA对铁路释放的粗颗粒特别敏感,OPDCFH对钢铁厂和家庭生物质供暖释放的细颗粒敏感,而OPDTT对工业和生物质燃烧源释放的细颗粒PM具有选择性敏感.
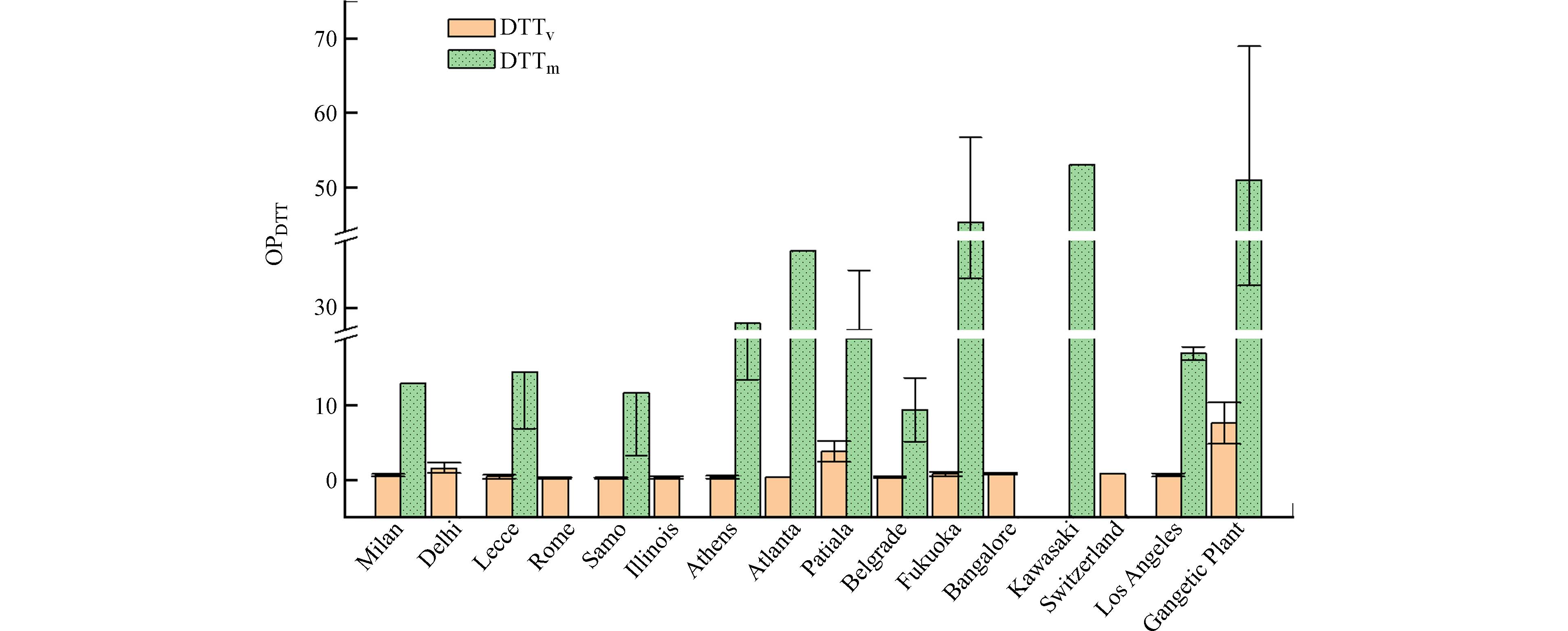
图11汇总了国外城市PM2.5的OP相关研究. 通过比较发现,Gangetic Plain在水稻秸秆燃烧时候的DTTv和DTTm较高;这说明生物质燃烧会导致PM的OP升高;其次较高DTTv水平的地区是:Patiala和Delhi,其DTTv低于国内北京、天津、武汉、广州、锦州以及烟台等地区;相对来说,国内报道的DTTv值高于发达国家,人体暴露风险也较高. 国外地区的DTTm值普遍比国内太原、北京、西安等城市要低. 其次,冬季的DTTv普遍要略高于其他季节,DTTm则未显示出明显季节差异. 国内与国外部分城市与地区的OP值相比发现我国OP值相对高于国外,尤其是秋冬季节. 这与我国由于国内寒冷季节大部分地区燃煤供暖以及人口众多,机动车尾气排放增加等原因所导致的大气污染以及雾霾直接相关. 这说明降低大气OP的关键还是治理我国目前面临的大气污染和雾霾,降低人体暴露,从而能保障人体健康风险.
-
大气PM的OP源解析是基于PM的源解析. PM2.5研究的一个重要方向就是来源识别,只有对来源精准识别,才能确定其污染类型,为PM2.5污染控制与减排提供可靠依据. 基于PM过程解析的模型方法包括:后向轨迹模型(hybrid single particle lagrangian integrated trajectory model,HYSPLIT)、扩散模型(diffusion model)、敏感性分析(sensitivity analysis)等. 基于PM源解析的受体模型包括:化学质量平衡(chemical mass balance,CMB)受体模型、富集因子(enrichment factor,EF)法、正交矩阵因子分解(positive matrix factorization,PMF)模型等[72]. 研究表明控制特定来源的颗粒物可能比控制总体颗粒物质量更有效[73]. 如表2,目前OP研究中大多采用受体模型对其进行贡献源解析,受体模型发展至今已有很多种方法,各种方法都存在一定的缺陷,在使用中会受到一定的限制,故部分研究也采用多种方法联用. 如Verma等[78]采用了PMF和CMB模型对美国佐治亚州PM的OP进行了贡献源解析,研究表明两种模型分析结果基本一致:即车辆排放全年占比为12%—25%(CMB分析结果车辆排放占比较高);夏季46%来自二次氧化过程;冬季生物质燃烧占47%.
不同来源PM诱导的OP存在差异,如交通源、生物质燃烧、二次源、燃料燃烧、扬尘、矿物粉尘、工业来源以及二次气溶胶形成过程(光化学反应)等诱导的OP值均有差别. 最新研究[79 − 80]表明光化学老化和二次源过程可以显著影响PM产生ROS的能力,例如新鲜的生物质燃烧产生的有机气溶胶在传输过程中发生光化学老化的OP值甚至会增加(2.1±0.9)倍. 另外,不同燃料燃烧产生的OP值也不同,如柴油燃烧的OP大于汽油燃烧. 生物质燃烧类型也会对PM的OP产生影响,小麦秸秆燃烧产生的OP最高,其次是秸秆燃烧、稻壳燃烧和大麦秸秆燃烧[81]. 交通源也是产生OP的驱动因素,特别是来自轮胎、制动器和道路磨损的非废气排放. 此外,Hara等[69]研究发现,亚洲尘埃事件期间细颗粒和粗颗粒的平均DTTv分别是非污染事件期间的1.5倍和2.7倍;细颗粒的DTTv与人为燃烧源高度相关,粗颗粒的DTTv与矿物粉尘衍生元素密切相关,表明矿物粉尘是粗颗粒产生OP的重要来源之一. 然而,撒哈拉沙漠[63]的沙尘对PM的OP的影响似乎并不显著,具有较低的OP. Ma等[78]首次发现,垃圾焚烧(17.7%)是OP的重要来源. 此外,不同的测定方法也会对不同OP来源有不一样的敏感度,比如意大利的一项研究得出3种OP检测对各PM10成分的不同敏感性:OPDCFH 和OPDTT 对交通、钢铁厂和生物质燃烧水溶性颗粒有明显的依赖性,OPAA 对非排气交通较为敏感[37].
由表2可知,PM的OP主要与人为源有关,其中重要的是生物质燃烧、汽车的尾气排放以及垃圾焚烧等. 在意大利的研究与以上研究观点类似,强调大多数OP主要与车辆交通排放和生物质燃烧有关[82]. 显然,控制生物质燃烧、机动车尾气以及垃圾焚烧等对于降低PM的OP是一个重要措施.
-
本文针对非细胞法测定PM中OP的几种重要方法进行了归纳总结,对于其方法原理、优缺点、OP的贡献源解析、OP的国内外研究进展等进行了分析. 虽然,研究者开展了诸多OP测定方法,国内外的OP研究也有了一定进展,但目前仍然缺少OP“标准”方法,另外几种方法存在粒径、污染源的敏感性等差异. 对大气PM的OP的来源方法还是基于PM的源解析的模型. 未来的研究可以将以下几个方面作为重点开展:
1) 当前测定PM中OP的方法发展较快,评估大气PM中OP的方法有细胞法和非细胞法两类. 然而,不同的OP测定方法所得的OP值存在差异和局限,这会影响全球大气PM中OP的数据的可比性. 因此,当前亟待建立标准化的分析测定手段和体系,从而促进OP引起的全球健康效应的准确评估.
2) 目前关于OP的研究数据仍然匮乏,我国研究主要集中于沿海及发达地区,对于偏远内陆地区还未全面展开研究. 然而,这些地区正在经历快速的城市化以及粗放式高速经济发展,空气状况不容乐观,PM2.5污染正在成为这些地区发展的主要制约因素和影响人体健康的重要原因. 国外研究虽然近年有所发展,但是占据人口众多的发展中国家和区域仍未开展关于OP的相关研究. 因此,想要评估全球PM的OP仍然缺少基础数据,需要进一步开展更系统、更全面的研究.
3) 当前研究集中于OP以及与组分的关系,仍未清楚哪些因素和组分是OP值的关键因素,未来研究需要充分考虑组分、气象因素、环境因素、污染源以及其他关键影响因素等,并应识别各因素的权重.
4) 现有部分OP源解析的研究主要还是依赖于PM的源解析基础上进行,并没有直接针对OP的源解析手段. 未来研究应重点之一仍然是OP的直接源解析方法,有针对性的控制OP污染源,从而降低机体暴露在大气PM中的健康风险.
大气颗粒物氧化潜势的非细胞测定方法及源解析研究进展
Research progress on non-cellular methods and source analysis of oxidation potential of atmospheric particulate matter
-
摘要: 大气颗粒物(particulate matter,PM)污染是全球关注的环境问题之一. PM的氧化潜势(oxidative potential,OP)是用来表征PM对人体健康风险的重要参数,它通过产生活性氧化物(reactive oxygen species,ROS)等物种,引起机体氧化应激,因而OP是PM暴露引起不良健康影响的核心驱动机制. 作为评估OP引发的健康风险的基础技术,近年来,大气PM的OP测定技术取得了一定进展. 本文归纳了几种重要的非细胞法测定PM的OP的反应机理,并对PM的OP的源解析方法以及最近OP国内外研究进展进行了综述. 最后对今后的大气PM的OP研究领域与方向进行了展望.Abstract: Atmospheric particulate matter (PM) pollution is one of the environmental issues of global concern. The oxidative potential (OP) of PM is a significant parameter applied to characterize the risk of PM to human health, which causes oxidative stress (OS) by producing reactive oxygen species (ROS). Therefore, OP is the crucial driving mechanism for the adverse health effects induced by PM exposure. As the fundamental technology for evaluating the health risks caused by OP, the considerable progress in determination of OP of atmospheric PM have been achieved in recent years. The present study reviewed the literature on the reaction mechanisms of several important non cellular methods, the source apportionment methods and recent research progress of OP of PM abroad and at home. Finally, the prospects for future research fields and directions of OP of atmospheric PM were presented.
-

-
表 1 大气OP的非细胞测定法对比
Table 1. Comparison of non-cellular determination methods for atmospheric OP
方法
Method优点
Advantage不足
Disadvantage敏感粒径
Sensitive particleOP物种
OP species检测方式
Detection modeDTT 价格低、操作简便、快速 光不稳定、物种特异性 0.32—1.8 µm PAHs、类腐殖质、水溶性TOC、醌类、Cu、Mn UV/酶标
412 nmAA 价格低、适用于自动化 灵敏度低、准确度低 3.2—5.6 µm 过渡金属(Fe、Cu、Cr、Mn、Pb、Zn、Co 和 Ni)、EC/OC UV/酶标仪
265 nmGSH 价格低、与健康效应相关性高 交通源相关性低 — 金属如Al、Fe和Pb UPLC
/MS-MSDCFH 价格低、操作简便 光不稳定、灵敏度低 0.32—1.8 µm 有机化合物(OC、PAH以及一些金属或其氧化物)、无机离子 荧光显微镜
485/535 nmCRAT 反应条件温和、重现性好 — 与PM质量浓度相关 Cu、Fe离子和醌类 发光仪
光信号ESR 灵敏度高、准确度高 仪器复杂、价格高 粗/细颗粒 EPFRs、过渡金属(Cu、Fe、V) ESR波谱仪
磁场检测BAc 机理简单 只测·OH,可检测种类少 — Fe、Cu 酶标仪 表 2 部分地区OP源解析情况[49,50,52,66,74 − 77]
Table 2. The source apportionment of OP in some regions[49,50,52,66,74 − 77]
地区
Region模型
Model主要贡献源
Major contributor国内 保定市 PMF 二次源、生物质燃烧、交通源 太原市 PMF 二次源及燃煤、生物质燃烧 西安市 PMF、MLR 机动车排放、燃煤源、二次硫酸盐 绵阳市 EF 生物质燃烧、二次硫酸盐 北京 PMF、MLR 生物质、垃圾及煤燃烧、汽车尾气 国外 美国 PMF、CMB 交通源、燃烧 亚特兰大(美国) PMF、CMB 交通排放、生物质燃烧、二次源 萨尔诺(意大利) PMF、MLR 生物质燃烧、二次硫酸盐、交通源 喀尔巴阡(欧洲) PMF 生物质燃烧、燃油燃烧、交通源 巴塞罗那(西班牙) PMF 燃烧、道路灰尘、重油 曼谷(印度) PMF、MLR 燃料燃烧、船舶排放、生物质燃烧 -
[1] 刘鹏, 常莉敏, 潘成珂, 等. 张掖市大气颗粒物水溶性离子污染特征、来源[J]. 环境化学, 2023, 42(9): 2993-3003. doi: 10.7524/j.issn.0254-6108.2022041402 LIU P, CHANG L M, PAN C K, et al. Characteristics and source apportionment of water-soluble ion as well as countermeasures for atmospheric particulate matter in Zhangye City[J]. Environmental Chemistry, 2023, 42(9): 2993-3003 (in Chinese). doi: 10.7524/j.issn.0254-6108.2022041402
[2] 蒋星星, 陈庆彩, 熊梦琪, 等. 疫情管控对关中城市群大气污染特征及颗粒物化学组成的影响[J]. 环境化学, 2023, 42(8): 2640-2650. doi: 10.7524/j.issn.0254-6108.2022032503 JIANG X X, CHEN Q C, XIONG M Q, et al. Influence of epidemic control on air pollution characteristics and chemical composition of particulate matter in Guanzhong urban agglomeration[J]. Environmental Chemistry, 2023, 42(8): 2640-2650 (in Chinese). doi: 10.7524/j.issn.0254-6108.2022032503
[3] 潘光, 杨雨欣, 王在峰, 等. 济南市钢铁集聚区大气细颗粒物中碳组分污染特征[J]. 环境化学, 2024, 43(4): 1177-1187. doi: 10.7524/j.issn.0254-6108.2022093002 PAN G, YANG Y X, WANG Z F, et al. Carbon component pollution characteristics of atmospheric fine particulate matter in iron and steel agglomeration area[J]. Environmental Chemistry, 2024, 43(4): 1177-1187(in Chinese). doi: 10.7524/j.issn.0254-6108.2022093002
[4] 李智饶. 长三角(临安)大气本底站细颗粒物中活性氧类物质季节特征研究[D]. 南京: 南京信息工程大学, 2021. LI Z R. Study on seasonal characteristics of reactive oxygen species in fine particles at atmospheric background station in Yangtze River Delta (Lin 'an)[D]. Nanjing: Nanjing University of Information Science & Technology, 2021 (in Chinese).
[5] WANG S M, ZHOU Q X, TIAN Y Z, et al. The lung microbiota affects pulmonary inflammation and oxidative stress induced by PM2.5 exposure[J]. Environmental Science & Technology, 2022, 56(17): 12368-12379. [6] DAI P Y, SHEN D, SHEN J K, et al. The roles of Nrf2 and autophagy in modulating inflammation mediated by TLR4 - NFκB in A549 cell exposed to layer house particulate matter 2.5 (PM2.5)[J]. Chemosphere, 2019, 235: 1134-1145. doi: 10.1016/j.chemosphere.2019.07.002 [7] UTINGER B, CAMPBELL S J, BUKOWIECKI N, et al. An automated online field instrument to quantify the oxidative potential of aerosol particles via ascorbic acid oxidation[J]. Atmospheric Measurement Techniques, 2023, 16(10): 2641-2654. doi: 10.5194/amt-16-2641-2023 [8] KERMANI M, RAHMATINIA T, OSKOEI V, et al. Potential cytotoxicity of trace elements and polycyclic aromatic hydrocarbons bounded to particulate matter: A review on in vitro studies on human lung epithelial cells[J]. Environmental Science and Pollution Research, 2021, 28(40): 55888-55904. doi: 10.1007/s11356-021-16306-y [9] TANG Z Y, SARNAT J A, WEBER R J, et al. The oxidative potential of fine particulate matter and biological perturbations in human plasma and saliva metabolome[J]. Environmental Science & Technology, 2022, 56(11): 7350-7361. [10] ZHANG H S, WANG L M, CHU Y W. Reactive oxygen species: The signal regulator of B cell[J]. Free Radical Biology and Medicine, 2019, 142: 16-22. doi: 10.1016/j.freeradbiomed.2019.06.004 [11] CROBEDDU B, BAUDRIMONT I, DEWEIRDT J, et al. Lung antioxidant depletion: A predictive indicator of cellular stress induced by ambient fine particles[J]. Environmental Science & Technology, 2020, 54(4): 2360-2369. [12] 周海涛. 大气细颗粒物的健康风险及其诱导羟基自由基的潜势分析[D]. 南京: 南京信息工程大学, 2021. ZHOU H T. Health risks of atmospheric fine particles and their potential to induce hydroxyl radicals[D]. Nanjing: Nanjing University of Information Science & Technology, 2021 (in Chinese).
[13] VINSON A, SIDWELL A, BLACK O, et al. Seasonal variation in the chemical composition and oxidative potential of PM2.5[J]. Atmosphere, 2020, 11(10): 1086. doi: 10.3390/atmos11101086 [14] PIETROGRANDE M C, DEMARIA G, COLOMBI C, et al. Seasonal and spatial variations of PM10 and PM2.5 oxidative potential in five urban and rural sites across Lombardia region, Italy[J]. International Journal of Environmental Research and Public Health, 2022, 19(13): 7778. doi: 10.3390/ijerph19137778 [15] 张东, 张元勋, 尚晶, 等. 北京市PM2.5中类腐殖质的生物氧化应激效应初探[J]. 环境科学研究, 2022, 35(8): 1986-1995. ZHANG D, ZHANG Y X, SHANG J, et al. Preliminary study on biological oxidative stress effects of humic-like substances in PM2.5 in Beijing[J]. Research of Environmental Sciences, 2022, 35(8): 1986-1995 (in Chinese).
[16] BERG K E, CLARK K M, LI X Y, et al. High-throughput, semi-automated dithiothreitol (DTT) assays for oxidative potential of fine particulate matter[J]. Atmospheric Environment, 2020, 222: 117132. doi: 10.1016/j.atmosenv.2019.117132 [17] QUINN C, MILLER-LIONBERG D D, KLUNDER K J, et al. Personal exposure to PM2.5 black carbon and aerosol oxidative potential using an automated microenvironmental aerosol sampler (AMAS)[J]. Environmental Science & Technology, 2018, 52(19): 11267-11275. [18] PIETROGRANDE M C, BACCO D, TRENTINI A, et al. Effect of filter extraction solvents on the measurement of the oxidative potential of airborne PM2.5[J]. Environmental Science and Pollution Research, 2021, 28(23): 29551-29563. doi: 10.1007/s11356-021-12604-7 [19] 张曼曼, 李慧蓉, 杨闻达, 等. 基于DTT法测量广州市区PM2.5的氧化潜势[J]. 中国环境科学, 2019, 39(6): 2258-2266. doi: 10.3969/j.issn.1000-6923.2019.06.003 ZHANG M M, LI H R, YANG W D, et al. Measurement based on DTT method of the PM2.5 oxidative potential in Guangzhou urban area[J]. China Environmental Science, 2019, 39(6): 2258-2266 (in Chinese). doi: 10.3969/j.issn.1000-6923.2019.06.003
[20] FREZZINI M A, de FRANCESCO N, MASSIMI L, et al. Effects of operating conditions on PM oxidative potential assays[J]. Atmospheric Environment, 2022, 268: 118802. doi: 10.1016/j.atmosenv.2021.118802 [21] 张俊美. 山东典型地区PM2.5中无机元素、多环芳烃及其衍生物污染特征和氧化潜势[D]. 济南: 山东大学, 2019. ZHANG J M. Pollution characteristics and oxidation potential of inorganic elements, polycyclic aromatic hydrocarbons and their derivatives in PM2.5 in typical areas of Shandong Province[D]. Jinan: Shandong University, 2019 (in Chinese).
[22] MA X Y, NIE D Y, CHEN M D, et al. The relative contributions of different chemical components to the oxidative potential of ambient fine particles in Nanjing area[J]. International Journal of Environmental Research and Public Health, 2021, 18(6): 2789. doi: 10.3390/ijerph18062789 [23] KUMAGAI Y, KOIDE S, TAGUCHI K, et al. Oxidation of proximal protein sulfhydryls by phenanthraquinone, a component of diesel exhaust particles[J]. Chemical Research in Toxicology, 2002, 15(4): 483-489. doi: 10.1021/tx0100993 [24] CHO A K, SIOUTAS C, MIGUEL A H, et al. Redox activity of airborne particulate matter at different sites in the Los Angeles Basin[J]. Environmental Research, 2005, 99(1): 40-47. doi: 10.1016/j.envres.2005.01.003 [25] CHARRIER J G, ANASTASIO C. On dithiothreitol (DTT) as a measure of oxidative potential for ambient particles: Evidence for the importance of soluble transition metals[J]. Atmospheric Chemistry and Physics, 2012, 12(5): 11317-11350. [26] FANG T, VERMA V, GUO H, et al. A semi-automated system for quantifying the oxidative potential of ambient particles in aqueous extracts using the dithiothreitol (DTT) assay: Results from the Southeastern Center for Air Pollution and Epidemiology (SCAPE)[J]. Atmospheric Measurement Techniques, 2015, 8(1): 471-482. doi: 10.5194/amt-8-471-2015 [27] MUDWAY I S, STENFORS N, DUGGAN S T, et al. An in vitro and in vivo investigation of the effects of diesel exhaust on human airway lining fluid antioxidants[J]. Archives of Biochemistry and Biophysics, 2004, 423(1): 200-212. doi: 10.1016/j.abb.2003.12.018 [28] DONISELLI N, MONZEGLIO E, dal PALÙ A, et al. The identification of an integral membrane, cytochrome c urate oxidase completes the catalytic repertoire of a therapeutic enzyme[J]. Scientific Reports, 2015, 5: 13798. doi: 10.1038/srep13798 [29] BATES J T, FANG T, VERMA V, et al. Review of acellular assays of ambient particulate matter oxidative potential: Methods and relationships with composition, sources, and health effects[J]. Environmental Science & Technology, 2019, 53(8): 4003-4019. [30] RAO L F, ZHANG L Y, WANG X Z, et al. Oxidative potential induced by ambient particulate matters with acellular assays: A review[J]. Processes, 2020, 8(11): 1410. doi: 10.3390/pr8111410 [31] SHAHPOURY P, HARNER T, LAMMEL G, et al. Development of an antioxidant assay to study oxidative potential of airborne particulate matter[J]. Atmospheric Measurement Techniques, 2019, 12(12): 6529-6539. doi: 10.5194/amt-12-6529-2019 [32] RIPLEY S, MINET L, ZALZAL J, et al. Predicting spatial variations in multiple measures of PM2.5 oxidative potential and magnetite nanoparticles in Toronto and Montreal, Canada[J]. Environmental Science & Technology, 2022, 56(11): 7256-7265. [33] WEICHENTHAL S, SHEKARRIZFARD M, TRAUB A, et al. Within-city spatial variations in multiple measures of PM2.5 oxidative potential in Toronto, Canada[J]. Environmental Science & Technology, 2019, 53(5): 2799-2810. [34] SIMONETTI G, CONTE E, MASSIMI L, et al. RETRACTED: Oxidative potential of particulate matter components generated by specific emission sources[J]. Journal of Aerosol Science, 2018, 126: 99-109. doi: 10.1016/j.jaerosci.2018.08.011 [35] FANG T, VERMA V, BATES J T, et al. Oxidative potential of ambient water-soluble PM2.5 in the southeastern United States: Contrasts in sources and health associations between ascorbic acid (AA) and dithiothreitol (DTT) assays[J]. Atmospheric Chemistry and Physics, 2016, 16(6): 3865-3879. doi: 10.5194/acp-16-3865-2016 [36] CALAS A, UZU G, BESOMBES J L, et al. Seasonal variations and chemical predictors of oxidative potential (OP) of particulate matter (PM), for seven urban French sites[J]. Atmosphere, 2019, 10(11): 698. doi: 10.3390/atmos10110698 [37] FULLER S J, WRAGG F P H, NUTTER J, et al. Comparison of on-line and off-line methods to quantify reactive oxygen species (ROS) in atmospheric aerosols[J]. Atmospheric Environment, 2014, 92: 97-103. doi: 10.1016/j.atmosenv.2014.04.006 [38] FREZZINI M A, Di IULIO G, TIRABOSCHI C, et al. A new method for the assessment of the oxidative potential of both water-soluble and insoluble PM[J]. Atmosphere, 2022, 13(2): 349. doi: 10.3390/atmos13020349 [39] SHAN X F, LIU L, LI G, et al. PM2.5 and the typical components cause organelle damage, apoptosis and necrosis: Role of reactive oxygen species[J]. Science of the Total Environment, 2021, 782: 146785. doi: 10.1016/j.scitotenv.2021.146785 [40] GRANGE S K, UZU G, WEBER S, et al. Linking Switzerland’s PM10 and PM2.5 oxidative potential (OP) with emission sources[J]. Atmospheric Chemistry and Physics, 2022, 22(10): 7029-7050. doi: 10.5194/acp-22-7029-2022 [41] 孙浩堯, 王玛敏, 陈庆彩. 大气活性氧物质污染特征、机制及其来源研究进展[J]. 环境化学, 2022, 41(6): 2052-2061. doi: 10.7524/j.issn.0254-6108.2021082303 SUN H Y, WANG M M, CHEN Q C. Advances in research on the pollution characteristics, mechanisms and sources of active reactive oxygen species in the atmosphere[J]. Environmental Chemistry, 2022, 41(6): 2052-2061 (in Chinese). doi: 10.7524/j.issn.0254-6108.2021082303
[42] ZOMER B, COLLÉ L, JEDYŃSKA A, et al. Chemiluminescent reductive acridinium triggering (CRAT)—Mechanism and applications[J]. Analytical and Bioanalytical Chemistry, 2011, 401(9): 2945-2954. doi: 10.1007/s00216-011-5342-3 [43] YANG A, HELLACK B, LESEMAN D, et al. Temporal and spatial variation of the metal-related oxidative potential of PM2.5 and its relation to PM2.5 mass and elemental composition[J]. Atmospheric Environment, 2015, 102: 62-69. doi: 10.1016/j.atmosenv.2014.11.053 [44] 李升苹. 西安市大气颗粒物中环境持久性自由基的来源及其氧化潜能特征研究[D]. 西安: 陕西科技大学, 2021. LI S P. Study on the sources and oxidation potential characteristics of environmental persistent free radicals in atmospheric particles in Xi 'an[D]. Xi'an: Shaanxi University of Science & Technology, 2021 (in Chinese).
[45] LI X Y, KUANG X M, YAN C Q, et al. Oxidative potential by PM2.5 in the North China plain: Generation of hydroxyl radical[J]. Environmental Science & Technology, 2019, 53(1): 512-520. [46] JUNG H, GUO B, ANASTASIO C, et al. Quantitative measurements of the generation of hydroxyl radicals by soot particles in a surrogate lung fluid[J]. Atmospheric Environment, 2006, 40(6): 1043-1052. doi: 10.1016/j.atmosenv.2005.11.015 [47] MA S X, REN K, LIU X W, et al. Production of hydroxyl radicals from Fe-containing fine particles in Guangzhou, China[J]. Atmospheric Environment, 2015, 123: 72-78. doi: 10.1016/j.atmosenv.2015.10.057 [48] WEBER S, UZU G, CALAS A, et al. An apportionment method for the oxidative potential of atmospheric particulate matter sources: Application to a one-year study in Chamonix, France[J]. Atmospheric Chemistry and Physics, 2018, 18(13): 9617-9629. doi: 10.5194/acp-18-9617-2018 [49] WANG Y Q, WANG M M, LI S P, et al. Study on the oxidation potential of the water-soluble components of ambient PM2.5 over Xi'an, China: Pollution levels, source apportionment and transport pathways[J]. Environment International, 2020, 136: 105515. doi: 10.1016/j.envint.2020.105515 [50] LI Z R, NIE D Y, CHEN M D, et al. Seasonal variation of oxidative potential of water-soluble components in PM2.5 and PM1 in the Yangtze River Delta, China[J]. Air Quality, Atmosphere & Health, 2021, 14(11): 1825-1836. [51] 马晓云. 南京地区PM2.5氧化潜能及细胞毒性研究[D]. 南京: 南京信息工程大学, 2021. MA X Y. Study on oxidation potential and cytotoxicity of PM2.5 in Nanjing[D]. Nanjing: Nanjing University of Information Science & Technology, 2021 (in Chinese).
[52] YU S Y, LIU W J, XU Y S, et al. Characteristics and oxidative potential of atmospheric PM2.5 in Beijing: Source apportionment and seasonal variation[J]. Science of the Total Environment, 2019, 650: 277-287. doi: 10.1016/j.scitotenv.2018.09.021 [53] 任娇, 赵荣荣, 王铭, 等. 太原市冬季不同污染程度下PM2.5的化学组成、消光特征及氧化潜势[J]. 环境科学, 2022, 43(5): 2317-2328. REN J, ZHAO R R, WANG M, et al. Chemical compositions, light extinction effect, and oxidative potential of PM2.5 under different pollution levels during winter in Taiyuan[J]. Environmental Science, 2022, 43(5): 2317-2328 (in Chinese).
[54] 吴继炎, 杨池, 张春燕, 等. 保定市冬季PM2.5的氧化潜势特征及其影响来源分析[J]. 环境科学, 2022, 43(6): 2878-2887. WU J Y, YANG C, ZHANG C Y [et al. Analysis on the characteristics of oxidation potential and influence sources of PM2.5 in Baoding city in winter[J]. Environmental Science, 2022, 43(6): 2878-2887 (in Chinese).
[55] 陈丹鈜, 张志豪, 张珅, 等. 武汉市冬季重污染期PM2.5的氧化潜势分析[J]. 环境科学与技术, 2020, 43(10): 171-176. CHEN D H, ZHANG Z H, ZHANG S, et al. Analysis of PM2.5 oxidative potential during a period of heavy pollution in winter, Wuhan[J]. Environmental Science & Technology, 2020, 43(10): 171-176 (in Chinese).
[56] WANG J P, LIN X, LU L P, et al. Temporal variation of oxidative potential of water soluble components of ambient PM2.5 measured by dithiothreitol (DTT) assay[J]. Science of the Total Environment, 2019, 649: 969-978. doi: 10.1016/j.scitotenv.2018.08.375 [57] LIU W J, XU Y S, LIU W X, et al. Oxidative potential of ambient PM2.5 in the coastal cities of the Bohai Sea, Northern China: Seasonal variation and source apportionment[J]. Environmental Pollution, 2018, 236: 514-528. doi: 10.1016/j.envpol.2018.01.116 [58] YANG F, LIU C, QIAN H. Comparison of indoor and outdoor oxidative potential of PM2.5: Pollution levels, temporal patterns, and key constituents[J]. Environment International, 2021, 155: 106684. doi: 10.1016/j.envint.2021.106684 [59] PUTHUSSERY J V, SINGH A, RAI P, et al. Real-time measurements of PM2.5 oxidative potential using a dithiothreitol assay in Delhi, India[J]. Environmental Science & Technology Letters, 2020, 7(7): 504-510. [60] PARASKEVOPOULOU D, BOUGIATIOTI A, STAVROULAS I, et al. Yearlong variability of oxidative potential of particulate matter in an urban Mediterranean environment[J]. Atmospheric Environment, 2019, 206: 183-196. doi: 10.1016/j.atmosenv.2019.02.027 [61] LIN M F, YU J Z. Assessment of interactions between transition metals and atmospheric organics: Ascorbic acid depletion and hydroxyl radical formation in organic-metal mixtures[J]. Environmental Science & Technology, 2020, 54(3): 1431-1442. [62] WONG J P S, TSAGKARAKI M, TSIODRA I, et al. Effects of atmospheric processing on the oxidative potential of biomass burning organic aerosols[J]. Environmental Science & Technology, 2019, 53(12): 6747-6756. [63] PUTHUSSERY J V, ZHANG C, VERMA V. Development and field testing of an online instrument for measuring the real-time oxidative potential of ambient particulate matter based on dithiothreitol assay[J]. Atmospheric Measurement Techniques, 2018, 11(10): 5767-5780. doi: 10.5194/amt-11-5767-2018 [64] PATEL A, SATISH R, RASTOGI N. Remarkably high oxidative potential of atmospheric PM2.5 coming from a large-scale paddy-residue burning over the northwestern indo-gangetic plain[J]. ACS Earth and Space Chemistry, 2021, 5(9): 2442-2452. doi: 10.1021/acsearthspacechem.1c00125 [65] CESARI D, MERICO E, GRASSO F M, et al. Source apportionment of PM2.5 and of its oxidative potential in an industrial suburban site in South Italy[J]. Atmosphere, 2019, 10(12): 758. doi: 10.3390/atmos10120758 [66] CHIRIZZI D, CESARI D, GUASCITO M R, et al. Influence of Saharan dust outbreaks and carbon content on oxidative potential of water-soluble fractions of PM2.5 and PM10[J]. Atmospheric Environment, 2017, 163: 1-8. doi: 10.1016/j.atmosenv.2017.05.021 [67] VISENTIN M, PAGNONI A, SARTI E, et al. Urban PM2.5 oxidative potential: Importance of chemical species and comparison of two spectrophotometric cell-free assays[J]. Environmental Pollution, 2016, 219: 72-79. doi: 10.1016/j.envpol.2016.09.047 [68] FANG T, GUO H Y, VERMA V, et al. PM 2.5 water-soluble elements in the southeastern United States: Automated analytical method development, spatiotemporal distributions, source apportionment, and implications for heath studies[J]. Atmospheric Chemistry and Physics, 2015, 15: 11667-11682. doi: 10.5194/acp-15-11667-2015 [69] JEDYNSKA A, HOEK G, WANG M, et al. Spatial variations and development of land use regression models of oxidative potential in ten European study areas[J]. Atmospheric Environment, 2017, 150: 24-32. doi: 10.1016/j.atmosenv.2016.11.029 [70] JOVANOVIC M V, SAVIC J Z, SALIMI F, et al. Measurements of oxidative potential of particulate matter at Belgrade tunnel;comparison of BPEAnit, DTT and DCFH assays[J]. International Journal of Environmental Research and Public Health, 2019, 16(24): 4906. doi: 10.3390/ijerph16244906 [71] NISHITA-HARA C, HIRABAYASHI M, HARA K, et al. Dithiothreitol-measured oxidative potential of size-segregated particulate matter in Fukuoka, Japan: Effects of Asian dust events[J]. GeoHealth, 2019, 3(6): 160-173. doi: 10.1029/2019GH000189 [72] 胡敏, 唐倩, 彭剑飞, 等. 我国大气颗粒物来源及特征分析[J]. 环境与可持续发展, 2011, 36(5): 15-19. doi: 10.3969/j.issn.1673-288X.2011.05.004 HU M, TANG Q, PENG J F, et al. Study on characterization and source apportionment of atmospheric particulate matter in China[J]. Environment and Sustainable Development, 2011, 36(5): 15-19 (in Chinese). doi: 10.3969/j.issn.1673-288X.2011.05.004
[73] DAELLENBACH K R, UZU G, JIANG J H, et al. Sources of particulate-matter air pollution and its oxidative potential in Europe[J]. Nature, 2020, 587(7834): 414-419. doi: 10.1038/s41586-020-2902-8 [74] VÖRÖSMARTY M, UZU G, JAFFREZO J, et al. Oxidative potential in rural, suburban and city centre atmospheric environments in central Europe[J]. Atmospheric Chemistry and Physics, 2023, 1206. [75] VELD M I ', PANDOLFI M, AMATO F, et al. Discovering oxidative potential (OP) drivers of atmospheric PM10, PM2.5, and PM1 simultaneously in North-Eastern Spain[J]. The Science of the Total Environment, 2023, 857(Pt 2): 159386. [76] WANG J Q, JIANG H Y, JIANG H X, et al. Source apportionment of water-soluble oxidative potential in ambient total suspended particulate from Bangkok: Biomass burning versus fossil fuel combustion[J]. Atmospheric Environment, 2020, 235: 117624. doi: 10.1016/j.atmosenv.2020.117624 [77] MA Y Q, CHENG Y B, QIU X H, et al. Sources and oxidative potential of water-soluble humic-like substances (HULISWS) in fine particulate matter (PM2.5) in Beijing[J]. Atmospheric Chemistry and Physics, 2018, 18(8): 5607-5617. doi: 10.5194/acp-18-5607-2018 [78] REFEREE M P. Interactive comment on “Reactive oxygen species associated with water-soluble PM2.5 in the southeastern United States: Spatiotemporal trends and source apportionment[J]. Atmospheric Chemistry and Physics, 2014, 14(23): 12915-12930. doi: 10.5194/acp-14-12915-2014 [79] LIU T, WANG X, DENG W, et al. Secondary organic aerosol formation from photochemical aging of light-duty gasoline vehicle exhausts in a smog chamber[J]. Atmospheric Chemistry and Physics, 2015, 15(15): 9049-9062. doi: 10.5194/acp-15-9049-2015 [80] MASSIMI L, RISTORINI M, SIMONETTI G, et al. Spatial mapping and size distribution of oxidative potential of particulate matter released by spatially disaggregated sources[J]. Environmental Pollution, 2020, 266: 115271. doi: 10.1016/j.envpol.2020.115271 [81] GUO H B, JIN L, HUANG S J. Effect of PM characterization on PM oxidative potential by acellular assays: A review[J]. Reviews on Environmental Health, 2020, 35(4): 461-470. doi: 10.1515/reveh-2020-0003 [82] PIETROGRANDE, RUSSO, ZAGATTI. Review of PM oxidative potential measured with acellular assays in urban and rural sites across Italy[J]. Atmosphere, 2019, 10(10): 626. doi: 10.3390/atmos10100626 -



 下载:
下载: